Method Article
Inchaço na Organóides intestinal induzida por forscolina: An
Neste Artigo
Resumo
This protocol describes an assay for measuring CFTR function and CFTR modulator responses in cultured tissue from subjects with cystic fibrosis (CF). Biopsy-derived intestinal organoids swell in a cAMP-driven fashion, a response that is defective (or strongly reduced) in CF organoids and can be restored by exposure to CFTR modulators.
Resumo
Recently-developed cystic fibrosis transmembrane conductance regulator (CFTR)-modulating drugs correct surface expression and/or function of the mutant CFTR channel in subjects with cystic fibrosis (CF). Identification of subjects that may benefit from these drugs is challenging because of the extensive heterogeneity of CFTR mutations, as well as other unknown factors that contribute to individual drug efficacy. Here, we describe a simple and relatively rapid assay for measuring individual CFTR function and response to CFTR modulators in vitro. Three dimensional (3D) epithelial organoids are grown from rectal biopsies in standard organoid medium. Once established, the organoids can be bio-banked for future analysis. For the assay, 30-80 organoids are seeded in 96-well plates in basement membrane matrix and are then exposed to drugs. One day later, the organoids are stained with calcein green, and forskolin-induced swelling is monitored by confocal live cell microscopy at 37 °C. Forskolin-induced swelling is fully CFTR-dependent and is sufficiently sensitive and precise to allow for discrimination between the drug responses of individuals with different and even identical CFTR mutations. In vitro swell responses correlate with the clinical response to therapy. This assay provides a cost-effective approach for the identification of drug-responsive individuals, independent of their CFTR mutations. It may also be instrumental in the development of future CFTR modulators.
Introdução
FC é causada por mutações no gene da fibrose cística regulador da condutância transmembranar (CFTR), que codifica um canal de anião epitelial. CF afeta cerca de 85.000 pessoas em todo o mundo 1. Mais de 2.000 mutações CFTR foram identificados ( www.genet.sickkids.on.ca ). Esta diversidade explica parcialmente um amplo espectro de fenótipos da doença observados ( www.CFTR2.org ) 2, 3. Seis classes de mutações CFTR são definidos com base no seu efeito na expressão da proteína de CFTR e função de: (i) nenhuma síntese, (II) tráfico prejudicada, (III) gating canal defeituoso, (IV) condutância alterada, (v) níveis de normalmente reduzida CFTR funcional, e (VI) a estabilidade da superfície de células deficientes 4. Embora as mutações CFTR comuns são bem estudadas, a função de CFTR e sua relação com o estado clínico permanecem poorlY compreendido no nível do indivíduo, em particular para a grande grupo de "órfãos" mutações raras ( www.CFTR2.org ) 1, 3.
Recentemente, as drogas que têm sido desenvolvidos como alvo a proteína CFTR de um modo específico da mutação. Duas classes de CFTR drogas-alvo proteínas estão atualmente em uso clínico e têm modos distintos de ação. Potenciadores, tais como VX-770, aumentar a probabilidade, aberto de CFTR mutante apical-localizados e agir diretamente sobre sua adição às células 5. Correctores, tais como VX-809, restaurar o tráfico de endoplasmático CFTR misfolded localizada-retículo e exigem pré-incubação com células antes que os efeitos são observados 6. O potenciador CFTR, VX-770, foi registrado para indivíduos com a mutação G551D 7, 8, bem como para outros oitoCFTR gating mutações, incluindo S1251N 9; em conjunto, estas mutações são realizados por 5% de todos os pacientes com FC. Outros estudos clínicos indicaram que VX-770, combinado com o corrector de VX-809, tem limitado ainda efeitos significativos sobre a função pulmonar e provoca uma diminuição nas taxas de exacerbação em indivíduos homozigóticos para a mutação F508del transportadas por 45-50% dos pacientes 10, 11.
ensaios clínicos convencionais para identificar temas de droga-responsivo dentro os restantes 50% de pacientes com FC são dispendiosos e consumidores de tempo e não são viáveis para os indivíduos com genótipos CFTR extremamente raros. Novel,, métodos personalizados de baixo custo são cruciais para coincidir com o número crescente de moduladores de CFTR aos indivíduos portadores de qualquer tipo de mutação CFTR. Até agora, a inclusão julgamento de grupos de pacientes portadores de mutações CFTR específicas tem sido orientada por estudos utilizando mutante transfecção gene CFTR em hsistemas de células de eterologous, seguidos por estudos eletrofisiológicos em câmaras de Ussing 5, 6, 12. Devido a uma falta de modelos animais adequados, CF estudos de eficácia de drogas em células epiteliais brônquicas ar-líquido da interface diferenciadas derivadas de materiais de explante pulmonar FQ têm sido utilizados para o desenvolvimento de fármacos 13, 14, 15. No entanto, a disponibilidade limitada de tecidos de explantes pulmonares e os procedimentos invasivos para obter células brônquicas de indivíduos sem a doença em fase terminal dificultar a análise de mutações CFTR menos comuns e impedir que o teste de drogas de forma personalizada. Para superar essas limitações, tecidos "fácil acesso", como Organóides colorretais, células das vias aéreas nasais e células das vias respiratórias derivadas de células-tronco pluripotentes induzidas, estão actualmente a ser exploradas para tratamentos com medicamentos personalizados.
Anteriormente, estabelecemos protocolos para a cultura de células estaminais epiteliais de qualquer órgão gastrointestinal na forma de 3D Organóides 16, 17. factores de crescimento para o cólon / recto humana, definidos envolvem as condições de cultura (Factor de Crescimento Epitelial (EGF), gastrina, Wnt-3A, R-espondina 3 (Rspo3), e Noggin) combinado com pequenas moléculas (nicotinamida, A83-01, e SB202190) numa matriz de membrana basal. Sob estas condições, as células estaminais individuais ou pequenos fragmentos de tecido crescer até formarem cística, estruturas 3D fechado formado por epitélio altamente polarizada com o lado basal orientada para o exterior. Todos os tipos de células normalmente aparecem em suas proporções normais e posições. Organóides pode ser expandida ao longo de períodos longos por ruptura mecânica semanal e re-plaqueamento. Eles são geneticamente e fenotipicamente estáveis e podem ser armazenados, permitindo a expansão de longo prazo e bio-banking 17. Eles são passíveis detodas as manipulações de células-biológico padrão / genéticos e técnicas de análise desenvolvido para linhas celulares 2D 18.
Recentemente, demonstramos que a função CFTR pode ser facilmente medido em Organóides colorretais em um ensaio de edema induzido por forscolina (FIS) 19, 20. Quando exposto a forscolina (FSK) ou, alternativamente, a toxina da cólera, Organóides aumentar rapidamente a sua monofosfato de adenosina cíclico níveis (cAMP), que por sua vez, resulta na abertura do canal CFTR 19. Organóides de indivíduos saudáveis, ou a partir de indivíduos com mutações de CFTR associado com função residual, vai inchar subsequentemente como uma consequência de iões e de transporte de água para o lúmen, organ�de o equivalente in vitro de diarreia secretora. A resposta de FIS Organóides colorrectais foi mostrado previamente para ser totalmente CFTR-dependente, tal como indicado por Organóides derivadas de indivíduos CFTR-null, umnd pela utilização de inibidores de CFTR farmacológicas específicas 19. Grandes conjuntos de dados específicos de um assunto pode ser derivada dentro de várias semanas depois de tomar uma biópsia.
Para o ensaio de FIS descrito em detalhe aqui, Organóides são cultivadas a partir de biópsias rectais que podem ser obtidos em qualquer idade e com apenas desconforto limitada 21. Organóides são passadas semanalmente por perturbação mecânica em criptas de solteiro que facilmente fechado hermético e formar novos Organóides. Para a execução do ensaio de FIS, ~ 30-80 destes Organóides pequenos rompidas foram semeadas em cada poço de uma placa de 96 poços 19. No dia do ensaio, as Organóides são coradas com verde calceína, um corante fluorescente de células-permeável que é mantido dentro de células vivas, facilitando imagens ao vivo. Em seguida, Fsk, o que aumenta o AMPc intracelular e deste modo activa CFTR, é adicionado a fim de estimular o inchaço organ�de. Potenciadores que atuam sobre CFTR apical são adicionados simultaneamente wom o forskolin, enquanto corretores que restauram tráfico CFTR são adicionados 24 horas antes da adição de Fsk. O inchaço organ�de é quantificada pela análise de imagem automatizado que calcula o aumento relativo da área total de todos os objectos fluorescentes para cada ponto de tempo após a adição de forscolina.
3D organ�de inchaço oferece vantagens e desvantagens sobre leituras CFTR eletrofisiológicos existentes nas células das vias aéreas cultivadas em 2D em Ussing câmaras. Uma grande vantagem é a capacidade do ensaio de inchamento. As células são cultivadas e analisadas utilizando um único tipo de meio de cultura, e um técnico experiente pode cultura até 25 amostras organ�de numa base semanal, enquanto quantificando cerca de 1.200 pontos de dados por semana em 12 amostras de pacientes. Nós convencionalmente digitar uma única condição experimental por meio de medições em duplicado ou triplicado por placa e repetir tais medições em três momentos de incubação independentes. No total, cerca de 300-500 single organ�de estruturas são então medidos por condição experimental, o que leva a medições muito precisas da função CFTR com variabilidade técnica limitada. Esta precisão permite-nos definir claramente diferenças na função residual e resposta para moduladores de CFTR e nos permite escolher facilmente se os efeitos genéticos fundo entre os pacientes portadores de mutações CFTR idênticos 19, 22, 23, 24, 25. A qualidade dos dados pode ser facilmente avaliada a partir de imagens de microscópio. Enquanto FIS é totalmente CFTR-dependente, é uma medida de resultado indirecto para a função CFTR, o seu fora de leitura causada pelo acoplamento de transporte de íons para o transporte de fluidos. Isto contrasta com medições da função CFTR diretos em câmaras Ussing, que medem transepiteliais correntes iônicas 26. câmaras de Ussing permitir a estimulação seleccionado de apical ou basolateral Compartments (que o ensaio organ�de não permite); por permeabilização de membranas basolaterais, a secreção dependente de anião CFTR apical pode ser medido selectivamente 27.
Protocolo
Todos os experimentos usando tecidos humanos aqui descritos foi aprovado pelo comitê de ética da Universidade Medical Center Utrecht (UMCU; TcBio # 14-008). O consentimento informado para a recolha de tecidos, geração, armazenamento e uso dos Organóides foram obtidas junto aos pacientes do Hospital (WKZ) -UMCU de Wilhelmina Children.
| Equipamento | consumível | Ferramentas |
| câmara de fluxo laminar | 15 e 50 ml de tubos cónicos | Zeiss LSM 800 - Zen 2 (edição azul) software para medir imagens |
| Incubadora de CO 2 | tubos de microcentrífuga | programa Microsoft Excel |
| Microscópio de cultura de células (luz microscópio óptico /) | 0,22 filtros | |
| centrifugador | pipetas serológicos | |
| rolamento Shaker | pontas com filtro micropipeta | |
| Sala C 4 ° ou 4 ° C frigorífico para incubadora | criotubos | |
| CoolCell celular Freezing Container | ||
| Pipetadora sorológica | ||
| Micropippette (1000, 200 e 20 ul) | ||
| Viaflo Repita pipeta | ||
| (Células vivas) Confocal Microscópio | ||
| Computador | ||
| tanque de nitrogênio líquido | ||
| Multicanal (200 ul) |
1. Reagentes preparando para Cultura
NOTA: Todas as etapas são executadas dentro de uma cabine de segurança biológica e seguindo diretrizes padrão para trabalhar com culturas de células. A fim de facilitar a formação de gotas de agradáveis matriz da membrana basal, manter um material pré-aquecido de 96-, 24-, e placas de 6 poços na incubadora a 37 ° C.
- Meio Basal Preparação
NOTA: meio basal (BM) refere-se a Avançado do Dulbecco Modified Eagle Médium com Mistura de Ham Nutriente F-12 (Ad-DF) suplementado com 4- (2-hydroxyethil) ácido -1piperazineethanesulfonic (HEPES), glutamina, e penicilina / estreptomicina (Pen / Strep).- Numa forma frasco de 500 ml Ad-DF, adicionar 5 ml de glutamina 200 mM, 5 mL de HEPES 1 M, e 5 ml de soluções de pen / estrep (10.000 U / ml, 10000 ug / ml).
- BM guarde na geladeira a 4 ° C durante pelo menos 4 semanas.
- -Wnt-3A Preparação de meio condicionado
NOTA: medium Wnt-3A-condicionado é feito in-house using a linha celular de Wnt-L-3A de acordo com as instruções do fabricante.- Para colher o meio condicionado de Wnt-3A, recolher a forma exposto às células durante uma semana e girá-lo para baixo durante 5 minutos a 450 xg para remover as células flutuantes.
- Filtra-se o meio de Wnt-3a-condicionado através de um filtro de 0,22 um e dividi-lo em alíquotas de 40 ml em tubos de 50 mL cónicos. Armazená-los a 4 ° C durante pelo menos 4 meses sem perda de actividade.
- Testar a actividade do meio condicionado de Wnt-3A num ensaio de TOP / FOP utilizando rim embrionário humano (HEK) -293 células transfectadas com o topo e FOP-luciferase de Renilla e TK- e medidos com um estojo de ensaio de Renilla -luciferase segundo as instruções do fabricante.
NOTA: TOP-luciferase é um plasmídeo repórter que contém regiões de ligação TCF de tipo selvagem. Se o meio de Wnt-3A-condicionado está ativa, a sinalização Wnt canônica é ativado. Beta-catenina transloca-se para o núcleo para associar with TCF / LEF factores de transcrição e activa a transcrição do repórter de luciferase, induzindo um aumento na actividade de luciferase relativa quando o substrato é adicionado. A FOP-luciferase é usado como um controlo negativo porque o TCF regiões de ligação a montante do gene de luciferase são mutados.
- Colon Médio Preparação
Nota: Preparar e diluir todos os fatores de crescimento e reagentes de acordo com as recomendações dos fabricantes. Use alíquotas de pequeno porte uma Evitar ciclos de congelamento e descongelamento. factores de crescimento funcionais são essenciais para os resultados.- Prepare a forma do cólon (CM), completando com 1x BM B27, 1,25 mM de N-acetilcisteína, 50 ng / ml de hEGF, 5 nM de gastrina, nicotinamida a 10 mM, 300 ng / ml hRspo3, 100 ng / ml hNoggin, 500 uM A83-01 , 10 uM SB202190, e 100 ug / ml de um agente antimicrobiano para as células primárias.
- Dividir o CM em alíquotas e congelá-las a -20 ° C durante até 4 meses. Descongelar as alíquotas para preparar cólon completomédia (FCM) por adição de 50% de meio de Wnt-3a-conditoned para a CM. Loja FCM até 7 dias a 4 ° C sem perda de actividade.
- Para o estabelecimento de uma cultura de biópsias organ�de rectais, complementar FCM com 50 ug / ml de vancomicina, 50 ug / ml de gentamicina, e 10 uM associada a Rho proteína serina / treonina quinase inibidor coiled-coil-forming (RhoKi). Usar este meio, chamado de meio de isolamento (IM), para os primeiros dois ou três dias em cultura.
- EDTA da Preparação de Solução
- Prepare M de ácido 0,5 etilenodiaminotetracético (EDTA), pH 8, em ultrapura H2O, esterilizadas com um filtro de 0,22 um.
- Manipulação da membrana basal Matrix
- Prepare a matriz da membrana basal (BMM) de acordo com a recomendação do fabricante.
- Thaw BMM noite no gelo.
- Ao transferir o BMM do frasco para um tubo cónico de 15 ml, a utilizaçãouma pipeta de 5 ml e um tubo de 15 ml pré-arrefecido a -20 ° C.
- Uma vez descongelado, o BMM armazenar no frigorífico a 4 ° C e incubar em gelo durante pelo menos 30-60 minutos antes da utilização.
NOTA: Para obter os melhores resultados, o BMM deve ser frio e devidamente misturados antes incorporação criptas ou Organóides.
2. Estabelecer Organóides cólon a partir de uma biópsia do paciente CF
NOTA: Após a recolha de tecido, é importante para manter a amostra em gelo em solução salina, fosfato de Dulbecco tamponado salino sem Ca 2+ e Mg 2+ (DPBS), ou BM. o processamento rápido das biópsias é recomendável, mas provou possível para estabelecer culturas organ�de a partir de biópsias armazenados em gelo durante um máximo de 7 dias.
- Deixe as biópsias assentar no fundo de um tubo cónico de 15 ml e remover o sobrenadante.
- Adicionar 10 ml de DPBS para as biópsias e pipeta cima e para baixo 10-20 vezes utilizando uma pipeta de 10 mL.
NOTA: A pipeta tem de ser pré-humedecido com BM antes de pipetar a biópsia. - Deixe que as biópsias se depositam no fundo e remover o sobrenadante.
- Repita os passos 2.2 e 2.3 4-5 vezes até que o sobrenadante é clara.
- Adicionar 10 ml de DBPS e 200 ul de EDTA (0,5 M) para as biopsias e colocar o tubo no tubo de uma plataforma de balanço durante 60-120 min a 4 ° C.
NOTA: O tempo de incubação pode variar de paciente. Se criptas são liberados, DPBS torna-se turva. incubação EDTA pode ser finalizado quando criptas pode ser observado sob um microscópio. - Permitir que as criptas para resolver. Descartar o sobrenadante.
- Tome-se 2 ml de BM e adicioná-lo para um novo tubo de 15 ml. Agitar este novo tubo manualmente, de tal maneira que o interior é coberto com a BM.
- Usando uma pipeta de pré-humedecidas com a BM, adicionar 2 ml de DPBS para o tubo contendo as biópsias e pipeta-se para baixo e 10-20 vezes.
- Permitir que as biópsias para liquidar e transferir os DPBS com as criptas para o novotubo contendo os 2 ml de BM que foi preparado no passo 2.7.
- Repita os passos 2.8 e 2.9 até que não mais criptas são liberados.
- Rodar as criptas para baixo a 130 xg durante 5 min a 8 ° C.
- Nesse meio tempo, transferir IM para o gabinete de segurança, à temperatura ambiente (RT).
- Descartar o sobrenadante e adicionar 10 ml de BM ao sedimento cripta e repita o passo 2.11.
- Ressuspender o sedimento em 1 ml de BM. Leve 5-10 ul e contar o número de criptas por olho sob um microscópio.
- Rodar as criptas para baixo a 130 xg durante 5 min a 8 ° C.
- Remover o sobrenadante e ressuspender o sedimento em 55% BMM (BMM v para v IM).
NOTA: As criptas são ressuspensas no volume correspondente de 55% a 1 BMM cripta por ul. Se não houver criptas suficientes, o volume mínimo de BMM é de 40 mL. - Para a semeadura, pipeta 35 ul por cavidade (em uma placa de 24 poços). Dividir os 35 ul de BMM em 3-5 gotas separadamente, a fim de melhorar a difusão de growth fatores para a BMM. Não crie bolhas.
- Coloque e deixar a placa de cabeça para baixo na incubadora a 37 ° C durante pelo menos 20 min para o BMM para solidificar.
- Adicionar 500 ul de IM por poço e mantê-lo na incubadora a 37 ° C e 5% de CO 2.
- Refrescar o meio cada 2-3 dias. Remover o meio antigo por pipetagem para fora com uma pipeta P1000, deixando o BMM gotas intacta. Cuidadosamente adicionar FCM pipetando-o ao lado do poço, não directamente sobre o BMM gotas.
NOTA: Se não criptas são liberados no protocolo de isolamento, centrifugar o sobrenadante, lavar o pellet 2-3 vezes com a BM, e ressuspender-lo em BMM. Tome o tecido de sobra e corte-o em pequenos pedaços com uma navalha. Recolha estes para um tubo cónico de 15 ml e centrifugar para clarificação, e ressuspender-los na mesma BMM. Se as células-tronco epiteliais estão presentes, estes também irá gerar Organóides.
3. Passaging de Organóides cólon para Manutenção, congelamento e Paraskolin induzida Inchaço Assay (FIS)
NOTA: Cada cultura organ�de tem seu próprio tempo de duplicação. Normalmente, Organóides CF colorrectal pode ser expandido 1: 3-1: 5 vezes cada 7-10 dias. É um bom sinal se são observadas estruturas de brotamento. Organóides colorrectal CF são menos cística (Figura 2A - 2C) de Organóides colorrectais normais (Figura 2D). Para o estabelecimento e manutenção, Organóides são cultivadas em placas de 24 poços; por congelamento, em placas de 6 poços; e para o ensaio de FIS, em patês de 96 poços.
- Passaging de Organóides
- Manter o BMM em gelo durante pelo menos 30-60 minutos antes de o utilizar.
- Manter a FCM à temperatura ambiente durante pelo menos 1 hr antes de o utilizar.
- Rotular um tubo de 15 ml cônico com o nome da amostra e um outro tubo como "lavado".
- Aspirar cuidadosamente o meio dos poços usando uma pipeta P1000 sem perturbar o BMM gotas.
- Adicionar 1 ml de BM para um bem e break o BMM cai usando uma pipeta P1000. Transferir este 1 ml para o tubo de 15 ml com o nome da amostra.
- Lava-se a bem com mais 1 ml de BM e transferi-lo para o mesmo tubo de 15 ml.
- Repita os passos 3.1.5 e 3.1.6 com mais 5 poços (até 6 poços de uma placa de 24 poços serão lavadas em um tubo de 15 ml).
- Encha o tubo até 12 ml com o BM. Pipeta cima e para baixo usando um pré-humedecido 5 ml pipeta.
- Centrifugação a 85 xg durante 5 min a 8 ° C.
- Descartar o sobrenadante e adicionar 1 ml de MF à pelete. Com a mesma ponta P1000 pipeta, levanta uma ponta P10 sem um filtro, e pipeta cima e para baixo 20 vezes. Descarte P1000 e dicas P10.
- Adicionar 4 ml de BM com uma pipeta de 5 mL e segurar o tubo inclinado em cerca de 70 ° em relação à vertical para um lado. Pré-molhar uma nova ponta P1000 e misture vigorosamente 2-3 vezes com o P1000 (volume 1 ml).
- Conte até 10, permanecendo na posição inclinada, recolher a camada superior com cuidado wom a pipeta P1000, e transferência de 4 x 1 ml para dentro do tubo rotulado como "lavado".
- Observe as Organóides de sedimentação para o fundo no tubo inclinado; Organóides ininterrupto e pedaços maiores vai afundar até o fundo. Centrífuga de 15 ml "lavada" tubo por 5 min a 85 xg e 8 ° C.
- Descartar o sobrenadante e adicionar a quantidade necessária de meio de BMM e ao sedimento organ�de para uma concentração final de 55% de BMM. Misturar por pipetagem cima e para baixo sem criar bolhas (Figura 3B).
NOTA: Uma boa densidade é conseguida por sementeira 25-30 Organóides em 10 ul de BMM. - Siga os passos de 2,17-2,19.
- Passaging para congelamento
- Mantenha o BM no gelo por pelo menos 30-60 min antes do uso. Manter a FCM à temperatura ambiente durante pelo menos 1 hora antes da utilização.
- Prepare FCM suplementado com RhoKi (Passo 1.3.3).
- Aqui tripsina do frigorífico e deixá-la à temperatura ambiente durante pelo menos 30 min antes da utilização.
- Siga os passos 3.1.5-3.1.10.
- Remover tanto sobrenadante quanto possível, adicionar 4 ml de tripsina, e agitar com vortex durante 30 seg.
- Colocar o tubo num banho de água quente a 37 ° C durante 1 min e agitar vigorosamente em vórtice durante 30 seg.
- Inspeccionar a solução no tubo. Se Organóides intactas ainda são visíveis ao microscópio, repita o passo 3.2.7.
- Quando os Organóides são interrompidas, adicionar 8 mL de BM para neutralizar a tripsina e a pipeta de 10 vezes.
- Rotação durante 3 min a 450 xg, a 8 ° C.
- Descartar o sobrenadante e adicionar a quantidade necessária de meio de BMM e aos Organóides para chegar a uma solução de BMM de 55%. Misturar por pipetagem cima e para baixo sem criar bolhas.
NOTA: Para o congelamento, Organóides devem ser inoculadas numa proporção de 1: 1 após tripsinização. - Semente de 250 ul de um único poço de uma placa de 6 poços de cultura de tecidos pré-aquecido, que produzem gotículas separadas, de ~ 10 mL. Colocar a placa de cabeça para baixo na incubadora a 37 ° C e deixar aBMM para solidificar por 20-30 min.
- Adicionar 2,5 ml de FCM fresco + RhoKi em cada placa de 6 poços e assim transferir a placa para a incubadora (Figura 3C).
- Passaging Organóides para o Ensaio FIS
NOTA: Dependendo do número e tamanho dos Organóides, entre 4 e 6 cavidades de uma placa de 24 poços são suficientes para semear 27 cavidades de uma placa de 96 poços.- Processar os Organóides como descrito a partir das etapas 3.1-3.1.13.
- Ressuspender o sedimento em 120 ul de 50% de BMM.
- Confirmar o número de Organóides (30-50) na proporção de 3 ul de BMM gota sob o microscópio.
- Placa os Organóides utilizando uma única gota de 3 ul colocados no meio de cada poço de uma pasta de 96 poços.
- Colocar a placa na incubadora a 37 ° C durante 15 min para a BMM a solidificar; outros passos estão descritos no passo 6.1.1.
4. Colon Congelamento CF Organóides
NOTA: Organoids está pronto para ser congelada até 1-2 dias após tripsinização e de cultura, de modo Organóides ainda será pequeno, o que aumenta a eficiência de sobrevivência após a descongelação.
- Adicionar 1 ml da BM e quebrar a BMM gotas com uma pipeta P1000. Transfira para um tubo de 15 ml.
- Lave o poço com mais 1 ml de BM e transferência para o mesmo tubo de 15 ml.
- Repita os passos 4.1 e 4.2 com todos os poços.
NOTA: Para evitar o excesso de BMM, 3 poços de uma placa de 6 poços são reunidas em um tubo de 15 ml. - Encha o tubo de 15 ml contendo os Organóides com 12 ml de BM frio e pipeta cima e para baixo com uma pipeta de 5 ml. Deixar o tubo em gelo durante 5 min.
- Girar durante 3 min a 450 xg e 8 ° C e remover o sobrenadante.
- Dissolver o sedimento de Organóides com meio de congelamento e pipeta cima e para baixo para voltar a suspender adequadamente os Organóides.
NOTA: 500 ul de meio de congelação é utilizado para cada 100 mL de BMM. - Usando uma pipeta de 5 ml, 0,5 ml de transferirOrganóides novamente suspensas em meio de congelamento de estéreis frascos criogênicos.
- Transferir os frascos para um recipiente de congelação de células e colocá-lo a -80 ° C.
- Após 24 h, transferem os frascos para armazenamento em azoto líquido.
5. Estabelecer culturas de Organóides congelados
NOTA: Descongelar o BMM no gelo e mantê-lo em gelo. Deixe o BM atingir a TA, e aquecer a 10 ml de aliquota a 37 ° C antes de iniciar o procedimento de descongelação um criotubo.
- Descongelar o frasco rapidamente por agitação em um banho de água a 37 ° C até que não é ainda um pouco material congelado.
- Transferir os Organóides descongeladas para um tubo cónico de 15 ml usando uma pipeta P1000.
- Imediatamente depois, adicionar 1 ml de gota a gota BM quente, agitando o fundo do tubo. Uma vez que os 1 ml de meio é adicionado, mistura-se cuidadosamente, pipetando para cima e para baixo algumas vezes para diluir o meio de congelamento.
- Lentamente (gota a gota) adicionar 9 ml de BM quente para a Conta tubo cônicoining os Organóides. Inverta algumas vezes.
- Girar a suspensão de células durante 3 min a 85 xg e 8 ° C.
- Descartar o sobrenadante cuidadosamente, sem perturbar o sedimento. Ressuspender o organóide em 90 ul de FCM suplementadas com RhoKi (passo 1.3.3). Em seguida, adicione 110 mL de BMM.
- Adicionar 35 ul a cada poço de uma placa de 24 poços pré-aquecido, fazendo pequenas gotículas, separadas.
- Transferir a placa à temperatura de 37 ° C incubadora, deixando a placa de cabeça para baixo durante 20-30 min.
- Adicionar 500 ul de FCM com RhoKi a cada poço e transferir a placa de novo na incubadora (Figura 4A - 4C).
- Uma vez Organóides ter recuperado corretamente de descongelamento, diluir em mais BMM assim cada 10 mL de BMM contém 25-30 Organóides. Este procedimento pode ser feito de 2-3 dias após a descongelação (Figura 4D - 4G) e garante o bom crescimento do organ�de.
6. induzida Forskolin-inchaço,dizer (FIS)
NOTA: FSK titulação permite a medição da função residual CFTR. Por modulação de CFTR, Organóides são expostos a uma dada corrector (por exemplo, VX-809) e / ou potenciador (por exemplo, VX-770), dependendo do genótipo. Normalmente, VX-809 é adicionado 18-24 h antes da medição, enquanto que VX-770 e FSK, são adicionados imediatamente antes de iniciar as medições. Estar ciente de que alguns moduladores (correctores / potenciadores) pode ligar-se à superfície de plástico da placa de ensaio.
- Chapeamento para o Ensaio
NOTA: VX-809 existências são aliquotadas a 20 mM e armazenado a -80 ° C. Ao descongelar, deixe à temperatura ambiente e proteger da luz.- Processar os Organóides como descrito na seção 3.3.
- Se o teste de corrector de VX-809, preparar uma curva de dose-resposta em triplicado com as seguintes concentrações: 0,0003, 0,003, 0,03, 0,3, 3,0, e 30 fiM. Prepare as diluições em FCM.
- Para a placa de 96 poços, quer adicionar 100 μ; L de FCM com as respectivas concentrações ou 100 pi de VX-809 FCM única e incubar a placa.
- Medindo o Ensaio
NOTA: VX-770 existências são aliquotadas a 20 mM, enquanto Fsk é a 10 mM; ambos são armazenadas a -80 ° C. Ao descongelar, deixe à temperatura ambiente e proteger da luz.- Tomar um frasco de calceína e DMSO e deixar à temperatura ambiente durante 15 min.
- Adicionar 5,1 mL de DMSO para o frasco onde a calceina é fornecido como um pó, se fechada. Caso contrário, utilizar um frasco de calceína já ressuspensas contendo 2,5 ul de calceína.
- Adicionar 2,5 ul de calceína com 580 ul de BM em um tubo de 1,5 ml e rotulá-la.
- Adicionar 10 ul desta solução corante (BM + calceína) para cada poço utilizando uma pipeta de repetição.
- Ressuspender uma vez com uma multicanal para garantir que o corante é bem misturado.
- Incubar a placa numa incubadora a 37 ° C durante 30 min.
- Durante a incubação calceína, começar a preparar a Fske soluções de VX-770, se necessário.
- Se usar um potenciador de VX-770, preparar uma curva de dose-resposta, em triplicado, com as seguintes concentrações: 0,0003, 0,003, 0,03, 0,3, 3,0, e 30 fiM. No caso de uma titulação Fsk, as concentrações são: 0, 0,008, 0,02, 0,05, 0,12, 0,32, 0,8, 2,0, e 5,0 uM. Preparar diluições em BM.
NOTA: FSK, VX-770, ou qualquer outro fármaco adicionado no segundo dia, as diluições devem ser preparados numa concentração final de 2 x, uma vez que 100 ul de Fsk solução / titulação da droga serão adicionados a cada poço, os quais já contêm 100 ul da FCM. - Transfira a Fsk e VX-770 soluções, uma pipeta p200, e dicas para a sala de microscópio.
- Para imagiologia do ensaio de FIS, usar um microscópio confocal de imagens de células vivo equipado com um estágio automatizado, uma câmara aquecida, e o fluxo de CO 2.
NOTA: Os passos seguintes referem-se a um microscópio específico. Diferentes configurações devem ser aplicadas a outros microscópios seguinte fabricanteinstruções. - Colocar a placa de 96 poços no suporte da placa.
- Insira as configurações confocal para a imagem latente.
- Predefinir a ferramenta de imagem ao vivo para 37 ° C e 5% de CO 2 e deixar a câmara de pré-incubar durante um mínimo de 30 minutos antes da medição.
- Use a opção "setup inteligente" para selecionar a faixa Alexa fluor-488.
- Ajuste a lente 5X e área de digitalização para 0,6x para diminuir o zoom e capturar todo o bem.
- Adaptar a sensibilidade potência do laser e um detector para permitir a detecção ideal de Organóides rotulados calce�a-verde sobre o fundo. O orifício pode ser aumentada para 130 um e a média da imagem pode ser fixado em duas.
- Defina a profundidade de bits de 8 e o tamanho do quadro de 512 x 512.
- Use a opção de séries temporais para definir a medição do tempo, frequência e intervalos.
NOTA: Sugerido para medições regulares: 1 hora com 10 min de intervalo: ciclos = 7 (ciclo 1 é T = 0). Para as medições do inchaço reduzida, Organoids podem ser visualizados por até 3 horas. - Use a opção de telha para determinar manualmente as posições bem individuais.
- Adicionar 100 ul da Fsk e / ou VX-770 soluções para os poços correspondentes, seguindo o mesmo fim como a medição. Começar a adicionar as soluções na primeira fotografada bem e continuar com a ordem de imagem.
- Inicie a medição.
- Após o experimento for concluído, salve o arquivo.
- Análise do FIS Ensaio de Dados
- Criar uma macro "análise organ�de" para a análise dos dados do ensaio de FIS usando a ferramenta de análise em um software de análise de imagem que reconhece todas as estruturas fotografadas através da faixa de Alexa-488 e preenche as estruturas identificadas para calcular o aumento da área total organ�de através da diferentes pontos de tempo.
- Abra o arquivo de dados com as imagens adquiridas no programa de análise de imagem.
- Seleccione a macro para análise organ�de.
- Definir o limiar para equilibrar a relação sinal-ruído de um poço no ponto 1 hora e assegurar que todas as estruturas organ�de são reconhecidos e preenchido.
- Verifique em 4-6 poços para ver se todas as estruturas também são reconhecidos no ponto 7. tempo de modificar ligeiramente o limiar para garantir que os sinais de fundo no ponto 7 do tempo não são reconhecidos como estruturas (o limite específico pode variar um pouco entre os experimentos).
- Defina os critérios de tamanho dos objetos reconhecidos mínima área a 1.000 mm 2.
- Pressione o botão "Analisar" para iniciar. A análise leva aproximadamente 3 minutos, dependendo do software utilizado.
- Quando o software estiver concluída, vá para "criar a tabela" e selecione os seguintes dados: bem os números (tabela deve aumentar nesta ordem), os pontos de tempo e área total por poço.
- Salve o arquivo como um .xlm para exportar para um programa de planilha.
- Neste programa, calcular o aumento relativo na área por well, definindo a área de ponto de 1 hora a 100%. Calcula-se a área sob a curva (AUC) a partir de 1-7 pontos de tempo por condição; o limite inferior da zona (Y-valor) é fixado em 100%. FSK ou drogas titulações (eixo X) são representados graficamente contra a AUC (eixo Y).
Resultados
A Figura 1A mostra um isolamento fresco representante da criptas incorporados em BMM. As criptas são a partir de uma biópsia de um sujeito colorrectal CF. Normalmente, um organ�de é gerado a partir de cada cripta (Figura 1A - C). Devido à disfunção da CFTR, a maioria dos Organóides cólon CF não são cística, mas sim são compactos e com projecções e brotos (Figura 2A - 2B). No entanto, alguns CF organ�de culturas, especialmente com elevada função residual, tem algumas Organóides com uma forma cística (Figura 2C), como culturas de tipo selvagem organ�de (Figura 2D).
Antes de passagem das Organóides para a expansão da cultura de sementeira ou num ensaio de FIS, é importante que os Organóides têm um grande tamanho com múltiplos germinações, como mostrado na Figura 3A. Se os Organóides são pequenos e sem ngerminações umerous quando processados para passaging, a cultura organ�de é afetada negativamente. Dependendo da qualidade e da actividade dos factores de crescimento essenciais, como EGF, Wnt-3A, e Rspo3, os Organóides atingir o tamanho desejado entre 7 e 12 dias (Figura 3A). Após a ruptura mecânica, os brotos são rompidas e usadas para gerar novos Organóides na seguinte passagem (Figura 3B). Se o processamento dos Organóides para congelamento, é importante que eles são tripsinizadas para um tamanho pequeno, como representado na Figura 3C. Após tripsinização, as Organóides são banhados por 1 ou 2 dias, a fim de deixá-los recuperar do stress da manipulação. Este passo, juntamente com o pequeno tamanho das Organóides, assegura uma recuperação de células 98% após o descongelamento (Figura 4A).
Quando os Organóides são descongeladas, é importante ter-los em alta densidade, portanto, normalmente, eles são descongeladas numpequeno volume (Figure4A). Depois de um ou dois dias em cultura, e depois de observar que as Organóides estão a aumentar de tamanho (comparar com a figura 4A com a Figura 4B - 4C), os Organóides são diluídos numa proporção de 20-30 Organóides por 10 ul de BMM, proporcionando a densidade direita para crescer em um tamanho maior. Se os Organóides são demasiado diluída, eles podem retardar o crescimento e pode mesmo diferenciar e morrer. Se os Organóides são demasiado cheio, a falta de espaço ou a falta de factores de crescimento também retarda o crescimento dos Organóides e reduz o número de brotos.
O chapeamento de Organóides de culturas viáveis com restos celulares limitado deve resultar em condições em que> 95% das Organóides incham após estimulação Fsk, desde que a função de CFTR suficiente está presente (Figura 5A - 5B). Organóides inchar de uma forma genótipo e fármaco-dependentes, comoilustrada por imagens representativas de Organóides com dois alelos F508del (Figura 5A) e o composto Organóides heterozigóticos para F508del e S1251N (Figura 5B), uma mutação de CFTR de propagação associado com alguma função residual.
Para quantificar inchaço, as áreas de superfície total de calceina-verde são seleccionados para cada ponto de tempo e expressos como percentagem de T = 0 (fixado em 100%; Figura 6A). Detritos e estruturas pequenas, não intumescentes são tipicamente abaixo de 5% da área total da superfície. O aumento da área relativa é expressa por intervalo de tempo de 10 min, e AUC (unidades arbitrárias) medições são gerados para cada condição (t = 0 a 60 min, limiar da linha de base fixado em 100%; Figura 6B). Encontrámos AUC para ser o mais robusto, uma vez que incorpora alguma variação na iniciação de inchaço, bem como uma relação curvilínea para além de 30-40 min FSK a níveis de função alta CFTR.
medições função residual em F508del / Organóides F508del geralmente atingem 0-200 unidades AUC (100-110% do aumento de área de superfície após 60 min de 5 mM tratamento Fsk) , o que pode aumentar para ~ 2,500-3,500 unidades AUC após incubação com moduladores de CFTR (VX770 + VX809; Figura 6C). Organóides associados com a função de CFTR residual pode atingir até 4.500 unidades AUC após 60 min de 5 uM estimulação Fsk na ausência de moduladores de CFTR (área superficial de 200-220% de condições pré-FSK). inchaço organ�de atinge um teto em ~ 4.500 unidades AUC, presumivelmente devido às limitações físicas das estruturas organ�de, o impacto limitante da taxa de transporte de íons basolateral, eo estabelecimento de homeostase de íons e fluido de transporte em condições "esticada". FSK pode ser titulada para expandir ainda mais a gama dinâmica do ensaio a estes níveis elevados de função residual CFTR para melhor quantificar a função residual ou altamente eficaz tratamento com o composto (por exemplo, tal como indicado pela maior actividade de VX770 no inchaço de Organóides S1251N após estimulação com concentrações mais baixas FSK; Figura 6D).

Figura 1: Estabelecimento de CF Organóides colorretais de biópsias. (A) Imagens representativas de material isolado a partir de uma biópsia retal depois de ser incorporado em BMM no dia de isolamento (passagem 0, dia 0). Alargamento da cripta indicado é mostrado no painel inferior direito. (B) O mesmo criptas foram seguidos após 7 dias em cultura (passagem 0, dia 7). O alargamento da mesma cripta apresentados no painel A é mostrado. (C) Imagem representativa da mesma cultura organ�de 11 dias depois de ser split (passagem 1, dia 11). Barras de escala = 100 pm.
159fig1large.jpg "target =" _ blank "> Clique aqui para ver uma versão maior desta figura.

Figura 2: Imagens representativas de Organóides colorretais CF derivadas de indivíduos com diferentes mutações CFTR. Imagens representativas de CF Organóides colorretais de indivíduos com F508del / F508del (A), F508del / R117H-T7 (B), e F508del / S1251N mutações (C). (D) Imagem representativa de uma cultura organ�de colorectal de um sujeito do tipo selvagem CFTR. Barras de escala = 100 pm. Estas imagens foram obtidas sem estimulação Fsk. Por favor clique aqui para ver uma versão maior desta figura.
5159 / 55159fig3.jpg "/>
Figura 3: Processamento Organóides cólon CF de manutenção e de ensaio ou para congelamento. (A) Imagens representativas de uma cultura organ�de CF cólon pronto para ser processado para qualquer passaging (B) ou de congelação (C). (B) Após a sua ruptura mecânica, pequenos pedaços são formados, o que irá gerar os novos Organóides na próxima passagem. (C) Após tripsinização, muito pequenas, Organóides redondos são geradas, facilitando a sua viabilidade durante o processo de congelamento. Barras de escala = 100 pm. Por favor clique aqui para ver uma versão maior desta figura.
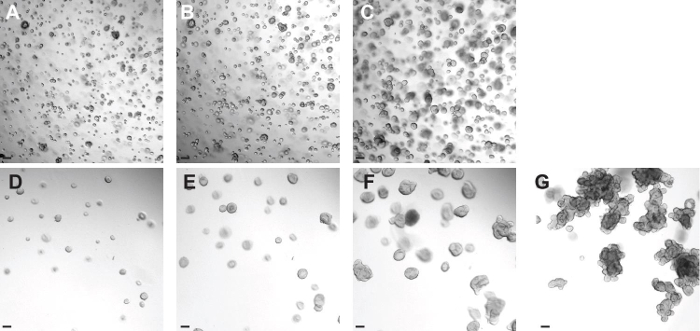
Figura 4: Estabelecer uma cultura organ�de colorectal CF de Organóides congelados. ( A - C) Imagens representativas de uma cultura organ�de colorrectal CF descongeladas no dia 0 (A). As imagens do mesmo poço foram levados um (B) e dois (C) dias após. (D - G) Imagens representativas da etapa de diluição descrito na secção 5.9. Uma vez que os Organóides ter recuperado corretamente de descongelamento (dia 3 após o descongelamento), eles são diluídos para que eles tenham espaço para crescer (D). Imagens da mesma cavidade foram tomadas seis (E), dez (F), e (C) quinze dias após a descongelação. Barras de escala = 100 pm. Por favor clique aqui para ver uma versão maior desta figura.

Figura 5: inchaço induzido por forscolina de CFOrganóides. (A e B) Imagens representativas de F508del / F508del (A) ou F508del / S1251N (B) Organóides colorectal antes ou após 60 minutos de estimulação com FSK (5 ^ M) na ausência ou na presença de VX-770 (3 uM]) ou VX-770 em combinação com o VX-809 (3 uM). Barras de escala = 200 pm. Por favor clique aqui para ver uma versão maior desta figura.
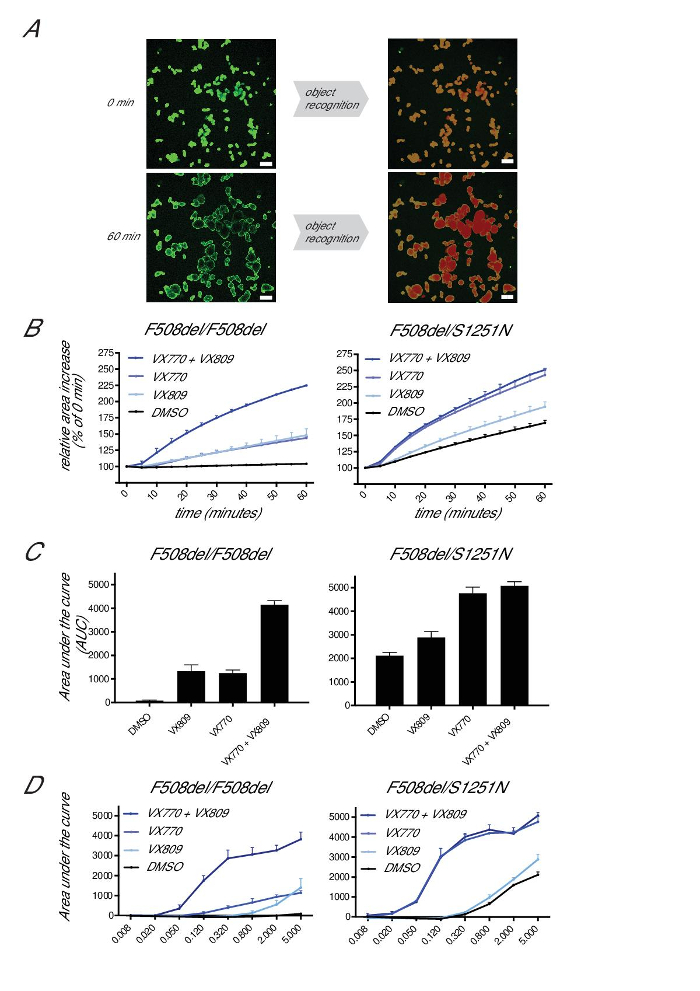
Figura 6: inchaço Quantificação Forskolin-induzida. (A) Imagens representativas de selecção da área de uma imagem organ�de por software de análise de F508del / S1251N Organóides antes (0 min) e após 60 minutos de estimulação com FSK (5 uM) e VX770 (3 uM). Barras de escala = 200 pm. (B) Represtante de imagens do aumento de F508del / F508del ou F508del Organóides / S1251N Área Relativa durante 60 min de FSK (5 uM) a estimulação na ausência ou na presença de VX770 (3 uM) e / ou VX809 (3 uM). (C) Área sob a curva de medições condições indicadas em (B) (t = 60 min, da linha de base = limiar de 100%). (D) a área sob a curva de medições F508del / F508del ou Organóides F508del / S1251N em diferentes concentrações de Fsk. Os dados representam as médias ± SD de experiências representativas individuais. Por favor clique aqui para ver uma versão maior desta figura.
Discussão
Aqui, nós fornecemos um protocolo completo para a geração, a expansão, o congelamento e descongelamento das Organóides colorectal humanos. Enquanto nós estabelecemos culturas organ�de humanos há algum tempo atrás 17, tem por vezes sido difícil para estabelecer a tecnologia em outros laboratórios, sem treinamento prático. Prevemos que esses protocolos irá substituir essa formação.
-Wnt-3A meio condicionado é um dos reagentes mais importantes para ter sucesso no estabelecimento e manutenção de um organ�de cultura de longo prazo. Na verdade, as culturas organ�de pode "crash" quando expostos ao meio Wnt-3A-conditoned com baixa atividade. Desde médio Wnt-3A-condicionado é feito em casa, há vários aspectos que devem ser levados em consideração ao gerar um meio ativo. Activo de Wnt-3A só podem ser produzidos em meio com soro fetal de bovino de alta qualidade (FBS) que fornece os sinais de crescimento adequado para as células L e à estabilização das hidrofóbicomoléculas de Wnt-3-A. Quando a atividade Wnt-3A é baixa (ou seja, Low Top rácios / FOP, veja abaixo), é geralmente os FBS que está causando o problema.
Comercial Wnt recombinante funciona mal, por isso não recomendo usá-lo como controle positivo para o ensaio repórter TOP / FOP Wnt. A relação entre a parte superior / Renilla e FOP / Renilla é uma indicação da actividade de Wnt do meio condicionado, de modo que uma boa lote de meio de Wnt-3a-condicionado dá uma proporção TOP / FOP superior a 25, em comparação com o valor de cima / FOP de o controlo negativo: meio não expostos a Wnt-produzindo-3A células. Noggin recombinante e R-espondina pode ser substituído por Noggin e R-espondina com ar-meio 28, 29.
O protocolo atual também descreve um teste funcional para CFTR-ensaio FIS. Recentemente, demonstrou a relação entre o genótipo CFTR e FIS e como este reflecte genoty CFTR publicadarelações pe-fenótipo obtidos a partir de registros clínicos (www.CFTR2.org) 25. Usando este ensaio, foram identificados dois indivíduos com mutações CFTR extremamente raros cuja Organóides respondiam ao ivacaftor (VX-770) 25. subsequente prescrição desta droga resultou em resposta clínica clara, evidenciando o valor do ensaio FIS para coincidir com medicamentos específicos com pacientes com mutações raras na ausência de dados de ensaios clínicos. Essencial para a quantificação da FIS são condições de crescimento e de ensaio óptimas, indicados apenas por uma fracção limitada de Organóides não intumescentes (normalmente inferior a 5%). Altos níveis de chumbo detritos à subestimação de inchaço, como uma maior proporção de não-viáveis, estruturas não intumescentes são reconhecidos pelo software de análise de imagem.
Correlações entre in vitro respostas FIS e biomarcadores dependente do CFTR previamente estabelecidos (concentração de cloreto no suor e intestmedições de corrente Inal) no nível personalizado foram prontamente demonstrável em nossos estudos anteriores 19, 25. Este apoiou a noção de que as medidas funcionais residuais utilizando FIS em indivíduos com CF podem complementar as abordagens atuais como marcador diagnóstico ou prognóstico de uma forma personalizada. O rendimento do ensaio FIS em comparação com outros biomarcadores da função CFTR, tais como medições da concentração de cloro no suor in vivo e medições de corrente intestinais em ex vivo da biópsia retal, permite um melhor controle da variabilidade técnica. Ele também fornece uma leitura totalmente CFTR-dependente e uma grande faixa dinâmica usando uma titulação de Fsk que precisamente os tipos de função CFTR residual.
No entanto, o ensaio de FIS reflecte apenas o impacto do genótipo individual sobre a variabilidade da eficácia do medicamento, enquanto que a modulação da doença CF é afectada por mais do que única função de CFTR. para Drug resposta, o ensaio é o reflexo de uma resposta do tecido potencial. Embora muito preciso na medição de CFTR, variação humana na farmacocinética não é incorporado, em oposição a outros in vivo, 7, 8 ou ex vivo do gene CFTR medições directas 32. Como discutido anteriormente, modificadores CF não (genéticos e ambientais) também estão influenciando fenótipo, causando uma desconexão entre observações in vitro ou biomarcadores CFTR e fenótipo clínico 2. Além disso, a identificação de mutações que respondem potenciais utilizando linhas celulares 33 está associada com menos impacto sobre os pacientes que precisam de obter uma biópsia retal para o estabelecimento de Organóides.
Múltiplas drogas-alvo CFTR estão atualmente em desenvolvimento 1. Prevê-se que os ensaios clínicos não irá permitir uma previsão da eficácia clínica correcta bduziu no estado mutacional CFTR sozinho. À medida que o ensaio mede a função de CFTR FIS e funcionalmente a resposta à droga, pode tornar-se o método de escolha para determinar qual o fármaco funciona melhor para os quais paciente. O ensaio FIS podem também ser úteis para a identificação de grupos de pacientes a serem incluídos em ensaios de registo e para o desenvolvimento de novas modalidades de droga. Estimulação da Organóides colorretais com plasma antes e durante o tratamento pode ajudar ainda mais para quantificar valores funcionais circulantes de moduladores de CFTR no sangue, potencialmente facilitando a dosagem personalizada e a seleção de doses de droga em ensaios clínicos 30, 31. Finalmente, a FIS pode ser útil para uma melhor compreensão básica da função de CFTR e as suas interacções com outros modificadores genéticos -SO muito largamente unknown- de sua função.
Divulgações
Hans Clevers is an inventor on patents for organoid culture and the Forskolin-induced swelling assay. Jeffrey M Beekman is an inventor on a patent for the Forskolin-induced swelling assay. Sylvia F Boj and Robert Vries are employed by the Foundation Hubrecht Organoid Technology (HUB), which holds the exclusive license to the Organoid Technology. Otherwise, the authors have nothing to disclose.
Agradecimentos
Este trabalho foi apoiado pelo programa HIT-CF dos holandeses CF fundação (CNSF), ZonMW (40-00812-98-14103), Fundo de Investigação Hospital Infantil de Wilhelmina e CZ, e Zilverenkruis / Achmea. Nós gostaríamos de agradecer a S. Heida-Michel, M. Geerdink, KM de Winter-de Groot, e G. Berkers (Departamento de Pneumologia Pediátrica, Hospital de Wilhelmina Children, UMC Utrecht), e RHJ Houwen (Departamento de Gastroenterologia Pediátrica, Wilhelmina Hospital infantil, UMC Utrecht) para abordar os pacientes e recebendo as biópsias para a geração de um CF Biobank.
Materiais
| Name | Company | Catalog Number | Comments |
| Advanced Dulbecco’s Modified Eagles Medium with Nutrient Mixture F-12 Hams (Ad-DF) 500ml | Thermo Fisher Scientific: Invitrogen | #12634 | stored at 4 °C |
| GlutaMax | Thermo Fisher Scientific: Invitrogen | #35050 | stored at 4 °C |
| Hepes | Thermo Fisher Scientific: Invitrogen | # 15630-056 | stored at 4 °C |
| Penicillin/Streptomycin | Thermo Fisher Scientific: Invitrogen | #15140-122 | stored at -20 °C |
| 96 well culture plate | Cellstar | #655180 | |
| 24 well culture plate | Cellstar | #662160 | |
| 6 well culture plate | Cellstar | #657160 | |
| Dulbecco's Phosphate Buffered Saline (-) CaCl2 (-) MgCl2) (DPBS) | Life Technologies: Gibco | #14190-094 | stored at 4 °C |
| Dulbecco’s Modified Eagles Medium (DMEM) 500ml | Thermo Fisher Scientific: Invitrogen | #31966-021 | For Wnt-3A Conditioned Medium Production. Stored at 4 °C |
| Fetal Bovine Serum (FBS) | Bovogen | #SFBS LOT#11113 | For Wnt-3A Conditioned Medium Production. Stored at -20 °C |
| L Wnt3A cell line | ATCC | #CRL-2647 | For Wnt-3A Conditioend Medium Production. |
| TOP/FOP plasmids | Millipore | #17-285 | For measuring Wnt activity |
| pTK-Renilla | Promega | #E2241 | For measuring Wnt activity |
| HEK-293 | ATCC | #CRL-1573 | For measuring Wnt activity |
| Dual-Luciferase Reporter Assay System | Promega | #E1910 | For measuring Wnt activity |
| Zeocin | Thermo Fisher Scientific: Invitrogen | #R250-01 | For Wnt-3A Cell line selection |
| B27 supplement | Thermo Fisher Scientific: Invitrogen | #17504-044 | stored at -20 °C |
| N-Acetylcysteine | Sigma Aldrich | #A9165-5G | stored at -20 °C |
| Nicotinamide | Sigma Aldrich | #N0636 | stored at -20 °C |
| Human Epithelial Growth Factor (hEGF) | PrepoTech | #AF-100-15 | stored at -20 °C |
| Gastrin | Sigma Aldrich | #G9145 | stored at -20 °C |
| TGFb type I Receptor inhibitor (A83-01) | Tocris | #2939 | stored at -20 °C |
| Y-27632 dihydrochloride (RhoKi) | Selleckchem | #S1049 | stored at -20 °C |
| p38 MAPK inhibitor (p38i) (SB202190) | Sigma Aldrich | #S7067 | stored at -20 °C |
| Primocin | InvivoGen | #ant-pm-1 | stored at -20 °C |
| Human Noggin (hNoggin) | PrepoTech | #120-10C | stored at -20 °C |
| Human R-spondin 3 (hRspo-3) | R&D Systems | #3500-RS/CF | stored at -20 °C |
| Vancomycin | Sigma Aldrich | #861987- 250mg | stored at -20 °C |
| Gentamycin | Life Technologies: Gibco | #15710-049 | stored at -20 °C |
| Ethylenediamine tetraacetic acid (EDTA) | Sigma Aldrich | #431788 | Stored at 4 °C |
| Matrigel | Corning | #354230 | stored at -80 °C |
| TryplE Express | Life Technologies: Gibco | #12605-010 | for trypsinizing organoids for freezing |
| Recovery Cell Culture Freezing Medium | Life Technologies: Gibco | #12648010 | for freezing |
| Calcein | Life Technologies: Gibco | #C3100MP | stored at -20 °C |
| Forskolin | R&D Systems | #1099-50 mg | stored at -80 °C |
| Lumacaftor (VX-809) | Selleckchem | #s1565 | stored at -80 °C |
| Ivacaftor (VX-770) | Selleckchem | #s1144 | stored at -80 °C |
| Name of Reagents/Material | Solvent | Stock Concentration | Final Concentration |
| GlutaMax | 200 mM | 2m M | |
| Hepes | 1 M | 10 mM | |
| Penicillin/Streptomycin | 10K U/ml 10K µg/ml | 100 U/ml 100 µg/ml | |
| Zeocin | 100 mg/ml | 125 µg/ml | |
| B27 supplement | 100 x | 1 x | |
| N-Acetylcysteine | MiliQ H20 | 500 mM | |
| Nicotinamide | DPBS | 1 M | 10 mM |
| Human Epithelial Growth Factor (hEGF) | DPBS 0.1%BSA | 0.5 mg/ml | 50 ng/ml |
| Gastrin | DPBS | 100 µM | 10 nM |
| TGFb type I Receptor inhibitor (A83-01) | DMSO | 5 mM | 500 nM |
| Y-27632 dihydrochloride (RhoKi) | DMSO | 10 mM | 10 µM |
| p38 MAPK inhibitor (p38i) (SB202190) | DMSO | 30 mM | 10 µM |
| Primocin | 50 mg/ml | 100 µg/ml | |
| Human Noggin (hNoggin) | DPBS 0.1%BSA | 100 µg/ml | 100 ng/ml |
| Human R-spondin 3 (hRspo-3) | varies per lot | 300 ng/ml | |
| Vancomycin | 10 mg/ml | 50 µg/ml | |
| Gentamycin | 10 mg/ml | 50 µg/ml | |
| Ethylenediamine tetraacetic acid (EDTA) | MiliQ H20 | 0.5 M | 2 mM |
| Calcein | DMSO | 10 µg/ml | 3.3 ng/ml |
| Forskolin | DMSO | 10 mM | variable |
| Lumacaftor (VX-809) | DMSO | 20 mM | variable |
| Ivacaftor (VX-770) | DMSO | 20 mM | variable |
Referências
- De Boeck, K., Amaral, M. D. Progress in therapies for cystic fibrosis. Lancet Respir Med. 4 (8), 662-674 (2016).
- Cutting, G. R. Cystic fibrosis genetics: from molecular understanding to clinical application. Nature Rev Genet. 16 (1), 45-56 (2015).
- Sosnay, P. R., Siklosi, K. R., et al. Defining the disease liability of variants in the cystic fibrosis transmembrane conductance regulator gene. Nature Genet. 45 (10), 1160-1167 (2013).
- Zielenski, J. Genotype and phenotype in cystic fibrosis. Respiration. 67 (2), 117-133 (2000).
- Van Goor, F., Hadida, S., et al. Rescue of CF airway epithelial cell function in vitro by a CFTR potentiator, VX-770. Proc Natl Acad Sci U.S.A. 106 (44), 18825-18830 (2009).
- Van Goor, F., Hadida, S., et al. Correction of the F508del-CFTR protein processing defect in vitro by the investigational drug VX-809. Proc Natl Acad Sci U.S.A. 108 (46), 18843-18848 (2011).
- Accurso, F. J., Rowe, S. M., et al. Effect of VX-770 in persons with cystic fibrosis and the G551D-CFTR mutation. N Engl J Med. 363 (21), 1991-2003 (2010).
- Ramsey, B. W., Davies, J., et al. A CFTR potentiator in patients with cystic fibrosis and the G551D mutation. N Engl J Med. 365 (18), 1663-1672 (2011).
- De Boeck, K., Munck, A., et al. Efficacy and safety of ivacaftor in patients with cystic fibrosis and a non-G551D gating mutation. J Cyst Fibros. 13 (6), 674-680 (2014).
- Boyle, M. P., Bell, S. C., et al. A CFTR corrector (lumacaftor) and a CFTR potentiator (ivacaftor) for treatment of patients with cystic fibrosis who have a phe508del CFTR mutation: a phase 2 randomised controlled trial. Lancet Respir Med. 2 (7), 527-538 (2014).
- Wainwright, C. E., Elborn, J. S., et al. Lumacaftor-Ivacaftor in Patients with Cystic Fibrosis Homozygous for Phe508del CFTR. N Engl J Med. 373 (3), 220-231 (2015).
- Van Goor, F., Yu, H., Burton, B., Hoffman, B. J. Effect of ivacaftor on CFTR forms with missense mutations associated with defects in protein processing or function. J Cyst Fibros. 13 (1), 29-36 (2014).
- Neuberger, T., Burton, B., Clark, H., Van Goor, F. Use of primary cultures of human bronchial epithelial cells isolated from cystic fibrosis patients for the pre-clinical testing of CFTR modulators. Methods Mol Biol. 741, 39-54 (2011).
- Randell, S. H., Fulcher, M. L., O'Neal, W., Olsen, J. C. Primary epithelial cell models for cystic fibrosis research. Methods Mol Biol. 742, 285-310 (2011).
- Karp, P. H., Moninger, T. O., et al. An in vitro model of differentiated human airway epithelia. Methods for establishing primary cultures. Methods Mol Biol. 188, 115-137 (2002).
- Sato, T., Vries, R. G., et al. Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche. Nature. 459 (7244), 262-265 (2009).
- Sato, T., Stange, D. E., et al. Long-term expansion of epithelial organoids from human colon, adenoma, adenocarcinoma, and Barrett's epithelium. Gastroenterology. 141 (5), 1762-1772 (2011).
- Clevers, H. Modeling development and disease with Organoids. Cell. 165 (7), 1586-1597 (2016).
- Dekkers, J. F., Wiegerinck, C. L., et al. A functional CFTR assay using primary cystic fibrosis intestinal organoids. Nature Med. 19 (7), 939-945 (2013).
- Dekkers, J. F., van der Ent, C. K., Beekman, J. M. Novel opportunities for CFTR-targeting drug development using organoids. Rare Diseases. 1 (1), e27112 (2014).
- Servidoni, M. F., Sousa, M., et al. Rectal forceps biopsy procedure in cystic fibrosis: technical aspects and patients perspective for clinical trials feasibility. BMC gastroenterology. 13, 91 (2013).
- Ommen, D. D. Z. -. V., Vijftigschild, L. A. W., et al. Limited premature termination codon suppression by read-through agents in cystic fibrosis intestinal organoids. J Cyst Fibros. 15 (2), 158-162 (2016).
- Dekkers, J. F., Gogorza Gondra, R. A., et al. Optimal correction of distinct CFTR folding mutants in rectal cystic fibrosis organoids. Eur Respir J. , (2016).
- Dekkers, J. F., Van Mourik, P., et al. Potentiator synergy in rectal organoids carrying S1251N, G551D, or F508del CFTR mutations. J Cyst Fibros. , (2016).
- Dekkers, J. F., Berkers, G., et al. Characterizing responses to CFTR-modulating drugs using rectal organoids derived from subjects with cystic fibrosis. Sci Transl Med. 8 (344), 344ra84 (2016).
- Li, H., Sheppard, D. N., Hug, M. J. Transepithelial electrical measurements with the Ussing chamber. J Cyst Fibros. 3, 123-126 (2004).
- Sheppard, D. N., Carson, M. R., Ostedgaard, L. S., Denning, G. M., Welsh, M. J. Expression of cystic fibrosis transmembrane conductance regulator in a model epithelium. Am J Physiol. 266 (4 Pt 1), L405-L413 (1994).
- Farin, H. F., van Es, J. H., Clevers, H. Redundant sources of Wnt regulate intestinal stem cells and promote formation of Paneth cells. Gastroenterology. 143 (6), 1518-1529 (2012).
- Drost, J., et al. Organoid culture systems for prostate epithelial and cancer tissue. Nat Protoc. 11 (2), 347-358 (2016).
- Vijftigschild, L. A. W., Berkers, G., et al. β2-adrenergic receptor agonists activate CFTR in organoids and subjects with cystic fibrosis. Eur Respir J. 48 (3), 768-779 (2016).
- Dekkers, R., et al. A bioassay using intestinal organoids to measure CFTR in human plasma. J Cyst Fibros. 14 (2), 178-181 (2015).
- Graeber, S. Y., et al. Intestinal Current Measurements Detect Activation of Mutant CFTR in Patients with Cystic Fibrosis with the G551D Mutation Treated with Ivacaftor. Am J Respir Crit Care Med. 192 (10), 1252-1255 (2015).
- Van Goor, F., et al. Ivacaftor potentiation of multiple CFTR channels with gating mutations. Journal of Cystic Fibrosis: Official Journal of the Eur Cyst Fibrosis. 11 (3), 237-245 (2012).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados