Method Article
Forskoline induite par Gonflement dans Intestinal organites: Un
Dans cet article
Résumé
This protocol describes an assay for measuring CFTR function and CFTR modulator responses in cultured tissue from subjects with cystic fibrosis (CF). Biopsy-derived intestinal organoids swell in a cAMP-driven fashion, a response that is defective (or strongly reduced) in CF organoids and can be restored by exposure to CFTR modulators.
Résumé
Recently-developed cystic fibrosis transmembrane conductance regulator (CFTR)-modulating drugs correct surface expression and/or function of the mutant CFTR channel in subjects with cystic fibrosis (CF). Identification of subjects that may benefit from these drugs is challenging because of the extensive heterogeneity of CFTR mutations, as well as other unknown factors that contribute to individual drug efficacy. Here, we describe a simple and relatively rapid assay for measuring individual CFTR function and response to CFTR modulators in vitro. Three dimensional (3D) epithelial organoids are grown from rectal biopsies in standard organoid medium. Once established, the organoids can be bio-banked for future analysis. For the assay, 30-80 organoids are seeded in 96-well plates in basement membrane matrix and are then exposed to drugs. One day later, the organoids are stained with calcein green, and forskolin-induced swelling is monitored by confocal live cell microscopy at 37 °C. Forskolin-induced swelling is fully CFTR-dependent and is sufficiently sensitive and precise to allow for discrimination between the drug responses of individuals with different and even identical CFTR mutations. In vitro swell responses correlate with the clinical response to therapy. This assay provides a cost-effective approach for the identification of drug-responsive individuals, independent of their CFTR mutations. It may also be instrumental in the development of future CFTR modulators.
Introduction
CF est causée par des mutations dans le gène régulateur de la conductance transmembranaire de la fibrose kystique (CFTR) qui code pour un canal anionique épithéliale. CF touche environ 85.000 personnes dans le monde 1. Plus de 2000 mutations du gène CFTR ont été identifiées ( www.genet.sickkids.on.ca ). Cette diversité explique en partie un large spectre de phénotypes de la maladie observés ( www.CFTR2.org ) 2, 3. Six classes de mutations du gène CFTR sont définies en fonction de leur effet sur l'expression et la fonction de la protéine CFTR: (I) pas de synthèse, (II) avec facultés affaiblies le trafic, (III) canal défectueux gating, (IV) conductance modifié, (V) les niveaux de normalement réduite fonctionnant CFTR et (VI) ayant une déficience cellulaire stabilité de la surface 4. Bien que les mutations du gène CFTR communes sont bien étudiés, la fonction CFTR et relation avec l'état clinique restent poorly compris au niveau de l'individu, en particulier pour le grand groupe de rares "orphelines" mutations ( www.CFTR2.org ) 1, 3.
Récemment, les médicaments ont été développés qui ciblent la protéine CFTR de manière spécifique à la mutation. Deux classes de CFTR médicaments protéiques de ciblage sont actuellement en usage clinique et ont des modes d'action distincts. Potentialisateurs, tels que le VX-770, d' améliorer l'open-probabilité de CFTR mutant apicale-localisé et agissent directement sur leur addition aux cellules 5. Correcteurs, tels que le VX-809, restaurer le trafic de endoplasmique misfolded CFTR réticulum localisée et nécessitent une pré-incubation avec des cellules avant que les effets sont observés 6. Le potentialisateur de CFTR, le VX-770, a été enregistrée pour les sujets atteints de la mutation G551D 7, 8, ainsi que pour les huit autresCFTR gating mutations, y compris S1251N 9; ensemble, ces mutations sont portés par 5% de tous les sujets des FC. D' autres essais cliniques ont indiqué que le VX-770, combiné avec le correcteur VX-809, a des effets limités mais significatifs sur la fonction pulmonaire et provoque une diminution des taux d'exacerbation chez les sujets homozygotes pour la mutation F508del porté par 45-50% des patients 10, 11.
essais cliniques classiques pour identifier les sujets de drogue sensible dans les 50% restants des patients atteints de mucoviscidose sont coûteux et prend du temps et ne sont pas réalisables pour les personnes ayant de très rares génotypes de CFTR. Novel, méthodes personnalisées rentables sont cruciales pour correspondre au nombre croissant de modulateurs de CFTR à des individus porteurs de tout type de mutation CFTR. Jusqu'à présent, l'inclusion d'essai de groupes de patients porteurs de mutations du gène CFTR spécifique a été guidée par des études utilisant mutant transfection du gène CFTR dans hdes systèmes de cellules eterologous, suivie par des études électrophysiologiques dans des chambres d' Ussing 5, 6, 12. En raison d'un manque de modèles animaux de CF adéquates, des études d'efficacité des médicaments dans les cellules épithéliales bronchiques air-liquide-interfaces différenciées dérivées de matériaux explants pulmonaires CF ont été utilisées pour le développement de médicaments 13, 14, 15. Cependant, la disponibilité limitée des tissus d'explants pulmonaires et les procédures invasives pour obtenir des cellules bronchiques de sujets sans maladie en phase terminale d'entraver l'analyse des mutations du gène CFTR moins fréquentes et prévenir le dépistage des drogues d'une manière personnalisée. Pour surmonter ces limitations, les tissus «accès facile», comme organites colorectaux, les cellules des voies respiratoires nasales, et les cellules des voies respiratoires dérivées de cellules souches pluripotentes induites, sont actuellement à l'étude pour les traitements médicamenteux personnalisés.
Auparavant, nous avons établi des protocoles à des cellules souches épithéliales culture de tout organe digestif sous forme de 3D organites 16, 17. facteurs de croissance pour le côlon / rectum humain, les conditions de culture impliquent définis (épithéliale Growth Factor (EGF), Gastrin, Wnt-3A, R-spondine 3 (Rspo3), et Noggin) combiné avec de petites molécules (nicotinamide, A83-01, et SB202190) dans une matrice de membrane basale. Dans ces conditions, les cellules souches individuelles ou de petits fragments de tissu développent dans fermées, kystique, des structures 3D formées par un épithélium hautement polarisé avec son côté de base orientée vers l'extérieur. Tous les types de cellules apparaissent généralement dans leurs rapports et positions normales. Organites peuvent être étendues sur de longues périodes par rupture mécanique hebdomadaire et re-placage. Ils sont génétiquement et phénotypiquement stables et peuvent être stockés, ce qui permet l' expansion à long terme et de la bio-banking 17. Ils se prêtent àtoutes les manipulations de cellules biologiques standards / génétiques et des techniques analytiques développées pour les lignées cellulaires 2D 18.
Nous avons récemment démontré que la fonction CFTR peut être facilement mesurée en organites colorectaux dans une enflure induite par la forskoline (FIS) dosage 19, 20. Lorsqu'il est exposé à la forskoline (FSK) ou, en variante, à la toxine du choléra, organoïdes augmentent rapidement leur adénosine monophosphate cyclique (AMPc) niveaux, ce qui entraîne à son tour l'ouverture du canal CFTR 19. Organites d'individus sains ou de sujets avec des mutations du gène CFTR associées à la fonction résiduelle, seront ensuite gonfler comme une conséquence de l' ion et le transport de l' eau à la lumière organoïdes, l'équivalent in vitro de la diarrhée sécrétoire. La réponse des organites FIS colorectales a été montré précédemment pour être entièrement dépendant de la CFTR, comme indiqué par les organites provenant d'individus CFTR-null, unnd par l'utilisation d'inhibiteurs de CFTR pharmacologiques spécifiques 19. Les grands ensembles de données spécifiques au sujet peuvent être obtenus en quelques semaines après la prise d'une biopsie.
Pour le dosage de la FIS décrit en détail ici, organites sont cultivées à partir de biopsies rectales qui peuvent être obtenus à tout âge et avec seulement une gêne limitée 21. Organites sont repiquées chaque semaine par une rupture mécanique dans cryptes simples qui RESEAL facilement et forment de nouveaux organites. Pour exécuter le test FIS, ~ 30-80 de ces petits organites dissociées sont étalées dans chaque puits d'une plaque à 96 puits 19. Le jour de l'essai, les organites sont colorées avec du vert de la calcéine, un colorant fluorescent perméable aux cellules qui est retenu à l'intérieur des cellules vivantes, ce qui facilite l'imagerie en temps réel. Ensuite, FSK, ce qui augmente l'AMPc intracellulaire et active CFTR ainsi, est ajouté afin de stimuler le gonflement organoïde. Potentialisateurs qui agissent sur le CFTR apicale sont ajoutés simultanément wvec la forskoline, alors que les correcteurs qui rétablissent le trafic de CFTR sont ajoutés 24 heures avant l'addition de Fsk. Le gonflement organoide est quantifiée par une analyse d'image automatisé qui calcule l'augmentation relative de la superficie totale de tous les objets fluorescents pour chaque point de temps après l'addition de forskoline.
3D organoide gonflement fournit des avantages et des inconvénients sur les lectures CFTR électrophysiologiques existantes en 2D cellules des voies respiratoires cultivées dans des chambres de Ussing. Un avantage majeur est le débit de l'essai de gonflement. Les cellules sont cultivées et testées en utilisant un seul type de milieu de culture, et un technicien expérimenté peut culture jusqu'à 25 échantillons organoïdes sur une base hebdomadaire tout en quantifiant environ 1200 points de données par semaine dans 12 échantillons de patients. Nous tapons classiquement une seule condition expérimentale par des mesures double ou en triple par plaque et répéter ces mesures en trois points de temps d'incubation indépendants. Au total, environ 300-500 sIngle organoide structures sont ensuite mesurées par condition expérimentale, ce qui conduit à des mesures très précises de la fonction CFTR avec la variabilité technique limitée. Cette précision nous permet de définir clairement les différences de fonction résiduelle et la réponse à des modulateurs de CFTR et nous permet de prendre facilement des effets de fond génétiques entre les patients porteurs de mutations du gène CFTR identiques 19, 22, 23, 24, 25. La qualité des données peut être facilement évaluée à partir d'images de microscope. Alors que la FIS est entièrement dépendant de la CFTR, il est une mesure de résultat indirect pour la fonction CFTR, son hors lecture causé par le couplage du transport d'ions pour le transport des fluides. Cela contraste avec les mesures de la fonction CFTR directe dans des chambres de Ussing, qui mesurent les courants ioniques transépithéliaux 26. chambres Ussing permettent la stimulation de sélection de apical ou basolatéral compartments (dont le test organoide ne permet pas); par perméabilisation membranes basolatérale, la apical anion sécrétion dépendant de la CFTR peut être mesurée de manière sélective 27.
Protocole
Toutes les expériences en utilisant des tissus humains décrits ici a été approuvé par le comité d'éthique à l'Université Medical Center Utrecht (UMCU; TcBio # 14-008). Le consentement éclairé pour la collecte des tissus, la production, le stockage et l'utilisation des organites a été obtenu à partir des patients à l'hôpital (WKZ) de -UMCU de Wilhelmina enfants.
| Équipement | consommable | Outils |
| hotte à flux laminaire | 15 et 50 ml tubes coniques | Zeiss LSM 800 - Zen 2 (édition Bleu) logiciel pour mesurer les images |
| Incubateur à CO2 | tubes Microfuge | programme Microsoft Excel |
| Microscope de culture cellulaire (microscope optique / lumière) | 0,22 um filtres | |
| Centrifuger | pipettes sérologiques | |
| Rouler Shaker | conseils de filtre Micropipette | |
| 4 ° C ambiante ou à 4 ° C pour réfrigérateur incubateur | cryotubes | |
| CoolCell Cellule de congélation Conteneur | ||
| Pipettor sérologiques | ||
| Micropippette (1000, 200 et 20 ul) | ||
| Viaflo Répétez pipette | ||
| (Cellules vivantes) Microscope confocal | ||
| Ordinateur | ||
| réservoir d'azote liquide | ||
| Multichannel (200 pi) |
1. Réactifs Préparation pour la culture
NOTE: Toutes les étapes sont effectuées à l'intérieur d'une enceinte de sécurité biologique et à la suite des directives standard pour travailler avec des cultures de cellules. Afin de faciliter la formation de belles gouttes de sous-sol matrice de la membrane, maintenir un stock préchauffée de 96-, 24-, et des plaques de 6 puits dans l'incubateur à 37 ° C.
- Basal Medium Préparation
NOTE: medium Basal (BM) se réfère à Modified Eagle Medium avancée Dulbecco avec des éléments nutritifs du mélange de Ham F-12 (Ad-DF) additionné de 4- (2-hydroxyethil) acide -1piperazineethanesulfonic (HEPES), la glutamine et de la pénicilline / streptomycine (Pen / Strep).- Dans un milieu bouteille de 500 ml Ad-DF, ajouter 5 ml de glutamine 200 mM, 5 ml de 1 M HEPES, et 5 ml de solutions / streptocoque de stylo (10.000 U / ml, 10 000 pg / ml).
- BM de magasin dans le réfrigérateur à 4 ° C pendant au moins 4 semaines.
- Moyen Préparation Wnt-3A-conditionné
NOTE: moyenne Wnt-3A-conditionné est fait maison de using la lignée cellulaire L-Wnt-3A conformément aux instructions du fabricant.- Pour récolter le moyen Wnt-3A-conditionné, de recueillir le milieu exposé aux cellules pendant une semaine et tourner vers le bas pendant 5 min à 450 xg pour éliminer les cellules flottantes.
- Filtrez le moyen Wnt-3A-conditionné à travers un filtre de 0,22 um et le diviser en aliquotes de 40 ml dans 50 ml tubes coniques. Conservez-les à 4 ° C pendant au moins 4 mois sans perte d'activité.
- Tester l'activité du milieu de Wnt-3A conditionné dans un dosage TOP / FOP en utilisant de rein embryonnaire humain (HEK) , les cellules transfectées avec -293 supérieure et FOP-luciférase de Renilla et TK- et mesurées avec un Renilla -luciferase kit de dosage selon la les instructions du fabricant.
NOTE: TOP-luciférase est un plasmide rapporteur qui contient des régions de liaison TCF de type sauvage. Si le milieu Wnt-3A-conditionné est actif, la signalisation Wnt canonique est activée. Beta-caténine translocation dans le noyau d'associer l'esprith TCF / facteurs de transcription LEF et active la transcription du rapporteur de la luciférase, induisant une augmentation de l'activité relative de la luciférase lorsque le substrat est ajouté. La FOP-luciférase est utilisé comme témoin négatif parce que le TCF régions de liaison en amont du gène de la luciférase sont mutés.
- Colon moyen Préparation
NOTE: Préparer et diluer tous les facteurs de croissance et de réactifs selon les recommandations du fabricant. Utilisez aliquotes de petite taille un éviter les cycles de gel-dégel. facteurs de croissance fonctionnels sont essentiels pour les résultats.- Préparer le milieu du côlon (CM) en complétant BM avec 1x B27, 1,25 mM N-acétylcystéine, 50 ng / ml de hEGF, 5 nM gastrine, 10 mM de nicotinamide, 300 ng / ml hRspo3, 100 ng / ml hNoggin, 500 uM A83-01 , 10 pM SB202190 et 100 pg / ml d'un anti-infectieux pour les cellules primaires.
- Diviser le CM en aliquotes et les congeler à -20 ° C pendant jusqu'à 4 mois. Décongeler les aliquotes pour préparer complète du côlonmoyen (FCM) en ajoutant 50% de milieu Wnt-3A-conditoned au CM. FCM magasin jusqu'à 7 jours à 4 ° C sans perte d'activité.
- Pour la mise en place d'une culture organoide à partir de biopsies rectales, compléter la FCM avec 50 pg / ml de vancomycine, 50 pg / ml de gentamicine, et un inhibiteur de 10 pM de rho-associé à enroulement en spirale formant la protéine sérine / thréonine kinase (RhoKi). Utilisez ce moyen, moyen d'isolation appelé (IM), seulement pour les deux à trois premiers jours de culture.
- Solution EDTA Stock Préparation
- Préparer l' acide 0,5 M éthylènediaminetétraacétique (EDTA), pH 8, en ultra - pur H 2 O, stérilisé avec un filtre de 0,22 um.
- La manipulation de la membrane basale Matrice
- Préparer la matrice de la membrane basale (BMM) selon les recommandations du fabricant.
- Thaw BMM nuit sur la glace.
- Lors du transfert de la BMM de la bouteille à 15 ml tube conique, l'utilisationune pipette de 5 ml et un tube de 15 ml conique pré-refroidi à -20 ° C.
- Une fois décongelé, rangez le BMM dans un réfrigérateur à 4 ° C et incuber sur la glace pendant au moins 30-60 minutes avant utilisation.
NOTE: Afin d'obtenir les meilleurs résultats, le BMM doit être froid et correctement mélangés avant l'incorporation cryptes ou organites.
2. L'établissement organites Colon à partir d'une biopsie des patients CF
REMARQUE: après la collecte des tissus, il est important de maintenir l'échantillon sur de la glace dans une solution saline, une solution saline tamponnée au phosphate de Dulbecco sans Ca 2+ et Mg 2+ (DPBS) ou BM. Le traitement rapide des biopsies est recommandé, mais il est avéré possible d'établir des cultures organoïdes à partir de biopsies stockées sur la glace pendant jusqu'à 7 jours.
- Que les biopsies se déposent au fond d'un tube conique de 15 ml et éliminer le surnageant.
- Ajouter 10 ml de DPBS pour les biopsies et la pipette vers le haut et vers le bas 10-20 fois en utilisant une pipette de 10 ml.
REMARQUE: La pipette doit être pré-humidifiée avec BM avant pipetage la biopsie. - Que les biopsies se déposent au fond et enlever le surnageant.
- Répétez les étapes 2.2 et 2.3 4-5 fois jusqu'à ce que le surnageant soit clair.
- Ajouter 10 ml de DBP et 200 ul d'EDTA (0,5 M) aux biopsies et placer le tube sur une plate-forme de tube à bascule pour 60-120 min à 4 ° C.
NOTE: Le temps d'incubation peut varier par patient. Si cryptes sont libérés, DPBS devient trouble. EDTA incubation peut être finalisé lorsque cryptes peuvent être observées au microscope. - Permettre aux cryptes de se déposer. Jeter le surnageant.
- Prenez 2 ml de BM et l'ajouter à un nouveau tube de 15 ml conique. Agiter ce nouveau tube manuellement d'une manière telle que la face intérieure est recouverte de BM.
- En utilisant une pipette de pré-humidifiée avec BM, ajouter 2 ml de DPBS dans le tube contenant les biopsies et la pipette vers le haut et vers le bas 10-20 fois.
- Autoriser les biopsies à établir et à transférer les DPBS avec les cryptes à la nouvelletube contenant 2 ml de BM qui a été préparé à l'étape 2.7.
- Répétez les étapes 2.8 et 2.9 jusqu'à ce qu'aucune cryptes sont libérés.
- Faites tourner les cryptes vers le bas à 130 xg pendant 5 min à 8 ° C.
- En attendant, le transfert IM à l'armoire de sécurité à la température ambiante (RT).
- Jeter le surnageant et ajouter 10 ml de BM à la crypte culot et répétez l'étape 2.11.
- Remettre en suspension le culot dans 1 ml de BM. Prenez 5-10 pl et compter le nombre de cryptes par oeil sous un microscope.
- Faites tourner les cryptes vers le bas à 130 xg pendant 5 min à 8 ° C.
- Retirer le surnageant et remettre le culot dans 55% BMM (v BMM à v IM).
NOTE: Les cryptes sont remises en suspension dans le volume correspondant de 55% BMM à 1 crypte par ul. S'il n'y a pas assez cryptes, le volume minimum de BMM est de 40 pi. - Pour le semis, pipette 35 ul par puits (dans une plaque de 24 puits). Divisez les 35 pi de BMM dans 3-5 gouttes séparément afin d'améliorer la diffusion de growth facteurs dans le BMM. Ne pas créer de bulles.
- Placer et laisser la plaque à l'envers dans l'incubateur à 37 ° C pendant au moins 20 min pour la BMM se solidifier.
- Ajouter 500 ul de IM par puits et le maintenir dans l'incubateur à 37 ° C et 5% de CO 2.
- Actualiser le moyen tous les 2-3 jours. Retirer l'ancien milieu par aspiration avec une pipette P1000, en laissant tomber BMM intacte. Ajouter délicatement la FCM par pipetage dans le côté du puits, et non pas directement sur le BMM tombe.
REMARQUE: Si aucun cryptes sont libérés dans le protocole d'isolement, centrifuger le surnageant, laver le culot 2-3 fois avec BM, et resuspendre dans BMM. Prenez le tissu des restes et le couper en petits morceaux avec un rasoir. Recueillir ces derniers dans un tube conique de 15 ml, centrifuger, et les remettre en suspension dans le même BMM. Si des cellules souches épithéliales sont présents, ceux-ci seront également générer des organites.
3. repiquage des organites Colon pour la maintenance, de congélation, et pourskolin induite par Gonflement Assay (FIS)
NOTE: Chaque culture organoide a son propre temps de doublement. Normalement, organites des FC colorectaux peuvent être étendues 1: 3-1: 5 fois tous les 7-10 jours. Il est un bon signe si les structures en herbe sont observées. Organites Colorectal CF sont moins kystique (Figure 2A - 2C) que organites normales colorectaux (Figure 2D). Pour l'établissement et la maintenance, organites sont cultivées dans des plaques à 24 puits; pour la congélation, dans des plaques à 6 puits; et pour le dosage de ski, dans patés de 96 puits.
- Repiquage des organites
- Gardez le BMM sur la glace pendant au moins 30-60 minutes avant de l'utiliser.
- Gardez la FCM à la température ambiante pendant au moins 1 heure avant de l'utiliser.
- Etiqueter le tube un 15 ml conique avec le nom de l'échantillon et un autre tube comme «lavé».
- Aspirer soigneusement le milieu des puits en utilisant une pipette P1000 sans perturber le BMM tombe.
- Ajouter 1 ml de BM à 1 puits et bReak la BMM gouttes à l'aide d'une pipette P1000. Transférez ce 1 ml dans le tube de 15 ml conique avec le nom de l'échantillon.
- Laver les puits avec encore 1 ml de BM et la transfère dans le même tube de 15 ml.
- Répétez les étapes 3.1.5 et 3.1.6 avec 5 puits plus (jusqu'à 6 puits d'une plaque de 24 puits seront lavés dans un 15 ml tube conique).
- Remplir le tube jusqu'à 12 ml avec BM. Pipette de haut en bas à l'aide d'une pipette ml pré-humidifié 5.
- Spin à 85 xg pendant 5 min à 8 ° C.
- Jeter le surnageant et ajouter 1 ml de BM au culot. Avec la même pointe P1000 de pipette, prendre jusqu'à une pointe de P10 sans filtre, et la pipette de haut en bas 20 fois. Jeter les deux P1000 et des conseils de P10.
- Ajouter 4 ml de BM avec une pipette de 5 ml et maintenir le tube incliné à environ 70 ° par rapport à la verticale d'un côté. Mouillez un nouvel embout de P1000 et mélanger vigoureusement 2-3 fois avec le P1000 (volume 1 ml).
- Comptez jusqu'à 10 tout en restant dans la position inclinée, recueillir soigneusement la couche supérieure wvec la pipette P1000, et le transfert 4 x 1 ml dans le tube étiqueté comme «lavé».
- Observer les organites de décantation vers le bas dans le tube incliné; organites sans perturbation et de plus gros morceaux vont tomber au fond. Centrifuger les 15 ml "lavé" tube pendant 5 minutes à 85 xg et 8 ° C.
- Jeter le surnageant et ajouter la quantité de milieu nécessaire et BMM à la pastille organoïde à une concentration finale de 55% BMM. Mélanger par pipetage de haut en bas sans créer de bulles (figure 3B).
NOTE: Une bonne densité est obtenue par ensemencement 25-30 organites dans 10 pi de BMM. - Suivez les étapes de 2,17 à 2,19.
- Repiquage pour congélation
- Gardez la BM dans la glace pendant au moins 30-60 minutes avant utilisation. Gardez la FCM à la température ambiante pendant au moins 1 h avant de l'utiliser.
- Préparer FCM supplémenté avec RhoKi (étape 1.3.3).
- Prenez trypsine du réfrigérateur et le laisser à température ambiante pendant au moins 30 min avant utilisation.
- Suivez les étapes 3.1.5-3.1.10.
- Retirez autant que possible surnageant, ajouter 4 ml de trypsine, et vortex pendant 30 sec.
- Placer le tube dans un bain d'eau chaude à 37 ° C pendant 1 min et vortex vigoureusement pendant 30 sec.
- Inspecter la solution dans le tube. Si organites intacts sont encore visibles sous le microscope, répétez l'étape 3.2.7.
- Lorsque les organites sont perturbés, ajouter 8 ml de BM pour neutraliser la trypsine et la pipette 10 fois.
- Spin pendant 3 min à 450 xg à 8 ° C.
- Jeter le surnageant et ajouter la quantité requise de moyen et BMM aux organites pour parvenir à une solution BMM 55%. Mélanger par pipetage de haut en bas sans créer de bulles.
NOTE: Pour la congélation, organites doivent être ensemencées dans un rapport 1: 1 après trypsinisation. - Graine de 250 pi dans un seul puits d'une plaque à 6 puits de culture de tissu pré-chauffé, produisant de minuscules gouttelettes séparées de ~ 10 pi. Placer la plaque à l'envers dans l'incubateur à 37 ° C et laisser leBMM se solidifier pendant 20-30 min.
- Ajouter 2,5 ml de FCM fraîche + RhoKi dans chaque plaque de 6 puits puits et transférer la plaque dans l'incubateur (figure 3C).
- Repiquage organites pour le dosage de la FIS
NOTE: Selon le nombre et la taille des organites, entre 4 et 6 puits d'une plaque de 24 puits sont suffisamment pour l'ensemencement de 27 puits d'une plaque de 96 puits.- Traiter les organites comme décrit des étapes 3.1-3.1.13.
- Reprendre le culot dans 120 ul de 50% BMM.
- Confirmer le nombre d'organites (30-50) dans un 3 pl BMM goutte sous le microscope.
- Plate les organites en utilisant une seule goutte de 3 ul placés au milieu de chaque puits d'un pâté de 96 puits.
- Placer la plaque dans l'incubateur à 37 ° C pendant 15 min pour le BMM se solidifier; d'autres étapes sont décrites dans l'étape 6.1.1.
4. Colon congélation organites CF
NOTE: Organoids sont prêts à être congelés jusqu'à 1-2 jours après trypsinisation et la culture, de sorte que organites sera toujours faible, ce qui augmente l'efficacité de la survie après décongélation.
- Ajouter 1 ml de BM et briser la BMM gouttes à l'aide d'une pipette P1000. Transférer dans un tube conique de 15 ml.
- Laver le bien avec un autre 1 ml de BM et le transfert vers le même tube de 15 ml.
- Répétez les étapes 4.1 et 4.2 avec tous les puits.
NOTE: Pour éviter l'excès de BMM, 3 puits d'une plaque à 6 puits sont regroupés dans un tube de 15 ml. - Remplir le tube de 15 ml contenant les organites avec 12 ml de BM à froid et la pipette de haut en bas avec une pipette de 5 ml. Laisser le tube sur la glace pendant 5 min.
- Spin pendant 3 min à 450 xg et 8 ° C et retirer le surnageant.
- Dissoudre le culot de organites avec un milieu de congélation et la pipette de haut en bas pour remettre en suspension correctement les organites.
NOTE: 500 pi de milieu de congélation est utilisé pour chaque 100 pi de BMM. - L'utilisation d'un 5 ml pipette, transférer 0,5 ml deorganites remises en suspension dans milieu de congélation à stériles flacons cryogéniques.
- Transférer les flacons dans un récipient de congélation de cellules et de le mettre à -80 ° C.
- Après 24 h, transférer les flacons pour le stockage dans de l'azote liquide.
5. Mise en place des cultures de Frozen organites
NOTE: Décongeler le BMM sur la glace et le garder sur la glace. Laissez le BM atteindre RT, et réchauffer une aliquote de 10 ml à 37 ° C avant de commencer la procédure de décongélation d'un cryovial.
- Décongeler le flacon rapidement par agitation dans un bain d'eau C 37 ° jusqu'à ce qu'il reste un peu de matériel congelé.
- Transférer les organites décongelé dans un tube conique de 15 ml à l'aide d'une pipette P1000.
- Immédiatement après, ajouter 1 ml de chute de BM chaude à goutte tout en agitant le fond du tube. Une fois les 1 ml de milieu est ajouté, mélanger soigneusement par pipetage de haut en bas plusieurs fois pour diluer le milieu de congélation.
- Lentement (goutte à goutte) ajouter 9 ml de chaud BM à la conta de tube coniqueIning les organites. Inversez quelques fois.
- Faites tourner la suspension cellulaire pendant 3 min à 85 xg et 8 ° C.
- Jeter soigneusement le surnageant sans perturber le culot. Reprendre le organoide dans 90 pi de FCM complété avec RhoKi (étape 1.3.3). Ensuite, ajouter 110 pi de BMM.
- Ajouter 35 ul à chaque puits d'une plaque de 24 puits pré-chauffé, faisant de minuscules gouttelettes séparées.
- Transférer la plaque à l'étuve 37 ° C, en laissant la plaque de tête en bas pendant 20 à 30 min.
- Ajouter 500 pi de la FCM avec RhoKi à chaque puits et transférer la plaque arrière à l'incubateur (figure 4A - 4C).
- Une fois organites ont récupéré correctement à partir de la décongélation, diluer plus BMM de sorte que chaque 10 pi de BMM contient 25-30 organites. Cette procédure peut être effectuée 2-3 jours après la décongélation (figure 4D - 4G) et assure la bonne croissance du organoïde.
6. forskoline induite par Gonflement Commedire (FIS)
NOTE: Fsk titration permet la mesure de la fonction résiduelle CFTR. CFTR pour la modulation, organites sont exposés à un correcteur donné (par exemple, VX-809) et / ou de potentialisation (par exemple, VX-770), selon le génotype. En général, le VX-809 est ajouté 18 à 24 h avant la mesure, tandis que le VX-770 et FSK sont ajoutés juste avant le début des mesures. Soyez conscient que certains modulateurs (Correcteurs / potentialisateurs) peuvent se lier à la surface en plastique de la plaque d'essai.
- Placage pour le dosage
NOTE: VX-809 stocks sont aliquotées à 20 mM et conservées à -80 ° C. Lors de la décongélation, laisser à la température ambiante et de protéger de la lumière.- Traiter les organites comme décrit dans la section 3.3.
- Si le test du correcteur VX-809, préparer une courbe dose-réponse en triple exemplaire avec les concentrations suivantes: 0,0003, 0,003, 0,03, 0,3, 3,0 et 30 uM. Préparer les dilutions dans la FCM.
- Pour la plaque de 96 puits, ajouter soit 100 μ; L de la FCM avec les VX-809 de concentration ou de 100 ul respectives de la FCM seulement et incuber la plaque.
- Mesurer le dosage
NOTE: VX-770 stocks sont aliquotées à 20 mM, tandis que Fsk est à 10 mM; les deux sont conservés à -80 ° C. Lors de la décongélation, laisser à température ambiante et protéger de la lumière.- Prenez un flacon de calcéine et de DMSO et de laisser à température ambiante pendant 15 min.
- Ajouter 5,1 ul de DMSO à la fiole lorsque la calcéine est fourni sous forme de poudre, suivant l'achat. Sinon, utilisez un flacon de calcéine déjà remis en suspension contenant 2,5 pi de calcéine.
- Ajouter 2,5 ul de calcéine à 580 pl de PR dans un tube de 1,5 ml et étiqueter.
- Ajouter 10 pi de cette solution de colorant (BM + calcéine) dans chaque puits en utilisant une pipette à répétition.
- Remettre en suspension une fois avec un multi-canaux pour garantir que le colorant est bien mélangé.
- Incuber la plaque dans un incubateur à 37 ° C pendant 30 min.
- Au cours de l'incubation de la calcéine, commencer à préparer le Fsket des solutions VX-770, si nécessaire.
- Si l'on utilise un potentialisateur VX-770, préparer une courbe dose-réponse en triple exemplaire avec les concentrations suivantes: 0,0003, 0,003, 0,03, 0,3, 3,0 et 30 uM. Dans le cas d'un titrage Fsk, les concentrations sont les suivantes: 0, 0,008, 0,02, 0,05, 0,12, 0,32, 0,8, 2,0 et 5,0 uM. Préparer les dilutions dans BM.
NOTE: Pour Fsk, VX-770, ou tout autre médicament ajouté le deuxième jour, les dilutions doivent être préparées à une concentration finale 2x, puisque 100 pi de Fsk solution / de titration de médicament sera ajouté à chaque puits, qui contiennent déjà 100 pi de la FCM. - Transférez le Fsk et VX-770 solutions, une pipette P200, et des conseils pour la salle de microscope.
- Pour l' imagerie du test FIS, utiliser une imagerie cellulaire microscope confocal en direct équipé d'une étape automatisée, une chambre chauffée, et flux de CO 2.
REMARQUE: Les étapes suivantes se réfèrent à un microscope spécifique. Différentes configurations doivent appliquer à d'autres microscopes suivant fabricantinstructions. - Mettez la plaque de 96 puits dans le support de plaque.
- Entrez les paramètres confocale pour l'imagerie.
- Preset l'outil d'imagerie en direct à 37 ° C et 5% de CO 2 et de laisser la chambre pré-incuber pendant un minimum de 30 minutes avant la mesure.
- Utilisez l'option "Smart Setup" pour sélectionner la piste Alexa Fluor-488.
- Placez l'objectif 5X et la zone de numérisation à 0.6X pour rétrécir et capturer l'ensemble du bien.
- Adapter la sensibilité de la puissance du laser et du détecteur pour permettre la détection optimale des organites marqués calcéine-vert sur le fond. Le sténopé peut être augmentée à 130 um et l'image de la moyenne peut être réglée à 2.
- Régler la profondeur de bits à 8 et la taille de l'image à 512 x 512.
- Utilisez l'option de séries chronologiques pour définir les mesures à temps, la fréquence et les intervalles.
NOTE: suggérée pour des mesures régulières: 1 h avec 10 min d'intervalle: cycles = 7 (cycle 1 est T = 0). Pour les mesures de gonflement réduite, organoïdes peuvent être imagées jusqu'à 3 heures. - Utilisez l'option de tuiles pour déterminer manuellement les positions de puits individuels.
- Ajouter 100 ul de la Fsk et / ou VX-770 des solutions aux puits correspondants, en suivant le même ordre que celui de la mesure. Commencer à ajouter les solutions dans le premier imagées bien et continuer avec l'ordre d'imagerie.
- Démarrez la mesure.
- Après l'expérience est terminée, enregistrez le fichier.
- Analyse des données FIS Assay
- Créer une macro "analyse organoide" pour l'analyse des données de l'essai de la FIS en utilisant l'outil d'analyse dans un logiciel d'analyse d'image qui reconnaît toutes les structures imagées par la piste Alexa-488 et remplit les structures identifiées pour calculer l'augmentation de la superficie organoide total sur la différents points de temps.
- Ouvrez le fichier de données avec les images acquises dans le programme d'analyse d'image.
- Sélectionnez la macro pour l'analyse organoide.
- Définir le seuil d'équilibrer le rapport signal-bruit dans un puits à 1 point de temps et de veiller à ce que toutes les structures organoïdes sont reconnus et remplis.
- Arrivée 4-6 puits pour voir si toutes les structures sont également reconnues au point 7. de temps légèrement modifier le seuil pour veiller à ce que les signaux de fond au point 7 de temps ne sont pas reconnus comme des structures (le seuil spécifique peut changer quelque peu entre les expériences).
- Définissez les critères de taille de zone minimale d'objets reconnus à 1000 um 2.
- Appuyez sur "analyser" pour démarrer. L'analyse prend environ 3 min, en fonction du logiciel utilisé.
- Lorsque le logiciel est terminé, allez à «créer la table" et sélectionnez les données suivantes: bien numéros (tableau devrait augmenter dans cet ordre), des points de temps, et la superficie totale par puits.
- Enregistrer le fichier en tant .xlm à exporter vers un tableur.
- Dans ce programme, calculer l'augmentation relative de la surface par well en définissant la superficie de 1 point de temps à 100%. Calculer l'aire sous la courbe (AUC) à partir de points de temps 1-7 par condition; la limite inférieure de la zone (valeur Y) est fixé à 100%. FSK ou de drogue titrages (axe X) sont tracées en fonction de l'ASC (axe Y).
Résultats
La figure 1A montre un isolement frais représentatif de cryptes embarqués sur BMM. Les cryptes sont d'une biopsie du côlon d'un sujet CF. Habituellement, un organoïde est généré à partir de chaque crypte (figure 1A - C). En raison du dysfonctionnement du CFTR, la plupart des organites colon des FC ne sont pas kystique, mais sont compacts et avec des projections et des bourgeonnements (Figure 2A - 2B). Cependant, certains CF organoide cultures, en particulier avec la fonction résiduelle élevée, ont quelques organites avec une forme kystique (figure 2C), comme de type sauvage cultures organoïdes (figure 2D).
Avant repiquage des organites d'expansion de la culture ou de l' ensemencement d' un test FIS est important que les organites ont une grande taille , avec de multiples bourgeonnements, comme représenté sur la figure 3A. Si les organites sont petites et sans nécussonnages ombreux lorsqu'ils sont traités pour repiquage, la culture organoide est négativement affectée. Selon la qualité et l' activité des facteurs de croissance essentiels tels que l' EGF, Wnt 3a et Rspo3, les organites atteignent la taille désirée entre 7 et 12 jours (figure 3A). Après une rupture mécanique, les bourgeonnements sont perturbées et utilisées pour générer de nouveaux organites dans le passage suivant (figure 3B). Si le traitement des organites pour la congélation, il est important qu'ils sont trypsinisées à une petite taille, comme cela est représenté sur la figure 3C. Après trypsinisation, les organites sont plaquées pour 1 ou 2 jours afin de les laisser se remettre du stress de la manipulation. Cette étape, conjointement avec la petite taille des organites, assure une récupération des cellules de 98% après décongélation (figure 4A).
Lorsque les organites sont décongelés, il est important de les avoir en haute densité, donc normalement, ils sont décongelés dans unpetit volume (Figure4A). Après un ou deux jours de culture, et après avoir constaté que les organites augmentent la taille (comparer la figure 4A à la figure 4B - 4C), les organites sont dilués dans un rapport de 20-30 organites par 10 pi de BMM, fournissant la bonne densité de se développer dans une plus grande taille. Si les organites sont trop dilués, ils peuvent ralentir la croissance et peut même se différencier et de mourir. Si les organites sont trop de monde, le manque d'espace ou de la pénurie de facteurs de croissance ralentit également la croissance des organites et réduit le nombre de bourgeonnements.
Le placage des organites de cultures viables avec des débris cellulaires limitée devrait entraîner des conditions dans lesquelles> 95% des organites houle sur Fsk stimulation, à condition que la fonction CFTR suffisante est présente (figure 5A - 5B). Organites gonfler de façon génotype-et toxicomane, commeillustré par des images représentatives des organites avec deux allèles F508del (figure 5A) et organites hétérozygote pour F508del et S1251N (figure 5B), une mutation CFTR de déclenchement associé à une fonction résiduelle.
Pour quantifier le gonflement, le total des surfaces calcéine-vert sont sélectionnés pour chaque point de temps et exprimés en pourcentage de T = 0 (fixé à 100%; la figure 6A). Les débris et les petites structures, non gonflantes sont en général inférieures à 5% de la surface totale. L'augmentation de la surface relative est exprimée par 10 min intervalle de temps, et l' AUC (unités arbitraires) des mesures sont générées pour chaque condition (T = 0 à 60 min, seuil de référence fixé à 100%; la figure 6B). Nous avons trouvé l'ASC pour être le plus robuste, car il intègre une certaine variation dans l'initiation de l'enflure, ainsi qu'une relation curviligne au-delà de 30-40 min de Fsk à des niveaux de fonction haute CFTR.
mesures de la fonction résiduelle dans F508del / F508del organites atteignent généralement 0-200 unités AUC (100-110 de% d'augmentation de la surface après 60 min de 5 uM traitement FSK) , ce qui peut augmenter à ~ 2.500-3.500 unités AUC lors de l' incubation avec des modulateurs de CFTR (VX770 + VX809; Figure 6C). Organites associés à une fonction résiduelle CFTR peut atteindre jusqu'à 4500 unités AUC après 60 min de 5 uM Fsk stimulation en l'absence de modulateurs de CFTR (200-220% de la zone de conditions pré-FSK surface). gonflement organoide atteint un plafond à ~ 4500 unités AUC, vraisemblablement en raison des limitations physiques des structures organoïdes, l'impact de limitation de vitesse de transport d'ions basolatéral, et la mise en place de l'homéostasie d'ions et le fluide de transport dans des conditions "tendues". Fsk peut être titré pour étendre la plage dynamique de l'essai à ces CFTR niveaux de fonction résiduelle élevées pour mieux quantifier la fonction résiduelle ou très efficace traitement du composé (par exemple, comme indiqué par l'activité plus élevée de VX770 sur le gonflement des organites S1251N lors d'une stimulation avec des concentrations plus faibles FSK, la figure 6D).

Figure 1: Mise en place de CF organites colorectaux de biopsies. (A) Des images représentatives d' un matériau isolé à partir d' une biopsie rectale , après avoir été incorporé dans BMM le jour d'isolement (passage 0, jour 0). L'élargissement de la crypte indiquée est affichée sur le panneau inférieur droit. (B) Les mêmes cryptes ont été suivis après 7 jours de culture (passage 0, jour 7). L'élargissement de la même crypte présentée dans le panneau A est représenté. (C) d'image représentant de la même culture organoide 11 jours après avoir été fendu (passage 1, jour 11). Les barres d'échelle = 100 um.
159fig1large.jpg "target =" _ blank "> S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.

Figure 2: Des images représentatives de organites colorectaux FC provenant de sujets avec différentes mutations du gène CFTR. Des images représentatives des FC organites colorectaux chez des sujets avec F508del / F508del (A), F508del / R117H-7T (B), et F508del / S1251N (C) mutations. (D) d'image représentant d'une culture organoide colorectal à partir d' un objet de type sauvage CFTR. Les barres d'échelle = 100 um. Ces images ont été obtenues sans stimulation Fsk. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
5159 / 55159fig3.jpg "/>
Figure 3: Traitement organites du côlon des FC pour l' entretien et le dosage ou pour la congélation. (A) Des images représentatives d'une culture organoide du côlon CF prête à être traitée soit pour repiquage (B) ou la congélation (C). (B) Après leur rupture mécanique, de petits morceaux sont formés, ce qui va générer les nouveaux organites dans le passage suivant. (C) Après trypsinisation, de très petits organites ronds sont générés, ce qui facilite leur viabilité au cours du processus de congélation. Les barres d'échelle = 100 um. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
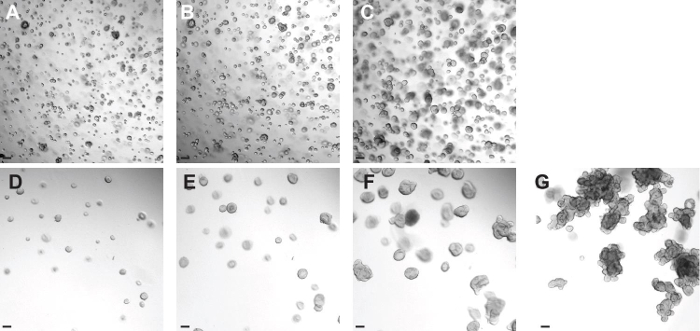
Figure 4: Instaurer une culture organoide colorectal CF de organites congelés. ( A - C) Des images représentatives d'une culture organoide colorectal CF décongelés le jour 0 (A). Les images du même puits ont été l' un (B) et (C) deux jours après. (D - G) images représentatifs de l'étape de dilution décrite à la section 5.9. Une fois que les organites ont récupéré correctement à partir de la décongélation (jour 3 après décongélation), ils sont dilués afin qu'ils aient l' espace pour se développer (D). Les images du même puits ont été prises six (E), dix (F), et quinze (C) jours après la décongélation. Les barres d'échelle = 100 um. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.

Figure 5: gonflement induite par la forskoline de CForganites. (A et B) images représentatives de F508del / F508del (A) ou F508del / S1251N (B) organites colorectal avant-770 VX ou après 60 minutes de stimulation avec Fsk (5 de um) en l'absence ou en présence de (3 pm]) ou VX-770 en combinaison avec VX-809 (3 pm). Les barres d'échelle = 200 um. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
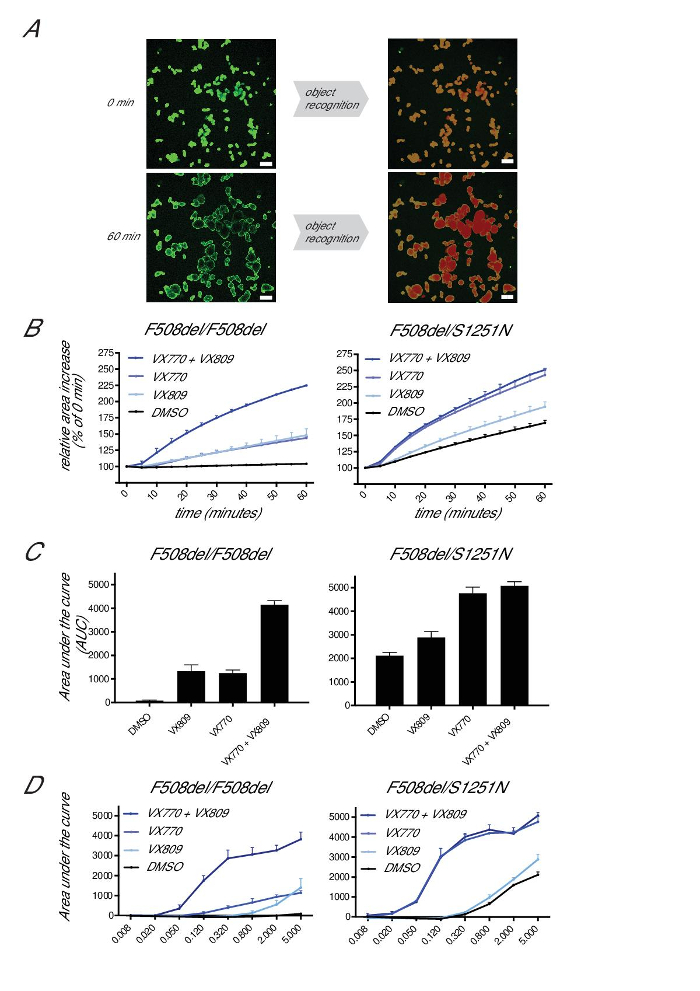
Figure 6: gonflement Quantifier forskoline induite. (A) Des images représentatives de la sélection de la zone organoïde par un logiciel de F508del / S1251N d'analyse d'image avant organites (0 min) et après 60 minutes de stimulation avec Fsk (5 uM) et VX770 (3 uM). Les barres d'échelle = 200 um. (B) Represimages repré- de l'augmentation de la zone relative de F508del / F508del ou F508del organites / de S1251N pendant 60 min de Fsk (5 um) stimulation en l'absence ou la présence de VX770 (3 pm) et / ou VX809 (3 pm). (C) aire sous la courbe des mesures de conditions indiquées dans (B) (T = 60 min, seuil de référence = 100%). (D) aire sous la courbe des mesures de F508del / F508del ou organites F508del / de S1251N à différentes concentrations de Fsk. Les données représentent les moyennes ± écart-type à partir d'expériences représentatives simples. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
Discussion
Ici, nous fournissons un protocole complet pour la génération, l'expansion, la congélation et la décongélation des organites colorectales humaines. Alors que nous avons établi des cultures de organoïdes humains il y a quelque temps 17, il a parfois avéré difficile d'établir la technologie dans d' autres laboratoires sans formation pratique. Nous prévoyons que ces protocoles remplaceront une telle formation.
Wnt-3A-milieu conditionné est l'un des réactifs les plus cruciaux pour réussir dans l'établissement et le maintien à long terme organoide culture. En effet, les cultures organoïdes pourraient "crash" lorsqu'il est exposé à moyen Wnt-3A-conditoned avec une faible activité. Depuis moyen Wnt-3A-conditionné est fait maison, il y a plusieurs aspects qui doivent être pris en compte lors de la génération d'un milieu actif. Wnt-actif 3A ne peut être produit dans un milieu avec du sérum de foetus de bovin de haute qualité (FBS) qui fournit des signaux de croissance appropriés pour les cellules L et la stabilisation hydrophobemolécules Wnt-3A. Lorsque l' activité Wnt-3A est (c. -à faibles rapports TOP / FOP, voir ci - dessous) faibles, ce sont généralement les FBS qui est l' origine du problème.
Commercial recombinant Wnt fonctionne mal, donc nous ne recommandons pas l'utiliser comme témoin positif pour le dosage rapporteur TOP / FOP Wnt. Le rapport entre TOP / Renilla et FOP / Renilla est une indication de l'activité Wnt du milieu conditionné, donc un bon lot de milieu Wnt-3A-conditionné donne un rapport TOP / FOP supérieur à 25, par rapport à la valeur TOP / FOP de le contrôle négatif: milieu non exposé à des cellules-3A produisant Wnt. Noggine recombinante et R-spondine peuvent être remplacés par noggine et R-spondine conditionnés fluide 28, 29.
Le protocole actuel décrit également un test fonctionnel pour CFTR le test FIS. Récemment , nous avons démontré la relation entre le génotype et CFTR FIS et comment cela reflète genoty publié CFTRrelations pe-phénotypes obtenus à partir des registres cliniques (www.CFTR2.org) 25. L' utilisation de ce test, deux individus avec des mutations du gène CFTR extrêmement rares ont été identifiés dont les organites étaient sensibles à ivacaftor (VX-770) 25. Après la prescription de ce médicament a donné lieu à une réponse clinique claire, mettant en évidence la valeur de l'essai de la FIS pour correspondre à des médicaments spécifiques aux patients présentant des mutations rares en l'absence de données d'essais cliniques. Essentiels pour la quantification de la FIS sont la croissance et d'analyse des conditions optimales, indiqués uniquement par une fraction limitée d'organites non gonflantes (habituellement inférieure à 5%). Des niveaux élevés de débris de plomb à la sous-estimation de gonflement, comme une plus grande proportion de structures non viables, non-gonflement sont reconnus par le logiciel d'analyse d'image.
Les corrélations entre vitro FIS réponses dans et biomarqueurs CFTR dépendant précédemment établies (concentration de chlorure de sueur et Intestles mesures de courant tones) au niveau personnalisé étaient facilement démontrable dans nos études précédentes 19, 25. Cette prise en charge de la notion que les mesures de fonction résiduelles en utilisant FIS sur des sujets atteints de mucoviscidose peuvent compléter les approches actuelles en tant que marqueur diagnostique ou pronostique de façon personnalisée. Le débit de l'essai de la FIS par rapport à d' autres biomarqueurs de la fonction CFTR, tels que les mesures de concentration de chlorure de sueur in vivo et des mesures de courant intestinales en ex vivo biopsies rectales, permet un meilleur contrôle de la variabilité technique. Il fournit également une lecture entièrement dépendant de la CFTR et une grande plage dynamique en utilisant un titrage de Fsk que les types avec précision de la fonction CFTR résiduelle.
Cependant, le dosage de la FIS ne reflète que l'effet du génotype individuel sur la variabilité de l'efficacité du médicament, tandis que la modulation de la fibrose kystique est affecté par plus de la seule fonction CFTR. Pour druréponse g, le dosage est le reflet d'une réponse tissulaire potentielle. Bien qu'il soit très précis dans la mesure CFTR, la variation de la pharmacocinétique humaine n'a pas été incorporée, par opposition aux autres in vivo 7, 8 ou ex vivo des mesures directes CFTR 32. Comme indiqué précédemment, les modificateurs des FC non ( à la fois génétiques et environnementaux) influencent également le phénotype, ce qui provoque un décalage entre les observations in vitro ou biomarqueurs CFTR et phénotype clinique 2. En outre, l'identification des mutations sensibles potentielles en utilisant des lignées de cellules 33 est associée à moins d' impact sur les patients qui ont besoin d'obtenir une biopsie rectale pour la mise en place d'organites.
Plusieurs médicaments CFTR ciblage sont actuellement en développement 1. Il est prévu que les essais cliniques ne permettent pas une prédiction correcte de l'efficacité clinique belon les CFTR statut mutationnel seul. Comme l'essai de FIS mesure la fonction CFTR et la réponse aux médicaments fonctionnellement, il peut devenir la méthode de choix pour déterminer quel médicament fonctionne le mieux pour quel patient. Le dosage de la FIS peut également être utile pour l'identification des groupes de patients à inclure dans les essais d'enregistrement et pour le développement de nouvelles modalités de drogue. La stimulation de la organites colorectal avec du plasma avant et pendant le traitement peut en outre contribuer à quantifier les quantités fonctionnelles de faire circuler les modulateurs de la protéine CFTR dans le sang, ce qui peut faciliter le dosage personnalisé et la sélection des doses de médicaments dans des essais cliniques 30, 31. Enfin, la FIS peut être utile pour une meilleure compréhension de base de la fonction CFTR et ses interactions avec d'autres modificateurs génétiques -SO jusqu'ici largement unknown- de sa fonction.
Déclarations de divulgation
Hans Clevers is an inventor on patents for organoid culture and the Forskolin-induced swelling assay. Jeffrey M Beekman is an inventor on a patent for the Forskolin-induced swelling assay. Sylvia F Boj and Robert Vries are employed by the Foundation Hubrecht Organoid Technology (HUB), which holds the exclusive license to the Organoid Technology. Otherwise, the authors have nothing to disclose.
Remerciements
Ce travail a été soutenu par le programme des FC fondation néerlandaise (NCFS), ZonMW (40-00812-98-14103), le Fonds de recherche de l'Hôpital de Wilhelmina enfants et CZ et Zilverenkruis / Achmea HIT-CF. Nous tenons à remercier S. Heida-Michel, M. Geerdink, KM de Winter-de Groot, et G. Berkers (Département de pneumologie pédiatrique, Hôpital de Wilhelmina enfants, UMC Utrecht), et RHJ Houwen (Département de gastro-entérologie pédiatrique, Wilhelmina Hôpital pour enfants, UMC Utrecht) pour approcher les patients et d'obtenir les biopsies pour la génération d'un Biobanque CF.
matériels
| Name | Company | Catalog Number | Comments |
| Advanced Dulbecco’s Modified Eagles Medium with Nutrient Mixture F-12 Hams (Ad-DF) 500 ml | Thermo Fisher Scientific: Invitrogen | #12634 | stored at 4 °C |
| GlutaMax | Thermo Fisher Scientific: Invitrogen | #35050 | stored at 4 °C |
| Hepes | Thermo Fisher Scientific: Invitrogen | # 15630-056 | stored at 4 °C |
| Penicillin/Streptomycin | Thermo Fisher Scientific: Invitrogen | #15140-122 | stored at -20 °C |
| 96 well culture plate | Cellstar | #655180 | |
| 24 well culture plate | Cellstar | #662160 | |
| 6 well culture plate | Cellstar | #657160 | |
| Dulbecco's Phosphate Buffered Saline (-) CaCl2 (-) MgCl2) (DPBS) | Life Technologies: Gibco | #14190-094 | stored at 4 °C |
| Dulbecco’s Modified Eagles Medium (DMEM) 500 ml | Thermo Fisher Scientific: Invitrogen | #31966-021 | For Wnt-3A Conditioned Medium Production. Stored at 4 °C |
| Fetal Bovine Serum (FBS) | Bovogen | #SFBS LOT#11113 | For Wnt-3A Conditioned Medium Production. Stored at -20 °C |
| L Wnt3A cell line | ATCC | #CRL-2647 | For Wnt-3A Conditioend Medium Production. |
| TOP/FOP plasmids | Millipore | #17-285 | For measuring Wnt activity |
| pTK-Renilla | Promega | #E2241 | For measuring Wnt activity |
| HEK-293 | ATCC | #CRL-1573 | For measuring Wnt activity |
| Dual-Luciferase Reporter Assay System | Promega | #E1910 | For measuring Wnt activity |
| Zeocin | Thermo Fisher Scientific: Invitrogen | #R250-01 | For Wnt-3A Cell line selection |
| B27 supplement | Thermo Fisher Scientific: Invitrogen | #17504-044 | stored at -20 °C |
| N-Acetylcysteine | Sigma Aldrich | #A9165-5G | stored at -20 °C |
| Nicotinamide | Sigma Aldrich | #N0636 | stored at -20 °C |
| Human Epithelial Growth Factor (hEGF) | PrepoTech | #AF-100-15 | stored at -20 °C |
| Gastrin | Sigma Aldrich | #G9145 | stored at -20 °C |
| TGFb type I Receptor inhibitor (A83-01) | Tocris | #2939 | stored at -20 °C |
| Y-27632 dihydrochloride (RhoKi) | Selleckchem | #S1049 | stored at -20 °C |
| p38 MAPK inhibitor (p38i) (SB202190) | Sigma Aldrich | #S7067 | stored at -20 °C |
| Primocin | InvivoGen | #ant-pm-1 | stored at -20 °C |
| Human Noggin (hNoggin) | PrepoTech | #120-10C | stored at -20 °C |
| Human R-spondin 3 (hRspo-3) | R&D Systems | #3500-RS/CF | stored at -20 °C |
| Vancomycin | Sigma Aldrich | #861987- 250mg | stored at -20 °C |
| Gentamycin | Life Technologies: Gibco | #15710-049 | stored at -20 °C |
| Ethylenediamine tetraacetic acid (EDTA) | Sigma Aldrich | #431788 | Stored at 4 °C |
| Matrigel | Corning | #354230 | stored at -80 °C |
| TryplE Express | Life Technologies: Gibco | #12605-010 | for trypsinizing organoids for freezing |
| Recovery Cell Culture Freezing Medium | Life Technologies: Gibco | #12648010 | for freezing |
| Calcein | Life Technologies: Gibco | #C3100MP | stored at -20 °C |
| Forskolin | R&D Systems | #1099-50 mg | stored at -80 °C |
| Lumacaftor (VX-809) | Selleckchem | #s1565 | stored at -80 °C |
| Ivacaftor (VX-770) | Selleckchem | #s1144 | stored at -80 °C |
| Name of Reagents/Material | Solvent | Stock Concentration | Final Concentration |
| GlutaMax | 200 mM | 2 mM | |
| Hepes | 1 M | 10 mM | |
| Penicillin/Streptomycin | 10K U/ml 10K µg/ml | 100 U/ml 100 µg/ml | |
| Zeocin | 100 mg/ml | 125 µg/ml | |
| B27 supplement | 100x | 1x | |
| N-Acetylcysteine | MiliQ H2O | 500 mM | |
| Nicotinamide | DPBS | 1 M | 10 mM |
| Human Epithelial Growth Factor (hEGF) | DPBS 0.1% BSA | 0.5 mg/ml | 50 ng/ml |
| Gastrin | DPBS | 100 µM | 10 nM |
| TGFb type I Receptor inhibitor (A83-01) | DMSO | 5 mM | 500 nM |
| Y-27632 dihydrochloride (RhoKi) | DMSO | 10 mM | 10 µM |
| p38 MAPK inhibitor (p38i) (SB202190) | DMSO | 30 mM | 10 µM |
| Primocin | 50 mg/ml | 100 µg/ml | |
| Human Noggin (hNoggin) | DPBS 0.1%BSA | 100 µg/ml | 100 ng/ml |
| Human R-spondin 3 (hRspo-3) | varies per lot | 300 ng/ml | |
| Vancomycin | 10 mg/ml | 50 µg/ml | |
| Gentamycin | 10 mg/ml | 50 µg/ml | |
| Ethylenediamine tetraacetic acid (EDTA) | MiliQ H2O | 0.5 M | 2 mM |
| Calcein | DMSO | 10 µg/ml | 3.3 ng/ml |
| Forskolin | DMSO | 10 mM | variable |
| Lumacaftor (VX-809) | DMSO | 20 mM | variable |
| Ivacaftor (VX-770) | DMSO | 20 mM | variable |
Références
- De Boeck, K., Amaral, M. D. Progress in therapies for cystic fibrosis. Lancet Respir Med. 4 (8), 662-674 (2016).
- Cutting, G. R. Cystic fibrosis genetics: from molecular understanding to clinical application. Nature Rev Genet. 16 (1), 45-56 (2015).
- Sosnay, P. R., Siklosi, K. R., et al. Defining the disease liability of variants in the cystic fibrosis transmembrane conductance regulator gene. Nature Genet. 45 (10), 1160-1167 (2013).
- Zielenski, J. Genotype and phenotype in cystic fibrosis. Respiration. 67 (2), 117-133 (2000).
- Van Goor, F., Hadida, S., et al. Rescue of CF airway epithelial cell function in vitro by a CFTR potentiator, VX-770. Proc Natl Acad Sci U.S.A. 106 (44), 18825-18830 (2009).
- Van Goor, F., Hadida, S., et al. Correction of the F508del-CFTR protein processing defect in vitro by the investigational drug VX-809. Proc Natl Acad Sci U.S.A. 108 (46), 18843-18848 (2011).
- Accurso, F. J., Rowe, S. M., et al. Effect of VX-770 in persons with cystic fibrosis and the G551D-CFTR mutation. N Engl J Med. 363 (21), 1991-2003 (2010).
- Ramsey, B. W., Davies, J., et al. A CFTR potentiator in patients with cystic fibrosis and the G551D mutation. N Engl J Med. 365 (18), 1663-1672 (2011).
- De Boeck, K., Munck, A., et al. Efficacy and safety of ivacaftor in patients with cystic fibrosis and a non-G551D gating mutation. J Cyst Fibros. 13 (6), 674-680 (2014).
- Boyle, M. P., Bell, S. C., et al. A CFTR corrector (lumacaftor) and a CFTR potentiator (ivacaftor) for treatment of patients with cystic fibrosis who have a phe508del CFTR mutation: a phase 2 randomised controlled trial. Lancet Respir Med. 2 (7), 527-538 (2014).
- Wainwright, C. E., Elborn, J. S., et al. Lumacaftor-Ivacaftor in Patients with Cystic Fibrosis Homozygous for Phe508del CFTR. N Engl J Med. 373 (3), 220-231 (2015).
- Van Goor, F., Yu, H., Burton, B., Hoffman, B. J. Effect of ivacaftor on CFTR forms with missense mutations associated with defects in protein processing or function. J Cyst Fibros. 13 (1), 29-36 (2014).
- Neuberger, T., Burton, B., Clark, H., Van Goor, F. Use of primary cultures of human bronchial epithelial cells isolated from cystic fibrosis patients for the pre-clinical testing of CFTR modulators. Methods Mol Biol. 741, 39-54 (2011).
- Randell, S. H., Fulcher, M. L., O'Neal, W., Olsen, J. C. Primary epithelial cell models for cystic fibrosis research. Methods Mol Biol. 742, 285-310 (2011).
- Karp, P. H., Moninger, T. O., et al. An in vitro model of differentiated human airway epithelia. Methods for establishing primary cultures. Methods Mol Biol. 188, 115-137 (2002).
- Sato, T., Vries, R. G., et al. Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche. Nature. 459 (7244), 262-265 (2009).
- Sato, T., Stange, D. E., et al. Long-term expansion of epithelial organoids from human colon, adenoma, adenocarcinoma, and Barrett's epithelium. Gastroenterology. 141 (5), 1762-1772 (2011).
- Clevers, H. Modeling development and disease with Organoids. Cell. 165 (7), 1586-1597 (2016).
- Dekkers, J. F., Wiegerinck, C. L., et al. A functional CFTR assay using primary cystic fibrosis intestinal organoids. Nature Med. 19 (7), 939-945 (2013).
- Dekkers, J. F., van der Ent, C. K., Beekman, J. M. Novel opportunities for CFTR-targeting drug development using organoids. Rare Diseases. 1 (1), e27112 (2014).
- Servidoni, M. F., Sousa, M., et al. Rectal forceps biopsy procedure in cystic fibrosis: technical aspects and patients perspective for clinical trials feasibility. BMC gastroenterology. 13, 91 (2013).
- Ommen, D. D. Z. -. V., Vijftigschild, L. A. W., et al. Limited premature termination codon suppression by read-through agents in cystic fibrosis intestinal organoids. J Cyst Fibros. 15 (2), 158-162 (2016).
- Dekkers, J. F., Gogorza Gondra, R. A., et al. Optimal correction of distinct CFTR folding mutants in rectal cystic fibrosis organoids. Eur Respir J. , (2016).
- Dekkers, J. F., Van Mourik, P., et al. Potentiator synergy in rectal organoids carrying S1251N, G551D, or F508del CFTR mutations. J Cyst Fibros. , (2016).
- Dekkers, J. F., Berkers, G., et al. Characterizing responses to CFTR-modulating drugs using rectal organoids derived from subjects with cystic fibrosis. Sci Transl Med. 8 (344), 344ra84 (2016).
- Li, H., Sheppard, D. N., Hug, M. J. Transepithelial electrical measurements with the Ussing chamber. J Cyst Fibros. 3, 123-126 (2004).
- Sheppard, D. N., Carson, M. R., Ostedgaard, L. S., Denning, G. M., Welsh, M. J. Expression of cystic fibrosis transmembrane conductance regulator in a model epithelium. Am J Physiol. 266 (4 Pt 1), L405-L413 (1994).
- Farin, H. F., van Es, J. H., Clevers, H. Redundant sources of Wnt regulate intestinal stem cells and promote formation of Paneth cells. Gastroenterology. 143 (6), 1518-1529 (2012).
- Drost, J., et al. Organoid culture systems for prostate epithelial and cancer tissue. Nat Protoc. 11 (2), 347-358 (2016).
- Vijftigschild, L. A. W., Berkers, G., et al. β2-adrenergic receptor agonists activate CFTR in organoids and subjects with cystic fibrosis. Eur Respir J. 48 (3), 768-779 (2016).
- Dekkers, R., et al. A bioassay using intestinal organoids to measure CFTR in human plasma. J Cyst Fibros. 14 (2), 178-181 (2015).
- Graeber, S. Y., et al. Intestinal Current Measurements Detect Activation of Mutant CFTR in Patients with Cystic Fibrosis with the G551D Mutation Treated with Ivacaftor. Am J Respir Crit Care Med. 192 (10), 1252-1255 (2015).
- Van Goor, F., et al. Ivacaftor potentiation of multiple CFTR channels with gating mutations. Journal of Cystic Fibrosis: Official Journal of the Eur Cyst Fibrosis. 11 (3), 237-245 (2012).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon