Method Article
Forskolin-induzierte Quellung in Intestinale Organoide: Ein
In diesem Artikel
Zusammenfassung
This protocol describes an assay for measuring CFTR function and CFTR modulator responses in cultured tissue from subjects with cystic fibrosis (CF). Biopsy-derived intestinal organoids swell in a cAMP-driven fashion, a response that is defective (or strongly reduced) in CF organoids and can be restored by exposure to CFTR modulators.
Zusammenfassung
Recently-developed cystic fibrosis transmembrane conductance regulator (CFTR)-modulating drugs correct surface expression and/or function of the mutant CFTR channel in subjects with cystic fibrosis (CF). Identification of subjects that may benefit from these drugs is challenging because of the extensive heterogeneity of CFTR mutations, as well as other unknown factors that contribute to individual drug efficacy. Here, we describe a simple and relatively rapid assay for measuring individual CFTR function and response to CFTR modulators in vitro. Three dimensional (3D) epithelial organoids are grown from rectal biopsies in standard organoid medium. Once established, the organoids can be bio-banked for future analysis. For the assay, 30-80 organoids are seeded in 96-well plates in basement membrane matrix and are then exposed to drugs. One day later, the organoids are stained with calcein green, and forskolin-induced swelling is monitored by confocal live cell microscopy at 37 °C. Forskolin-induced swelling is fully CFTR-dependent and is sufficiently sensitive and precise to allow for discrimination between the drug responses of individuals with different and even identical CFTR mutations. In vitro swell responses correlate with the clinical response to therapy. This assay provides a cost-effective approach for the identification of drug-responsive individuals, independent of their CFTR mutations. It may also be instrumental in the development of future CFTR modulators.
Einleitung
CF wird durch Mutationen in der Mukoviszidose - Transmembran Regulator (CFTR) -Gen verursacht , die eine epitheliale Anionenkanals kodiert. CF betrifft etwa 85.000 Menschen weltweit 1. Über 2.000 CFTR - Mutationen wurden identifiziert ( www.genet.sickkids.on.ca ). Diese Vielfalt erklärt zum Teil , ein breites Spektrum an beobachteten Krankheitsphänotypen ( www.CFTR2.org ) 2, 3. Sechs Klassen von CFTR-Mutationen definiert sind, auf der Grundlage ihrer Wirkung auf CFTR-Protein-Expression und Funktion: (I) keine Synthese, (II) beeinträchtigt Handel, (III) defekte Kanal-Gating, (IV) geändert Leitfähigkeit, (V) reduzierte Mengen von in der Regel CFTR funktioniert, und (VI) beeinträchtigt Zelloberflächenstabilität 4. Obwohl die gemeinsame CFTR-Mutationen gut untersucht sind, die CFTR-Funktion und die Beziehung mit dem klinischen Zustand bleiben poorly verstanden auf der Ebene des Individuums, vor allem für die große Gruppe der seltenen "orphan" Mutationen ( www.CFTR2.org ) 1, 3.
Kürzlich wurden Arzneimittel entwickelt, das CFTR-Protein in einem mutationsspezifischen Art und Weise auszurichten. Zwei Klassen von CFTR-Protein-Targeting Medikamente befinden sich in der klinischen Anwendung und haben unterschiedliche Wirkungsweisen. Potenziatoren, wie VX-770, verbessern die Open-Wahrscheinlichkeit von apikal lokalisierten mutierten CFTR und direkt auf ihre Zugabe zu den Zellen 5 handeln. Korrektoren, wie VX-809, den Handel des endoplasmatischen Reticulum lokalisierten misfolded CFTR wieder herzustellen und erfordern Vorinkubation mit Zellen vor den Auswirkungen 6 beobachtet werden. Das CFTR potentiator, VX-770 wurde für Patienten mit der G551D - Mutation 7, 8, sowie für die acht anderen registriertenCFTR - Gating - Mutationen, einschließlich S1251N 9; gemeinsam werden diese Mutationen durch 5% aller CF Probanden getragen. Andere Studien haben gezeigt , dass VX-770, mit dem Korrektor VX-809 kombiniert, hat begrenzte noch mit erheblichen Auswirkungen auf die Lungenfunktion und führt zu einer Abnahme in Exazerbationsraten in Subjekten homozygot für die F508del von 45-50% der Patienten durch mutation 10, 11.
Herkömmliche Studien arzneimittelreaktions Subjekten innerhalb der verbleibenden 50% der CF-Patienten sind kostspielig und zeitaufwendig und sind nicht durchführbar für Personen mit extrem selten CFTR-Genotypen zu identifizieren. Neuartige, kostengünstige, personalisierte Methoden sind entscheidend, um die wachsende Zahl von CFTR-Modulatoren Personen zuordenbar jede Art von CFTR Mutation trägt. unter Verwendung von mutierten CFTR-Gen-Transfektion in h Bisher hat die Studie die Aufnahme von Patientengruppen tragen bestimmte CFTR-Mutationen wurden durch Studien geführteterologous Zellsysteme, gefolgt von elektrophysiologischen Studien in Ussing - Kammern 5, 6, 12. Aufgrund eines Mangels an ausreichenden CF Tiermodellen, Arzneimittelwirksamkeitsstudien an der Luft-Flüssigkeits-Grenzfläche differenzierten für die Arzneimittelentwicklung 13 bronchialen Epithelzellen abgeleitet von CF Lungen Explantat Materialien wurden 14 verwendet wird , 15. die begrenzte Verfügbarkeit von Lungen Explantation Gewebe und den invasiven Verfahren jedoch zu bronchiale Zellen von Probanden ohne Endstadium der Erkrankung behindern die Analyse seltener CFTR-Mutationen erhalten und Drogentests in einem personalisierten Mode verhindern. Um diese Einschränkungen zu, "easy access" Gewebe, wie kolorektalen Organoiden, nasale Atemwegszellen und Atemwegszellen stammen aus induzierten pluripotenten Stammzellen zu überwinden, werden derzeit für personalisierte medikamentöse Behandlungen erforscht.
Bisher haben wir Protokolle zur Kultur epithelialen Stammzellen aus beliebigen gastrointestinalen Organ in Form von 3D - Organoiden 16, 17. Für den menschlichen Kolon / Rektum beinhalten die Kulturbedingungen definierten Wachstumsfaktoren (Epithelial Growth Factor (EGF), Gastrin, Wnt-3A, R-spondin 3 (Rspo3) und Noggin), kombiniert mit kleinen Molekülen (Nicotinamid, A83-01, und SB202190) in einer Basalmembranmatrix. Unter diesen Bedingungen wachsen einzelne Stammzellen oder kleine Gewebefragmente aus in geschlossene, zystische, 3D-Strukturen durch hochpolarisierten Epithel mit seinem basalen Seite gebildet außen orientiert. Alle Zelltypen erscheinen typischerweise in ihren normalen Verhältnissen und Positionen. Organoide kann durch wöchentliche mechanische Zerstörung und Wieder plating über lange Zeiträume erweitert werden. Sie sind genetisch und phänotypisch stabil und kann gespeichert werden, so dass langfristige Expansion und Bio-Banking - 17. Sie sind zugänglichalle Standard - zellbiologische / genetische Manipulationen und Analysetechniken für 2D - Zelllinien 18 entwickelt.
Wir haben kürzlich gezeigt , dass die CFTR - Funktion kann leicht in kolorektalen Organoiden in einer Forskolin-induzierte Schwellung (FIS) -Test 19, 20 gemessen werden. Wenn ausgesetzt Forskolin (FSK) oder alternativ an Choleratoxin, Organoiden schnell ihre zyklisches Adenosinmonophosphat (cAMP) Spiegel erhöhen, was wiederum in der Öffnung des CFTR - Kanals 19. Organoide von gesunden Individuen oder von Patienten mit CFTR - Mutationen mit Restfunktion zugeordnet ist , wird anschließend als Folge des Ionen- und Wassertransport zu den organoiden Lumen schwellen, die in vitro - Äquivalent von sekretorischen Diarrhoe. Die FIS Antwort von kolorektalen Organoiden wurde zuvor gezeigt, vollständig CFTR-abhängig zu sein, wie abgeleitet von Organoiden angegeben von CFTR-null-Personen einnd durch die Verwendung von spezifischen pharmakologischen Inhibitoren CFTR 19. Große fachspezifische Datensätze können innerhalb weniger Wochen nach der Einnahme eine Biopsie entnommen werden.
Für die FIS - Assay im Detail hier beschrieben, Organoide gezüchtet werden aus rektale Biopsien , die in jedem Alter und nur mit begrenztem Unannehmlichkeit 21 erhalten werden kann. Organoide werden wöchentlich durch mechanische Störung in einzelne Krypten agierten, die leicht wieder verschließen und neue Organoide bilden. Für den FIS - Test läuft, ~ 30-80 dieser gestört wenig Organoide werden in jede Vertiefung einer 96-Well - Platte 19 plattiert. Am Tag des Assays werden die Organoide mit Calcein grün gefärbt, ein fluoreszierendes zellpermeablen Farbstoff, der es innerhalb von lebenden Zellen zurückgehalten wird, Echtzeit-Bildgebung zu erleichtern. Dann Fsk, die die intrazelluläre cAMP erhöht und aktiviert dadurch CFTR, wird hinzugefügt, um organoide Schwellung zu stimulieren. Potenziatoren, die auf apikal CFTR wirken, werden gleichzeitig zugegeben with der Forskolin, während Korrektoren, die CFTR Handel wiederherzustellen 24 h vor der Zugabe von Fsk zugegeben. Die organoiden Quellung wird durch eine automatisierte Bildanalyse quantifiziert, die in der Gesamtfläche aller fluoreszierender Objekte für jeden Zeitpunkt auf Forskolin zusätzlich die relative Zunahme berechnet.
3D organoiden Schwellung Vor- und Nachteile gegenüber bestehenden elektro CFTR Ablesungen in 2D in Ussing-Kammern kultiviert Atemwegszellen liefert. Ein Hauptvorteil ist der Durchsatz des Quelltest. Die Zellen werden kultiviert und untersucht eine einzige Art von Kulturmedium verwenden, und ein erfahrener Techniker kann die Kultur bis zu 25 organoiden Proben auf einer wöchentlichen Basis, während rund 1.200 Datenpunkte pro Woche in 12 Patientenproben zu quantifizieren. Wir geben üblicherweise einen einzigen experimentellen Bedingungen durch doppelte oder dreifachen Messungen pro Platte und wiederholen Sie solche Messungen bei drei unabhängigen Inkubationszeit Punkte. Insgesamt etwa 300 bis 500 single organoide Strukturen werden dann pro experimentellen Bedingungen gemessen, die mit begrenzten technischen Variabilität sehr präzise Messungen der CFTR-Funktion führt. Diese Präzision ermöglicht es uns, deutliche Unterschiede definieren in Restfunktion und die Reaktion auf CFTR - Modulatoren und ermöglicht es uns leicht genetischen Hintergrund Effekte zwischen Patienten tragen identische CFTR - Mutationen 19, 22, 23, 24, 25 aufzunehmen. Die Datenqualität kann leicht von Mikroskopbildern beurteilt werden. Während FIS vollständig CFTR-abhängig ist, ist es ein indirektes Ergebnis Maßnahme für CFTR-Funktion, dessen Auslesung durch die Kopplung des Ionentransports zu den Fluidtransport verursacht. Dies steht im Gegensatz direkte CFTR - Funktion Messungen in Ussing - Kammern, die transepithelialen Ionenströme 26 messen. Ussing-Kammern ermöglichen die Auswahl Stimulation der apikalen oder basolateralen compartments (die die organoiden Test nicht erlaubt); von permeabilisierender basolateralen Membranen kann die apikal CFTR-abhängige Anion Sekretion selektiv 27 gemessen werden.
Protokoll
(; TcBio # 14-008 UMCU) Alle Experimente unter Verwendung von menschlichen Geweben beschrieben hier wurde von der Ethikkommission der Universität Medical Center Utrecht genehmigt. Die Einwilligungserklärung für die Gewebesammlung, Erzeugung, Speicherung und Nutzung der Organoide wurde von den Patienten an Wilhelmina Kinderkrankenhaus (WKZ) -UMCU erhalten.
| Ausrüstung | Verbrauchsgut | Werkzeuge |
| Laminarströmungsabzug | 15 und 50 ml konische Röhrchen | Zeiss LSM 800 - Zen 2 (blaue Ausgabe) Software für Bilder Messen |
| CO 2 -Inkubator | Mikrozentrifugenröhrchen | Microsoft Excel-Programm |
| Zellkultur-Mikroskop (Licht / Lichtmikroskop) | 0,22 um Filter | |
| Zentrifuge | Die serologischen Pipetten | |
| Roll Shaker | Mikrofilterspitzen | |
| 4 ° C Zimmer oder 4 ° C Kühlschrank für Inkubator | Kryoröhrchen | |
| Coolcell Zell Container Einfrieren | ||
| Die serologischen Pipetten | ||
| Micropippette (1000, 200 und 20 & mgr; l) | ||
| Viaflo Wiederholen Pipette | ||
| (Live-Zelle) Konfokalmikroskop | ||
| Computer | ||
| Flüssigstickstofftank | ||
| Mehrkanal (200 ul) |
1. Vorbereiten Reagenzien für die Kultur
Hinweis: Alle Schritte werden in einem Biosicherheitsschrank und nach einheitlichen Richtlinien durchgeführt, um mit Zellkulturen zu arbeiten. Um die Bildung von schönen Tropfen Basalmembranmatrix zu erleichtern, wurde eine vorgewärmte Lager von 96-, 24- und 6-Well-Platten im Inkubator bei 37 ° C halten.
- Basal Medium Vorbereitung
HINWEIS: Basal Medium (BM) bezieht sich auf erweiterte Dulbeccos Modified Eagle Medium mit Hams Nutrient Mixture F-12 (Ad-DF), das mit 4- (2-hydroxyethil) -1piperazineethanesulfonic Säure (HEPES), Glutamin und Penicillin / Streptomycin (Pen / Strep).- In einem 500-ml Ad-DF-Medium Flasche, 5 ml 200 mM Glutamin, 5 ml 1 M HEPES und 5 ml Pen / Strep-Lösungen (10.000 U / ml, 10.000 ug / ml).
- Speicher BM im Kühlschrank bei 4 ° C für mindestens 4 Wochen.
- Wnt-3A-konditioniertem Medium Vorbereitung
HINWEIS: Wnt-3A-konditionierte Medium wird in-house gemacht using der L-Wnt-3A-Zelllinie gemäß den Anweisungen des Herstellers.- Für die Ernte der Wnt-3A-konditioniertes Medium, sammeln das Medium zu den Zellen für eine Woche ausgesetzt und drehen Sie es für 5 Minuten bei 450 × g bis zu schwimmenden Zellen zu entfernen.
- Filtriere den Wnt-3A-konditioniertem Medium durch einen 0,22 um-Filter und teilen sie in 40 ml-Aliquots in 50 ml konischen Röhrchen. Lagern sie bei 4 ° C für mindestens 4 Monate ohne Aktivitätsverlust.
- Testen der Aktivität des Wnt-3A-konditioniertes Medium in einem TOP / FOP Assay menschlicher embryonaler Niere (HEK) -293 - Zellen , transfiziert mit TOP- und FOP-Luciferase und Renilla TK- und gemessen mit einem Renilla Verwendung -luciferase Testkit gemäß Anweisungen des Herstellers.
HINWEIS: TOP-Luciferase ist ein Reporter-Plasmid, das Wildtyp-TCF-Bindungsregionen enthält. Wenn die Wnt-3A-konditionierten Medium aktiv ist, wird die kanonische Wnt aktiviert. Beta-Catenin transloziert in den Zellkern Witz zu assoziierenh TCF / LEF-Transkriptionsfaktoren und aktiviert die Transkription des Luciferase-Reporter, eine Zunahme der relativen Luciferase-Aktivität zu induzieren, wenn das Substrat hinzugefügt wird. Die FOP-Luciferase wird als negative Kontrolle verwendet, da die TCF Regionen stromaufwärts des Luciferase-Gens Bindung mutiert sind.
- Colon Medium Vorbereitung
HINWEIS: Bereiten Sie und alle Wachstumsfaktoren und Reagenzien verdünnen nach den Empfehlungen der Hersteller. Verwenden Sie kleine Größe Aliquots ein gesperrtes Gefrier-Auftau-Zyklen. Funktionelle Wachstumsfaktoren sind von wesentlicher Bedeutung für die Ergebnisse.- Bereiten Sie Kolon Medium (CM) durch Ergänzung BM mit 1x B27, 1,25 mM N-Acetylcystein, 50 ng / ml hEGF, 5 nM Gastrin, 10 mM Nicotinamid, 300 ng / ml hRspo3, 100 ng / ml hNoggin, 500 uM A83-01 , 10 & mgr; M SB202190 und 100 & mgr; g / ml eines antimikrobiellen für Primärzellen.
- Teilen Sie die CM in aliquote Teile und frieren sie bei -20 ° C für bis zu 4 Monaten. Auftauen Aliquots vollständige Doppelpunkt vorzubereitenMedium (FCM) um 50% Zugabe von Wnt-3A-conditoned Medium zum CM. Store FCM bis zu 7 Tage bei 4 ° C ohne Aktivitätsverlust.
- Für die Einrichtung eines organoiden Kultur von rektalen Biopsien, ergänzen FCM mit 50 ug / ml Vancomycin, 50 ug / ml Gentamycin und 10 & mgr; M rho-assoziierte Coiled-Coil-bildende Protein-Serin / Threonin-Kinase-Inhibitor (RhoKi). Verwenden Sie dieses Medium, die so genannte Isolationsmedium (IM), nur für die ersten zwei bis drei Tagen in der Kultur.
- EDTA - Stammlösung Vorbereitung
- Bereiten 0,5 M Ethylendiamintetraessigsäure (EDTA), pH 8, in ultrareines H 2 O, mit einem 0,22 um - Filter sterilisiert.
- Eine Manipulation der Basalmembranmatrix
- Bereiten Sie die Basalmembranmatrix (BMM) gemäß den Empfehlungen des Herstellers.
- Thaw BMM über Nacht auf Eis.
- Bei der Übertragung der BMM aus der Flasche zu einem 15 ml konischen Röhrchen, die Verwendungeine 5 ml-Pipette und eine 15 ml konischen Röhrchen bei -20 ° C vorgekühlt.
- Nach dem Auftauen, speichern Sie die BMM in einem Kühlschrank bei 4 ° C und für mindestens 30 bis 60 Minuten vor der Verwendung auf Eis inkubiert.
HINWEIS: Um die besten Ergebnisse zu erzielen, muss der BMM kalt sein und richtig gemischt, bevor sie Krypten oder Organoide einzubetten.
2. Festlegung Colon Organoide von einer CF-Patienten Biopsy
HINWEIS: Nach Gewebesammlung ist es wichtig , um die Probe auf Eis in Kochsalzlösung, Dulbecco-phosphatgepufferter Kochsalzlösung ohne Ca 2+ und Mg 2+ (DPBS) oder BM aufrechtzuerhalten. Schnelle Verarbeitung der Biopsien wird empfohlen, aber es hat sich als möglich organoiden Kulturen aus Biopsien auf Eis gelagert zu etablieren für bis zu 7 Tage.
- Lassen Sie die Biopsien am Boden eines 15 ml konischen Röhrchen absetzen und den Überstand zu entfernen.
- 10 ml DPBS zu den Biopsien und Pipette auf und ab 10-20 mal eine 10 ml Pipette.
HINWEIS: Die Pipette muss mit BM werden vorbenetzt vor der Biopsie Pipettieren. - Lassen Sie die Biopsien am Boden absetzen und den Überstand zu entfernen.
- Wiederholen Sie die Schritte 2.2 und 2.3 4-5 mal, bis der Überstand klar ist.
- 10 ml DBP und 200 & mgr; l EDTA (0,5 M) zu den Biopsien und legen Sie den Schlauch auf einem Schwingrohr-Plattform für 60-120 min bei 4 ° C.
Hinweis: Die Inkubationszeit pro Patient unterscheiden. Wenn Krypten freigegeben werden, wird DPBS trüb. EDTA Inkubation kann abgeschlossen werden, wenn Krypten unter einem Mikroskop beobachtet werden. - Lassen Sie die Krypten zu begleichen. Überstand verwerfen.
- Nehmen Sie bis 2 ml BM und fügen Sie es zu einem neuen 15 ml konischen Röhrchen. Schütteln diese neue Rohr manuell in der Weise, dass die innen mit BM bedeckt.
- Mit einer Pipette mit BM vorbenetzt, 2 ml DPBS in das Röhrchen die Biopsien und Pipette auf und ab 10-20 mal enthalten.
- Lassen Sie die Biopsien zu begleichen und die DPBS mit den Krypten auf den neuen übertragenRöhre, die 2 ml BM enthält, die in Schritt 2.7 hergestellt.
- Wiederholen Sie die Schritte 2.8 und 2.9, bis keine mehr Krypten freigegeben werden.
- Drehen Sie die Krypten nach unten bei 130 g für 5 min bei 8 ° C.
- In der Zwischenzeit übertragen IM auf den Sicherheitsschrank bei Raumtemperatur (RT).
- Überstand verwerfen und 10 ml BM zur Krypta Pellet und wiederholen Sie den Schritt 2.11.
- Resuspendieren des Pellets in 1 ml BM. Nehmen Sie 5-10 ul und zählen die Anzahl der Krypten mit dem Auge unter dem Mikroskop.
- Drehen Sie die Krypten nach unten bei 130 g für 5 min bei 8 ° C.
- Entfernen Sie den Überstand und das Pellet in 55% BMM (v BMM v IM).
HINWEIS: Die Krypten in dem entsprechenden Volumen von 55% BMM in 1 Krypta pro ul resuspendiert. Wenn nicht genügend Krypten sind, ist das Mindestvolumen von 40 ul BMM. - Für Aussaat, Pipette 35 ul pro Vertiefung (in einer 24-Well-Platte). Teilen Sie die 35 & mgr; l von BMM in 3-5 Tropfen getrennt, um die Diffusion von GRO zu verbessernwth Faktoren in den BMM. Nicht Blasen erstellen.
- Setzen Sie und lassen Sie die Platte den Kopf in den Inkubator bei 37 ° C für mindestens 20 min für die BMM zu verfestigen.
- In 500 ul IM pro Vertiefung und halten Sie es in den Inkubator bei 37 ° C und 5% CO 2.
- Aktualisieren Sie das Medium alle 2-3 Tage. Entfernen Sie das alte Medium, indem sie mit einer P1000 Pipette Pipettieren aus, so dass die BMM intakt fällt. Sorgfältig FCM hinzufügen, indem Sie in der Seite des gut Pipettieren, nicht direkt auf die BMM fällt.
HINWEIS: Wenn keine Krypten im Isolierungsprotokoll freigegeben werden, Zentrifuge den Überstand, waschen Sie das Pellet 2-3 mal mit BM und resuspendieren es in BMM. Nehmen Sie die übrig gebliebenen Gewebe und schneiden Sie es in kleine Stücke mit einem Rasiermesser. Sammeln, diese in einem 15 ml konischen Röhrchen, zentrifugieren und resuspendieren sie in der gleichen BMM. Wenn irgendwelche epithelialen Stammzellen vorhanden sind, werden diese auch Organoide erzeugen.
3. Passagierung von Colon Organoide für Wartung, Einfrieren und fürskolin-induzierte Quellung Assay (FIS)
HINWEIS: Jede organoiden Kultur ihre eigene Verdopplungszeit hat. 3-1: 5-mal alle 7-10 Tage Normalerweise kann colorectal CF Organoiden 1 erweitert werden. Es ist ein gutes Zeichen, wenn angehende Strukturen beobachtet werden. Colorectal CF Organoiden sind weniger zystische (2A - 2C) als kolorektalen normalen Organoiden (2D). Für Einrichtung und Wartung sind Organoide kultiviert in 24-Well-Platten; zum Einfrieren, in 6-Well-Platten; und für den FIS-Assay, in 96-Well-Pasteten.
- Passagierung von Organoide
- Halten Sie die BMM auf Eis für mindestens 30-60 Minuten vor dem Einsatz.
- Halten Sie die FCM bei RT für mindestens 1 Stunde vor dem Einsatz.
- Beschriften Sie eine 15 ml konischen Röhrchen mit dem Probennamen und ein anderes Rohr als "gewaschen".
- aspirieren vorsichtig das Medium aus den Vertiefungen eine P1000-Pipette ohne Störung der BMM fällt.
- 1 ml BM bis 1 gut und bREAK bis die BMM fällt durch einen P1000 Pipette. Übertragen Sie diese 1 ml in 15 ml konischen Röhrchen mit der Probe Namen.
- Waschen Sie die gut mit weiteren 1 ml BM und übertragen sie auf den gleichen 15-ml-Tube.
- Wiederholen Sie die Schritte 3.1.5 und 3.1.6 mit 5 weitere Brunnen (bis zu 6 Vertiefungen einer 24-Well-Platte wird in einem 15 ml konischen Röhrchen gewaschen werden).
- Füllen Sie das Rohr bis zu 12 ml mit BM. Pipette nach oben und unten eine vorbenetztes 5 ml Pipette.
- Spin bei 85 × g für 5 min bei 8 ° C.
- Überstand verwerfen und 1 ml BM zu dem Pellet. Mit der gleichen P1000 Pipettenspitze, nehmen Sie eine P10 Spitze ohne Filter auf und Pipette nach oben und unten 20-mal. Entsorgen Sie beide P1000 und P10 Tipps.
- 4 ml BM mit einer 5 ml Pipette und halten das Rohr bei etwa 70 ° von der Vertikalen zur Seite geneigt. Vorbefeuchtenden eine neue P1000 Spitze und kräftig 2-3 mal mit dem P1000 (1 ml Volumen) mischen.
- Zählen Sie bis 10, während in der gekippten Position verbleibt, sammeln die oberste Schicht sorgfältig wit der P1000-Pipette und Transfer 4 x 1 ml in die Röhre, die als "gewaschen".
- Beachten Sie die Organoide auf den Boden in der gekippten Rohr begleicht ungestörter Organoiden und größere Brocken wird auf den Boden sinken. Zentrifugation der 15 ml für 5 min bei 85 Rohr xg und 8 ° C "ausgewaschen".
- Überstand verwerfen und fügen Sie die erforderliche Menge an Medium und BMM zum organoiden Pellet bis zu einer Endkonzentration von 55% BMM. Mischen durch Pipettieren auf und ab , ohne die Schaffung Blasen (3B).
HINWEIS: Eine gute Dichte durch Animpfen 25-30 Organoiden in 10 ul BMM erreicht wird. - Führen Sie die Schritte 2,17-2,19.
- Die Passage für Freezing
- Halten Sie die BM in Eis für mindestens 30-60 Minuten vor dem Gebrauch. Halten Sie die FCM bei RT für mindestens 1 Stunde vor dem Gebrauch.
- Bereiten Sie FCM ergänzt mit RhoKi (Schritt 1.3.3).
- Nehmen Sie Trypsin aus dem Kühlschrank und lassen Sie es bei RT für mindestens 30 min vor dem Gebrauch.
- Folgen Sie den Schritten 3.1.5-3.1.10.
- Entfernen Sie so viel Überstand wie möglich, 4 ml Trypsin und Vortex für 30 Sekunden.
- Setzen Sie das Rohr in einem warmen Wasserbad bei 37 ° C für 1 min und Vortex kräftig für 30 Sekunden.
- Überprüfen Sie die Lösung in der Röhre. Wenn intakte Organoiden noch unter dem Mikroskop sichtbar sind, wiederholen Sie Schritt 3.2.7.
- Wenn die Organoide gestört werden, fügen Sie 8 ml BM die Trypsin und Pipette 10 Mal zu neutralisieren.
- Spin 3 min bei 450 × g bei 8 ° C.
- Überstand verwerfen und fügen Sie die erforderliche Menge an Medium und BMM den Organoiden eine 55% ige BMM-Lösung zu erreichen. Mischen durch Pipettieren von oben und unten, ohne Blasen zu schaffen.
HINWEIS: 1-Verhältnis nach Trypsinierung: Zum Einfrieren Organoiden muss in einem 1 ausgesät werden. - Seed 250 & mgr; l in einer einzigen Vertiefung einer vorgewärmten 6-Well-Gewebekulturplatte, die Herstellung von winzigen, getrennten Tröpfchen von ~ 10 & mgr; l. Legen Sie die Platte den Kopf in den Inkubator bei 37 ° C und lassen Sie dieBMM zu 20-30 min erstarren.
- In 2,5 ml frischem FCM + RhoKi in jeder 6-Well - Platte gut und übertragen Sie die Platte in den Inkubator (3C).
- Die Passage Organoide für den FIS - Assay
HINWEIS: In Abhängigkeit von der Anzahl und Größe der Organoide, zwischen 4 und 6 Vertiefungen einer Platte mit 24 Vertiefungen genug für Animpfen 27 Wells einer 96-Well-Platte.- Verarbeiten Sie die Organoide wie aus den Schritten 3.1-3.1.13 beschrieben.
- Das Pellet in 120 ul 50% BMM.
- Bestätigen Sie die Anzahl der Organoide (30-50) in einem 3 ul BMM Tropfen unter dem Mikroskop.
- Platte die Organoide einen einzigen Tropfen von 3 & mgr; l in der Mitte jeder Vertiefung einer 96-Well-Pastete platziert werden.
- Die Platte wird in dem 37 ° C Inkubator für 15 Minuten für die BMM zu verfestigen; Weitere Schritte werden in Schritt 6.1.1 beschrieben.
4. Einfrieren Colon CF Organoide
HINWEIS: Orgeloids bereit sind 1-2 Tage nach Trypsinisierung und Kultivierung werden eingefroren, so Organoiden noch klein sein, was die Effizienz des Überlebens nach dem Auftauen erhöht.
- 1 ml der BM und brechen die BMM eine P1000 Pipettentropfen verwenden. Transfer zu einem 15 ml konischen Röhrchen.
- Waschen Sie die gut mit weiteren 1 ml BM und Übertragung auf den gleichen 15-ml-Tube.
- Wiederholen Sie die Schritte 4.1 und 4.2 mit allen Vertiefungen.
HINWEIS: Um überschüssige BMM vermeiden, 3 Vertiefungen einer 6-Well-Platte werden in einem 15-ml-Röhrchen vereinigt. - Füllen Sie die 15-ml-Röhrchen, die Organoide mit 12 ml kaltem BM und Pipette nach oben und unten mit einer 5 ml Pipette enthält. Lassen Sie das Röhrchen auf Eis für 5 min.
- Spin 3 min bei 450 · g und 8 ° C und entfernen Sie den Überstand.
- Man löst das Pellet von Organoiden mit Einfriermedium und Pipette nach oben und unten richtig die Organoide wieder zu suspendieren.
HINWEIS: 500 ul Einfriermedium wird für jeweils 100 & mgr; l BMM verwendet. - Mit einem 5-ml-Pipette, Transfer 0,5 mlOrganoiden in Einfriermedium resuspendiert Kryoröhrchen zu steril.
- Übertragen Sie die Fläschchen in eine Zelle Gefrierbehälter und setzen sie bei -80 ° C.
- Nach 24 Stunden, übertragen Sie die Fläschchen für die Lagerung in flüssigem Stickstoff.
5. Aufbau Kulturen von Gefrorene Organoide
HINWEIS: Um die BMM auf Eis auftauen und auf Eis halten. Lassen Sie die BM RT erreichen und erwärmen 10 ml aliquoten bis 37 ° C, bevor das Verfahren zum Auftauen eines Cryovial beginnen.
- Tauen Sie das Fläschchen schnell durch Rühren in einem C-Wasserbad 37 ° bis dort noch ein wenig gefrorenes Material ist.
- Übertragen Sie die aufgetauten Organoiden zu einem 15 ml konischen Röhrchen eine P1000 Pipette.
- Unmittelbar danach 1 ml warmem BM Tropfen für Tropfen, während die Unterseite des Rohres schütteln. Sobald die 1 ml Medium hinzugefügt wird, vorsichtig mischen durch Pipettieren nach oben und unten ein paar Mal das Gefriermedium zu verdünnen.
- Langsam (tropfen) 9 ml warmem BM zu dem konischen Rohr conta hinzufügenining die Organoide. Invert ein paar Mal.
- Drehen die Zellsuspension 3 Minuten bei 85 x g und 8 ° C.
- Überstand vorsichtig verwerfen, ohne das Pellet zu stören. Resuspendieren organoiden in 90 ul FCM ergänzt mit RhoKi (Schritt 1.3.3). Dann fügen Sie 110 ul BMM.
- In 35 ul zu jeder Vertiefung einer vorgewärmten Platte mit 24 Vertiefungen, so dass winzige, getrennt Tröpfchen.
- Übertragen Sie die Platte mit dem 37 ° C Inkubator, um die Platte zu verlassen den Kopf für 20-30 min.
- In 500 ul FCM mit RhoKi in jede Vertiefung und übertragen Sie die Platte zurück in den Inkubator (4A - 4C).
- Sobald Organoiden richtig aus dem Auftauen erholt haben, in mehr BMM verdünnen, so dass jeweils 10 ul BMM 25-30 Organoiden enthält. Und sorgt für die richtige Entwicklung des organoiden - Dieser Vorgang kann 2-3 Tage nach dem Auftauen (4G 4D) durchgeführt werden.
6. Forskolin-induzierte Quellung Wiesagen (FIS)
HINWEIS: Fsk Titration ermöglicht die Messung von CFTR Restfunktion. Für CFTR Modulation werden Organoiden zu einem gegebenen Korrektor ausgesetzt (beispielsweise VX-809) und / oder Potentiators (beispielsweise VX-770), je nach Genotyp. Üblicherweise VX-809 hinzugefügt wird 18-24 h vor der Messung, während VX-770 und Fsk hinzugefügt werden unmittelbar vor Beginn der Messungen. Seien Sie sich bewusst, dass einige Modulatoren (Korrektoren / potentiators) an der Kunststoffoberfläche der Assayplatte binden kann.
- Überzug für den Assay
HINWEIS: VX-809 Bestände werden bei 20 mM und gelagert bei -80 ° C aliquotiert. Beim Auftauen bei RT verlassen und vor Licht schützen.- Verarbeiten Sie die Organoide, wie in Abschnitt 3.3 beschrieben.
- Wenn die Prüfung der VX-809 Korrektor, bereiten eine Dosis-Wirkungs-Kurve in dreifacher Ausführung mit den folgenden Konzentrationen: 0,0003, 0,003, 0,03, 0,3, 3,0 und 30 & mgr; M. Bereiten Sie die Verdünnungen in FCM.
- Zum 96-Well-Platte, fügen Sie entweder 100 μ; Mit den jeweiligen VX-809-Konzentration oder 100 ul FCM von FCM l nur und die Platte inkubiert.
- Die Messung der Assay
HINWEIS: VX-770-Aktien werden bei 20 mM portioniert, während Fsk bei 10 mM ist; beide werden bei -80 ° C gelagert. Beim Auftauen bei Raumtemperatur belassen und vor Licht schützen.- Nehmen Sie ein Fläschchen mit Calcein und DMSO und lassen für 15 Minuten bei RT.
- In 5,1 ul DMSO in das Fläschchen, wo die Calcein als Pulver zur Verfügung gestellt, wenn ungeöffnet. Andernfalls verwenden Sie eine bereits wieder suspendiert Calcein Fläschchen 2,5 ul von Calcein enthält.
- In 2,5 ul von Calcein bis 580 & mgr; l von BM in einem 1,5-ml-Röhrchen und beschriften Sie es.
- In 10 ul dieser Farbstofflösung (BM + Calcein) in jede Vertiefung eine Wiederholung Pipette.
- Resuspendieren einmal mit einem mehrkanaligen, um sicherzustellen, dass der Farbstoff gut vermischt wird.
- Inkubieren der Platte in einem 37 ° C Inkubator für 30 min.
- Während der Calcein Inkubation, starten Sie die Fsk Vorbereitungund VX-770-Lösungen, wenn nötig.
- Bei Verwendung eines VX-770 potentiator, bereiten eine Dosis-Wirkungs-Kurve in dreifacher Ausfertigung mit den folgenden Konzentrationen: 0,0003, 0,003, 0,03, 0,3, 3,0 und 30 & mgr; M. Im Falle eines Fsk Titration sind die Konzentrationen: 0, 0,008, 0,02, 0,05, 0,12, 0,32, 0,8, 2,0 und 5,0 uM. Bereiten Sie die Verdünnungen in BM.
HINWEIS: Für Fsk, VX-770, oder jede andere am zweiten Tag zugegeben Medikament, müssen die Verdünnungen bei 2x Endkonzentration hergestellt werden, da 100 ul Fsk / Arzneimittel Titrierlösung wird zu jeder Vertiefung gegeben werden, die bereits 100 ul enthalten von FCM. - Übertragen Sie die Fsk und VX-770-Lösungen, eine p200-Pipette und Tipps zum Mikroskop Raum.
- Für die Abbildung des FIS - Assay verwenden , um eine Live - Cell - Imaging - konfokalen Mikroskop mit einem automatisierten Bühne ausgestattet, eine beheizte Kammer, und CO 2 fließen.
HINWEIS: Die folgenden Schritte zu einem bestimmten Mikroskop beziehen. Verschiedene Einstellungen sollten auf andere Mikroskope folgende Herstellers geltenAnleitung. - Legen Sie die 96-Well-Platte in den Plattenhalter.
- Geben Sie die konfokale Einstellungen für die Bildgebung.
- Preset die Live - Imaging - Tool auf 37 ° C und 5% CO 2 und ließ die Kammer vorge inkubieren für mindestens 30 Minuten vor der Messung.
- Mit der "Smart Setup" Option, die Alexa Fluor-488-Titel zu wählen.
- Stellen Sie die 5X Objektiv und Scan-Bereich zu 0,6x zu verkleinern und erfassen die gesamte gut.
- Passen Sie die Laserleistung und die Empfindlichkeit des Detektors die optimale Detektion von Calcein-grün markierten Organoiden über den Hintergrund zu ermöglichen. Das Pinhole kann auf 130 & mgr; m erhöht werden, und die Bildmittelung kann auf 2 gesetzt werden.
- Stellen Sie die Bit-Tiefe bei 8 und die Bildgröße auf 512 x 512.
- Verwenden Sie die Zeitreihe Option, um die Messzeit, Frequenz einzustellen, und Intervalle.
HINWEIS: Empfohlene für regelmäßige Messungen: 1 Std 10 min Intervall: Zyklen = 7 (Zyklus 1 ist T = 0). Bei Messungen von reduzierter Schwellung, orgaphyllen kann für bis zu 3 Stunden abgebildet werden. - Verwenden Sie die Kachel-Option, um manuell die einzelnen Positionen gut bestimmen.
- Füge 100 & mgr; l des FSK- und / oder VX-770-Lösungen in die entsprechenden Wells, in der gleichen Reihenfolge wie die Messung. Starten Sie die Lösungen in der ersten Zugabe bebildert gut und weiterhin mit der Imaging-Reihenfolge.
- Starten Sie die Messung.
- Nachdem das Experiment beendet ist, speichern Sie die Datei.
- Die Analyse der FIS Assay Daten
- Erstellen Sie eine "organoide Analyse" Makro für die Datenanalyse des FIS-Test, um die Analyse-Tool in einer Bildanalyse-Software, die alle Strukturen durch die Alexa-488-Spur abgebildet erkennt und füllt die identifizierten Strukturen die Zunahme der gesamten organoiden Fläche über die zur Berechnung verschiedenen Zeitpunkten.
- Öffnen Sie die Datei mit den aufgenommenen Bildern in der Bildanalyseprogramm.
- Wählen Sie das Makro für organoiden Analyse.
- Stellen Sie den Schwellenwert des Signal-zu-Rausch-Verhältnis in einem gut zu dem Zeitpunkt 1 und gewährleisten zu balancieren, dass alle organoide Strukturen erkannt und gefüllt.
- Überprüfen Sie in 4-6 Brunnen zu sehen, ob alle Strukturen auch zu einem Zeitpunkt erkannt werden, 7. leicht die Schwelle ändern, um sicherzustellen, dass die Hintergrundsignale zu dem Zeitpunkt 7 nicht als Strukturen erkannt (die spezifische Schwelle kann etwas zwischen den Experimenten ändern).
- Legen Sie die Kriterien der minimalen Flächengröße von erkannten Objekten bis 1000 um 2.
- Drücken Sie die "Analyse" zu starten. Die Analyse dauert ca. 3 min, abhängig von der verwendeten Software.
- Wenn die Software fertig ist, gehen Sie auf "Tabelle erstellen" und wählen Sie die folgenden Daten: gut Zahlen (Tabelle in dieser Reihenfolge erhöhen sollte), Zeitpunkte und Gesamtfläche pro Vertiefung.
- Speichern Sie die Datei als .xlm in ein Tabellenkalkulationsprogramm zu exportieren.
- In diesem Programm berechnet die relative Zunahme der Fläche pro well durch den Bereich der Zeitpunkt 1 auf 100% einstellen. Berechnen Sie die Fläche unter der Kurve (AUC) von Zeitpunkten 1-7 pro Zustand; die untere Grenze des Bereichs (Y-Wert) wird auf 100% gesetzt. Fsk oder Drogen Titrationen (X-Achse) aufgetragen gegen die AUC (Y-Achse).
Ergebnisse
1A zeigt eine repräsentative frische Isolierung von Krypten auf BMM eingebettet. Die Krypten sind aus einem kolorektalen Biopsie einer CF Thema. Üblicherweise wird ein organoid aus jeder Krypta (1A - C) erzeugt. Aufgrund der Funktionsstörung der CFTR, sind die meisten der colon CF Organoide nicht cystic, sondern sind kompakt und mit Vorsprüngen und buddings (2A - 2B). Allerdings organoiden einige CF Kulturen, vor allem bei hohen Restfunktion, haben ein paar Organoide mit zystischer Form (Abbildung 2C), wie Wildtyp organoiden Kulturen (2D).
Bevor Passagieren der Organoide für die Kultur erweitern oder einen FIS - Assay Impfen ist wichtig , dass die Organoide eine große Größe mit mehreren buddings haben, wie in 3A gezeigt. Wenn die Organoide sind klein und ohne nahlreiche buddings wenn für Passagierbarkeit verarbeitet, die organoiden Kultur negativ beeinflusst. Je nach Qualität und Aktivität der wesentlichen Wachstumsfaktoren , wie EGF, Wnt-3A und Rspo3 erreichen die Organoide die gewünschte Größe zwischen 7 und 12 Tage (3A). Nach der mechanischen Störungen werden die buddings gestört und verwendet , um neue Organoiden in der folgenden Passage (3B) zu erzeugen. Wenn die Organoide Verarbeitung zum Gefrieren, ist es wichtig , dass sie auf eine kleine Größe mit Trypsin behandelt werden, wie in 3C dargestellt. Nach Trypsinisierung werden die Organoide für 1 oder 2 Tage überzogen, um sie von dem Stress der Manipulation erholen zu lassen. Dieser Schritt, zusammen mit der geringen Größe der Organoide, sorgt für eine 98% ige Zellwiederherstellung nach (4A) aufgetaut.
Wenn die Organoide aufgetaut werden, ist es wichtig, sie in hoher Dichte zu haben, so normalerweise werden sie in einem aufgetautenkleines Volumen (Abbildung 4a). Nach ein oder zwei Tagen in Kultur, und nach der Feststellung , dass die Organoide Größe zunehmen (4A mit 4B vergleichen - 4C), werden die Organoide in einem Verhältnis von 20-30 Organoide verdünnt pro 10 ul BMM, die richtige Dichte Bereitstellen in eine größere Größe zu wachsen. Wenn die Organoiden zu stark verdünnt werden, können sie das Wachstum verlangsamen und kann sogar zu differenzieren und zu sterben. Wenn die Organoiden zu überfüllt sind, verlangsamt sich der Platzmangel oder der Mangel an Wachstumsfaktoren auch das Wachstum der Organoide und reduziert die Anzahl der buddings.
Die Beschichtung von Organoiden von lebenden Kulturen mit begrenzten Zelltrümmer sollte auf Fsk Stimulation in Bedingungen , in denen> 95% der Organoide quellen führen, vorausgesetzt , dass eine ausreichende CFTR - Funktion vorhanden ist (5A - 5B). Organoide quellen in einem Genotyp und drogenabhängig, wiedargestellt durch repräsentative Bilder von Organoiden mit zwei F508del - Allele (5A) und Organoiden Verbindung-heterozygot für F508del und S1251N (5B), eine Mutation CFTR - Gating mit einem gewissen Restfunktion zugeordnet ist .
Zur Quantifizierung der Schwellung, insgesamt Calcein-grüne Flächen sind für jeden Zeitpunkt ausgewählt und als Prozentsatz von T = 0 (auf 100% gesetzt ; 6A). Debris und kleine, nicht-quellenden Strukturen sind in der Regel weniger als 5% der Gesamtoberfläche. Die relative Flächenzuwachs ist je 10 min Zeitintervall ausgedrückt und AUC (willkürliche Einheiten) Die Messungen werden für jeden Zustand (T = 0 bis 60 min, Basislinien - Schwelle auf 100% gesetzt , 6B) erzeugt wird . Wir fanden AUC die robusteste zu sein, da es eine gewisse Variation in Einleitung der Quellung enthält, sowie eine gekrümmte Beziehung über 30-40 min von Fsk bei hohen CFTR Funktionsebenen.
Restfunktionsmessungen in F508del / F508del Organoiden typischerweise erreichen 0-200 AUC-Einheiten (100-110% der Flächenzunahme nach 60 min von 5 uM Fsk Behandlung) , was zu ~ 2.500-3.500 AUC - Einheiten nach der Inkubation mit CFTR - Modulatoren erhöhen können (VX770 + VX809; 6C). Organoide, die mit CFTR Restfunktion kann bis zu 4.500 Einheiten AUC nach 60 min von 5 uM Fsk Stimulation in Abwesenheit von CFTR-Modulatoren (200-220% Oberfläche von vorge Fsk Bedingungen) erreichen. Organoiden Schwellung erreicht eine Obergrenze bei ~ 4.500 AUC-Einheiten, vermutlich aufgrund der physikalischen Einschränkungen der organoiden Strukturen, die geschwindigkeitsbegrenzenden Wirkung der basolateralen Ionentransport und die Einrichtung von Ionen- und Flüssigkeitstransport Homöostase unter "gestreckt" Bedingungen. Fsk kann den Dynamikbereich des Assays bei diesen hohen CFTR Restfunktion Ebenen weiter ausbauen titriert werden, um eine bessere Restfunktion zu quantifizieren oder hochwirksame Verbindung Behandlung (beispielsweise wie durch die höhere Aktivität der VX770 auf der Quellung von S1251N Organoide nach Stimulation mit niedriger Fsk angegebenen Konzentrationen; 6D).

Abbildung 1: Aufbau von CF kolorektalen Organoiden aus Biopsien. (A) Repräsentative Bilder von isolierten Material aus einer Rektumbiopsie nach dem Einschalten der Isolation Tag (Passage 0, Tag 0) in BMM eingebettet ist. Die Erweiterung der angegebenen Krypta befindet sich auf der rechten unteren Bereich angezeigt. (B) Die gleichen Krypten wurden nach 7 Tagen in Kultur (Passage 0, Tag 7) gefolgt. Die Erweiterung der gleichen Krypta in Tafel A dargestellt wird gezeigt. (C) Repräsentative Bild der gleichen organoiden Kultur 11 Tage nach der Spaltung zu sein (Passage 1, Tag 11). Maßstabsbalken = 100 & mgr; m.
159fig1large.jpg "target =" _ blank "> Bitte hier klicken, um eine größere Version dieser Figur zu sehen.

Abbildung 2: Repräsentative Bilder von CF kolorektalen Organoide von Patienten mit verschiedenen CFTR - Mutationen abgeleitet. Repräsentative Bilder von CF colorectal Organoide von Probanden mit F508del / F508del (A), F508del / R117H-7T (B) und F508del / S1251N (C) Mutationen. (D) Repräsentative Bild eines kolorektalen organoiden Kultur von einem Subjekt Wildtyp- CFTR. Maßstabsbalken = 100 & mgr; m. Diese Bilder wurden ohne Fsk Stimulation erhalten. Bitte klicken Sie hier , um eine größere Version dieser Figur zu sehen.
5159 / 55159fig3.jpg "/>
Abbildung 3: Die Verarbeitung CF Kolon Organoiden für Wartung und Test oder zum Einfrieren. (A) Repräsentative Bilder eines CF colon organoiden Kultur bereit zu verarbeitenden entweder Passagierung (B) oder Einfrieren (C). (B) Nach ihrer mechanischen Störung, kleine Stücke gebildet werden , die die neuen Organoiden im nächsten Durchgang zu generieren. (C) Nach der Trypsinierung, sehr klein ist , sind runde Organoide erzeugt, ihre Lebensfähigkeit während des Gefrierprozesses zu erleichtern. Maßstabsbalken = 100 & mgr; m. Bitte klicken Sie hier , um eine größere Version dieser Figur zu sehen.
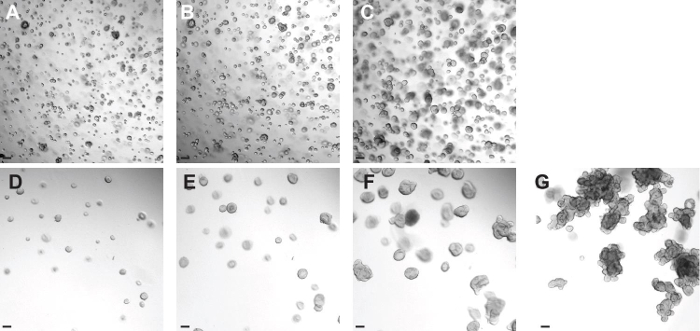
Abbildung 4: einen CF kolorektalen organoiden Kultur aus gefrorenen Organoiden etablieren. ( A - C) Repräsentative Bilder eines CF kolorektalen organoiden Kultur am Tag 0 (A aufgetaut). Bilder aus der gleichen Vertiefung wurden ein (B) und zwei (C) Tage nach der Aufnahme. (D - G) Repräsentative Bilder des Verdünnungsschritt in Abschnitt 5.9 beschrieben. Sobald die Organoide richtig aus dem Auftauen (Tag 3 nach dem Auftauen) erholt haben, werden sie so verdünnt , dass sie Raum zu wachsen (D). Bilder aus der gleichen Vertiefung wurden sechs (E) entnommen, zehn (F), und fünfzehn (C) Tage nach dem Auftauen. Maßstabsbalken = 100 & mgr; m. Bitte klicken Sie hier , um eine größere Version dieser Figur zu sehen.

Abbildung 5: Forskolin-induzierte Schwellung von CFOrganoiden. (A und B) Repräsentative Bilder F508del / F508del (A) oder F508del / S1251N (B) colorectal Organoide vor oder nach 60 min Stimulation mit Fsk (5 & mgr; m) in Abwesenheit oder Anwesenheit von VX-770 (3 & mgr; m]) oder VX-770 in Kombination mit VX-809 (3 & mgr; m). Maßstabsbalken = 200 & mgr; m. Bitte klicken Sie hier , um eine größere Version dieser Figur zu sehen.
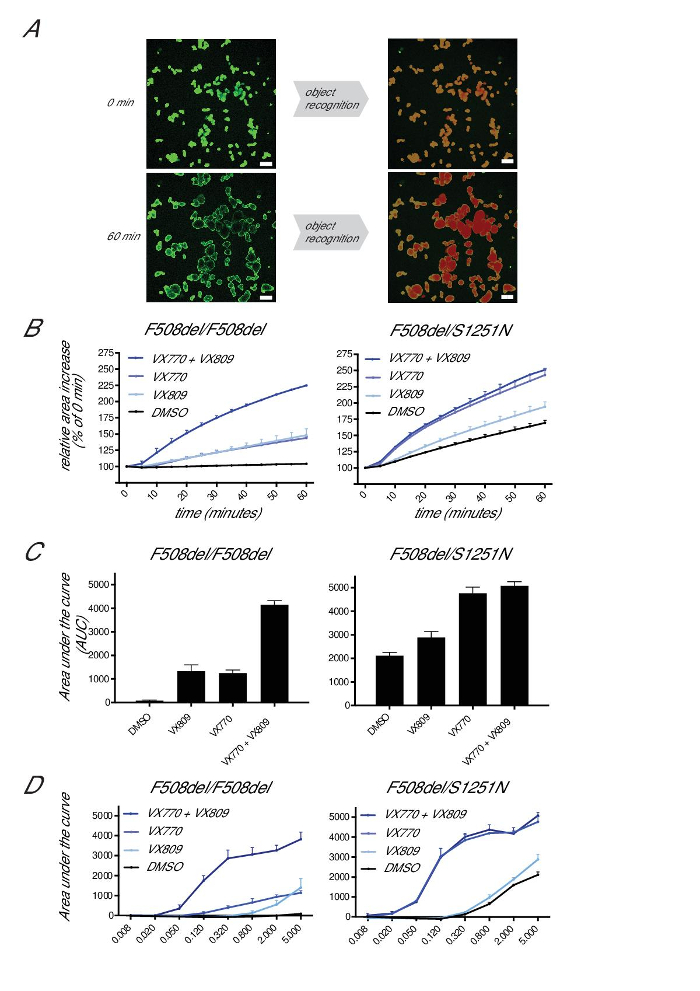
Abbildung 6: Quantifizieren Forskolin-induzierte Schwellung. (A) Repräsentative Bilder von organoiden Bereichsauswahl durch eine Bildanalyse - Software von F508del / S1251N Organoide vor (0 min) und nach 60 min Stimulation mit Fsk (5 uM) und VX770 (3 uM). Maßstabsbalken = 200 & mgr; m. (B) Representative Bilder der relativen Flächenzuwachs von F508del / F508del oder F508del / S1251N Organoide während 60 min von Fsk (5 um) Stimulation in Abwesenheit oder Gegenwart von VX770 (3 & mgr; m) und / oder VX809 (3 um). (C) Fläche unter der Kurve Messungen von Zuständen , die in (B) (T = 60 min, Basislinien - Schwelle = 100%). (D) Fläche unter der Kurve Messungen von F508del / F508del oder F508del / S1251N Organoiden bei verschiedenen Konzentrationen von Fsk. Die Daten stellen die Mittelwerte ± SD von einzelnen repräsentativen Experimenten. Bitte klicken Sie hier , um eine größere Version dieser Figur zu sehen.
Diskussion
Hier bieten wir ein komplettes Protokoll für die Erzeugung, Expansion, Einfrieren und Auftauen von menschlichen kolorektalen Organoiden. Während wir uns vor 17 einige Zeit menschliche organoiden Kulturen etabliert haben, hat es sich manchmal als schwierig erwiesen , die Technologie in anderen Labors ohne zu etablieren praktische Ausbildung. Wir gehen davon aus, dass diese Protokolle eine solche Ausbildung ersetzen wird.
Wnt-3A-konditioniertes Medium ist eines der wichtigsten Reagenzien, um bei der Schaffung und Aufrechterhaltung einer langfristigen organoiden Kultur erfolgreich zu sein. Tatsächlich könnte organoiden Kulturen "Crash", wenn an Wnt-3A-conditoned Medium mit geringer Aktivität ausgesetzt. Da Wnt-3A-konditionierten Mediums im Haus hergestellt ist, gibt es mehrere Aspekte, die berücksichtigt werden müssen, wenn ein aktives Medium zu erzeugen. Aktive Wnt-3A kann nur mit hochwertigen fötalen Rinderserum (FBS), zur Verfügung stellt, die richtigen Wachstumssignale für L-Zellen und die Stabilisierung von hydrophoben in Medium hergestellt werdenWnt-3A-Moleküle. Wenn Wnt-3A - Aktivität niedrig ist (dh niedrige TOP / FOP - Verhältnisse, siehe unten), ist es in der Regel die FBS, die das Problem verursacht.
Kommerzielle rekombinante Wnt funktioniert schlecht, so dass wir es nicht empfehlen als positive Kontrolle für die TOP / FOP Wnt Reporter Assay. Das Verhältnis zwischen TOP / Renilla und FOP / Renilla ist ein Hinweis auf Wnt Aktivität des konditionierten Mediums, so eine gute Partie von Wnt-3A-konditionierten Medium gibt ein TOP / FOP-Verhältnis höher als 25 ist, im Vergleich zu den TOP / FOP-Wert von die negative Kontrolle: Medium nicht an Wnt-3A-produzierenden Zellen ausgesetzt. Rekombinante Noggin und R-spondin kann durch Noggin ersetzt werden und R-spondin konditionierten-Medium 28, 29.
Das aktuelle Protokoll beschreibt auch ein Funktionstest für CFTR-FIS-Test. Wir haben vor kurzem gezeigt , die Beziehung zwischen dem Genotyp und CFTR FIS und wie dies spiegelt veröffentlicht CFTR genotype-Phänotyp - Beziehungen aus klinischen Registern erhalten (www.CFTR2.org) 25. Unter Verwendung dieses Assays werden zwei Personen mit extrem selten CFTR Mutationen wurden identifiziert , deren Organoide waren , die auf Ivacaftor (VX-770) 25. Nachfolgende Verschreibung dieses Medikaments führte zu klaren klinischen Reaktion, um den Wert des FIS-Test hervorheben spezifische Arzneimittel mit seltenen Mutationen in Abwesenheit von Daten aus klinischen Studien mit Patienten zu entsprechen. Wesentlich für die Quantifizierung von FIS sind optimales Wachstum und optimale Assaybedingungen zeigte nur durch einen begrenzten Teil der nicht-quell Organoide (gewöhnlich unter 5%). Hohe Konzentrationen von Ablagerungen führen zur Unterschätzung der Schwellung, als ein größerer Anteil von nicht lebensfähigen, nicht-quellenden Strukturen, die durch die Bildanalyse-Software erkannt werden.
Korrelationen zwischen den in - vitro - FIS Antworten und vorher festgelegten CFTR-abhängige Biomarker (Schweißchloridkonzentration und intestinal Strommessungen) an waren die personalisierte Ebene leicht nachweisbar in unseren früheren Studien 19, 25. Dies unterstützt die Vorstellung, dass Restmessungen Funktion FIS mit auf Patienten mit CF aktuelle Ansätze ergänzen können als diagnostische oder prognostischer Marker in einer persönlichen Art und Weise. Der Durchsatz des FIS - Test im Vergleich zu anderen Biomarker der CFTR - Funktion, wie zum Beispiel Schweißchloridkonzentration Messungen in vivo und Darm-Strommessungen in Ex - vivo - rektale Biopsien, ermöglicht eine bessere Kontrolle der technischen Variabilität. Es bietet auch eine voll CFTR-abhängige Anzeige und einen großen Dynamikbereich durch eine Titration von Fsk verwenden, die genau Typen Rest CFTR-Funktion.
Allerdings reflektiert die FIS-Assay nur die Auswirkungen der einzelnen Genotyps auf die Variabilität der Arzneimittelwirksamkeit, während die Modulation der CF Krankheit um mehr als nur die CFTR-Funktion betroffen ist. Für drug Antwort ist der Test einer potentiellen Gewebeantwort reflektierend. Obwohl sehr präzise in CFTR Messung wird menschliche Variation in Pharmakokinetik nicht einbezogen, wie für andere im Gegensatz in vivo 7, 8 oder direkt ex vivo Messungen CFTR 32. Wie zuvor diskutiert, beeinflussen Phänotyp auch nicht CF Modifizierungsmittel (beide genetischen und Umwelt), eine Trennung zwischen den in vitro Beobachtungen oder CFTR Biomarkern und klinischen Phänotyp 2 verursacht. Ferner wird die Identifizierung von potentiellen reaktions Mutationen unter Verwendung von Zelllinien 33 mit weniger Auswirkungen auf die Patienten assoziiert , die eine rektale Biopsie für die Einrichtung von Organoiden erhalten müssen.
Mehrere CFTR-Targeting Drogen sind derzeit in Entwicklung 1. Es wird erwartet, dass unsere klinischen Studien nicht eine korrekte Vorhersage der klinischen Wirksamkeit b erlaubenasierend auf CFTR-Mutationsstatus allein. Da die FIS-Test CFTR-Funktion und Arzneimittelreaktion funktionell misst, kann es die Methode der Wahl, um zu bestimmen, welches Medikament am besten für die Patienten arbeitet. Der FIS-Test kann auch nützlich sein für die Identifizierung von Patientengruppen in Zulassungsstudien und für die Entwicklung neuer Arzneimittel Modalitäten einbezogen werden. Stimulation of colorectal Organoide mit Plasma vor und während der Behandlung können weitere funktionelle helfen Mengen von CFTR - Modulatoren im Blut quantitativ zu bestimmen Zirkulieren potentiell personalisierte Dosierung zu erleichtern und die Auswahl von Medikamentendosierungen in klinischen Versuchen 30, 31. Schließlich kann der FIS für ein besseres Grundverständnis für die CFTR-Funktion und ihre Wechselwirkungen mit anderen -so weit weitgehend unknown- genetischen Modifikatoren seiner Funktion nützlich sein.
Offenlegungen
Hans Clevers is an inventor on patents for organoid culture and the Forskolin-induced swelling assay. Jeffrey M Beekman is an inventor on a patent for the Forskolin-induced swelling assay. Sylvia F Boj and Robert Vries are employed by the Foundation Hubrecht Organoid Technology (HUB), which holds the exclusive license to the Organoid Technology. Otherwise, the authors have nothing to disclose.
Danksagungen
Diese Arbeit wurde von der HIT-CF-Programm der niederländischen CF-Stiftung (NCFS), ZonMW (40-00812-98-14103) unterstützt, der Wilhelmina Kinderkrankenhaus Research Fund und der Tschechischen Republik und Zilverenkruis / Achmea. Wir möchten S. Heida-Michel, M. Geerdink, KM de Winter-de Groot, und G. Berkers (Abteilung für Pädiatrische Pneumologie, Wilhelmina Kinderkrankenhaus, UMC Utrecht) und RHJ Houwen (Abteilung für Pädiatrische Gastroenterologie, Wilhelmina zu danken Kinderkrankenhaus, UMC Utrecht) für die Patienten heranzugehen und die Biopsien für die Erzeugung eines CF Biobank zu bekommen.
Materialien
| Name | Company | Catalog Number | Comments |
| Advanced Dulbecco’s Modified Eagles Medium with Nutrient Mixture F-12 Hams (Ad-DF) 500ml | Thermo Fisher Scientific: Invitrogen | #12634 | stored at 4 °C |
| GlutaMax | Thermo Fisher Scientific: Invitrogen | #35050 | stored at 4 °C |
| Hepes | Thermo Fisher Scientific: Invitrogen | # 15630-056 | stored at 4 °C |
| Penicillin/Streptomycin | Thermo Fisher Scientific: Invitrogen | #15140-122 | stored at -20 °C |
| 96 well culture plate | Cellstar | #655180 | |
| 24 well culture plate | Cellstar | #662160 | |
| 6 well culture plate | Cellstar | #657160 | |
| Dulbecco's Phosphate Buffered Saline (-) CaCl2 (-) MgCl2) (DPBS) | Life Technologies: Gibco | #14190-094 | stored at 4 °C |
| Dulbecco’s Modified Eagles Medium (DMEM) 500ml | Thermo Fisher Scientific: Invitrogen | #31966-021 | For Wnt-3A Conditioned Medium Production. Stored at 4 °C |
| Fetal Bovine Serum (FBS) | Bovogen | #SFBS LOT#11113 | For Wnt-3A Conditioned Medium Production. Stored at -20 °C |
| L Wnt3A cell line | ATCC | #CRL-2647 | For Wnt-3A Conditioend Medium Production. |
| TOP/FOP plasmids | Millipore | #17-285 | For measuring Wnt activity |
| pTK-Renilla | Promega | #E2241 | For measuring Wnt activity |
| HEK-293 | ATCC | #CRL-1573 | For measuring Wnt activity |
| Dual-Luciferase Reporter Assay System | Promega | #E1910 | For measuring Wnt activity |
| Zeocin | Thermo Fisher Scientific: Invitrogen | #R250-01 | For Wnt-3A Cell line selection |
| B27 supplement | Thermo Fisher Scientific: Invitrogen | #17504-044 | stored at -20 °C |
| N-Acetylcysteine | Sigma Aldrich | #A9165-5G | stored at -20 °C |
| Nicotinamide | Sigma Aldrich | #N0636 | stored at -20 °C |
| Human Epithelial Growth Factor (hEGF) | PrepoTech | #AF-100-15 | stored at -20 °C |
| Gastrin | Sigma Aldrich | #G9145 | stored at -20 °C |
| TGFb type I Receptor inhibitor (A83-01) | Tocris | #2939 | stored at -20 °C |
| Y-27632 dihydrochloride (RhoKi) | Selleckchem | #S1049 | stored at -20 °C |
| p38 MAPK inhibitor (p38i) (SB202190) | Sigma Aldrich | #S7067 | stored at -20 °C |
| Primocin | InvivoGen | #ant-pm-1 | stored at -20 °C |
| Human Noggin (hNoggin) | PrepoTech | #120-10C | stored at -20 °C |
| Human R-spondin 3 (hRspo-3) | R&D Systems | #3500-RS/CF | stored at -20 °C |
| Vancomycin | Sigma Aldrich | #861987- 250mg | stored at -20 °C |
| Gentamycin | Life Technologies: Gibco | #15710-049 | stored at -20 °C |
| Ethylenediamine tetraacetic acid (EDTA) | Sigma Aldrich | #431788 | Stored at 4 °C |
| Matrigel | Corning | #354230 | stored at -80 °C |
| TryplE Express | Life Technologies: Gibco | #12605-010 | for trypsinizing organoids for freezing |
| Recovery Cell Culture Freezing Medium | Life Technologies: Gibco | #12648010 | for freezing |
| Calcein | Life Technologies: Gibco | #C3100MP | stored at -20 °C |
| Forskolin | R&D Systems | #1099-50 mg | stored at -80 °C |
| Lumacaftor (VX-809) | Selleckchem | #s1565 | stored at -80 °C |
| Ivacaftor (VX-770) | Selleckchem | #s1144 | stored at -80 °C |
| Name of Reagents/Material | Solvent | Stock Concentration | Final Concentration |
| GlutaMax | 200 mM | 2m M | |
| Hepes | 1 M | 10 mM | |
| Penicillin/Streptomycin | 10K U/ml 10K µg/ml | 100 U/ml 100 µg/ml | |
| Zeocin | 100 mg/ml | 125 µg/ml | |
| B27 supplement | 100 x | 1 x | |
| N-Acetylcysteine | MiliQ H20 | 500 mM | |
| Nicotinamide | DPBS | 1 M | 10 mM |
| Human Epithelial Growth Factor (hEGF) | DPBS 0.1%BSA | 0.5 mg/ml | 50 ng/ml |
| Gastrin | DPBS | 100 µM | 10 nM |
| TGFb type I Receptor inhibitor (A83-01) | DMSO | 5 mM | 500 nM |
| Y-27632 dihydrochloride (RhoKi) | DMSO | 10 mM | 10 µM |
| p38 MAPK inhibitor (p38i) (SB202190) | DMSO | 30 mM | 10 µM |
| Primocin | 50 mg/ml | 100 µg/ml | |
| Human Noggin (hNoggin) | DPBS 0.1%BSA | 100 µg/ml | 100 ng/ml |
| Human R-spondin 3 (hRspo-3) | varies per lot | 300 ng/ml | |
| Vancomycin | 10 mg/ml | 50 µg/ml | |
| Gentamycin | 10 mg/ml | 50 µg/ml | |
| Ethylenediamine tetraacetic acid (EDTA) | MiliQ H20 | 0.5 M | 2 mM |
| Calcein | DMSO | 10 µg/ml | 3.3 ng/ml |
| Forskolin | DMSO | 10 mM | variable |
| Lumacaftor (VX-809) | DMSO | 20 mM | variable |
| Ivacaftor (VX-770) | DMSO | 20 mM | variable |
Referenzen
- De Boeck, K., Amaral, M. D. Progress in therapies for cystic fibrosis. Lancet Respir Med. 4 (8), 662-674 (2016).
- Cutting, G. R. Cystic fibrosis genetics: from molecular understanding to clinical application. Nature Rev Genet. 16 (1), 45-56 (2015).
- Sosnay, P. R., Siklosi, K. R., et al. Defining the disease liability of variants in the cystic fibrosis transmembrane conductance regulator gene. Nature Genet. 45 (10), 1160-1167 (2013).
- Zielenski, J. Genotype and phenotype in cystic fibrosis. Respiration. 67 (2), 117-133 (2000).
- Van Goor, F., Hadida, S., et al. Rescue of CF airway epithelial cell function in vitro by a CFTR potentiator, VX-770. Proc Natl Acad Sci U.S.A. 106 (44), 18825-18830 (2009).
- Van Goor, F., Hadida, S., et al. Correction of the F508del-CFTR protein processing defect in vitro by the investigational drug VX-809. Proc Natl Acad Sci U.S.A. 108 (46), 18843-18848 (2011).
- Accurso, F. J., Rowe, S. M., et al. Effect of VX-770 in persons with cystic fibrosis and the G551D-CFTR mutation. N Engl J Med. 363 (21), 1991-2003 (2010).
- Ramsey, B. W., Davies, J., et al. A CFTR potentiator in patients with cystic fibrosis and the G551D mutation. N Engl J Med. 365 (18), 1663-1672 (2011).
- De Boeck, K., Munck, A., et al. Efficacy and safety of ivacaftor in patients with cystic fibrosis and a non-G551D gating mutation. J Cyst Fibros. 13 (6), 674-680 (2014).
- Boyle, M. P., Bell, S. C., et al. A CFTR corrector (lumacaftor) and a CFTR potentiator (ivacaftor) for treatment of patients with cystic fibrosis who have a phe508del CFTR mutation: a phase 2 randomised controlled trial. Lancet Respir Med. 2 (7), 527-538 (2014).
- Wainwright, C. E., Elborn, J. S., et al. Lumacaftor-Ivacaftor in Patients with Cystic Fibrosis Homozygous for Phe508del CFTR. N Engl J Med. 373 (3), 220-231 (2015).
- Van Goor, F., Yu, H., Burton, B., Hoffman, B. J. Effect of ivacaftor on CFTR forms with missense mutations associated with defects in protein processing or function. J Cyst Fibros. 13 (1), 29-36 (2014).
- Neuberger, T., Burton, B., Clark, H., Van Goor, F. Use of primary cultures of human bronchial epithelial cells isolated from cystic fibrosis patients for the pre-clinical testing of CFTR modulators. Methods Mol Biol. 741, 39-54 (2011).
- Randell, S. H., Fulcher, M. L., O'Neal, W., Olsen, J. C. Primary epithelial cell models for cystic fibrosis research. Methods Mol Biol. 742, 285-310 (2011).
- Karp, P. H., Moninger, T. O., et al. An in vitro model of differentiated human airway epithelia. Methods for establishing primary cultures. Methods Mol Biol. 188, 115-137 (2002).
- Sato, T., Vries, R. G., et al. Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche. Nature. 459 (7244), 262-265 (2009).
- Sato, T., Stange, D. E., et al. Long-term expansion of epithelial organoids from human colon, adenoma, adenocarcinoma, and Barrett's epithelium. Gastroenterology. 141 (5), 1762-1772 (2011).
- Clevers, H. Modeling development and disease with Organoids. Cell. 165 (7), 1586-1597 (2016).
- Dekkers, J. F., Wiegerinck, C. L., et al. A functional CFTR assay using primary cystic fibrosis intestinal organoids. Nature Med. 19 (7), 939-945 (2013).
- Dekkers, J. F., van der Ent, C. K., Beekman, J. M. Novel opportunities for CFTR-targeting drug development using organoids. Rare Diseases. 1 (1), e27112 (2014).
- Servidoni, M. F., Sousa, M., et al. Rectal forceps biopsy procedure in cystic fibrosis: technical aspects and patients perspective for clinical trials feasibility. BMC gastroenterology. 13, 91 (2013).
- Ommen, D. D. Z. -. V., Vijftigschild, L. A. W., et al. Limited premature termination codon suppression by read-through agents in cystic fibrosis intestinal organoids. J Cyst Fibros. 15 (2), 158-162 (2016).
- Dekkers, J. F., Gogorza Gondra, R. A., et al. Optimal correction of distinct CFTR folding mutants in rectal cystic fibrosis organoids. Eur Respir J. , (2016).
- Dekkers, J. F., Van Mourik, P., et al. Potentiator synergy in rectal organoids carrying S1251N, G551D, or F508del CFTR mutations. J Cyst Fibros. , (2016).
- Dekkers, J. F., Berkers, G., et al. Characterizing responses to CFTR-modulating drugs using rectal organoids derived from subjects with cystic fibrosis. Sci Transl Med. 8 (344), 344ra84 (2016).
- Li, H., Sheppard, D. N., Hug, M. J. Transepithelial electrical measurements with the Ussing chamber. J Cyst Fibros. 3, 123-126 (2004).
- Sheppard, D. N., Carson, M. R., Ostedgaard, L. S., Denning, G. M., Welsh, M. J. Expression of cystic fibrosis transmembrane conductance regulator in a model epithelium. Am J Physiol. 266 (4 Pt 1), L405-L413 (1994).
- Farin, H. F., van Es, J. H., Clevers, H. Redundant sources of Wnt regulate intestinal stem cells and promote formation of Paneth cells. Gastroenterology. 143 (6), 1518-1529 (2012).
- Drost, J., et al. Organoid culture systems for prostate epithelial and cancer tissue. Nat Protoc. 11 (2), 347-358 (2016).
- Vijftigschild, L. A. W., Berkers, G., et al. β2-adrenergic receptor agonists activate CFTR in organoids and subjects with cystic fibrosis. Eur Respir J. 48 (3), 768-779 (2016).
- Dekkers, R., et al. A bioassay using intestinal organoids to measure CFTR in human plasma. J Cyst Fibros. 14 (2), 178-181 (2015).
- Graeber, S. Y., et al. Intestinal Current Measurements Detect Activation of Mutant CFTR in Patients with Cystic Fibrosis with the G551D Mutation Treated with Ivacaftor. Am J Respir Crit Care Med. 192 (10), 1252-1255 (2015).
- Van Goor, F., et al. Ivacaftor potentiation of multiple CFTR channels with gating mutations. Journal of Cystic Fibrosis: Official Journal of the Eur Cyst Fibrosis. 11 (3), 237-245 (2012).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten