Method Article
Forskolin indotta Gonfiore intestinale organoidi: An
In questo articolo
Riepilogo
This protocol describes an assay for measuring CFTR function and CFTR modulator responses in cultured tissue from subjects with cystic fibrosis (CF). Biopsy-derived intestinal organoids swell in a cAMP-driven fashion, a response that is defective (or strongly reduced) in CF organoids and can be restored by exposure to CFTR modulators.
Abstract
Recently-developed cystic fibrosis transmembrane conductance regulator (CFTR)-modulating drugs correct surface expression and/or function of the mutant CFTR channel in subjects with cystic fibrosis (CF). Identification of subjects that may benefit from these drugs is challenging because of the extensive heterogeneity of CFTR mutations, as well as other unknown factors that contribute to individual drug efficacy. Here, we describe a simple and relatively rapid assay for measuring individual CFTR function and response to CFTR modulators in vitro. Three dimensional (3D) epithelial organoids are grown from rectal biopsies in standard organoid medium. Once established, the organoids can be bio-banked for future analysis. For the assay, 30-80 organoids are seeded in 96-well plates in basement membrane matrix and are then exposed to drugs. One day later, the organoids are stained with calcein green, and forskolin-induced swelling is monitored by confocal live cell microscopy at 37 °C. Forskolin-induced swelling is fully CFTR-dependent and is sufficiently sensitive and precise to allow for discrimination between the drug responses of individuals with different and even identical CFTR mutations. In vitro swell responses correlate with the clinical response to therapy. This assay provides a cost-effective approach for the identification of drug-responsive individuals, independent of their CFTR mutations. It may also be instrumental in the development of future CFTR modulators.
Introduzione
CF è causata da mutazioni nel gene della fibrosi cistica regolatore della conduttanza transmembrana (CFTR), che codifica per un canale anionico epiteliale. CF colpisce circa 85.000 persone in tutto il mondo 1. Oltre 2.000 mutazioni CFTR sono state identificate ( www.genet.sickkids.on.ca ). Questa diversità spiega in parte un ampio spettro di fenotipi della malattia osservati ( www.CFTR2.org ) 2, 3. Sei classi di mutazioni CFTR sono definiti in base alla loro effetto sulla espressione della proteina CFTR e la funzione: (I) N. sintesi, (II) il traffico compromessa, (III) del canale difettoso gating, (IV) la conduttanza alterato, (V) i livelli di norma ridotta funzionamento CFTR, e (VI) cellula compromessa la stabilità della superficie 4. Anche se le mutazioni CFTR comuni sono ben studiati, la funzione CFTR e relazione con lo stato clinico rimangono poorly inteso a livello del singolo, in particolare per il grande gruppo di rare "orfani" mutazioni ( www.CFTR2.org ) 1, 3.
Recentemente, i farmaci sono stati sviluppati che hanno come bersaglio la proteina CFTR in maniera specifica per la mutazione. Due classi di farmaci proteici CFTR-targeting sono attualmente in uso clinico e hanno distinte modalità di azione. Potenziatori, come il VX-770, migliorano l'open-probabilità di CFTR mutata direzione apicale-localizzata e agiscono direttamente sulla loro aggiunta a cellule 5. Correttori, come il VX-809, ripristinare il traffico di reticolo endoplasmatico-localizzato misfolded CFTR e richiedono pre-incubazione con si osservano cellule prima che gli effetti 6. Il potenziatore CFTR, VX-770, è stato registrato per i soggetti con la mutazione G551D 7, 8, così come per altri ottoCFTR gating mutazioni, tra cui S1251N 9; insieme, queste mutazioni sono trasportati da 5% di tutti i soggetti CF. Altri studi clinici hanno indicato che VX-770, in combinazione con il correttore VX-809, ha effetti limitati ma significativi sulla funzione polmonare e provoca una diminuzione della frequenza di esacerbazioni nei soggetti omozigoti per la mutazione F508del portato da 45-50% dei pazienti 10, 11.
studi clinici convenzionali per identificare i soggetti farmaco-sensibile all'interno del restante 50% dei pazienti affetti da FC sono costosi e che richiede tempo e non sono realizzabili per gli individui con genotipo CFTR estremamente rari. Novel, metodi personalizzati di costo-efficacia sono cruciali per soddisfare il crescente numero di modulatori CFTR a individui portatori di qualsiasi tipo di CFTR mutazione. Fino ad ora, l'inclusione di prova di gruppi di pazienti che trasportano specifiche mutazioni CFTR è stata guidata da studi che utilizzano mutante trasfezione del gene CFTR in hsistemi cellulari eterologous, seguiti da studi elettrofisiologici in Camera di Ussing 5, 6, 12. A causa della mancanza di modelli animali CF adeguate, studi di efficacia del farmaco nelle cellule epiteliali bronchiali aria-liquido-interfaccia dissociati derivati da CF polmonari materiali espianti sono stati utilizzati per lo sviluppo di farmaci 13, 14, 15. Tuttavia, la limitata disponibilità di tessuti espianto polmonari e le procedure invasive per ottenere cellule bronchiali da soggetti senza malattia allo stadio terminale ostacolare l'analisi delle mutazioni CFTR meno comuni e prevenire test anti-droga in un modo personalizzato. Per superare queste limitazioni, i tessuti "easy access", come organoidi del colon-retto, cellule delle vie aeree nasali, e le cellule delle vie aeree derivate da cellule staminali pluripotenti indotte, sono attualmente oggetto di studio per trattamenti farmacologici personalizzati.
In precedenza, abbiamo stabilito i protocolli per le cellule staminali epiteliali cultura da qualsiasi organo gastrointestinale in forma di 3D organoidi 16, 17. fattori di crescita per il colon / retto umana, le condizioni di coltura comportano definiti (fattore di crescita epiteliale (EGF), gastrina, Wnt-3A, R-spondina 3 (Rspo3), e Noggin) in combinazione con piccole molecole (nicotinamide, A83-01, e SB202190) in una matrice membrana basale. In queste condizioni, le cellule staminali singoli o piccoli frammenti di tessuto crescono in chiusi, cistica, strutture 3D formate da epitelio altamente polarizzata con il lato basale orientato verso l'esterno. Tutti i tipi di cellule compaiono tipicamente nei loro rapporti normali e posizioni. Organoidi possono essere espanse per periodi di tempo lunghi per rottura meccanica settimanale e ri-placcatura. Sono geneticamente e fenotipicamente stabili e possono essere memorizzati, permettendo l'espansione a lungo termine e bio-banking 17. Esse sono suscettibili ditutte le manipolazioni standard di cellulari-biologici / genetici e tecniche analitiche sviluppate per linee cellulari 2D 18.
Abbiamo recentemente dimostrato che la funzione CFTR può essere facilmente misurato in organoidi del colon-retto in un saggio forskolin indotta gonfiore (FIS) 19, 20. Se esposto a forskolin (FSK) o, in alternativa, tossina del colera, organoidi rapidamente aumentano la loro adenosina monofosfato ciclico livelli (cAMP), che a sua volta provoca l'apertura del canale CFTR 19. Organoidi da individui sani o da pazienti con CFTR mutazioni associate alla funzione residua, saranno successivamente gonfiarsi come conseguenza di trasporto di ioni e acqua al lume organoide, l'equivalente in vitro di diarrea secretoria. La risposta FIS di organoidi del colon-retto è stato precedentemente dimostrato di essere pienamente CFTR-dipendente, come indicato dalla organoidi derivati da individui CFTR-udenti and mediante l'uso di specifici inibitori farmacologici CFTR 19. Grandi insiemi di dati specifici per soggetti possono essere derivate entro alcune settimane dopo l'assunzione di una biopsia.
Per il saggio FIS descritto in dettaglio qui, organoidi sono coltivati da biopsie rettali ottenibili a qualsiasi età e con solo disagio limitata 21. Organoidi sono diversi passaggi ogni settimana dalla rottura meccanica in singoli cripte che facilmente richiudere e formano nuove organoidi. Per l'esecuzione del test FIS, ~ 30-80 di queste piccole organoidi perturbato sono placcati in ciascun pozzetto di una piastra a 96 pozzetti 19. Al giorno del test, i organoidi sono colorate con calceina verde, un colorante cellula-permeabile fluorescente che viene trattenuto all'interno delle cellule viventi, facilitando l'imaging dal vivo. Poi, FSK, che solleva cAMP intracellulare e quindi attiva CFTR, viene aggiunto per stimolare gonfiore organoide. Potenziatori che agiscono su CFTR apicale sono aggiunti contemporaneamente won la forskolina, mentre correttori che ripristinano il traffico di CFTR si aggiungono 24 ore prima dell'aggiunta di Fsk. Il gonfiore organoide viene quantificato un'analisi automatica delle immagini che calcola il relativo aumento della superficie totale di tutti gli oggetti fluorescenti per ogni punto di tempo dopo l'aggiunta forskolin.
3D organoide gonfiore offre vantaggi e svantaggi sopra letture CFTR elettrofisiologici esistenti in cellule in coltura delle vie aeree 2D in Camera di Ussing. Un importante vantaggio è la velocità del test gonfiore. Le cellule sono coltivate e analizzati utilizzando un unico tipo di terreno di coltura, e un tecnico esperto può cultura fino a 25 campioni organoide su base settimanale, mentre la quantificazione circa 1.200 punti dati a settimana in 12 campioni di pazienti. Abbiamo convenzionalmente digitare una singola condizione sperimentale da misure doppio o triplo, per piastra e ripetere tali misurazioni in tre punti di tempo di incubazione indipendenti. In totale, circa 300-500 single organoide strutture sono poi misurati per ogni condizione sperimentale, che porta a misure molto precise della funzione CFTR con variabilità tecnico limitato. Questa precisione ci permette di definire in modo chiaro le differenze nella funzione residua e la risposta a modulatori CFTR e ci permette di raccogliere facilmente fino effetti di sfondo genetiche tra i pazienti portatori di mutazioni CFTR identici 19, 22, 23, 24, 25. La qualità dei dati può essere facilmente valutata da immagini al microscopio. Mentre FIS è completamente CFTR-dipendente, è una misura di esito indiretto per la funzione CFTR, la sua out lettura causata dall'accoppiamento di trasporto ionico per il trasporto di fluidi. Questo contrasta con le misurazioni della funzione CFTR dirette in camere ussing, che misurano correnti ioniche transepiteliali 26. camere ussing permettono di selezione stimolazione apicale del o basolaterale compartments (che il test organoide non permette); da permeabilizzante membrane basolaterale, il apicale CFTR-dipendente la secrezione di anione può essere selettivamente misurato 27.
Protocollo
Tutti sperimentazione utilizzando tessuti umani qui descritti è stato approvato dal Comitato Etico presso University Medical Center di Utrecht (UMCU; TcBio # 14-008). Il consenso informato per la raccolta dei tessuti, la generazione, la conservazione e l'uso delle organoidi è stato ottenuto dai pazienti a Hospital (WKZ) -UMCU Wilhelmina bambini.
| attrezzatura | consumabili | Utensili |
| cappa a flusso laminare | 15 e 50 ml provette coniche | Zeiss LSM 800 - Zen 2 (edizione blu) software per misurare le immagini |
| CO 2 incubatore | tubi microcentrifuga | programma di Microsoft Excel |
| Colture cellulari microscopio (microscopio ottico / ottico) | 0,22 micron filtri | |
| Centrifuga | pipette sierologiche | |
| rotolamento Shaker | puntali con filtro Micropipetta | |
| 4 ° camera C o 4 ° C frigo per incubatrice | cryovials | |
| CoolCELL cellulare congelamento Container | ||
| Pipetta sierologica | ||
| Micropippette (1000, 200 e 20 microlitri) | ||
| Viaflo Ripetere pipetta | ||
| (Cella Live) microscopio confocale | ||
| Computer | ||
| serbatoio di azoto liquido | ||
| Multicanale (200 ml) |
1. Reagenti Preparazione per la cultura
Nota: Tutti i passaggi vengono eseguiti all'interno di un armadio biosicurezza e seguendo linee guida standard per lavorare con colture cellulari. Per facilitare la formazione di belle gocce di matrice membrana basale, mantenere un archivio di pre-riscaldato di 96-, 24-, e 6 pozzetti nell'incubatrice a 37 ° C.
- Basale medio Preparazione
NOTA: Terreno di base (BM) si riferisce a Modified Eagle Medium Advanced Dulbecco con Nutrient Mixture di Ham F-12 (Ad-DF) integrato con 4- (2-hydroxyethil) Acido -1piperazineethanesulfonic (HEPES), glutammina, e la penicillina / streptomicina (Pen / Strep).- In un flacone media 500 ml Ad-DF, aggiungere 5 ml di 200 mM glutammina, 5 ml di 1 M HEPES e 5 ml di soluzioni pen / strep (10.000 U / ml, 10.000 mg / ml).
- Conservare BM in frigorifero a 4 ° C per almeno 4 settimane.
- Wnt-3A-condizionata Media Preparazione
NOTA: medio Wnt-3A-condizionata è fatto in casa using la linea cellulare L-Wnt-3A secondo le istruzioni del produttore.- Per la raccolta medio Wnt-3A-condizionata, raccogliere il mezzo esposto alle cellule per una settimana e spin giù per 5 min a 450 xg per rimuovere le cellule galleggianti.
- Filtrare il mezzo Wnt-3A condizionata attraverso un filtro di 0,22 micron e dividerlo in 40 ml aliquote in 50 ml provette coniche. conservarli a 4 ° C per almeno 4 mesi senza perdita di attività.
- Testare l'attività del mezzo Wnt-3A-condizionata in un test di TOP / FOP utilizzando renali embrionali umane (HEK) -293 cellule trasfettate con TOP- e FOP-luciferasi e TK-Renilla e misurati con un Renilla -luciferase kit di analisi in base alle le istruzioni del produttore.
NOTA: TOP-luciferasi è un plasmide giornalista che contiene wild-type TCF regioni vincolanti. Se il mezzo Wnt-3A condizionata è attiva, la canonica Wnt è attivato. Beta-catenina trasloca nel nucleo di associare ingegnoh TCF / LEF fattori di trascrizione e attiva la trascrizione del reporter luciferasi, inducendo un aumento dell'attività di luciferasi relativa quando viene aggiunto il substrato. La FOP-luciferasi viene usato come controllo negativo perché il TCF vincolante regioni a monte del gene della luciferasi sono mutato.
- Colon Media Preparazione
NOTA: Preparare e portare tutti i fattori di crescita e reagenti in base alle raccomandazioni del fabbricante. Utilizzare aliquote di piccole dimensioni un Evitare cicli di congelamento-scongelamento. fattori di crescita funzionali sono essenziali per i risultati.- Preparare media punti (CM), completandola con BM 1x B27, 1,25 mm N-acetilcisteina, 50 ng / ml hEGF, 5 nM gastrina, 10 mM nicotinamide, 300 ng / ml hRspo3, 100 ng / ml hNoggin, 500 micron A83-01 , 10 mM SB202190, e 100 ug / ml di un antimicrobico per le cellule primarie.
- Dividere il CM in aliquote e congelarli a -20 ° C per un massimo di 4 mesi. Scongelare le aliquote per la preparazione completa del colonmedio (FCM) aggiungendo 50% Wnt-3A-conditoned mezzo al CM. Conservare FCM fino a 7 giorni a 4 ° C senza perdita di attività.
- Per la creazione di una cultura organoide da biopsie rettali, integrare FCM con 50 mg / ml vancomicina, 50 mg / ml gentamicina, e 10 micron proteina serina / treonina chinasi avvolto a spire Rho-associata (RhoKi). Usare questo mezzo, chiamato terreno di isolamento (IM), solo per i primi due o tre giorni in coltura.
- EDTA della Soluzione Preparazione
- Preparare 0,5 M di acido etilendiamminotetraacetico (EDTA), pH 8, in ultrapura H 2 O, sterilizzato con un filtro da 0,22 micron.
- La manipolazione della matrice di membrana basale
- Preparare la matrice membrana basale (BMM) secondo le raccomandazioni del fabbricante.
- Disgelo BMM durante la notte sul ghiaccio.
- Durante il trasferimento del BMM dalla bottiglia a un tubo conico 15 ml, usouna pipetta da 5 ml e un tubo da 15 ml pre-raffreddata a -20 ° C.
- Una volta scongelate, conservare la BMM in frigorifero a 4 ° C e incubare in ghiaccio per almeno 30-60 minuti prima dell'uso.
NOTA: Al fine di ottenere i migliori risultati, la BMM deve essere freddo e adeguatamente miscelati prima di incorporare cripte o organoidi.
2. Stabilire organoidi Colon da una biopsia paziente CF
NOTA: Dopo la raccolta dei tessuti, è importante mantenere il campione in ghiaccio in soluzione salina, Dulbecco fosfato-Buffered Saline senza Ca 2+ e Mg 2+ (DPBS), o BM. Si raccomanda l'elaborazione rapida delle biopsie, ma si è dimostrato possibile stabilire culture organoide da biopsie memorizzati sul ghiaccio per un massimo di 7 giorni.
- Che le biopsie depositano sul fondo di una provetta conica da 15 ml e rimuovere il surnatante.
- Aggiungere 10 ml di DPBS alle biopsie e pipetta su e giù 10-20 volte con una pipetta 10 ml.
NOTA: la pipetta deve essere pre-bagnato con BM prima pipettaggio la biopsia. - Lasciate che le biopsie si depositano sul fondo e rimuovere il surnatante.
- Ripetere i punti 2.2 e 2.3 4-5 volte fino a quando il surnatante è chiaro.
- Aggiungere 10 ml di DBPs e 200 microlitri EDTA (0,5 M) per le biopsie e posizionare il tubo su una piattaforma oscillante tubo per 60-120 min a 4 ° C.
NOTA: il tempo di incubazione può variare per paziente. Se cripte vengono rilasciati, DPBS diventa torbida. incubazione EDTA può essere finalizzato quando cripte possono essere osservate al microscopio. - Lasciare le cripte di stabilirsi. Eliminare il surnatante.
- Raccogliere 2 ml di BM e aggiungerlo a un nuovo tubo da 15 ml. Agitare questo nuovo tubo manualmente in modo tale che l'interno è coperto con BM.
- Usando una pipetta pre-bagnato con BM, aggiungere 2 ml di DPBS per il tubo contenente le biopsie e pipetta su e giù per 10-20 volte.
- Lasciare le biopsie di stabilirsi e di trasferire i DPBS con le cripte per il nuovoprovetta contenente 2 ml di BM che è stato preparato nel passo 2.7.
- Ripetere i punti 2.8 e 2.9 fino a quando non più cripte vengono rilasciati.
- Spin le cripte giù a 130 xg per 5 min a 8 ° C.
- Nel frattempo, trasferire IM alla cabina di sicurezza a temperatura ambiente (RT).
- Eliminare il surnatante e aggiungere 10 ml di BM alla cripta pellet e ripetere il punto 2.11.
- Risospendere il pellet in 1 ml di BM. Prendere 5-10 microlitri e contare il numero di cripte occhio al microscopio.
- Spin le cripte giù a 130 xg per 5 min a 8 ° C.
- Rimuovere il surnatante e risospendere il pellet in 55% BMM (v BMM di v IM).
NOTA: Le cripte sono risospese nel volume corrispondente di 55% BMM a 1 cripta per ml. Se non ci sono abbastanza cripte, il volume minimo di BMM è di 40 ml. - Per la semina, pipetta 35 microlitri per bene (in una piastra da 24 pozzetti). Dividere i 35 pl di BMM in 3-5 gocce separatamente per migliorare la diffusione del growth fattori nel BMM. Non creare bolle.
- Posizionare e lasciare la piastra capovolta in incubatore a 37 ° C per almeno 20 min per il BMM solidificazione.
- Aggiungere 500 ml di IM per pozzetto e mantenere in incubatore a 37 ° C e 5% CO 2.
- Aggiornare la media ogni 2-3 giorni. Rimuovere il vecchio mezzo di pipettando con una pipetta P1000, lasciando la BMM scende intatto. Aggiungere con cautela FCM pipettando nel lato del bene, non direttamente sulla BMM gocce.
NOTA: Se non cripte vengono rilasciati nel protocollo di isolamento, centrifugare il surnatante, lavare il pellet 2-3 volte con BM, e risospendere in BMM. Prendere il tessuto residuo e tagliatela a piccoli pezzi con un rasoio. Raccogliere questi in una provetta conica da 15 ml, li centrifugare e risospendere nella stessa BMM. Se le cellule staminali epiteliali sono presenti, questi generano anche organoidi.
3. Passaging di organoidi Colon per la manutenzione, congelamento, e perskolin indotta Gonfiore Assay (FIS)
NOTA: Ogni cultura organoide ha il suo tempo di raddoppio. Normalmente, organoidi CF-retto possono essere ampliati 1: 3-1: 5 volte ogni 7-10 giorni. E 'un buon segno se si osservano strutture in erba. Organoidi colon-CF sono meno cistica (Figura 2A - 2C) rispetto organoidi normali del colon-retto (Figura 2D). Per la creazione e la manutenzione, organoidi sono coltivate in piastre da 24 pozzetti; per il congelamento, in 6 pozzetti; e per il test FIS, a 96 pozzetti paté.
- Passaging di organoidi
- Mantenere la BMM in ghiaccio per almeno 30-60 minuti prima di utilizzarlo.
- Mantenere il FCM a temperatura ambiente per almeno 1 ora prima di utilizzarlo.
- Etichettare un tubo di 15 ml conica con il nome del campione e un altro tubo come "lavati".
- aspirare accuratamente la media dei pozzetti usando una pipetta P1000 senza disturbare il BMM scende.
- Aggiungere 1 ml di BM a 1 bene e Break la BMM scende utilizzando una pipetta P1000. Trasferire questa 1 ml in tubo da 15 ml con il nome del campione.
- Lavare il bene con altre 1 ml di BM e trasferirlo stesso tubo 15 ml.
- Ripetere i punti 3.1.5 e 3.1.6 con più 5 pozzi (fino a 6 pozzetti di una piastra da 24 pozzetti saranno lavati in una tubo da 15 ml).
- Riempire il tubo fino a 12 ml con BM. Pipetta su e giù con un pre-bagnato 5 ml pipetta.
- Spin a 85 xg per 5 min a 8 ° C.
- Eliminare il surnatante e aggiungere 1 ml di BM al pellet. Con la stessa punta della pipetta P1000, prendere una punta P10 senza filtro, e pipetta su e giù per 20 volte. Gettare sia P1000 e suggerimenti P10.
- Aggiungere 4 ml di BM con una pipetta da 5 ml e tenere il tubo inclinato a circa 70 ° rispetto alla verticale di un lato. Pre-bagnare una nuova punta P1000 e mescolare energicamente 2-3 volte con il P1000 (volume 1 ml).
- Contare fino a 10, pur rimanendo in posizione inclinata, raccogliere lo strato superiore con attenzione won la pipetta P1000, e il trasferimento di 4 x 1 ml nel tubo etichettato come "lavati".
- Osservare le organoidi di decantazione a fondo nel tubo inclinato; organoidi undisrupted e pezzi più grandi si depositano sul fondo. Centrifuga 15 ml "lavati" tubo per 5 min a 85 xg e 8 ° C.
- Eliminare il supernatante e aggiungere la quantità di terreno necessaria e BMM al pellet organoide ad una concentrazione finale del 55% BMM. Mescolare pipettando su e giù senza creare bolle (Figura 3B).
NOTA: una buona densità si ottiene semina 25-30 organoidi in 10 ml di BMM. - Seguire i passi 2,17-2,19.
- Passaging per congelamento
- Mantenere il BM in ghiaccio per almeno 30-60 minuti prima dell'uso. Mantenere dell'FCM a temperatura ambiente per almeno 1 ora prima dell'uso.
- Preparare FCM integrato con RhoKi (punto 1.3.3).
- Prendere tripsina dal frigorifero e lasciarlo a temperatura ambiente per almeno 30 minuti prima dell'uso.
- Seguire i passaggi 3.1.5-3.1.10.
- Rimuovere il più possibile surnatante, aggiungere 4 ml di tripsina, e vortex per 30 sec.
- Mettere la provetta in un bagno di acqua calda a 37 ° C per 1 min e vortex vigorosamente per 30 secondi.
- Controllare la soluzione nel tubo. Se organoidi intatte sono ancora visibili al microscopio, ripetere il punto 3.2.7.
- Quando i organoidi sono interrotti, aggiungere 8 ml di BM per neutralizzare la tripsina e pipetta 10 volte.
- Spin per 3 minuti a 450 xga 8 ° C.
- Eliminare il surnatante e aggiungere la quantità di terreno necessaria e BMM ai organoidi per raggiungere una soluzione BMM 55%. Mescolare pipettando su e giù senza creare bolle.
NOTA: Per il congelamento, organoidi devono essere seminate in un rapporto 1: 1 dopo tripsinizzazione. - Seed 250 microlitri in un singolo pozzo di un 6-pozzetti pre-riscaldato coltura di tessuti, producendo minuscole goccioline separati di ~ 10 microlitri. Posizionare la piastra capovolta in incubatore a 37 ° C e lasciare ilBMM a solidificare per 20-30 min.
- Aggiungere 2,5 ml di FCM fresco + RhoKi Ogni piastra da 6 pozzetti bene e trasferire la piastra per l'incubatore (Figura 3C).
- Passaging organoidi per il saggio FIS
NOTA: A seconda del numero e delle dimensioni delle organoidi, da 4 a 6 pozzetti di una piastra da 24 pozzetti sono sufficienti per seminare 27 pozzetti di una piastra a 96 pozzetti.- Elaborare i organoidi come descritto da piazza 3.1-3.1.13.
- Risospendere il pellet in 120 ml di 50% BMM.
- Conferma il numero di organoidi (30-50) in 3 microlitri goccia BMM al microscopio.
- Piastra le organoidi utilizzando una sola goccia di 3 ml poste al centro di ciascun pozzetto di una 96 pozzetti pate.
- Posizionare la piastra in incubatore a 37 ° per 15 min per il BMM solidificazione; ulteriori passi sono descritti al punto 6.1.1.
4. congelamento Colon CF organoidi
NOTA: OrganOID sono pronti per essere congelati giù 1-2 giorni dopo tripsinizzazione e coltura, così organoidi saranno ancora piccola, che aumenta l'efficienza della sopravvivenza dopo lo scongelamento.
- Aggiungere 1 ml di BM e spezzare la BMM gocce con una pipetta P1000. Trasferire in un tubo da 15 ml.
- Lavare il bene con un altro 1 ml di BM e trasferimento allo stesso tubo da 15 ml.
- Ripetere i punti 4.1 e 4.2 con tutti i pozzetti.
NOTA: per evitare l'eccesso BMM, 3 pozzetti di una piastra da 6 pozzetti sono riunito in un unico tubo da 15 ml. - Riempire il tubo da 15 ml contenente le organoidi con 12 ml di freddo BM e pipetta su e giù con una pipetta da 5 ml. Lasciare la provetta in ghiaccio per 5 min.
- Spin per 3 min a 450 xg e 8 ° C e rimuovere il surnatante.
- Sciogliere il pellet di organoidi con congelatore medio e pipetta su e giù per risospendere correttamente i organoidi.
NOTA: 500 ml di mezzo di congelamento viene utilizzato per ogni 100 ml di BMM. - Usando una pipetta da 5 ml, trasferire 0,5 ml diorganoidi risospesi in media di congelamento a sterilizzato fiale criogeniche.
- Trasferire le fiale in un contenitore di congelamento delle cellule e metterlo a -80 ° C.
- Dopo 24 ore, il trasferimento dei flaconi per la conservazione in azoto liquido.
5. Stabilire culture da congelati organoidi
NOTA: Scongelare il BMM sul ghiaccio e tenerlo in ghiaccio. Lasciate che il BM raggiungere RT, e riscaldare una aliquota di 10 ml a 37 ° C prima di iniziare la procedura di scongelamento uno esageratamente.
- Scongelare il flacone rapidamente mediante agitazione in un bagno d'acqua C 37 ° fino a quando c'è ancora un po materiale congelato.
- Trasferire i organoidi scongelati per un tubo da 15 ml con una pipetta P1000.
- Subito dopo, aggiungere 1 ml di caldo goccia BM a goccia agitando il fondo della provetta. Una volta aggiunto il 1 ml di terreno, si mescola accuratamente pipettando su e giù un paio di volte per diluire il mezzo di congelamento.
- Lentamente (goccia a goccia) aggiungere 9 ml di caldo BM alla conta tubo conicovorazio i organoidi. Invertire un paio di volte.
- Spin la sospensione cellulare per 3 min a 85 xg e 8 ° C.
- Scartare con attenzione il surnatante senza disturbare il pellet. Risospendere il organoide in 90 ml di FCM integrato con RhoKi (fase 1.3.3). Quindi, aggiungere 110 ml di BMM.
- Aggiungere 35 microlitri di ciascun pozzetto di una piastra da 24 pozzetti pre-riscaldato, rendendo minuscole goccioline separate.
- Trasferire la piastra al incubatore a 37 °, lasciando la piastra capovolta per 20-30 min.
- Aggiungere 500 ml di FCM con RhoKi di ogni bene e trasferire la piastra posteriore per l'incubatore (Figura 4A - 4C).
- Una volta organoidi hanno recuperato correttamente da scongelamento, diluire in più BMM in modo che ogni 10 ml di BMM contiene 25-30 organoidi. Questa procedura può essere eseguita 2-3 giorni dopo lo scongelamento (Figura 4D - 4G) e garantisce la corretta crescita del organoide.
6. Forskolin indotta gonfioredire (FIS)
NOTA: Fsk titolazione consente la misura della funzione residua CFTR. Per la modulazione CFTR, organoidi sono esposti a un dato correttore (ad esempio, VX-809) e / o potenziatore (ad esempio, VX-770), a seconda del genotipo. Di solito, VX-809 è aggiunto 18-24 h prima della misura, mentre il VX-770 e Fsk vengono aggiunti a destra prima di iniziare le misurazioni. Essere consapevoli del fatto che alcuni modulatori (correttori / potenziatori) possono legarsi alla superficie di plastica della piastra saggio.
- Placcatura per il saggio
NOTA: VX-809 scorte sono aliquotati a 20 mm e conservati a -80 ° C. Quando lo scongelamento, lasciare a temperatura ambiente e al riparo dalla luce.- Elaborare i organoidi come descritto nella sezione 3.3.
- Se il test correttore VX-809, preparare una curva dose-risposta in triplicato con le seguenti concentrazioni: 0,0003, 0,003, 0,03, 0,3, 3,0, e 30 mM. Preparare le diluizioni di FCM.
- Per la piastra a 96 pozzetti, aggiungere o 100 μ; L di FCM con le rispettive VX-809 concentrazione o 100 ml di FCM solo ed incubare la piastra.
- Misurare il Assay
NOTA: VX-770 scorte sono aliquotati a 20 mm, mentre FSK è a 10 mm; entrambi sono conservati a -80 ° C. Quando lo scongelamento, lasciare a temperatura ambiente e al riparo dalla luce.- Prendere una fiala di calceina e DMSO e lasciare a temperatura ambiente per 15 min.
- Aggiungere 5,1 ml di DMSO al flacone dove la calceina viene fornito come polvere, se non aperto. In caso contrario, utilizzare un flacone calceina già risospeso contenente 2,5 ml di calceina.
- Aggiungere 2,5 microlitri di calceina a 580 ml di BM in una provetta da 1,5 ml ed etichettarlo.
- Aggiungere 10 ml di questa soluzione colorante (BM + calceina) per ogni pozzetto usando una ripetizione pipetta.
- Risospendere una volta con un multicanale per garantire che il colorante viene mescolato bene.
- Incubare la piastra in un incubatore a 37 ° per 30 min.
- Durante l'incubazione calceina, iniziare a preparare FSKe soluzioni di VX-770, se necessario.
- Se si utilizza un potenziatore VX-770, preparare una curva dose-risposta in triplicato con le seguenti concentrazioni: 0,0003, 0,003, 0,03, 0,3, 3,0, e 30 mM. In caso di una titolazione Fsk, le concentrazioni sono: 0, 0,008, 0,02, 0,05, 0,12, 0,32, 0,8, 2,0 e 5,0 mM. Preparare le diluizioni di BM.
NOTA: Per FSK VX-770, o di qualsiasi altro farmaco aggiunto il secondo giorno, le diluizioni deve essere preparato ad una concentrazione finale di 2x, dal momento che 100 ml di Fsk soluzione / farmaco titolazione verrà aggiunto ad ogni pozzetto, che già contengono 100 pl di FCM. - Trasferire il FSK e VX-770 soluzioni, una pipetta P200, e suggerimenti per la stanza microscopio.
- Per l'imaging il saggio FIS, utilizzare un microscopio confocale imaging cellulare dal vivo dotata di una fase automatizzata, una camera riscaldata, e il flusso di CO 2.
NOTA: Le seguenti operazioni si riferiscono a un microscopio specifica. Diverse configurazioni dovrebbero applicarsi ad altri microscopi seguente costruttore diIstruzioni. - Mettere la piastra a 96 pozzetti nel supporto targa.
- Inserire le impostazioni confocale per l'imaging.
- Preselezionare lo strumento di imaging in tempo reale a 37 ° C e 5% CO 2 e lasciare la camera di pre-incubare per almeno 30 minuti prima della misurazione.
- Utilizzare l'opzione "Smart Setup" per selezionare la traccia Alexa Fluor-488.
- Impostare l'obiettivo 5X e area di scansione a 0.6x per diminuire e catturare l'intero bene.
- Adattare la sensibilità potenza del laser e rivelatore per consentire il rilevamento ottimale di organoidi etichettati calceina-verde sopra i precedenti. Il pinhole può essere aumentata a 130 micron e la media immagine può essere impostato a 2.
- Impostare la profondità di bit a 8 e la dimensione del frame di 512 x 512.
- Utilizzare l'opzione serie storiche per impostare la misurazione del tempo, la frequenza e gli intervalli.
NOTA: consigliato per le misurazioni regolari: 1 ora e 10 min con intervallo: cicli = 7 (Ciclo 1 è T = 0). Per le misure di gonfiore ridotta, organoidi possono essere esposte per un massimo di 3 ore. - Utilizzare l'opzione di piastrelle per determinare manualmente le singole posizioni così.
- Aggiungere 100 ml di FSK e / o VX-770 soluzioni ai rispettivi pozzetti, seguendo lo stesso ordine come misura. Iniziare ad aggiungere le soluzioni nel primo imaged bene e continuare con l'ordine di imaging.
- Avviare la misurazione.
- Dopo l'esperimento è finito, salvare il file.
- L'analisi dei dati FIS Assay
- Creare una macro "analisi organoide" per l'analisi dei dati del test FIS utilizzando lo strumento di analisi in un software di analisi delle immagini che riconosce tutte le strutture imaged attraverso la pista Alexa-488 e riempie le strutture individuate per calcolare l'aumento della superficie organoide totale sulla diversi punti di tempo.
- Aprire il file di dati con le immagini acquisite nel programma di analisi delle immagini.
- Selezionare la macro per l'analisi organoide.
- Imposta la soglia per bilanciare il rapporto segnale-rumore in un pozzetto al punto di tempo 1 e garantire che tutte le strutture organoide sono riconosciuti e riempiti.
- Il check-in 4-6 pozzi per vedere se tutte le strutture sono rilevati al punto 7. momento modificare leggermente la soglia per garantire che i segnali di fondo al punto 7 momento non sono riconosciuti come strutture (la soglia specifica può cambiare un po 'tra esperimenti).
- Impostare i criteri della dimensione area minima degli oggetti riconosciuti a 1.000 micron 2.
- Premere "analizzare" per iniziare. L'analisi richiede circa 3 minuti, a seconda del software utilizzato.
- Quando il software è finito, andare a "creare la tabella" e selezionare i seguenti dati: ben numeri (tabella dovrebbe aumentare in questo ordine), punti di tempo, e l'area totale per bene.
- Salvare file come .xlm esportare in un foglio di calcolo.
- In questo programma, calcolare il relativo aumento della superficie per well impostando l'area di punto temporale 1 a 100%. Calcolare l'area sotto la curva (AUC) di punti di tempo 1-7 a condizione; il limite inferiore della zona (Y-value) è fissata a 100%. FSK o droga titolazioni (asse X) sono tracciate contro l'AUC (asse Y).
Risultati
La figura 1A mostra un isolamento rappresentante fresco di cripte incorporati su BMM. Le cripte sono da una biopsia del colon-retto di un soggetto CF. Di solito, un organoide è generato da ogni cripta (Figura 1A - C). A causa della disfunzione del CFTR, la maggior parte dei organoidi colon CF non sono cistica, ma piuttosto sono compatti e con proiezioni e buddings (Figura 2A - 2B). Tuttavia, alcuni CF organoide culture, in particolare con alta funzione residuale, hanno un paio di organoidi con una forma cistica (Figura 2C), come wild-type culture organoide (Figura 2D).
Prima passaging i organoidi per espandere la cultura o semina un test FIS, è importante che i organoidi hanno una grande dimensione con più buddings, come mostrato nella Figura 3A. Se i organoidi sono piccoli e senza nbuddings umerous quando trattati per passaging, la cultura organoide è influenzato negativamente. A seconda della qualità e l'attività dei fattori di crescita essenziali come EGF, Wnt-3A, e Rspo3, le organoidi raggiungere la dimensione desiderata tra 7 e 12 giorni (Figura 3A). Dopo rottura meccanica, i buddings sono interrotti e utilizzati per generare nuove organoidi nel seguente passaggio (Figura 3B). Se l'elaborazione dei organoidi al congelamento, è importante che siano tripsinizzate a piccole dimensioni, come rappresentato nella Figura 3C. Dopo tripsinizzazione, i organoidi sono placcati per 1 o 2 giorni al fine di far loro recuperare dallo stress della manipolazione. Questa fase, insieme alla piccola dimensione delle organoidi, assicura un recupero delle cellule 98% dopo scongelamento (Figura 4A).
Quando i organoidi vengono scongelati, è importante avere in alta densità, così normalmente, vengono scongelati in unpiccolo volume (Figure4A). Dopo uno o due giorni in coltura, e dopo aver osservato che i organoidi stanno aumentando dimensioni (confrontare Figura 4A con la Figura 4B - 4C), i organoidi sono diluiti in un rapporto di 20-30 organoidi per 10 ml di BMM, fornendo la giusta densità a crescere in una dimensione più grande. Se i organoidi sono troppo diluiti, possono rallentare la crescita e possono anche differenziarsi e morire. Se i organoidi sono troppo affollate, la mancanza di spazio o carenza di fattori di crescita rallenta anche la crescita dei organoidi e riduce il numero di buddings.
La placcatura del organoidi da colture vitali con detriti cellulari limitata deve provocare condizioni in cui> 95% dei organoidi gonfiarsi dopo stimolazione Fsk, purché la funzione CFTR è considerata sufficiente (Figura 5A - 5B). Organoidi gonfiarsi in modo genotipo e tossicodipendenti, comeillustrato da immagini rappresentative di organoidi con due alleli F508del (Figura 5a) e organoidi compound-eterozigoti per F508del e S1251N (Figura 5B), una mutazione CFTR gating associata a qualche funzione residua.
Per quantificare gonfiore, superfici totali calceina-verde superficie sono selezionati per ogni punto di tempo ed espressi come percentuale di T = 0 (fissato al 100%; la figura 6A). Detriti e piccole strutture non gonfiore sono tipicamente sotto del 5% della superficie totale. L'incremento superficie relativa è espressa per intervallo di tempo di 10 min e AUC (unità arbitrarie) misurazioni vengono generati per ogni condizione (T = 0 a 60 min, soglia basale fissato al 100%; la figura 6B). Abbiamo trovato AUC per essere il più robusto, in quanto incorpora qualche variazione in apertura di gonfiore, nonché una relazione curvilinea oltre 30-40 min di Fsk a livelli funzionali alta CFTR.
misurazioni funzione residua in F508del / organoidi F508del in genere raggiungono 0-200 unità AUC (100-110% di incremento di superficie dopo 60 min di 5 micron trattamento FSK) , che può aumentare fino a ~ 2,500-3,500 unità AUC su incubazione con modulatori CFTR (VX770 + VX809, la figura 6C). Organoidi associati con la funzione residua CFTR possono raggiungere fino a 4.500 unità AUC dopo 60 min di 5 micron stimolazione Fsk in assenza di modulatori CFTR (200-220% superficie di condizioni pre-FSK). gonfiore organoide raggiunge un soffitto a ~ 4.500 unità AUC, presumibilmente a causa dei limiti fisici delle strutture organoide, l'impatto limita la velocità di trasporto di ioni basolaterale, e la creazione di omeostasi ionico e fluido di trasporto in condizioni di "allungata". FSK può essere titolata di ampliare ulteriormente la gamma dinamica del saggio a questi livelli di funzionalità residua alti CFTR per quantificare meglio la funzione residua o altamente efficace trattamento composto (per esempio, come indicato dalla maggiore attività del VX770 sul rigonfiamento organoidi S1251N dopo stimolazione con concentrazioni inferiori FSK; Figura 6D).

Figura 1: Creazione di CF organoidi del colon-retto da biopsie. (A) Immagini rappresentative di materiale isolato da una biopsia rettale dopo essere incorporato nel BMM il giorno isolamento (passaggio 0, giorno 0). L'allargamento della cripta indicato viene visualizzato sul pannello in basso a destra. (B) la stessa cripte sono stati seguiti dopo 7 giorni di coltura (passaggio 0, giorno 7). viene mostrato l'allargamento della stessa cripta, presentato nel pannello A. (C) immagine Rappresentante della stessa cultura organoide 11 giorni dopo essere stato diviso (passaggio 1, giorno 11). Barre di scala = 100 micron.
159fig1large.jpg "target =" _ blank "> Clicca qui per vedere una versione più grande di questa figura.

Figura 2: Immagini rappresentative della organoidi del colon-retto CF derivate da soggetti con differenti mutazioni CFTR. Immagini rappresentative della CF organoidi del colon-retto da soggetti con F508del / F508del (A), F508del / R117H-7T (B), e F508del / S1251N mutazioni (C). (D) immagine rappresentativa di una cultura organoide del colon-retto da un soggetto di tipo selvatico CFTR. Barre di scala = 100 micron. Queste immagini sono state ottenute senza stimolazione Fsk. Clicca qui per vedere una versione più grande di questa figura.
5159 / 55159fig3.jpg "/>
Figura 3: Elaborazione CF organoidi colon per la manutenzione e il dosaggio o per il congelamento. (A) Immagini rappresentative di una cultura organoide CF colon pronti per essere elaborati sia per passaging (B) o il blocco (C). (B) Dopo la loro rottura meccanica, si formano piccoli pezzi, che genererà i nuovi organoidi nel passaggio successivo. (C) Dopo tripsinizzazione, molto piccole, organoidi rotonde vengono generati, facilitando la loro vitalità durante il processo di congelamento. Barre di scala = 100 micron. Clicca qui per vedere una versione più grande di questa figura.
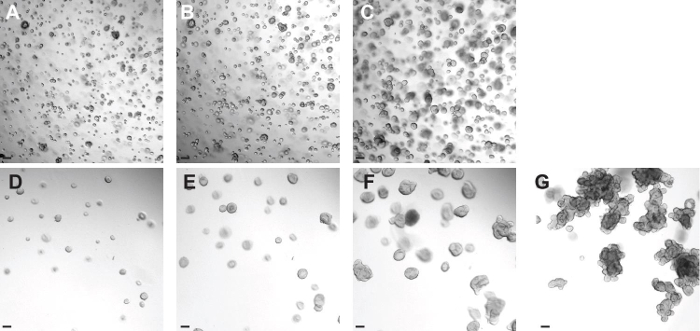
Figura 4: Creazione di una cultura organoide colorettale CF da organoidi congelati. ( A - C) Immagini rappresentative di una cultura organoide colorettale CF scongelati al giorno 0 (A). Immagini dalla stessa e sono stati presi uno (B) e due giorni (C) dopo. (D - G) Immagini rappresentative della fase di diluizione descritto nel paragrafo 5.9. Una volta che i organoidi hanno recuperato correttamente da scongelamento (giorno 3 dopo lo scongelamento), sono diluiti in modo da avere spazio per crescere (D). Immagini dallo stesso pozzo sono stati presi sei (E), dieci (F), e quindici (C) giorni dopo lo scongelamento. Barre di scala = 100 micron. Clicca qui per vedere una versione più grande di questa figura.

Figura 5: Forskolin indotta gonfiore della CForganoidi. (A e B) Immagini rappresentative della F508del / F508del (A) o F508del / S1251N (B) organoidi del colon-retto prima-770 VX o dopo 60 min di stimolazione con FSK (5 micron) in assenza o in presenza di (3 micron]) o VX-770 in combinazione con VX-809 (3 micron). Barre di scala = 200 micron. Clicca qui per vedere una versione più grande di questa figura.
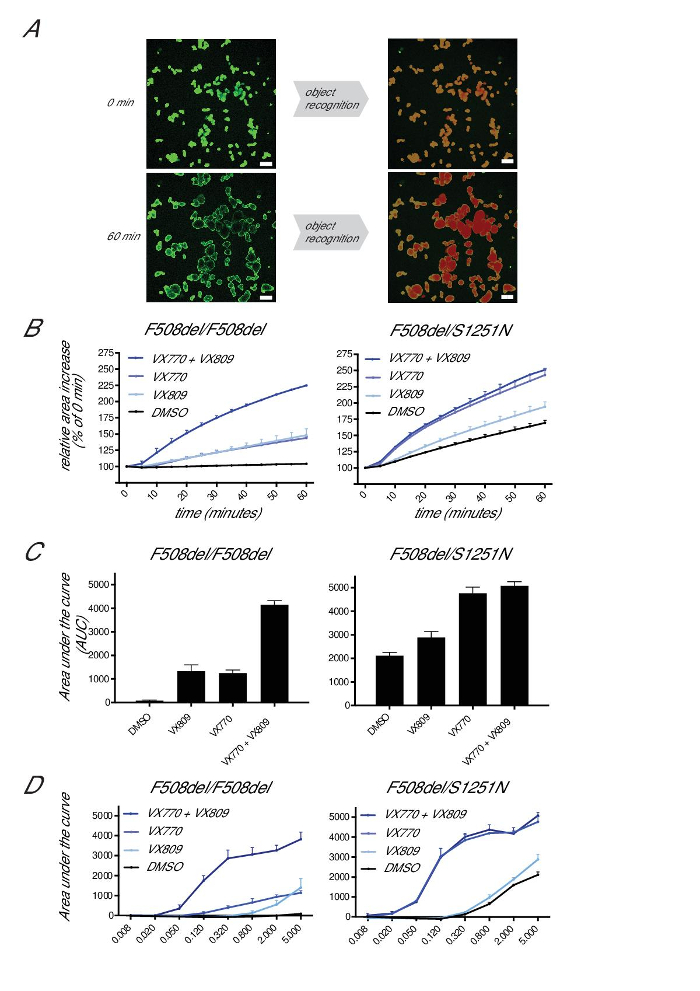
Figura 6: gonfiore Quantificare Forskolin-indotta. (A) Immagini rappresentative della selezione dell'area organoide di un software di analisi delle immagini di F508del / S1251N organoidi prima (0 min) e dopo 60 min di stimolazione con FSK (5 micron) e VX770 (3 micron). Barre di scala = 200 micron. (B) Represimmagini entative del relativo aumento di F508del / F508del o F508del organoidi / S1251N zona durante 60 min di FSK (5 micron) stimolazione in assenza o presenza di VX770 (3 micron) e / o VX809 (3 micron). (C) area sotto la curva di misurazioni condizioni indicate in (B) (T = 60 min, basale soglia = 100%). (D) area sotto la curva misure di F508del / F508del o organoidi F508del / S1251N a diverse concentrazioni di Fsk. I dati rappresentano le medie ± SD da singoli esperimenti rappresentativi. Clicca qui per vedere una versione più grande di questa figura.
Discussione
Qui, forniamo un protocollo completo per la generazione, l'espansione, il congelamento, lo scongelamento e di organoidi colorettali umani. Mentre abbiamo stabilito le culture umane organoide qualche tempo fa 17, è a volte dimostrato difficile stabilire la tecnologia in altri laboratori, senza una formazione pratica. Prevediamo che questi protocolli sostituiranno tale formazione.
Wnt-3A-condizionata mezzo è uno dei reagenti più importanti al fine di riuscire a stabilire e mantenere a lungo termine organoide cultura. In effetti, le culture organoide potrebbero "crash" quando esposti a medio Wnt-3A-conditoned con bassa attività. Dato medio Wnt-3A-condizionata è fatto in casa, ci sono diversi aspetti che devono essere presi in considerazione durante la generazione di un mezzo attivo. Attivo Wnt-3A può essere prodotto solo in mezzo con alta qualità di siero fetale bovino (FBS) che fornisce i segnali di crescita appropriati per le cellule L e la stabilizzazione di idrofobamolecole Wnt-3A. Quando l'attività Wnt-3A è basso (vale a dire, a bassa TOP / rapporti FOP, vedi sotto), di solito è la FBS che sta causando il problema.
Commercial ricombinante Wnt funziona male, quindi si consiglia di non usarlo come controllo positivo per il saggio giornalista TOP / FOP Wnt. Il rapporto tra TOP / Renilla e FOP / Renilla è indice di attività Wnt del terreno condizionato, quindi un buon lotto di substrato Wnt-3A condizionata dà un rapporto TOP / FOP superiore 25, rispetto al valore TOP / FOP da il controllo negativo: media non esposto alle cellule-3A-produzione di Wnt. Noggin ricombinante e R-spondina possono essere sostituiti da Noggin e R-spondina condizionati medie 28, 29.
L'attuale protocollo descrive anche un test funzionale per CFTR-test FIS. Abbiamo recentemente dimostrato la relazione tra il genotipo CFTR e FIS e di come questo si riflette pubblicato genoty CFTRrelazioni pe-fenotipo ottenuti da registri clinici (www.CFTR2.org) 25. Usando questo test, sono stati identificati due individui con rarissime mutazioni CFTR cui organoidi erano sensibili alle ivacaftor (VX-770) 25. Successivamente prescrizione di questo farmaco ha provocato la risposta clinica chiara, mettendo in evidenza il valore del saggio FIS per abbinare farmaci specifici con i pazienti con mutazioni rare in assenza di dati degli studi clinici. Essenziale per la quantificazione della FIS sono condizioni di crescita e di analisi ottimali, segnalate solo da una parte limitata di organoidi non gonfiore (di solito inferiore al 5%). Alti livelli di piombo detriti alla sottovalutazione di gonfiore, come una percentuale maggiore di non vitali, strutture non gonfiore sono riconosciuti dal software di analisi dell'immagine.
Le correlazioni tra in vitro FIS risposte e biomarcatori CFTR-dipendente precedentemente stabiliti (concentrazione di cloruro di sudore e intestmisure di corrente Inal) a livello personale erano facilmente dimostrabile nei nostri studi precedenti 19, 25. Questo ha sostenuto l'idea che le misurazioni funzione residua utilizzando FIS su soggetti con FC possono integrare gli approcci attuali come un marcatore diagnostico o prognostico in modo personalizzato. La portata del test FIS rispetto ad altri biomarcatori di funzione di CFTR, quali misure di concentrazione di cloruro di sudore in vivo e misure di corrente intestinali in ex vivo biopsie rettali, permette un migliore controllo della variabilità tecnica. Fornisce inoltre una lettura completamente CFTR-dipendente e una vasta gamma dinamica utilizzando una titolazione di Fsk che accuratamente tipi funzione di CFTR residua.
Tuttavia, il saggio FIS riflette solo l'impatto del genotipo individuale sulla variabilità di efficacia del farmaco, mentre la modulazione della malattia CF è influenzata da più unica funzione CFTR. per drug risposta, il saggio è riflettente di una risposta tissutale potenziale. Sebbene molto preciso nella misurazione CFTR, variazione umana nella farmacocinetica non è registrata, al contrario di altri in vivo 7, 8 o direttamente ex vivo misurazioni CFTR 32. Come discusso in precedenza, i modificatori CF non (sia genetici che ambientali) sono anche influenzando fenotipo, provocando uno scollamento tra le osservazioni in vitro o biomarcatori CFTR e fenotipo clinico 2. Inoltre, l'identificazione di potenziali mutazioni reattive che utilizzano linee cellulari 33 è associato ad un minore impatto sui pazienti che hanno bisogno di ottenere una biopsia rettale per l'istituzione di organoidi.
Più farmaci CFTR-targeting sono attualmente in fase di sviluppo 1. Si prevede che le sperimentazioni cliniche non consentono una previsione corretta di efficacia clinica based sulla sola CFTR stato mutazionale. Come il saggio FIS misura la funzione di CFTR e risposta ai farmaci in modo funzionale, può diventare il metodo di scelta per determinare quale farmaco funziona meglio per la quale il paziente. Il dosaggio FIS può anche essere utile per l'identificazione di gruppi di pazienti da includere in studi di registrazione e per lo sviluppo di modalità farmacologici. La stimolazione di organoidi del colon-retto con plasma prima e durante il trattamento può inoltre aiutare a quantificare gli importi funzionali di modulatori CFTR circolanti nel sangue, potenzialmente facilitare il dosaggio personalizzato e la selezione dei dosaggi di farmaci negli studi clinici 30, 31. Infine, FIS può essere utile per una migliore comprensione di base della funzione CFTR e le sue interazioni con altri modificatori genetici -quindi lontano ampiamente unknown- della sua funzione.
Divulgazioni
Hans Clevers is an inventor on patents for organoid culture and the Forskolin-induced swelling assay. Jeffrey M Beekman is an inventor on a patent for the Forskolin-induced swelling assay. Sylvia F Boj and Robert Vries are employed by the Foundation Hubrecht Organoid Technology (HUB), which holds the exclusive license to the Organoid Technology. Otherwise, the authors have nothing to disclose.
Riconoscimenti
Questo lavoro è stato sostenuto dal programma HIT-CF della olandese CF fondazione (NCFS), ZonMw (40-00812-98-14103), Fondo di ricerca dell'ospedale dei bambini di Wilhelmina e CZ, e Zilverenkruis / Achmea. Vorremmo ringraziare S. Heida-Michel, M. Geerdink, KM de Winter-de Groot, e G. Berkers (Dipartimento di Pneumologia Pediatrica, Ospedale Wilhelmina bambini, UMC Utrecht), e RHJ Houwen (Dipartimento di Gastroenterologia Pediatrica, Wilhelmina Ospedale pediatrico, UMC Utrecht) per avvicinare i pazienti e ottenere le biopsie per la generazione di un CF Biobank.
Materiali
| Name | Company | Catalog Number | Comments |
| Advanced Dulbecco’s Modified Eagles Medium with Nutrient Mixture F-12 Hams (Ad-DF) 500ml | Thermo Fisher Scientific: Invitrogen | #12634 | stored at 4 °C |
| GlutaMax | Thermo Fisher Scientific: Invitrogen | #35050 | stored at 4 °C |
| Hepes | Thermo Fisher Scientific: Invitrogen | # 15630-056 | stored at 4 °C |
| Penicillin/Streptomycin | Thermo Fisher Scientific: Invitrogen | #15140-122 | stored at -20 °C |
| 96 well culture plate | Cellstar | #655180 | |
| 24 well culture plate | Cellstar | #662160 | |
| 6 well culture plate | Cellstar | #657160 | |
| Dulbecco's Phosphate Buffered Saline (-) CaCl2 (-) MgCl2) (DPBS) | Life Technologies: Gibco | #14190-094 | stored at 4 °C |
| Dulbecco’s Modified Eagles Medium (DMEM) 500ml | Thermo Fisher Scientific: Invitrogen | #31966-021 | For Wnt-3A Conditioned Medium Production. Stored at 4 °C |
| Fetal Bovine Serum (FBS) | Bovogen | #SFBS LOT#11113 | For Wnt-3A Conditioned Medium Production. Stored at -20 °C |
| L Wnt3A cell line | ATCC | #CRL-2647 | For Wnt-3A Conditioend Medium Production. |
| TOP/FOP plasmids | Millipore | #17-285 | For measuring Wnt activity |
| pTK-Renilla | Promega | #E2241 | For measuring Wnt activity |
| HEK-293 | ATCC | #CRL-1573 | For measuring Wnt activity |
| Dual-Luciferase Reporter Assay System | Promega | #E1910 | For measuring Wnt activity |
| Zeocin | Thermo Fisher Scientific: Invitrogen | #R250-01 | For Wnt-3A Cell line selection |
| B27 supplement | Thermo Fisher Scientific: Invitrogen | #17504-044 | stored at -20 °C |
| N-Acetylcysteine | Sigma Aldrich | #A9165-5G | stored at -20 °C |
| Nicotinamide | Sigma Aldrich | #N0636 | stored at -20 °C |
| Human Epithelial Growth Factor (hEGF) | PrepoTech | #AF-100-15 | stored at -20 °C |
| Gastrin | Sigma Aldrich | #G9145 | stored at -20 °C |
| TGFb type I Receptor inhibitor (A83-01) | Tocris | #2939 | stored at -20 °C |
| Y-27632 dihydrochloride (RhoKi) | Selleckchem | #S1049 | stored at -20 °C |
| p38 MAPK inhibitor (p38i) (SB202190) | Sigma Aldrich | #S7067 | stored at -20 °C |
| Primocin | InvivoGen | #ant-pm-1 | stored at -20 °C |
| Human Noggin (hNoggin) | PrepoTech | #120-10C | stored at -20 °C |
| Human R-spondin 3 (hRspo-3) | R&D Systems | #3500-RS/CF | stored at -20 °C |
| Vancomycin | Sigma Aldrich | #861987- 250mg | stored at -20 °C |
| Gentamycin | Life Technologies: Gibco | #15710-049 | stored at -20 °C |
| Ethylenediamine tetraacetic acid (EDTA) | Sigma Aldrich | #431788 | Stored at 4 °C |
| Matrigel | Corning | #354230 | stored at -80 °C |
| TryplE Express | Life Technologies: Gibco | #12605-010 | for trypsinizing organoids for freezing |
| Recovery Cell Culture Freezing Medium | Life Technologies: Gibco | #12648010 | for freezing |
| Calcein | Life Technologies: Gibco | #C3100MP | stored at -20 °C |
| Forskolin | R&D Systems | #1099-50 mg | stored at -80 °C |
| Lumacaftor (VX-809) | Selleckchem | #s1565 | stored at -80 °C |
| Ivacaftor (VX-770) | Selleckchem | #s1144 | stored at -80 °C |
| Name of Reagents/Material | Solvent | Stock Concentration | Final Concentration |
| GlutaMax | 200 mM | 2m M | |
| Hepes | 1 M | 10 mM | |
| Penicillin/Streptomycin | 10K U/ml 10K µg/ml | 100 U/ml 100 µg/ml | |
| Zeocin | 100 mg/ml | 125 µg/ml | |
| B27 supplement | 100 x | 1 x | |
| N-Acetylcysteine | MiliQ H20 | 500 mM | |
| Nicotinamide | DPBS | 1 M | 10 mM |
| Human Epithelial Growth Factor (hEGF) | DPBS 0.1%BSA | 0.5 mg/ml | 50 ng/ml |
| Gastrin | DPBS | 100 µM | 10 nM |
| TGFb type I Receptor inhibitor (A83-01) | DMSO | 5 mM | 500 nM |
| Y-27632 dihydrochloride (RhoKi) | DMSO | 10 mM | 10 µM |
| p38 MAPK inhibitor (p38i) (SB202190) | DMSO | 30 mM | 10 µM |
| Primocin | 50 mg/ml | 100 µg/ml | |
| Human Noggin (hNoggin) | DPBS 0.1%BSA | 100 µg/ml | 100 ng/ml |
| Human R-spondin 3 (hRspo-3) | varies per lot | 300 ng/ml | |
| Vancomycin | 10 mg/ml | 50 µg/ml | |
| Gentamycin | 10 mg/ml | 50 µg/ml | |
| Ethylenediamine tetraacetic acid (EDTA) | MiliQ H20 | 0.5 M | 2 mM |
| Calcein | DMSO | 10 µg/ml | 3.3 ng/ml |
| Forskolin | DMSO | 10 mM | variable |
| Lumacaftor (VX-809) | DMSO | 20 mM | variable |
| Ivacaftor (VX-770) | DMSO | 20 mM | variable |
Riferimenti
- De Boeck, K., Amaral, M. D. Progress in therapies for cystic fibrosis. Lancet Respir Med. 4 (8), 662-674 (2016).
- Cutting, G. R. Cystic fibrosis genetics: from molecular understanding to clinical application. Nature Rev Genet. 16 (1), 45-56 (2015).
- Sosnay, P. R., Siklosi, K. R., et al. Defining the disease liability of variants in the cystic fibrosis transmembrane conductance regulator gene. Nature Genet. 45 (10), 1160-1167 (2013).
- Zielenski, J. Genotype and phenotype in cystic fibrosis. Respiration. 67 (2), 117-133 (2000).
- Van Goor, F., Hadida, S., et al. Rescue of CF airway epithelial cell function in vitro by a CFTR potentiator, VX-770. Proc Natl Acad Sci U.S.A. 106 (44), 18825-18830 (2009).
- Van Goor, F., Hadida, S., et al. Correction of the F508del-CFTR protein processing defect in vitro by the investigational drug VX-809. Proc Natl Acad Sci U.S.A. 108 (46), 18843-18848 (2011).
- Accurso, F. J., Rowe, S. M., et al. Effect of VX-770 in persons with cystic fibrosis and the G551D-CFTR mutation. N Engl J Med. 363 (21), 1991-2003 (2010).
- Ramsey, B. W., Davies, J., et al. A CFTR potentiator in patients with cystic fibrosis and the G551D mutation. N Engl J Med. 365 (18), 1663-1672 (2011).
- De Boeck, K., Munck, A., et al. Efficacy and safety of ivacaftor in patients with cystic fibrosis and a non-G551D gating mutation. J Cyst Fibros. 13 (6), 674-680 (2014).
- Boyle, M. P., Bell, S. C., et al. A CFTR corrector (lumacaftor) and a CFTR potentiator (ivacaftor) for treatment of patients with cystic fibrosis who have a phe508del CFTR mutation: a phase 2 randomised controlled trial. Lancet Respir Med. 2 (7), 527-538 (2014).
- Wainwright, C. E., Elborn, J. S., et al. Lumacaftor-Ivacaftor in Patients with Cystic Fibrosis Homozygous for Phe508del CFTR. N Engl J Med. 373 (3), 220-231 (2015).
- Van Goor, F., Yu, H., Burton, B., Hoffman, B. J. Effect of ivacaftor on CFTR forms with missense mutations associated with defects in protein processing or function. J Cyst Fibros. 13 (1), 29-36 (2014).
- Neuberger, T., Burton, B., Clark, H., Van Goor, F. Use of primary cultures of human bronchial epithelial cells isolated from cystic fibrosis patients for the pre-clinical testing of CFTR modulators. Methods Mol Biol. 741, 39-54 (2011).
- Randell, S. H., Fulcher, M. L., O'Neal, W., Olsen, J. C. Primary epithelial cell models for cystic fibrosis research. Methods Mol Biol. 742, 285-310 (2011).
- Karp, P. H., Moninger, T. O., et al. An in vitro model of differentiated human airway epithelia. Methods for establishing primary cultures. Methods Mol Biol. 188, 115-137 (2002).
- Sato, T., Vries, R. G., et al. Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche. Nature. 459 (7244), 262-265 (2009).
- Sato, T., Stange, D. E., et al. Long-term expansion of epithelial organoids from human colon, adenoma, adenocarcinoma, and Barrett's epithelium. Gastroenterology. 141 (5), 1762-1772 (2011).
- Clevers, H. Modeling development and disease with Organoids. Cell. 165 (7), 1586-1597 (2016).
- Dekkers, J. F., Wiegerinck, C. L., et al. A functional CFTR assay using primary cystic fibrosis intestinal organoids. Nature Med. 19 (7), 939-945 (2013).
- Dekkers, J. F., van der Ent, C. K., Beekman, J. M. Novel opportunities for CFTR-targeting drug development using organoids. Rare Diseases. 1 (1), e27112 (2014).
- Servidoni, M. F., Sousa, M., et al. Rectal forceps biopsy procedure in cystic fibrosis: technical aspects and patients perspective for clinical trials feasibility. BMC gastroenterology. 13, 91 (2013).
- Ommen, D. D. Z. -. V., Vijftigschild, L. A. W., et al. Limited premature termination codon suppression by read-through agents in cystic fibrosis intestinal organoids. J Cyst Fibros. 15 (2), 158-162 (2016).
- Dekkers, J. F., Gogorza Gondra, R. A., et al. Optimal correction of distinct CFTR folding mutants in rectal cystic fibrosis organoids. Eur Respir J. , (2016).
- Dekkers, J. F., Van Mourik, P., et al. Potentiator synergy in rectal organoids carrying S1251N, G551D, or F508del CFTR mutations. J Cyst Fibros. , (2016).
- Dekkers, J. F., Berkers, G., et al. Characterizing responses to CFTR-modulating drugs using rectal organoids derived from subjects with cystic fibrosis. Sci Transl Med. 8 (344), 344ra84 (2016).
- Li, H., Sheppard, D. N., Hug, M. J. Transepithelial electrical measurements with the Ussing chamber. J Cyst Fibros. 3, 123-126 (2004).
- Sheppard, D. N., Carson, M. R., Ostedgaard, L. S., Denning, G. M., Welsh, M. J. Expression of cystic fibrosis transmembrane conductance regulator in a model epithelium. Am J Physiol. 266 (4 Pt 1), L405-L413 (1994).
- Farin, H. F., van Es, J. H., Clevers, H. Redundant sources of Wnt regulate intestinal stem cells and promote formation of Paneth cells. Gastroenterology. 143 (6), 1518-1529 (2012).
- Drost, J., et al. Organoid culture systems for prostate epithelial and cancer tissue. Nat Protoc. 11 (2), 347-358 (2016).
- Vijftigschild, L. A. W., Berkers, G., et al. β2-adrenergic receptor agonists activate CFTR in organoids and subjects with cystic fibrosis. Eur Respir J. 48 (3), 768-779 (2016).
- Dekkers, R., et al. A bioassay using intestinal organoids to measure CFTR in human plasma. J Cyst Fibros. 14 (2), 178-181 (2015).
- Graeber, S. Y., et al. Intestinal Current Measurements Detect Activation of Mutant CFTR in Patients with Cystic Fibrosis with the G551D Mutation Treated with Ivacaftor. Am J Respir Crit Care Med. 192 (10), 1252-1255 (2015).
- Van Goor, F., et al. Ivacaftor potentiation of multiple CFTR channels with gating mutations. Journal of Cystic Fibrosis: Official Journal of the Eur Cyst Fibrosis. 11 (3), 237-245 (2012).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon