Method Article
Um hidrogel Construir e fibrina à base de cola Approach to Deliver Therapeutics em um Infarto do Miocárdio modelo murino.
Neste Artigo
Resumo
This protocol aims to alleviate the limitation of poor cell engraftment for stem cell treatment of myocardial infarctions through the use of a hydrogel system and a fibrin-based glue. With this approach, cell-to-tissue contact post-infarction can be maintained, increasing the therapeutic potential of beneficial agents at the site of injury.
Resumo
The murine MI model is widely recognized in the field of cardiovascular disease, and has consistently been used as a first step to test the efficacy of treatments in vivo1. The traditional, established protocol has been further fine-tuned to minimize the damage to the animal. Notably, the pectoral muscle layers are teased away rather than simply cut, and the thoracotomy is approached intercostally as opposed to breaking the ribs in a sternotomy, preserving the integrity of the ribcage. With these changes, the overall stress on the animal is decreased.
Stem cell therapies aimed to alleviate the damage caused by MIs have shown promise over the years for their pro-angiogenic and anti-apoptotic benefits. Current approaches of delivering cells to the heart surface typically involve the injection of the cells either near the damaged site, within a coronary artery, or into the peripheral blood stream2-4. While the cells have proven to home to the damaged myocardium, functionality is limited by their poor engraftment at the site of injury, resulting in diffusion into the blood stream5. This manuscript highlights a procedure that overcomes this obstacle with the use of a cell-encapsulated hydrogel patch. The patch is fabricated prior to the surgical procedure and is placed on the injured myocardium immediately following the occlusion of the left coronary artery. To adhere the patch in place, biocompatible external fibrin glue is placed directly on top of the patch, allowing for it to dry to both the patch and the heart surface. This approach provides a novel adhesion method for the application of a delicate cell-encapsulating therapeutic construct.
Introdução
Um enfarte do miocárdio (MI) é definida como a interrupção de sangue para uma região do coração causada por oclusão de uma artéria coronária principal. O dano resultante de um MI é devido à remodelação do tecido cardíaco viável em tecido cicatricial não-funcional, o que diminui a capacidade do coração ou, mais especificamente, no ventrículo esquerdo, para bater apropriadamente. Isto resulta numa diminuição no volume de sangue que pode ser entregue ao corpo com cada batimento cardíaco, conhecido como o volume de curso, e a percentagem de sangue que é bombeado para fora do coração com cada batimento cardíaco, conhecido como a fracção de ejecção 6. Estas, juntamente com outras funções diminuídas, aumenta a pressão sobre o resto do coração para manter a função adequada. Muitas vezes, esse aumento da pressão pode se tornar tão grave que faz com que um segundo ataque cardíaco, um fenômeno visto em aproximadamente 10% dos indivíduos 7.
Enquanto práticas médicas têm evoluído para tratarrescaldo de um MI, nenhuma técnica foi desenvolvida para parar, reduzir ou reverter os efeitos colaterais negativos da remodelação do tecido. Terapias com células-tronco surgiram como uma via possível para um tal tratamento, no entanto, apesar do seu potencial promissor, as células-tronco não têm sido bem sucedidos no contexto clínico. Uma teoria para as suas deficiências é a incapacidade de garantir as células benéficos permanecer no local de enfarte longo o suficiente para gerar resultados favoráveis 5. Demonstrou-se que não mais do que 24% de células que são simplesmente injectada no local de enfarte sobreviveram e permaneceram no local danificado um dias pós-parto 2. A perspectiva possível para resolver este problema de retenção celular é desenvolver sistemas de hidrogel biocompatíveis que encapsulam células ou terapêuticas, que podem ser entregues com o sítio danificado. O hidrogel de escolha neste protocolo é um poli (etileno-glicol) dimetacrilato devido ao seu uso anterior em encapsulamento de células procedures, no entanto, qualquer hidrogel capaz de encapsulação pode ser utilizado 8. A entrega do remendo directamente para o local da lesão assegura o contacto célula-a-tecido durante um período prolongado de tempo, aumentando o período de tempo as células podem fornecer factores benéficos para o miocárdio subjacente.
Um gargalo para o remendo abordagem é a dificuldade de fazer aderir o penso à superfície do coração. Muitos grupos superar este através de uma variedade de técnicas, sendo o mais prevalente de uma sutura simples amarrar a construção à superfície do coração de 9,10. Isto tem sido bem sucedida num certo número de casos em que a construção é feita de um material mais rígido, mas falha quando tentada em um sistema de hidrogel, devido à concentração elevada de água e delicada natureza da construção remendo. Para superar isto, nós utilizamos um sistema de adesivo externa cola de fibrina que imita a química da formação de coágulos. A cola de fibrina tem sido utilizada em vários gabinetes médicos, Including lágrimas Dura, fístulas brônquicas, e transplante da córnea, destacando a biocompatibilidade do produto na forma de um selante de ferida 11-13. Além disso, a fibrina tem sido usado para uma variedade de fins cardíacas, incluindo o tratamento cirúrgico das rupturas do ventrículo esquerdo e cirurgias de revascularização miocárdica, no entanto, a sua utilização como uma cola de aderência para uma correção cardíaca não é comumente usado 14-17. Uma formulação simples de trombina e fibrinogénio resulta em uma cola biocompatível que pode ser colocado directamente no lado de fora de um remendo cardíaca externa, proporcionando um sistema de adesão viável para garantir a interacção remendo coração.
Protocolo
Procedimento está em total compatibilidade com o número de protocolo do IACUC 13302 e foi aprovado pela divisão de recursos animais.
1. Instrumento Preparação
- Autoclave todos os instrumentos não descartáveis usados antes do procedimento cirúrgico para garantir a esterilidade.
- Esterilizar instrumentos utilizados várias vezes em uma sessão com um esterilizador talão de vidro entre os usos.
2. Preparação Hidrogel
- Descongelar e células-tronco placa pelo menos 24 horas antes da criação do constructo hidrogel.
- Prepare remendos um dia antes do procedimento cirúrgico usando um aparelho de estereolitografia (ou instrumento similar), que foi descrito em detalhes em publicações anteriores 8,18.
- Para criar o hidrogel, gerar primeiro um design (CAD) modelo assistido por computador do patch desejado e exportar o projeto para o formato stereolithographic (STL).
- Criar uma solução pré-gel por dissolving de poli (etilenoglicol) dimetacrilato (PEGDMA) em 1x PBS estéril para obter uma solução a 20% w / v. Ao mesmo tempo, dissolve-se o fotoiniciador 1- [4- (2-hidroxi-etoxi) -fenil] -2-hidroxi-2-metil-1-propano-1-ona em DMSO. Adicionar o fotoiniciador para a solução final de PEGDMA com um w / v de 0,5%. Directamente antes da reticulação, adicionar 100 ml de a densidade de células desejada. Nota: A densidade de células entre 2,0 x 10 5 -2,0 x 10 6 células / ml é recomendada.
- Pipetar a solução de pré-gel em um prato no centro da plataforma de SLA e executar o software SLA com o desenho STL formatada previamente carregado.
- Remover os remendos do aparelho e incubar os hidrogéis O / N em meio de Eagle modificado por Dulbecco (DMEM) suplementado com soro a 5% de bovino fetal (FBS), 100 U / ml de penicilina, e 100 mg / ml de estreptomicina para permitir células para ajustar para o ambiente dentro do patch.
3. Preparação Animal e intubati Oralem
- Avalie cada rato antes do procedimento para garantir que o animal está em boas condições de saúde, como determinado a partir de seus hábitos de higiene e interações com seus companheiros de gaiola. Nota: fêmeas de 8-10 semanas de idade C57BL / 6J foram usadas para este procedimento, no entanto, qualquer tipo ou idade do rato pode ser utilizado.
- Inserir os animais numa câmara de anestesia e expor a 5% de isofluorano com de 1 L / min de O2 suporte. Monitorar o nível de anestesia por toe pitada reflexo.
- Uma vez que o animal está devidamente anestesiados, pesar e colocá-los no stand intubação.
- Dirigir uma fonte de luz em direcção cavidade torácica do animal e utilizar uma pinça para retrair a superfície da laringe e expor as cordas vocais. Passe cuidadosamente um G angiocath 20 entre as cordas vocais, e suavemente inserir na traquéia. Detectar uma inserção correcta por um movimento mecânico da cavidade torácica uma vez que o cateter está ligado ao ventilador pequeno de animais.
- Ajustar as definições de ventilação para poe peso do animal com base nas orientações do fabricante.
- Uma vez entubado, colocar o animal em decúbito dorsal sobre uma almofada de aquecimento para evitar a hipotermia. Certifique-se de que a almofada de aquecimento não deve exceder 40 ° C. Se necessário, colocar uma barreira entre o animal e a almofada de aquecimento para minimizar a possibilidade de queimaduras.
- Remover o cabelo do local cirúrgico através da utilização de um creme depilatório. Esterilizar o site por 3 esfrega alternadas de betadine e etanol 75% para garantir a esterilização adequada. Inserir uma cortina para expor apenas o local cirúrgico, e colocar veterinário unguento para os olhos para evitar a secura durante o procedimento.
4. Procedimento Cirúrgico
- A toracotomia é realizada no lado esquerdo do animal, portanto, fazer uma incisão na pele aproximadamente 1 cm para a esquerda do esterno, que atravessa o comprimento do esterno.
- Use uma pinça para separar a camada muscular subjacente da caixa torácica em dois passos. Observar uma Delineating linha que representa os músculos peitorais maiores do animal. Levante esta muscular ligeiramente, separá-lo do músculo oblíquo externo subjacente e retrair medial. Em seguida, liberar o músculo oblíquo externo da caixa torácica subjacente da mesma maneira, e retrair lateralmente, proporcionando uma vista desafogada das segunda, terceira e quarta costelas.
- Realizar a toracotomia entre a terceira ea quarta costelas. Suavemente levantar a quarta costela e usar um cauterizador para abrir a cavidade do peito entre as terceira e quarta costela. Coloque afastadores para abrir ainda mais a cavidade e expor o coração.
- Use uma pinça para romper o pericárdio do coração fina.
- Ligadura da artéria coronária esquerda com uma sutura de nylon 8-0 monofilamento. Coloque a sutura de aproximadamente 4 mm a partir do vértice do coração, directamente abaixo da extremidade inferior do átrio esquerdo. Determinar a colocação adequada de sutura por um branqueamento do miocárdio ventricular e um aumento no tamanho do átrio esquerdo, após o Suture foi amarrado.
5. remendo Colocação e Glue
- Manter manchas a 37 ° C e 5% de CO 2 condições até à sua utilização.
- Suavemente levantar o remendo com uma espátula plana terminada e colocá-lo suavemente na superfície do coração, no local do enfarte.
Nota: Para evitar que escorregue do ventrículo esquerdo, o patch pode ser mantido no lugar por levemente mantendo contato usando a espátula ou a ponta de um par de fórceps. - Preparar a cola por mistura de uma proporção de 4: 1 de fibrinogénio a trombina. Misture a solução por pipetagem repetida até que começa a engrossar, geralmente dentro de 1 min após o início da preparação.
- Uma vez que a viscosidade da solução atinge o nível desejado, transferir rapidamente aproximadamente 10 ml a superfície do emplastro. Nota: O tempo de coagulação da cola de fibrina é rápido, proporcionando uma pequena janela de oportunidade para a transferência eficiente da cola.
6. Sutura
- Executar todas as suturas de fechamento usando uma sutura de nylon 6-0 monofilamento.
- Feche a camada de costela com 3-4 suturas interrompidas individuais.
- Antes do fechamento completo da camada intercostal, inserir uma cânula de PE-10 para dentro da incisão para evacuar a cavidade torácica após o encerramento é completa e restabelecer a pressão intrapleural adequada.
- Feche os músculos peitorais com 3-4 suturas interrompidas individuais.
- Selar a camada de pele com sutura contínua.
- Depois do encerramento completo, anexar uma seringa de 1,0 ml para a extremidade da cânula e usá-lo para evacuar a cavidade torácica.
- Aplicar um adesivo de tecido para o local da incisão para reforçar o local da sutura.
7. O tratamento pós-operatório
- Submeter ratinhos uma injecção de buprenorfina (0,05-1,0 mg / kg) e carprofeno (2,2 mg / kg) por via subcutânea imediatamente após a ligação coronária e pelo menos 20 min antes da avivamento. Administrar as duas drogas 6-8 horas após a cirurgiaE, em seguida, dar duas vezes por dia por até três dias para controlar a dor e angústia.
- Monitorar continuamente os animais até consciente e cada hora para a seguinte primeira cirurgia 4 horas. Realize um segundo exame a noite da cirurgia (2-4 horas mais tarde) para administrar uma segunda dose de analgésico.
- Monitorar os animais diariamente após o segundo dia após o procedimento, até que os animais parecem estáveis.
8. Análise da função cardíaca e Histologia
- Realizar ecocardiógrafos nos ratos 4 semanas após o procedimento para determinar a extensão dos danos após a MI.
- Anestesiar ratos com 4-5% de isoflurano dentro de uma câmara de anestesia para a indução da anestesia inalatória e, em seguida 2% de isoflurano através de máscara facial para manutenção da anestesia.
- Limpe a área de imagem com um creme depilatório e usar um pequeno ultra-som animal para obter uma varredura ecocardiografia 2D M-mode do batimento cardíaco e gravar os parâmetros asso funcionalciados com ele.
- Eutanásia os ratos numa câmara de dióxido de carbono, em seguida, recolher os corações dos animais e em lugar de uma solução de formalina a 10% durante 24 h. Após 24 horas, transferir os corações para 70% de etanol e manter a 4 ° C até o processamento de tecidos.
- Processar os corações e incorporá-los em blocos de parafina.
- Cortar 5 milímetros secções através da região ventricular do coração, começando no vértice e terminando no átrio.
- Stain fatias com tanto tricrômico de Masson e hematoxilina e eosina utilizando protocolos padrão segmentado.
Resultados
Durante o procedimento cirúrgico, a ligação da artéria coronária esquerda pode ser identificado por um acentuado branqueamento a jusante da artéria oclusa. Como um teste antes de amarrar o nó, a sutura pode ser apertado brevemente para verificar se ele está no lugar apropriado. Além disso, uma vez que a oclusão da artéria os resultados na redução quase instantâneo na capacidade do átrio esquerdo para bater apropriadamente, átrio esquerdo irá aumentar em resposta a um refluxo de sangue no sistema.
Medições de ecocardiografia em modo-M tomado tão cedo quanto dois dias pós-infarto mostrar uma cessação de movimento da parede esquerda, indicativo da reconstrução muscular. Cálculos qualitativos feitos a partir dos dados mostram uma diminuição da fração de ejeção e volume sistólico nos corações infartados. No final da experiência, quando os corações são recolhidos para fins histológicos, uma clara dilatação do ventrículo esquerdo, pode ser visto, juntamente com um adelgaçamento do ventrículo esquerdoda parede, e a deposição de colagénio que indica a deposição de tecido de cicatriz no local de funcionamento cardiomiócitos (Figura 1).
Também visto na análise histológica é a presença do hidrogel construir graças à administração do gel de fibrina (Figura 2). Para nossos propósitos, o sistema adesivo deve ser suficiente para permitir o controle posicionamento preciso e minimizar o escoamento subsequente em órgãos circunvizinhos viscoso, mas o suficiente para não maleável para interferir com a função do coração. Foram realizados testes preliminares para calcular a viscosidade, tempo de gelificação, e a rigidez de várias proporções de fibrinogénio / trombina, a fim de determinar a combinação adequada que se adapte às nossas necessidades. Análise in vivo foi realizada para testar a capacidade da cola de fibrina para manter patch- -adesão ao tecido permitindo ainda para a função cardíaca completo (dados não mostrados). Deve notar-se que a cola de fibrina não prejudicar o miocárdio, tal como evidenciado pela lack de remodelação do tecido ou afinamento ventricular no local (Figura 2). Os cardiomiócitos permanecem intactas apesar da adição de um emplastro tanto cardíaca e sua cola que acompanha. Além disso, o teste de viabilidade que confirma que a administração de cola de fibrina para a superfície externa de um emplastro de hidrogel encapsulando células não afectou a sobrevivência das células dentro do remendo (Figura 3).
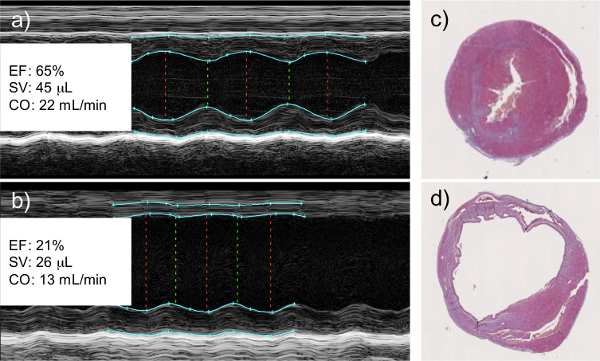
Figura 1:. Coronários Artery Resultados Ligadura deixado em uma diminuição da função cardíaca medida ao ecocardiograma modo-M ecocardiografia de saudáveis (a) e infartados (b) corações. Corações infartados mostram uma clara falta de movimento da parede onde o tecido viável foi substituído por tecido cicatricial. Isso se correlaciona com uma diminuição mensurável na fração de ejeção do ventrículo esquerdo (FE), acidente vascular cerebral cardíacade volume (SV), e o débito cardíaco (CO). A análise histológica de saudável (c) e (d) corações infartados mostra dilatação do ventrículo esquerdo e afinamento da parede do ventrículo esquerdo do miocárdio infartado, ambos os sinais de remodelação do tecido e deposição de tecido cicatricial. Imagens histológicas são fatias secções transversais que capturam a menor (câmara) ventrículos direito e esquerdo (maior câmara) e.
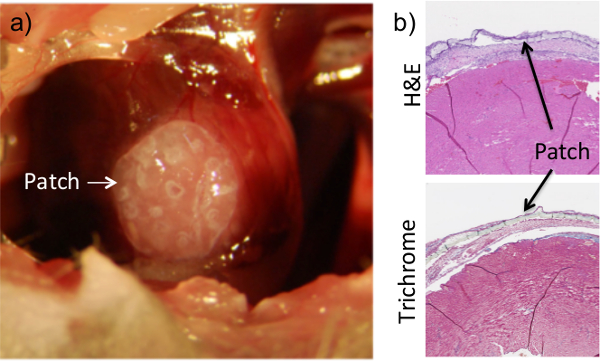
Figura 2:. Aplicação de fibrina Flue Garante remendo Adesão ao coração O penso é colocado sobre a superfície do coração, enquanto a cavidade torácica é exposto durante o procedimento (a). Uma vez colocado, uma cola à base de fibrina é adicionado no topo do coração e deixou-se secar. O patch pode ser claramente visto em cortes histológicos de tecido cardíaco que foram coletadas em uma semana pós-procedimento (b).Dissociação do remendo da superfície do coração em imagens histológicas é um artefato do processo de cobrança e corte. Os resultados são consistentes até 8 semanas de adesão.

Figura 3: cola à base de fibrina-não prejudique encapsulados Tecidos A viabilidade celular foi medida através de análise MTT de 1 semana após a administração de uma cola à base de fibrina utilizando protocolos descritos em pormenor em publicações anteriores 8.. A viabilidade das células dentro do emplastro não foi afectada pela adição da cola à superfície da construção.
Discussão
Com esta abordagem para o modelo murino MI, desenvolvemos um sistema que minimiza o dano para as zonas não miocárdio, que estão associados a outras técnicas de MI de murino. Estas áreas incluem danos causados por uma traqueostomia, o corte da camada muscular, e à ruptura de nervuras para expor a cavidade torácica. Nós acreditamos que estas mudanças melhorar os resultados globais cirúrgicos graças ao cuidado para manter o máximo das principais estruturas, incluindo as costelas e camadas musculares, intacta durante o procedimento cirúrgico.
Deve notar-se que existem algumas limitações para esta técnica, com a maior sendo a sua natureza morosa, resultando em apenas 8-10 procedimentos cirúrgicos completos num único dia. Para superar isto, um segundo ventilador pode ser utilizado, permitindo que o procedimento a ser realizado em dois animais simultaneamente. Além disso, grandes vasos, tais como os vasos intercostais einterior artéria torácica, devem ser evitadas quando se realiza a toracotomia. Se perto de um destes recipientes, um cauterizador deve ser usada para evitar o sangramento devido a ruptura de uma artéria.
A cola de fibrina é conhecido tanto no laboratório e na clínica, graças à sua capacidade para ajudar rapidamente a formação de coágulos, bem como o seu potencial para entregar e MSCs hospedeiras 14-17,19. Para os nossos propósitos, a cola de fibrina serve como uma abordagem biocompatível para aderir um hidrogel à base de água para construir a superfície do coração. A utilização de uma cola à base de fibrina tem sido bem sucedida em manter a construção de hidrogel no local danificado durante até 8 semanas, com a possibilidade de contacto com o tecido de um longo período de tempo. A utilização deste sistema permitiu a adesão de controlo para a colocação do construto delicada, sem a necessidade de suturas adicionais que prejudicam o miocárdio, bem como a própria construção. Verificou-se que a própria cola não é tóxico para as células encapsuladas umO ND não afectar negativamente o tecido subjacente. O hidrogel e do sistema de cola à base de fibrina pode ser aplicada a uma variedade de outras finalidades de engenharia de tecidos que desejam célula ou contacto terapêutico por um período prolongado de tempo. Além disso, com a utilização do método de fabricação de SLA, desenhos e estruturas podem ser incorporados dentro do remendo para criar um sistema mais complexo para a entrega de célula 18.
Um revés para a utilização da cola à base de fibrina é o facto de mais do que um investigador deve estar presente na sala durante a colocação cirúrgica de remendo e adição de cola. É o trabalho do primeiro pesquisador para garantir que o sistema permanece no lugar e não se perder na cavidade torácica, enquanto o segundo investigador mistura a solução e aplica-lo para o patch depois de viscosidade adequada é atingido. Para optimizar o momento da entrega cola, sugere-se que o segundo investigador e também testa vezes a gelificação da cola antes da colocação do remendo,desde gelificação adequada da cola utilizada é crítica para a aderência remendo.
Há uma série de passos críticos e áreas propensas erro no âmbito do protocolo, com a primeira sendo a indução do infarto do miocárdio. É imperativo para verificar se há sinais, tais como o branqueamento da parede do ventrículo esquerdo e do alargamento do átrio esquerdo, para garantir a oclusão da artéria coronária esquerda. Isto pode ser feito antes da adição do ponto de cruzamento e simplesmente apertando a extremidade das cordas de sutura. Se for determinado que a artéria coronária esquerda não está fechada por sutura, a cadeia pode ser retirado e reaplicado. A segunda medida é crítica para continuar a acompanhar o tubo de intubação durante todo o procedimento, para garantir que ele permaneça dentro da traquéia e não ficar puxado para fora meados de cirurgia. Finalmente, durante toda a cirurgia, todas as tentativas devem ser feitas para evitar o contato com os pulmões, como qualquer contato tem o potencial de levar a um colapso pulmonar.Se, durante a cirurgia, colapso do pulmão ocorre, simplesmente bloquear o tubo de saída do intubator por até 3 segundos em uma tentativa de re-inflacionar regiões conturbadas dos pulmões.
Divulgações
The authors declare that they have no competing financial interests.
Agradecimentos
Este trabalho foi financiado pelo US Army Grant (W81XWH-08-1-0701) e uma bolsa de Carle Hospital Foundation.
Materiais
| Name | Company | Catalog Number | Comments |
| Harvard Model 687 Mouse Ventilator | Harvard Apparatus | 55-0001 | |
| Inintech Biosciences LLC Dry Glass Bead Sterilizer | Fisher Scientific | NC9531961 | |
| Leica MZ6 surgical microscope | Leica | ||
| Cautery Kit | Gemini | GEM 5917 | |
| Delicate Forceps - 0.4 mm Tips Angled | Fine Science Tools | 11063-07 | |
| Agricola Retractor - 3.5 cm Spread | Fine Science Tools | 17005-04 | |
| Spring Scissors - 2.5 mm Blades Straight | Fine Science Tools | 15000-08 | |
| Castroviejo Needle Holder - w/Lock Tungsten Carbide 14 cm | Fine Science Tools | 12565-14 | |
| Iris Scissors - Delicate Straight 10.5 cm | Fine Science Tools | 14060-10 | |
| 8-0 monofilament suture | Ethicon | 8730P | |
| 6-0 Silk suture | Ethicon | 639G | |
| Thrombin | Sigma | T7009 | |
| Fibrinogen | Sigma | F3879 | |
| Vetbond Tissue Adhesive | 3M | 1469SB |
Referências
- Kolk, M. V., et al. LAD-ligation: a murine model of myocardial infarction. Journal of visualized experiments : JoVE. , (2009).
- Li, Y., Yao, Y., Sheng, Z., Yang, Y., Ma, G. Dual-modal tracking of transplanted mesenchymal stem cells after myocardial infarction. International journal of nanomedicine. 6, 815-823 (2011).
- Nagaya, N., et al. Intravenous administration of mesenchymal stem cells improves cardiac function in rats with acute myocardial infarction through angiogenesis and myogenesis. American journal of physiology. Heart and circulatory physiology. 287, H2670-H2676 (2004).
- Wang, J. S., Shum-Tim, D., Chedrawy, E., Chiu, R. C. The coronary delivery of marrow stromal cells for myocardial regeneration: pathophysiologic and therapeutic implications. The Journal of thoracic and cardiovascular surgery. 122, 699-705 (2001).
- Cashman, T. J., Gouon-Evans, V., Costa, K. D. Mesenchymal stem cells for cardiac therapy: practical challenges and potential mechanisms. Stem cell reviews. 9, 254-265 (2013).
- Sutton, M. G., Sharpe, N. Left ventricular remodeling after myocardial infarction: pathophysiology and therapy. Circulation. 101, 2981-2988 (2000).
- Smolina, K., Wright, F. L., Rayner, M., Goldacre, M. J. Long-term survival and recurrence after acute myocardial infarction in England, 2004 to 2010. Circulation. Cardiovascular quality and outcomes. 5, 532-540 (2012).
- Chan, V., Zorlutuna, P., Jeong, J. H., Kong, H., Bashir, R. Three-dimensional photopatterning of hydrogels using stereolithography for long-term cell encapsulation. Lab on a chip. 10, 2062-2070 (2010).
- Kai, D., et al. Stem cell-loaded nanofibrous patch promotes the regeneration of infarcted myocardium with functional improvement in rat model. Acta biomaterialia. 10, 2727-2738 (2014).
- Serpooshan, V., et al. The effect of bioengineered acellular collagen patch on cardiac remodeling and ventricular function post myocardial infarction. Biomaterials. 34, 9048-9055 (2013).
- Cavallo, L. M., Solari, D., Somma, T., Savic, D., Cappabianca, P. The Awake Endoscope-Guided Sealant Technique with Fibrin Glue in the Treatment of Postoperative Cerebrospinal Fluid Leak After Extended Transsphenoidal Surgery: Technical Note. World neurosurgery. , (2013).
- Chung, H. W., Mehta, J. S. Fibrin glue for Gundersen flap surgery. Clinical Ophthalmology. 7, 479-484 (2013).
- Dunn, C. J., Goa, K. L. Fibrin sealant: a review of its use in surgery and endoscopy. Drugs. 58, 863-886 (1999).
- Chi, N. H., et al. Cardiac repair achieved by bone marrow mesenchymal stem cells/silk fibroin/hyaluronic acid patches in a rat of myocardial infarction model. Biomaterials. 33, 5541-5551 (2012).
- Erb, M. A., Claus, T., Hartrumpf, M., Bachmann, S., Albes, J. M. The use of Tachosil surgical patch or fibrin glue in coronary artery surgery does not affect quality of anastomosis or provoke postoperative adhesions in pigs. European journal of cardio-thoracic surgery : official journal of the European Association for Cardio-thoracic Surgery. 36, 703-707 (2009).
- Okada, K., et al. Surgical treatment for rupture of left ventricular free wall after acute myocardial infarction. Interactive cardiovascular and thoracic surgery. 4, 203-206 (2005).
- Simpson, D., Liu, H., Fan, T. H., Nerem, R., Dudley, S. C. A tissue engineering approach to progenitor cell delivery results in significant cell engraftment and improved myocardial remodeling. Stem Cells. 25, 2350-2357 (2007).
- Jeong, J. H., et al. Living' microvascular stamp for patterning of functional neovessels; orchestrated control of matrix property and geometry. Advanced Materials. 24, 58-63 (2012).
- Wu, X., Ren, J., Li, J. Fibrin glue as the cell-delivery vehicle for mesenchymal stromal cells in regenerative medicine. Cytotherapy. 14, 555-562 (2012).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados