Method Article
Ein Hydrogel Konstruieren und Fibrin-basierte Kleber Umgangs Therapeutics in einem murinen Myokardinfarkt Modell liefern.
In diesem Artikel
Zusammenfassung
This protocol aims to alleviate the limitation of poor cell engraftment for stem cell treatment of myocardial infarctions through the use of a hydrogel system and a fibrin-based glue. With this approach, cell-to-tissue contact post-infarction can be maintained, increasing the therapeutic potential of beneficial agents at the site of injury.
Zusammenfassung
The murine MI model is widely recognized in the field of cardiovascular disease, and has consistently been used as a first step to test the efficacy of treatments in vivo1. The traditional, established protocol has been further fine-tuned to minimize the damage to the animal. Notably, the pectoral muscle layers are teased away rather than simply cut, and the thoracotomy is approached intercostally as opposed to breaking the ribs in a sternotomy, preserving the integrity of the ribcage. With these changes, the overall stress on the animal is decreased.
Stem cell therapies aimed to alleviate the damage caused by MIs have shown promise over the years for their pro-angiogenic and anti-apoptotic benefits. Current approaches of delivering cells to the heart surface typically involve the injection of the cells either near the damaged site, within a coronary artery, or into the peripheral blood stream2-4. While the cells have proven to home to the damaged myocardium, functionality is limited by their poor engraftment at the site of injury, resulting in diffusion into the blood stream5. This manuscript highlights a procedure that overcomes this obstacle with the use of a cell-encapsulated hydrogel patch. The patch is fabricated prior to the surgical procedure and is placed on the injured myocardium immediately following the occlusion of the left coronary artery. To adhere the patch in place, biocompatible external fibrin glue is placed directly on top of the patch, allowing for it to dry to both the patch and the heart surface. This approach provides a novel adhesion method for the application of a delicate cell-encapsulating therapeutic construct.
Einleitung
Einen Myokardinfarkt (MI) ist als die Unterbrechung des Blut zu einem Bereich des Herzens durch den Verschluss einer Koronararterie verursacht großen definiert. Der Schaden durch eine resultierende MI ist auf die Umgestaltung der lebensfähigen Herzgewebe in nichtfunktionelle Narbengewebe, das die Fähigkeit des Herzens, oder, genauer gesagt, die linke Herzkammer, um richtig zu schlagen abnimmt. Dies führt zu einer Abnahme des Volumens an Blut, die auf den Körper mit jedem Herzschlag, wie das Hubvolumen bekannt, und der Prozentsatz von Blut, das mit jedem Herzschlag aus dem Herzen gepumpt wird, da die Auswurffraktion 6 bekannt geliefert werden kann. Diese, zusammen mit anderen Funktionen vermindert, erhöht sich die Belastung für den Rest des Herzens, um eine angemessene Funktion aufrecht zu erhalten. Oft kann diese erhöhte Belastung so schwerwiegend werden, dass sie einen zweiten Herzinfarkt, ein Phänomen, bei etwa 10% der Individuen 7 ersichtlich bewirkt.
Während Arztpraxen entwickelt haben, um zu behandeln,Unmittelbar nach einem MI hat keine Technik entwickelt, um anzuhalten, langsam, oder umgekehrt die negativen Nebenwirkungen der Gewebeumbau. Stammzelltherapien als mögliche Weg für eine solche Behandlung trotz ihrer vielversprechendes Potential sich jedoch gezeigt, wurden Stammzellen in der Klinik nicht bewährt. Eine Theorie für ihre Mängel ist die Unfähigkeit, zu gewährleisten, die positiven Zellen an der Stelle des Infarkts lang genug, um gute Ergebnisse zu erzeugen 5 bleibt. Es hat sich gezeigt, dass nicht mehr als 24% der Zellen, die einfach in der Stelle des Infarkts injiziert lebten und blieb an der beschädigten Stelle 1 Tag nach der Lieferung 2. Eine mögliche Perspektive für Lösung dieses Problems der Zellrückhaltung ist es, biokompatibles Hydrogel-Systeme, die entweder Zellen oder Therapeutika, die mit dem geschädigten Ort geliefert werden kann kapseln zu entwickeln. Hydrogel nach Wahl in diesem Protokoll ist ein Poly (ethylenglycol) dimethacrylat aufgrund seiner vorherigen Verwendung in Zellverkapselung procedures jedoch jede Hydrogels fähig Verkapselung 8 verwendet werden. Die Lieferung der Patch direkt an der Stelle der Verletzung gewährleistet Zell-Gewebekontakt über einen längeren Zeitraum, was die Länge der Zeit, die Zellen begünstigende Faktoren an der darunterliegenden Myokard bereitzustellen.
Ein Hindernis für den Patch-Ansatz ist die Schwierigkeit des Anklebens des Pflasters auf der Herzoberfläche. Viele Gruppen haben dies durch eine Vielzahl von Techniken, die am häufigsten als eine einfache Naht, um das Konstrukt zur Herzoberfläche 9,10 binden überwinden. Dies wurde in einer Reihe von Fällen, in denen das Konstrukt aus einem steiferen Material hergestellt als erfolgreich erwiesen, aber nicht, wenn sie auf einem Hydrogel-System versucht, aufgrund der hohen Wasserkonzentration und empfindliche Natur der Patch-Konstrukt. Um dies zu überwinden, haben wir ein Fibrinkleber äußere Klebersystem, das die Chemie der Gerinnselbildung verwendet nachahmt. Fibrinkleber wurde in zahlreichen Arztpraxen eingesetzt, including dura Tränen Bronchusfisteln und Hornhauttransplantation, Hervorhebung der Biokompatibilität des Produkts als ein Wunddichtungsmittel 11-13. Zusätzlich hat Fibrin für eine Vielzahl von kardialen Zwecke, einschließlich der chirurgischen Behandlung der linksventrikulären Brüche und koronaren Bypass-Operationen, wird jedoch seine Verwendung als Haftklebstoff für einen Herz Patch nicht gebräuchlich 14-17 verwendet. Eine einfache Formulierung von Thrombin und Fibrinogen Ergebnisse in einem biokompatiblen Klebstoff, der direkt auf der Außenseite einer äußeren Herz Pflaster platziert werden kann, wodurch eine lebensfähige Haftsystem Patch Herz Interaktion gewährleisten.
Protokoll
Vorgehensweise ist in die volle Kompatibilität mit IACUC Protokollnummer 13302 und wurde von der Abteilung von Tier Ressourcen genehmigt.
1. Instrumentenaufbereitung
- Autoklaven alle Nicht-Einweginstrumente vor dem chirurgischen Verfahren verwendet werden, um Sterilität zu gewährleisten.
- Sterilisieren Instrumente mehrfach in einer Session mit einer Glasperle Sterilisator zwischen den Anwendungen verwendet.
2. Hydrogelpräparat
- Auftauen und Platte Stammzellen mindestens 24 Stunden vor der Erstellung des Hydrogels Konstrukt.
- Vorbereitung Patches einen Tag vor dem chirurgischen Eingriff unter Verwendung eines Stereolithographievorrichtung (oder ein ähnliches Instrument), welches in allen Einzelheiten in früheren Publikationen 8,18 beschrieben wurde.
- Um das Hydrogel zu erstellen, zuerst einen Computer Aided Design (CAD) Modell des gewünschten Patches erzeugen und exportieren Sie das Design an Stereolithographie Format (STL).
- Erstellen Sie eine pre-Gel-Lösung durch dissolving Poly (ethylenglycol) dimethacrylat (PEGDMA) in sterile 1x PBS, um eine 20% w / v-Lösung zu erhalten. Gleichzeitig lösen sich die Photoinitiator 1- [4- (2-hydroxy- ethoxy) phenyl] -2-hydroxy-2-methyl-1-propan-1-on in DMSO. Fügen den Photoinitiator zu dem PEGDMA Lösung bei einem End w / v von 0,5%. Direkt vor der Vernetzung, werden 100 ml der gewünschten Dichte der Zellen. Hinweis: eine Zelldichte zwischen 2,0 x 10 5 -2.0 x 10 6 Zellen / ml empfohlen.
- Pipettieren Sie die Pre-Gel-Lösung in eine Schale in der Mitte des SLA-Plattform und führen Sie die SLA-Software mit dem zuvor hochgeladenen STL formatiert Design.
- Entfernen Sie die Flecken aus der Vorrichtung und inkubieren der Hydrogele O / N in Dulbeccos modifiziertem Eagle-Medium (DMEM) mit 5% fötalem Rinderserum (FBS), 100 U / ml Penicillin und 100 mg / ml Streptomycin, damit für die Zellen zu justieren an die Umgebung im Pflaster.
3. Vorbereitung der Tiere und Oral intubatiauf
- Beurteilen Sie jede Maus vor dem Verfahren, um sicherzustellen, dass das Tier in guter Gesundheit, wie aus ihrer Pflege Gewohnheiten und Interaktionen mit ihren Käfiggenossen bestimmt. Anmerkung: Weiblich 8-10 Wochen alte C57BL / 6J-Mäusen wurden für dieses Verfahren verwendet wird, jedoch jede Maus Alter oder der Art verwendet werden kann.
- Zeigen die Tiere in einem Narkosekammer und setzen auf 5% Isofluran mit einem 1 l / min O 2 Unterstützung. Überwachen Sie das Niveau der Anästhesie durch toe Prise Reflex.
- Sobald das Tier richtig betäubt wird, wiegen und legen sie auf die Intubation Ständer.
- Leiten eine Lichtquelle in Richtung Brustkorb des Tieres und verwenden Pinzette, um den Kehlkopf-Oberfläche zurückziehen und setzen die Stimmbänder. Sorgfältig führen eine 20 G Angiocath zwischen den Stimmbändern und reibungslos in die Trachea einzuführen. Erkennen die richtige Einsetzen durch eine mechanische Bewegung des Brustkorbs, wenn der Katheter mit dem Kleintierbeatmungsgerät angeschlossen.
- Passen Beatmungseinstellungen zu the Gewicht des Tieres anhand von Richtlinien des Herstellers.
- Sobald intubiert, legen Sie das Tier in Rückenlage auf einem Heizkissen, um Unterkühlung zu verhindern. Sicherzustellen, daß die Heizmatte nicht über 40 ° C nicht überschreiten. Falls erforderlich, stellen eine Barriere zwischen dem Tier und dem Heizkissen, um die Möglichkeit von Verbrennungen zu minimieren.
- Entfernen Haare von der Operationsstelle durch die Verwendung einer Enthaarungscreme. Sterilisieren Sie die Website von 3 Wechsel scheuert von Betadin und 75% Ethanol, um die ordnungsgemäße Sterilisation gewährleistet. Legen Sie ein Tuch, um nur die Operationsstelle freizulegen, und legen Sie vet Salbe auf die Augen bis zur Trockenheit während des Verfahrens zu verhindern.
4. Chirurgische Verfahren
- Der Thorakotomie auf der linken Seite des Tieres durchgeführt wird, erschweren daher einen Hautschnitt von ungefähr 1 cm auf der linken Seite des Brustbeins, die die Länge des Brustbeins verläuft.
- Verwenden einer Pinzette, um die Muskelschicht von der darunter liegenden Brustkorb in zwei Schritten zu trennen. Beachten Sie eine delinetriebs Linie, die die großen Brustmuskulatur des Tieres darstellt. Heben Sie diesen Muskel leicht, trennen sie von der zugrunde liegenden Äußerer Schrägmuskel und zurückzuziehen medial. Dann befreien den Äußerer Schrägmuskel von der darunter liegenden Brustkorb in der gleichen Weise, und zurückzuziehen seitlich und bietet einen ungehinderten Blick von der zweiten, dritten und vierten Rippen.
- Führen Sie die Thorakotomie zwischen der dritten und vierten Rippen. Heben Sie die vierte Rippe und verwenden Sie ein Ausbrenner, um den Brustraum zwischen der dritten und vierten Rippen zu öffnen. Zeigen Wundhaken, um den Hohlraum weiter zu öffnen und setzen die Herzen.
- Verwenden einer Pinzette, um die dünne Perikard des Herzens brechen.
- Ligieren der linken Koronararterie mit einem 8-0-Monofilament-Nylonnaht. Platzieren der Naht etwa 4 mm von der Spitze des Herzens, befindet sich direkt unterhalb der unteren Spitze des linken Atriums. Bestimmen richtige Nahtplatzierung durch einen Blanchieren des ventrikulären Myokards und eine Zunahme der Grße des linken Vorhofs nach Suture wurde gebunden.
5. Patch-Placement und Kleber
- Halten Patches bei 37 ° C und 5% CO 2 Bedingungen bis zur Verwendung.
- Heben Sie den Patch mit einem flachen ended Spachtel und legen Sie sie vorsichtig auf der Oberfläche des Herzens, an der Stelle des Infarkts.
Hinweis: Um ein Abrutschen der linken Herzkammer zu verhindern, kann der Patch an Ort und Stelle durch leichtes ständig in Kontakt entweder mit dem Spachtel oder die Spitze einer Pinzette gehalten werden. - Vorbereitung des Klebers durch Mischen eines 4: 1-Verhältnis von Fibrinogen zu Thrombin. Mische die Lösung durch wiederholtes Pipettieren, bis es zu verdicken beginnt, in der Regel innerhalb von 1 min nach dem Beginn der Zubereitung.
- Sobald die Viskosität der Lösung das gewünschte Niveau erreicht, etwa 10 ml schnell auf die Patch-Oberfläche zu übertragen. Anmerkung: Die Gerinnungszeit des Fibrinklebers schnell ist, die eine kleine Zeitfenster für eine effiziente Übertragung des Klebers.
6. Naht
- Führen Sie alle Schließnähte mit einem 6-0 Monofilament-Nylonnaht.
- Schließen Sie die Rippenschicht drei bis vier Einzelknopfnähten.
- Vor der vollständigen Schließung der Zwischenrippenschicht, legen Sie eine PE-10-Kanüle in den Einschnitt, den Brustraum zu evakuieren nach dem Schließen und Wiederherstellung abgeschlossen ist richtige intrapleural Druck.
- Schließen Sie die Brustmuskeln drei bis vier Einzelknopfnähten.
- Verschließen Sie die Hautschicht mit einer fortlaufenden Naht.
- Nach Vollsperrung, legen Sie eine 1,0 ml Spritze mit dem Ende der Kanüle und es verwenden, um den Brustkorb zu evakuieren.
- Tragen Sie eine Gewebekleber auf der Einschnittstelle, um die Naht Ort zu verstärken.
7. Post-operative Behandlung
- Geben Mäuse eine Injektion von Buprenorphin (0,05 bis 1,0 mg / kg) und Carprofen (2,2 mg / kg) subkutan unmittelbar nach dem Koronarligatur und mindestens 20 Minuten vor der Wiederbelebung. Beide Medikamente verabreichen 6-8 Stunden nach der Operation, Und geben Sie dann zweimal täglich für bis zu drei Tage, um Schmerzen und Leiden zu kontrollieren.
- Die Tiere bis zum bewussten und jede Stunde für den ersten 4 Stunden nach der Operation zu überwachen. Führen Sie eine zweite Überprüfung der Nacht nach der Operation (2-4 Stunden später), um eine zweite Dosis Analgetikum zu verabreichen.
- Überwachen Sie die Tiere täglich nach dem zweiten Tag nach dem Eingriff, bis Tieren stabil erscheinen.
8. Analyse der Herzfunktion und Histologie
- Führen Echokardiographen auf den Mäusen 4 Wochen nach dem Eingriff, um das Ausmaß der Schäden nach dem MI bestimmen.
- Betäuben Mäusen mit 4-5% Isofluran in einer Narkose Kammer für die Induktion der Inhalationsnarkose, und dann 2% Isofluran via Gesichtsmaske zur Aufrechterhaltung der Narkose.
- Deaktivieren Sie den Imaging-Bereich mit einer Enthaarungscreme und verwenden Sie ein kleines Tier Ultraschall, um eine 2D-M-Mode-Echokardiographie Scan des schlagenden Herzens zu erhalten, und notieren Sie die Funktionsparameter assomit ihm abgeschrieben.
- Euthanize die Mäuse in einer Kohlendioxidkammer, dann sammeln die Herzen von den Tieren und in eine 10% Formalin-Lösung für 24 Stunden. Nach 24 Stunden übertragen, die Herzen zu 70% Ethanol und halten bei 4 ° C bis zur Gewebeverarbeitung.
- Verarbeiten Sie die Herzen und betten sie in Paraffinblöcken.
- 5 mm geschnitten Schnitte durch den ventrikulären Bereich des Herzens, beginnend an der Spitze beginnt und am Atrium.
- Stain geschnittene Scheiben sowohl mit Massons Trichrom und Hämatoxylin und Eosin-Färbung unter Verwendung von Standardprotokollen.
Ergebnisse
Während des chirurgischen Eingriffs, kann die Ligation der linken Koronararterie durch eine deutliche Blanc stromab der verschlossenen Arterie identifiziert werden. Als Test vor den Bund fürs Leben, kann die Naht kurz angezogen, um zu überprüfen, ob es an der entsprechenden Stelle ist werden. Zusätzlich kann, da Okklusion der Arterie fast sofortige Abnahme der Fähigkeit des linken Atriums, um richtig zu schlagen, das linke Atrium wird in Reaktion auf einen Rückfluss des Blutes in dem System zu vergrößern.
M-Mode-Echokardiographie Messungen bereits 2 Tage nach dem Infarkt zeigen eine Einstellung der linken Wand Bewegung, welches die Muskelrekonstruktion. Qualitative Berechnungen aus den Daten gemacht zeigen eine Abnahme der Ejektionsfraktion und Schlagvolumen in den Infarktherzen. Bei Beendigung des Versuchs, als die Herzen werden für die histologische Zwecke gesammelt hat, kann eine klare Dilatation des linken Ventrikels zu sehen ist, zusammen mit einer Verdünnung der linksventrikulärenWand, und die Abscheidung von Kollagen, Narbengewebeablagerung an Ort und Stelle funktionieren Kardiomyozyten (Figur 1) bezeichnet.
Auch angeschaut Das histologische Analyse ist dank der Anwesenheit des Hydrogels zu konstruieren, um die Verwaltung des Fibrin-Gel (Abbildung 2). Für unsere Zwecke ist das Klebstoffsystem viskos genug, um präzise Platzierung Kontrolle ermöglichen und anschließende Abfluss minimieren in umliegenden Organe, aber formbar genug, um nicht mit der Herzfunktion stören. Vorversuche wurden durchgeführt, um die Viskosität, Gelierzeit und Steifheit der verschiedenen Fibrinogen / Thrombin-Verhältnis zu berechnen, um die richtige Kombination, die unsere passt zu bestimmen. In vivo-Analyse wurde durchgeführt, um die Fähigkeit der Fibrinkleber patch- aufrechtzuerhalten testen to-Gewebeadhäsion ermöglichen trotzdem eine vollständige Herzfunktion (Daten nicht gezeigt). Es sei darauf hingewiesen, dass der Fibrinkleber nicht schadet dem Myokard, wie die l nachgewiesen werdenack von Gewebeumbau oder ventrikuläre Ausdünnung an der Stelle (Abbildung 2). Die Kardiomyozyten bleiben trotz der Zugabe von sowohl einer Herzklappe und der dazugehörigen Kleber intakt. Zusätzlich bestätigt die Lebensfähigkeit Tests, dass die Verabreichung von Fibrinkleber auf die äußere Oberfläche einer Zelle mit eingekapseltem Hydrogelpflaster hat (Figur 3) nicht berührt Zellüberleben im Pflaster.
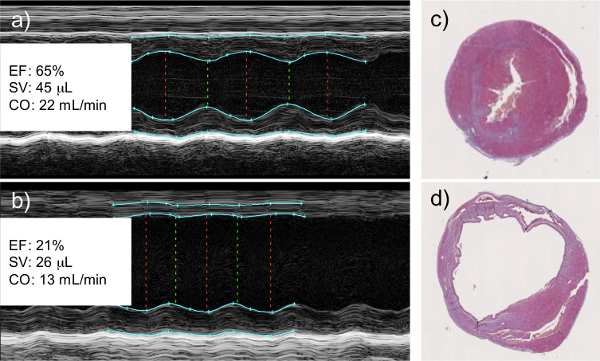
Abb. 1: Left Coronary Artery Ligation führt zu einer Abnahme der Herzfunktion, wie durch Echokardiographie gemessen M-Mode-Echokardiographie von gesunden (a) und Infarkt (b) Herzen. Infarktherzen zeigen einen klaren Mangel an Wandbewegung, wo lebensfähige Gewebe durch Narbengewebe ersetzt. Dies korreliert mit einer meßbaren Abnahme der linksventrikulären Auswurffraktion (EF), das HerzschlagVolumen (SV) und das Herzminutenvolumen (CO). Die histologische Analyse von gesunden (C) und mit Infarkt (d) Herzen zeigt Dilatation des linken Ventrikels und Verdünnung der linksventrikulären Wand des infarzierten Myokards beiden Zeichen der Gewebe-Remodellierung und Narbengewebeablagerung. Die histologische Bilder sind Querschnittsscheiben der Erfassung der linken Seite (größere Kammer) und rechts (kleinere Kammer) Ventrikel.
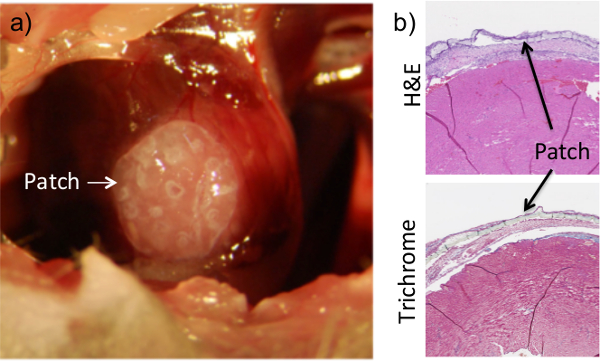
Fig. 2: Verwendung des Fibrin Flue sichert Flecken Adhesion zum Herzen wird das Pflaster auf der Oberfläche des Herzens angeordnet, während die Brusthöhle während des Verfahrens ausgesetzt ist, (a). Einmal angeordnet ist, wird eine auf Fibrin basierende Klebstoff auf der Oberseite des Herz gegeben und trocknen gelassen. Der Patch kann eindeutig auf histologischen Schnitten von Herzgewebe, die nach 1 Woche nach dem Eingriff (b) gesammelt wurden, zu sehen.Dissoziation der Patch von der Herzoberfläche in histologischen Bilder ist ein Artefakt der Sammlung und Schneideprozess. Ergebnisse sind konsistent mit bis zu 8 Wochen nach der Haftung.

Abbildung 3: Fibrin-basierte Kleber nicht schadet Encapsulated Gewebe Lebensfähigkeit der Zellen wurde mittels MTT-Analyse von 1 Woche nach der Verabreichung eines Fibrin-basierte Kleber Verwendung im Detail in früheren Publikationen 8 beschriebenen Protokolle gemessen.. Die Lebensfähigkeit von Zellen innerhalb des Pflasters wurde nicht durch die Zugabe des Klebers auf die Oberfläche des Konstrukts betroffen.
Diskussion
Mit diesem Ansatz konnte murinen MI-Modell haben wir ein System, das die Schädigung von Nicht-Myokard Bereichen, die mit anderen murinen MI Techniken verbunden werden minimiert entwickelt. Diese Bereiche umfassen Schädigung durch eine Tracheostomie verursacht, das Schneiden der Muskelschicht, und das Brechen der Rippen, um die Brusthöhle freizulegen. Wir glauben, dass diese Änderungen zur Verbesserung der allgemeinen Operationsergebnis durch die Sorgfalt, so viel von der Hauptstrukturen, einschließlich der Rippen und Muskelschichten intakt während des chirurgischen Eingriffs zu halten.
Es sollte beachtet werden, dass es einige Einschränkungen dieser Technik mit dem größten wobei seine Zeitaufwendigkeit werden, was nur 8-10 vollständige chirurgische Verfahren an einem Tag. Um dies zu überwinden, kann ein zweiter Ventilator eingesetzt werden, so dass für das Verfahren auf zwei Tiere gleichzeitig durchgeführt werden. Zusätzlich großen Gefäße, wie beispielsweise die Interkostalgefäße undInnere Brustwandarterie, sollte bei der Durchführung der Thorakotomie vermieden werden. Wenn in der Nähe eines dieser Schiffe, sollte ein Ausbrenner verwendet werden Ausbluten aufgrund einer geplatzten Arterie zu verhindern.
Fibrinkleber wird sowohl in der Labor- und klinischen dank seiner Fähigkeit, schnell in die Gerinnselbildung zu unterstützen, ebenso wie das Potential zu liefern und Wirts MSCs 14-17,19 bekannt. Für unsere Zwecke gedient Fibrinkleber als biokompatibles Ansatz Anhaften eines Wasserbasis Hydrogel zu konstruieren, um die Oberfläche des Herzens. Die Verwendung einer auf Fibrin basierende Kleber bei der Beibehaltung der Hydrogel-Konstrukt an der beschädigten Stelle für bis zu 8 Wochen, wobei die Möglichkeit für Gewebekontakt einer längeren Zeitspanne erfolgreich erwiesen. Die Verwendung dieses Haftsystem erlaubt Steuer zur Plazierung der empfindlichen Konstrukt ohne die Notwendigkeit für zusätzliche Nähte, die den Herzmuskel und das Konstrukt selbst schaden. Wir haben festgestellt, dass der Klebstoff selbst ist nicht-toxisch für die verkapselten Zellen and nicht negativ auf das darunter liegende Gewebe. Das Hydrogel und Fibrin basierende Klebersystem kann auf eine Vielzahl anderer Zwecke des Tissue Engineering, die Zelle oder therapeutischen Kontakt Wunsch nach einem längeren Zeitraum angewendet werden. Ferner mit der Verwendung des SLA-Herstellungsverfahren, Designs und Strukturen können im Pflaster eingearbeitet werden, um ein komplexes System zur Zellabgabe 18 zu schaffen.
Ein Rückschlag für die Nutzung der auf Fibrin basierende Kleber ist die Tatsache, dass mehr als ein Forscher muss im Operationssaal während der Patch-Platzierung und Kleber zusätzlich vorhanden sein. Es ist die Aufgabe der ersten Forscher, um sicherzustellen, dass der Patch bleibt bestehen und nicht in der Brusthöhle verloren gehen, während die zweite Forscher mischt die Lösung und wendet sie auf dem Pflaster, nachdem geeignete Viskosität erreicht ist. Um den Zeitpunkt der Abgabe des Klebers zu optimieren, wird vorgeschlagen, dass der zweite Forscher auch Tests und Zeiten die Gelierung des Klebstoffs vor dem Patch-Platzierung,Da korrekte Gelierung des Klebers kritisch für Patch Haftung.
Es gibt eine Anzahl von wichtigen Schritte und fehleranfällige Bereiche innerhalb des Protokolls, wobei die erste ist die Induktion der Myokardinfarkt. Es ist zwingend, für Schilder, wie Blanchieren der linksventrikulären Wand und der Vergrößerung des linken Atriums zu überprüfen, um Okklusion der linken Koronararterie zu gewährleisten. Dies kann durch einfaches Anziehen der Kreuzung und des Nahtmateriales Saiten vor der Zugabe der Masche erfolgen. Wenn bestimmt wird, dass die linke Koronararterie wird nicht durch die Naht eingeschlossen sind, kann die Schnur herausgenommen und wieder aufgebracht werden. Eine zweite kritische Maßnahme weiterhin den Intubationsschlauch während des gesamten Verfahrens zu überwachen, um sicherzustellen, dass sie innerhalb der Trachea verbleibt und nicht heraus Mitte Operation gezogen bekommen. Schließlich in der gesamten Operation sollten alle Versuche unternommen werden, um den Kontakt mit den Lungen zu vermeiden, da jeder Kontakt das Potential hat, zu einem Lungenkollaps führen.Wenn während der Operation, Lunge Kollabieren auftritt, einfach blockieren die Ausflussrohr des Intubator für bis zu 3 Sekunden in einem Versuch, wieder aufgehen unruhigen Regionen der Lunge.
Offenlegungen
The authors declare that they have no competing financial interests.
Danksagungen
Diese Arbeit wurde vom US-Armee Grant (W81XWH-08-1-0701) und ein Stipendium Carle Foundation Hospital finanziert.
Materialien
| Name | Company | Catalog Number | Comments |
| Harvard Model 687 Mouse Ventilator | Harvard Apparatus | 55-0001 | |
| Inintech Biosciences LLC Dry Glass Bead Sterilizer | Fisher Scientific | NC9531961 | |
| Leica MZ6 surgical microscope | Leica | ||
| Cautery Kit | Gemini | GEM 5917 | |
| Delicate Forceps - 0.4 mm Tips Angled | Fine Science Tools | 11063-07 | |
| Agricola Retractor - 3.5 cm Spread | Fine Science Tools | 17005-04 | |
| Spring Scissors - 2.5 mm Blades Straight | Fine Science Tools | 15000-08 | |
| Castroviejo Needle Holder - w/Lock Tungsten Carbide 14 cm | Fine Science Tools | 12565-14 | |
| Iris Scissors - Delicate Straight 10.5 cm | Fine Science Tools | 14060-10 | |
| 8-0 monofilament suture | Ethicon | 8730P | |
| 6-0 Silk suture | Ethicon | 639G | |
| Thrombin | Sigma | T7009 | |
| Fibrinogen | Sigma | F3879 | |
| Vetbond Tissue Adhesive | 3M | 1469SB |
Referenzen
- Kolk, M. V., et al. LAD-ligation: a murine model of myocardial infarction. Journal of visualized experiments : JoVE. , (2009).
- Li, Y., Yao, Y., Sheng, Z., Yang, Y., Ma, G. Dual-modal tracking of transplanted mesenchymal stem cells after myocardial infarction. International journal of nanomedicine. 6, 815-823 (2011).
- Nagaya, N., et al. Intravenous administration of mesenchymal stem cells improves cardiac function in rats with acute myocardial infarction through angiogenesis and myogenesis. American journal of physiology. Heart and circulatory physiology. 287, H2670-H2676 (2004).
- Wang, J. S., Shum-Tim, D., Chedrawy, E., Chiu, R. C. The coronary delivery of marrow stromal cells for myocardial regeneration: pathophysiologic and therapeutic implications. The Journal of thoracic and cardiovascular surgery. 122, 699-705 (2001).
- Cashman, T. J., Gouon-Evans, V., Costa, K. D. Mesenchymal stem cells for cardiac therapy: practical challenges and potential mechanisms. Stem cell reviews. 9, 254-265 (2013).
- Sutton, M. G., Sharpe, N. Left ventricular remodeling after myocardial infarction: pathophysiology and therapy. Circulation. 101, 2981-2988 (2000).
- Smolina, K., Wright, F. L., Rayner, M., Goldacre, M. J. Long-term survival and recurrence after acute myocardial infarction in England, 2004 to 2010. Circulation. Cardiovascular quality and outcomes. 5, 532-540 (2012).
- Chan, V., Zorlutuna, P., Jeong, J. H., Kong, H., Bashir, R. Three-dimensional photopatterning of hydrogels using stereolithography for long-term cell encapsulation. Lab on a chip. 10, 2062-2070 (2010).
- Kai, D., et al. Stem cell-loaded nanofibrous patch promotes the regeneration of infarcted myocardium with functional improvement in rat model. Acta biomaterialia. 10, 2727-2738 (2014).
- Serpooshan, V., et al. The effect of bioengineered acellular collagen patch on cardiac remodeling and ventricular function post myocardial infarction. Biomaterials. 34, 9048-9055 (2013).
- Cavallo, L. M., Solari, D., Somma, T., Savic, D., Cappabianca, P. The Awake Endoscope-Guided Sealant Technique with Fibrin Glue in the Treatment of Postoperative Cerebrospinal Fluid Leak After Extended Transsphenoidal Surgery: Technical Note. World neurosurgery. , (2013).
- Chung, H. W., Mehta, J. S. Fibrin glue for Gundersen flap surgery. Clinical Ophthalmology. 7, 479-484 (2013).
- Dunn, C. J., Goa, K. L. Fibrin sealant: a review of its use in surgery and endoscopy. Drugs. 58, 863-886 (1999).
- Chi, N. H., et al. Cardiac repair achieved by bone marrow mesenchymal stem cells/silk fibroin/hyaluronic acid patches in a rat of myocardial infarction model. Biomaterials. 33, 5541-5551 (2012).
- Erb, M. A., Claus, T., Hartrumpf, M., Bachmann, S., Albes, J. M. The use of Tachosil surgical patch or fibrin glue in coronary artery surgery does not affect quality of anastomosis or provoke postoperative adhesions in pigs. European journal of cardio-thoracic surgery : official journal of the European Association for Cardio-thoracic Surgery. 36, 703-707 (2009).
- Okada, K., et al. Surgical treatment for rupture of left ventricular free wall after acute myocardial infarction. Interactive cardiovascular and thoracic surgery. 4, 203-206 (2005).
- Simpson, D., Liu, H., Fan, T. H., Nerem, R., Dudley, S. C. A tissue engineering approach to progenitor cell delivery results in significant cell engraftment and improved myocardial remodeling. Stem Cells. 25, 2350-2357 (2007).
- Jeong, J. H., et al. Living' microvascular stamp for patterning of functional neovessels; orchestrated control of matrix property and geometry. Advanced Materials. 24, 58-63 (2012).
- Wu, X., Ren, J., Li, J. Fibrin glue as the cell-delivery vehicle for mesenchymal stromal cells in regenerative medicine. Cytotherapy. 14, 555-562 (2012).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten