Method Article
ヒドロゲルは、構築し、マウス心筋梗塞モデルにおける治療薬を送達するためのフィブリンベースの接着剤のアプローチ。
要約
This protocol aims to alleviate the limitation of poor cell engraftment for stem cell treatment of myocardial infarctions through the use of a hydrogel system and a fibrin-based glue. With this approach, cell-to-tissue contact post-infarction can be maintained, increasing the therapeutic potential of beneficial agents at the site of injury.
要約
The murine MI model is widely recognized in the field of cardiovascular disease, and has consistently been used as a first step to test the efficacy of treatments in vivo1. The traditional, established protocol has been further fine-tuned to minimize the damage to the animal. Notably, the pectoral muscle layers are teased away rather than simply cut, and the thoracotomy is approached intercostally as opposed to breaking the ribs in a sternotomy, preserving the integrity of the ribcage. With these changes, the overall stress on the animal is decreased.
Stem cell therapies aimed to alleviate the damage caused by MIs have shown promise over the years for their pro-angiogenic and anti-apoptotic benefits. Current approaches of delivering cells to the heart surface typically involve the injection of the cells either near the damaged site, within a coronary artery, or into the peripheral blood stream2-4. While the cells have proven to home to the damaged myocardium, functionality is limited by their poor engraftment at the site of injury, resulting in diffusion into the blood stream5. This manuscript highlights a procedure that overcomes this obstacle with the use of a cell-encapsulated hydrogel patch. The patch is fabricated prior to the surgical procedure and is placed on the injured myocardium immediately following the occlusion of the left coronary artery. To adhere the patch in place, biocompatible external fibrin glue is placed directly on top of the patch, allowing for it to dry to both the patch and the heart surface. This approach provides a novel adhesion method for the application of a delicate cell-encapsulating therapeutic construct.
概要
心筋梗塞(MI)は、主要な冠動脈の閉塞によって引き起こされる心臓の領域への血液の中断として定義されます。 MIに起因する損傷が原因または、より具体的には、左心室は、適切に打つ心臓の能力を低下させる非機能的瘢痕組織に生存可能心臓組織のリモデリングです。これは、一回拍出量としても知られているすべてのハートビート、および駆出率6と呼ばれる各心拍で心臓から送り出される血液の割合で身体に送達することができる血液の量の減少をもたらします。これらは、他の減少の機能とともに、十分な機能を維持するために、心臓の残りの部分に負担を増加させます。多くの場合、これは、株は、それが第二の心臓発作、個人7の約10%に見られる現象を引き起こすほど重症になることができます増加しました。
医療行為は、治療のために進化してきたがMIの直後には、何の技術は遅く、停止、または組織リモデリングの負の副作用を逆転するように開発されていません。幹細胞療法は、それらの有望な潜在的にもかかわらず、しかし、そのような治療のための可能な道として出現した幹細胞は、臨床設定において成功することが証明されていません。その欠点の一つの理論は、有益な細胞が良好な結果5を生成するのに十分な長さ梗塞部位に残って確保することができないことです。これは単に、梗塞の部位に注射された細胞のない24%以上が生存していないと損傷部位1日後に配達2にとどまったことが示されています。細胞保持のこの問題に対処するための可能な見通しは、細胞または損傷部位に送達することができる治療薬のいずれかをカプセル化する生体適合性ヒドロゲル系を開発することです。このプロトコルにおける選択のヒドロゲルは、ポリ(エチレングリコール)は、細胞のカプセル化では、直前の使用広報によるメタクリレートでありますoceduresしかし、カプセル化することができる任意のヒドロゲルが8を使用してもよいです。直接損傷部位へのパッチの送達は、細胞が、下にある心筋に有益な因子を提供することができる時間の長さを増加させ、長期間にわたる細胞 - 組織接触を確実にします。
パッチアプローチのボトルネックは、心臓の表面にパッチを接着するのが困難です。多くのグループが、最も普及しているが、心臓の表面9,10に構造物を結びつけるための簡単な縫合糸である、種々の技術によってこれを克服しています。これは、構築物はより硬い材料で作られたケースの数は成功しますが、高い水濃度とパッチ構築物の繊細な性質のために、ヒドロゲル系にしようとしたときに失敗しました。これを克服するために、我々は、血栓形成の化学的性質を模倣するフィブリン糊外部接着剤系を利用しています。フィブリン糊は、INC、多数の医療手術で使用されています創傷シーラント11〜13として、製品の生体適合性を強調し、硬膜涙、気管支瘻、及び角膜移植をluding。さらに、フィブリンは、左心室破裂および冠動脈バイパス手術の外科的治療を含む心臓の目的の種々のために使用されている、しかし、心臓パッチの接着糊としてのその使用は、一般的に14〜17を使用していません。心臓の相互作用にパッチを確実にするために実行可能な接着システムを提供すること、外部心臓パッチの外側に直接配置することができる生体適合性の接着剤でトロンビンおよびフィブリノーゲン結果の単純な製剤。
プロトコル
手順はIACUCプロトコル番号13302との完全な互換性であり、動物資源の部門によって承認されています。
1.機器の準備
- 無菌性を確保するために、外科手術の前に使用されるすべての非使い捨て器具をオートクレーブ。
- 使用の間、ガラスビーズ滅菌器とのセッションで複数回使用される器具を滅菌します。
2.ハイドロゲルの調製
- 解凍し、ヒドロゲル構築物の作成に少なくとも24時間前にプレート幹細胞。
- 以前の刊行物8,18に完全に詳細に記載されているステレオリソグラフィー装置を用いて、外科的処置(または類似の器具)を一日前にパッチを準備します。
- ハイドロゲルを作成するには、第1の所望のパッチのコンピュータ支援設計(CAD)モデルを生成し、立体造形形式(STL)に設計をエクスポートします。
- dissolvinによってプレゲル溶液を作成します滅菌1×PBS中のGポリ(エチレングリコール)ジメタクリレート(PEGDMA)は20%のw / v溶液を得ました。同時に、光開始剤、1- [4-(2-ヒドロキシエトキシ) - フェニル] -2-ヒドロキシ-2-メチル-1-プロパン-1-オンDMSO中に溶解させます。 0.5%w / vの最終でPEGDMA溶液に光開始剤を追加します。直接架橋の前に、細胞の所望の密度の100ミリリットルを追加します。注:2.0×10 5 -2.0×10 6細胞/ mlの間の細胞密度が推奨されます。
- SLAプラットフォームの中央に皿にプレ - ゲル溶液をピペットで、以前にアップロードしたSTLフォーマットされたデザインで、SLAのソフトウェアを実行します。
- 細胞を調節するために可能にするために装置からパッチを取り外し、ダルベッコ改変イーグル培地中でヒドロゲルO / Nインキュベート(DMEM)、5%ウシ胎児血清(FBS)を補充した、100 U / mlペニシリン、および100mg / mlストレプトマイシンパッチ内の環境に。
3.動物の準備とオーラルintubatiオン
- ケージの仲間とのグルーミング習慣との相互作用から決定されるような動物は、健康であることを確認する手順の前に、各マウスを評価します。注:女性8-10週齢のC57BL / 6Jマウスは、この手順のために使用された、しかし、任意のマウスの年齢やタイプを使用することができます。
- 麻酔室に動物を置き、1リットル/分O 2をサポートして5%のイソフルランに公開します。つま先ピンチ反射によって麻酔のレベルを監視します。
- 動物を適切に麻酔された後、計量し、挿管台の上に置きます。
- 動物の胸腔に向けて光源を直接および喉頭面を撤回し、声帯を公開するために鉗子を使用しています。慎重に声帯の間の20のG血管カテーテルをガイドし、スムーズに気管に挿入します。カテーテルは小動物人工呼吸器に接続されると、胸腔の機械的な動きによって適切な挿入を検出します。
- 目に換気設定を調整メーカーのガイドラインに基づいて、動物の電子体重。
- 挿管後、低体温症を防ぐために加熱パッド上に仰臥位で動物を配置します。加熱パッドは40℃を超えないことを確認してください。必要に応じて、火傷の可能性を最小限にするために、動物や加熱パッドとの間の障壁を配置します。
- 脱毛クリームを使用することにより、手術部位から髪を削除します。適切な滅菌を確実にするためにベタジンと75%エタノールの3交互スクラブしてサイトを滅菌します。ただ、手術部位を露出させるためにドレープを置き、手順の間に乾燥を防ぐために、目に獣医軟膏を配置します。
4.手術手順
- 開胸したがって、胸骨の長さを実行する胸骨の左側に皮膚切開約1cmを行い、動物の左側に実行されます。
- 二段階で、基礎となる胸郭から筋層を分離するために鉗子を使用してください。 delineを観察動物の大胸筋を表すレーティングライン。 、少しこの筋肉を持ち上げ、基礎となる外腹斜筋から分離し、内側に後退。そして、同様に、基礎となる胸郭から外腹斜筋を解放し、第2、第3、第4肋骨の暗くされていないビューを提供する、横方向に後退させます。
- 第三及び第四肋骨の間開胸術を行います。静か第4肋骨を持ち上げ第3および第4肋骨の間胸腔を開くために焼灼器を使用しています。さらにキャビティを開き、心臓を露出させるためにリトラクターを配置します。
- 心の薄い心膜を破裂させるために鉗子を使用してください。
- 8-0モノフィラメントナイロン縫合糸で左冠動脈を結紮。直接左心房の下部先端の下、約4mm心尖から縫合糸を配置します。心室筋のブランチングとスツ語の後に左心房の大きさの増加により、適切な縫合糸の配置を決定します再結ばれています。
5.パッチの配置とグルー
- 使用するまで37℃でパッチを維持し、5%CO 2の条件。
- ゆっくりフラットエンドへらを使用してパッチを持ち上げ、ゆっくりと梗塞部位で、心臓の表面の上に置きます。
注:左心室の脱落防止のために、パッチが軽くへら又はピンセットの先端のいずれかを使用して接触を維持することによって所定の位置に保持することができます。 - トロンビンへのフィブリノゲンの1の比率:4を混合して接着剤を準備します。それは準備の開始後、通常1分以内に、厚く始めるまで繰り返しピペッティングにより溶液を混合。
- 溶液粘度が所望のレベルに達すると、すぐにパッチ表面に約10 mlで移します。注:フィブリン糊の凝固時間は迅速であり、接着剤の効率的な転送のための機会の小窓を提供します。
6.縫合
- 6-0モノフィラメントナイロン縫合糸を使用して、すべての閉鎖縫合糸を実行します。
- 三から四個々の結節縫合でリブ層を閉じます。
- 肋間層の完全閉鎖する前に、閉鎖が完了した後、胸腔を排気し、適切な胸腔内圧を再確立するために切開部にPE-10カニューレを挿入します。
- 三から四個々の結節縫合で胸筋を閉じます。
- 連続縫合で皮膚層を封止します。
- 完全閉鎖後、カニューレの端に1.0ミリリットルの注射器を接続して、胸腔を排出するためにそれを使用。
- 縫合部位を補強するために切開部位に組織接着剤を適用します。
7.手術後の処置
- マウスにブプレノルフィン(0.05〜1.0ミリグラム/ kg)および皮下直前復活に冠動脈結紮および少なくとも20分以下のカルプロフェン(2.2ミリグラム/ kg)を注射を与えます。両薬剤を手術後6-8時間の管理、その後痛みや苦痛を制御するために最大3日間、1日2回与えます。
- 継続的に手術後の最初の4時間を意識し、すべての時間になるまで動物を監視します。鎮痛剤の第二の用量を投与するために、第2の検診を手術(2-4時間後)の夜を実行します。
- 動物が安定した表示されるまで、手順に従って、二日後に毎日動物を監視します。
心機能と組織学の8解析
- マウスのechocardiographs MI後の損傷の程度を決定するための手順を次の4週間を実行します。
- 吸入麻酔の誘導のための麻酔チャンバー内の4〜5%イソフルラン、およびメンテナンス麻酔用フェイスマスクを介した後、2%イソフルランでマウスを麻酔。
- 脱毛クリームで撮像領域をクリアし、拍動する心臓の2D Mモード心エコー検査スキャンを得るために、小動物の超音波を使用して、機能パラメータのASSOを記録それにciated。
- その後、24時間、10%ホルマリン溶液中で動物と場所からの心臓を集め、二酸化炭素チャンバーにマウスを安楽死させます。 24時間後、70%エタノールに心を転送し、組織処理まで4℃で維持。
- 心を処理し、パラフィンブロックでそれらを埋め込みます。
- 頂点で始まり、心房で終わる、心臓の心室領域を介して、5mmのセクションをカット。
- 染色は、標準的なプロトコルを使用して、マッソン三色、ヘマトキシリンおよびエオシン染色の両方でスライスを切断しました。
結果
外科的処置の間に、左冠動脈の結紮は、閉塞した動脈の下流のブランチングマークすることによって同定することができます。結び目を作る前の試験のように、縫合糸は、それが適切な場所にあるかどうかを確認するために簡単に締め付けることができます。さらに、適切にビートに左心房の能力のほぼ瞬時減少動脈結果の閉塞ので、左心房は、システム内の血液の逆流に応じて拡大します。
Mモード心エコー検査の測定は、梗塞後は、筋肉の再構築を示す、左の壁運動の停止を示し、早くも2日としました。データから作られた定性的な計算は、梗塞心での駆出率とストローク量の減少を示します。心臓を組織学的目的のために収集されたときに実験の終了時に、左心室の明確な拡張は、左心室の薄型化に伴って、見ることができます壁、および機能の心筋細胞( 図1)の代わりに、瘢痕組織の沈着を示し、コラーゲンの沈着。
また、( 図2)は 、組織学的分析にヒドロゲルの存在は、フィブリンゲルの投与のおかげで構成で見られます。我々の目的のために、接着剤系は、正確な配置の制御を可能にし、周囲の器官に後続の流出を最小限にするのに十分に粘性でなければならないが、十分な展性心臓機能に干渉しません。予備試験は、我々のニーズに合った適切な組み合わせを決定するために、粘度、ゲル化時間、および様々なフィブリノゲン/トロンビン比の剛性を計算するために行われた。 インビボ分析はpatch-を維持するためにフィブリン糊の能力を試験するために行きました。の組織接着まだ完全心機能を可能にしながら(データは示さず)。これは、Lによって証明されるように、フィブリン糊は、心筋を傷つけるしなかったことに留意すべきです部位における組織リモデリング又は心室間伐のACK( 図2)。心筋細胞は、心臓パッチとそれに付随する接着剤の両方の添加にもかかわらず、無傷のままです。さらに、生存能力試験は、細胞カプセル化ハイドロゲルパッチの外部表面にフィブリン接着剤の投与は、( 図3)は 、パッチ内の細胞の生存に影響を及ぼさなかったことをことを確認しました。
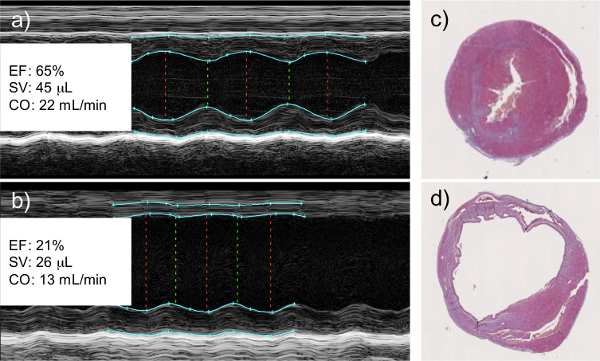
図1:心エコー検査により測定される心機能の低下を左冠動脈結紮の結果(a)は、健康で、(b)は、梗塞心のMモード心エコー検査。梗塞心は、生存組織が瘢痕組織に置き換えられた壁運動の明確な欠如を示します。これは、左室駆出率(EF)で測定可能な減少と相関し、心臓発作ボリューム(SV)、および心拍出量(CO)。健康(c)および梗塞(d)の心臓の組織学的分析は、左心室および梗塞心筋の左心室壁の菲薄化、組織リモデリングおよび瘢痕組織沈着の両方の徴候の拡張を示しています。組織学的画像は、左(より大きな室)と右(小さい室)心室を捕獲する断面のスライスです。
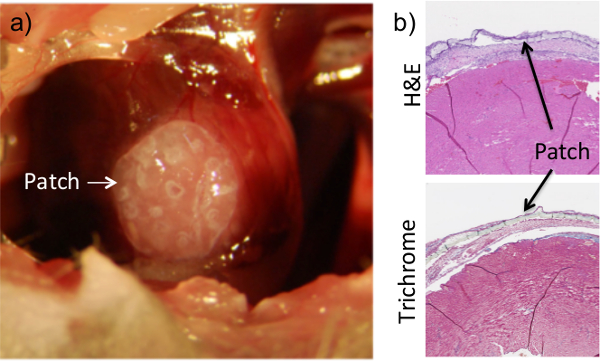
図2。胸腔を手順(a)の間に露出している心臓にフィブリン煙を確実に接着パッチの適用は、パッチは、心臓の表面上に配置されます。配置されたら、フィブリンベースの接着剤は、心臓の上部に添加し、乾燥させます。パッチは、明らかに1週間後手順(B)で採取した心臓組織の組織学的切片上で見ることができます。組織学的画像における心臓表面からパッチの解離が収集および切削プロセスの成果物です。結果は、接着までの8週間で一致しています。

図3:フィブリンベースの接着剤は、カプセル化された組織を損傷しない細胞の生存率は、1週間前の刊行物8に詳細に記載されたプロトコルを使用して、フィブリンベースの接着剤の投与後にMTT分析により測定しました。パッチ内の細胞の生存率は、構造物の表面に接着剤を添加することによって影響されませんでした。
ディスカッション
マウスMIモデルにこの方法では、我々は他のマウスのMI技術と関連している非心筋領域へのダメージを最小限に抑えるシステムを開発しました。これらの領域は、気管切開による損傷、筋層の切断、および胸腔を露出させるために、リブの破損を含みます。我々は、これらの変更は、外科手術中など、肋骨や筋肉の層を含む、主要な構造の多くの無傷を保つように注意する全体的な手術結果のおかげで改善することを考えています。
これは、最大の一日の唯一の8-10完全手術手順の結果、その時間がかかる性質であることで、この手法にはいくつかの制限があることに留意すべきです。これを克服するために、第二の人工呼吸器は、手順は、同時に2匹の動物に対して実行されるのを可能にする、使用することができます。加えて、肋間血管のような主要な血管、および開胸術を行う際に、内部胸動脈は、避けるべきです。これらの血管の近くにいる場合は、焼灼が原因破裂動脈にブリードアウトを防止するために使用されるべきです。
フィブリン糊は、すぐに血栓形成を助けるために、その能力、ならびにその潜在的な提供するために、ホストのMSC 14-17,19に実験室および臨床現場の両方のおかげで知られています。私たちの目的のために、フィブリン糊は、水ベースのヒドロゲルは、心臓の表面に付着した構築物の生体適合性のアプローチを務めました。フィブリンベースの接着剤の使用は、時間の長い量の組織との接触の可能性で、最大8週間、損傷部位でのヒドロゲル構造体を維持するのに成功しました。この接着システムの使用は、心筋などの構築物自体に害を与える追加の縫合を必要とせずにデリケートな構造物を配置するための制御を可能にしました。我々は、接着剤自体がカプセル化されたセルAに対して非毒性であることを見出しましたND負下にある組織には影響を与えません。ヒドロゲルおよびフィブリンベースの接着剤システムは、長期間の細胞または治療の接触を望む他の組織工学の様々な目的に適用することができます。また、SLAの製造方法を用いて、デザインおよび構造は細胞送達18より複雑なシステムを作成するために、パッチ内に組み込むことができます。
フィブリンベースの接着剤の使用に対する一つの後退は、複数の研究者が、パッチの配置と接着剤の添加の間に、外科用の部屋に存在しなければならないという事実です。これは、最初の研究者の仕事は第二の研究者は、溶液を混合し、適切な粘度に達した後にパッチに適用しながら、パッチは、所定の位置に残り、胸腔内に失われないことを確認することです。接着剤供給のタイミングを最適化するために、それは、第二の研究者は、パッチを配置する前に接着剤のゲル化をテストし回ことが示唆されています接着剤の適切なゲル化は、パッチの接着のために重要であるため。
最初は、心筋梗塞の誘導であるとのプロトコル内の重要なステップと、エラーが発生しやすい地域の数があります。これは、左冠状動脈の閉塞を確実にするために、例えば、左心室壁のブランチング及び左心房の拡大などの徴候を確認することが不可欠です。これは、単に交差縫合糸列の端部を締め付けて縫目を添加する前に行うことができます。それは左冠状動脈を縫合によって囲まれていないと判定された場合、文字列を取り出すことができる、再適用しました。第二の重要な尺度は、気管内に残り、中間手術引き出されないことを確実にするために、手順全体を通して挿管チューブを監視し続けることです。最後に、手術を通して、すべての試みは、任意の連絡先がつぶれた肺につながる可能性を秘めているように、肺に接触しないようになされるべきです。、手術中に、肺の崩壊が発生し、単純にするための試みで、最大3秒間挿管の流出管をブロックした場合、肺の問題を抱えた領域を再膨張させます。
開示事項
The authors declare that they have no competing financial interests.
謝辞
この作品は、米軍グラント(W81XWH-08-1-0701)とカール財団病院からフェローシップによって資金を供給されました。
資料
| Name | Company | Catalog Number | Comments |
| Harvard Model 687 Mouse Ventilator | Harvard Apparatus | 55-0001 | |
| Inintech Biosciences LLC Dry Glass Bead Sterilizer | Fisher Scientific | NC9531961 | |
| Leica MZ6 surgical microscope | Leica | ||
| Cautery Kit | Gemini | GEM 5917 | |
| Delicate Forceps - 0.4 mm Tips Angled | Fine Science Tools | 11063-07 | |
| Agricola Retractor - 3.5 cm Spread | Fine Science Tools | 17005-04 | |
| Spring Scissors - 2.5 mm Blades Straight | Fine Science Tools | 15000-08 | |
| Castroviejo Needle Holder - w/Lock Tungsten Carbide 14 cm | Fine Science Tools | 12565-14 | |
| Iris Scissors - Delicate Straight 10.5 cm | Fine Science Tools | 14060-10 | |
| 8-0 monofilament suture | Ethicon | 8730P | |
| 6-0 Silk suture | Ethicon | 639G | |
| Thrombin | Sigma | T7009 | |
| Fibrinogen | Sigma | F3879 | |
| Vetbond Tissue Adhesive | 3M | 1469SB |
参考文献
- Kolk, M. V., et al. LAD-ligation: a murine model of myocardial infarction. Journal of visualized experiments : JoVE. , (2009).
- Li, Y., Yao, Y., Sheng, Z., Yang, Y., Ma, G. Dual-modal tracking of transplanted mesenchymal stem cells after myocardial infarction. International journal of nanomedicine. 6, 815-823 (2011).
- Nagaya, N., et al. Intravenous administration of mesenchymal stem cells improves cardiac function in rats with acute myocardial infarction through angiogenesis and myogenesis. American journal of physiology. Heart and circulatory physiology. 287, H2670-H2676 (2004).
- Wang, J. S., Shum-Tim, D., Chedrawy, E., Chiu, R. C. The coronary delivery of marrow stromal cells for myocardial regeneration: pathophysiologic and therapeutic implications. The Journal of thoracic and cardiovascular surgery. 122, 699-705 (2001).
- Cashman, T. J., Gouon-Evans, V., Costa, K. D. Mesenchymal stem cells for cardiac therapy: practical challenges and potential mechanisms. Stem cell reviews. 9, 254-265 (2013).
- Sutton, M. G., Sharpe, N. Left ventricular remodeling after myocardial infarction: pathophysiology and therapy. Circulation. 101, 2981-2988 (2000).
- Smolina, K., Wright, F. L., Rayner, M., Goldacre, M. J. Long-term survival and recurrence after acute myocardial infarction in England, 2004 to 2010. Circulation. Cardiovascular quality and outcomes. 5, 532-540 (2012).
- Chan, V., Zorlutuna, P., Jeong, J. H., Kong, H., Bashir, R. Three-dimensional photopatterning of hydrogels using stereolithography for long-term cell encapsulation. Lab on a chip. 10, 2062-2070 (2010).
- Kai, D., et al. Stem cell-loaded nanofibrous patch promotes the regeneration of infarcted myocardium with functional improvement in rat model. Acta biomaterialia. 10, 2727-2738 (2014).
- Serpooshan, V., et al. The effect of bioengineered acellular collagen patch on cardiac remodeling and ventricular function post myocardial infarction. Biomaterials. 34, 9048-9055 (2013).
- Cavallo, L. M., Solari, D., Somma, T., Savic, D., Cappabianca, P. The Awake Endoscope-Guided Sealant Technique with Fibrin Glue in the Treatment of Postoperative Cerebrospinal Fluid Leak After Extended Transsphenoidal Surgery: Technical Note. World neurosurgery. , (2013).
- Chung, H. W., Mehta, J. S. Fibrin glue for Gundersen flap surgery. Clinical Ophthalmology. 7, 479-484 (2013).
- Dunn, C. J., Goa, K. L. Fibrin sealant: a review of its use in surgery and endoscopy. Drugs. 58, 863-886 (1999).
- Chi, N. H., et al. Cardiac repair achieved by bone marrow mesenchymal stem cells/silk fibroin/hyaluronic acid patches in a rat of myocardial infarction model. Biomaterials. 33, 5541-5551 (2012).
- Erb, M. A., Claus, T., Hartrumpf, M., Bachmann, S., Albes, J. M. The use of Tachosil surgical patch or fibrin glue in coronary artery surgery does not affect quality of anastomosis or provoke postoperative adhesions in pigs. European journal of cardio-thoracic surgery : official journal of the European Association for Cardio-thoracic Surgery. 36, 703-707 (2009).
- Okada, K., et al. Surgical treatment for rupture of left ventricular free wall after acute myocardial infarction. Interactive cardiovascular and thoracic surgery. 4, 203-206 (2005).
- Simpson, D., Liu, H., Fan, T. H., Nerem, R., Dudley, S. C. A tissue engineering approach to progenitor cell delivery results in significant cell engraftment and improved myocardial remodeling. Stem Cells. 25, 2350-2357 (2007).
- Jeong, J. H., et al. Living' microvascular stamp for patterning of functional neovessels; orchestrated control of matrix property and geometry. Advanced Materials. 24, 58-63 (2012).
- Wu, X., Ren, J., Li, J. Fibrin glue as the cell-delivery vehicle for mesenchymal stromal cells in regenerative medicine. Cytotherapy. 14, 555-562 (2012).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved