Method Article
Split-and-piscina Síntese e Caracterização de Peptídeos Terciário Amide Biblioteca
Neste Artigo
Resumo
Peptídeo amidas terciárias (PTA) são uma super família de peptidomiméticos que incluem mas não estão limitados a péptidos, peptóides e peptídeos N-metilados. Aqui nós descrevemos um método sintético que combina split-and-piscina e estratégias sub-monômero para sintetizar um talão biblioteca de um composto de PTAs.
Resumo
Peptidomimetics são excelentes fontes de proteínas ligantes. A natureza oligomérica destes compostos nos permite aceder a grandes bibliotecas sintéticos em fase sólida, utilizando química combinatória. Uma das classes mais bem estudados da peptidomimetics é peptoids. Peptóides são fáceis de sintetizar e têm mostrado ser resistentes à proteólise e célula-permeável. Ao longo da última década, muitos ligantes protéicos úteis foram identificados através de pesquisa de bibliotecas peptoid. No entanto, a maioria dos ligantes identificados a partir de bibliotecas peptoid não exibem uma elevada afinidade, com raras excepções. Isto pode ser devido, em parte, à falta de centros quirais e restrições conformacionais em moléculas peptoid. Recentemente, descrevemos uma nova rota sintética para acessar peptídeo amidas terciárias (PTAs). APCs são uma super família de peptidomiméticos que incluem mas não estão limitados a peptídeos, peptóides e peptídeos N-metilados. Com cadeias laterais em ambos α-carbono e principais átomos de nitrogênio da cadeia,a conformação, estas moléculas são grandemente limitado por impedimento estérico e alílico 1,3 estirpe. (Figura 1) O nosso estudo sugere que estas moléculas PTA são altamente estruturado em solução e pode ser utilizada para identificar ligandos de proteína. Acreditamos que estas moléculas podem ser uma fonte de futuro ligandos proteicos de alta afinidade. Aqui nós descrevemos o método sintético que combina o poder de ambos split-and-piscina e estratégias sub-monômero para sintetizar uma amostra de um talão de um composto (OBOC) biblioteca de PTAs.
Introdução
Os peptidomiméticos são compostos que imitam a estrutura dos péptidos naturais. Eles são concebidos para reter a bioactividade ao superar alguns dos problemas associados com os péptidos naturais, incluindo a permeabilidade celular e a estabilidade contra a proteólise 1-3. Devido à natureza oligomérica destes compostos, grandes bibliotecas sintéticas pode ser facilmente acedido através de vias sintéticas monoméricas ou sub-monoméricos 4-7. Uma das classes mais estudados da peptidomimetics é peptoids. Peptóides são oligómeros de glicinas N-alquilados que podem ser facilmente sintetizados utilizando uma estratégia de sub-monómero de 8, 9. Muitos ligantes de proteínas úteis foram identificados com sucesso desde a triagem de grandes bibliotecas peptoid sintética contra alvos da proteína 1, 10-14. No entanto, os "hits" identificados a partir de bibliotecas peptoid raramente arquivar muito elevada afinidade para proteínas alvo 1,10-14,22. Uma major diferença entre peptóides e péptidos naturais é que a maioria dos peptóides geralmente não têm a capacidade de formar estruturas secundárias devido à falta de centros quirais e restrições conformacionais. Para resolver este problema, várias estratégias foram desenvolvidas ao longo da última década, em grande parte, com foco na modificação de cadeias laterais contidos os principais átomos de nitrogênio da cadeia de 15-22. Recentemente, desenvolvemos uma nova via de síntese para introduzir as cadeias laterais de aminoácidos naturais em uma espinha dorsal peptoid para criar péptidos amidas terciárias 23.
Peptídeo amidas terciárias (PTA) são uma super-família de peptidomiméticos que incluem mas não estão limitados a péptidos (R 2 = H), peptóides (R1 = H) e os péptidos N-metilados (R1 ≠ H, R2 = Me) . (Ver Figura 1) A via sintética emprega aminoácidos de ocorrência natural como fonte de quiralidade e cadeias laterais na45; de carbono, e as aminas primárias disponíveis comercialmente para proporcionar N-substituições. Por conseguinte, um espaço maior do que o químico de péptidos simples, peptóides ou péptidos N-metilados podem ser exploradas. Os espectros de dicroísmo circular demonstraram que as moléculas de PTA são altamente estruturado em solução. Caracterização de um dos complexos de proteína-PTA mostra claramente que os constrangimentos conformacionais de ATP são necessários para a ligação. Recentemente, nós também descobrimos que algumas das moléculas de PTA possuem melhorada a permeabilidade celular do que os seus homólogos peptoid e peptídicas. Acreditamos que essas bibliotecas PTA pode ser uma boa fonte de ligantes de alta afinidade para proteínas alvo. Neste artigo, vamos discutir a síntese de uma amostra de um talão de um composto (OBOC) biblioteca de PTA em detalhes, juntamente com alguns melhores condições para o acoplamento e clivagem destes compostos.
Protocolo
1. Noções básicas de Split-and-piscina Síntese
A fim de gerar de forma eficiente um grande número de compostos em fase sólida, síntese de divisão-e-piscina é frequentemente utilizado como uma estratégia geral. Como mostrado na Figura 4, TentaGel grânulos são primeiro divididos em três porções. Cada porção é reagida com um reagente diferente, gerando o primeiro resíduo em grânulos. Após a primeira reacção, todas as três porções são reunidas em conjunto, misturados, e em seguida, novamente dividida em três porções. Cada parte irá novamente reagir com um reagente diferente, gerando o segundo resíduo em grânulos. Depois de duas etapas de divisão-e-piscina, nove compostos são gerados.
Em síntese sub-monómero, os grânulos são primeiro divididas em várias porções a reagir com diferentes ácidos bromo, na presença de reagente de acoplamento. Depois de lavar com o solvente, todos os grânulos vão ser analisadas em conjunto e misturados, em seguida, de novo dividido em várias porções, a reagir com diferentesaminas primárias. Depois de aminação, todos os grânulos são reunidas e lavadas exaustivamente, completando um total de monómeros em cada grânulo. Este processo pode ser repetido até que a diversidade desejada seja atingida.
2. Preparação de brometo de ácido a partir natural Aminoácidos
Em síntese sub-monómero, a síntese de cada monómero é dividido em duas fases separadas: 1. Acoplamento de brometo de ácido e 2 aminação com aminas primárias (Figura 2).. A fim de sintetizar um péptido amida terciária, brometos de ácidos quirais com as cadeias laterais do carbono alfa serão preparados a partir de aminoácidos naturais. Aqui nós descrevemos o método de transformar um aminoácido natural para o brometo de ácido correspondente com alta fidelidade de som. Usamos alanina como um exemplo; outros aminoácidos, incluindo serina, treonina, ácido aspártico, ácido glutâmico, asparagina, glutamina, glicina, valina, isoleucina, fenilalanina, também podem ser transformados em ácidos bromo sob condi semelhantens. Note-se que alguns dos aminoácidos com grupos funcionais, como o fenol, guanidina e amina precisam de ser protegidos antes da transformação. A instalação da reacção é mostrado na Figura 3.
Precauções de Segurança: Para são necessários os seguintes reações envolvendo HBr, NaNO 2 e outros produtos químicos corrosivos / tóxicos, equipamentos de segurança adequados, como óculos de segurança, jaleco e luvas resistentes a produtos químicos. Todos os comentários deverão ser realizadas em um exaustor pelo químico experiente.
- Adicionar 370 ml de água em 630 ml de solução de HBr a 48% para preparar um 1 L, solução de HBr a 30%. Adicione 500 ml de etileno glicol em um recipiente de banho 1 L; adicionar gelo seco para manter a temperatura a -10 ° C. Atenção: solução HBr 48% é fortemente ácido e corrosivo, manusear com cuidado. Leia o MSDS antes de usar.
- Adicionar D-alanina (8,9 g, 0,1 mol) e KBr (11,9 g, 0,1 mol) a uma 250 ml de três tubuladuras balão de fundo redondo com uma barra de agitação magnética. Adicionam-se 100 ml, e o HBr a 30% preparada em tele etapa anterior. Colocar o frasco no banho de etileno glicol preparado no passo 2.1 e manter a temperatura a -10 ° C. Bolha de árgon através de uma agulha longa a partir do fundo do balão durante 10 minutos, como mostrado na Figura 3. Agita-se a solução com a barra de agitação magnética a 300 rpm.
- Dissolve-se NaNO2 (8,28 g, 0,12 mol) num copo de 100 ml com 20 ml de água. Adicionar a solução para a igualização de pressão funil de carga e selar a ampola de carga com um septo. Transformar lentamente na válvula do funil de escoamento e deixar que a solução de NaNO2 cair para dentro do frasco. Controlar a válvula de ajuste da taxa de gotejamento de cerca de 2 gotas por segundo. Continue a agitação a 300 rpm e manter o árgon borbulhar do fundo do frasco. O frasco deve ser mantida em etileno glicol banho à temperatura de -10 ° C até que seja adicionado toda NaNO2. Atenção: Esta etapa gera calor e gás durante a adição de NaNO2 solução. Taxa de gotejamento deve ser cuidadosamente concontrolada e todo o sistema deve ser aberto através da saída de argônio.
- Continue mexendo por mais 3 horas e deixe a temperatura esquentar de -10 ° C à temperatura ambiente. A solução resultante deve ser clara a amarelo claro; Se a cor é demasiado escura, aplicar vácuo para remover o excesso de óxido de azoto e possível Br2 produzido durante a reacção.
- Extrair o produto a partir da solução com 3 x 35 ml de éter dietílico utilizando um funil de extração. Combinar a fase orgânica e lavá-la com solução salina saturada. A fase orgânica também pode ser lavado com uma pequena quantidade de NaHCO 3 antes de se lavar com uma solução salina para remover a cor se estiver escuro. Seca-se a fase orgânica sobre Na 2 SO 4 durante 6 horas.
- Filtre o Na 2 SO 4 e evapora-se o solvente sob vácuo, o produto em bruto deve ser obtida como claro para óleo amarelo pálido. O produto bruto pode ser ainda purificado por destilação a 115 ° C, com 3 mm de Hg, ou pelacoluna de sílica com 3:1 hexano: acetato de etilo.
- O produto puro é obtido na forma de óleo límpido, 6,6 g (rendimento de 74%), densidade = 1,69 g / mL, [α] D20 = +24 ° (metanol), RMN de 1H (400 MHz, CDCl3) δ 4,41 (q, J = 7,0 Hz, 1H), 1,86 (d, J = 7,0 Hz, 3H). No caso de (S)-2-bromopropanóico ácido d-4 (preparado a partir de 4 d-L-alanina), o produto puro é obtido na forma de óleo límpido, rendimento 78%, densidade = 1,72 g / mL, [α] D20 = -19 ° (metanol). 1H NMR, nenhum sinal H significativa é observada. ESI-MS - [M-1] - = 155,1 (esperado 154,97). Para (S)-4-metilpentanóico, 2-bromo-ácido (preparada a partir de L-leucina, utilizando o mesmo procedimento) do produto puro é obtido na forma de óleo límpido, rendimento 89%, [α] D20 = +37 ° (metanol), 1 H RMN (400 MHz, CDCl3) δ 4,30 (t, J = 7,7 Hz, 1H), 1,94 (dd, J = 10,8, 3,9 Hz, 2H), 1,81 (tt, J = 13,2, 6,5 Hz, 1H), 0,96 (dd, J = 18,2, 6,6 Hz, 7H). No caso de (S)-2-bromo-3-pheácido nylpropanoic (preparado a partir de L-fenilalanina utilizando o mesmo procedimento) do produto puro é obtido como um óleo amarelo pálido, rendimento de 72%, [α] D20 = +17 ° (metanol), RMN de 1H (400 MHz, CDCl3) 7,38 δ - 7,19 (m, 5H), 4,42 (dd, J = 8,1, 7,3 Hz, 1H), 3,47 (dd, J = 14,2, 8,2 Hz, 1H), 3,25 (dd, J = 14,2, 7,2 Hz, 1H).
3. Marcação isotópica de alanina transaminase Usando
Na síntese de biblioteca combinatória, em especial na síntese de divisão-e-associação de um talão de um composto (OBOC) bibliotecas, a quantidade de composto que pode ser obtido a partir de cada uma das esferas é relativamente pequena. (Tipicamente, um pmol a 10 nmol). Além disso, a espectrometria de massa é utilizada para a identificação e caracterização do composto final, devido à sua alta sensibilidade. A fim de utilizar a espectrometria de massa para determinar a estereoquimica absoluta dos centros quirais dos produtos finais de PTA, enantiómeros de ácido bromo deve ser isotopically rotulados antes de usar. Aqui nós descrevemos o método de usar transaminase e D 2 O rótulo de L-alanina.
- Dissolve-se L-alanina (300 mg, 3,36 mmol) com 10 mL de D 2 O, em um tubo de polietileno 50 ml. Adicionar α-cetoglutarato (10 mg, 0,068 mmol) como co-substrato. Aquecer-se o tubo a 37 ° C, e ajustar o PD para 8,5-8,7 usando uma soution 1 M NaOD. Nota: PD é determinada por tiras de teste de pH. Medidor de pH electro tradicional equipado com eletrodo de vidro seletivo para H + pode dar errado ler para D +.
- Adicionar alanina transaminase (0,1 mg, EC 2.6.1.2 de coração de porco, Roche Diagnostics, Indianapolis, IN) para o pD 8,5-8,7, 37 ° C uma solução preparada a partir da etapa anterior. Colocar o tubo num banho a 37 ° C incubadora e incubar durante a noite com agitação moderada, de 10 a 30 rpm, é o preferido.
- Após incubação durante a noite, ter de 0,5 ml da solução de D 2 O e verificar o progresso da reacção por 1H-RMN. Todos os sinais de protão de umlanine, δ 3,76 (q, J = 7,2 Hz, 1H), 1,46 (d, J = 7,3 Hz, 3H), 1 H RMN 400 MHz, deve ser significativamente suprimida devido à deuteração. Mais de 98% dos protões devem ser trocadas para deutério, conforme descrito anteriormente 23. Nota: D 2 O pode ser parcialmente recuperada por destilação, se a reacção for realizada em larga escala (> 200 ml de D 2 O). Normalmente, entre 60% e 80% de D 2 O pode ser destilado a partir da solução.
- Congelar a solução acima com nitrogênio líquido e liofilização-lo usando um liofilizador obter pó branco L-alanina deuterada.
4. Síntese de peptoid Linker Região
A região de ligação não é necessária para a síntese da biblioteca de PTA. No entanto, a fim de evitar o elevado ruído de fundo na gama mais baixa de peso molecular (100-600) de espectroscopia de massa MALDI e para melhorar a ionização dos compostos, de um ligante peptoid com múltiplos resíduos polares é frequentemente utilizado. Este peptoid linker pode ser sintetizado através de procedimento de síntese peptoid padrão. Aqui teremos sintetizar um pentâmero de N-metoxietil glicina como ligante (como mostrado na Figura 5).
- Inchar 90 mM grânulos TentaGel com ligante RAM (1 g, 0,27 mmol / g) em 10 ml de DMF durante 3 horas num reactor de seringa de 12 ml com agitação suave.
- Drenar a DMF a partir do reactor e adicionar solução de piperidina a 10 ml de DMF 20% para desproteger o grupo Fmoc a partir da amida ligante Rink. Agitar os grânulos com uma solução de piperidina a 20% durante 30 min. Lavar com DMF 5x para remover todos piperidina.
- Tome algumas esferas para fora da seringa e testá-lo com o teste de cloranil. Contas devem girar o marrom escuro (teste positivo para cloranil amina primária) se fmoc desprotegido com sucesso.
- Prepare as seguintes soluções:. 1 de 20 ml, bromoacï solução ácido / DMF 2 M; 2 20 ml, solução 2 M de DIC / DMF.; 3. 10 ml, 1 M methoxylethylamine / solução de DMF.
- Adicionar 5 ml de 2 M de solução de ácido bromoacético / DMF paraas contas, agitar suavemente. Em seguida, adicionam-se 5 ml de 2 M solução de DIC / DMF para os grânulos; vedar a seringa com o êmbolo e colocá-lo no agitador. Agitar durante 10 min.
- Lave as contas com DMF completamente. Adicionar 2 ml de solução 1 M metoxietilamina / DMF preparada a partir do passo 4.4 para os grânulos. Selar a seringa com o êmbolo e agitar no agitador durante 30 min.
- Lave as contas com DMF 5x. Confira algumas contas com o teste de cloranil, se positivas (esferas ficar azul), então continue para a próxima etapa. Caso contrário, repita o passo 4.6.
- Repita os passos de 4,5-4,7, 4x para completar o pentâmero.
. 5 Split-e-piscina Síntese de PTA Biblioteca com (R) - e (S)-2-bromopropiónico Ácidos
Aqui descreve-se a síntese de uma biblioteca de PTA pequeno com uma diversidade teórica de 9261 compostos, usando a 1 g de grânulos do passo 4.8. Note-se que um TentaGel talão 90 mM contém aproximadamente 2,9 milhões de grânulos por grama; Por conseguinte, a redundância dea biblioteca pode ser um 2,9 x 10 6/9261 = 312 cópias. Usaremos ácido bromoacético, (R)-2-bromopropanóico e isotópica marcado (S)-2-bromopropanóico ácido d-4, tal como os ácidos, e aminas 7 diferentes (A1 ~ A7, ver Figura 5 para detalhes) por aminação. Reactores de seringa e um colector de vácuo irá ser utilizado para realizar a síntese.
- Adicionar 10 ml de 01:01 de DCM: DMF para a seringa do passo 4.8; usar uma pipeta de 1000 mL com uma ponteira truncado para dividir todas as esferas de 1 g uniformemente em três reatores 5 ml seringas. Classificá-los como B (ácido bromoacético), R ((R)-2-bromopropanóico) e S ((S)-2-bromopropanóico ácido d-4). Lave todos os três seringas com DCM 3x, e lavar as seringas marcadas com R e S com THF anidro 3x, lavar seringa marcada com B 3x com DMF.
- Seringa R e S. BTC acoplamento de ácido bromopropanóico.
- Prepare uma solução BTC / THF fresco. Adicionar umapproximately 200 mg de BTC para o frasco em um exaustor, selá-lo com a tampa. Pesar a quantidade de BTC no frasco. Calcula-se a quantidade de solvente necessária e adicionar THF anidro para dentro do frasco para fazer um ml de solução de 20 mg / BTC / THF.
- Prepare a ácidos bromo / mistura BTC. Adicionar (R)-2-bromopropanóico ácido (89 ul, 0,95 mmol) e (S)-2-bromopropanóico ácido d-4 (89 mL, 0,95 mmol) em dois frascos pequenos separadamente. Para cada frasco, adicionar 5 ml de solução a 20 mg / mL de BTC / THF acima. Selar os dois frascos e colocá-los no freezer -20 ° C por 20 min.
- Adicionar 1125 mL, 2:1 THF / DIPEA (750 mL de THF, 375 mL de DIPEA, 2,2 mmol) à seringa, R e S separadamente. Misturar os grânulos com a ponta da pipeta. Deixe-os descansar por 5 min.
- Tomar dois arrefecida ácidos bromo / misturas BTC do passo 5.2.2, adicionar 2,4,6-trimetilpiridina (356 ul, 2,7 mmol) a cada frascos. Precipitados brancos irão formar-se imediatamente. Aplicar a suspensão correspondente diretamenteàs esferas alcalinizados (seringa R e S na etapa 5.2.3), logo que possível e, em seguida, colocá-los em um shaker a tremer sob 120 rpm durante 2 horas.
Nota: A solução nos reactores de seringa deve ser uma suspensão amarelada clara durante todo o curso da reacção. A cor mais escura é uma indicação de calor excessivo libertado durante a adição inicial da solução de cloreto de ácido. Isso pode ser resolvido por mais de arrefecimento ou diluir o ácido bromo / mistura BTC.
- Seringa B. Acoplamento ácido bromoacï com DIC
- Prepare uma frescos de 20 ml, uma solução de ácido bromoacético a 2 M / DMF. Prepare uma solução de 20 ml, 2 M de DIC / DMF.
- Adicionar 2 ml de solução de ácido bromoacï / DMF 2 M a seringa B, agitar suavemente. Adicionar 2 ml de solução 2 M DIC / DMF a seringa B, agitar suavemente.
- Coloque seringa B no mesmo shaker como seringa R e S , Agitá-lo para 2 horas. Note-se que a reacção de acoplamento do ácido bromoacético / DIC é feita dentro de 30 min; tempo de reacção prolongado é para a conveniência de síntese split-e-piscina.
- Depois de 2 horas, tomar seringa R, S e B do shaker. Lave todos os três seringas exaustivamente com DCM 5x. Em seguida, lave com DMF 5x. Note-se que a seringa R e S não pode ser lavada com DMF, antes de ser lavada com DCM ou THF primeiro.
- Piscina todas as esferas de seringas R, S e B em um reator de 12 ml seringa. Lave todas as contas com DMF 5x.
- Adicionar 10 ml de 01:01 de DCM: DMF para a seringa; usar uma pipeta de 1000 mL com uma ponteira truncado para dividir todas as esferas uniformemente em 7 individuais 2 ml seringas, classificá-los como A1-A7.
- Amination. Preparar 10 ml, 2 M de soluções de amina / DMF primárias para cada um dos 7 aminas listadas na Figura 5. Adicionar 5 ml de each solução de amina para a seringa correspondente A1-A7. Incubar todas as 7 seringas em uma incubadora a 60 ° C com agitação durante a noite.
- Após a incubação, todos os grânulos de lavar cuidadosamente com DMF. Tome algumas das contas de cada seringa e verificar com teste de cloranil. Se as contas de ficar verde (positivo) dentro de 3 min, continue com o próximo passo. Se negativo, repita o passo 5.7 para as seringas negativos.
- Repita os passos 5,1-5,8 2x para completar o trímero. Etapa opcional: Após cada ciclo, é recomendável verificar a qualidade síntese por espectroscopia de massa, como descrito abaixo. Todos os compostos 9261 são agora sintetizados em pérolas TentaGel como biblioteca OBOC.
- Confirmação espectroscópica Missa de PTAs.
PTAs são oligômeros altamente estruturadas e possuem muitas características comuns de peptídeos N-metilados. Um dos problemas comuns de síntese em fase sólida de péptidos N-metilado é a degradação do ácido durante a clivagem de TFA. Para suprimir a degradação de ácidos, a clivagem de moléculas como a ciclosporina a partir desuporte sólido é muitas vezes realizado sob baixa temperatura. Foram comparadas diferentes condições de clivagem para clivar diferentes moléculas de PTA do suporte sólido. Descobrimos que, em geral, baixa temperatura e concentração reduzida TFA poderia suprimir eficazmente a degradação de ácidos e fornecer compostos puros.- Preparar 10 ml de solução 1:1 de TFA / DCM em um tubo de 15 ml. Selar o tubo e colocá-lo em um freezer -20 ° C por 20 min.
- Lave as contas que devem ser clivadas com DCM 5x. Agitar os grânulos em DCM durante 15 min e lava-se os grânulos novamente com DCM 5x.
- Escorra o DCM da seringa. Use de um microscópio de luz e uma pipeta com ponta truncada para transferir cada grânulo indivíduo em uma placa de 96 poços, um grânulo por poço.
- Cubra a placa de 96 poços com uma lamínula. Colocar a placa num congelador de -20 ° C durante 15 min.
- Leve a solução arrefecida 01:01 TFA / DCM a partir do passo 5.10.1 e adicionar 20 ul de cada um dos poços que contém um grânulo. Coloque o pedaço tampa traseira e put da placa de 96 poços em um agitador no -20 ° C frigorífico.
- Agitar durante 20 min. Pegue a placa de 96 poços para fora e retire a lamínula. Seque o TFA / DCM de cada poço por um sopro de ar ou argônio sobre ele. Se mais do que 10 grânulos são clivados, um speedvac pode ser usado para secar o TFA / DCM de toda a placa. Note-se que nesta altura, nem todos os compostos são clivados os grânulos, mas os compostos clivados deve ser mais do que suficiente para realizar a análise de espectroscopia de massa.
- Adicionar 20 ul 06:04 ACN: H 2 O Solução para dissolver os compostos clivados a partir de cada poço. Manchar 0,6 ul de cada solução do composto em conjunto com 0,6 mL de matriz MALDI CHCA na placa de MALDI.
- Use espectrometria de massa MALDI para determinar o peso molecular e sequência (MS / MS) de cada composto.
6. Cloranil Teste
- Preparar os seguintes reagentes fresco para cada teste. Solução A: 2% cloranil (CAS: 118-75-2) em DMF. SoluçãoB: 2% de acetaldeído (CAS: 75-07-0) em DMF.
- Misturar 100 ml de solução A com 100 ml de solução B, antes do teste em um tubo de 1,5 ml; soltar as contas e agitar suavemente. Se os grânulos tornam-se azuis dentro de 5 minutos, que indica a presença de amina secundária na superfície dos grânulos. Aminas primárias dar uma cor marrom escuro em vez de virar azul.
Resultados
Aqui nós mostramos três espectros MALDI representativas de um trímero PTA com vinculador. Como mostrado na Figura 6A, quando clivada sob condições de temperatura ambiente, utilizando 50% de solução de TFA / DCM, degradação significativa é observada. Na Figura 6A, o pico 593 e 484 correspondem ao ligante e o trímero de PTA, respectivamente, mostram que a molécula inteira foi sintetizado com sucesso no talão mas degradados durante a clivagem. Quando clivada sob a condição de baixa temperatura, como descrito acima, a quantidade de degradação induzida por TFA é grandemente suprimida, conforme mostrado na Figura 6B. O mecanismo de clivagem tal tem sido descrito na literatura anterior 24, e crê-se passar por um intermediário de oxazolidina. Moléculas PTA pode ser sequenciado por MS / MS e o padrão de fragmentação é semelhante ao de péptidos e peptóides, como mostrado na Figura 6C. PTA moléculas sintetizadas com (S)-2-bromopropanóico ácido d-4, geralmente give pico mais largo na MS e MS / MS espectros devido à presença de produtos de deuteração incompletas, tais como (S)-2-bromopropanóico ácido d-3 (Figuras 7A e 7B). Isto pode ser utilizado como uma indicação da presença do centro quiral do R (invertida de S durante aminação) durante o procedimento de sequenciação. Descobrimos também que as moléculas de PTA têm uma tendência a formar adutos mais sodiated que peptoid / peptídeo, portanto água de sódio baixo (como água deionizada) e aparelho de plástico são os preferidos (Figura 7C). Outro sub-produto que pode ser observado na síntese de ATP é a acrilamida formada a partir da eliminação de brometo durante aminação (Figura 7C). Uma vez que a acrilamida é formada, a sequência é terminada. Isto pode ser resolvido através da redução da concentração da amina primária de 1 M, a fim de reduzir a alcalinidade da solução. Recomendamos realizar o teste de cloranil após cada etapa de acilação e usando spectr massaoscopy para verificar o produto depois de cada etapa de aminação para garantir a qualidade da biblioteca.
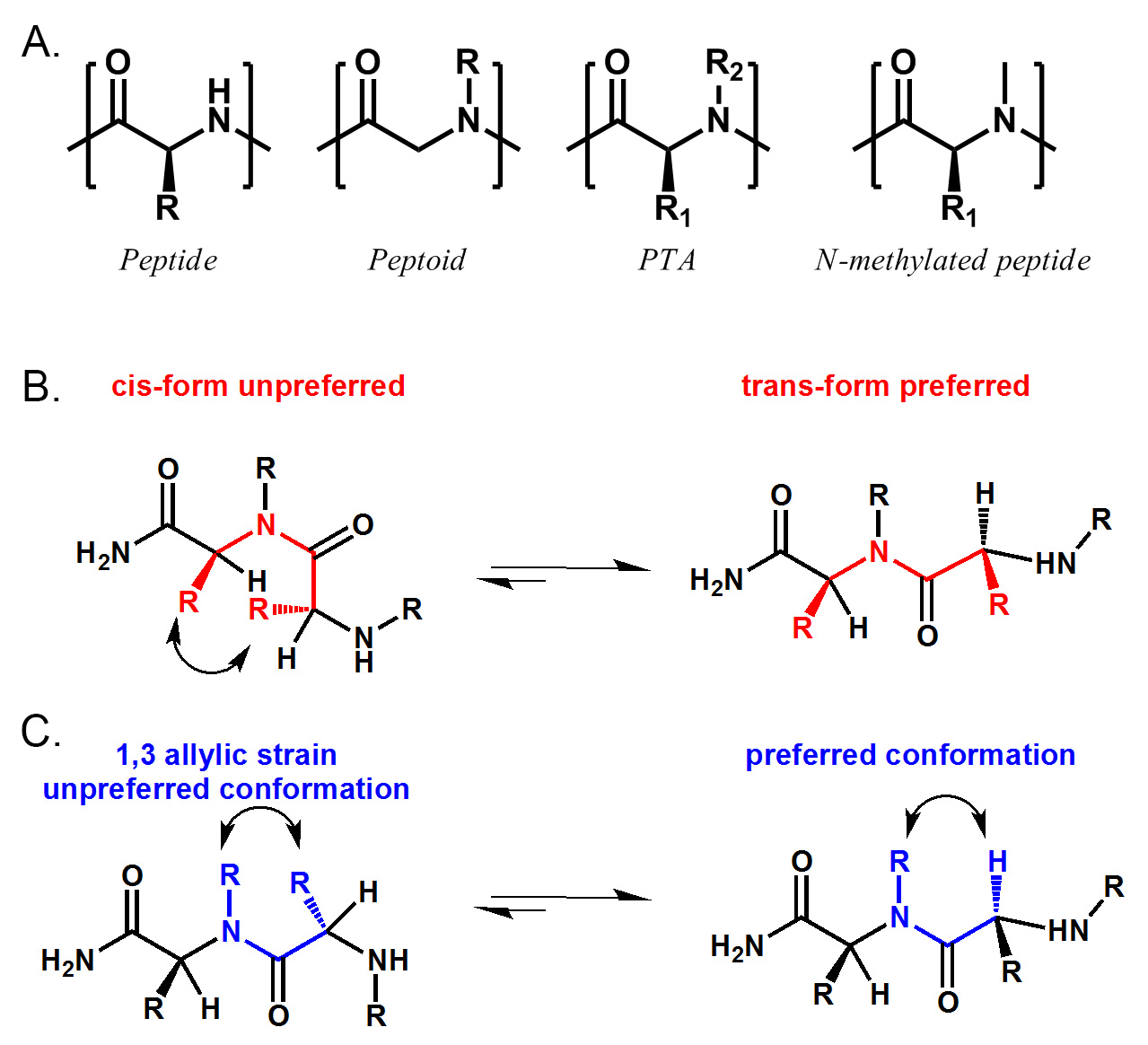
Figura 1. Estrutural comparação do péptido, peptoid, PTA e péptido N-metilado. PTA inclui péptido (R 2 = H), peptoid (R1 = H) e péptido N-metilado (R1 ≠ H, R2 = Me) . B) PTA prefere trans conformação ligação amida devido ao impedimento estérico entre dois cadeia α-side. C) PTA também tem uma conformação preferencial devido ao 1,3 alílico tensão entre N-substituto e cadeia α-side. Clique aqui para ver uma versão maior desta figura.
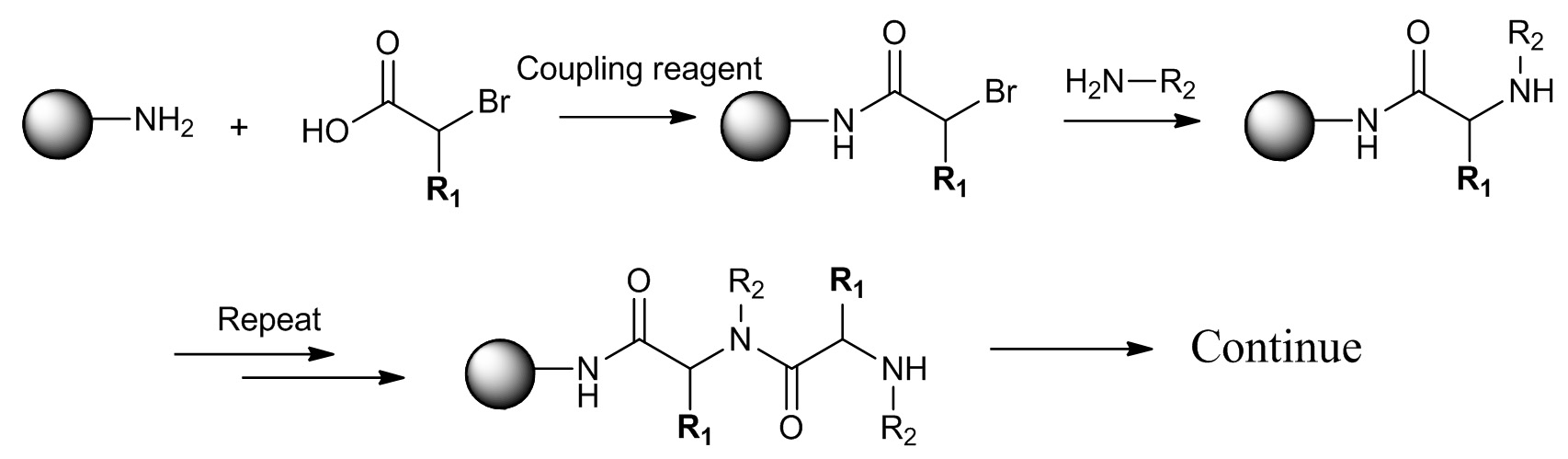
Figura 2 a síntese de peptoid Sub-monómero. (R 1 = H) e ATP (R1 ≠ H). Primeiro passo é a acilação do ácido da amina. O segundo passo é a aminação com aminas primárias. Clique aqui para ver uma versão maior desta figura.
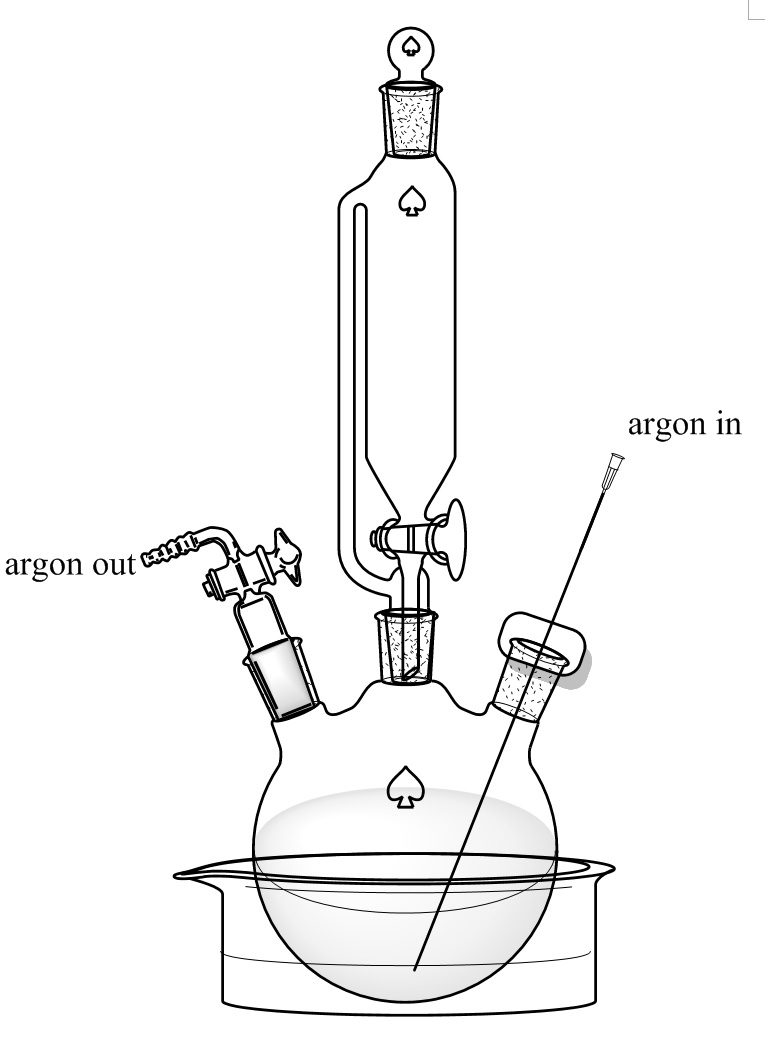
Instalação Figura 3. Reação. Um ml balão de fundo redondo com três gargalo 250 é colocado em um gelo / etileno glicol banho seco. O pescoço do meio está relacionada com uma pressão de 150 ml de equalização de um funil de gotejamento. Os pescoços esquerdo e direito são selados com um adaptador de controle de fluxo e um septo wom uma longa agulha que permite o fluxo de argônio passar. Clique aqui para ver uma versão maior desta figura.
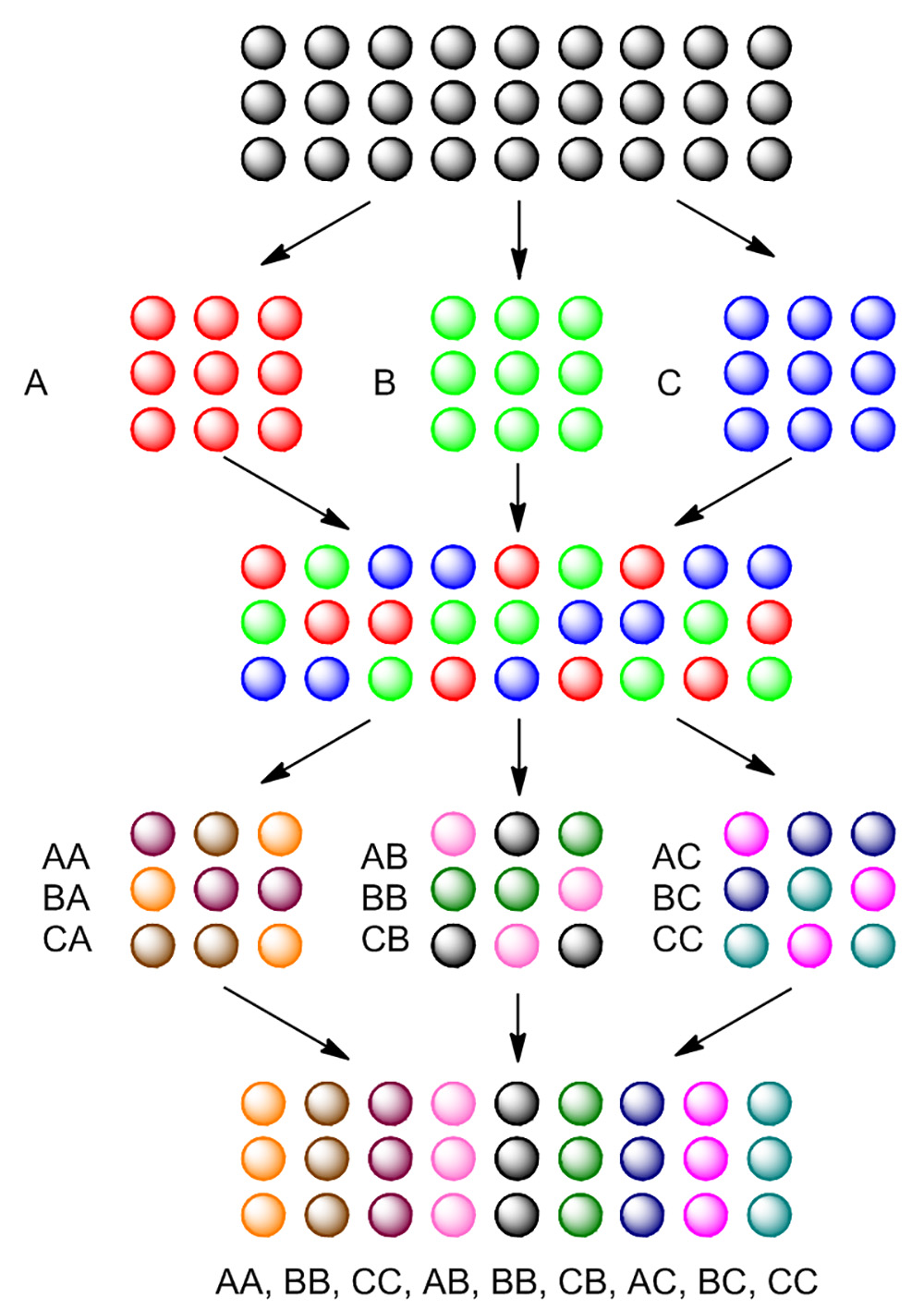
Figura 4. Fundamentos da síntese split-e-branco piscina. Grânulos estão divididos em três porções, tratados separadamente com reagente A, B e C. Depois de a primeira reacção, todas as três porções de grânulos são reunidas e misturadas. Contas agrupados são divididos novamente em três porções e novamente tratada com o mesmo reagente para cada porção individual. Após a segunda reação, 9 diferentes compostos são sintetizados. Clique aqui para ver uma versão maior desta figura.

Figura 5. Visão geral estrutura Library. Três PTAs são sintetizados após o vinculador pentâmero peptoid. Diversidade teórica, 3 3 X 7 3 = 9.261. Clique aqui para ver uma versão maior desta figura.
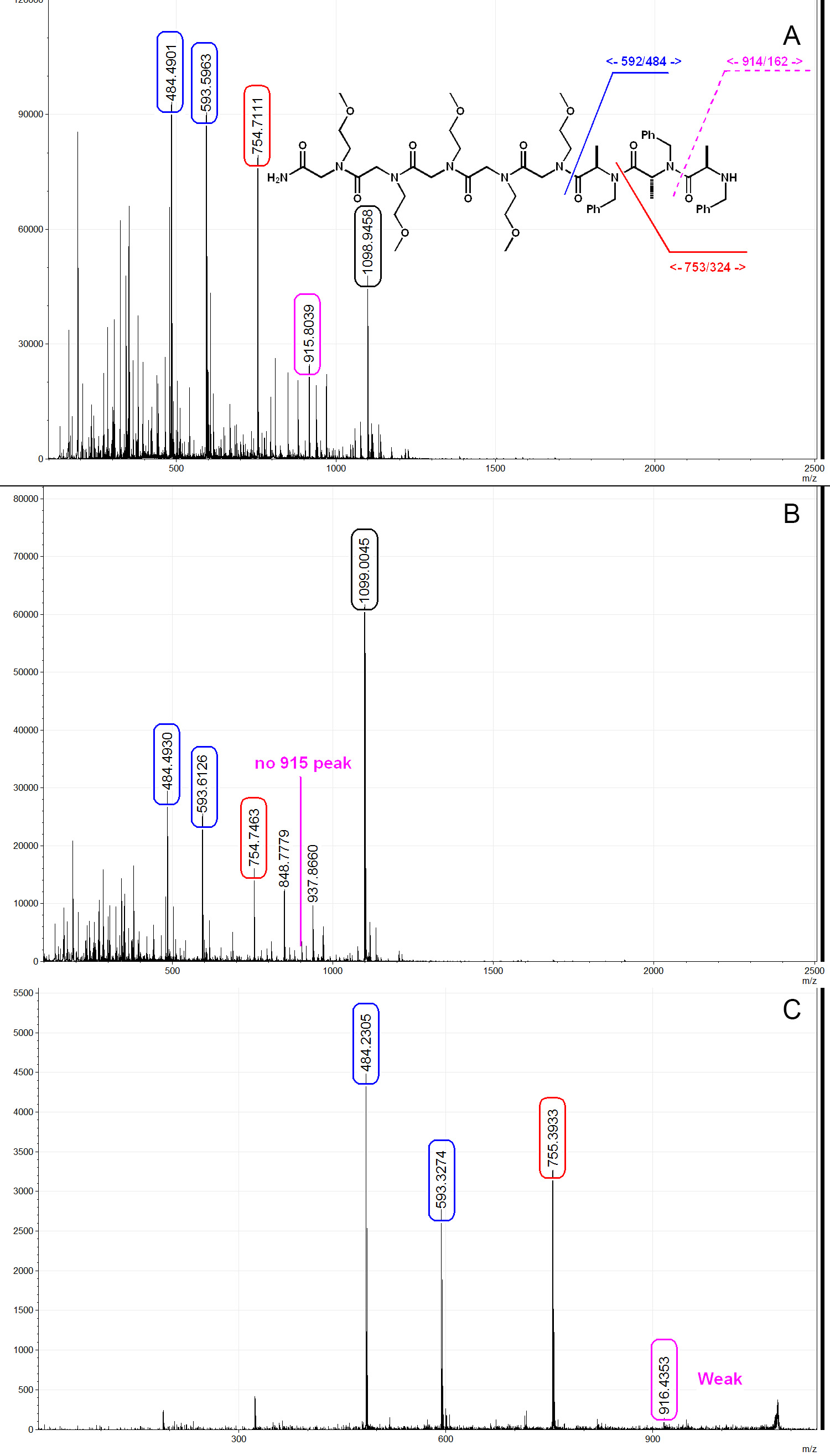
Figura 6. Espectros de massa MALDI típica de um trímero de PTA. UM) Trimer PTA clivado por 50% de TFA / DCM à temperatura ambiente. PTA estrutura, como mostrado, [M +1] + = 1077, [M + Na] + = 1.098,9, PTA fragmentação de clivagem de TFA pode ser claramente visto no espectro. B) Trimer cleaved de 50% de TFA / DCM sob condições optimizadas tal como descrito no documento. Degradação do ácido TFA-induzir é grandemente suprimida. C) Espectro MS / MS do trímero de PTA. Y7 Fraco (916) de sinal é observado, este é um comportamento típico de fragmentação para PTAs. Spectra analisados e gerados por mMass 32. Clique aqui para ver uma versão maior desta figura.

Os espectros de MALDI Figura 7. De síntese PTA com isotópica marcado monómero típico e subprodutos. D) Comparação MS espectros de moléculas sintetizadas por PTA azul: (R)-2-bromopropanóico [M +1] + = 760 [M + Na] + = 787 [M + K] + = 803 e vermelho: (S) - 2-bromopropanóico ácido d-4 [M +1] + = 764 [M + Na] + = 783 [M + K] + = 799. B) padrões de fragmentação MS / MS das duas moléculas mostradas em A). Note-se que, devido à presença de d 1, d 2 d 3 e especiarias (deuteração incompleto de alanina), moléculas sintetizadas por (S)-2-bromopropanóico ácido d-4 geralmente dão picos mais largos C) Vermelho:. Espectro de um PTA dímero sintetizada e clivada sob condição otimizada. Azul:. PTA dímero sintetizado com 2 solução M metoxietilamina e clivada em água filtrada normal, por favor clique aqui para ver uma versão maior desta figura.
Discussão
Peptídeo amidas terciárias (PTAs) são uma superfamília de oligômeros peptidomiméticas. Além dos peptídeos bem estudadas, peptoids e peptídeos N-metilados, uma grande parte dos compostos que compõem a família permanece pouco estudado, majoritariamente devido à falta de método sintético para acessar gerais peptídeos N-alquilados. Aqui, descrevemos um método eficiente para sintetizar APCs com os blocos de construção quirais derivados de amino ácidos. Anteriormente, relataram usar uma nova rota sub-monômero para bibliotecas de síntese de moléculas de PTA 23. Nós mostramos que PTAs são oligômeros altamente estruturadas que possuem restringe conformação através do backbone. Quando testado in vivo, as moléculas de PTA apresentaram maior permeabilidade celular e, portanto, melhoria da atividade 25. No entanto, ao lado com todas as vantagens, PTAs também vêm com alguns desafios sintéticos, majoritariamente da acilação de aminas secundárias em posições prejudicada. A cadeia α-side que fornece conformacionalrestrição também traz impedimento estérico para o passo seguinte de acoplamento. Para superar estes desafios sintéticos, foi realizado um estudo de otimização extensa e determinado BTC como o melhor reagente de acoplamento para esta reação 23.
O passo chave da via de síntese é facilitada BTC acilação da amina secundária. Durante este processo, BTC permite a geração de um cloreto ácido in situ 26,27. A maioria dos outros reagentes de acoplamento, que forma quer de ésteres activos ou anidridos ácidos como intermediários não forneceu acilação limpo para síntese PTA contínua. A existência de unidades de PTA anteriores prejudica grandemente a eficiência de acoplamento da unidade seguinte PTA devido a impedimento estérico. Portanto, para a síntese de várias APCs, um intermediário altamente activo com um pequeno grupo de saída é fortemente preferido. Entre todas as condições de acoplamento que testamos, in situ gerada cloreto de ácido pelo BTC trabalha os best em nossa mão. No entanto, mesmo com os cloretos de ácido altamente activos, é recomendável evitar aminas impedidas altamente estérico, tais como aminas primárias ramificadas-α na síntese da biblioteca, a menos testados previamente. Aminas aromáticas, tais como anil conduzem frequentemente a substituição incompleta e, portanto, devem também ser evitadas. Durante o passo de acoplamento BTC, a solução deve ser sempre uma cor amarelo pálido para laranja; uma solução de cor escura é uma indicação de sobreaquecimento e podem resultar em rendimentos mais baixos e aumento da formação de subprodutos. Esta geralmente pode ser resolvido por um arrefecimento adicional da solução BTC, reduzir o tamanho da reacção e transferência mais rápida da solução BTC / ácido activado. Além BTC, N-etoxicarbonil-2-etoxi-1 ,2-di-hidroquinolina (EEDQ) é um outro agente de acoplamento que funciona bem na síntese de ATP. O intermediário-chave é um anidrido carbónico misto com um relativamente pequeno grupo de saída. No caso de EEDQ, 3 equivalente de EEDQ são dissolvidos em conjunto com o ácido em DCM e, em seguida, apmanejado para os grânulos à temperatura ambiente. A reacção é normalmente realizada a cerca de 2 horas com agitação suave. Esta reacção liberta CO 2 durante a reacção; Por conseguinte, o sistema de reacção não deve ser fechada.
Outro passo fundamental é a clivagem ea caracterização de moléculas de ATP. Um padrão distinto de fragmentação MS / MS foi observada quando sequenciar moléculas PTA através MALDI-MS/MS (Figura 6). Ele consiste com uma baixa intensidade do último ião Y (mostrado na roxo na Figura 6C e o aumento da intensidade de y6, y5, y4, b2, b3) iões. Padrões análogos foram observados a partir de fragmentação peptídeo N-metilado no relatório anterior 28. Devido ao aumento da estabilidade da oxazolidina intermediária, os péptidos N-metilados tendem a dar fortes iões b 28. Além disso, é bem sabido que o péptido N-metilado é lábil a ácidos, durante tanto a clivagem de TFA e espectroscopia de massa MALDI 24,28, 29. Mecanicista estudo mostrou que, devido à restrição conformacional na espinha dorsal, o átomo de oxigénio de carbonilo do resíduo anterior é muitas vezes na proximidade do grupo carbonilo no local de clivagem, promovendo, assim, a formação da oxazolidina intermediária 29. Pelas razões mencionadas acima, ambas as APCs e peptídeos N-metilados precisam de ser clivado a partir de suportes sólidos, a baixa temperatura, com concentrações controladas de TFA a 26, 30. Na nossa experiência, o método de clivagem mais conveniente para os resíduos de PTA individuais ocorre a -20 ° C com uma solução pré-arrefecida de -20 ° C de 50% de TFA / DCM. Este procedimento elimina grandemente a formação de produtos degradados de ácido.
Depois de dominar esta técnica, com a biblioteca de PTA monómero derivadas de outros ácidos aminados naturais, tais como leucina, fenilalanina, glutamina, etc, podem ser sintetizados como bem. Uma biblioteca PTA alta qualidade pode ser rastreada against vários alvos proteína usando nossos previamente publicados on-talão de triagem protocolos 31. Hit compostos identificados a partir do rastreio podem ser caracterizados por espectroscopia de massa e ressintetizados para outro ensaio utilizando o protocolo descrito acima.
Divulgações
Os autores declaram que não têm interesses financeiros concorrentes.
Agradecimentos
Os autores gostariam de agradecer ao Dr. Jumpei Morimoto e Dr. Todd Doran para a assistência valiosa. Este trabalho foi apoiado por um contrato do NHLBI (no1-HV-00242).
Materiais
| Name | Company | Catalog Number | Comments |
| 2,4,6 trimethylpyridine | ACROS | 161950010 | CAS:108-75-8 |
| 2-morpholinoethanamine | Sigma-Aldrich | 06680 | CAS:2038-03-1 |
| 48% HBr water solution | ALFA AESAR | AA14036AT | CAS:10035-10-6 |
| Acetaldehyde | Sigma-Aldrich | 402788 | CAS:75-07-0 |
| Acetonitrile | Fisher | SR015AA-19PS | CAS:75-05-8 |
| Anhydrous tetrahydrofuran (THF) | EMD | EM-TX0277-6 | CAS:109-99-9 |
| Benzylamine | Sigma-Aldrich | 185701 | CAS:100-46-9 |
| bis(Trichloromethyl) carbonate (BTC) | ACROS | 258950050 | CAS:32315-10-9 |
| Bromoacetic acid | ACROS | 106570010 | CAS:79-08-3 |
| Chloranil | Sigma-Aldrich | 23290 | CAS:118-75-2 |
| Cyclohexanemethylamine | Sigma-Aldrich | 101842 | CAS:3218-02-8 |
| D2O | Cambridge Isotope | DLM-4-99.8-1000 | CAS:7789-20-0 |
| D-Alanine | Anaspec | 61387-100 | CAS:338-69-2 |
| Dichloromethane (DCM) | Fisher | BJ-NS300-20 | CAS:75-09-2 |
| Dimethylformamide (DMF) | Fisher | BJ-076-4 | CAS:68-12-2 |
| Ethylene glycol | Oakwood | 44710 | CAS:107-21-1 |
| Isopentylamine | Sigma-Aldrich | W321907 | CAS:107-85-7 |
| KBr | ACROS | 424070025 | CAS:7758-02-3 |
| L-Alanine | Anaspec | 61385-100 | CAS:56-41-7 |
| 3-Methoxypropylamine | Sigma-Aldrich | M25007 | CAS:5332-73-0 |
| 2-Methoxyethylamine | Sigma-Aldrich | 143693 | CAS:109-85-3 |
| N-(3-Aminopropyl)-2-pyrrolidinone | Sigma-Aldrich | 136565 | CAS:7663-77-6 |
| N,N'-Diisopropylcarbodiimide (DIC) | ACROS | 115211000 | CAS:693-13-0 |
| N,N-Diisopropylethylamine (DIPEA) | Sigma-Aldrich | D125806 | CAS:7087-68-5 |
| NaNO2 | ACROS | 424340010 | CAS:7631-99-4 |
| NAOD 40% solution in water | ACROS | 200058-506 | CAS:7732-18-5 |
| Piperidine | ALFA AESAR | A12442-AE | CAS:110-89-4 |
| Piperonylamine | Sigma-Aldrich | P49503 | CAS:2620-50-0 |
| Propylamine | Sigma-Aldrich | 240958 | CAS:107-10-8 |
| Trifluoroacetic acid | Sigma-Aldrich | 299537 | CAS:76-05-1 |
| α-Cyano-4-hydroxycinnamic acid | Sigma-Aldrich | 39468 | CAS:28166-41-8 |
| α-Ketoglutarate | ALFA AESAR | AAA10256-22 | CAS:328-50-7 |
| Tentagel Resin with RINK linker | Rapp-Polymere | S30023 | |
| Alanine transaminase | Roche | 10105589001 | AKA: Glutamate-Pyruvate Transaminase (GPT) |
| Incubator | New Brunswick Scientific | Innova44 | |
| NMR | Bruker | 400 MHz | |
| MALDI mass spectrometer | Applied Biosystems | 4800 MALDI-TOF/TOF | |
| Lyophilizer | SP Scientific | VirTis benchtop K | |
| Syringe reactor | INTAVIS | Reaction Column | 3 ml, 5 ml, 10 ml, 20 ml |
| Vacuum manifold | Promega | A7231 | Vac-Man |
Referências
- Xiao, X., Yu, P., Lim, H. -S., Sikder, D., Kodadek, T. Design and Synthesis of a Cell-Permeable Synthetic Transcription Factor Mimic. Journal of Combinatorial Chemistry. 9, 592-600 (2007).
- Miller, S. M., et al. Proteolytic Studies of Homologous Peptide and N-Substituted Glycine Peptoid Oligomers. Bioorganic & Medicinal Chemistry Letters. 4, 2657-2662 (1994).
- Grauer, A., Konig, B. Peptidomimetics - A Versatile Route to Biologically Active Compounds. European Journal of Organic Chemistry. 30, 5099-5111 (2009).
- Zuckermann, R. N., Kerr, J. M., Kent, S. B. H., Moos, W. H. Efficient method for the preparation of peptoids [oligo(N-substituted glycines)] by submonomer solid-phase synthesis. Journal of the American Chemical Society. 114, 10646-10647 (1992).
- Figliozzi, G. M., Goldsmith, R., Ng, S. C., Banville, S. C., Zuckermann, R. N. Synthesis of N-substituted glycine peptoid libraries. Methods in Enzymology. 267, 437-447 (1996).
- Seebach, D., et al. beta-peptides: Synthesis by Arndt-Eistert homologation with concomitant peptide coupling. Structure determination by NMR and CD spectroscopy and by X-ray crystallography. Helical secondary structure of a beta-hexapeptide in solution and its stability towards pepsin. Helv Chim Acta. 79, 913-941 (1996).
- Lam, K. S., et al. A New Type of Synthetic Peptide Library for Identifying Ligand-Binding Activity. Nature. 354, 82-84 (1991).
- Simon, R. J., et al. Peptoids - a Modular Approach to Drug Discovery. Proceedings of the National Academy of Sciences of the United States of America. 89, 9367-9371 (1992).
- Burkoth, T. S., et al. Toward the synthesis of artificial proteins: the discovery of an amphiphilic helical peptoid assembly. Chem Biol. 9, 647-654 (2002).
- Alluri, P. G., Reddy, M. M., Bachhawat-Sikder, K., Olivos, H. J., Kodadek, T. Isolation of protein ligands from large peptoid libraries. Journal of the American Chemical Society. 125, 13995-14004 (2003).
- Lim, H. S., Archer, C. T., Kodadek, T. Identification of a peptoid inhibitor of the proteasome 19S regulatory particle. Journal of the American Chemical Society. 129, 7750-7751 (2007).
- Wrenn, S. J., Weisinger, R. M., Halpin, D. R., Harbury, P. B. Synthetic ligands discovered by in vitro selection. Journal of the American Chemical Society. 129, 13137-13143 (2007).
- Aina, O. H., Marik, J., Liu, R. W., Lau, D. H., Lam, K. S. Identification of novel targeting peptides for human ovarian cancer cells using "one-bead one-compound" combinatorial libraries. Mol Cancer Ther. 4, 806-813 (2005).
- Udugamasooriya, D. G., Dineen, S. P., Brekken, R. A., Kodadek, T. A Peptoid “Antibody Surrogate” That Antagonizes VEGF Receptor 2 Activity. Journal of the American Chemical Society. 130, 5744-5752 (2008).
- Shah, N. H., et al. Oligo( N-aryl glycines): A New Twist on Structured Peptoids. Journal of the American Chemical Society. 130, 16622-16632 (2008).
- Chongsiriwatana, N. P., et al. Peptoids that mimic the structure, function, and mechanism of helical antimicrobial peptides. Proceedings of the National Academy of Sciences of the United States of America. 105, 2794-2799 (2008).
- Paul, B., et al. N-Naphthyl Peptoid Foldamers Exhibiting Atropisomerism. Organic Letters. 14, 926-929 (2012).
- Crapster, J. A., Guzei, I. A., Blackwell, H. E. A peptoid ribbon secondary structure. Angewandte Chemie. 52, 5079-5084 (2013).
- Gorske, B. C., Stringer, J. R., Bastian, B. L., Fowler, S. A., Blackwell, H. E. New strategies for the design of folded peptoids revealed by a survey of noncovalent interactions in model systems. J Am Chem Soc. 131, 16555-16567 (2009).
- Stringer, J. R., Crapster, J. A., Guzei, I. A., Blackwell, H. E. Extraordinarily robust polyproline type I peptoid helices generated via the incorporation of alpha-chiral aromatic N-1-naphthylethyl side chains. J Am Chem Soc. 133, 15559-15567 (2011).
- Huang, K., et al. A threaded loop conformation adopted by a family of peptoid nonamers. Journal of the American Chemical Society. 128, 1733-1738 (2006).
- Lee, J. H., Kim, H. S., Lim, H. S. Design and Facile Solid-Phase Synthesis of Conformationally Constrained Bicyclic Peptoids. Organic Letters. 13, 5012-5015 (2011).
- Gao, Y., Kodadek, T. Synthesis and Screening of Stereochemically Diverse Combinatorial Libraries of Peptide Tertiary Amides. Chem Biol. 20, 360-369 (2013).
- Urban, J., Vaisar, T., Shen, R., Lee, M. S. Lability of N-alkylated peptides towards TFA cleavage. Int J Pept Protein Res. 47, 182-189 (1996).
- Rzuczek, S. G., Gao, Y., Tang, Z., Thornton, C. A., Kodadek, T., Disney, M. D. Features of Modularly Assembled Compounds That Impart Bioactivity Against an RNA Target. ACS Chemical Biology. 8 (10), 2312-2321 (2013).
- Thern, B., Rudolph, J., Jung, G. Triphosgene as highly efficient reagent for the solid-phase coupling of N-alkylated amino acids—total synthesis of cyclosporin O. Tetrahedron Letters. 43, 5013-5016 (2002).
- Sleebs, M. M., Scanlon, D., Karas, J., Maharani, R., Hughes, A. B. Total Synthesis of the Antifungal Depsipeptide Petriellin A. J Org Chem. 76, 6686-6693 (2011).
- Vaisar, T., Urban, J. Gas-phase fragmentation of protonated mono-N-methylated peptides. Analogy with solution-phase acid-catalyzed hydrolysis. Journal of Mass Spectrometry. 33, 505-524 (1998).
- Creighton, C. J., Romoff, T. T., Bu, J. H., Goodman, M. Mechanistic studies of an unusual amide bond scission. Journal of the American Chemical Society. 121, 6786-6791 (1999).
- Sewald, N., Sewald, N. Efficient, racemization-free peptide coupling of N-alkyl amino acids by using amino acid chlorides generated in situ--total syntheses of the cyclopeptides cyclosporin O and omphalotin A. Angewandte Chemie (International ed. in English). 41, 4661-4663 (2002).
- Astle, J. M., et al. Seamless Bead to Microarray Screening: Rapid Identification of the Highest Affinity Protein Ligands from Large Combinatorial Libraries. Chem Biol. 17, 38-45 (2010).
- Strohalm, M., Kavan, D., Novak, P., Volny, M., Havlicek, V. mMass 3: a cross-platform software environment for precise analysis of mass spectrometric data. Anal Chem. 82, 4648-4651 (2010).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados