솔루션 및 농도
Overview
출처: 마이클 에반스 박사 연구소 — 조지아 공과대학
용액은 소량의 솔루트라고 불리는 일부 성분을 포함하는 균일한 혼합물이며, 용매라고 하는 다량의 하나의 성분이다. 고체 액체 용액에는 액체 용매에 용해된 하나 이상의 고체 솔루트가 포함되어 있습니다. 솔루션은 화학에서 유비쿼터스: 소량의 물질을 저장 및 처리하고 화학 반응을 수행하며 제어 가능한 특성을 가진 물질을 개발하는 데 사용됩니다.
용액에서 솔ute의 밀도는 솔트의 농도로 알려져 있다. 농도는 여러 가지 방법으로 발현될 수 있으며, 솔트, 용매 및 용액의 양을 전달하는 데 사용되는 단위가 다릅니다.
이 데모는 정밀분석 기법을 사용하여 표적 농도로 자당 용액을 준비하는 방법을 보여줍니다. 또한, 이 용액의 농도에 대한 다양한 측정이 제시되고 설명된다.
Principles
물에 담그면 많은 고체가 물 분자에 둘러싸인 입자 (분자 또는 이온)로 분해됩니다. 이 용해 공정은 고체와 액체의 이질적인 혼합물을 액체 물과 용해된 솔루트 입자로 구성된 단일 균질 혼합물로 변환합니다. 자당용 용해 공정은 고체 및 수성 상 설계기를 사용하여 화학 방정식으로 작성될 수 있습니다. 종에 따른(aq)지정자는 물 분자가 그 종을 둘러싸고 졸개하고 있음을 의미한다.

상이한 용액은 용존입자의 수가 다를 수 있으며, 농도는 용액 내에서 용성 입자의 밀도를 정량화하는 척도이다. 농도의 한 가지 근본적인 척도는 솔ute의 두더지 분획(x)입니다: 용액 성분의 총 두더지 수(모든 솔루트 및 용매)로 나눈 솔루트입자(nsolute)의두더지 수입니다.

두더지 분획을106으로 곱하면 백만 (ppm) 농도당 부품, 용액의 백만 입자 당 용성 입자의 수를 제공합니다. 용액 리터 당 solute의 수, 또는 어금니 (M), 농도의 두 번째 일반적인 측정이다.
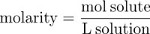
농도는 또한 덩어리에 의해 부품으로 표현될 수 있으며, 용액 질량의 분수는 솔테에 의한 것이다.
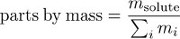
질량 농도를 100% 곱하면 질량 퍼센트가 됩니다.
마지막으로, 용액의 부피가 아닌 용매의 질량을 용액의 "크기"의 척도로 사용하는 농도의 척도이다. 몰랄티는 킬로그램내용매의 질량에 대한 솔ute의 두더지 수의 비율입니다.
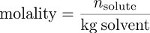
대상 어모함을 가진 솔루션을 정확하고 정확하게 준비하려면 신중한 분석 기술이 필요합니다. 고체 솔루트는 신중하게 계량하고 양적 플라스크에 정량적으로 (완전히) 옮겨져야 합니다. 용매는 용액이 유리 제품의 마크에 도달할 때까지 신중하게 추가할 수 있습니다. 최상의 결과를 얻으려면 솔벤트의 총 부피 보다 적게 완전히 용해될 수 있어야 하며, 고체 솔벤트가 보이지 않을 때 남은 용매를 첨가해야 합니다.
Procedure
1. 0.0100 M 수크로즈 솔루션의 100mL 준비
- 용액의 100mL에 용해될 자당(C12H22O11)의두더지 및 질량수를 결정한다.
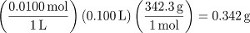
- 균형에 자당의 질량을 무게. 먼저 저울에 계량 보트를 배치하고 "타레 무게"를 설정합니다. 그런 다음 스쿠쿨라를 사용하여 원하는 양을 얻을 때까지 시약 병에서 계량 보트로 고체 솔루트를 조심스럽게 이송합니다.
- 파우더 깔때기를 깨끗하고 건조한 100mL 체피 플라스크에 넣습니다. 계량 보트에서 깔때기를 통해 플라스크에 고체를 붓습니다.
- 증류수(용매)가 들어 있는 워시 병을 사용하여 계량 보트에서 남은 고체를 깔때기를 통해 플라스크로 헹구세요.
- 액체 수준이 플라스크의 목에 도달 할 때까지 증류 수돗물을 사용하여 용매를 추가 (하지만 마크). 플라스크를 뚜껑을 뚜껑을 부드럽게 돌리면 솔루트를 녹입니다.
- 솔루트가 모두 용해되면 세척병을 사용하여 액체 수준이 마크에 도달할 때까지 조심스럽게 용매를 추가하십시오.
- 캡 및 용액의 좋은 혼합을 보장하기 위해 볼륨 플라스크를 여러 번 반전.
2. 초포화 수당 용액 만들기
- 증류수 100mL를 600mL 비커에 넣습니다.
- 220 g의 자당을 비커에 넣습니다.
- 비커에 마그네틱 스터드 바를 넣고 혼합물을 15분 동안 저어줍니다.
- 혼합물을 검사 : 자당이 모두 용해되지 않았습니다. 혼합물을 50ºC로 가열하고 10분 더 저어줍니다.
- 혼합물을 검사 : 자당의 모든 50 ºC에서 용해했다.
- 용액이 실온으로 냉각되도록 합니다. 해결책 검사: 50 ºC에서 용해된 추가 자당은 실온에서 용해된 채로 남아 있습니다. 실온의 용액은 과포화입니다.
Results
프로시저 1은 0.0100 M 자당 용액의 100mL를 생성합니다. 어금니 가아닌 농도의 측정으로 변환하려면 용액을 준비하는 데 사용되는 물의 질량을 결정합니다. 이를 정확하게 측정할 수 있지만, 측정이 없는 경우 용존 솔루트 입자의 부피가 무시할 수 있다고 가정할 수 있다(즉, 사용된 물의 부피는 100mL). 물의 밀도를 사용하여 ...

이 솔루션에서 자당증의 당밀성은 다음과 같습니다.
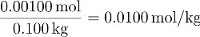
자당 질량에 의한 부품은 다음과 같습니다.
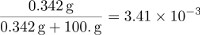
자당의 두더지 분수는 물 100g에서 두더지 의 수를 결정하고 용액의 입자의 총 양으로 자당의 양을 나누어 계산할 수 있습니다.

절차 2는 물에서 자당의 용해도가 온도에 따라 달라지는 것을 보여줍니다. 가열시, 포화 용액에 누워 용해되지 않은 자당은 용해되어 고온에서 더 높은 농도의 포화 용액을 형성합니다. 이 솔루션이 냉각되면 자당이 용액에서 침전되지 않습니다. 생성된 냉각 된 용액은 자당으로 과포화됩니다. 소량의 추가 자당 분말을 이 솔루션에 첨가하면 용존된 자당의 신속한 재결정을 유발할 수 있습니다.
Application and Summary
고체 액체 용액은 화학 분야에서 유비쿼터스입니다. 용해 된 솔루트는 빠르게 혼합하고 서로 부딪칠 정도로 이동성이 있기 때문에 대부분의 화학 반응은 용액에서 실행됩니다. 또한 소량의 솔루트를 거시적이고 쉽게 처리할 수 있는 볼륨에 소량의 솔루트를 저장하는 데 사용할 수도 있습니다. 솔루션은 용매에서 솔루트를 용해시키는 엔트로픽 효과에 기인 할 수있는 컬링 특성이라는 몇 가지 흥미로운 물리적 특성을 나타낸다.
솔루션 농도의 많은 다른 측정이 존재하는 이유를 궁금해 할 수 있습니다. 그 해답은 솔루션의 많은 응용 프로그램과 농도가 넘는 많은 크기의 범위에 있습니다. 예를 들어, 환경으로부터의 물 샘플에서 금속 이온 의 농도는 백만 분의 몇 부분의 범위에있을 수 있습니다 - 그것은 비현실적이고 잠재적으로 이 작은 농도를 어금니 또는 두더지 분획으로 표현하는 오해의 소지가 있습니다. 어금니가 화학 반응을 포함하는 금습술 계산을 위한 집중의 편리한 척도이지만, 약동은 특정 컬글리시컬 특성의 연구에 더 적합합니다.
많은 맥락에서 집중력에 대한 정확한 지식이 필수적이기 때문에 솔루션 준비 기술을 완성하는 것이 중요합니다. 예를 들어 화학 반응을 실행할 때 너무 많거나 너무 적게 사용하면 낭비된 반응제나 제품 수율이 낮아질 수 있습니다. 맥주의 법칙과 같은 농도와 관련된 경험적 관계에 대한 연구는 정확하게 알려진 농도에 달려 있습니다. 종종 용액 농도의 부정확성은 반응 엔탈피와 같은 계산된 값의 불확실성으로 직접 이어집니다. 부정확성을 완전히 제거하는 것은 불가능하지만 솔루션에 대한 분석 기법을 사용하면 불확실성이 최소화됩니다.
Tags
건너뛰기...
이 컬렉션의 비디오:

Now Playing
솔루션 및 농도
General Chemistry
274.1K Views

일반적인 실험실 유리 제품 및 사용
General Chemistry
655.8K Views

고체 및 액체밀도 결정
General Chemistry
556.0K Views

수성 솔루션에서 질량 백분율 구성 결정
General Chemistry
383.4K Views

경험적 공식 결정
General Chemistry
181.7K Views

이온 화합물의 용해도 규칙 결정
General Chemistry
141.4K Views

pH 미터 사용
General Chemistry
345.5K Views

적정 소개
General Chemistry
424.2K Views

이상적인 가스 법
General Chemistry
78.4K Views

평형 상수의 분광측정 결정
General Chemistry
158.4K Views

르 샤텔리에의 원리
General Chemistry
265.1K Views

알 수 없는 화합물을 결정 하는 동결 포인트 우울증
General Chemistry
160.7K Views

금리법 및 대응 순서 결정
General Chemistry
196.0K Views

차동 스캐닝 열량측정을 사용하여 엔탈피의 변화를 측정합니다.
General Chemistry
44.5K Views

조정 화학 단지
General Chemistry
91.4K Views
Copyright © 2025 MyJoVE Corporation. 판권 소유