Method Article
췌장 목-신체 암에 대한 등-꼬리 동맥 접근법을 통한 복강경 근치 전방 모듈 식 췌장 비장 절제술
요약
복강경 기술의 발전으로 복강경 근치 전향 모듈식 췌장 비장 절제술(L-RAMPS)이 널리 인식되었습니다. 그러나이 절차의 몇 가지 기술적 어려움으로 인해 L-LAMPS의 동맥 우선 접근법은 여전히 흔하지 않습니다. 여기에서 우리는 췌장 경부 종양에 안전하고 유익할 수 있는 L-LAMPS에 대한 등-꼬리 동맥 접근법을 개발했습니다.
초록
췌장 경부의 복강경 근치 적 절제술은 췌장암, 특히 신 보조 화학 요법을받은 환자에게 가장 복잡한 근치 적 수술 중 하나입니다. 여기에서는 복강경의 고화질 시력 및 수술 모드를 최대한 활용하여 등-꼬리 동맥 접근법을 사용하여 복강경 근치 전향 모듈 식 췌장 비장 절제술 (L-RAMPS)을 수행하는 기술을 제시합니다.
이 작업의 혁신과 최적화는 프로토콜에서 제공됩니다. 상 장간막 동맥 (SMA)의 등쪽, 췌장 머리의 등쪽, 체강 동맥 (CeA)의 뿌리, 왼쪽 신장 혈관의 복부 쪽 및 신장 hilum을 포함한 등쪽 절제면에 우선 순위를 부여해야합니다. 췌장 경부암에 대한 수술이 실현 가능하고 안전하다는 조건에서, 두 번째 단계는 꼬리에서 두부 쪽까지 SMA와 CeA를 둘러싸고 종양 절제술을 일 괄 적으로 수행하여 R0 (라디칼 제로) 절제율과 추가 예후를 증가시키는 것입니다.
서문
급진적 인 전향 모듈 식 췌장 비장 절제술 (RAMPS)은 2003 년 Strasberg가 처음 설명한 췌장 신체 또는 꼬리에 위치한 악성 종양에 대한 절묘한 절차입니다. 이 수술 전략은 종양이없는 해부면과 국소 림프절의 근치 적 절제를 달성하기 위해 췌장의 혈액 및 림프절 배액을 기반으로 설계되었습니다1. LAMPS는 종양이 없는 마진과 상대적으로 유리한생존 결과를 얻는 데 도움이 될 수 있기 때문에 외과의에 의해 점점 더 가치가 높아지고 있습니다2,3,4. 최소 침습 수술 기구 및 기술의 발전으로 복강경 RAMPS(L-RAMPS)는 수술 중 출혈 감소, 수혈 요구 감소, 통증 및 감염과 같은 절개 사건 감소등 몇 가지 이점으로 인해 점차 대중화되었습니다1. 원위 췌장 관 선암 (PDAC)을 가진 잘 선택된 환자의 경우, 최근 연구에 따르면 L-RAMPS가 효과적이고 안전한 접근법이 될 수 있음이 입증되었습니다 1,5,6.
췌장 머리 부위 주변의 악성 종양에 대한 췌장 십이지장 절제술 (PD)에서 동맥 우선 접근법은 몇 가지 장점이있는 널리 받아 들여지는 전략입니다. 이 방법의 핵심 원리는 췌장 절개 전 근치 절제 또는 주요 혈관 7,8,9의 결찰 가능성을 결정하기 위해 수술 초기 단계에서 상 장간막 동맥 (SMA)을 탐색하는 것입니다. 최근 연구에 따르면 이러한 동맥 우선 접근법은 원위 췌장과 비장의 정맥 울혈 형성을 완화하고 수술 부위의 효과적인 출혈 조절에 기여할 수 있음이 입증되었습니다. 게다가, 그것은 SMA 주변의 림프절 박리를 더 적절하게 만듭니다 7,10,11. 이러한 이유로 동맥 우선 전략은 PD의 중요한 구성 요소가되고 있으며 왼쪽 췌장암에 대한 통찰력을 제공합니다.
지금까지 L-RAMPS 절차에 대한 일부 동맥 우선 접근법 만보고되었습니다 5,6. 이러한 접근법의 핵심 개념은 췌장암 수술 동안, 췌장 실질의 절개 또는 주요 혈관의 결찰 및 절제술과 같은 비가역적 수술 단계의 수행 전에 SMA로의 종양 침윤이 검출되어야 한다는 것이다(12,13).
여기에서 우리는 L-LAMPS에 대한 등-꼬리 동맥 접근법을 개발했는데, 이는 췌장 경부의 종양에 안전하고 유익할 수 있습니다. 우리의 절차는 Yamamoto와 Kawabata12,14에 의해보고 된 L-RAMPS 절차에 대한 일상적인 동맥 우선 접근법을 더욱 최적화했습니다. 즉, 우리는 이전에 보고된 적이 없는 방법인 등-꼬리 접근 방식을 통해 SMA를 먼저 탐색하고 분리했습니다. 이 절차의 목표와 장점은 췌장 경부암에 대한 수술의 타당성과 안전성을 보장하여 R0 절제율과 추가 예후를 개선할 수 있는 것입니다.
그러나이 절차를 사용하려는 외과의는 복강경 췌장 수술에 대한 상당한 경험이 있어야합니다. 학습 곡선을 통과했더라도 이 절차에는 정교한 절제 기술이 필요하기 때문에 종양 유형, 혈관 상태 및 기타 매개변수를 포함한 환자의 상태를 평가하는 것이 중요합니다.
이 기사에서는 수술 전 신 보조 화학 요법 후 L-RAMPS를받은 내시경 초음파 유도 미세 바늘 흡인 (EUS-FNA) 생검으로 확인 된 PDAC가있는 50 세 남성 환자의 사례를 제시합니다. 우리의 목표는 등-꼬리 동맥 접근법을 사용하여 L-LAMPS의 임상 적 안전성과 타당성을 입증하고 췌장 목, 신체 또는 꼬리에 위치한 PDAC 환자에서 종양 학적 결과를 입증하는 것입니다.
프로토콜
본 의정서는 광저우 중의과 대학 제 2 부속 병원의 윤리 지침을 따릅니다. 이 기사와 비디오에 대해 환자로부터 정보에 입각 한 동의를 얻었습니다.
1. 환자 선택
- 환자가 췌장 목, 몸, 꼬리에 PDAC가 있는지 확인하고 조영제 강화 컴퓨터 단층 촬영(CT)으로 확인합니다. 이 절차는 다음과 같은 경우에 표시됩니다 : 절제 가능한 췌장암 및 신 보조 치료 후 경계 성 절제 가능한 췌장암. 근치 적 절제의 가능성은 효과적인 신 보조 치료 후 종양이 현저하게 퇴행 할 때 증가합니다.
참고 : 제시된 경우, CT 영상은 환자의 췌장 목에 종양을 나타 냈으며, 이는 암일 가능성이 큽니다. - 다음의 조건에서는 이 수술을 수행하지 마십시오: (1) 전이성 PDAC; (2) 신체가 주요 수술을 견딜 수없는 전반적인 환자 건강이 좋지 않습니다. (3) 비장 정맥 또는 비장 동맥 이외의 주요 혈액 동맥에 침윤하는 췌장 종양이있는 경우.
- 학습 곡선의 어린 나이에 다음과 같은 어려운 경우를 선택하지 마십시오 : 신체 최대 지수 (BMI) >35 kg / m2 인 비만 환자; 재발 성 췌장염으로 고통받는 환자, 그들은 매우 가난한 췌장 실질 상태를 가질 수 있기 때문에; 췌장 표적 방사선 요법을받는 환자; 이전 개복술 환자 등 복강경 수술에 대한 광범위한 경험이 얻어지면 이러한 상태의 환자도 선택할 수 있습니다15.
2. 수술 기술
- 작동 설정
- 마취 된 환자를 앙와위 자세로 수술대에 놓습니다. 다리가 벌어져 있는지 확인하십시오.
- 멸균 작업 중에 Pfannenstiel 절개로 표본을 추출할 수 있도록 치골 상부 영역을 충분히 노출시킵니다. 첫 번째 외과의가 환자의 오른쪽에 있고, 첫 번째 조수가 왼쪽에 있고, 복강경을 가진 두 번째 조수가 환자의 다리 사이에 있는지 확인하십시오. 이 절차에서는 그림 1과 같이 5포트 기술을 사용합니다.
- 기복막을 확립 한 후 배꼽 아래에 12mm 투관침을 삽입하십시오. 복강경 시야의 도움으로 반원형 배열 모드로 복벽에 다음 4 개의 투관침을 안전하게 설치하십시오.
- 탐사 단계
- 처음부터 일상적인 진단 복강경 검사를 수행하여 간과 복막 표면을 검사하여 추가 췌장 전이를 확인합니다.
- 위 경을 사용하여 위 상피 동맥과 정맥에서 약 2cm 떨어진 위 인대를 나누어 작은 주머니를 엽니 다.
- 짧은 위 혈관을 해부하고 절제하여 비장 절제술을 용이하게합니다.
알림: 더 나은 출혈 조절을 위해이 단계에서 가장 우수한 짧은 위 혈관도 감지 할 수 있습니다. - 간 견인기로 췌장 표면 위의 위를 매달아 췌장 상부 부위 주위에 수술 절차를위한 충분한 공간을 만듭니다.
- 초음파 칼로 비장 및 비장 주위 인대를 분리하고 절제하여 결장의 비장 굴곡과 췌장 꼬리를 더 노출시킵니다.
참고: 국소 구조가 명확하게 식별되지 않은 경우 수술 중 초음파 검사를 사용하십시오. 췌장 선암종은 수술 중 초음파 검사 (미국)에서 마진이 명확하지 않은 저 에코 덩어리로 나타납니다. - 췌장 목의 뒤쪽 표면과 SMV의 접합 부분, 문맥 (PV) 및 비장 정맥 사이의 틈을 나누어 통과시킵니다. 그런 다음이 부위를 조심스럽게 청소하여 췌장 절개를 준비하십시오.
- 해부 단계
- SMA의 등쪽, 췌장 머리의 등쪽, CeA의 뿌리, 왼쪽 신장 동맥 혈관의 복부 쪽 및 신장 hilum을 포함한 등쪽 절제면을 결정합니다.
- 횡단 결장과 장간막을 췌장 머리의 등쪽에서 먼저 올리십시오. 왼쪽 신장 정맥 (LRV)의 앞쪽 표면을 노출시키기 위해 Kocher 기동을 수행하십시오.
참고: 이 시점에서 LRV의 몇 센티미터 보기는 LRV를 다른 쪽에서 처리할 수 있는 이후 절차 단계에 유용합니다. 그룹 16 림프절 (대동맥 주위 노드)을 탐색하십시오. - SMA의 등쪽에 접근할 수 있도록 전체 소장을 오른쪽에 놓습니다. LRV 위의 SMA를 확인한 다음 전방 왼쪽 가장자리의 외막주위 평면을 따라 해부하고 췌장16에서 분리합니다.
- 단계 2.3.5에 설명 된대로 신장 동맥 혈관과 신장 힐럼의 복부 쪽에서 접근을 수행하십시오.
- 부신 뒤의 왼쪽 및 후방 평면과 후방 경사로의 왼쪽 신장 표면으로 절제 범위를 수행하십시오.
참고: 대동맥의 왼쪽에는 왼쪽 신장 동맥이 이어집니다. - 2.3.7-2.3.10 단계에 따라 CeA 방법의 핵심에 도달하십시오.
- 상위 콜론 영역으로 돌아갑니다. 총 간동맥과 위 십이지장 동맥 (GDA)을 해부화 한 다음 올바른 간동맥을 확인하십시오.
- 위 십이지장 림프절, 특히 림프절의 여덟 번째 그룹17을 해부합니다.
- 고무줄을 사용하여 GDA를 오른쪽으로 이동하여 PV의 앞쪽 표면을 노출시킵니다.
- CeA의 루트를 노출합니다. 이렇게하려면 총 간동맥을 원점까지 해부하고 복부 대동맥에서 기원에서 CeA를 자유롭게 해부하십시오.
- 꼬리쪽에서 두부 쪽까지 SMA와 CeA 주위를 해부합니다. 이 방법을 사용하려면 2.3.12-2.3.14단계를 수행합니다.
- 왼쪽 전방 가장자리의 외막주위 평면을 따라 SMA를 해부합니다.
알림: SMA의 앞쪽 표면은 이전에 췌장 목 아래에 생성 된 터널 아래에 잘 표시됩니다. 등쪽 췌장 동맥은 췌장으로 분기되는 동맥으로 SMA의 뿌리에서 탐구됩니다. - 원위 췌장을 후 복막에서 분리 한 다음 하부 장간막 정맥 (IMV)을 관리합니다.
참고: 등-꼬리 동맥 접근 기술을 사용하면 SMA와 췌장 사이에 해부학적 공간을 만드십시오. 지금까지 SMA의 왼쪽 공간에 있는 대부분의 공간이 이미 노출되어 있기 때문에 SMA의 출혈 제어를 쉽게 달성할 수 있습니다. - SMA의 전방 표면의 종양 침윤을 배제한 후, SMV는 췌장 목 아래에 노출된다.
알림: 수술 중에 SMA를 둘러싼 혈관 신경총과 신경 신경총이 완전히 절단될 수 있으므로 SMA 앞쪽 표면의 종양 침윤을 제외하십시오. - 췌장 목의 췌장 두께 및 질감에 따라, 상응하는 카트리지(18,19)를 갖는 기계식 스테이플러 장치를 사용하여 췌장 실질을 횡단시킨다. 5-0 폴리 프로필렌 봉합사로 췌장 덕트를 봉합하십시오. 췌장 목 가장자리의 냉동 병리학 적 검사를 수행하십시오.
- 비장 정맥의 뿌리를 혈관 클램프로 결찰하고 급격히 심하게하십시오.
- 총 간동맥 (CHA), 좌 위 동맥, 비장 동맥 (SpA) 및 CeA를 골격화하려면 췌장 상부 림프절 을 해부하고 제거합니다.
- 꼬리에서 SMA 및 CeA의 두부 쪽으로 지방과 섬유질 조직을 절제합니다.
- PV, CeA 및 SMA로 둘러싸인 하이델베르크 삼각형에서 림프절을 제거합니다.
- 이 절차 동안 생성된 더 큰 등쪽 및 꼬리 공간 때문에 SpA의 원점을 분리하고 나눕니다.
- LRV를 노출하여 등쪽 해부 평면을 결정합니다.
알림: 왼쪽 부신과 Gerota의 근막은 후방 경사로20,21을 위해 완전히 제거되어야 합니다. - 마지막으로, 전향 방법 (오른쪽에서 왼쪽으로)을 사용하여 원위 췌장과 비장뿐만 아니라 주변 연조직을 해부합니다.
참고: 그림 2에서 볼 수 있듯이 절제 부위의 두부 경계는 횡격막 크루스, 꼬리 경계는 LRV, 내부 범위는 대동맥의 왼쪽 측면 부분에 있습니다. 마지막으로 췌장 그루터기와 비장 홈에 두 개의 배액관을 도입하고 배치합니다.
3. 수술 후 추적 관찰
- 복부 상태를 평가하기 위해 수술 후 7 일째에 복부의 컬러 도플러 초음파 또는 CT 스캔을 수행하십시오.
- 수술 후 3일, 5일, 7일째에 복부 배액액의 아밀라아제 수치를 확인하여 심각한 합병증 중 하나인 췌장 누공을 평가합니다.
참고: 수술 후 췌장 누공(POPF)은 배액의 아밀라아제 수치가 정상 혈청 아밀라아제 활성의 상한의 3배 이상일 때 진단할 수 있으며, 이는 췌장 누공과 직접 관련된 임상적으로 관련된 발달/상태와 관련이있습니다22. - 아밀라아제 수치가 정상 혈청 아밀라아제 상한의 3배 미만인 경우 배수구를 제거한다.
- 수술 후 6-8 주 후에 젬시 타빈과 nab-paclitaxel 프로그램을 사용하여 6-8주기의 보조 화학 요법을 수행하십시오.
- 수술 후 장기 추적 관찰을 수행하십시오. 첫 해에는 3개월마다, 두 번째 해에는 3-6개월마다, 그 이후에는 6개월마다 후속 조치를 실시합니다. 탄수화물 항원 199 (CA-199), CeA, 복부 색 도플러 초음파 또는 CT 스캔은 추적 관찰 중에 다시 확인해야합니다.
결과
상복부 불편 함과 만성 영양 실조가있는 50 세 남성은 췌장 목에 3.2cm x 2.5cm 종양이 확인되었습니다. 그는 이전에 건강했고 정상적인 BMI (19.9kg / m2)를 가졌습니다.
수술 전 영상 평가에서 원격 전이, 주요 혈관(비장 동맥 및 정맥 제외) 또는 림프절 침윤이 감지되지 않았습니다. PDAC의 병리적 진단을 확인하기 위하여 내시경 초음파 유도 미세바늘흡인(EUS-FNA)을 수행하였다. 환자는 젬시타빈과 나브-파클리탁셀 프로그램을 사용하여 4주기의 신보조 화학요법을 받았습니다. 이 약물은 임상 증상을 완화하는 데 도움이 되었으며 탄수화물 항원 199(CA-199)는 4,666U/mL에서 1,350U/mL로 감소한 반면 종양의 최대 직경은 3.2cm에서 2.5cm로 감소했습니다( 그림 3 참조).
수술 결과는 표 1에 나와 있습니다. 시술의 총 시간은 240 분이었고 혈액 손실은 50mL였습니다. 환자의 회복은 복잡하지 않았으며 수술 후 9일 째에 퇴원했습니다. 수술 후 3일차(POD 3)에 배액의 아밀라아제 수치는 1,645U/L였습니다. 배수구는 아밀라아제 수준이 7 U / L 일 때 POD 54에서 제거되었습니다. 이것은 A 등급 POPF로 등급이 매겨졌습니다. POD 7의 수술 후 CT 검사에서 복막액이 발견되지 않았습니다( 그림 4 참조). 환자는 잘 회복되었고 POD 9에서 퇴원했습니다.
조직 병리학은 간질 섬유증이있는 중등도의 분화가 잘 안되는 유관 선암종을 밝혀 수술 전 진단을 확인했습니다. 췌장 간질 섬유증은 수술 전 신 보조 화학 요법으로 인한 것일 수 있습니다 ( 표 1 참조). 췌장 목과 후 복막의 절제 마진은 현미경으로 급진적이었습니다 (R0). 15 개의 림프절 만 발견되었으며 그 중 어느 것도 관련되지 않았습니다. 종양은 T2N0M0 (AJCC 8판) 으로 병기화되었다. 환자는 젬시타빈과 나브-파클리탁셀 프로그램을 사용하여 6주기의 보조 화학 요법을 받았습니다.
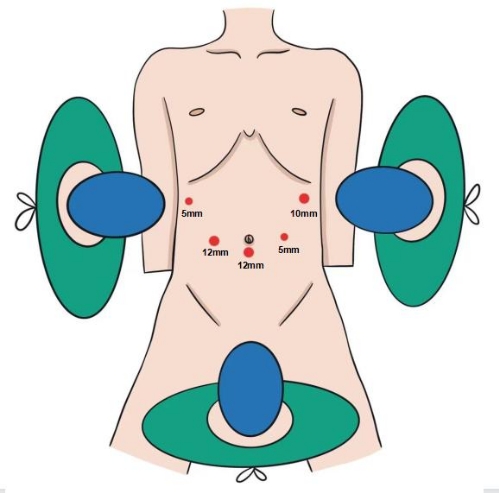
그림 1: 외과 의사의 위치. 첫 번째 외과의는 환자의 오른쪽에, 첫 번째 조수는 왼쪽에, 복강경을 들고있는 두 번째 조수는 환자의 다리 사이에 있습니다. 절차는 5 포트 기술을 사용하여 수행됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
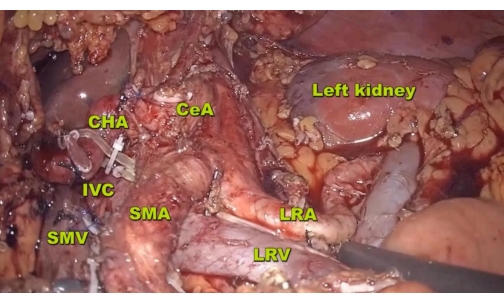
그림 2: 절제술. 절제 범위는 횡격막 crus까지, LRV까지, 그리고 뒤쪽에있는 대동맥의 뒤쪽 왼쪽 측면 부분까지 확장됩니다. 약어 : LRA = 왼쪽 신장 동맥, IVC = 하대 정맥. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 3: 이미지는 췌장 목의 질량을 보여줍니다. 신보조 화학요법 후, 종양 최대 직경을 (A) 3.2 cm에서 (B) 2.5 cm로 감소시켰다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 4: CT 이미지는 POD 7에서 복막액이 발견되지 않았음을 보여줍니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
| 변수 | 결과 |
| 수술 중 | |
| 작동 시간, 분 | 240 |
| 수술 중 혈액 손실, mL | 50 |
| 수술 | |
| 수술 후 췌장 누공 (POPF) | A를 등급을 매기십시오 |
| 배수구 제거, 수술 후 하루 | 7 |
| 수술 후 입원, 일 | 9 |
| 병리학 적 진단 | 근본적으로 (R0) 간질 섬유증이있는 덕트 선암, 2cm 절제 |
표 1: 수술의 대표 결과.
토론
PDAC의 5 년 생존율에도 불구하고, 이것은 근치 적 절제의 기회가있는 환자에게는 여전히 불만족 스럽다. 수술은 지금까지 유일한 치료 방법이었습니다22. 절제 가능성은 대부분 SMA, CeA, CHA 및 SMV24,25를 포함한 지역 중요 선박의 조건에 의해 평가됩니다. 수술 전 방사선 촬영은 혈관 상태에 대한 적절한 정보를 제공할 수 있지만, 외과적 탐색은 모호성 평가가 있는 환자, 특히 이전에 신보조 화학 요법을 받은 환자에게 간단한 방법입니다. 따라서 불필요한 후속 수술을 피하고 R0 절제율을 향상시키기 위해 수술 중 근치 적 절제술의 조기 평가가 매우 중요합니다.
췌장 목의 복강경 근치 적 절제술은 췌장암에 대한 가장 복잡한 근치 적 수술 중 하나입니다. 이 연구는 등-꼬리 동맥 접근법을 통해 L-RAMPS 수술 전략을 제공하며, 이는 숙련된 외과의가 있는 대량 센터에서 표준화되고 재현 가능하며 종양학적으로 효과적인 절차로 발전할 수 있습니다. 최소 침습적 접근을 통해 동맥 우선 측면에 대한 새로운 비전을 제공 할 수 있으며 LAMPS의 초기 단계에서 근치 적 절제의 타당성을 결정할 수 있습니다.
이 기술의 가장 중요한 부분은 다음 부분을 포함하는 등쪽 절제면을 확인하는 데 우선 순위를 부여해야한다는 것입니다 : 상 장간막 동맥 (SMA)의 등쪽, 췌장 머리의 등쪽, 체강 동맥의 뿌리 (CeA), 왼쪽 신장 혈관의 복부 쪽 및 신장 hilum. 모든 중요한 부분이 종양에 의해 침투되지 않는 조건에서 외과의 사는 급진적 인 수술의 타당성과 안전성을 보장 한 다음 꼬리 쪽에서 두부 측으로 SMA 및 CeA 주변의 종양 을 절제 할 수 있습니다. 이 수술 전략은 R0 절제율과 장기 생존율을 향상시키는 것을 목표로합니다.
이 복잡한 절차는 개방 및 복강경 췌장 수술 기술을 모두 갖춘 고도로 숙련 된 수술 팀이 수행해야합니다. 이 수술 방법의 구현은 수술 팀의 협력, 이 복잡한 영역의 해부학적 인지, 예상치 못한 변화에 대한 유연한 대응 능력에 대한 요구 사항이 높기 때문에 학습 곡선이 가파르다. 이러한 이유로 제한된 사례로 인해 무작위 임상 시험을 설계하고 달성하기 어렵 기 때문에이 기술의 수술 전후 및 생존 결과에 대한 높은 수준의 증거를 확립하기가 어렵습니다.
공개
없음.
감사의 말
없음.
자료
| Name | Company | Catalog Number | Comments |
| 3D Laparoscope | STORZ | TC200,TC302 | |
| Echelon Flex Powered Plus Articulating Endoscopic Linear Cutter and Endopath Echelon Endoscopic Linear Cutter Reloads with Gripping Surface Technology | Ethicon Endo-Surgery | ECR60G/GST60G | |
| HARMONIC ACE Ultrasonic Surgical Devices | Ethicon Endo-Surgery | HAR36 | |
| Ligating Clips | Teleflex Medical | 5,44,22,05,44,23,05,44,000 | |
| Ultrasonic Surgical & Electrosurgical Generator | Ethicon Endo-Surgery | GEN11CN |
참고문헌
- Kim, E. Y., Hong, T. H. Initial experience with laparoscopic radical antegrade modular pancreatosplenectomy for left-sided pancreatic cancer in a single institution: technical aspects and oncological outcomes. BMC Surgery. 17 (1), 2(2017).
- Strasberg, S. M., Fields, R. Left-sided pancreatic cancer: distal pancreatectomy and its variants: radical antegrade modular pancreatosplenectomy and distal pancreatectomy with celiac axis resection. The Cancer Journal. 18 (6), 562-570 (2012).
- Strasberg, S. M., Linehan, D. C., Hawkins, W. G. Radical antegrade modular pancreatosplenectomy procedure for adenocarcinoma of the body and tail of the pancreas: ability to obtain negative tangential margins. Journal of the American College of Surgeons. 204 (2), 244-249 (2007).
- Strasberg, S. M., Drebin, J. A., Linehan, D. Radical antegrade modular pancreatosplenectomy. Surgery. 133 (5), 521-527 (2003).
- Sunagawa, H., Harumatsu, T., Kinjo, S., Oshiro, N. Ligament of Treitz approach in laparoscopic modified radical antegrade modular pancreatosplenectomy: report of three cases. Asian Journal of Endoscopic Surgery. 7 (2), 172-174 (2014).
- Choi, S. H., Kang, C. M., Lee, W. J., Chi, H. S. Multimedia article. Laparoscopic modified anterior RAMPS in well-selected left-sided pancreatic cancer: technical feasibility and interim results. Surgical Endoscopy. 25 (7), 2360-2361 (2011).
- Weitz, J., Rahbari, N., Koch, M., Büchler, M. W. The "artery first" approach for resection of pancreatic head cancer. Journal of the American College of Surgeons. 210 (2), 1-4 (2010).
- Cho, A., Yamamoto, H., Kainuma, O. Tips of laparoscopic pancreaticoduodenectomy: superior mesenteric artery first approach (with video). Journal of Hepato-Biliary-Pancreatic Sciences. 21 (3), 19-21 (2014).
- Morales, E., et al. Follow "the superior mesenteric artery": laparoscopic approach for total mesopancreas excision during pancreaticoduodenectomy. Surgical Endoscopy. 33 (12), 4186-4191 (2019).
- Nagakawa, Y., et al. Surgical approaches to the superior mesenteric artery during minimally invasive pancreaticoduodenectomy: A systematic review. Journal of Hepato-Biliary-Pancreatic Sciences. 29 (1), 114-123 (2021).
- Pessaux, P., Varma, D., Arnaud, J. P. Pancreaticoduodenectomy: superior mesenteric artery first approach. Journal of Gastrointestinal Surgery. 10 (4), 607-611 (2006).
- Yamamoto, M., et al. New laparoscopic procedure for left-sided pancreatic cancer-artery-first approach laparoscopic RAMPS using 3D technique. World Journal of Surgical Oncology. 15 (1), 213(2017).
- Rosso, E., et al. Laparoscopic radical antegrade modular pancreatosplenectomy with venous tangential resection: focus on periadventitial dissection of the superior mesenteric artery for obtaining negative margin and a safe vascular resection. Annals of Surgical Oncology. 27 (8), 2902-2903 (2020).
- Kawabata, Y., et al. Laparoscopic versus open radical antegrade modular pancreatosplenectomy with artery-first approach in pancreatic cancer. Langenbeck's Archives of Surgery. 405 (5), 647-656 (2020).
- Vissers, F. L., et al. Laparoscopic radical left pancreatectomy for pancreatic cancer: surgical strategy and technique video. Journal of Visualized Experiments. (160), e60332(2020).
- Ome, Y., Seyama, Y., Muto, J. Laparoscopic distal pancreatectomy for left-sided pancreatic cancer using the "Caudo-Dorsal Artery First Approach". Annals of Surgical Oncology. 26 (13), 4464-4465 (2019).
- Tol, J. A., et al. Definition of a standard lymphadenectomy in surgery for pancreatic ductal adenocarcinoma: a consensus statement by the International Study Group on Pancreatic Surgery (ISGPS). Surgery. 156 (3), 591-600 (2014).
- Asbun, H. J., Stauffer, J. A. Laparoscopic approach to distal and subtotal pancreatectomy: a clockwise technique. Surgical Endoscopy. 25 (8), 2643-2649 (2011).
- Asbun, H. J., et al. Technique and audited outcomes of laparoscopic distal pancreatectomy combining the clockwise approach, progressive stepwise compression technique, and staple line reinforcement. Surgical Endoscopy. 34 (1), 231-239 (2020).
- Abu Hilal, M., et al. Laparoscopic radical 'no-touch' left pancreatosplenectomy for pancreatic ductal adenocarcinoma: technique and results. Surgical Endoscopy. 30 (9), 3830-3838 (2016).
- Song, K. B., et al. Single-center experience of laparoscopic left pancreatic resection in 359 consecutive patients: changing the surgical paradigm of left pancreatic resection. Surgical Endoscopy. 25 (10), 3364-3372 (2011).
- Bassi, C., et al. The 2016 update of the International Study Group (ISGPS) definition and grading of postoperative pancreatic fistula: 11 Years After. Surgery. 161 (3), 584-591 (2017).
- Mizrahi, J. D., Surana, R., Valle, J. W., Shroff, R. T. Pancreatic cancer. Lancet. 395 (10242), 2008-2020 (2020).
- Varadhachary, G. R., et al. Borderline resectable pancreatic cancer: definitions, management, and role of preoperative therapy. Annals of Surgical Oncology. 13 (8), 1035-1046 (2006).
- Abrams, R. A., et al. Combined modality treatment of resectable and borderline resectable pancreas cancer: expert consensus statement. Ann of Surgical Oncology. 16 (7), 1751-1756 (2009).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유