Method Article
전이율을 제어하는 절단을 가진 신제닉 직소 성 골육종 스프라그 Dawley 쥐 모델
요약
여기서, 전이 생물학의 전임상 조사에 사용될 수 있는 자발적인 폐 전이와 함께 골육종의 절단 절차를 따르는 회제 성 직소 이식이 기술되고 새로운 치료법의 개발이 설명된다.
초록
골육종 (OS)의 치료에 가장 최근의 사전은 다중 에이전트 화학 요법이 수술 에 비해 전반적인 생존을 개선하는 것으로 나타났을 때 1980 년대에 발생했습니다. 이 문제를 해결하기 위해, 연구의 목적은 생존을 연장 포괄적 인 히스토마이트, 이미징, 생물학적, 이식 및 절단 수술 접근으로 쥐에서 OS의 덜 알려진 모델을 정제하는 것입니다. 우리는 면역 능력, 근친근 Sprague-Dawley (SD), 이식 UMR106 OS 세포주 (SD 쥐에서 유래)와 시너지 쥐 모델을 사용 (SD 쥐에서 유래) 3 주 된 남성과 여성 쥐에 3 주 된 남성과 여성 쥐 소아 OS를 모델링. 우리는 쥐가 재현 가능한 1 차및 전이성 폐 종양을 개발하고, 3 주 이식 후 이식 후 사지 절단이 폐 전이의 발생률을 현저히 감소시키고 예기치 않은 죽음을 방지하는 것을 발견했습니다. 조직학적으로, 쥐의 1차 및 전이성 OS는 인간 OS와 매우 유사하였다. 면역 조직 화학 방법을 사용하여, 연구 결과는 쥐 OS가 대식세포및 T 세포로 침투한다는 것을 보여줍니다. OS 세포의 단백질 발현 조사는 이 종양이 ErbB 가족 키나아제표현을 한다는 것을 밝힙니다. 이 키나아제는 또한 대부분의 인간 적인 OSs에서 높게 표현되기 때문에, 이 쥐 모형은 치료를 위한 ErbB 통로 억제제를 시험하기 위하여 이용될 수 있었습니다.
서문
골육종 (OS)은 어린이, 청소년 및 젊은 성인에서 가장 흔한 1 차 적인 뼈 종양입니다. OS의 치료에 가장 최근의 사전은 다중 에이전트 화학 요법이 수술 혼자 에 비해 전반적인 생존을 개선하는 것으로 나타났다 때 1980 년대에 발생1. OS는 빠른 뼈 성장 도중 발전합니다, 일반적으로 대퇴골과 같은 긴 관 뼈에서 생기는, 경골, 및 상완골. 그들은 골연성, 골세포, 또는 주목할만한 periosteal 반응2와혼합 된 외관을 특징으로한다. 화학요법과 외과 절제술은 환자의 65%를 위한 5년 생존을 가진 환자를 위한 결과를 향상할 수있습니다2,3. 불행히도, 전이성 질환을 가진 고급 OS 환자는 20 %의 생존을 가지고 있습니다. OS는 지역적으로 침략하고 폐 또는 그밖 뼈에 주로 전이하고 남성에서 더 널리 퍼집니다. 이 젊은 환자를 위한 가장 강력한 필요는 먼 전이의 생존을 방지하고 제거하는 새로운 치료입니다.
OS 전임상 모델은4,5,6,7및 정형토피OS의 절단을 이용한 사용 가능한 면역능력모델이 거의 개발되었다. 2000년에는 정형소 성 합성 OS 및 절단8을가진 BALB/c 마우스를 사용하여 중요한 모델을 개발하였다. 이 마우스 모델에 비해, 쥐 모델은 유전적 근친교와 10 배 더 큰 동물을 기반으로 몇 가지 장점으로 이어지는. 쥐 UMR106 모델은 세포주9로파생된 스프라그 다울리(SD) 쥐에서 32P유도 OS로부터 개발되었다. 2001년, UMR106-01의 직교 이식은 인간에서 OS와 공통적으로 신속하고 일관된 1차 종양 발달 및 방사선학적, 조직학적 특징을 가진 아티믹 마우스의 이식된 티바이스에서 처음 기술되었다. 폐 전이개발 및 골 미세환경(10)에UMR106의 직교 배치에 의존했다. 2009년, Yu et al.11은 더 큰 수컷 SD 쥐에 UMR106 세포를 사용하여 재현 가능한 직교 대퇴골 OS 쥐 모델을 확립하였다. 절단없이 쥐에서 성공적인 종양 이식 및 폐 전이율은 여기에 제시 된 데이터와 유사했다. 이 연구에서는, 젊은 쥐를 사용하여 모델에 추가 절단이 수행되었다, 이는 1 차 종양 제거의 타이밍이 OS 모델링에 중요하다는 것을 시사, 특히 전이성 진행과 관련된. 이 세련미, 절단 및 생체 내 이미징은 OS에 대한 새로운 약물 평가를 위한 전임상 연구를 위한 이 모델을 향상시킵니다.
프로토콜
쥐와 관련된 모든 절차와 실험은 존스 홉킨스 동물 관리 및 사용위원회에 의해 승인 된 프로토콜에 따라 수행되었다.
1. SD 쥐 OS 세포주 UMR-106 세포 배양 프로토콜
- DMEM에서 세포를 성장, 10% (v/v) FBS, 페니실린 (10 U/mL)-연쇄 절제술 (10 U/mL) 37°C에서 가습 5% CO2 대기. 2-812의구절을 가진 세포를 사용하여 실험을 수행합니다.
2. OS 셀 프로토콜의 내적 주입
참고: 시간 제고 임신 한 SD 쥐는 동물 시설에서 출산하고 3 주에, 쓰레기가 사용됩니다 (UMR 106 세포주는 SD 쥐에 합성되기 때문에, 조사가 필요하지 않습니다).
- 유도
- 중간 크기의 유도 챔버에 쥐를 놓고 2 %-3 %의 이소플루란으로 마취를 유도합니다. 발가락 핀치, 호흡 속도 및 문자에 반사하여 마취의 깊이를 지속적으로 모니터링합니다.
- 코를 노세콘에 삽입합니다. 필요한 경우 테이프로 고정하십시오.
- 오른쪽 다리의 머리카락을 복부까지 제거하고 등쪽 하복부를 클리퍼로 제거하거나 탈필제를 사용하십시오. 쥐를 척추 위치에 놓습니다.
- 수술 부위를 70% 에탄올을 사용하여 무균으로 스크럽하고 클로르헨시딘 아세테이트를 희석하거나 베타딘을 희석시하십시오. 무릎 의 영역 주위에 시작하고 근교와 dismally 모두 원형 모션으로 스크럽. 이 단계를 세 번 반복합니다. 어떤 커튼종양 이식에 사용 되지 않습니다.
- 마취로 인한 각막 탈수를 방지하기 위해 쥐의 양쪽 눈에 눈 윤활제를 적용하십시오. 쥐를 낮은 열 세팅 가열 패드에 놓습니다. 쥐가 정상 체온(37°C)과 정상 호흡속도를 가지고 있는지 확인합니다.
- 외과
- 이소플루란을 ~1.5%-2%에서 켭니다(유지 보수용). 동물이 발가락 핀치 반사의 부족을 통해 마취의 적절한 평면에 있는지 확인합니다. 그렇지 않은 경우 이소플루란 비율을 2.5%로 늘립니다.
- 멸균 바늘(약 22G)을 팁으로부터 10mm로 표시하여 삽입할 깊이를 안내합니다.
- 바늘을 경골 고원의 중간에 구부러진 무릎을 입력하여 경골의 diaphysis에 10mm 아래로 삽입하고, 경질 드릴 과 같은 움직임을 사용하여 diaphysis로 메타피시스를 통해 바늘을 확장합니다. 바늘을 제거합니다.
- 경골에 주입하기 전에 직접 해밀턴 주사기에 셀 서스펜션을로드합니다. 이렇게 하려면 중력으로 세포가 튜브 의 바닥에 정착하게됨에 따라 주사기로 그리기 전에 세포를 부드럽게 섞습니다.
참고: 세포는 조심스럽게 혼합한 후 해밀턴 주사기(100 μL)로 그리기 전에 1.5~2mL 튜브(실온)에 보관할 수 있다. 세포는 이식 절차 동안 2-3 시간 동안 실온에서 보관 할 수 있습니다. 이식 세션 전후에 항상 튜브에서 세포의 세포 생존 가능성을 확인하십시오. Trypan 파란색 제외는 세포 생존 가능성 평가를위한 가장 쉬운 방법입니다. - 뼈가 첫 번째 바늘로 통과되면 세포가 로드된 100 μL 해밀턴 주사기에 부착된 두 번째 바늘(10mm으로 표시된 작은 직경 바늘)을 삽입합니다. 10mm 마크까지 바늘을 동일한 구멍에 삽입하여 다이아피시스로 확장되도록 하십시오.
- PBS에서 75,000개의 OS 세포 현탁액의 20 μL을 부드럽게 방전하여 다이아피증과 골수 캐비티로 배출합니다.
참고 : 바늘이 뼈에 흔들리지 않아야하며 안전하다고 느껴야합니다. 바늘이 쉽게 움직이면 피질이 다이아피시스에서 통과되었을 수 있습니다. 세포의 주입 전에 더 단단한 배치를 얻기 위해 삽입을 다시 반복합니다. - 뼈에서 해밀턴 바늘을 제거합니다.
참고: 혈액이 작은 방울이 형성되면 가벼운 압력을 가하십시오. 천지 부위에 명확한 유체 낙하 형태가 있는 경우, 바늘은 뼈에서 충분히 확장되지 않았을 수 있으며 종양 세포 현탁액은 구멍을 통해 다시 유출되었을 수 있습니다. 노트에 이것을 기록하지만 일반적으로 종양 이식은 성공할 것입니다. 경험을 통해 종양 이식 절차는 쥐 당 5 분정도 소요됩니다. 경험을 통해 뼈에 있는 세포의 종양 이식이 쉬워질 것입니다. 뼈 주위 근육에 세포의 우발적 인 주입, 폐 전이에 필요한 종양 미세 환경으로 이어질 수 없습니다.
- 복구
- 쥐가 규범인지 확인하십시오. 복구를 위해 케이지 아래에 놓인 가열 패드가 있는 새장에 쥐를 놓습니다.
- 완전히 깨어, 모바일, 그리고 잘 호흡 후, Buprenorphine와 쥐를 주입 (1.0-1.2 mg/kg SC).
참고: Buprenorphine에 액세스하려면 수의학 직원을 통해 승인 옵션을 확인하여 주문을 하십시오. - 쥐를 다시 케이지청소로 옮기고 매주 하루에 한 번 모니터링합니다.
3. 측정 및 모니터링
- 종양 크기를 측정 9-10 이식 후 다음 2 일마다 3 주 까지 이식 후 성장 속도를 설정 합니다. 전자 또는 수동 캘리퍼를 사용하여 경골의 최대 직경을 측정합니다. 종양 볼륨을 계산하기 위해 수식을 사용하여 스프레드시트에 데이터를 저장합니다. 기준선으로 모순 (이식되지 않은 경골)을 측정합니다.
참고: 이식된 뒷다리 직경은 종양 크기의 대리로 사용됩니다. 뒷다리는 사지의 두 가지 측정, 복부/등주 및 미디어/측면 측정을 위해 가장 큰 직경의 경골 긴 축에 수직으로 측정됩니다. 추정종양 부피는 포뮬러11:종양 부피(mm3)= 가장 큰 직경(mm) x 가장 작은 직경(mm)2/2에의해 계산된다. - 종양이 가장 큰 차원에서 15mm 또는 3 주 후 종양 이식에 접근할 때 생존 절단 또는 화학 요법 치료를위한 쥐를 고려하십시오. 이 나이에 대부분의 쥐에 있는 약 7-9 mm를 측정하는 반대로 사지.
4. 독소루비신 정맥 투여
- 쥐를 2% 이소플루아네로 마취시합니다. 13에기술된 바와 같이 베타딘과 알코올을 사용하여 세 가지 수술 용 세차로 경정맥위에 피부를 준비한다.
- 주의 깊은 해부에서 오른쪽 또는 왼쪽 경정맥을 시각화합니다. 바늘을 과대 근육에 삽입한 다음 쥐의 머리를 경정맥 루멘으로 직접 삽입하여 경정맥 전방에서 가슴 근육에 시각화됩니다.
- 바늘이 경정맥에 삽입되면, 적절한 삽입을 보장하기 위해 주사기에 혈액을 부드럽게 그립니다. 바늘이 정맥을 통해 있다고 믿을 수 있지만 바늘은 정맥 아래에 있지 않고 루멘에 있지 않습니다. 경정맥이 너무 작아지면 무딘 해부시 주사가 너무 작아져 서 경정맥을 노출하면 주사에 대한 다른 경정맥을 사용하십시오.
- 독소루비신(2 mg/kg)을 100-150 μL의 부피로 1분 이상 천천히 주입한다. 용액은 납품 하는 동안 경정맥에서 정맥으로 시각화될 수 있다.
- 제어 쥐에 정상적인 식염수의 유사한 볼륨을 주입.
- 바늘을 제거하고 멸균 거즈로 정맥에 부드러운 압력을 가하십시오.
- 3-4 상처 클립을 사용하여 피부 절개를 닫습니다. 7-10 일 사후 주입에서 클립을 제거합니다.
참고 : 쥐는 일반적으로 금속 클립을 제거하려고하지 않지만 물고 봉합사를 제거합니다. 경정맥 주사 방법은 혈관 외부에 누출되는 약물이 꼬리 절단을 요구할 수 있는 꼬리괴를 유발하기 때문에 독소루비신에 대한 꼬리 정맥 주사를 사용하는 것이 바람직하다.
5. 뒷다리 절단 프로토콜
- 유도
- 중간 크기의 유도 챔버에 쥐를 놓고 2 %-4 %의 이소플루란으로 마취를 유도합니다. 마취의 깊이를 위해 쥐를 지속적으로 모니터링합니다.
참고: 유도 챔버는 숯 통으로 청소되고 다른 모든 가스는 수술에 사용되는 다운 드래프트 테이블에 의해 제거됩니다. - 코를 노세콘에 삽입합니다. 필요한 경우 테이프로 고정하십시오.
참고: 이 절차는 과도한 휘발성 가스(즉, 이소플루란)를 청소하기 위해 다운 드래프트 테이블에서 수행됩니다. - 오른쪽 다리의 머리카락을 복부까지 제거하고 등쪽 하복부를 클리퍼로 제거하거나 탈필제를 사용하십시오. 쥐를 척추 위치에 놓습니다.
- 수술 부위를 70% 에탄올을 사용하여 무균으로 스크럽하고 클로르헨시딘 아세테이트를 희석하거나 베타딘을 희석시하십시오. 오른쪽 하복부의 엉덩이 관절 바로 위에 피부 부위에 종아리 의 중간에서 수술을위한 피부를 준비합니다. 다리 근위와 탈경 부위를 둘레로 문질러보시면 됩니다. 이 단계를 세 번 반복합니다.
- 쥐의 양쪽 눈에 눈 윤활제를 적용합니다. 쥐에 정상 체온(37°C)과 정상적인 활력 징후가 있는지 확인합니다. 직장 온도 프로브 모니터에 연결된 가열 패드를 사용하여 체온을 모니터링하고 조절합니다.
- 중간 크기의 유도 챔버에 쥐를 놓고 2 %-4 %의 이소플루란으로 마취를 유도합니다. 마취의 깊이를 위해 쥐를 지속적으로 모니터링합니다.
- 외과
- 1.5%-3%(유지보수)로 이소플루란을 켭니다. 발가락 핀치에 대한 반응, 호흡 속도 및 문자에 대한 반응을 포함하여 마취 깊이를 모니터링합니다. 마취의 적절한 평면을 유지하기 위해 필요에 따라 이소플루란의 속도를 조정합니다.
참고: 마취 하에 있는 동안 호흡 속도는 분당 50-100 호흡 사이여야 합니다. 깊고 드물게 호흡은 쥐가 너무 깊이 마취되었다는 것을 나타냅니다. - 멸균 기기 팩과 커튼, 돈 멸균 장갑을 엽니다. 절차 의 기간을 통해 멸균을 유지하기 위해주의하십시오. 필요한 기본 멸균 수술 기구는 메스 블레이드 홀더, 집게, hemostats, 바늘 홀더, 가위 및 상처 클립 applier를 포함한다.
- 멸균 수술 커튼의 통풍구를 통해 쥐의 다리를 당깁니다. 동물이 발가락 핀치 반사를 통해 마취의 적절한 평면에 있는지 확인합니다.
- 메스 블레이드 또는 외과 가위를 사용하여, 할례, 황장 (무릎 관절)에 단지 근위절을 합니다.
- 후드 사지의 복부 내측 표면에 대퇴 동맥과 정맥을 노출하기 위해 거즈 또는 무딘 해부를 사용하여 뒷사지를 데글링합니다.
- 중간 대퇴골 및 과도 한 분리의 수준에서 4-0 흡수 봉합사를 사용하여 혈관을 리게이트.
- 정맥을 염기 적으로 고정하여 근육 해부 중 누출을 줄입니다.
참고: 대퇴동맥혈관 결찰및 근육의 수준으로 대퇴골관절의 수준으로 대퇴양동을 이식한다. - 무딘 해부를 사용하여 측면 바깥쪽 회전으로 엉덩이 관절을 납치합니다.
- 대퇴골의 머리를 찾아 아세타불룸에서 분리하십시오. 남은 조직을 잘라내어 다리에 부착된 다리를 유지합니다.
- 약 6 mg / kg Ropivacaine와 아세타불룸과 sciatic 신경에 스플래시 블록을 제공합니다.
- 간단한 중단 봉합사 (4-0, 흡수 봉합사)를 사용하여 아세타불룸 위에 근육을 닫습니다.
참고: 추가 0.5% 부피바카인 또는 리도카인(0.15-0.2 mg 합계)은 폐쇄된 근육 층(국소 침투/스플래시 블록)을 따라 여러 부위에 주입될 수 있다. - 5-10mm마다 분리된 상처 클립을 사용하여 피부 의 가장자리를 반대하고 닫습니다.
- 1.5%-3%(유지보수)로 이소플루란을 켭니다. 발가락 핀치에 대한 반응, 호흡 속도 및 문자에 대한 반응을 포함하여 마취 깊이를 모니터링합니다. 마취의 적절한 평면을 유지하기 위해 필요에 따라 이소플루란의 속도를 조정합니다.
- 복구
- 케이지 아래에 놓인 가열 패드를 사용하여 열 지지대를 갖춘 깨끗한 복구 케이지에 쥐를 배치합니다.
참고 : 고열증을 방지하기 위해, 가열 패드는 동물과 직접 접촉해서는 안되며 40 ° C를 초과해서는 안됩니다. - 동물이 완전히 회복되고 normothermic (37.5-39 °C)가 될 때까지 동물을 모니터링하십시오.
참고: 동물은 완전히 의식하고 엄격하게 구부러지고 케이지 주위를 쉽게 움직일 때까지 방치해서는 안됩니다. - 완전히 깨어, 모바일, 그리고 잘 호흡 후, Buprenorphine와 쥐를 주입 (1.0-1.2 mg/kg SC).
참고: 마취된 쥐에 부프레노르핀을 주면 회복이 손상될 수 있습니다. - 견갑골 사이에 10mL의 따뜻한 수유 링거 용액을 피하로 관리하십시오.
- 쥐를 깨끗한 케이지로 다시 옮기고 동종으로 재결합합니다.
- 홍반, 화농성 분비물 또는 상처 절개를 포함한 모든 동물을 다음 달 동안 매일 두 번 모니터링하여 필로직기, 구부러진 자세 또는 절개 부위 감염의 징후와 같은 통증과 고통의 징후를 모니터링하십시오.
참고: 현재까지 우리는 어떤 동물에서 수술 후 회복 에 이어 임상 징후 (감염 등)를 관찰하지 않았습니다. 단 한 마리의 쥐만이 봉합사로 변함을 보였고, 그 후 상처 클립은 더 이상 문제 없이 상처를 닫는 데 사용되었습니다. - 실험실 동물 수의사와 협의하여 출판 된 복용량에서 통증의 임상 징후를 제시하는 동물에게 buprenorphine 또는 멜록시캠을 투여하십시오.
- 항생제 (즉, 세팔로스포린)를 실험실 동물 수의사와 협의하여 출판 된 복용량에서 통증의 임상 징후를 제시하는 동물에게 투여하십시오.
참고: 항생제에 반응하지 않는 감염의 표시를 전시하는 진통제 또는 동물로 향상되지 않는 고통 또는 고통의 연장된 표시를 전시하는 어떤 동물든지 인도적으로 안락사될 필요가 있습니다.
- 케이지 아래에 놓인 가열 패드를 사용하여 열 지지대를 갖춘 깨끗한 복구 케이지에 쥐를 배치합니다.
6. 엑스레이를 가진 화상 진찰
- 종양 이식 후, 설치류를 위해 설계된 기계로 X 선을 사용하여 종양 성장을 검출하기 위해 비침습적으로 티바이어스와 폐를 이미지합니다.
- 쥐를 이전에 수행한 것처럼 마취시화합니다.
- 25 kV에서 6s에 대한 3 배율로 이미지를 가져 가라.
- X선 프로세서를 사용하여 필름을 처리합니다. 방사선 사진도 디지털 스캔할 수 있습니다.
7. 부검 절차
- CO2로쥐를 안락사시다. 심장 박동의 부족을 통해 죽음을 확인하고 즉시 혈청 또는 혈장 샘플을 위한 심혼에서 3 mL 혈액을 그립니다.
- 검사를 위해 흉부와 복부를 엽니다.
- 기관을 분리하고 (18 G) 카테터로 캐너레이트합니다. 기관지에서 카테터를 고정하려면 카테터와 함께 두 기관 주변에 실크 봉합사를 묶습니다.
- 주입 카테터를 3 mL 또는 5 mL 주사기에 연결합니다. 포르말린이나 식염수에 주입하여 더 나은 작사 표본을 위해 폐 엽을 부드럽게 팽창시다. 주입시 폐는 퍼프업되어 폐 전이의 더 나은 시각화를 가능하게 합니다.
- 검사, 해부, 모든 선택된 흉부 및 복부 장기 (간, 신장 등)를 무게.
- 조직 병리학에 대한 포르말린의 장기를 고정하거나 드라이 아이스, 2-메틸부탄 또는 액체 질소에 동결하십시오.
- 서양 얼룩을 사용하여 단백질 발현의 평가를 위해, 냉동 조직의 lysates를 합니다. 쥐 조직과 반응하는 항체는상세한 13입니다.
8. 면역 작용화학
- 파라핀에 포함 된 1 차 OS 조직을 처리하고 면역 조직 화학 염색을 위해 그것을 단면.
- 구연산 완충(pH 6.0)을 사용하여 항원분해 후 항원을 회수한다. 내생성 과옥시다아제에 30분 동안 메탄올에서 0.3% H2O2의 인큐베이션을 허용한다.
- 일반 혈청을 사용하여 5 μm 두께의 파라핀 섹션을 차단합니다.
- 4°C에서 하룻밤 사이에 1차 항 CD68 및 CD3 항체(테이블 참조)를 배양한다.
- PBS의 섹션을 헹구고 검출 키트를 사용하여 HRP 폴리머로 배양합니다.
참고: 면역염색은 염색체로서 디아미노벤지딘으로 개발되었습니다.
9. 웨스턴 블로팅
- 표준 젤 전기포고및 서부 블로팅을 수행하기 위해 200-300 μL의 용해완충제(14)에서 UMR-106 세포를 lyse.
- 4%에서 12%의 비스 트리스 젤을 사용하십시오.
- 항-ErbB2, 항-ErbB4, 안티 EGFR, 안티-ERK, β 액틴 또는 항마우스 β2-AR 1차 항체(표 참조) 및 고추냉이 과록시다제-연결된 이차 항체에서 배양한다.
- 화학 발광 기판을 추가합니다. 멤브레인을 X선 필름에 노출시킵니다.
참고: β 액틴 레벨은 로드 컨트롤로 사용됩니다.
결과
면역 능력 SD 근친쥐는 이러한 OS 연구에 사용되며, 이는 그대로 면역 체계를 가진 동물 모델을 제공합니다. 우리는 ATCC에서 UMR106 세포줄을 사용했습니다, SD 쥐에서 처음에 OS에서 격리된 세포에서 개발된. 우리는 SD 쥐에 세포를 이식, 따라서 OS에 대한 동기화 모델을 제공. UMR106 세포는 소아 OS 모델을 시뮬레이션, 3 주 된 남성과 여성 SD 쥐의 경골에 이식된다. 더욱이, 경골 대사/설사로 직접 UMR106 세포의 직교 이식은 관련 종양 미세환경을 제공한다.
종양 세포를 이식할 때, 바늘은 골의 중앙 캐비티로 약 10mm를 연장하는 올바른 각도(뼈 샤프트와 평행)에서 티비알 고원을 통해 올바르게 삽입되어야 한다. 이 절차로, 쥐의 95% (52/55) 무릎에 티바이어스 성향에 종양을 개발. 티비알 주사 경험으로, 쥐의 100%는 종양을 개발했습니다. 절단되지 않은 쥐의 그룹에서, 남성의 평균 종양 볼륨은 504 mm3 에서 3 주에 1195 mm3 5 주 이식 후. 여성의 경우, 종양 볼륨은 3주에서 285mm3, 이식 후 5주에서 495mm3로 평균합니다.
절단(23랫)(그림 2)과 절단이 없는 쥐(29마리)를 포함한 2마리의 쥐 집단을 비교하였다. 두 코호트는 폐에 종양 전이를 검사하기 위해 이식 후 7 주에 안락사되었다. 절단 군(3/23)에서 쥐는 폐 전이를 개발하였다. 이 3개의 쥐는 수술 후 합병증 때문에 수술의 24 시간 안에 정지하거나 안락사되었습니다. 외과 의사가 방법을 배우고 있는 동안 두 마리의 쥐가 장기간 마취로 사망했습니다. 한 쥐는 경멸을 일으켰고 다음 날 안락사되었다. 이 3개의 쥐의 폐는 평가되고 3개의 작은 전이 (>1 mm)는 조직학적으로 찾아냈습니다. 살아남은 20마리의 쥐는 이식 후 7주 동안 폐 전이가 없었습니다. 이것은 3 주 이식 후 절단이 폐 전이를 가진 쥐의 수를 감소시키기에 적당하다는 것을 표시했습니다. 절단 절차가 없는 29마리의 쥐의 두 번째 그룹에서, 26/29마리의 쥐는 이전에 발표된데이터(11)와일치하는 폐 전이가 있었다. 우리는 이 쥐에 있는 전이의 크기 또는 수에 있는 아무 패턴도 보았습니다. 대부분의 쥐에는 부검 중에 쉽게 샘플링된 10개 이상의 심하게 눈에 띄는 2-7mm 직경 전이가 있습니다. 때때로, 쥐는 직경이 10mm까지의 더 큰 전이를 가지고 있었다. 연구 결과에 따르면 10개 이상의 통로 수를 가진 세포가 이식 후 2-3주 일찍 보다 공격적이고 전이된다는 것이 입증되었기 때문에 UMR106 세포를 낮은 통로 번호로 이식하는 것이 중요합니다. 자연에 대 한 이유는 알려져 있지 않습니다 하지만 추측 문화권에 있는 세포 전이 를 선호 하는 돌연변이를 개발할 수 있습니다.
절단 수술 이외에, 방법의 또 다른 구체화는 종양 감시 또는 부검을 위한 엑스레이 화상 진찰을 포함했습니다. 이 방법은 연구원이 마취하에 쥐에 있는 뼈 종양 침공을 확인하는 것을 허용합니다. 평면 방사선 촬영 방법은 최근에 절단 된 사지 또는 포르말린 고정 사지에 사용할 수 있습니다. 이 방법은 빠른 (쥐 당 5 분) 및 저렴 ($2-5/쥐) 계산 단층 촬영에 비해 (CT). 생체 내 모니터링을 위해서는 쥐가 이미징 중에 마취되어야 합니다. 도 3은 이전에 절단된 두 개의 사지의 X선 이미징에 의해 보인 상세한 형태를 보여줍니다. 이 방법은 이러한 종양의 골연및 골세포 성질을 조명합니다. 두 예(흰색 화살표)에서 경골과 비골의 정상적인 골 피질 아키텍처가 중단된 점에 유의하십시오. 도 4는 전이의 유무에 관계없이 폐의 방사선 학적 형태를 보여줍니다. 엑스레이에 의한 화상 진찰은 불필요한 자발적인 죽음을 방지하기 위하여 안락사에 대한 필요인 실험실에 빨리 드러낼 수 있습니다.
폐에 1차 및 전이성 종양은 조직학적으로 골성 및 골성 종양 형태를 모두 나타내는 인간 OS와 유사합니다. 쥐 OS에서, 골성 및 골성 종양 형태는 도 5 및 도 6에서절단 된 사지의 조직 병리학에 의해 확인된다. 이 예에서는 피질 뼈가 존재하지 않으며 인접한 뼈도 피질의 기존 샤프트에 수직으로 지향되는 새로운 직조 뼈(exostoses)에 의해 교체또는 강화된다. 미성숙 골다이드(비정질 외세포 물질)의 섬이 종양 예내에서 나타난다. 추가적으로, 폐 전이의 현미경 형태, 광물화된 뼈를 가진 몇몇 및 종양 혈관 색전증은 도 7에도시된다.
OS를 가진 사지 절단은 쥐에 있는 생존을 증가시킵니다. 쥐는 폐 전이 7 주 이상 이식 후 보관으로 인해 자발적으로 죽을 수 있습니다. 절단의 사용은이 모델에서 표준 또는 표적 암 치료의 추가 조사를 허용 할 수 있습니다. 종양 이식과 절단 사이의 시간을 연장하면 전이 발생률이 증가합니다.
독소루비신은 인간에서 OS를 치료하는 데 사용되는 화학 요법 에이전트입니다. 쥐에서, 독소루비신은 여기에 설명된 바와 같이 경정맥 주사13 또는 카테터15를 통해 주어질 수 있다. 경정맥 주사는 쥐 당 5-10 분 필요 하지만 노출 된 정맥에서 복용량의 배달을 보장. 전반적으로, 경정맥 주사는 쥐 꼬리 정맥 주사에 비해 훨씬 더 재현할 수 있습니다. 꼬리 정맥 주사 중 진피로 독소루비신이 누출되면 꼬리의 괴사가 발생하고 추가 치료를 방지 할 수 있습니다. 본 연구에서는, 5마리의 쥐가 도 5A,B에도시된 바와 같이 종양에서 세포사멸을 조사하기 위해 독소루비신2 mg/kg 용량으로 치료되었고, 48h 포스트 주사를 통해 종양에서 세포사명을 조사하였다.
식염수로 치료된 5개의 대조군 쥐는 또한 쥐 의 면역스테인 면역 세포에 사용될 수 있는 항체를 선택하도록 평가되었다. 여기서, 2개의 항체는 면역 반응성을 위해 시험되었습니다. 면역히스토화학 연구를 위해 종양은 48-72h의 포르말린에 고정된 다음 포르말린에서 발생하는 단백질 교차 연결을 줄이기 위해 70%로 이동하였다. 면역히스토케는 1차 OS 종양에서 면역세포 침투를 위해 수행되었고 대식세포(CD68) 및 T 세포(CD3)를 위해 면역염색하였다. 도 8은 종양 마이크로 환경 내에서 침투하는 면역 세포의 면역 스테인의 두 가지 예를 나타낸다.
치료 개입을 위한 잠재적인 표적은 또한 탐구되었습니다. 종양으로 사지를 절단 한 후, 쥐 OS 샘플은 미래의 단백질 격리를 위해 동결되었다. 이 연구에서, 우리는 UMR106 세포가 ErbB 가족 통로 단백질을 표현한다는 것을 것을을 발견했습니다. UMR106 세포 단백질 리사테에서 수행된 서양 얼룩은 ErbB2, EGFR, ErbB4 및 이러한 경로와 상호 작용하는 기타 단백질의 발현을 입증한다(도9).

그림 1: 종양 이식 바늘이 삽입 된 경골. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

도 2: 양성 절단 시 피부 제거(A), 노출된 대퇴동맥 및 정맥(B), 대퇴골(C)에서 근육이 상승하는 경우, 쥐3주 후 절단 수술(D). 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
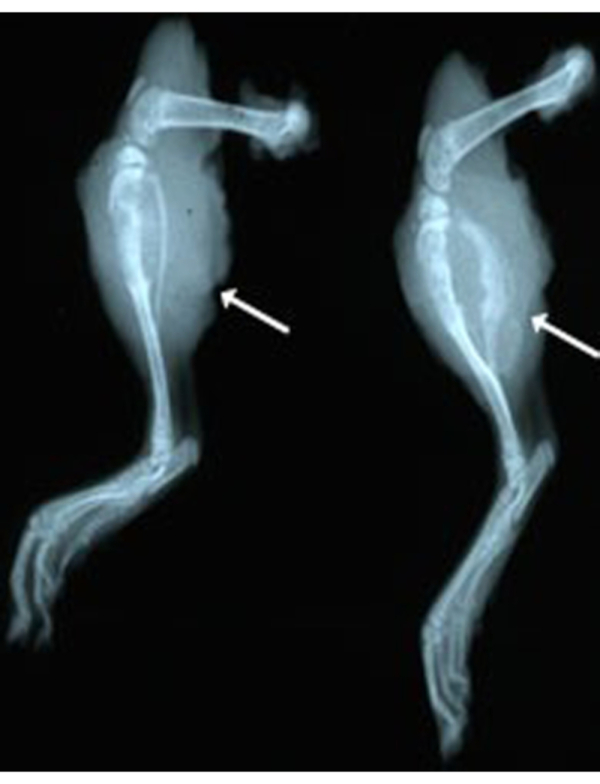
그림 3: OS를 가진 두 마리의 쥐로부터 절단(ex vivo) 후 오른쪽 다리의 엑스레이 방사선 사진. 종양의 골연및 골세포 성질을 유의하십시오. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

도 4: 폐 전이가 없는쥐 폐의 엑스레이 영상. (A). (B)OS 폐 전이. (C)팽창된 폐에서 전이의 총 병리학에 상관 관계가 있습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

도 5: (A)2 mg/kg 독소루비신의 투여 후 경골 종양48h에서 세포사를 나타내는 세포의 90%를 가진 OS의 조직병리학. (B)2mg/kg 독소루비신의 투여 후 48h에서 티비알 1차 OS에서 종양 세포 사멸(arrow). 오른쪽 상단과 왼쪽 모서리에는 실행 가능한 셀이 있습니다. (C)피질 뼈에 OS 침입. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

도 6: (A)골수 세포를 대체하고 경골의 코르티체에 침투한 OS의 조직 병리학. 기존 피질에 수직으로 겹쳐져 있기 때문에 동반된 반응성 새로운 뼈 성장을 주목하십시오. (B)뼈섬에 인접한 OS 종양 세포의 높은 전력 검사. (C)분홍색에서 파란 세포외 매트릭스(osteoid)에 내장된 OS 세포의 높은 전력 검사. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

도 7: (a)경골 종양 이식을 가진 쥐의 다중 폐 전이. (B)혈관 아래 기관지에 인접한 작은 폐 동맥 분지 용기에서 색전으로 종양 OS 세포. (C)일부 폐 전이는 뼈의 섬을 포함하고 다른 전이는 더 세포입니다. (D)미네랄화된 뼈의 섬과 혼합된 OS 세포를 가진 전이의 높은 힘. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 8: (A) CD68 면역염색 대식세포및 (B) 경골에서 OS에서 CD3 양성 세포를 나타내는 면역염색 T 세포의 면역염색 T 세포의 면역염색.이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

도 9: 경골 종양으로부터 UMR106 OS 세포에서 발현된 ErbB 통로 단백질. 1차 종양으로부터의 용해는 ErbB2, EGFR, ErbB4, AKT, ERK1/2 및 β2-아드레진 수용체를 포함하는 ErbB 가족 신호 변환 경로로부터단백질 발현을 검사했다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
토론
OS 티비알 임플란트를 가진 쥐는 이식 후 3 주까지 측정 가능한 종양을 개발합니다. 종양을 가진 사지가 이식 후 3 주 절단되는 경우에, 폐 전이의 부각은 현저하게 감소됩니다. OS는 골연및 골세포학 둘 다입니다. 절단이 없는 쥐는 방사선 촬영또는 부검시 7주 까지 여러 가지 와 가변크기인 폐 전이를 개발합니다. EGFR, ErbB2 및 ErbB4는 인간OS16,17,18과유사한 쥐 UMR106 OS로 표현된다. CD3 T 세포 및 대식세포는 면역히스토화학 방법에 의해 OS에서 쉽게 검출된다. 경정맥 주사는 OS 환자에게 주어지는 약물인 화학요법 독소루비신의 전달을 위해 정맥을 꼬리에 담는 것을 선호한다. 여기에 설명된 방법은 완전한 콕소페모랄 절단입니다. 이 절차는 정제이며 뼈가 절단되어 환자를 위한 그루터기를 떠나는 수술 방법 (대퇴 골 절제술)을 제거하는 종양을 대체하는 것으로 간주 될 수있습니다 8. 연구 결과는 수술 후 고통 및 합병증의 가능성을 감소시키기 위하여 완전한 사지 제거를 건의합니다.
이 프로토콜에는 여러 가지 중요한 단계가 있습니다. 첫째, 종양 세포의 통과를 기록하고 실험에서 실험에 이르는 모델을 일관되게 유지하기 위해 연구를 위해 세포의 더 낮은 통로를 사용하는 것이 중요하다. 오래된 통로 세포는 문화에 있는 시간으로 더 공격적이됩니다. 둘째, 적절한 크기의 바늘과 해밀턴 주사기를 사용하면 매우 작은 부피인 20 μL의 경골세포를 경골에 올바르게 주입하는 데 도움이 되며, 부피는 최적으로 결정되고 누출을 일으키지 않았다. 셋째, 외과 의사는 절차의 역학을 배우기 위해 유사한 노인 쥐에 부검을 할 때 처음에 자진 술을 연습해야합니다. 넷째, 절단의 성공을 위해, 온도 조절을 유지하고 수술 시간을 제한. 숙련 된 외과 의사는 15 분 안에 절단을 완료 할 수 있습니다.
더 큰 보어 바늘이 초기 개구부를 만드는 데 사용되었을 때 경골에 있는 세포의 implantation가 크게 향상된 것을 관찰하였고, 그 다음에 는 더 작은 보어 해밀턴 주사기 바늘의 삽입에 선행하였다. 이것은 시간이 지남에 따라 파손과 둔한에서 해밀턴 주사기를 보호합니다. 해밀턴 주사기는 10 μL의 작은 부피를 가질 수 있습니다. 1 mL 결핵 주사기는 20 μL의 이식에 충분히 정확하지 않을 것입니다. 동일한 해밀턴 주사기는 하루에 이식된 모든 쥐에 사용되었지만 각 쥐의 외과 수술 사이에 세척되었습니다. 해밀턴 주사기 주사기를 오토클레이브하는 것을 피하십시오. 시술이 끝나면 식염수(10회)로 세척한 다음 100% 에탄올(10회)으로 세척한 다음 플런저를 제거하여 보관합니다.
피부와 피하 봉합사는 처음에 절개를 닫는 데 사용되었지만 수술 다음날 한 마리의 쥐가 해독으로 발견되었습니다. 절개를 닫기 위해 상처 클립과 수술 접착제를 사용하면 방법이 향상되었습니다. 이 세련미로, 다른 쥐는 수술 후 합병증이 없었다. X 선에 의한 폐의 방사선 촬영의 포함은 적시에 예기치 않은 죽음을 방지하는 안락사를 허용하는 쥐에 있는 폐 전이를 보여주기 위하여 이 모형을 정제합니다. 엑스레이 심상을 통해 인간 OS와 유사한 이 쥐 의 골성 및 골성 특성을 결정할 수 있습니다.
절단 절차를 수행하기 위해서는 적당한 수준의 외과 적 전문 지식이 필요합니다. 가장 어려운 단계는 콕코페모랄 관절을 찾기 위해 근로로 해부입니다. 이 단계에서는 배율과 좋은 조명이 중요합니다. 외과 전문 지식은 안락사 된 동물에 대한 연습으로 달성 될 수있다. 약 10 마리의 쥐 후, 외과 의사는 마취하에 살아있는 쥐에서 OS로 사지를 절단할 수 있다고 확신해야합니다.
마우스와 쥐에서 육종으로 사지를 제거하는 기존의 방법은 대퇴골뼈와 근육 중간 샤프트를 절단하고 그루터기8을떠나경골을 제거하는 데 기초한다. 비록, 이것은 일부 조사에 대 한 유용 할 수 있습니다., 이 연구에서, 완전 한 다리 제거를 시도 했다. 절차는 만족스럽지 않다는 것을 것을을 발견하고 수술 후 합병증을 제안하지 않았습니다. 뒷다리 그루터기를 가진 쥐에서는 수술 후 피부, 근육 또는 신경 통증이 더 있을 수 있습니다. 그루터기를 떠나, 쥐는 주위에 도달하고 수술 사이트에 액세스 할 수 있습니다. 쥐는 절단 후 아주 잘하고 하나의 뒷다리와 케이지에서 잘 절단.
전체 사지 절단의 장점은 쥐에 대한 너무 크고 고통스러운되기 전에 기본 종양을 제거하는 것을 포함한다. 중요한 것은, 1 차적인 종양의 제거는 폐에 1 차적인 종양 전이를 통제하는 것을 도울 것입니다. 절단을 가진 쥐는 폐 또는 그밖 뼈의 모세 혈관에 있는 혈액 또는 micrometastases에 있는 순환 종양 세포에 새로운 치료의 효험을 시험하기 위하여 더 공부될 수 있습니다.
OS 및 기타 육종, 특히 전이성 진행에 대한 약물 활동이 있는 치료제를 위한 새로운 암 치료제 의 개발에 대한 상당한 필요성이 있습니다. 다른 암을 위해 개발된 새로운 치료법과 비교하면, OS에 대한 치료법은 불행히도 수십 년 동안 진행되지 않았습니다. 이 문제에 대응하여 OS 및 전이의 주요 리더 및 전문가 회의가 소집되어 OS 약물 개발 개선에 대한가이드라인을 개발했습니다 19. 패널의 제안에 따라, 연구는 쥐 전 임상 모델, OS의 덜 알려진 모델을 개선하기 위해 밖으로 설정되었다. 요약하자면, 절단 및 화상 진찰은 육종 연구 지역 사회에 의해 추가 사용을 위한 쥐 전 임상 모형을 정제합니다. 절단 절차는 마이크로 메타제또는 휴면 종양에 새로운 처리의 효험의 평가를 가능하게 하거나 더 나은 장수를 가진 모형을 가진 처리의 독성을 위해 시험하는 것을 가능하게 하는 다개월 동안 향상된 참을성 있는 생존을 허용할 것입니다.
요약하면, 우리는이 OS 모델의 장점을 제공합니다. 면역 능력 SD 근친쥐는 SD 쥐 OS로부터 분리된 이식된 UMR106 OS 세포주와 함께 합성 모델을 제공하는 데 사용됩니다. 1차 및 전이성 종양은 인간에 있는 OS와 조직학적으로 유사합니다. 청소년 남성과 여성 쥐는 소아 육종을 모델링 하는 UMR106 종양 이식 연구에 사용 됩니다. 이식된 세포의 직교 배치는 관련 종양 미세 환경에 대한 경골내로 직접 수행된다. 1 차적인 종양은 폐와 전이에 전이엑스레이를 가진 X 선 방법을 가진 생체 내 화상 진찰에 의해 감시될 수 있습니다. 쥐 OS는 ErbB2와 같은 인간 OS와 공통적으로 단백질을 표현합니다. 개 OS에 비해 쥐 모델은 더 많은 수의 동물을 동시에 사용할 수 있습니다. 쥐는 정골 주사, 수술, 화상 진찰, 혈액 무승부 및 생검의 용이성을 위해 마우스 보다는 10 시간 더 큽습니다. 쥐의 장수는 절단으로 더 보장되며,이 모델은 미세 메타 아스타제 또는 휴면 종양에 대한 치료의 효능의 평가를 가능하게 향상 된 환자 생존을 가능하게 하는 neoadjuvant 치료, 절단 및 보조 요법을 결합 할 수 있습니다. 오프 표적 독성 평가는 또한 쥐가 독소루비신과 같은 암 치료로 치료될 수 있고 OS의 독소루비신 유도심장 독성 또는 재발을 위해 장기적으로 모니터링될 수 있는 이 모형에서 평가될 수 있다. 이를 통해 OS를 갖춘 모델에서 심장 보호 에이전트를 테스트할 수 있습니다.
공개
선언할 공개가 없습니다.
감사의 말
국립 암 연구소를 통해 NIH 자금 지원, 보조금 # CA228582. 이시야마 순은 현재 도레이 메디컬(주)으로부터 보조금을 받고 있습니다.
자료
| Name | Company | Catalog Number | Comments |
| AKT | Cell Signaling TECHNOLOGY | 4685S | |
| absorbable suture | Ethicon | J214H | |
| β-actin | SANTA CRUZ BIOTECHNOLOGY | sc-47778 | |
| β2-AR antibody | SANTA CRUZ BIOTECHNOLOGY | sc-569 | replaced by β2-AR (E-3): sc-271322 |
| Bis–Tris gels | Thermo Fisher | NP0321PK2 | |
| Buprenorphine SR Lab | ZooPharm | IZ-70000-201908 | |
| CD3 antibody | Dako | #A0452 | |
| CD68 antibody | eBioscience | #14-0688-82 | |
| Chemiluminescent substrate | cytiva | RPN2232 | |
| CL-Xposure film | Thermo Fisher | 34089 | |
| Complete Anesthesia System | EVETEQUIP | 922120 | |
| diaminobenzidine | VECTOR LABORATORIES | SK-4100 | |
| Doxorubicin | Actavis | NDC 45963-733-60 | |
| EGFR antibody | SANTA CRUZ BIOTECHNOLOGY | sc-03 | replaced by EGFR (A-10): sc-373746 |
| ERBB2 antibody | SANTA CRUZ BIOTECHNOLOGY | sc-284 | replaced by Neu (3B5): sc-33684 |
| ERBB4 antibody | SANTA CRUZ BIOTECHNOLOGY | sc-283 | replaced by ErbB4 (C-7): sc-8050 |
| ERK antibody | SANTA CRUZ BIOTECHNOLOGY | sc-514302 | |
| eye lubricant | PHARMADERM | NDC 0462-0211-38 | |
| Hamilton syringe (100 µL) | Hamilton | Model 1710 SN SYR | |
| horseradish peroxidase-linked secondary antibody | cytiva | NA934 | |
| HRP polymer detection kit | VECTOR LABORATORIES | MP-7401 | |
| HRP polymer detection kit | VECTOR LABORATORIES | MP-7402 | |
| isoflurane | BUTLER SCHEIN | NDC 11695-6776-2 | |
| isoflurane vaporizer | EVETEQUIP | 911103 | |
| UMR-106 cell | ATCC | CRL-1661 | |
| X-ray | Faxitron | UltraFocus | |
| X-ray processor | Hope X-Ray Peoducts Inc | MicroMax X-ray Processor | Hope Processors are not available in USA anymore |
| wound clips | BECTON DICKINSON | 427631 |
참고문헌
- Link, M. P., et al. The effect of adjuvant chemotherapy on relapse-free survival in patients with osteosarcoma of the extremity. New England Journal of Medicine. 314 (25), 1600-1606 (1986).
- Bielack, S. S., et al. Prognostic factors in high-grade osteosarcoma of the extremities or trunk: an analysis of 1,702 patients treated on neoadjuvant cooperative osteosarcoma study group protocols. Journal of Clinical Oncology. 20 (3), 776-790 (2002).
- Botter, S. M., Neri, D., Fuchs, B. Recent advances in osteosarcoma. Current Opinion in Pharmacology. 16, 15-23 (2014).
- Ek, E. T. H., Dass, C. R., Choong, P. F. M. Commonly used mouse models of osteosarcoma. Critical Reviews in Oncology Hematology. 60 (1), 1-8 (2006).
- Guijarro, M. V., Ghivizzani, S. C., Gibbs, C. P. Animal models in osteosarcoma. Frontiers Oncology. 4, 189 (2014).
- Janeway, K. A., Walkley, C. R. Modeling human osteosarcoma in the mouse: From bedside to bench. Bone. 47 (5), 859-865 (2010).
- Mohseny, A. B., Hogendoorn, P. C., Cleton-Jansen, A. M. Osteosarcoma models: from cell lines to zebrafish. Sarcoma. 2012, 417271 (2012).
- Khanna, C., et al. An orthotopic model of murine osteosarcoma with clonally related variants differing in pulmonary metastatic potential. Clinical & Experimental Metastasis. 18 (3), 261-271 (2000).
- Martin, T. J., et al. Parathyroid hormone-responsive adenylate cyclase in induced transplantable osteogenic rat sarcoma. Nature. 260 (5550), 436-438 (1976).
- Fisher, J. L., Mackie, P. S., Howard, M. L., Zhou, H., Choong, P. F. The expression of the urokinase plasminogen activator system in metastatic murine osteosarcoma: an in vivo mouse model. Clinical Cancer Research. 7 (6), 1654-1660 (2001).
- Yu, Z., et al. Establishment of reproducible osteosarcoma rat model using orthotopic implantation technique. Oncology Reports. 21 (5), 1175-1180 (2009).
- Zhang, P., et al. Homologous mesenchymal stem cells promote the emergence and growth of pulmonary metastases of the rat osteosarcoma cell line UMR-106. Oncology Letters. 8 (1), 127-132 (2014).
- Gabrielson, K., et al. Heat shock protein 90 and ErbB2 in the cardiac response to doxorubicin injury. Cancer Research. 67 (4), 1436-1441 (2007).
- Sysa-Shah, P., et al. Bidirectional cross-regulation between ErbB2 and β-adrenergic signalling pathways. Cardiovascular Research. 109 (3), 358-373 (2016).
- Wachtman, L. M., Browning, M. D., Bedja, D., Pin, S., Gabrielson, K. L. Validation of the use of long-term indwelling jugular catheters in a rat model of cardiotoxicity. Journal of American Association Laboratory Animal Science. 45, 55-64 (2006).
- Abdou, A. G., et al. The Prognostic role of Ezrin and HER2/neu expression in osteosarcoma. Applied Immunohistochemistry & Molecular Morphology. 24 (5), 355-363 (2016).
- Hughes, D. P., Thomas, D. G., Giordano, T. J., McDonagh, K. T., Baker, L. H. Essential erbB family phosphorylation in osteosarcoma as a target for CI-1033 inhibition. Pediatric Blood & Cancer. 46 (5), 614-623 (2006).
- Wen, Y. H., et al. Epidermal growth factor receptor in osteosarcoma: expression and mutational analysis. Human Pathology. 38 (8), 1184-1191 (2007).
- Khanna, C., et al. Toward a drug development path that targets metastatic progression in osteosarcoma. Clinical Cancer Research. 20 (16), 4200-4209 (2014).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유