Method Article
압력 과부하의 쥐 모델은 오버트 수축기 심부전과 반대로 적당한 리모델링 및 수축기 기능 장애를 유도했습니다.
요약
우리는 리모델링 과정의 개시에 관여하는 신호 변환 경로가 활성화되는 압력 과부하 유도 적당한 리모델링 및 초기 수축기 기능 장애의 쥐 모델의 생성을 설명합니다. 이 동물 모델은 심부전을 위한 초기 치료 반대로 리모델링 전략을 적용하기 위한 분자 표적을 확인하는 것을 도울 것입니다.
초록
심근 경색, 장기간 고혈압 또는 심장 독성 제와 같은 부상에 대한 응답으로 심장은 처음에는 신호 전달 경로의 활성화를 통해 적응하여 단기적으로 심장 근세포 손실 및 벽 스트레스 의 증가를 중화시화합니다. 그러나, 이러한 경로의 장기간 된 활성화 는 심장 리모델링의 개시 및 전파 좌심실 기하학의 변화로 이어지는 해로운 되 고 좌심 실 볼륨증가; 수축기 심부전 (HF)을 가진 환자에서 보인 표현형. 여기서, 우리는 2mm2의내부 영역을 가진 혈관 클립을 통해 대동맥 밴딩(AAB)을 상승시킴으로써 적당한 리모델링 및 초기 수축기 기능 장애(MOD)를 유도하는 압력 과부하의 래트 모델의 생성을 설명한다. 수술은 200 g 의 스프라그 -Dawley 쥐에서 수행됩니다. MOD HF 표현형은 AAB 후에 8-12 주에서 발전하고 심초음파를 통해 비침습적으로 특징입니다. 이전 연구는 인간 수축기 HF에서 본 것을 모방하는 MOD HF 표현형에서 단백질의 신호 트랜스덕션 경로 및 변경된 유전자 발현 및 번역 후 변형의 활성화를 제안합니다. 따라서, MOD HF 표현형을 HF에서 잠재적인 치료 적 리모델링 표적을 식별하고 테스트하기 위한 번역 연구에 적합한 모델로 삼는다. MOD HF 표현형의 장점은 오버트 수축기 HF 표현형에 비해 초기 리모델링 과정 및 치료 적 개입의 조기 적용에 관여하는 분자 표적의 식별을 허용한다는 것입니다. MOD HF 표현형의 한계는 인간에서 수축기 HF로 이어지는 질병의 스펙트럼을 모방하지 않을 수 있다는 것입니다. 더욱이, AAB 수술은 원하는 HF 표현형을 개발하는 수술 된 쥐의 단지 20 %와 높은 사망률및 실패율과 연관되기 때문에, 만드는 도전적인 표현형이다.
서문
심부전(HF)은 널리 퍼지는 질병이며 높은 사망률 및 사망률1과관련이 있습니다. 오름차순 또는 횡대동맥 밴딩에 의해 생성 된 HF의 설치류 압력 과부하 (PO) 모델은 일반적으로 HF로 이어지는 분자 메커니즘을 탐구하고 HF에서 잠재적 인 새로운 치료 목표를 테스트하는 데 사용됩니다. 그(것)들은 또한 머리말을 붙인 조직 고혈압 또는 가혹한 대동맥 협착증에 인간 HF 이차에서 보인 변경을 모방합니다. PO에 이어, 좌심실(LV) 벽은 점차 두께가 증가하며, 동심 LV 비대(LVH)로 알려진 공정은 LV 벽 응력의 증가를 보상하고 적응시킨다. 그러나, 이것은 칼슘 사이클링 및 항상성, 대사 및 세포 외 매트릭스 리모델링 및 유전자 발현의 변화뿐만 아니라 향상된 세포 사멸 및 자가 포식2,,3,,4,,5,,6의여러 가지 적응 장애 신호 경로의 활성화와 관련이 있다. 이 분자 변경은 심근 개조의 개시 그리고 전파를 위한 트리거를 구성하고 보상된 HF 표현형으로 전환합니다.
근친 설치류 균주의 사용과 클립 크기 및 수술 기술의 표준화에도 불구하고, 대동맥 밴딩 모델7,,8,,9에서LV 챔버 구조 및 기능의 엄청난 현상형 가변성이 있다. 쥐, 스프라그-다울리 균주에서 PO 후 발생하는 표현형 가변성은 다른곳에서 10,,11에기재되어 있다. 그 중, 2개의 HF 표현형은 고조된 산화 긴장의 상태로 이끌어 내는 신호 transduction 통로의 심근 개조 그리고 활성화의 기록으로 발생합니다. 이는 대사 리모델링, 유전자 발현 및 단백질의 번역 후 변형의 변화와 관련이 있으며, 리모델링 과정10,,12에서모두 역할을 한다. 첫 번째는 적당한 리모델링 및 초기 수축기 기능 장애 (MOD)의 표현형이며 두 번째는 과장된 수축기 HF (HFrEF)의 표현형입니다.
HF의 PO 모델은 PO-유도된 원주 및 자오선 벽 응력이 심근의 모든 세그먼트에 균일하게 분포되기 때문에 HF의 심근 경색(MI) 모델보다 유리하다. 그러나, 두 모델 모두 HF의 MI 모델에서 관찰되는 흉벽 및 주변 조직에 대한 유착뿐만 아니라 경색부위(15)에서 강렬한 염증 및 흉터와 함께 PO10,,11 및 경색 크기13,,14의 중증도에서 의 가변성을 앓고 있다. 더욱이, 랫트 PO 유도 HF 모델은 MOD HF 표현형10을개발하는 조작된 랫트의 20%만이 높은 사망률 및고장률(10)과연관되기 때문에 생성하기가 어렵다.
MOD는 매력적인 HF 표현형이며, 특히 미토콘드리아 역학 및 기능, 심근 대사, 칼슘 사이클링 및 세포 외 매트릭스의 교란과 관련된 경우 심근 변환 경로의 조기 타겟팅을 허용하기 때문에 전통적으로 생성 된 HFrEF 표현형의 진화를 구성합니다. 이러한 병리생리학적 과정은 MOD HF 표현형11에서매우 분명하다. 이 원고에서는 MOD 및 HFrEF 표현형을 만드는 방법을 설명하고 오름차순 대동맥 밴딩(AAB) 절차를 수행하는 동안 함정을 해결합니다. 우리는 또한 심초음파에 의해 가장 잘 특성화하는 방법에 정교, 두 HF 표현형, MOD 와 HFrEF, 심각한 PO를 개발하지 못하는 다른 표현형에서 그들을 구별하는 방법 또는 심각한 PO와 동심 리모델링을 개발하지만 상당한 편심 리모델링없이.
프로토콜
여기에 설명된 모든 방법과 절차는 툴레인 대학 의과 대학의 기관 동물 관리 및 사용 위원회 (IACUC)에 의해 승인되었습니다.
1. AAB 모델 생성을위한 도구 및 악기
- 70% 이소프로필 알코올 및 포비도 요오드와 같은 소독제를 구하십시오.
- 마취를 위한 케타민과 자일라진을 얻고 진통을 위한 부프레노르핀을 얻으시면 됩니다.
- 18 인치 x 30 인치의 치수로 가열 패드와 무거운 흡수성 일회용 언더 패드를 구하십시오.
- 100% 면 꼬기 롤, 테이프, 이발기를 구하십시오.
- 20cm × 25cm 플라스틱 보드, 두께 범위는 3 ~ 5mm입니다.
- Z-LITE 광섬유 조명을 구합니다.
- 작은 동물용 기계식 인공호흡기(예: SAR-830/AP)를 구하십시오.
- 2-0 및 3-0 비릴 테이퍼 봉합사 및 나일론 3-0 모로필라멘트 봉합사, 멸균 거즈 패드 및 멸균 엑스트라 대형 면 팁 및 멸균 장갑을 획득하십시오.
- 삽관에 대한 16 G 각옥을 가져옵니다.
- 다음 수술 도구를 구입하십시오.
- Weck 스테인레스 스틸 헤모클립 결찰 및 스테인리스 스틸 결찰 클립을 구하십시오.
- 경화 된 미세 홍채 가위를 구하십시오.
- 흡착집 획득.
- 구부러진 그레이페 집게 두 개를 구합니다.
- 할스테드 모기 지혈대 직선 집게를 얻으라.
- 마요 히가르 바늘 홀더를 구하십시오.
- 무딘 이빨로 Alm 가슴 리트랙터를 얻으소.
- 오토클레이브와 비드 멸균기를 활용하고 구합니다.
2. 상승 대동맥 밴딩 수술
- 75-100 mg/kg 케타민과 10 mg/kg 자일라진을 혼합하여 복강 내 주사로 동물을 마취시다.
참고: 동물이 완전히 진정되고 부록이 될 수 있도록 몇 분 간 기다립니다. 마취 용량이 충분하지 않고 동물이 여전히 케이지에서 이동하는 경우, 충분한 시간을 허용 한 후 동일한 마취 용량으로 동물을 다시 주입, 후속 주사 사이에 약 5-10 분. 대부분의 동물은 깊은 감미와 마취를 달성하기 위해 1-2 주사가 필요합니다. - 오른쪽 겨드랑이 아래 오른쪽 측면 흉부 부위에있는 수술 부위의 머리카락을 면도하십시오.
- 플라스틱 보드에 네 개의 팔다리를 모두 부드럽게 테이핑하여 동물을 안정시십시오. 그런 다음 16 G angiocath로 내측 관착을 수행합니다. 동물이 성공적으로 삽관 된 후, 50 사이클 / 분및 FiO2에서 2mL의 조수 부피와 21 %의 기계 환기를 시작합니다. 각 호흡과 가슴 벽에 대칭 상승을 찾습니다.
- 동물을 천천히 돌려 왼쪽 측면에 누른 다음 꼬리를 U 자형 방식으로 구부린 다음 플라스틱 보드에 부드럽게 테이핑하여 안정화하십시오. 그런 다음 povidone-요오드의 국소 적용으로 면도 부위를 소독하십시오.
- 절개를 하기 전에 선제 진통으로 1-2 % 리도카인 / 0.25-0.5 % 부피바카인의 부피에 의해 50/50 혼합으로 절개 부위에 피부에 침투하십시오.
- 오른쪽 겨드랑이 아래 오른쪽 겨드랑이 영역 1cm에서 오른쪽 수평 피부 절개를 수행, 1-2 센티미터 길이. 그런 다음 흉부 흉곽 케이지에 도달 할 때까지 흉부 근육 층을 해부하십시오. 2nd와 3rd 흉곽 사이에 1cm 흉부 절제술을 합니다.
- 가슴의 근육 층을 해부하는 동안, 조심하고 오른쪽 겨드랑이 아래 실행 오른쪽 겨드랑이 동맥의 부상을 방지 할 수 있습니다.
참고 : 1st와 2nd 갈비뼈 사이에 수행 된 흉부 절제술은 오름차순 대동맥 대신 오른쪽 brachiocephalic 동맥을 밴딩의 위험을 수반합니다. 3rd와 네 번째 갈비뼈 사이의 흉부 절제술은 오름차순 대원을 시각화하고 밴드화하기 어렵게 만듭니다.
참고 : 흉부 절제술을 흉골쪽으로 너무 내디엄으로 확장하여 오른쪽 내부 유방 동맥을 해부하고 손상시키지 않도록하십시오.
- 가슴의 근육 층을 해부하는 동안, 조심하고 오른쪽 겨드랑이 아래 실행 오른쪽 겨드랑이 동맥의 부상을 방지 할 수 있습니다.
- 흉선의 두 엽을 부드럽게 해부하고 옆으로 밀어 넣습니다. 그런 다음 오름차순 대동맥을 식별하고 곡선 그레페 집게를 통해 무딘 해부에 의해 우수한 정맥에서 분리.
참고 : 흉선의 중요한 조작은 부어 렌더링하고 상승 대동맥을 시각화하기 어렵게.- 부상이나 치명적인 우수한 정맥의 파열을 방지하기 위해 여분의주의 대동맥에서 우수한 정맥 카바를 해부. 이것은 절차의 까다로운 부분이 될 수 있으며, 심지어 대부분의 경험이 풍부한 손에 수시로 일어날 것으로 예상된다, 하지만 종종 초보자와 학습자와.
- 구부러진 Graefe 집게로 오름차순 대동맥을 부드럽게 들어 올리고 오름차순 대동맥 주위에 혈관 클립을 놓습니다.
- 플라스틱 프리 컷 7"조각을 통해 혈관 혈장 결찰 도구를 조정하여 원하는 HF 모델이 원하는 HF 모델에 따라 1.5 mm2 또는 2 mm2의원하는 내부 영역의 혈관 클립을 얻습니다.
- 비릴 2-0 모노필라멘트 봉합사를 통해 흉부 봉합사. 그런 다음 3-0 Vicryl 테이퍼 봉합사를 통해 가슴의 근육 층을 봉합하십시오. 그런 다음 나일론 3-0 모노필라멘트 봉합사를 통해 피부 절개를 봉합합니다.
- 수술 후 48-72시간 동안 진통역할을 하는 수술 이완료 후 다음 약물의 조합을 투여: 1) 부프레노르핀 0.01-0.05 mg/kg 피하 모든 8-12시간, 2) 멜록시캄 2 mg/kg 피하 12시간마다, 3) 심한 통증에 필요한 경우 2-4h마다 2.5 mg/kg의 모르핀을 피하로 제거합니다.
참고: 동물을 방치하여 정기적인 모니터링 하에 가열 패드에서 회복하십시오. 일단 동물이 마취에서 회복의 징후를 보여주면 (2 분 이상 부속 근육을 헐떡이거나 사용하지 않고 자발적으로 숨을 쉴 수 있으며 좋은 반사 신경, 빨간색 및 따뜻한 사지가 있음) 동물을 발굴하고 케이지로 되돌려 줍니다.
3. 심초음파
- 80-100 mg /kg 케타민의 복강 내 주사로 동물을 진정시. 좋은 품질의 에코 이미지를 적절하게 수집하기 위해 적절한 완화를 보장합니다.
참고: 마취제로서 이소플루란을 사용하는 것은 심장 우울기 효과, 특히 심한 압력 과부하의 설정에서 권장되지 않으며 동물이 마취를 해제하면 해결 LV 팽창 및 수축기 기능 장애의 잘못된 인상을 줄 수 있습니다.- HFrEF 표현형을 개발했다는 의심으로 호흡 곤란과 빈시피닉을 보이는 동물에서 케타민 투여량의 절반 또는 3분의 1을 주의해야 합니다.
- 완전히 진정 된 동물에서 가슴의 머리카락을 앞쪽으로 면도하십시오.
- 동물을 등에 눕게 하고 플라스틱 판에 안정시다.
- 유두 근육 의 수준에서 2D 파라스테날 긴 축 및 2D 파라스테날 짧은 축 뷰 클립을 획득합니다. 또한 유두 근육 의 수준에서 짧은 파라스테른 축 보기에서 M 모드 이미지를 얻어 LV 단막 및 말단 수축기 직경뿐만 아니라 LV 경각형 및 말단 수축기 직경의 LV 격막 및 후방 벽 두께를 측정합니다.
- LV 크기 및 기능을 적절하게 평가할 수 있도록 분당 370-420비트의 심박수로 이미지 또는 클립을 수집합니다. 낮은 심박수에서 이미지를 획득하면 우울한 LV 기능 및 LV 팽창에 대한 잘못된 인상을 초래할 수 있습니다.
참고: 단축된 2D 긴 축 뷰 이미지/클립을 수집하면 잘못된 측정이 가능합니다. 품질 관리를 위해 LV 정점과 대동맥 승모각이 동일한 평면 절단 내에서 시각화되어 있는지 확인하십시오. - 중간 유두 근육의 수준에서 2D 짧은 파라스테날 축 보기 이미지/클립을 수집합니다. 이것은 연구 기간 내내 동물을 따르는 동안 신뢰할 수있는 직렬 및 후속 LV 측정을 얻기 위한 참조로 작용할 것입니다.
- LV 크기 및 기능을 적절하게 평가할 수 있도록 분당 370-420비트의 심박수로 이미지 또는 클립을 수집합니다. 낮은 심박수에서 이미지를 획득하면 우울한 LV 기능 및 LV 팽창에 대한 잘못된 인상을 초래할 수 있습니다.
- 대동맥 판막 의 수준에서 긴 파라스테날 축 뷰에서 M 모드 이미지를 얻어 끝 시스톨에서 좌측 심방(LA) 직경에 대한 상대 대동맥을 평가합니다.
참고: MOD 및 HFrEF 표현형을 가진 동물은 HFrEF 표현형10에서MOD HF 표현형및 ≥1.5에서 ≥1.25 및 <1.5인 LA/Ao 비율을 가진 LA 팽창의 증거를 보여주어야 합니다.
결과
AAB 다음 8-12 주를 개발하는 HF 표현형의 특성화는 심초음파를 통해 쉽게 수행 될 수 있습니다. Sham, 주 3 포스트 AAB, MOD 및 HFrEF 표현형의 대표적인 M 모드 이미지는 그림 1A에제시되어 있습니다. 도 1B 및 도 1C는 각각 MOD HF 표현형 및 HFrEF 표현형의 생성을 위한 혈관 클립 크기를 나타내고 있다. LV 끝 확장기 (LVEDV) 및 끝 수축기 (LVESV) 볼륨은 영역 길이 방법의 공식을 사용하여 계산 할 수 있습니다 : V = 5 / 6 × A × L, V는 ml의 볼륨입니다; A는 LV 캐비티의 단면적을cm2로,디아스톨(Ad)과 실세포(As)에서 중간 유두 근육의 수준에서 짧은 파라스테날 축 뷰로부터 얻어진다; 및 L은 긴 내분비 LV 정점으로부터 디아스톨(Ld) 및 시스톨(Ls)의 승모판 대동맥 접합까지의 거리로서 긴 파라스테날 축 뷰로부터 측정된 CMLV 캐비티의 길이이다. 대표적인 2D 긴 파라스테날 축 및 짧은 파라스테날 축 심초음파 이미지는 Ld, Ls, Ad 및 As를 측정하는 방법에 대한 예와 함께, Sham 및 MOD HF 표현형은 도 2에제시된다. MOD HF 표현형의 LVEDV는 일반적으로 600- 700 μL 사이의 범위이며, LVEDV가 700 μL 보다 크고 최대 1000 μL을 갖는 동물은 거의 없습니다. 동안, MOD 표현형의 LVESV 범위는 120 - 160 μL 사이이다(표1). 도 2에제시된 2D 짧은 파라스테날 축 뷰 심초음파 이미지로부터, 하나는 SHAM에 비해 MOD 표현형에서 LVH의 정도를 이해할 수 있었다. Sham, 주 3 포스트 AAB, MOD 및 HFrEF 표현형의 대표적인 압력 볼륨 루프 추적은 그림 3에제시되어 있습니다. LV 최대 압력은 적어도 200 mmHg, 심지어 주에 3 포스트 AAB, 그리고 주8 포스트 AAB에서 더 증가 동물과 대불의 성장과 오름차순에서 고정 생성 협착 사이의 불일치로 인해. AAB 후 3주차에 있는 동물들은 샴에 비해 LVEDV와 LVESV를 왼쪽으로 이동하여 완전히 보상됩니다. 진보적인 편심 비대 및 리모델링으로, 주 3 포스트 AAB에 비해 MOD 및 HFrEF 표현형에서 오른쪽으로 LVEDV와 LVESV의 변화가 있다. 하나는 또한 MOD 표현형에 있는 LVESV에 있는 중요한 증가 및 HFrEF 표현형에 있는 LVESV에 있는 심오한 증가를 이해할 수 있었습니다, 이는 MOD와 HFrEF 표현형에 있는 유의하고 심오한 감소를 반영하는, 각각 3 주 후 AAB에 비해. 더욱이, AAB 후 3주차에 LVEF의 현저한 증가와 Sham에 비해 HFrEF 표현형에서 LVEF의 현저한 감소를 이해할 수 있었다.
랫트 PO 유도 HF 모델은 높은 사망률 및 고장률과 연관된다. AAB를 겪는 쥐의 약 20%만이 내부 직경에서 2 mm2mm의 혈관 클립을 사용하여 MOD HF 표현형을 개발하기 위해 전이됩니다. 실패한 표현형의 대표적인 M 모드 이미지는 그림 4에제시되어 있습니다. 도 4A는 AAB 후 8주차에 LVH를 개발하지 않았고, LVH(sham-like)의 완전한 회귀로 PO를 완전히 상실했거나, 8주 후 AAB에서 LVH 및 PO의 가변 정도를 가변하여 경미한 중등도 LVH 표현형을 유발하는 동물의 대표적인 M-모드 이미지를 나타내고 있다. 두 번째 실패한 표현형 그룹은 심술한PO(LV 최대 압력 >200 mmHg)를 가진 동물의 대표적인 M 모드 이미지와 편심 리모델링, 동심 리모델링(CR) 그룹 또는 마일드(MILD group) 편심 리모델링의 증거없이 보정된 심한 LVH를 보여주는 그림 4B에 제시된다. sham, 실패 및 성공/원하는 표현형의 심초음파 및 혈역학 데이터는 그림 5 및 표 1에제시되어 있습니다. 동물이 보상 된 표현형에서 더 편심 및 리모델링 표현형으로 전환함에 따라 심장 무게와 LV 무게의 점진적 증가를 주목하십시오. 또한, LVESV의 기하급수적 증가와 동물이 보상된 동심 리모델링에서 보상된 편심 리모델링 표현형으로 전환함에 따라 LVEF의 감소가 있습니다. 특히 관심있는 것은 MOD와 HFrEF HF 표현형 모두 종말 확장기 압력 부피 관계의 강성 계수 β에 의해 측정된 것과 유사한 수준의 심근 강성을 가지는 것입니다(EDPVR(mmHg/μL))는 다른 모든 표현형에 비해 동물이 편심형으로 전환함에 따라 LV 효율이 점진적으로 감소하는 반면, 더 많은 편심형으로 전환됨에 따라 LV효율가 점진적으로 감소하는 것입니다. LV 효율은 동맥 엘라스테스(EA)로 나눈 말단 수축기 압력 부피 관계(ESPVR)로부터 계산됩니다. MOD와 HFrEF 표현형과 샴 그룹 사이에 ESPVR 및 ESPVR/EA에 유의한 통계적 차이가 없음에도 불구하고, 이것은 MOD 및 HFrEF 표현형이 sham에 비해 LV 말단 수축기 압력이 상당히 높기 때문에 거짓으로 사례이며, ESPVR 경사면은 V0에서 오른쪽으로 이동하여 거짓으로 가파르게 만듭니다. 더욱이, MOD 와 HFrEF 표현형이 동일한 정도의 PO를 가진 보상 및 동심 리모델링 표현형과 비교될 때, MOD 및 HFrEF 표현형에서 관찰된 바와 같이, MOD 및 HFrEF 표현형과 비교하여 5.0.1과 HFrEF 표현형에서 관찰된Figure 5 바와 같이, 진행성 편심 리모델링을 가진 ESPVR 및 ESPVR/EA에서 LVESV및 드롭의 유의하고 점진적인 증가를 이해할 수 있었다. Table 1

그림 1: 대동맥 밴딩 다음 8주차에 대표적인 심부전 표현형. (A)대표적인 M모드 이미지의 가짜 동물, 동물3주 후 오름차순 대동맥 밴딩(AAB) 및 AAB 이후 8주. 그림 1A는 Chaanine 외, 생리학 심혼 및 순환 생리학의 미국 전표, 2016에서 수정되었습니다. (B)중등도 편심 리모델링 (MOD)으로 심한 좌심실 비대 (LVH)의 생성을위한 혈관 클립 크기. (C)심한 LVH의 생성을 위한 혈관 클립 크기와 과장된 수축기 심부전(HFrEF). 도면 1B 및 1C는 2018년 분자 생물학의 방법인 Chaanine 등에서 획득 및 수정되었습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
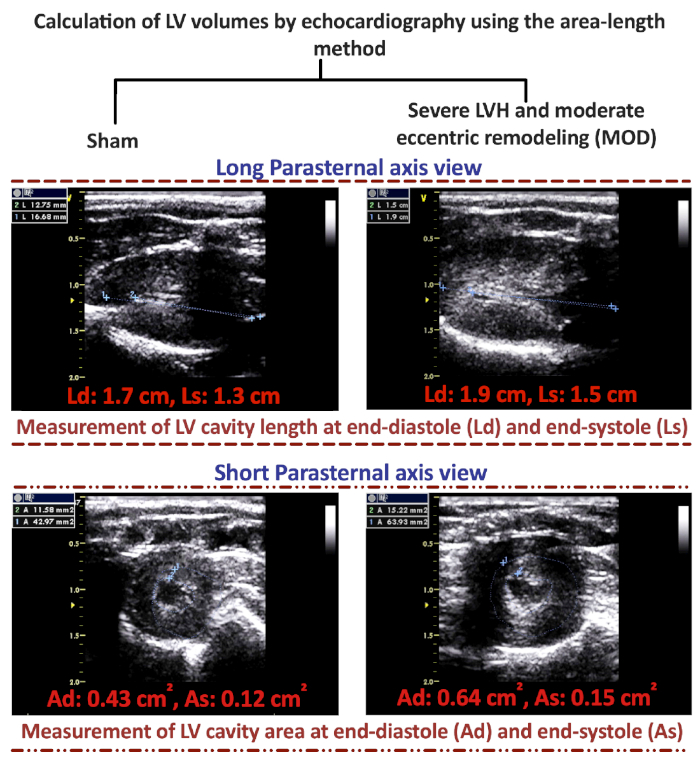
그림 2: 면적 길이 방법을 사용하여 심실 부피를 심초음파에 의해 계산합니다. 대표적인 2D 긴 파라스테날 및 2D 짧은 파라스테른 축 뷰 심초음파 이미지는 디아스톨(Ld)과 실로(Ls) 및 LV 캐비티 단면적의 좌심실(LV) 공동 길이를 측정하여 디아스톨(Ad) 및 시스톨(As)에서 디아스톨 및 시스톨 의 끝에 LV 체적을 계산합니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
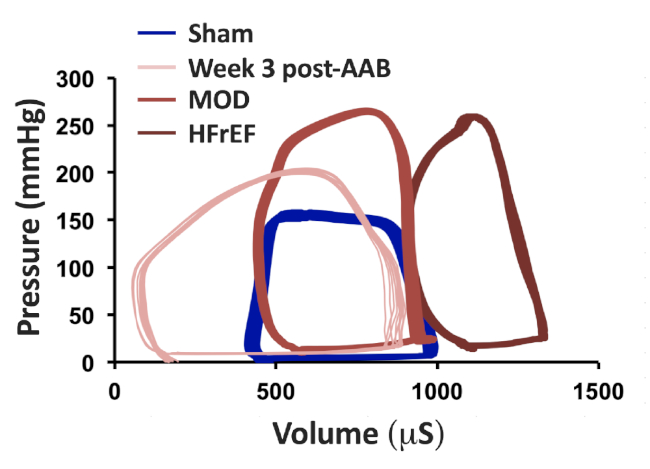
도 3: 압력-부피 루프 트레이싱은 열린 가슴 및 좌심실 상점 천자 접근법을 사용하여 1.9 F 래트 압력-체적 카테터를 통해 수득되었다. AAB, MOD 및 HFrEF 표현형에 이어 3주차에 AAB에 이어 8주차에 AAB의 대표적인 압력-볼륨 루프 추적이 AAB에 이어. 그림은 Chaanine 외에서 수정되었습니다., 순환: 심부전, 2013. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
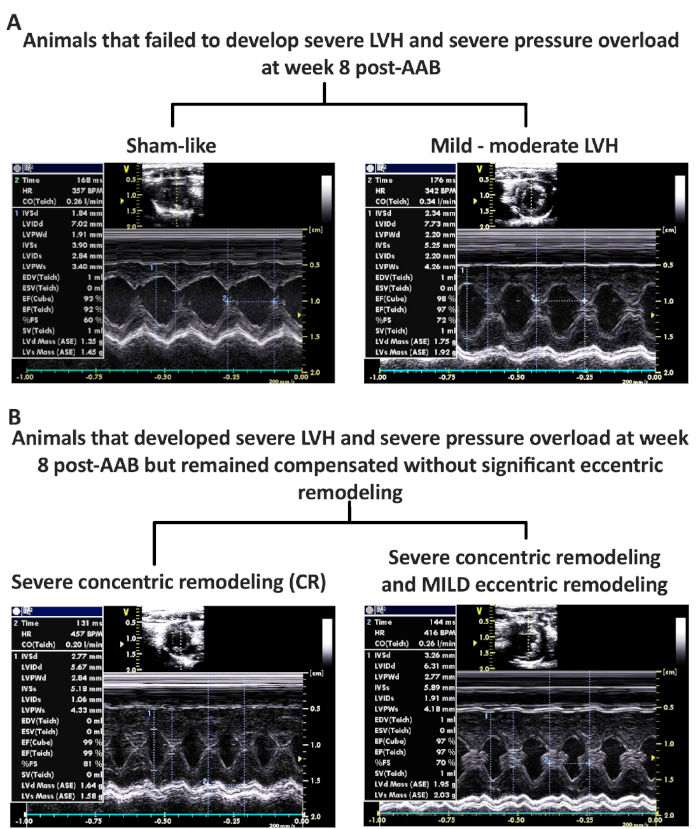
도 4: 원하는 심부전 표현형을 개발하지 못하는 AAB 다음 8주차에 현상형이 발생하였다. (a)압력 과부하(PO)를 상실하고 LVH(Sham-like) 및 가변 PO 및 LVH(온화한-보통 LVH) 표현형을 가진 동물의 대표적인 M 모드 이미지. (B)심한 PO, LVH 및 동심 리모델링 (CR)을 개발하지만 (CR) 또는 온화한 (MILD) 편심 리모델링 표현형을 개발 한 동물의 대표적인 M 모드 이미지. 그림 4B는 Chaanine 외., 미국 심장 협회의 전표, 2017에서 수정되었습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 5: 상이한 표현형의 심초음파 및 압력-체적 루프 파라미터. 데이터는 AAB 이후 8주차에 서로 다른 표현형에서 중앙값(수평선)이 있는 개별 값(점)으로 표시됩니다. 상이한 표현형에서 제시된 데이터의 통계 적 분석 결과는 표 1에 도시되어 있다. LVESV: 좌심실 말단 수축기 부피, LVEF: 좌심실 배출 분획, EDPVR: 말단 확장기 압력 부피 관계, ESPVR: 말단 수축기 압력 볼륨 관계, EA: 동맥 엘라스테인. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
| 샴 (n = 5) | 샴형(n=5) | 마일드 모드 LVH (n=8) | CR(n=11) | 마일드(n=14) | 모드(n=14) | HFrEF (n=5) | |
| 본체 중량(g) | 594 ± 37 | 466 ± 66 | 464 ± 22 | 497 ± 43 | 530 ± 59 | 478 ± 39 | 546 ± 18 |
| HW (mg) | 1269 ± 124.5 | 1328 ± 119 | 1614 ± 177 | 1645 ± 191a | 1821 ± 169a, b | 2106 ± 292a, b, c,d, e | 2897 ± 182a, b, c,d, e, f |
| LVW (mg) | 897 ± 94 | 968 ± 91 | 1161 ± 144 | 1222 ± 152a | 1372 ± 135a, b | 1580 ± 219a, b, c,d, e | 1726 ± 82a, b, c,d, e |
| RVW (mg) | 218± 22 | 218 ± 23 | 266 ± 24 | 239 ± 26 | 249 ± 26 | 283 ± 42a, b | 565 ± 76a, b, c, d, e, f |
| IVSd (cm) | 0.19 ± 0.01 | 0.21 ± 0.01 | 0.23 ± 0.01a | 0.29 ± 0.01a, b, c | 0.28 ± 0.02a, b, c | 0.28 ± 0.01a, b, c | 0.28 ± 0.02a, b, c |
| LVPWd (cm) | 0.20 ± 0.01 | 0.21 ± 0.02 | 0.24 ± 0.01a, b | 0.29 ± 0.02a, b, c | 0.28 ± 0.02a, b, c | 0.28 ± 0.01a, b, c | 0.30 ± 0.02a, b, c |
| LVEDV (μl) | 560.5 ± 25.8 | 570 ± 32 | 668 ± 143 | 442 ± 42, c | 583 ± 45d | 697 ± 129d,e | 881.5 ± 55.7a, b, c, d, e, f |
| LVESV (μl) | 105.9 ± 8.9 | 93 ± 15 | 111 ± 20 | 59 ± 7a, b, c | 85.3 ± 10.6d | 139.7 ± 22.5a, b, c,d, e | 319.2 ± 51.5a, b, c, d, e, f |
| LVEF (%) | 81.1 ± 1.2 | 83.7 ± 2.9 | 83.1 ± 2.5 | 86.5 ± 2.2a, c | 85.4 ± 1.7a | 79.8 ± 1.9b, c,d, e | 64.1 ± 3.6a, b, c,d, e, f |
| LVPmax (mmHg) | 121 ± 19 | 126 ± 23 | 186 ± 23a, b | 218 ± 18a, b | 221 ± 22a, b, c | * 234 ± 25a, b, c | 262 ± 16a, b, c, d, e |
| EDPVR (mmHg/μl) | 0.018 ± 0.005 | 0.017 ± 0.004 | 0.041 ± 0.013 | 0.043 ± 0.017 | 0.039 ± 0.015 | * 0.068 ± 0.025a, b, c,d, e | 0.079 ± 0.017a, b, c,d, e |
| ESPVR/EA | 1.57 ± 0.67 | 1.96 ± 0.61 | 2.63 ± 1.52 | 3.35 ± 1.23a | 2.62 ± 0.55 | *1.63 ± 0.41d | 0.82 ± 0.24c,d, e |
| 데이터는 평균 ± 표준 편차로 표시됩니다. 단방향 ANOVA를 사용하여 통계 분석을 수행했습니다. P< 0.05는 유의한 것으로 간주되었다. | |||||||
| aP < 0.05 vs 샴 | |||||||
| bP < 0.05 vs 샴라이프 | |||||||
| cP < 0.05 vs 마일드 모데르테 LVH | |||||||
| dP < 0.05 대 CR | |||||||
| eP < 0.05 vs 마일드 | |||||||
| fP < 0.05 대 MOD | |||||||
| *n=6 | |||||||
| 약어: HW: 심장 무게, LVW: 좌심실 무게, RVW: 우심실 무게, IVSd: 격막 두께 의 저온, LVPWd: 좌심실 후방 벽 두께. LVEDV: 좌심실 말단 확장기 부피, LVESV: 좌심실 말단 수축체 부피, LVEF: 좌심실 분출 분획, LVPmax: 좌심실 최대 압력, EDPVR: 끝 확장기 압력 볼륨 관계, ESPVR: 끝 수축기 압력 부피 관계, EA: 동맥 경화. | |||||||
표 1: 샴, 샴, 샴과 같은, 온화한 중간 LVH, CR, MILD, MOD 및 HFrEF 표현형의 심초음파 및 압력 부피 파라미터.
토론
쥐의 AAB와 관련된 PO에 이어, LV는 LV 벽 응력의 증가를 상쇄하기 위한 보상 메커니즘으로서 동심 LVH로 알려진 LV 벽 두께를 증가시킴으로써 동심 리모델링을 거칩니다. LV 벽 두께의 증가는 AAB 다음 첫 주 동안 눈에 띄게되고 AAB 후 2-3 주에서 최대 두께에 도달합니다. 이 기간 동안, 부적응 신호 감전 경로의 활성화는 LV 부피의 증가와 함께 LV의 점진적 확대로 이어질, 편심 비대 또는 리모델링으로 알려진 과정. 쥐에 있는 HF 표현형은 AAB 다음 주에 HF를 개발하는 몇몇을 가진 동물의 대부분에 있는 AAB 다음 약 8 주 발전할 것으로 예상됩니다. 2개의 HF 표현형은 AAB의 엄격에 따라서 계속됩니다. MOD 표현형은 내부 직경에서 2 mm2mm의 혈관 클립으로 오름차순 대동맥 밴딩 (AAB)의 생성을 통해 수득되는 반면, HFrEF 표현형의 생성은 내부 직경에서 1.5mm2의 더 단단한 혈관 클립을 가진 AAB를 필요로 한다. 가혹한 동심 LVH의 존재를 확인하기 위하여 상승 대동맥 밴딩 다음 2-3 주에 심초음파를 능력을 발휘하는 것이 중요합니다. 심한 LVH는 LV 중격 및 후방 벽 두께 ≥1.5 배 정상 (0.19 cm)으로 정의되며, 일반적으로 0.27 - 0.3 cm 사이의 범위. AAB 다음 주 3에 심한 LVH를 개발하지 않는 동물은 실패한 AAB가 있는 것으로 간주되며 그 이후에 는 수행되어서는 안된다. AAB 다음 3 주에 가혹한 LVH를 개발한 사람들은, 원하는 HF 표현형의 발달을 평가하기 위하여 AAB 다음 주에 심초음파를 겪을 것입니다. AAB 다음 주 3에 심한 LVH가 있는 동물을 만나는 것은 드문 일이 아니며, 토론의 후반 부에서 다루게 될 이유로 AAB 다음 8 주에 LVH의 회귀 또는 해결을 할 수 있습니다. 심한 LVH와 동심 리모델링이 없는 동물은 AAB 다음 주 8시에 경미한 편심 리모델링을 하지 않고, 따라서 CR과 MILD 표현형은 각각 한 달 또는 두 달 동안 계속 진행되더라도 편심 리모델링을 더 이상 개발할 가능성이 낮습니다. 온화한 MOD 표현형 사이 인 사람들은, 그(것)들이 1 달 동안 따르는 경우에 MOD HF 표현형을 개발할 수 있습니다.
PO 쥐 모델은 관련 높은 사망률 및실패율(10)으로인해 좌절될 수 있으며, 표준화된 혈관 클립 크기 및 외과 적 기술의 사용에도 불구하고, 또한 연구 비용에 추가되며, 원하는 표적 수(n)를 달성하기 위해 AAB를 받아야 하는 많은 수의 동물들로 인해, 그리고 동물이 원하는 HF 표현형을 개발하기 전에 따라야 할 시간의 길이로 인해 좌절될 수 있다. 가혹한 LVH를 개발하는 실패는 드물지 않은 대동맥 대신 에우측 brachiocephalic 동맥의 실패한 밴딩 또는 밴딩과 관련이 있습니다. 후속 후속 평가에서 심한 LVH의 회귀 및/또는 해결은 PO 9의 중증도에서 손실로 이어지는 동맥류 형성 및 peri-band 대동맥 리모델링과 관련이있다. 그것은 왜 심한 LVH와 PO를 가진 동물은 동일한 클립 크기, 성별 및 변형을 가지고에도 불구하고 편심 리모델링에 관한 현상형 가변성을 개발 하는 이유는 불분명 남아 있다. 그것은 peri 밴드 대동맥 리모델링 및 동맥류 형성을 위해 스크린상승 대동맥을 시각화하는 것이 좋습니다. 오름차순 대동맥류 ≥1 cm 직경을 개발하는 동물은 안락사되어야합니다, 이것은 주변 구조에 충돌로 인해 동물에 호흡 곤란과 고통을 일으킬 수 있기 때문에. 또한, 색상 도플러에 의해 밴드를 가로 질러 난류 흐름을 확인하는 것이 좋습니다, 하지만 불행하게도 연속 도플러에 의해 밴드를 통해 압력 그라데이션의 정확한 추정은 오름차순 대류에서 혈류 방향과 연속 도플러를 정렬할 수 없기 때문에 가능하지 않다.
MOD는 매력적인 HF 표현형이며, 특히 미토콘드리아 역학 및 기능, 심근 대사 및 칼슘 대사 및 칼슘 및 칼슘 과 외의 질화의 교란과 관련된 경우 질병 과정 초기에 심근 리모델링에 중요한 역할을하는 신호 트랜스덕션 경로를 타겟팅 할 수 있기 때문에 전통적으로 생성 된 HFrEF 표현형의 진화를 구성합니다. MOD HF 표현형11에서매우 분명한 특징. 또한, 초기 수술 후 사망률(AAB 후 처음 7일 간 사망률로 정의)은 클립 크기가 2 mm2로낮고, MOD 표현형의 생성을 위해 1.5 mm2의클립 크기보다, HFrEF 표현형10의생성을 위해, (5% 대 21%, P= 0.009 피셔의 정확한 시험을 사용하여). 그러나 MOD 및 HFrEF 표현형의 생성을 위한 두 클립 크기 간의 성공률은 통계적으로 유의하지않습니다(20%대 13%, P = 0.56 피셔의 정확한 테스트를 사용). 더욱이, 혈관 클립에 의한 대동맥 밴딩은 27 G 바늘에 대해 나일론 봉합사를 조여 대동맥 밴딩에 유리하며, 마우스에서 횡대동맥을 수축시키는 데 자주 사용되는 기법은 봉합기술에 비해 클립 크기의 변화와 대동맥에 대한 외상이 적기 때문이다.
HF의 PO 모델은 PO-유도된 원주 및 자오선 벽 응력이 심근의 모든 세그먼트에 균일하게 분포되어 있기 때문에 HF의 심근 경색(MI) 모델보다 유리하다. 그러나, 두 모델 모두 HF의 MI 모델에서 관찰된 흉벽 및 주변 조직에 대한 유착뿐만 아니라 경색부위(15)에서의 강렬한 염증 및 흉터와 함께 PO10,,11 및 경색 크기13,,14의 중증도에서의 가변성을 앓고 있다. 더욱이, 랫트 PO 유도 HF 모델은 MOD HF 표현형10을개발하는 조작된 랫트의 20%만이 높은 사망률 및고장률(10)과연관되기 때문에 생성하기가 어렵다. 자발적으로 고혈압 쥐 (SHR) 모델에 비해, PO 유도 HF 모델은 심근 리모델링과 관련된 경로를 연구하는 더 나은 모델이다. 수축기에서의 애프터로드 및 심근 벽 응력의 증가는 SHR 모델보다 PO 유도 HF 모델에서 훨씬 더 높습니다. SHR이 수축기 HF를 개발하는 데 약 2 년이 걸리며 수축기 HF의 메커니즘은 완전히 알려져 있지 않으며16노화로 인해 혼란스러워합니다. DocA 염 모델과 같은 고혈압의 SHR 모델 및 다른 모델은 고혈압 및 아마도 확장기 기능 장애와 관련된 메커니즘 및 치료법을 조사하기 위해 더 자주 사용된다16.
결론적으로, MOD HF 표현형은 심근 리모델링의 맥락에서 신호 전향 경로를 연구하는 매력적인 모델이며, 큰 동물 모델및 인간 심부전에서 그 효능을 검증하기 전에 잠재적 인 치료 전략의 적용 및 테스트에 활용될 수 있습니다.
공개
모든 저자는 이해 상충을 보고하지 않습니다.
감사의 말
NIH는 P.D에 HL070241을 부여합니다.
자료
| Name | Company | Catalog Number | Comments |
| Adson forceps | F.S.T. | 11019-12 | surgical tool |
| Alm chest retractor with blunt teeth | ROBOZ | RS-6510 | surgical tool |
| Graefe forceps, curved | F.S.T. | 11152-10 | surgical tool |
| Halsted-Mosquito Hemostats, straight | F.S.T. | 13010-12 | surgical tool |
| Hardened fine iris scissors, straight | Fine Science Tools F.S.T. | 14090-11 | surgical tool |
| hemoclip traditional-stainless steel ligating clips | Weck | 523735 | surgical tool |
| Mayo-Hegar needle holder | F.S.T. | 12004-18 | surgical tool |
| mechanical ventilator | CWE inc | SAR-830/AP | mechanical ventilator for small animals |
| Weck stainless steel Hemoclip ligation | Weck | 533140 | surgical tool |
참고문헌
- McMurray, J. J., Petrie, M. C., Murdoch, D. R., Davie, A. P. Clinical epidemiology of heart failure: public and private health burden. European Heart Journal. 19 (Suppl P), P9-P16 (1998).
- Berk, B. C., Fujiwara, K., Lehoux, S. ECM remodeling in hypertensive heart disease. Journal of Clinical Investigation. 117 (3), 568-575 (2007).
- Frey, N., Olson, E. N. Cardiac hypertrophy: the good, the bad, and the ugly. Annual Review of Physiology. 65, 45-79 (2003).
- Hill, J. A., Olson, E. N. Cardiac plasticity. New England Journal of Medicine. 358 (13), 1370-1380 (2008).
- Kehat, I., Molkentin, J. D. Molecular pathways underlying cardiac remodeling during pathophysiological stimulation. Circulation. 122 (25), 2727-2735 (2010).
- Rothermel, B. A., Hill, J. A. Autophagy in load-induced heart disease. Circulation Research. 103 (12), 1363-1369 (2008).
- Barrick, C. J., et al. Parent-of-origin effects on cardiac response to pressure overload in mice. American Journal of Physiology-Heart and Circulatory Physiology. 297 (3), H1003-H1009 (2009).
- Barrick, C. J., Rojas, M., Schoonhoven, R., Smyth, S. S. Cardiac response to pressure overload in 129S1/SvImJ and C57BL/6J mice: temporal- and background-dependent development of concentric left ventricular hypertrophy. American Journal of Physiology-Heart and Circulatory Physiology. 292 (5), H2119-H2130 (2007).
- Lygate, C. A., et al. Serial high resolution 3D-MRI after aortic banding in mice: band internalization is a source of variability in the hypertrophic response. Basic Research in Cardiology. 101 (1), 8-16 (2006).
- Chaanine, A. H., Hajjar, R. J. Characterization of the Differential Progression of Left Ventricular Remodeling in a Rat Model of Pressure Overload Induced Heart Failure. Does Clip Size Matter?. Methods in Molecular Biology (Clifton, N.J.). 1816, 195-206 (2018).
- Chaanine, A. H., et al. Mitochondrial Integrity and Function in the Progression of Early Pressure Overload-Induced Left Ventricular Remodeling. Journal of the American Heart Association. 6 (6), (2017).
- Chaanine, A. H., et al. Potential role of BNIP3 in cardiac remodeling, myocardial stiffness, and endoplasmic reticulum: mitochondrial calcium homeostasis in diastolic and systolic heart failure. Circulation: Heart Failure. 6 (3), 572-583 (2013).
- Takagawa, J., et al. Myocardial infarct size measurement in the mouse chronic infarction model: comparison of area- and length-based approaches. Journal of Applied Physiology (Bethesda, Md. : 1985). 102 (6), 2104-2111 (2007).
- Vietta, G. G., et al. Early use of cardiac troponin-I and echocardiography imaging for prediction of myocardial infarction size in Wistar rats. Life Sciences. 93 (4), 139-144 (2013).
- Frangogiannis, N. G. The inflammatory response in myocardial injury, repair, and remodelling. Nature Reviews. Cardiology. 11 (5), 255-265 (2014).
- Doggrell, S. A., Brown, L. Rat models of hypertension, cardiac hypertrophy and failure. Cardiovascular Research. 39 (1), 89-105 (1998).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유