Method Article
Un modelo de rata de sobrecarga de presión inducida remodelación moderada y disfunción sistólica en comparación con la insuficiencia cardíaca sistólica excesiva
En este artículo
Resumen
Describimos la creación de un modelo de rata de sobrecarga de presión inducida remodelación moderada y disfunción sistólica temprana donde se activan las vías de transducción de señales implicadas en el inicio del proceso de remodelación. Este modelo animal ayudará a identificar dianas moleculares para aplicar estrategias terapéuticas tempranas anti-remodelación para la insuficiencia cardíaca.
Resumen
En respuesta a una lesión, como el infarto de miocardio, la hipertensión prolongada o un agente cardiotóxico, el corazón se adapta inicialmente a través de la activación de vías de transducción de señal, para contrarrestar, a corto plazo, la pérdida de miocitos cardíacos y el aumento del estrés en la pared. Sin embargo, la activación prolongada de estas vías se vuelve perjudicial para la iniciación y propagación de la remodelación cardíaca que conduce a cambios en la geometría ventricular izquierda y aumentos en los volúmenes ventriculares izquierdos; un fenotipo observado en pacientes con insuficiencia cardíaca sistólica (HF). Aquí, describimos la creación de un modelo de rata de sobrecarga de presión inducida remodelación moderada y disfunción sistólica temprana (MOD) por bandas aórticas ascendentes (AAB) a través de un clip vascular con un área interna de 2 mm2. La cirugía se realiza en ratas Sprague-Dawley de 200 g. El fenotipo MOD HF se desarrolla a las 8-12 semanas después de AAB y se caracteriza no invasivamente por medio de ecocardiografía. Los trabajos anteriores sugieren la activación de las vías de transducción de señales y la expresión génica alterada y la modificación post-traduccional de proteínas en el fenotipo MOD HF que imitan a las que se ven en la IC sistólica humana; por lo tanto, haciendo del fenotipo MOD HF un modelo adecuado para la investigación traslacional para identificar y probar posibles dianas terapéuticas anti-remodelación en HF. Las ventajas del fenotipo MOD HF en comparación con el fenotipo sistólico de HF es que permite la identificación de dianas moleculares implicadas en el proceso de remodelación temprana y la aplicación temprana de intervenciones terapéuticas. La limitación del fenotipo MOD HF es que puede no imitar el espectro de enfermedades que conducen a la IC sistólica en humanos. Además, es un fenotipo desafiante para crear, ya que la cirugía AAB se asocia con altas tasas de mortalidad y fracaso con sólo 20% de ratas operadas desarrollando el fenotipo HF deseado.
Introducción
La insuficiencia cardíaca (HF) es una enfermedad prevalente y se asocia con una alta morbilidad y mortalidad1. Los modelos de sobrecarga de presión de roedores (PO) de HF, producidos por bandas aórticas ascendentes o transversales, se utilizan comúnmente para explorar mecanismos moleculares que conducen a la IC y para probar posibles dianas terapéuticas novedosas en la IC. También imitan los cambios observados en la IC humana secundaria a la hipertensión sistémica prolongada o la estenosis aórtica grave. Después de PO, la pared del ventventricular izquierdo (LV) aumenta gradualmente en grosor, un proceso conocido como hipertrofia concéntrica de LV (LVH), para compensar y adaptarse al aumento de la tensión de la pared del VL. Sin embargo, esto se asocia con la activación de una serie de vías de señalización maladaptive, que conducen a destornaduras en el ciclo de calcio y homeostasis, remodelación metabólica y de matriz extracelular y cambios en la expresión génica, así como apoptosis mejorada y autofagia2,3,4,5,6. Estos cambios moleculares constituyen el desencadenante de la iniciación y propagación de la remodelación miocárdica y la transición a un fenotipo de IC descompensado.
A pesar del uso de cepas de roedores endogámicos y la estandarización del tamaño del clip y la técnica quirúrgica, hay una tremenda variabilidad fenotípica en la estructura y función de la cámara LV en los modelos de bandas aórticas7,8,9. La variabilidad fenotípica encontrada después de PO en rata, cepa Sprague-Dawley, se describe en otros lugares10,11. De ellos, dos fenotipos de ONDAS decatonados se encuentran con evidencia de remodelación miocárdica y activación de vías de transducción de señales que conducen a un estado de mayor estrés oxidativo. Esto se asocia con la remodelación metabólica, la expresión génica alterada y los cambios en la modificación posttranslacional de las proteínas, jugando un papel en el proceso de remodelación10,,12. El primero es un fenotipo de remodelación moderada y disfunción sistólica temprana (MOD) y el segundo es un fenotipo de HF sistólica indecida (HFrEF).
El modelo PO de HF es ventajoso sobre el modelo de infarto de miocardio (MI) de HF porque las tensiones circunferenciales y de pared meridional inducidas por PO se distribuyen homogéneamente en todos los segmentos del miocardio. Sin embargo, ambos modelos sufren de variabilidad en la gravedad de PO10,,11 y en infarto tamaño13,14 junto con inflamación intensa y cicatrices en el sitio del infarto15, así como la adhesión a la pared torácica y los tejidos circundantes, que se observan en el modelo MI de HF. Por otra parte, el modelo de HF inducido por PO de rata es difícil de crear, ya que se asocia con altas tasas de mortalidad y fracaso10,con sólo 20% de las ratas operadas desarrollando el fenotipo MOD HF10.
El MOD es un fenotipo HF atractivo y constituye una evolución del fenotipo HFrEF creado tradicionalmente, ya que permite la focalización temprana de las vías de transducción de señales que juegan un papel en la remodelación miocárdica, especialmente cuando se refiere a perturbaciones en la dinámica y función mitocondrial, metabolismo miocárdico, ciclo de calcio y remodelación de matriz extracelular. Estos procesos fisiopatológicos son muy evidentes en el fenotipo MOD HF11. En este manuscrito, describimos cómo crear los fenotipos MOD y HFrEF y abordamos los escollos mientras realizamos el procedimiento de banda sortica ascendente (AAB). También profundizamos en cómo caracterizar mejor con ecocardiografía los dos fenotipos HF, MOD y HFrEF, y cómo diferenciarlos de otros fenotipos que no desarrollan PO severo o que desarrollan PO severo y remodelación concéntrica pero sin remodelación excéntrica significativa.
Protocolo
Todos los métodos y procedimientos descritos aquí han sido aprobados por el Comité Institucional de Cuidado y Uso de Animales (IACUC) de la Escuela de Medicina de la Universidad de Tulane.
1. Herramientas e instrumentos para la creación de modelos AAB
- Obtener desinfectantes, como 70% alcohol isopropílico y povidona-yodo.
- Obtener ketamina y xilazina para la anestesia y buprenorfina para la analgesia.
- Obtenga una almohadilla de calentamiento y una almohadilla inferior desechable de alta absorbencia con las dimensiones de 18 pulgadas x 30 pulgadas.
- Consigue un rollo de hilo 100% algodón, una cinta y un cortapelos.
- Obtener una placa de plástico de 20 cm x 25 cm, rango de espesor entre 3-5 mm.
- Obtenga un iluminador de fibra óptica Z-LITE.
- Obtener un ventilador mecánico para animales pequeños (por ejemplo, SAR-830/AP).
- Obtenga 2-0 y 3-0 suturas córset Vicryl y sutura de monofilamento de nylon 3-0, almohadillas de gasa estériles y puntas de algodón extra grandes estériles y guantes estériles.
- Obtener angiocath 16 G para intubación.
- Compre las siguientes herramientas quirúrgicas.
- Obtenga una ligadura Hemoclip de acero inoxidable Weck y clips de ligaduras de acero inoxidable.
- Obtenga tijeras de iris finas endurecidas.
- Obtener fórceps adsón.
- Consigue dos fórceps Graefe curvos.
- Consigue un fórceps recto Hemostats de Mosquito Halsted.
- Obtenga un soporte de aguja Mayo-Hegar.
- Consigue un retractor torácico de Alm con dientes romos.
- Utilizar y obtener un autoclave y un esterilizador de cuentas.
2. Procedimiento quirúrgico de banda aórtica ascendente
- Anestetizar al animal con una inyección intraperitoneal de una mezcla de 75-100 mg/kg de ketamina y 10 mg/kg de xilazina.
NOTA: Deje unos minutos para que el animal esté completamente sedado y flácido. Si la dosis anestésica no es suficiente y el animal todavía se mueve en la jaula, vuelva a inyectar al animal con la misma dosis anestésica después de permitir suficiente tiempo, alrededor de 5-10 minutos entre las inyecciones posteriores. La mayoría de los animales requieren 1-2 inyecciones para lograr sedación profunda y anestesia. - Afeitar el cabello en el sitio quirúrgico ubicado en el área torácica lateral derecha debajo de la axila derecha.
- Estabilice al animal pegando suavemente las cuatro extremidades a la tabla de plástico. Luego realice la intubación endotraqueal con una angiocath de 16 G. Después de que el animal sea intubado con éxito, iniciar la ventilación mecánica con volúmenes de marea de 2 mL a 50 ciclos/min y FiO2 del 21%. Busque el aumento simétrico en la pared torácica con cada respiración.
- Gire al animal lentamente para que se acueste en su lado lateral izquierdo, y luego doble la cola de una manera en forma de U y estabilice golpeándola suavemente a la tabla de plástico. A continuación, siga adelante y desinfecte el área arasda con la aplicación tópica de povidona-yodo.
- Infiltrar la piel en el lugar de la incisión con una mezcla de 50/50 en volumen de 1-2% de lidocaína/0.25-0.5 % de bupivacaína como analgesia preventiva antes de hacer la incisión.
- Realizar una incisión cutánea horizontal derecha, de 1-2 centímetros de largo, en el área axilar derecha 1 cm por debajo de la axila derecha. Luego, disecciona la capa muscular torácica hasta llegar a la caja torácica torácica. Haga una toracotomía de 1 cmrd entre la caja torácica 2y 3.
- Mientras disecte la capa muscular del pecho, tenga cuidado y evite lesiones en la arteria axilar derecha, que corre debajo de la axila derecha.
NOTA: La toracotomía realizada entre la1a y la costilla2a conlleva el riesgo de unir la arteria braquiocéfala derecha en lugar de la aorta ascendente. La toracotomía entre la3a y la cuarta costilla hace que sea difícil de visualizar y banda rindar la aorta ascendente, ya que el operador estará mirando la aurícula derecha.
NOTA: Evite extender la toracotomía demasiado medialiente hacia el esternón para evitar disocción y lesiones en la arteria mamaria interna derecha.
- Mientras disecte la capa muscular del pecho, tenga cuidado y evite lesiones en la arteria axilar derecha, que corre debajo de la axila derecha.
- Disecciona los dos lóbulos de la glándula del timo suavemente y empújalos de lado. Luego identifica la aorta ascendente y aíslala de la vena cava superior por disección contundente a través de un fórceps Graefe curvo.
NOTA: La manipulación significativa de la glándula del timo la hará hinchada y dificultará la visualización de la aorta ascendente.- Diseccionar la vena cava superior de la aorta con especial precaución para evitar lesiones o roturas de la vena cava superior, que es fatal. Esta puede ser la parte más difícil del procedimiento y se espera que suceda de vez en cuando, incluso en la mayoría de las manos experimentadas, pero a menudo con principiantes y estudiantes.
- Levante suavemente la aorta ascendente con un fórceps Graefe curvo y coloque el clip vascular alrededor de la aorta ascendente.
- Ajuste la herramienta de ligadura de hemorclips vasculares a través de una pieza de plástico precortada de 7" para obtener un clip vascular del área interna deseada de 1,5 mm2 o 2 mm2,dependiendo del modelo de IC que se desee.
- Sutura el tórax a través de una sutura de monofilamento Vicryl 2-0. A continuación, sutura la capa muscular del pecho a través de una sutura cónico 3-0 Vicryl. A continuación, sutura la incisión de la piel a través de una sutura monofilamento de nylon 3-0.
- Administrar una combinación de los siguientes medicamentos después de la finalización de la cirugía durante 48-72 horas para servir como analgesia en el período postoperatorio: 1) Buprenorfina 0,01-0,05 mg/kg por vía subcutánea cada 8-12h, 2) Meloxicam 2 mg/kg por vía subcutánea cada 12h, y 3) Morfina 2,5 mg/kg por vía subcutánea cada 2-4h según sea necesario para el dolor intenso.
NOTA: Deje que el animal se recupere en una almohadilla de calefacción bajo monitoreo regular. Una vez que el animal muestra signos de recuperación de la anestesia (capaz de respirar espontáneamente - sin evidencia de jadeo o uso de los músculos accesorios durante más de dos minutos - y tiene buenos reflejos, extremidades rojas y cálidas), extubar al animal y devolverlo a la jaula.
3. Ecocardiografía
- Sedar al animal con inyección intraperitoneal de 80-100 mg/kg de ketamina. Asegurar una sedación adecuada para la adquisición adecuada de imágenes de eco de buena calidad.
NOTA: Se desaconseja el uso de isoflurano como anestésico por su efecto cardiodepresor, especialmente en el entorno de una sobrecarga de presión grave y podría dar una falsa impresión de dilatación del VL y disfunción sistólica que se resuelve una vez que el animal está fuera de la anestesia.- Tenga cuidado y administre la mitad o incluso un tercio de la dosis de ketamina en animales que se ven dispneicos y taquipneicos con sospecha de que han desarrollado el fenotipo HFrEF.
- Afeitar el pelo del pecho, anteriormente, en el animal completamente sedado.
- Poner al animal en su espalda y estabilizarlo en la tabla de plástico.
- Adquiera clips de vista de eje largo parasternal 2D y 2D parasternales a nivel del músculo papilar. Además, obtenga imágenes en modo M desde la vista corta del eje parasternal a nivel del músculo papilar para medir el espesor de la pared septal y posterior del VI en diastole, así como el diámetro diastólico final y sistólico final de LV.
- Adquiera imágenes o clips a una frecuencia cardíaca de 370 - 420 latidos por minuto para garantizar una evaluación adecuada del tamaño y la función del LV. La adquisición de imágenes a frecuencias cardíacas más bajas dará lugar a una falsa impresión de la función de LV deprimida y la dilatación del VL.
NOTA: La adquisición de imágenes/clips de vista de eje parasternal largo 2D escorzados conducen a mediciones falsas. Para fines de control de calidad, asegúrese de que el ápice LV y el ángulo aorto-mitral se visualicen dentro del mismo corte de plano. - Adquirir imágenes/clips de vista de eje parasternal corto 2D a nivel del músculo papilar medio. Esto servirá como referencia para obtener mediciones fiables de lvablaense en serie y posteriores mientras sigue a los animales a lo largo del tiempo durante el período de estudio.
- Adquiera imágenes o clips a una frecuencia cardíaca de 370 - 420 latidos por minuto para garantizar una evaluación adecuada del tamaño y la función del LV. La adquisición de imágenes a frecuencias cardíacas más bajas dará lugar a una falsa impresión de la función de LV deprimida y la dilatación del VL.
- Obtenga imágenes en modo M en vista larga del eje parasternal a nivel de la válvula aórtica para evaluar el diámetro relativo de la aortica a la aurícula izquierda (LA) en la sístole final.
NOTA: Los animales con los fenotipos MOD y HFrEF deben mostrar evidencia de dilatación LA con una relación LA/Ao que sea de 1,25 y 1,5 euros en fenotipo MOD HF y 1,5 en el fenotipo10de HFrEF.
Resultados
La caracterización de los fenotipos de ondas decavío, que se desarrollan 8-12 semanas después de AAB, podría realizarse fácilmente a través de ecocardiografía. Las imágenes representativas en modo M de los fenotipos Sham, Week 3 post-AAB, MOD y HFrEF se presentan en la Figura 1A. La Figura 1B y la Figura 1C muestran el tamaño del clip vascular para la creación del fenotipo MOD HF y el fenotipo HFrEF, respectivamente. Los volúmenes diastólicos finales (LVEDV) y end-sistólicos (LVESV) del LV podrían calcularse utilizando las fórmulas del método de longitud de área: V-5/6-A-L, donde V es el volumen en ml; A es el área seccional transversal de la cavidad LV en cm2,obtenida de la vista corta del eje parasternal a nivel del músculo medio papilar en diastole (Ad) y en sístole (As); y L es la longitud de la cavidad LV en cm, medida desde la vista larga del eje parasternal como la distancia desde el ápice endocardial LV hasta la unión mitral-aórtica en diastole (Ld) y en sístole (Ls). En la Figura 2se presentan imágenes representativas de ecocardiografía parasternal y de eje parasternal corto, con ilustraciones sobre cómo medir Ld, Ls, Ad y As, en el fenotipo Sham y MOD HF. El LVEDV en el fenotipo MOD HF generalmente oscila entre 600 - 700 l, con muy pocos animales con LVEDV superior a 700 ol y hasta 1000 l; mientras que el LVESV en el fenotipo MOD oscila entre 120 - 160 l(Tabla 1). A partir de las imágenes de ecocardiografía de vista de eje parasternal corto 2D presentadas en la Figura 2,se podría apreciar el grado de LVH en el fenotipo MOD en comparación con la farsa. En la Figura 3se presentan los trazados representativos de bucles de volumen de presión de los fenotipos Sham, Week 3 post-AAB, MOD y HFrEF. La presión máxima del LV es de al menos 200 mmHg, incluso en la semana 3 después de AAB, y aumenta aún más en la semana 8 después de AAB debido a la desajuste entre el crecimiento del animal y la aorta y la estenosis creada fija en la aorta ascendente. Tenga en cuenta que los animales en la semana 3 post-AAB son completamente compensados con el desplazamiento de la LVEDV y LVESV a la izquierda en comparación con la farsa. Con la hipertrofia excéntrica progresiva y la remodelación, hay un cambio en LVEDV y LVESV hacia la derecha en los fenotipos MOD y HFrEF en comparación con la semana 3 post-AAB. Se podría apreciar también el aumento significativo de LVESV en el fenotipo MOD y el profundo aumento de LVESV en el fenotipo HFrEF, que refleja las disminuciones significativas y profundas en el volumen de accidente cerebrovascular y la FEVI en los fenotipos MOD y HFrEF, respectivamente, en comparación con la semana 3 post-AAB. Además, se podría apreciar el aumento significativo de la FEVI en la semana 3 después de la AAB y la disminución significativa de la FEVI en el fenotipo HFrEF en comparación con la farsa.
El modelo de HF inducido por PO de rata se asocia con altas tasas de mortalidad y fracaso. Sólo alrededor del 20% de las ratas que se someten a AAB, con un clip vascular de 2 mm2 de diámetro interno, pasarán a desarrollar el fenotipo MOD HF. En la Figura 4se presentan imágenes representativas en modo M de los fenotipos fallidos. La Figura 4A muestra imágenes representativas en modo M de animales que no desarrollaron LVH en la semana 8 después de AAB, y habían perdido completamente el PO con regresión completa de LVH (como una farsa) o tenían un grado variable de LVH y PO en la semana 8 después de AAB causando un fenotipo lvH leve-moderado. El segundo grupo de fenotipos fallidos se presenta en la Figura 4B que muestra imágenes representativas en modo M de animales con PO severo (presión máxima de LV >200 mmHg) y LVH severo que permaneció compensado sin evidencia de remodelación excéntrica, remodelación concéntrica (CR) grupo, o con una remodelación excéntrica leve (grupo MILD) . Los fenotipos de ecocardiografía y hemodinámica de la farsa, los fenotipos fallidos y exitosos/deseados se presentan en la Figura 5 y la Tabla 1. Observe los aumentos progresivos en el peso del corazón y el peso del VL a medida que los animales pasan de un fenotipo compensado a un fenotipo más excéntrico y remodelado. Además, hay un aumento exponencial en el LVESV y una disminución en la FEVI a medida que los animales pasan de una remodelación concéntrica compensada a un fenotipo remodelado excéntricamente descompensado. De particular interés es que tanto los fenotipos MOD como los fenotipos HFrEF HF tienen un grado similar de rigidez miocárdica al medido por el coeficiente de rigidez de la relación de volumen de presión diastólica final (EDPVR (mmHg/L)) en comparación con todos los demás fenotipos, mientras que hay una disminución gradual en la eficiencia del LV a medida que los animales pasan a un fenotipo remodelado más excéntricamente. La eficiencia del LV se calcula a partir de la relación de volumen de presión sistólica final (ESPVR) dividida por la elastance arterial (EA). A pesar de que no hay ninguna diferencia estadística significativa en ESPVR y ESPVR/EA entre los fenotipos MOD y HFrEF y el grupo falso, esto es falsamente el caso, ya que los fenotipos MOD y HFrEF tienen una presión sistólica del FINAL del LV significativamente mayor en comparación con la farsa, lo que hace que la pendiente esPVR sea falsamente más empinada con el desplazamiento en V0 a la derecha en comparación con la sham. Además, cuando los fenotipos MOD y HFrEF se comparan con los fenotipos compensados y concéntricos remodelados, que tienen el mismo grado de PO, entonces se podría apreciar el aumento significativo y progresivo de LVESV y la caídaFigure 5 en ESPVR y ESPVR/EA con remodelación excéntrica progresiva, como se observa en los fenotipos MOD y HFrEF en comparación con el CR y los fenotipos MILD). Table 1

Figura 1: Fenotipos representativos de insuficiencia cardíaca en la semana 8 después de bandas aórticas ascendentes. (A) Imágenes representativas en modo M de animales falsos, animales tres semanas después de la banda aórtica ascendente (AAB) y ocho semanas después de AAB. La Figura 1A ha sido modificada de Chaanine et al., American Journal of Physiology-Heart and Circulatory physiology, 2016. (B) Tamaño del clip vascular para la creación de hipertrofia ventricular izquierda grave (LVH) con remodelación excéntrica moderada (MOD). (C) Tamaño del clip vascular para la creación de LVH grave con insuficiencia cardíaca sistólica (HFrEF). Las figuras 1B y 1C se han obtenido y modificado de Chaanine et al., Methods in Molecular Biology, 2018. Haga clic aquí para ver una versión más grande de esta figura.
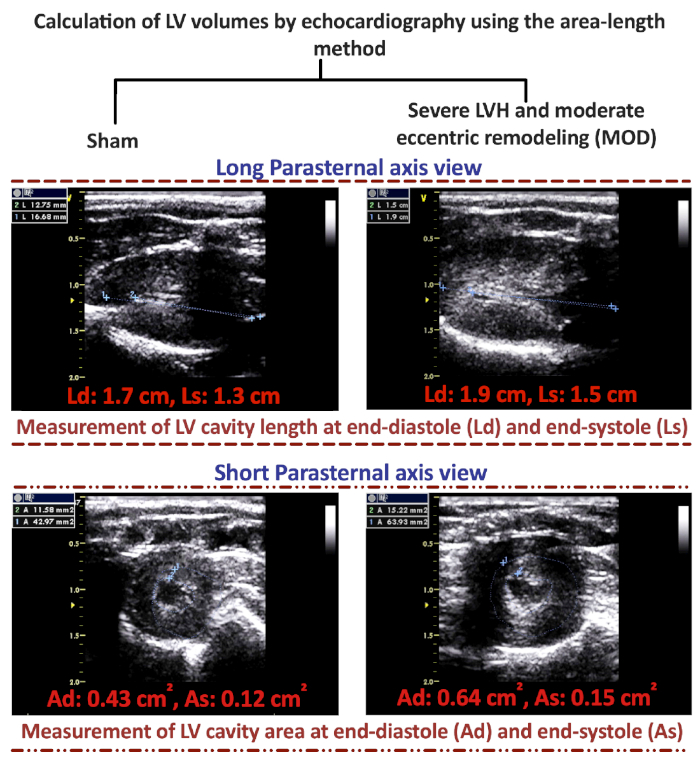
Figura 2: Cálculo de los volúmenes ventriculares izquierdos por ecocardiografía utilizando el método de longitud de área. Representante 2D largo parasternal y 2D corto eje parasternal vista imágenes de ecocardiografía para medir la longitud de la cavidad ventricular izquierda (LV) en diastole (Ld) y en el área transversal de la cavidad LV en diastole (Ad) y en sístole (As) con el fin de calcular los volúmenes de LV al final de la diástole y la sístole. Haga clic aquí para ver una versión más grande de esta figura.
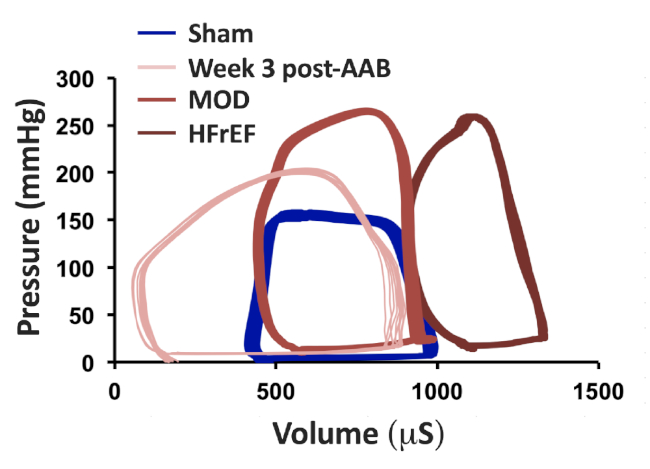
Figura 3: Los trazados de bucle de volumen de presión se obtuvieron a través de un catéter de volumen de presión de rata de 1,9 F utilizando el pecho abierto y el enfoque de punción apical ventricular izquierda. Seguimientos representativos de bucles de volumen de presión en Sham, semana 3 después de fenotipos AAB, MOD y HFrEF en la semana 8 después de AAB. Figura ha sido modificada de Chaanine et al., Circulation: Heart Failure, 2013. Haga clic aquí para ver una versión más grande de esta figura.
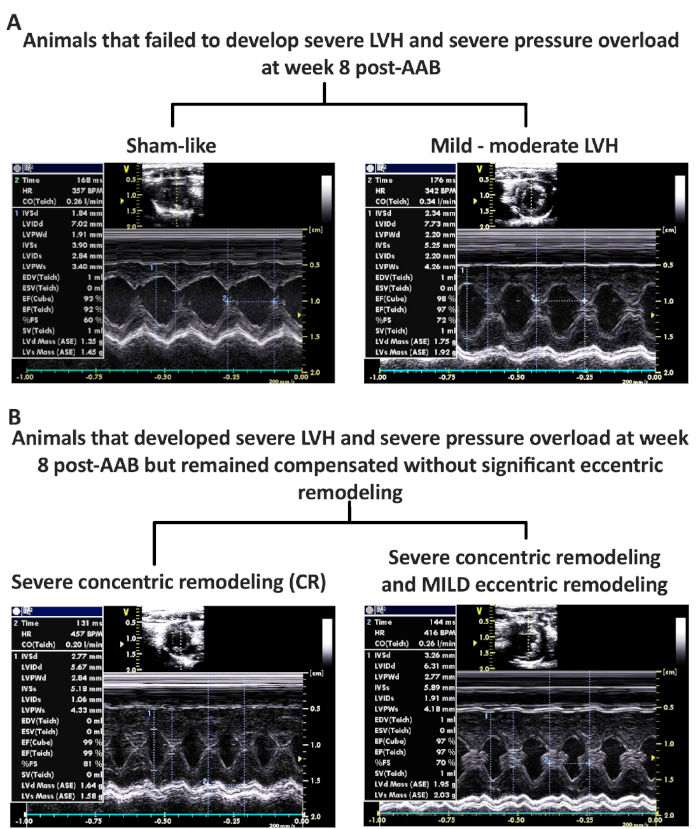
Figura 4: Se han encontrado fenotipos en la semana 8 después de AAB con la falta de desarrollo de los fenotipos de insuficiencia cardíaca deseados. (A) Imágenes representativas en modo M de animales que perdieron la sobrecarga de presión (PO) y no desarrollaron LVH (similar a Sham) y aquellos con fenotipos variables de PO y LVH (LVH leve-moderado). (B) Imágenes representativas en modo M de animales que desarrollaron PO severo, LVH y remodelación concéntrica (CR), pero sin (CR) o con fenotipos de remodelación excéntricos leves (MILD). La Figura 4B ha sido modificada de Chaanine et al., Journal of American Heart Association, 2017. Haga clic aquí para ver una versión más grande de esta figura.

Figura 5: Parámetros de ecocardiografía y bucle de volumen de presión en los diferentes fenotipos. Los datos se presentan como valores individuales (puntos) con mediana (línea horizontal) en los diferentes fenotipos en la semana 8 post-AAB. Los resultados del análisis estadístico de los datos presentados en los diferentes fenotipos se muestran en la tabla 1. LVESV: volumen sistólico final ventricular izquierdo, LVEF: fracción de eyección ventricular izquierda, EDPVR: relación de volumen de presión diastólica final, ESPVR: relación de volumen de presión sistólica final, EA: elastance arterial. Haga clic aquí para ver una versión más grande de esta figura.
| Sham (n.o 5) | Sham-like (n.o 5) | Mild-mod LVH (n-8) | CR (n-11) | MILD (n-14) | MOD (n-14) | HFrEF (n.o 5) | |
| Peso corporal (g) | 594 x 37 | 466 x 66 | 464 x 22 | 497 x 43 | 530 x 59 | 478 x 39 | 546 x 18 |
| HW (mg) | 1269 a 124,5 | 1328 a 119 | 1614 a 177 | 1645 a 191a | 1821 a 169a,b | 2106 a 292a,b,c,d,e | 2897 a 182a,b,c,d,e,f |
| LVW (mg) | 897 x 94 | 968 x 91 | 1161 a 144 | 1222 a 152a | 1372 a 135a,b | 1580 a 219a,b,c,d,e | 1726 a 82a,b,c,d,e |
| RVW (mg) | 218o 22 | 218 x 23 | 266 x 24 | 239 x 26 | 249 x 26 | 283 x 42a,b | 565 a 76a,b,c,d,e,f |
| IVSd (cm) | 0,19 a 0,01 | 0,21 a 0,01 | 0,23 a 0,01a | 0,29 a 0,01a,b,c | 0,28 á 0,02a,b,c | 0,28 á 0,01a,b,c | 0,28 á 0,02a,b,c |
| LVPWd (cm) | 0,20 á 0,01 | 0,21 a 0,02 | 0,24 á 0,01a,b | 0,29 a 0,02a,b,c | 0,28 á 0,02a,b,c | 0,28 á 0,01a,b,c | 0,30 a 0,02a,b,c |
| LVEDV (l) | 560,5 a 25,8 | 570 x 32 | 668 x 143 | 442 x 42,c | 583 x 45d | 697 a 129d,e | 881,5 a 55,7a,b,c,d,e,f |
| LVESV (l) | 105,9 a 8,9 | 93 x 15 | 111 x 20 | 59 x 7a,b,c | 85,3 á 10,6d | 139,7 a 22,5a,b,c,d,e | 319,2 a 51,5a,b,c,d,e,f |
| FEVI (%) | 81,1 a 1,2 | 83,7 x 2,9 | 83,1 a 2,5 | 86,5 x 2,2a,c | 85,4 x 1,7a | 79,8 a 1,9b,c,d,e | 64,1 a 3,6a,b,c,d,e,f |
| LVPmax (mmHg) | 121 x 19 | 126 x 23 | 186 x 23a,b | 218 x 18a,b | 221 a 22a,b,c | *234 x 25a,b,c | 262 a 16a,b,c,d,e |
| EDPVR (mmHg/l) | 0.018 a 0.005 | 0.017 a 0.004 | 0.041 a 0.013 | 0.043 a 0.017 | 0.039 a 0,015 | *0,068 a 0,025a,b,c,d,e | 0,079 a 0,017a,b,c,d,e |
| ESPVR/EA | 1,57 á 0,67 | 1,96 á 0,61 | 2,63 x 1,52 | 3,35 x 1,23a | 2,62 a 0,55 | *1,63 a 0,41d | 0,82 á 0,24c,d,e |
| Los datos se presentan como media - desviación estándar. El análisis estadístico se realizó utilizando ANOVA unidireccional. P < 0.05 se consideró significativo. | |||||||
| aP < 0.05 vs Sham | |||||||
| bP < 0.05 vs Sham-like | |||||||
| cP < 0.05 vs Mild-modearte LVH | |||||||
| dP < 0.05 vs CR | |||||||
| eP < 0.05 vs MILD | |||||||
| fP < 0.05 vs MOD | |||||||
| *n.o 6 | |||||||
| Abreviaturas: HW: peso cardíaco, LVW: peso ventricular izquierdo, RVW: peso ventricular derecho, IVSd: espesor de la pared septal en diastole, LVPWd: espesor de pared posterior ventricular izquierda en diastole. LVEDV: volumen diastólico final ventricular izquierdo, LVESV: volumen sistólico final ventricular izquierdo, LVEF: fracción de eyección ventricular izquierda, LVPmax: presión máxima ventricular izquierda, EDPVR: relación de volumen de presión diastólica final, ESPVR: relación de volumen de presión sistólica final, EA arterial: elastance. | |||||||
Tabla 1: Parámetros de ecocardiografía y volumen de presión en fenotipos Sham, Sham-like, Mild-moderate LVH, CR, MILD, MOD y HFrEF.
Discusión
Después de PO relacionado con AAB en rata, el LV se somete a una remodelación concéntrica mediante el aumento del espesor de la pared del VL, conocido como LVH concéntrico, como un mecanismo compensatorio para contrarrestar el aumento de la tensión de la pared del VL. El aumento en el espesor de la pared LV se hace notable durante la primera semana después de AAB y alcanza su espesor máximo en 2-3 semanas después de AAB. Durante este período de tiempo, la activación de las vías de transducción de señal maladaptive conduce a un agrandamiento progresivo del VI con aumentos en los volúmenes de LV, un proceso conocido como hipertrofia excéntrica o remodelación. Se espera que el fenotipo HF en rata se desarrolle alrededor de 8 semanas después de AAB en la mayoría de los animales con pocos de ellos desarrollando HF en la semana 12 después de AAB. Se emiten dos fenotipos de ONDAS decao en función de la gravedad de la AAB. El fenotipo MOD se obtiene mediante la creación de bandas aórticas ascendentes (AAB) con un clip vascular de 2 mm2 de diámetro interno, mientras que la creación del fenotipo HFrEF requiere AAB con un clip vascular más apretado de 1,5 mm2 de diámetro interno. Es importante realizar ecocardiografía a las 2-3 semanas siguientes a la banda aórtica ascendente para verificar la presencia de LVH concéntrico grave. La LVH grave se define como el espesor de la pared septal y posterior del LV 1,5 veces normal (0,19 cm), y por lo general oscila entre 0,27 - 0,3 cm. Los animales que no desarrollan LVH grave en la semana 3 después de AAB, se considerará que tienen AAB sin éxito y no deben ser seguidos a partir de entonces. Aquellos que han desarrollado LVH grave en la semana 3 después de AAB, se someterán a ecocardiografía en la semana 8 después de AAB para evaluar el desarrollo del fenotipo HF deseado. No es raro encontrar animales que tenían LVH grave en la semana 3 después de AAB para tener regresión o resolución de LVH en la semana 8 después de AAB, por razones que abordaremos en esta última sección de la discusión. Los animales con LVH grave y remodelación concéntrica sin o con remodelación excéntrica leve en la semana 8 después de AAB, por lo tanto, los fenotipos CR y MILD, respectivamente, es poco probable que desarrollen más remodelación excéntrica incluso si se siguen durante un mes o dos largos. Aquellos que están entre el fenotipo MILD y MOD, pueden desarrollar el fenotipo MOD HF si se siguen durante un mes más.
El modelo de rata PO puede ser frustrante debido a las altas tasas de mortalidad y fracasoasociadas 10,a pesar del uso de un tamaño de clip vascular estandarizado y técnica quirúrgica, que también se suma al gasto de investigación, debido al gran número de animales que necesitan someterse a AAB con el fin de lograr el número objetivo deseado (n), y el tiempo que los animales deben seguirse antes de desarrollar el fenotipo HF deseado. La falta de desarrollo de LVH grave está relacionada con bandas o bandas infructuosas de la arteria braquiocéfala derecha en lugar de la aorta, lo cual no es raro. La regresión y/o resolución de lvH grave en evaluaciones de seguimiento posteriores está relacionada con la formación de aneurisma y la remodelación aórtica peribanda que conduce a la pérdida de la gravedad de PO9. Todavía no está claro por qué los animales con LVH y PO severos desarrollan variabilidad fenotípica con respecto a la remodelación excéntrica a pesar de tener el mismo tamaño de clip, sexo y tensión. Se recomienda visualizar la aorta ascendente para detectar remodelación aórtica peribanda y formación aneurisma. Los animales que desarrollen aneurisma aortario ascendente de 1 cm de diámetro deben ser eutanasiados, ya que esto causará disnea y angustia al animal debido a la afectación en las estructuras circundantes. Además, se recomienda comprobar si hay flujo turbulento a través de la banda por color Doppler, pero desafortunadamente la estimación precisa del gradiente de presión a través de la banda por Doppler continuo no es factible debido a la incapacidad de alinear el Doppler continuo con la dirección del flujo sanguíneo en la aorta ascendente.
El MOD es un fenotipo HF atractivo y constituye una evolución del fenotipo HFrEF creado tradicionalmente, ya que permite la focalización de las vías de transducción de señales que desempeñan un papel en la remodelación miocárdica al principio del proceso de la enfermedad, especialmente cuando se refiere a perturbaciones en la dinámica y función mitocondrial, metabolismo miocárdico y ciclo de calcio y remodelación de matriz extracelular y rigidez miocárdica; características que son muy evidentes en el fenotipo MOD HF11. Además, la mortalidad postoperatoria temprana (definida como mortalidad en los primeros 7 días después de AAB) es menor con el tamaño del clip de 2 mm2,para la creación del fenotipo MOD, que el tamaño del clip de 1,5 mm2,para la creación del fenotipo10de HFrEF , (5% vs 21%, P a 0,09 utilizando la prueba exacta de Fisher). Sin embargo, la tasa de éxito entre los dos tamaños de clip, para la creación de fenotipos MOD y HFrEF, no es estadísticamente significativa10, (20% vs 13%, P a 0,56 usando la prueba exacta de Fisher). Por otra parte, la banda aórtica por clip vascular es ventajosa sobre el vendaje aórtico mediante el apriete de una sutura de nylon contra una aguja de 27 G, una técnica que se utiliza a menudo para restringir la aorta transversal en ratones, porque hay menos variación en el tamaño del clip y menos trauma tenso en la aorta en comparación con la técnica de sutura.
El modelo PO de HF es ventajoso sobre el modelo de infarto de miocardio (MI) de HF porque la tensión circunferencial y de pared meridional inducida por PO se distribuye homogéneamente en todos los segmentos del miocardio. Sin embargo, ambos modelos sufren de variabilidad en la gravedad de PO10,,11 y en infarto tamaño13,14 junto con inflamación intensa y cicatrices en el sitio del infarto15, así como la adhesión a la pared torácica y los tejidos circundantes observados en el modelo MI de HF. Por otra parte, el modelo de HF inducido por PO de rata es difícil de crear, ya que se asocia con altas tasas de mortalidad y fracaso10,con sólo 20% de las ratas operadas desarrollando el fenotipo MOD HF10. En comparación con el modelo de rata espontáneamente hipertensa (SHR), el modelo de IC inducido por PO es un mejor modelo para estudiar vías relacionadas con la remodelación del miocardio. El aumento de la tensión de la pared después de la carga y el miocardio en la sístole es mucho mayor en el modelo HF inducido por PO que el modelo SHR. El SHR tarda unos dos años en desarrollar la IC sistólica y el mecanismo de la IC sistólica no se conoce del todo y se confunde por el envejecimiento16. El modelo SHR y otros modelos de hipertensión, como el modelo de sal DOCA, se utilizan con más frecuencia para investigar mecanismos y terapias relacionadas con la hipertensión y posiblemente la disfunción diastólica16.
En conclusión, el fenotipo MOD HF es un modelo atractivo para estudiar las vías de transducción de señales en el contexto de la remodelación miocárdica y se puede utilizar para la aplicación y prueba de posibles estrategias terapéuticas, antes de la validación de su eficacia en grandes modelos animales y en la insuficiencia cardíaca humana.
Divulgaciones
Todos los autores no reportan conflicto de intereses.
Agradecimientos
NIH concede HL070241 a P.D.
Materiales
| Name | Company | Catalog Number | Comments |
| Adson forceps | F.S.T. | 11019-12 | surgical tool |
| Alm chest retractor with blunt teeth | ROBOZ | RS-6510 | surgical tool |
| Graefe forceps, curved | F.S.T. | 11152-10 | surgical tool |
| Halsted-Mosquito Hemostats, straight | F.S.T. | 13010-12 | surgical tool |
| Hardened fine iris scissors, straight | Fine Science Tools F.S.T. | 14090-11 | surgical tool |
| hemoclip traditional-stainless steel ligating clips | Weck | 523735 | surgical tool |
| Mayo-Hegar needle holder | F.S.T. | 12004-18 | surgical tool |
| mechanical ventilator | CWE inc | SAR-830/AP | mechanical ventilator for small animals |
| Weck stainless steel Hemoclip ligation | Weck | 533140 | surgical tool |
Referencias
- McMurray, J. J., Petrie, M. C., Murdoch, D. R., Davie, A. P. Clinical epidemiology of heart failure: public and private health burden. European Heart Journal. 19 (Suppl P), P9-P16 (1998).
- Berk, B. C., Fujiwara, K., Lehoux, S. ECM remodeling in hypertensive heart disease. Journal of Clinical Investigation. 117 (3), 568-575 (2007).
- Frey, N., Olson, E. N. Cardiac hypertrophy: the good, the bad, and the ugly. Annual Review of Physiology. 65, 45-79 (2003).
- Hill, J. A., Olson, E. N. Cardiac plasticity. New England Journal of Medicine. 358 (13), 1370-1380 (2008).
- Kehat, I., Molkentin, J. D. Molecular pathways underlying cardiac remodeling during pathophysiological stimulation. Circulation. 122 (25), 2727-2735 (2010).
- Rothermel, B. A., Hill, J. A. Autophagy in load-induced heart disease. Circulation Research. 103 (12), 1363-1369 (2008).
- Barrick, C. J., et al. Parent-of-origin effects on cardiac response to pressure overload in mice. American Journal of Physiology-Heart and Circulatory Physiology. 297 (3), H1003-H1009 (2009).
- Barrick, C. J., Rojas, M., Schoonhoven, R., Smyth, S. S. Cardiac response to pressure overload in 129S1/SvImJ and C57BL/6J mice: temporal- and background-dependent development of concentric left ventricular hypertrophy. American Journal of Physiology-Heart and Circulatory Physiology. 292 (5), H2119-H2130 (2007).
- Lygate, C. A., et al. Serial high resolution 3D-MRI after aortic banding in mice: band internalization is a source of variability in the hypertrophic response. Basic Research in Cardiology. 101 (1), 8-16 (2006).
- Chaanine, A. H., Hajjar, R. J. Characterization of the Differential Progression of Left Ventricular Remodeling in a Rat Model of Pressure Overload Induced Heart Failure. Does Clip Size Matter?. Methods in Molecular Biology (Clifton, N.J.). 1816, 195-206 (2018).
- Chaanine, A. H., et al. Mitochondrial Integrity and Function in the Progression of Early Pressure Overload-Induced Left Ventricular Remodeling. Journal of the American Heart Association. 6 (6), (2017).
- Chaanine, A. H., et al. Potential role of BNIP3 in cardiac remodeling, myocardial stiffness, and endoplasmic reticulum: mitochondrial calcium homeostasis in diastolic and systolic heart failure. Circulation: Heart Failure. 6 (3), 572-583 (2013).
- Takagawa, J., et al. Myocardial infarct size measurement in the mouse chronic infarction model: comparison of area- and length-based approaches. Journal of Applied Physiology (Bethesda, Md. : 1985). 102 (6), 2104-2111 (2007).
- Vietta, G. G., et al. Early use of cardiac troponin-I and echocardiography imaging for prediction of myocardial infarction size in Wistar rats. Life Sciences. 93 (4), 139-144 (2013).
- Frangogiannis, N. G. The inflammatory response in myocardial injury, repair, and remodelling. Nature Reviews. Cardiology. 11 (5), 255-265 (2014).
- Doggrell, S. A., Brown, L. Rat models of hypertension, cardiac hypertrophy and failure. Cardiovascular Research. 39 (1), 89-105 (1998).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados