Method Article
헬리컬 펩 티 드를 통해 사진 유도 Thiol-ene 또는 yne Hydrothiolation Thioether/비닐 황 화물-곁에 건설
요약
선물이 thioether/비닐의 건설에 대 한 프로토콜 황화 닿는 헬리컬 펩 티 드 사진 유도 thiol-ene/thiol-yne hydrothiolation를 사용 하 여.
초록
여기, 우리-수 지 intramolecular/intermolecular thiol-ene hydrothiolation를 사용 하 여 thioether-곁에 펩 티 드의 준비에 대 한 상세한 프로토콜을 설명 합니다. 또한,이 프로토콜 난, 난 + 4 개의 위치에 알 켄/alkyne 사이드 체인을 소유 하는 amino acids 및 시스테인 잔류물 사이 솔루션 intramolecular thiol-yne hydrothiolation를 사용 하 여 비닐 황화 닿는 펩 티 드의 준비를 설명 합니다. 선형 펩 티 드 표준 Fmoc 기반 단단한 단계 펩 티 드 합성 (SPPS)을 사용 하 여 합성 했다. Thiol 한 hydrothiolation는 intramolecular thio-ene 반응 또는 펩 티 드의 길이 따라 intermolecular thio-ene 반응 중 하나를 사용 하 여 실시 됩니다. 이 연구에서 intramolecular thio-ene 반응 수 지에 따라 선형 펩 티 드의 완전 한 합성 시스테인 잔류물의 trityl 그룹의 deprotection를 사용 하 여 짧은 펩 티 드의 경우 수행 됩니다. 수 지 photoinitiator 4 methoxyacetophenone (지도) 및 2-hydroxy-1-[4-(2-hydroxyethoxy)-phenyl]-2-methyl-1-propanone (MMP)를 사용 하 여 UV 방사선을 설정 합니다. Intermolecular thiol-ene 반응 Fmoc Cys 오 N, N-dimethylformamide (DMF) 용 매에 용 해 하 여 수행 됩니다. 이 다음 수 지를 켄 베어링 잔류물을 사용 하 여 펩 티 드와 함께 반응. 그 후에, macrolactamization는 활성화 시 약 지에로 benzotriazole-1-yl-oxytripyrrolidinophosphonium hexafluorophosphate (PyBop), 1-hydroxybenzotriazole (HoBt), 및 4-Methylmorpholine (NMM)를 사용 하 여 밖으로 수행 됩니다. Macrolactamization, 다음 펩 티 드 종합은 계속 표준 SPPS를 사용 하 여. Thio-yne hydrothiolation의 경우 선형 펩 티 드 수 지에서 죽 습, 건조, 이며 이후 degassed DMF에 녹아. 이것은 다음 photoinitiator 2, 2-dimethoxy-2-phenylacetophenone (DMPA)와 UV 빛을 사용 하 여 반구. 반응에 따라 DMF 증발 하 고 원유 찌 꺼 기 침전은 고성능 액체 크로마토그래피 (HPLC)를 사용 하 여 정화. 이러한 방법은 수 세대 thioether 곁 순환 펩 티 드의 우수한 기능 그룹 허용 및 좋은 수확량을가지고 thio-ene 또는 yne 클릭 화학의 사용을 단순화 하기 위해 작동 합니다. 펩 티 드로 thioether의 소개의 시스테인 잔류물 및 자연의를 이황화 채권 기준으로 redox 불활성 이다.
서문
단백질 단백질 상호 작용 (PPIs)를 변조 하는 ligands의 개발 현대 약물 발견에 대 한 매력적인 접근을 제공 합니다. 따라서, 많은 노력은 PPIs1,2,3변조 효율적으로 수 공부 소설 화학 형식으로 투자 되었다. PPIs는 일반적으로 얕은 크거나 단종 상호 작용 표면, 구성 하 고 작은 분자 PPIs4,5의 변조에 대 한 부적 절 한 ligands로 일반적으로 간주 됩니다. 적당 한 노출 상호 작용 표면 면적, 짧은 펩 티 드 단백질 인터페이스의 구조 기능을 모방 하는이 문제가6,7를 해결 하기 위해 이상적인 후보자를 나타냅니다. 그러나, 짧은 펩 티 드 일반적으로 수성 솔루션에 구조화 된 되지 않습니다. 이 물 분자의 펩 티 드 등뼈 및 잘 정의 된 conformations intramolecular 수소 결합 네트워크와 경쟁 하는 물8entropically 유리한는 사실 때문입니다. 또한, 펩 티 드의 본질적으로 낮은 안정성 및 세포 침투성 속성 주로 생물 학적 응용9,10에 그들의 사용을 제한. 단백질 데이터 은행 (PDB) 분석 > 짧은 α-나선 상호 작용11를 포함 하는 PPIs의 50%. 따라서, 다른 화학 방법 나선 안정화에 관한 개발 되었습니다. 이들은 이황화/thioether 유대 형성12,,1314, 반지-닫는 metathesis15, 락탐 반지 형성16를 포함, 화학17의 추가 "클릭" perfluoroarenes18,19, 그리고 비닐 황화 대형20.
안정된 헬리컬 펩 티 드 널리 p53, 등 다양 한 세포내 목표에 대 한 활용은 에스트로겐 수용 체, Ras, bcl-2 가족 단백질, 그리고 다른 사람21,22,,2324. ALRN-6924, 모든 탄화수소 MDM2 및 MDMX의 펩 티 드 이중 억제제를 붙인, 임상 조사25현재 사용 되 고. 지난 몇 년 동안, 우리의 그룹은 thiol ene와 thiol-yne 반응26,,2728를 사용 하 여 새로운 펩 티 드 안정화 방법의 개발에 집중 했다. 일반적으로, 우리는 자연스럽 게 풍부한 시스테인 사용 되 면 이러한 사진 시작 반응 온화한 조건 하에서 효율적인는 증명 하고있다. 또한, 우리가 이러한 반응 우수한 기능 그룹 허용 바이오 직교 고 펩 티 드 및 단백질 수정29적용할 수 입증 되었습니다 나타났습니다. 결과 thioether/비닐 황화 곁에 펩 티 드 크게 제약 펩 티 드의 화학 공간을 개선 정한 밧줄에 수정 센터를 제공 하 고 수많은 생물 학적 응용 프로그램30 사용에 대 한 적용할 수 입증 ,3132. 날짜 하려면, 제한 된 보고서만 thiol-ene/thiol-yne 펩 티 드 cyclization에 관한 설명 했습니다. 2009 년 Anseth 그 외 여러분 에 의해 출판, 연구에는 수 지에 intramolecular thiol-ene 시스테인과 활성화 된 알 켄 사이 펩 티 드 cyclization에 대 한 반응은 시연된33. 2015 년에 chou의 외. 2 구성 요소 급진 시작된 thiol-ene 반응34 와 후속, 순차 thiol-yne/한 커플링 반응35스테이플링 펩 티 드에 대 한 설명. 최근에, 우리는 thioether/비닐 황화 곁에 펩 티 드20,,2627에 따라 작품의 시리즈 설명. 이 프로토콜에는 광범위 한 연구 공동체에 대 한 도움이 될 것입니다 희망에서 위에서 언급 한 thioether/비닐 황화 곁에 펩 티 드의 상세한 종합을 설명 합니다.
프로토콜
1. 장비 준비
- 수동 펩 티 드 합성 장치에 대 한 효율적인 증기 두건에서 진공 매니폴드 (테이블의 재료)를 배치 합니다. 다음, 진공 매니폴드에 3 방향 stopcocks를 놓고 질소 또는 아르곤 가스 라인에 그들을 연결 합니다. 고무 격 막 사용 하 여 모든 사용 하지 않는 후미 모자.
- 수 지 가득 열 (0.8 x 4 cm, 10 mL 저수지, 재료의 표참조) 매니폴드 3 방향 stopcocks (그림 1)를 사용 하 여 연결 합니다. 진공 여과 또는 고무 피 펫 벌브로 밀어내어 진공 시스템에 연결 된 펌프를 사용 하 여 열에 있는 용 매를 제거 하.
- Photoreactor (그림 2)를 사용 하 여 UV 방사선에 대 한 10 350 nm 램프 (테이블의 재료)를 갖추고 있습니다. 아르곤 가스 탱크는 photoreactor 이전에 photoreactions 동안 아르곤 가스로 가득 되도록 photoreactor 공기 흡입구를 통해에 연결 합니다.
- photoreactor의 UV 램프에 전환 하기 전에 확인 경우에 자외선에서 방사선 photoreactor 문이 닫혀 있다.
2. 수 지 준비
참고: 일반적으로, 펩 티 드 기판의 건설 수행 됩니다 Fmoc 기반 단단한 단계 펩 티 드 합성 프로토콜을 사용 하 여. 이 C 터미널 아 미드 나머지 다음 펩 티 드 분열을 그대로 링크 아 미드 수 지를 사용 하 여 실시 됩니다. 이 프로토콜은 종이 걸쳐 사용 됩니다.
주의: N, N-dimethylformamide (DMF), dichloromethane (DCM), 4-methylmorpholine (NMM), 및 N, N-diisoproylethylamine (DIPEA)은 유독 하 고 유해한 흡입, 섭취, 또는 피부 접촉에 의해. Diethyl 에테르 가연성 이다입니다. Trifluoroacetic 산 (TFA) 부식성입니다. 1, 2-ethanedithiol (EDT)는 매우 악취를 풍기. 따라서, 모든 유기 용 제, 화학 물질, 적절 한 개인 보호 장비 (니트 릴 장갑, 실험실 외 투, 및 보호 안경) 처리와 있어야 화학 증기 두건 내부 처리 합니다.
- 다음 수식을 사용 하 여 필요한 수 지의 양을 계산 합니다.
확장 (mmol) / (적재 능력 (mmol/g) 1000 (mg/g)을 수 지) 수 지 (mg)의 질량 =
예를 들어, 링크 아 미드 MBHA 수 지 (0.5 m m o l/g) 25 µmol에 대 한 금액 = 0.025 m m o l / (0.5 m m o l/g 1000 mg/g) = 50 mg. 다음, 열 수 지의 50 밀리 그램 무게 하 고 3 방향 stopcocks를 사용 하 여 진공 매니폴드에 그것을 설정 합니다. - 열 (0.8 x 4 cm, 10 mL 저수지)에 수 지를 DCM의 1-2 mL를 추가 합니다. 수 지를, 부드럽게 교 반 하십시오 질소 또는 아르곤 stream을 사용 하 여 10 분. 다음, 진공 여과 사용 하 여 용 매를 제거.
3. N-터미널 Fmoc Deprotection 및 세척
- Deprotecting 솔루션 N 맨끝 Fmoc 준비: 50% (v/v) morpholine 유리병에 DMF에의 한 적절 한 볼륨 (200 mL)를 준비.
- 수 지에 deprotection 솔루션의 1-2 mL를 추가 하 고 부드럽게 10 분 동안 그것을 선동 한 다음 진공 청소기를 사용 하 여 솔루션을 배수. 그 순서 대로 DMF (1-2 mL)과 DCM (1-2 mL) using, 수 지와 반응 선박 3 배 총을 철저 하 게 세척. 다음 절차를 반복 합니다 deprotection 및 세척 1 x.
4. Fmoc 보호 아미노산 커플링
- Fmoc-크 람-오 (5 equiv., 41.4 mg), 무게 25 µ-스케일 수동 합성의 경우 예를 들어, 알라닌 잔류물의 커플링을 사용 하 여 2-(6-chloro-1H-benzotriazole-1-yl)-1,1,3,3-tetramethylaminium hexafluorophosphate (HCTU; 4.9 equiv., 50.5 m g)에 폴 리 프로필 렌 컨테이너 DMF (0.5 mL)에 녹 이십시오.
- DIPEA 추가 (10 equiv., 43.5 µ l) 0.25 M를 생성 하기 위해 활성화 아미노산 솔루션 (표 1). 대략 1 분 사전 활성화에 따라 수 지에 솔루션을 추가 하 고 약 1-2 h N2 와 거품.
- 이 단계에서 일련의 단계를로 펩 티 드 사슬에 있는 각 아미노산을 통합: N 맨끝 Fmoc 그룹, 그리고 세척의 deprotection HCTU를 사용 하 여 활성화를 통해 아미노산의 결합에 의해 뒤에 먼저.
참고: 더 이상 연결 시간 (예., 2 h) 것이 좋습니다 경우 sterically 방해 아미노산 잔류물에 따라 커플링 [예., Fmoc-목 (tBu)-오, Fmoc Cys (Trt)-오, Fmoc-그의 (Trt)-오, Fmoc Arg (Pbf)-오]. 비 천연 아미노산을 베어링 켄/alkyne 5 대신 3 항목에 사용 됩니다 그리고 3 h 반응 남아 있습니다. - Arora 외 에 설명 된 대로 카이 저 또는 chloranil 테스트를 사용 하 여 펩 티 드 합성 진행률 모니터링 36 이러한 테스트 무료 1 차 및 이차 아민의 유무는 존재의 질적 평가 제공합니다. 또는, 펩 티 드의 약 2-3 mg 수 지에서 죽 습 하 고 LC MS에 의해 분석 될 수 있습니다.
5. thiol-ene Hydrothiolation 및 Thiol-yne Cyclization
- 수 지에 cyclization (그림 3)를 통해 thioether 링커를 구성 합니다.
- Trt deprotection 솔루션 (TFA/TIS/DCM 0.03/0.06/1.0)의 약 50 mL를 준비 합니다. Cys-및 mS5치료-수 지 베어링 [NH2-R-mS5-A-A-A-Cys (Trt)-R'-수 지, 50 mg] 10 mL 열에서 Trt deprotection 솔루션의 1-2 mL와 함께. 부드럽게 N2를 사용 하 여 10 분 동안 해결책을 교 반 하십시오. 마지막으로, DCM로 그것을 씻어 (1-2 mL) x 3의 총.
참고: MS5 나타냅니다 alkylene 베어링 빌딩 블록 펩 티 드 결합 및 thio-ene cyclization38사용 (참조 그림 6에 묘사 된 구조). - 약 6 x 총 솔루션 색상은 노란색이 더 이상 때까지 시스테인, trityl 보호 그룹을 제거 하려면 위에서 설명한 절차를 반복 합니다.
- R-mS5-A-A-A-Cys(-SH)-R을 씻어 N2버블링 '-수 지 [무료 thio와 시스테인 (-SH)] 그 순서 대로 (1-2 mL) DCM와 DMF (1-2 mL). 2 분 동안 메탄올 (1-2 mL)을 사용 하 여 수 지를 축소 한 다음 용 매 여과 사용 하 여 제거. 그런 다음 순차적으로 열에 약 5 분에 대 한 N2 가스의 증기에서 수 지 건조.
- 준비 degassed DMF 미리 입 플라스 크 내의 용 매에 기지개 했다 긴 바늘을 통해 약 1 시간에 대 한 버블링 질소 가스에 의해.
- 무게 종이 통해 10 mL 둥근 바닥 플라스 크에 수 지를 전송 합니다. 2-hydroxy-1-[4-(2-hydroxyethoxy)-phenyl]-2-methyl-1-propanone photoinitiator의 추가 의해 따라 degassed DMF의 2 mL에 수 지를 중단 (MMP; 1 equiv., 5.6 밀리 그램), 4-methoxyacetophenone (지도; 1 equiv., 3.8 mg).
- 저 어 추가 (0.3 cm) 플라스 크로 바와 적당 한 고무 플러그 플라스 크 모자 다음 플라스 크에 어 오일 펌프를 사용 하는 질소 가스로 치환.
참고: 불활성 분위기 필요 하지 않습니다 엄격 하 게 효과적인 thio-ene photoreaction에 대 한 단단한 단계에. 그러나, 그것이 그림5에서 솔루션 단계에서 thio-yne photoreaction에 대 한 매우 필요 합니다. 그렇지 않으면, 유황 UV 방사선 조사 동안 산화 됩니다. - 반응 플라스 크를 photoreactor로 설정 하 고 실내 온도 (그림 2)에서 UV 방사선에서 1 시간에 대 한 수 지를 저 어.
주의: photoreactor UV 램프를 켜는, 사전 확인 하십시오 경우에 UV 빛에서 유해한 방사선 photoreactor 문이 닫혀 있다.
참고: 선형 펩 티 드 선구자는 제품의 동일한 분자량으로 새로운 시퀀스 좋습니다 자주는 photoreactions 동안 반응 혼합물을 샘플링. 일반적으로, 선형 및 주기적인 펩 티 드 크게 다른 화란을 표시합니다. 이 HPLC를 사용 하 여 쉽게 구별 될 수 있습니다. 또는, 5, 5'-dithiobis-(2-nitrobenzoic 산) (DTNB) 시 약 무료 thiol37의 존재를 공부 하는 데 사용 또한 수. - 열에 플라스 크에서 수 지를 전송 하 고 진공 여과 사용 하 여 용 매를 제거 합니다. 세척 하 고 단계 5.1.3에서에서 설명 된 대로 수 지를 건조.
- 분열 칵테일 (TFA/팁/EDT/H2O 94/1/2.5/2.5) 증기 두건에서의 약 10 mL를 준비 합니다.
- 2 mL 폴 리 프로필 렌 용기에 수 지를 전송, 컨테이너, 분열 칵테일 (TFA/팁/EDT/H2O 94/1/2.5/2.5)의 1 mL을 추가 하 고 밀접 하 게 나사 모자를 사용 하 여 컨테이너를 봉인. 다음,로 교 반 1.5-2 h에 대 한 증기 두건에서 60 rpm의 속도로 궤도 통에 컨테이너를 부드럽게 하십시오.
주의: TFA 매우 부식성입니다. 보호복을 착용 하 고 효율적인 증기 두건에서 작동. 동부 서머 타임은 매우 악취를 풍기는 물질 하 고 효율적인 증기 두건에서 처리 되어야 합니다. - 증발 증기 두건에는 N2 가스 스트림 아래 여 TFA 칵테일을 제거 합니다. 다음, 30 s 및 격리에 대 한 차가운 diethyl 에테르 (1 mL)을 사용 하 여 잔류물을 침전 2 분 12000 x g에서 원심 분리를 통해. 원심 분리, 다음 조심 스럽게 부 어 에테르 구성 요소를 줄. 2x 대 한 침전과 원심 분리 단계를 반복 합니다. 증발 건조에 잔류물.
- 마지막으로, 1 mL H2O/이기 (2:1)에 찌 꺼 기를 녹이 고 HPLC C18 분석 열을 사용 하 여 정화 (4.6 x 250 m m 흐름 속도 1.0 mL/min). 사용 H2O (포함 하는 0.1 %TFA)와 UV 280 nm와 220 nm 파장 (표 2)를 사용 하 여 25 분 모니터 HPLC 스펙트럼을 통해 70% 이기에 20%에서 2%/min 선형 그라데이션에서 용 매로 순수한 이기.
- Trt deprotection 솔루션 (TFA/TIS/DCM 0.03/0.06/1.0)의 약 50 mL를 준비 합니다. Cys-및 mS5치료-수 지 베어링 [NH2-R-mS5-A-A-A-Cys (Trt)-R'-수 지, 50 mg] 10 mL 열에서 Trt deprotection 솔루션의 1-2 mL와 함께. 부드럽게 N2를 사용 하 여 10 분 동안 해결책을 교 반 하십시오. 마지막으로, DCM로 그것을 씻어 (1-2 mL) x 3의 총.
- Macrolactamization (그림 4)에 의해 intermolecular thio-ene 반응, 그리고 cyclize 펩 티 드를 통해 thioether 링커를 구성 합니다.
- 선형 펩 티 드 H2N-A-A-A-mS5베어링 alkylene 잔류물을 합성 (2-R ')-R'-수 지 (50mg) 사용 하 여 표준 Fmoc 기반 단단한 단계 펩 티 드 합성 (SPPS)에 설명 된 대로 단계 2-4. 다음, 세척 하 고 단계 5.1.3에서에서 설명 된 대로 수 지를 건조.
- 10 mL 둥근 바닥 플라스 크 5.1.4 단계에서 설명한 대로 degassed DMF의 2 개 mL를 포함 하는 수 지를 일시 중단 합니다.
- 추가 photoinitiator MMP와 지도 (MMP: 1 equiv., 5.6 밀리 그램; 지도: 1 equiv., 3.8 m g), Fmoc-Cys-오 (3 equiv., 25.7 m g), 그리고 저 어 (0.3 cm) 플라스 크로 바. 적당 한 고무 플러그를 사용 하 여 플라스 크 모자 고 오일 펌프를 사용 하 여 플라스 크에 공기를 질소 바꿉니다.
- 반응 플라스 크를 photoreactor로 설정 합니다. 실내 온도 (그림 2)에서 UV 방사선에서 1-2 시간 저 어.
- LC MS 분석 아래 반응 모니터링: 분열 칵테일을 사용 하 여 수 지의 2-3 mg을 쪼개 다. 다음 찬 diethyl 에테르 (300 µ L)으로 찌 꺼 기를 침전, 원심 분리, 여 찌 꺼 기를 분리 하 고 5.1.11 단계에서 설명한 대로 건조에 잔류물을 증발. 그 후, H2O/이기 (2:1) 100 µ L에서 잔류물을 디졸브. 펩 티 드 솔루션 0.22 μ m 미소 한 구멍이 있는 필름을 사용 하 여 여과 하 고 분무 이온화 (ESI)에서 이온화 하 고 긍정적인 모드에서 운영 하는 화합물과 LC-MS를 사용 하 여 분석.
- 경우에 필요한, 반복 단계 5.2.2-반응 되도록 5.2.4 완료 수행 됩니다.
- 사진-반응의 완료 다음 열에 플라스 크에서 수 지를 전송 하 고 진공 여과 사용 하 여 용 매를 제거 합니다. 세척 하 고 단계 5.1.3에서에서 설명 된 대로 수 지를 건조.
- Benzotriazole-1-yl-oxytripyrrolidinophosphonium hexafluorophosphate의 DMF 솔루션 추가 (PyBob; 2.4 equiv., 31.2 mg), 1-hydroxybenzotriazole (HoBt; 2.4 equiv., 8.1 m g), 및 NMM (4 equiv., 11 µ L)는 macrolactamization에 대 한 열 수 지에. 버블 2 h N2 이 솔루션.
- 또한,이 커플링 반응 단계 5.2.3에에서 설명 된 대로 LC-MS를 사용 하 여 모니터링 합니다. 필요한 경우 반복 반응 되도록이 단계 완료를 수행 됩니다.
- 3, 4 단계에 설명 된 대로 표준 Fmoc 기반 SPPS를 사용 하 여 펩 티 드 연장
- 모든 아미노산 잔류물의 어셈블리 단계 5.1.10 5.1.11에에서 설명 된 대로 수 지에서 펩 티 드를 쪼개 고 5.1.12 단계에서 설명한 대로 그것을 정화.
- 솔루션 단계 (그림 5)에서 비닐 황화 링커를 구성 합니다.
- 2-4 단계에 설명 된 대로 표준 Fmoc 기반 SPPS를 사용 하 여 선형 펩 티 드 베어링 alkyne 잔류물을 음성 합성. 이전 연구20에 설명 된 대로 잘 설립 된 프로토콜에 따라 아미노산을 베어링 alkyne 음성 합성.
- 수 지에서 펩 티 드를 쪼개 고 5.1.11 5.1.9-단계에 설명 된 대로 찬 diethyl 에테르를 사용 하 여 침전. 절단, 수 지의 강 수에 따라 2 분 12000 x g에서 원심 분리를 사용 하 여 펩 티 드를 수집 합니다.
- 진공 상태에서 결과 잔류물을 건조. 0.5 m m의 최종 농도 도달 하기 위해서는 100 mL 둥근 바닥 플라스 크에 degassed DMF (50 mL)에 찌 꺼 기를 분해 (수 지, 0.025 m m o l의 로드에 따라 (1000 mL/L / 0.5 mmol/L) 50 mL =).
- Photoinitiator DMPA (0.5 equiv., 3.2 밀리 그램)를 추가 하 고 솔루션으로 뻗어 긴 바늘을 통해 N2 를 사용 하 여 10 분 동안 반응 솔루션을 드. 다음, 0.5-동요 없이 1 시간에 대 한 상 온에서 자외선 아래 샘플 비추는.
- 높은 진공 아래 DMF를 제거 하 고 그것의 유기 부산물을 분해 하려면 diethyl 에테르를 추가 하 여 원유 찌 꺼 기를 침전. 그런 다음 2 분 동안 12000 x g에서 원심 분리를 사용 하 여 찌 꺼 기 분리. 원심 분리, 다음 조심 스럽게 부 어 에테르 구성 요소를 줄. 증발 건조에 잔류물. 마지막으로, H2O/이기 (2:1) 1 mL에 찌 꺼 기를 녹이 고 정화 단계 5.1.7에에서 설명 된 대로 HPLC를 사용 하 여.
결과
펩 티 드 Ac YmS5AAAC NH2 와 그 cyclized 제품 Ac-Y-(쿠-1, 5)-[mS5AAAC]-의 HPLC 및 MS 스펙트럼 NH2 수 지에 intramolecular thiol-ene photoreaction를 사용 하 여 생성 된 그림에에서 묘사 6B. 주기적인 펩 티 드의 선형 전조를 기준으로 동일한 분자량을 발견. 그러나, HPLC 보존 시간이 약 2 분 같은 분리 조건 하에서 그것의 선구자 보다 이전 수 관찰 되었다. 서로 다른 시퀀스와 짧은 펩 티 드 모두 관찰 되었다 좋은 변환 해야 그림 6 c에서처럼.
그림 7B, thio-yne photoreaction 조건에 대 한 심사 과정은 묘사 그리고 이성질체 변환 및 비율 역 상 HPLC의 통합을 사용 하 여 결정 했다. 펩 티 드 2 c의 추적 수준만 UV 조사에 따라 관찰 했다. 이것은 가능성이 20 조화로 macrocycle에 계약 단계 동안 thiyl N-말단에 급진적인의 트래핑에 대 한 구조적 환경 때문 이다. 펩 티 드 1a 및 1b는 8 회원 비닐 황화 crosslink와 2 개의 성체 생성을 발견 했다. 펩 티 드 1a에서 생성 된 펩 티 드 2a-A와 2a-B, 전시 뿐만 아니라 다른 비율 (0-30 분) 시간 다른 UV 방사선에 대 한 뚜렷한 보존 시간 (그림 ℃). 이 때문에 1H NMR 분광학 (그림 7D)에 이중 결합 양성자 신호 E/Z이 성체로 할당 되었다. 펩 티 드 2d-2 층의 경우 Z 이성질체는 지배적인 제품 발견 됐다. 이것은 8-회원 비닐 황화 crosslink 상대적인 조밀한 구조의 건설 기간 동안 구조적 기본 설정으로 인해. 펩 티 드 2a-A/B 및 2b-A/B는 8 회원 비닐 황화 crosslink 펩 티 드 하는 동안 무작위 코일 전시 그림 7E, 원형이 색 성 (CD) 스펙트럼에 따라 같이 7-회원 비닐을가지고 2d 황화 crosslink 전시는 나선형 구조입니다. 요약, 비닐 황화 본드의 Z 이성질체 우선적으로 형성을 발견 하 고 더 나은 나선 유도 표시 합니다.

그림 1: 단단한 단계 펩 티 드 종합을 위한 수동 펩 티 드 합성 장치. 열 3 방향 stopcocks 통해 진공 매니폴드에 배치 했다 그리고 기구는 버블링에 대 한 질소 또는 아르곤 가스 라인에 연결 되었다. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.

그림 2: 사용 하는 photoreactions 대 photoreactor 장치. 장치는 photoreactor 이전에 photoreactions 동안 아르곤 가스로 가득 차 있었다 되도록 UV 방사선 및 아르곤 가스 탱크 10 350 nm 램프 (테이블의 재료)로 갖춰 졌다. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.

그림 3: 수 지 짧은 펩 티 드의 경우 intramolecular thiol-ene 반응. 이 반응 시스테인 잔류물 선형 펩 티 드의 완전 한 합성에 따라 trityl 그룹의 수 지에 deprotection를 사용 하 여 실행 하 고 지도 및 MMP photoinitiators를 사용 하 여 UV 방사선을 수 지를 설정 했다. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.

그림 4: 수 지 intermolecular thio-ene 반응. 이 반응은 Fmoc Cys 오 DMF 용 매에 용 해 하 여 실시 되었고 수 지, macrolactamization PyBop, 이지만, 그리고 NMM 활성화 시 약으로 사용 하 여 뒤에 켄 베어링 펩 티 드 잔류물과 반구. 펩 티 드 합성 계속 되었다 다음 표준 SPPS를 사용 하 여. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.

그림 5: 솔루션 단계에서 Intramolecular thiol-yne 반응. 이 반응은 다음 선형 펩 티 드, 후 선형 펩타이드 degassed DMF에 녹 았다와 UV 빛을 사용 하 여 photoinitiator DMPA와 반구의 완전 한 합성 솔루션 단계에서 실행 되었다. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.
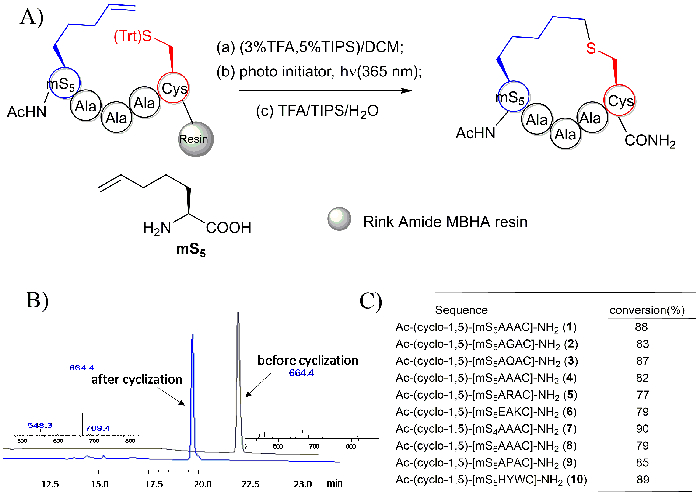
그림 6: Thioether 곁에 사용 하는 수 지에 intramolecular thiol-ene 반응 생성 주기적인 펩 티 드. A.이 패널 수 지에 intramolecular thio-ene 반응의 체계를 보여줍니다. mS5: "m" 모노 대체 olenic 아미노산, "S" S 구성 아미노산 나타냅니다 나타내고 "5" 사이드 체인 원자38의 수를 나타냅니다. B.이 패널 펩타이드 Ac YmS5AAAC NH2 이전 및 그것의 cyclization 다음의 HPLC 및 MS 스펙트럼을 보여줍니다. C.이 패널 표시 다른 시퀀스와 주기적인 펩 티 드의 변환. 이 그림에서 자오, B. 외.28 수정 되었습니다 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.
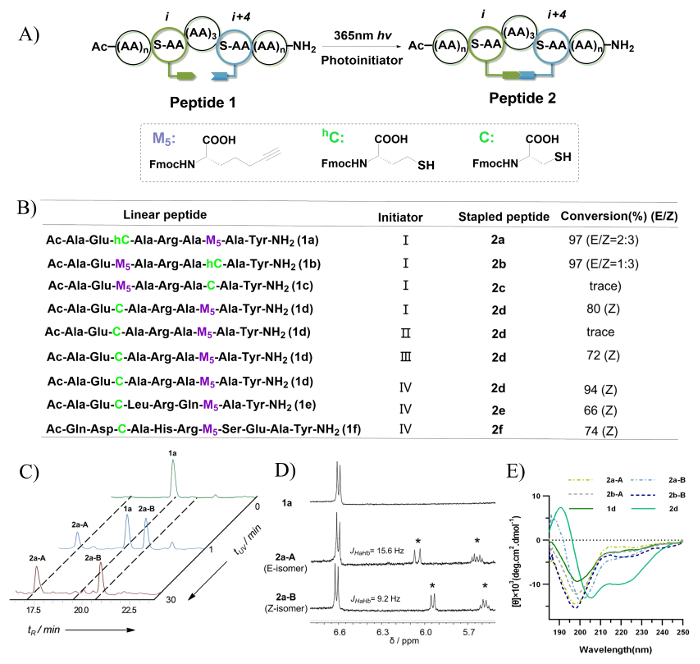
그림 7: 펩 티 드 사진 유도 thiol-yne hydrothiolation 통해 스테이플링. A.이 intramolecular thiol-yne hydrothiolation의 도식 적인 그림 이다. B.이 패널이이 연구에서 평가 된 펩 티 드 순서를 보여 줍니다. 초기자: (I) 0.5 식 DMPA, 1 h; (II) 초기자, 1 h; (III) 0.5 식 DMPA, 0.5 식 지도, 1 h; (IV) 0.5 식 MMP, 0.5 h. C. 이 패널 다른 UV 조사 시간으로 펩 티 드 1a의 반응 혼합물의 HPLC 흔적을 보여줍니다 그리고 220에서 모니터링 nm. D.이 패널 표시 1H NMR 스펙트럼의 1a, 2a-A와 2a-B (DMSO-d6 400mhz에서 측정). 별표는 UV 조사에 따라 비닐 황 이중 결합의 형성을 나타냅니다. E.이 패널 비닐 황화 상호 링크와 펩 티 드의 원형이 색 성 스펙트럼을 보여줍니다. 이 천, 영 외 에서 수정 되었습니다. 44 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.
| 재료 | MW | N(0.5mmol / g 수 지 × 0. 0 5 g × 5eq.) | M(아미노산) (mg) |
| (다) | (mmol) | ||
| Fmoc-Gly-오 | 297 | 0.125 | 37.1 |
| Fmoc-크 람-오 | 331 | 0.125 | 41.4 |
| Fmoc-발-오 | 339 | 0.125 | 42.4 |
| Fmoc 레이 오 | 353 | 0.125 | 44.1 |
| Fmoc-일-오 | 353 | 0.125 | 44.1 |
| Fmoc-프로-오 | 337 | 0.125 | 42.1 |
| Fmoc 페 오 | 387 | 0.125 | 48.4 |
| Fmoc Tyr (tBu)-오 | 460 | 0.125 | 57.5 |
| Fmoc Trp (Boc)-오 | 527 | 0.125 | 65.9 |
| Fmoc Ser (tBu)-오 | 384 | 0.125 | 48 |
| Fmoc-목 (tBu)-오 | 398 | 0.125 | 49.8 |
| Fmoc Cys (Trt)-오 | 586 | 0.125 | 73.3 |
| Fmoc 만났다 오 | 372 | 0.125 | 46.5 |
| Fmoc Asn (Trt)-오 | 597 | 0.125 | 74.6 |
| Fmoc Gln (Trt)-오 | 611 | 0.125 | 76.4 |
| Fmoc-Asp (OtBu)-오 | 412 | 0.125 | 51.5 |
| Fmoc Glu (OtBu)-오 | 426 | 0.125 | 53.3 |
| Fmoc 리스 (Boc)-오 | 469 | 0.125 | 58.6 |
| Fmoc Arg (Pbf)-오 | 617 | 0.125 | 77.1 |
| Fmoc-그의 (Trt)-오 | 620 | 0.125 | 77.5 |
| HCTU | 414 | 0.122 | 50.5 |
| DIPEA | 129 | 0.25 | 43.5(ΜL) |
| DMF | 0.5 mL | ||
표 1: 커플링 조건의 금액.
| 열 | Zorbax SB-Aq 열, 4.6 × 250 mm (기 공 크기 80 Å, 입자 크기 5 μ m) |
| 용 매 | A: 물, 0.1% (vol/vol) TFA; B: 이기 |
| 흐름 율 | 1 mL/min |
| 그라데이션 | 20-70% (vol/vol) B 25 분 이상; 70%-98% 이상 5 분; 98% 이상 5 분; |
| 사출 볼륨 | 30-500 Μ |
| 파장 (nm) | 280 (Fmoc-, Trp-또는 Tyr-포함 펩 티 드)에 대 한 또는 494 (FITC 표시 된 펩 티 드) 또는 220 (다른 사람)에 대 한 |
표 2: 고성능 액체 크로마토그래피 조건.
토론
그림 3에 설명 된 수 지에 intramolecular thio-ene cyclization trityl 그룹의 시스테인 잔류물의 제거 이후 photoreaction에 대 한 중요 한 단계가 될 발견 되었습니다. 또한, 이전에 펩 티 드 분자 무게와 반응으로 동일한 것으로 밝혀졌다 다음 그림 6B에 그려져 있습니다. 따라서, HPLC id 또는 DTNB 분석 결과 사용 하 여 반응을 모니터 하기 위해 필요 합니다. Intermolecular thio-ene 반응 그림 4에 설명 된 경우 MS 모니터링은 필요 합니다. 락탐 커플링의 추가 단계 thioether 밧줄의 건설에 대 한 필요를 발견 하는 동안이 프로토콜 긴 펩 티 드에 대 한 전반적으로 높은 효율성을 달성 하기 위하여 사용 될 것 이라고 하는 것이 좋습니다.
비닐 황화 본드 thio-yne photoreaction에 의해 생성 된 수 지 절단에 사용 되는 강산 TFA 솔루션에서 안정 됐다. 따라서, 솔루션 단계에서 thio-yne photoreaction 사용 하 여 채택 되었다. 이 반응은 잠재적인 intermolecular 의해-반응을 방지 하기 위해 낮은 농도 (0.5 m m)에 희석 되었다. 그것은 또한 용 매는 photoreactions 동안 제품 산화를 피하기 위하여 드도 중요입니다. 다음 반응, 유기 용 제 DMF의 진공 증발 한다 또한 신중 하 게 실시 펩 티 드 산화/저하 또는 기계 감가 방지 하기 위하여. 그림 5 에 묘사 된 thio-yne cyclization 반응 후 펩타이드 합성 수정35에 대 한 메커니즘을 제공 합니다.
Intramolecular thiol-ene 반응 좋은 변환 thioether 곁에 펩 티 드를 성공적으로 생성 하는 동안 원하는 나선형 구조에는 펩 티 드를 제한 하는 간단한 thioether 상호 연결 하지 못했습니다. 이 밧줄에 수정 전략을 바탕으로, 밧줄에 카이 랄 센터 유도 펩타이드 helicity 개념 개발 되었다, γ는 펩 티 드에 R 구성 그룹 대체 어디 C 터미널 펩 티 드의 나선형 구조 ( 유도 수 그림 4)39,40. 이 이렇게와 관련 된 제한 (α (S), γ(R)),41422 개의 카이 랄 센터와 enantiomerically 순수 부자연 스러운 아미노산의 합성입니다.
이 연구 에서처럼 그림 7Ethio-yne 반응 좋은 변환, 나선형 구조에 펩 티 드를 제한할 수 있습니다 설명 했다. 헬리컬 펩 티 드의 건설에서 thio-yne photoreaction을 헬리컬 펩 티 드의 건설 하는 것이 좋습니다. 수 지에 intramolecular thio-ene cyclization 긴 펩 티 드 너무 효과적인 cyclization를 위해 유연한 경우에 짧은 thioether 밧줄 펩 티 드 (이 하 15)의 건설에 적합 하도록 시연 했다. 또한, 수 지에 intermolecular thio-ene cyclization는 긴 펩 티 드 cyclization 권장 하 고 있습니다.
요약 하자면, 우리는 photoinduced thio-ene/thio-yne 클릭 화학의 사용을 통해 thioether/비닐 황화 곁에 펩 티 드의 건설에 대 한 화학 프로토콜의 시리즈를 개발 했습니다. 반응이 효율적 금속 촉매 무료, 편리한 조작, 그리고 우수한 기능 그룹 허용 오차를가지고 시연 및 바이오 직교 되었습니다. 또한,이 메서드는 β-머리 핀43,44같은 다른 펩 티 드 2 차 구조를 안정화 하기 위해 개발 되었다. 이 종이 thioether 밧줄 traceless 수정 사이트를 제공 합니다 보여줍니다. 이 주로 펩 티 드 합성 수정 다음 화학 공간을 확장 합니다. 또한,는 지방 족 thioether/비닐 황화 곁에 펩 티 드 탄화수소 주식 펩 티 드에 상대적인 감소 막 독성을 전시 하 고 시연된 좋은 bioactivity와 다양 한 생물 학적 응용 프로그램에 적용 되 고 bioavailability45,46
공개
저자는 공개 없다.
감사의 말
저자 인정 (제 21372023, 21778009 및 81701818); 중국 보조금의 자연 과학 재단에서 재정 지원 과학과 기술 (No. 2015DFA31590); 중화 인민 공화국의 심천 과학 및 기술 혁신 위원회 (제 JCYJ20170412150719814, JCYJ20170412150609690, JCYJ20150403101146313, JCYJ20160301111338144, JCYJ20160331115853521, JSGG20160301095829250, 및 GJHS20170310093122365); 그리고 중국 박사 후 과학 재단 (No. 2017 M 610704).
자료
| Name | Company | Catalog Number | Comments |
| Rink Amide MBHA resin(0.53 mmol/g) | HECHENG | GRM50407 | |
| Standard Fmoc-protected amino acids | GL Biochem (Shanghai) Ltd. | ||
| N-Methyl-2-pyrrolidinone | Shenzhen endi Biotechnology Co.Ltd. | 3230 | skin harmful |
| N,N-Dimethyl formamide | Energy | B020051 | skin harmful |
| Dichloromethane | Energy | W330229 | skin harmful |
| N,N-Diisoproylethylamine | Aldrich | 9578 | irritant |
| Trifluoroacetic acid | J&K | 101398 | corrosive |
| Triisopropylsilane | J&K | 973821 | |
| 1,2-Ethanedithiol | J&K | 248897 | Stench |
| 2-(6-Chloro-1H-benzotriazole-1-yl)-1,1,3,3-tetramethylaminium hexafluorophosphate | GL Biochem (Shanghai) Ltd. | 851012 | |
| Morpholine | Aldrich | M109062 | irritant |
| Diethyl ether | Aldrich | 673811 | flammable |
| Acetonitrile | Aldrich | 9758 | toxicity |
| Methanol | Aldrich | 9758 | toxicity |
| 2-hydroxy-1-[4-(2-hydroxyethoxy)-phenyl]-2-methyl-1-propanone | Energy | A050035 | |
| 4-methoxyacetophenone | Energy | A050098 | |
| 2,2-dimethoxy-2-phenylacetophenone | Energy | D070132 | |
| 5,5'-Dithiobis-(2-nitrobenzoic acid) | J&K | 281281 | |
| Benzotriazole-1-yl-oxytripyrrolidinophosphonium hexafluorophosphate | Energy | E020172 | |
| 1-Hydroxybenzotriazole | Energy | D050256 | |
| 4-Methylmorpholine | Energy | W320038 | |
| High Performance Liquid Chromatography | SHIMADZU | LC-30AD | |
| Electrospray Ionization Mass | SHIMADZU | LCMS-8030 | |
| Lyophilizer | Labconco | FreeZone | |
| SpeedVac concentration system | Thermo | Savant | |
| vacuum manifold | promega | A7231 | |
| three-way stopcocks | Bio-Rad | 7328107 | |
| poly-prep chromatography columns | Bio-Rad | 7311550 |
참고문헌
- Pelay-Gimeno, M., Glas, A., Koch, O., Grossmann, T. N. Structure-based design of inhibitors of protein-protein interactions: mimicking peptide binding epitopes. Angewandte Chemie International Edition. 54 (31), 8896-8927 (2015).
- Passioura, T., Katoh, T., Goto, Y., Suga, H. Selection-based discovery of druglike macrocyclic peptides. Annual Review of Biochemistry. 83, 727-752 (2014).
- Gonzalez, M. W., Kann, M. G. Protein interactions and disease. PLoS Computational Biology. 8 (12), 1-11 (2012).
- Wilson, A. J. Inhibition of protein-protein interactions using designed molecules. Chemical Society Reviews. 38 (12), 3289-3300 (2009).
- Teresa, A. F. C., Alessio, C. Cyclic and macrocyclic peptides as chemical tools to recognise protein surfaces and probe protein-protein interactions. ChemMedChem. 11 (8), 787-794 (2016).
- Craik, D. J., Fairlie, D. P., Liras, S., Price, D. The future of peptide-based drugs. Chemical Biology & Drug Design. 81 (1), 136-147 (2013).
- Cromm, P. M., Spiegel, J., Grossmann, T. N. Hydrocarbon stapled peptides as modulators of biological function. ACS Chemical Biology. 10 (6), 1362-1375 (2015).
- Zhang, Q. Z., Tian, Y., Lao, Y. Z., Li, Z. G. Peptides-staple method development and its application in cancer therapy. Current Medicinal Chemistry. 21 (21), 2438-2452 (2014).
- Cromm, P. M., Spiegel, J., Grossmann, T. N. Hydrocarbon stapled peptides as modulators of biological function. ACS Chemical Biology. 10 (6), 1362-1375 (2015).
- Wang, D., Liao, W., Arora, P. S. Enhanced metabolic stability and protein-binding properties of artificial alpha helices derived from a hydrogen-bond surrogate: application to Bcl-xL. Angewandte Chemie International Edition. 44 (40), 6525-6529 (2005).
- Bullock, B. N., Jochim, A. L., Arora, P. S. Assessing helical protein interfaces for inhibitor design. Journal of the American Chemical Society. 133, 14220-14223 (2011).
- Jackson, D. Y., King, D. S., Chmielewski, J., Singh, S., Schultz, P. G. General approach to the synthesis of short α-helical peptides. Journal of the American Chemical Society. 113 (24), 9391-9392 (1991).
- Timmerman, P., Beld, J., Puijk, W. C., Meloen, R. H. Rapid and quantitative cyclization of multiple peptide loops onto synthetic scaffolds for structural mimicry of protein surfaces. ChemBioChem. 6 (5), 821-824 (2005).
- Muppidi, A., Wang, Z., Li, X., Chen, J., Lin, Q. Achieving cell penetration with distance-matching cysteine cross-linkers: a facile route to cell-permeable peptide dual inhibitors of Mdm2/Mdmx. Chemical Communications. 47 (33), 9396-9398 (2011).
- Schafmeister, C. E., Po, J., Verdine, G. L. An all-hydrocarbon cross-linking system for enhancing the helicity and metabolic stability of peptides. Journal of the American Chemical Society. 122 (24), 5891-5892 (2000).
- Osapay, G., Taylor, J. W. Multicyclic polypeptide model compounds. 1. synthesis of a tricyclic amphiphilic alpha-helical peptide using an oxime resin, segment-condensation approach. Journal of the American Chemical Society. 112 (16), 6046-6051 (1990).
- Lau, Y. H., Andrade, d. P., Wu, Y., Spring, D. R. Peptide stapling techniques based on different macrocyclisation chemistries. Chemical Society Reviews. 44 (1), 91-102 (2015).
- Spokoyny, A. M., Zou, Y., Ling, J. J., Yu, H., Lin, Y. S., Pentelute, B. L. A perfluoroaryl-cysteine S(N)Ar chemistry approach to unprotected peptide stapling. Journal of the American Chemical Society. 135 (16), 5946-5949 (2013).
- Lautrette, G., Touti, F., Lee, H. G., Dai, P., Pentelute, B. L. Nitrogen arylation for macrocyclization of unprotected peptides. Journal of the American Chemical Society. 138 (27), 8340-8343 (2016).
- Tian, Y., et al. Stapling of unprotected helical peptides via photoinduced intramolecular thiol-yne hydrothiolation. Chemical Science. 7 (5), 3325-3330 (2016).
- Chang, Y. S., et al. Stapled α-helical peptide drug development: a potent dual inhibitor of MDM2 and MDMX for p53-dependent cancer therapy. Proceedings of the National Academy of Sciences of the United States of America. 110 (36), 3445-3454 (2013).
- Zhao, H., et al. Crosslinked aspartic acids as helix-nucleating templates. Angewandte Chemie International Edition. 55 (39), 12088-12093 (2016).
- Leshchiner, E. S., et al. Direct inhibition of oncogenic KRAS by hydrocarbon-stapled SOS1 helices. Proceedings of the National Academy of Sciences of the United States of America. 112 (6), 1761-1766 (2015).
- Wang, D., Qin, X., Zhao, H., Li, Z. N-cap helix nucleation: methods and their applications. Science China Chemistry. 60 (6), 689-700 (2017).
- Zorzi, A., Deyle, K., Heinis, C. Cyclic peptide therapeutics: past, present and future. Current Opinion in Chemical Biology. 38, 24-29 (2017).
- Hu, K., et al. An in-tether chiral center modulates the helicity, cell permeability, and target binding affinity of a peptide. Angewandte Chemie International Edition. 55 (28), 8013-8017 (2016).
- Lin, H., Jiang, Y., Zhang, Q., Hu, K., Li, Z. An in-tether sulfilimine chiral center induces helicity in short peptides. Chemical Communications. 52 (68), 10389-10391 (2016).
- Zhao, B., Zhang, Q., Li, Z. Constructing thioether-tethered cyclic peptides via on-resin intra-molecular thiol-ene reaction. Journal of Peptide Science. 22 (8), 540-544 (2016).
- Dondoni, A., Massi, A., Nanni, P., Roda, A. A new ligation strategy for peptide and protein glycosylation: photoinduced thiol-ene coupling. Chemistry. 15 (43), 11444-11449 (2009).
- Hu, K., Sun, C., Li, Z. Reversible and versatile on-tether modification of chiral-center-induced helical peptides. Bioconjugate Chemistry. 28 (7), 2001-2007 (2017).
- Shi, X., Jiang, Y., Yang, D., Zhao, H., Tian, Y., Li, Z. Reversibly switching the conformation of short peptide through in-tether chiral sulfonium auxiliary. Chinese Chemical Letters. , (2017).
- Jiang, Y., et al. Switching substitution groups on the in-tether chiral centre influences backbone peptides' permeability and target binding affinity. Organic & Biomolecular Chemistry. 15 (3), 541-544 (2017).
- Aimetti, A. A., Shoemaker, R. K., Lin, C. C., Anseth, K. S. On-resin peptide macrocyclization using thiol-ene click chemistry. Chemical Communications. 46 (23), 4061-4063 (2010).
- Wang, Y. X., Chou, D. H. C. A thiol-ene coupling approach to native peptide stapling and macrocyclization. Angewandte Chemie International Edition. 54 (37), 10931-10934 (2015).
- Wang, Y., et al. Application of thiol-yne/thiol-ene reactions for peptide and protein macrocyclizations. Chemistry. 23 (29), 7087-7092 (2017).
- Patgiri, A., Menzenski, M. Z., Mahon, A. B., Arora, P. S. Solid-phase synthesis of short α-helices stabilized by the hydrogen bond surrogate approach. Nature Protocols. 5 (11), 1857-1865 (2010).
- Ozyurek, M., Baki, S., Gungor, N., Celik, S. E., Guclu, K., Apak, R. Determination of biothiols by a novel on-line HPLC-DTNB assay with post-column detection. Analytica Chimica Acta. 750, 173-181 (2012).
- Zhang, Q. Z., et al. Chiral sulfoxide-induced single turn peptide α-helicity. Scientific Reports. 6, 38573 (2016).
- Lin, H., et al. An in-tether sulfilimine chiral center induces beta-turn conformation in short peptides. Organic & Biomolecular Chemistry. 14 (42), 9993-9999 (2016).
- Hu, K., Li, W., Yu, M., Sun, C., Li, Z. Investigation of cellular uptakes of the in-tether chiral-center-induced helical pentapeptides. Bioconjugate Chemistry. 27 (12), 2824-2827 (2016).
- Hu, K., et al. A precisely positioned chiral center in an i, i + 7 tether modulates the helicity of the backbone peptide. Chemical Communications. 53 (50), 6728-6731 (2017).
- Li, J., et al. An in-tether chiral center modulates the proapoptotic activity of the KLA peptide. Chemical Communications. 53 (75), 10452-10455 (2017).
- Zhao, B., et al. A thioether-stabilized-D-proline-L-proline-induced β-hairpin peptide of defensin segment increases its anti-Candida albicans ability. ChemBioChem. 17 (15), 1416-1420 (2016).
- Tian, Y., Yang, D., Ye, X., Li, Z. Thioether-derived macrocycle for peptide secondary structure fixation. The Chemical Record. 17 (9), 874-885 (2017).
- Hu, K., Yin, F., Yu, M., Sun, C., Li, J., Liang, Y., Li, W., Xie, M., Lao, Y., Liang, W., Li, Z. G. In-tether chiral center induced helical peptide modulators target p53-MDM2/MDMX and inhibit tumor growth in stem-like cancer cell. Theranostics. 7 (18), 4566-4576 (2017).
- Tian, Y., Jiang, Y., Li, J., Wang, D., Zhao, H., Li, Z. Effect of stapling architecture on physiochemical properties and cell permeability of stapled α-helical peptides: a comparative study. ChemBioChem. 18 (21), 2087-2093 (2017).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유