Method Article
ウサギの心的外傷後変形性関節症を発生させるための再現性軟骨衝撃モデル
* これらの著者は同等に貢献しました
要約
ウサギの開放内側大腿骨顆衝撃モデルは、心的外傷後変形性関節症(PTOA)およびPTOAの進行を緩和するための新しい治療戦略を研究するために信頼できます。このプロトコルは、インパクターヘッドを備えたキャリッジベースのドロップタワーを使用して、ウサギの後部内側大腿骨顆の孤立した軟骨欠損を生成します。
要約
心的外傷後変形性関節症(PTOA)は、米国における変形性関節症の全症例の12%を占めています。PTOAは、関節軟骨に作用する強い衝撃荷重などの単一の外傷性イベント、または前十字靭帯断裂で発生する関節の不安定性によって開始される可能性があります。現在、PTOAを予防する効果的な治療法はありません。軟骨損傷が進行するメカニズムをよりよく理解し、PTOAの進行を緩和または予防するための新しい治療戦略を調査するには、PTOAの信頼性の高い動物モデルを開発する必要があります。このプロトコルでは、軟骨の損傷を誘発するオープンドロップタワーベースのウサギ大腿骨顆衝撃モデルについて説明します。このモデルは、579.1 ± 71.1 N のピーク負荷と 81.9 ± 10.1 MPa のピーク応力、2.4 ± 0.5 ミリ秒のピーク負荷を実現しました。埋伏した内側大腿骨顆(MFC)の関節軟骨は、アポトーシス細胞の割合が高く(p = 0.0058)、非埋伏した反対側MFC(0.56±0.42)および埋伏した膝の他の軟骨表面(p < 0.0001)と比較して、3.38±1.43の変形性関節症研究協会(OARSI)スコアが高かった。非衝撃関節面ではOARSIスコアに差は検出されなかった(p > 0.05)。
概要
心的外傷後変形性関節症(PTOA)は、世界中の障害の主な原因であり、症候性変形性関節症(OA)の12%〜16%を占めています1。末期OA管理の現在のゴールドスタンダードは、末期の脛距骨または距骨下関節炎の場合と同様に、膝関節および股関節全置換術2または関節固定術です。関節形成術はおおむね成功していますが、費用がかかり、病的な合併症を引き起こす可能性があります3。さらに、関節形成術は、77%〜83%の低修正無修正インプラント生存率を考えると、50歳未満の患者ではあまり望ましくありません4,5。現在、PTOAの進行を予防または軽減するためのFDA承認の治療法はありません。
PTOAは、滑膜組織、軟骨下骨、関節軟骨を含む関節全体に影響を及ぼします。関節軟骨の変性、滑膜の炎症、軟骨下骨のリモデリング、骨棘の形成を特徴としています6,7。PTOAの表現型は、軟骨、滑膜、および軟骨下骨の間の相互作用の複雑なプロセスを介して発生します。現在の理解では、軟骨損傷は2型コラーゲン(COL2)やアグリカン(ACAN)などの細胞外マトリックス(ECM)成分の遊離につながるとされています。これらのECM成分フラグメントは炎症誘発性であり、IL-6、IL-1β、および活性酸素種の産生を増加させます。これらのメディエーターは軟骨細胞に作用し、MMP-13などのマトリックスメタロプロテアーゼ(MMP)のアップレギュレーションを引き起こし、関節軟骨を分解すると同時にマトリックス合成を減少させ、関節軟骨の全体的な異化環境を引き起こします8。さらに、原発性変形性関節症およびPTOAにおける軟骨細胞アポトーシスの増加の証拠があります9,10。ミトコンドリアの機能不全は、軟骨の超生理学的負荷後に発生し11,12,13,14、軟骨細胞のアポトーシスの増加につながる可能性があります12,15。軟骨細胞のアポトーシスの亢進は、プロテオグリカンの枯渇と軟骨異化の増加と関連しており、軟骨と軟骨下骨のリモデリングの変化に先行することが示されています16,17,18。
ほとんどのヒト疾患と同様に、疾患の病態生理学をさらに理解し、新しい治療法をテストするには、PTOAの信頼性の高いトランスレーショナルモデルが必要です。豚や犬などの大型動物は、PTOA17,19の関節内骨折および衝撃モデルで使用されてきましたが、コストがかかります。マウス、ラット、ウサギなどの小動物モデルは安価であり、関節の不安定化によって生成されるPTOAを研究するために使用されます、これは通常、前十字靭帯(ACL)の外科的離断および/または内側半月板の破壊を伴う20、21、22、23、24、25。関節の外傷は、靭帯損傷26を含むさまざまな結果につながる可能性がありますが、軟骨の機械的過負荷はほとんどすべてのケースで発生します。
靭帯不安定性(ACL離断など)および急性軟骨損傷後のPTOAの発症の背後にある病理学は、異なるメカニズムによるものであるという新たな証拠があります27。したがって、軟骨への直接的な損傷のモデルを開発することが重要です。現在、ラットおよびマウスに骨軟骨または軟骨損傷を引き起こす衝撃モデルの数は限られています28,29。しかし、マウス軟骨は孤立した軟骨欠損の生成にはあまり適していません。これは、マウスの関節軟骨の厚さがわずか3〜5細胞層であり、組織化された表在軟骨、放射状軟骨、および移行軟骨ゾーン、およびヒトおよび大型動物に見られる厚い石灰化軟骨層を欠いているためです。マウスモデルでは、軟骨部分欠損の自発的な解消も示される30,31。したがって、軟骨の厚さと組織がヒトに似ており、PTOAをもたらす一貫した軟骨衝撃を送達できる最小の動物モデルであるため、この衝撃モデルにウサギを選択しました。ウサギにおける大腿骨顆衝撃の以前の開腹手術モデルは、振り子32、手持ち型のバネ仕掛け軟骨埋伏装置33、およびウサギ特異的なインパクター作成を可能にするドロップタワー34を採用してきた。しかし、これらの研究にはin vivoデータが不足していた。また、振り子ベースの衝撃装置35、空気圧式36、およびバネ仕掛けの衝撃装置37を使用したin vivoデータ10を報告する研究もあり、これらの研究は、方法間のピーク応力と負荷率の変動率が高いことを示しています。しかし、この分野では、in vivoで急性軟骨外傷を確実にモデル化するための一貫したアプローチが欠けています。
現在のプロトコルは、ウサギの膝の後内側顆に一貫した衝撃を与えるために、ドロップタワーベースのシステムを採用しています。膝への後方アプローチは、後内側大腿骨顆を露出させるために採用されます。次に、スタインマンピンを大腿骨顆を横切って内側から外側に関節面に沿って配置し、プラットフォームに固定します。固定されると、荷重は後内側大腿骨顆に送られます。この方法により、ウサギの大腿骨遠位部の体重を支える面に一貫した軟骨損傷を与えることができます。
プロトコル
以下の手順は、インディアナ大学医学部の施設動物ケアおよび使用委員会(IACUC)の承認を得て実施されました。すべての生存手術は、NIHガイドラインで概説されているように、無菌条件下で実施されました。疼痛と感染のリスクは、適切な鎮痛薬と抗生物質で管理され、成功した結果を最適化しました。骨格的に成熟したオスのニュージーランド白ウサギ(体重3.0〜4.0 kg)を本研究に使用しました。
1. 落錘塔製作
- 落錘塔、ベースプラットフォーム、およびスタインマンピンを固定するためのメカニズムのコンポーネントのCAD図面を生成します(補足図1-14)。
- 市販のコンポーネントを購入します( 材料表を参照)。
- 装置の機械部品を調達するか、CAD図面を機械工に渡して製造します。
注:直径3mmのインパクターチップを製造するには、工具製作能力を備えた高精度の機械工が必要です(補足図1、パート20および 補足図13、14)。インパクターヘッドの衝突面は、内側ウサギ顆の曲率に合致するように、矢状面と冠状面でそれぞれ7.14mmと5.56mmの曲率を有していた35(補足図13,14)。 - ドロップタワーが固定アライメントリニアボールベアリング を介して 2本の垂直ロッド上を走行するキャリッジで構成され、ベースプラットフォームがウサギを支えてスタインマンピンを固定するように部品を組み立てます(図1 および 図2)。
注:この設計のキャリッジクロスビームは、許容可能な振動レベルを有する以前の落錘塔38 のそれに等しい曲げ剛性を有する。
2.動物の調製
- ウサギの体重を量り、2.5 mg / kgのアルファキサロンと0.15 mg / kgのミダゾラムIMを使用して麻酔をかけます( 材料表を参照)。誘導後、両眼に眼軟膏を塗布します。~2%-3%のイソフルランを使用して麻酔を維持します。鎮痛のためにブプレノルフィンSR(0.1 mg / kg)SQと周術期エンロフロキサシン(10 mg / kg)SQを与えます。ブプレノルフィンの代わりに、カルプロフェン、4mg / kgまたはメロキシカム、0.2〜0.3mg / kgまたはケトプロフェン、3mg / kgなどのNSAIDをSQ注射として投与できます。.
- ウサギの後ろ肢を足首から後肢まで剃ります。ウサギの脱毛では、切開部の汚染を防ぐために特に注意が必要です。専用の鋭利なウサギのバリカンのセットを使用することが重要です。
- ステンレス鋼の前脚ブロック(補足図1、部品番号2、 および補足図4)をインパクトプラットフォームの端の下に置き、プラットフォームを加熱パッドで覆います。ウサギの胸骨(つまり、うつ伏せ)を加熱パッドの上に置きます。反対側の股関節の下にパッド入りの隆起を置きます。
- 手術肢が膝の中心にあり、ポリエチレンブロックの上に載っていることを確認します(図2A1)。シルクテープを使用して、尾を手術肢の上側と反対側にそっと引っ込めます。
- クロロヘキシジンと70%アルコールに浸した滅菌ガーゼで手術部位を拭き取ります。手術部位を膝後部から外側に向かって円形にスイープしてこすります。新鮮なスクラブで少なくとも3回繰り返し、70%のアルコールで終わります。
- 手術中の足から足首まで滅菌手袋をかぶせ、滅菌の凝集ラップで包みます。
- 手術部位を3つのドレープで無菌的にドレープします:1つは手術下肢の真下、他の2つは体の残りの部分を覆います。タオルクランプでドレープを固定します。
3.外科的曝露
注:手術と衝撃の前に、軟骨下骨折を伴わずに目に見える軟骨損傷をもたらす体重と落下高さは、ウサギの特定の緊張、年齢、および性別について経験的に決定する必要があります。
- 膝蓋骨の位置を前方に触診して、膝蓋骨の遠位に位置する膝関節の位置を推定します。15枚刃を使用して、膝蓋骨の上極の高さから遠位まで、伸展した膝の後面に沿って3〜4cm切開します。
- 下にある表在性筋膜を通して鈍く鋭い解剖を行います。内側の皮膚と外側の内側腓腹筋の間の間隔を発達させます。この間隔に自己保持型のWeitlanerリトラクターを配置します( 材料表を参照)。
- 伏在動脈と静脈のすぐ上にある二次筋膜層が見えます。伏在の外側を解剖し、血管系を内側に、後腓腹筋複合体を外側に引っ込めます。
注:この血管系を切断しないように注意してください。この動脈が損傷している場合は、術後の出血性ショックが発生する可能性があるため、適切な結紮を行ってください。
- 伏在動脈と静脈のすぐ上にある二次筋膜層が見えます。伏在の外側を解剖し、血管系を内側に、後腓腹筋複合体を外側に引っ込めます。
- 後内側大腿骨顆の上に小さな可動性ファベラが特定されるまで遠位に解剖します。関節切開術を行って腓骨上外側を動員し、下にある内側大腿骨顆を露出させます。鈍く鋭い解剖によって軟部組織を静かに除去し、内側大腿骨顆の後面を露出させます。フリーアとクリケットのセルフリテーナー( 材料表を参照)を使用して、このレベルで軟部組織を引っ込めます。
- 顆を露出させたまま、大腿骨遠位部を横切って0.062インチのスタインマンピン( 資料表を参照)を前進させ、内側大腿骨顆の上面から開始し、内側大腿骨顆の前後方向を中心に、顆の後面から約5mmのところに進めます。
- バッテリー駆動のスタインマンピンドライバーを使用して、骨と外側の皮膚を関節面に平行に横方向に配線します。外側上顆の触診により、スタインマンピンの適切な軌道が確保されます。
- リトラクターを取り外し、3-0ポリソーブ縫合糸( 材料表を参照)で皮膚をランニングで閉じます。切開部を滅菌ガーゼで覆います。
4.大腿骨顆の影響
- 手術肢の下のドレープを取り外し、スタインマンピンをカスタマイズ可能で高さ調整可能なインパクトプラットフォームに固定します。まず、高さ調節可能なスタインマンピン固定装置の下側をピンの下に置きます(図2A2)。必要に応じてネジの高さを調整して、ワイヤがこのプラットフォームの地面と平行であることを確認します。
- スタインマンピンが地面と平行であることを確認した後、安全なプラットフォームの上部のネジベースの側面(図2A3)を、高さ調節可能な部品の下部のネジベースの側面に配置します。トップバーをピン保持プラットフォームの下側の高さ調整可能部分にねじ込んで、スタインマンピンがしっかりと固定されていることを確認します(図2A2)。
- スタインマンピンがプラットフォームに固定されたら、縫合糸を取り外し、切開を再開します。内側大腿骨顆を自己保持型のWeitlanerとクリケットリトラクターで露出させます。インパクターチップの経路から追加の軟部組織を引っ込めるには、追加のフリーアが必要になる場合があります(図2B)。
- 承認された消毒剤で落錘塔を拭き取ります。滅菌済みの3mmインパクターヘッド(図2A4)をドロップタワーキャリッジに取り付けます。ドロップタワーを手術の四肢の上に持ってきて、そのベース(図2A6)を衝突プラットフォーム(図3A)の下に置きます。
- インパクター(補足図2、パート20、 および補足図13)を大腿骨内側顆後部の中心にゆっくりと下げます。インパクターの経路に軟部組織がないことを確認します。
- 必要に応じてウサギまたはタワーを動かし、インパクターヘッドが後内側大腿骨顆の中心に来るようにします(図3B)。ウサギを移動または再配置するたびに、その手術部位に無菌性の破損の可能性がないか評価し、必要に応じてその領域を再滅菌する必要があります。.
- 適切な軌道を確保したら、トグルクランプを使用してタワーをプラットフォームにクランプします(図2A5、 材料表を参照)。
- 吸入麻酔を増やさずに、衝撃の5〜10分前にアルファキサロン(0.5〜0.7 mg / kg)を静脈内投与して、より深い麻酔を行います。.
注:眼瞼反射、ペダルの撤退、および耳介反射の欠如は、より深い麻酔の証拠です。この深い麻酔は、装置への留置中および衝撃中に起こりうる四肢の反応を防ぐのに役立ちます。
注意:アルファキサロンの投与が速すぎると、ウサギに一過性無呼吸と低酸素症を引き起こす可能性があるため、1〜2分かけてゆっくりと投与する必要があります。.低酸素症が発生した場合は、続行する前に、適切な酸素供給とバイタルの回復を確認してください。. - ドロップタワーのインパクターを、内側大腿骨顆の上の希望の高さに設定します。ベアリングを含む現在のキャリッジアセンブリの質量が1.41 kgの場合、これは7 cmの高さです。
注:ドロップタワーの高さは、死体組織のパイロット研究から決定されました。この高さは、この研究のウサギに目に見える軟骨損傷を引き起こしましたが、軟骨下骨折は発生しませんでした。 - スピンドルストップ(補足図2、項目番号14)を解放する直前に、LabVIEWデータ集録ソフトウェア(補足コーディングファイル1)のスタートボタンをクリックしてキャリッジを解除し、重力で落下させます。
注:データ収集ソフトウェアは、データ収集モジュールに接続されたラップトップを使用して、100 kHzでの衝撃中に、インパクターとキャリッジの間に配置されたロードセル(図1、6)と加速度計(図1、7)からデータを収集します。 - データ集録ソフトウェアで生成したtxtファイルを、Matlabデータ解析コード(Supplementary Coding File 2)と同じフォルダに配置し、データ解析コードを実行して生データをフィルタリングし、衝撃パラメータを計算します。
- 最大負荷が特定されていることを確認します。関連付けられた時点は、最大変形とゼロ速度の時間と見なされます。
注:データ分析コードは、フォルダ内のすべてのtxtファイルを分析し、各ファイルの結果を報告します。このコードは、読み込み時間データの変化に基づいて影響の開始と終了を決定します。加速度計からのデータは、速度を計算するために数値的に積分され、変位を計算するために再び積分されます。データ分析コードは、次の式からインパルス、仕事、および運動エネルギーを数値的に計算します。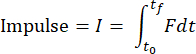


ここで、Fは荷重センサによって測定された力、x0およびt0は衝撃開始時の変位および時間、xおよびtfは衝撃終了時の変位および時間である。荷重率は、衝撃の荷重段階におけるdσ/dtの平均として数値的に計算されます。ピーク応力は、ピーク荷重をインパクターヘッドの接触面積で割ることによって計算されます。 - 軟骨表面を可視化して、適切な軟骨損傷が発生しているかどうかを判断します(図4A)。
5.手術部位の閉鎖
- 手術肢の上からドロップタワーを取り外します。使用済みの手術器具をすべて脇に置き、新しい滅菌手袋に交換します。
注:落錘塔は滅菌されていないため、衝撃までに使用されたすべてのツールは汚染されていると見なす必要があります。 - 滅菌ドレープを下肢に再適用し、未使用の滅菌セルフリトラクターを入手します。.
- 内側大腿骨顆を再露出させ、50〜60mLの滅菌生理食塩水で手術部位を完全に灌漑します。
- 5-0のポリソーブ縫合糸で後嚢を閉じ、続いて4-0のモノソーブ縫合糸で皮膚を閉鎖します( 材料表を参照)。
- 2 mLのリドカイン/ブピバカインを注射して、切開部の周囲に局所鎮痛剤を皮内投与します。
- Steinmanピンは、軟部組織の損傷を最小限に抑えるために、パワードライバセット( 材料表を参照)で振動させて取り外します。
- 非粘着性の包帯で傷口をドレッシングし、続いて粘着テープでドレッシングします。手術下肢のX線検査を行い、骨折が発生していないこと、および適切なピン配置を確認します(図4B)。
6.術後の管理
- ウサギをケージに戻し、麻酔から回復するまで(~25分)加熱した毛布で監視します。
- 手術後数日間はウサギを注意深く観察し続け、ウサギが適切に治癒し、可動性を取り戻すことを確認します。感染予防のために、術後2日間エンロフロキサシン(10 mg / kg)を投与します。ブプレノルフィンSR鎮痛剤(0.1 mg / kg)を手術後2〜3日ごと、必要に応じて皮下投与します。.ブプレノルフィンの代わりに、カルプロフェン、毎日4mg / kg SQなどのNSAIDs、メロキシカム、毎日0.2〜0.3mg / kg SQを最大3日間、またはケトプロフェン、毎日3mg / kg SQを手術後3〜5日、必要に応じて投与できます。
注:ウサギの舐めや咀嚼による術後創傷裂開を、ヒトの新生児用ズボンを後肢の上に配置することで防ぐことに成功した39。ウサギがズボンを噛む場合は、切開部の噛み傷を防ぐためにエリザベス朝の首輪( 資料表を参照)を配置する場合があります。
7.組織学的評価
- 受傷後16週間で、安楽死させたウサギから膝を採取し、10%中性緩衝ホルマリンで48時間固定した後、パラフィン包埋を行い、厚さ5μmのスライスに切片化します。
- 脱パラフィン処理と再水和の後、切片をサフラニンで染色します O 標準プロトコル40,41に従って高速緑色。
- ヘマトキシリン42 で対比染色したTUNEL発色アポトーシス検出キットを使用して、TUNEL発色アポトーシス検出キットを使用して、切片に対して末端デオキシヌクレオチジルトランスフェラーゼdUTPニックエンドラベリング(TUNEL)アッセイを実施します( 材料表を参照)。
結果
この手術の成功は、衝撃直後に外科医による顆の視覚化(図4A)とX線撮影によって監視され、骨折が発生していないことを確認しました(図4B)。顆の術中骨折につながる衝撃障害のリスクがあります。これは通常、Steinmanピンの配置が不適切であることが原因です(図5)。このモデルを用いた術中骨折に続発する骨折失敗率は9.0%(手術67件中6件)であった。平均ピーク衝撃応力は81.9±10.1MPa(CV=12.3%)、平均負荷率は36.6±11.0MPa/ms(CV=30.1%)であった。他のパラメータも一貫しており、CVは5%〜23.5%の範囲でした(表1)。
n = 8匹のウサギの膝関節のサフラニンO-fast緑色染色組織学的切片を、国際変形性関節症研究協会(OARSI)スコアリングシステム43を使用して軟骨分解および変形性関節症の病理について評価した。軟骨の損傷は、損傷を受けていない反対側の大腿骨顆では観察されず(図6A)、主に衝撃部位に局在していました(図6B)。罹患した16週間の内側大腿骨顆(MFC)は、対側対照MFCと比較して3.38±1.43のOARSIスコアが高く、OARSIスコアは0.56±0.42(p < 0.0001)でした(図6C)。さらに、埋伏した膝MFCは、同じ<膝の内側脛骨プラトー(MTP;0.71±0.59)、外側脛骨プラトー(LTP;0.88±0.64)、外側大腿骨顆(LFC;0.81±1.00)よりも高いOARSIスコアを示しました(図6D)。対照的に、反対側の非衝撃膝のMFC(0.56±0.42)、LTP(0.50±0.46)、MTP(0.28±0.45)、およびLFC(0.25±0.46)コンパートメント間でOARSIスコアに差は観察されませんでした(p>0.05)(図6E)。また、衝撃を受けたLFC、MTP、LTPの接合面と非衝撃との間に有意差はありませんでした(p >0.05)(図6F)。
16週目に採取された埋伏MFCの関節軟骨は、非埋伏MFC(53.4%±±12.4%)と比較して、TUNEL陽性率が高く(69.114.4%)、軟骨細胞アポトーシスの増加を示しました(p = 0.0058)(図7)。

図1:落錘式投下装置 。 (1)垂直ロッド。(2)棒が圧入されるアルミニウムプラットホーム。(3)ロッドをさらに拘束するためのプレート。(4)固定アライメントリニアボールベアリング。(5)キャリッジに取り付けられたインパクターヘッド。(6)ロードセル。(7)加速度計。 この図の拡大版をご覧になるには、ここをクリックしてください。

図2:外科的処置中および衝撃装置上でのウサギの配置中に使用されるコンポーネント。 (a)軟骨損傷を発生させるために使用される装置およびコンポーネントの識別: (1)ポリエチレンインパクトプラットフォーム、 (2)スタインマンピン保持装置の高さ調整可能な部分、 (3)高さ調節可能なスタインマンピン保持装置の上面、 (4)直径3mmの滅菌インパクターヘッド、 (5)衝撃プラットフォームをドロップタワー装置に保持するためのトグルクランプ、および(6)衝撃プラットフォームのベース。(B)後内側大腿骨顆の衝撃前に、スタインマンピン(赤い矢印で示されている)をプラットフォームに固定したウサギの後肢の位置決め。ドレープは、デモンストレーションの目的で図から省略されました。死体は写真を生成するために使用されました。この図の拡大版をご覧になるには、ここをクリックしてください。

図3:内側大腿骨顆への適切なインパクターの配置 。 (A)プラットフォームに固定されたウサギの後肢上の衝撃装置。(B)衝突前にインパクターチップを内側大腿骨顆に適切に配置すること。ドレープは、デモンストレーションの目的で図から省略されました。この図の拡大版をご覧になるには、ここをクリックしてください。
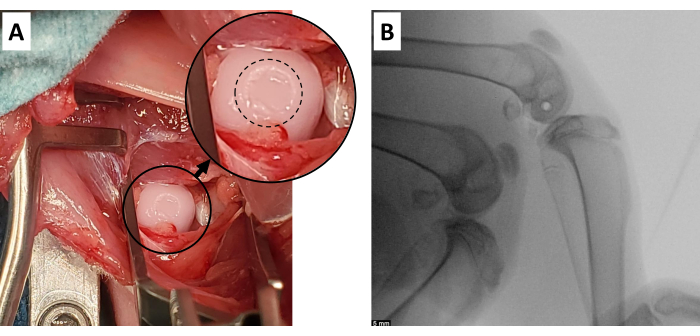
図4:軟骨欠損の成功例 。 (A)このモデルで発生する軟骨損傷の予想される肉眼的外観。挿入図は、埋伏軟骨表面の拡大領域であり、欠損は破線の円で輪郭が描かれています。(B)大腿骨遠位部の適切なスタインマンピン位置で、後軟骨表面から少なくとも5mmの距離があり、関節表面の角度に密接に近似しています(大腿骨顆の放射線透過円)。スケールバー = 5 mm。 この図の拡大版をご覧になるには、ここをクリックしてください。
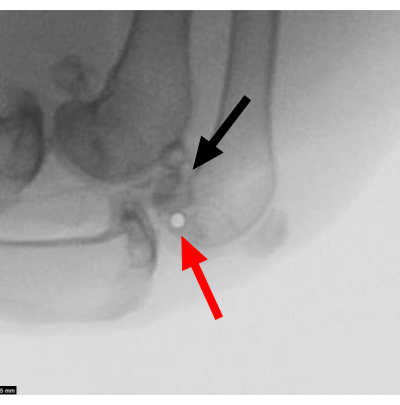
図5:軟骨欠損の失敗。 内側大腿骨顆のピンの位置がずれ、衝撃で骨軟骨骨折を引き起こしたことを示すX線写真。赤い矢印は、スタインマンピンの位置が間違っていることを示しています。黒い矢印は、骨折した内側大腿骨顆を指しています。スケールバー = 5 mm。 この図の拡大版をご覧になるには、ここをクリックしてください。

図6:影響を受けた内側大腿骨顆における変形性関節症の重症度の増加。 サフラニン-O(プロテオグリカン含有量の赤色染色)およびファストグリーン(プロテオグリカン含有量の低い結合組織の青緑色染色)で染色された代表的な(A)対側および(B)影響を受けた内側大腿骨顆(MFC)切片。倍率:400倍;スケールバー = 62.3 μm。 (C)影響を受けたMFCとコントロールMFCのOARSIスコアリング。(D)影響を受けた膝関節からのすべての関節コンパートメントのOARSIスコア。(E)非衝撃対側膝関節からの関節区画のOARSIスコア。(F)埋伏膝と非埋伏膝の関節コンパートメントのOARSIスコア。内側大腿骨顆 (MFC)、内側脛骨プラトー (MTP)、外側脛骨プラトー (LTP)、および外側大腿骨顆 (LFC)。グループ比較は、スチューデントのt検定またはANOVAを使用して実行され、続いてTukeyのHSD事後検定が行われました。 この図の拡大版をご覧になるには、ここをクリックしてください。
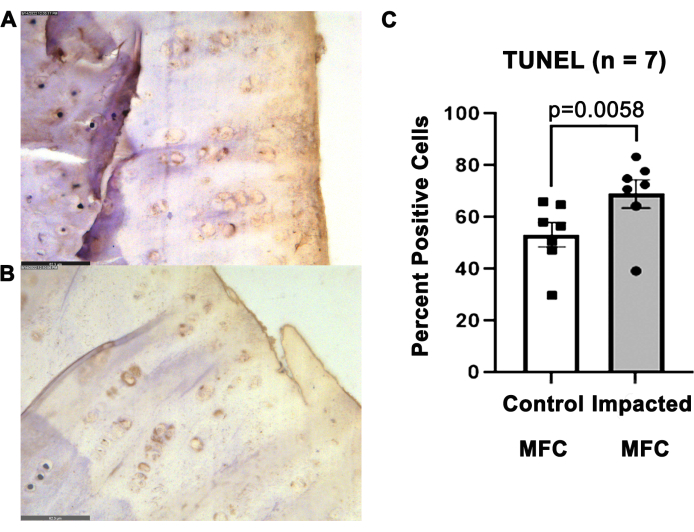
図7:影響を受けたMFCにおけるアポトーシス軟骨細胞の増加。 (A)損傷していないMFCの対側部分と(B)損傷したMFCのTUNEL染色切片を400倍の倍率で衝撃後16週間で撮影した代表的な画像。スケールバー = 62.3 μm. TUNEL陽性は褐色の核で示される。(C)影響を受けたMFCと対照のMFCにおけるTUNEL陽性細胞の定量化。 グループは、対応のあるスチューデントのt検定によって比較されました。 この図の拡大版をご覧になるには、ここをクリックしてください。
表1:研究の影響パラメータ。 これには、ピークストレス(メガパスカル;MPa)、ピーク負荷(ニュートン;N)、負荷率(メガパスカル/ミリ秒;MPa/ms)、衝撃持続時間(ミリ秒; ms)、作業量(ジュール;J)、インパルス(ニュートン秒;N・s)、運動エネルギー(ジュール;J)、加速度 (メートル/秒の 2 乗、m/s2)、およびピーク負荷までの時間 (ミリ秒; ms)。 この表をダウンロードするには、ここをクリックしてください。
表2:衝撃手術時間。この表をダウンロードするには、ここをクリックしてください。
表3:現在説明されているモデルの長所と短所。この表をダウンロードするには、ここをクリックしてください。
補足図1:ベースプラットフォームの詳細な部品説明と部品リスト。このファイルをダウンロードするには、ここをクリックしてください。
補足図2:落錘塔の詳細な部品説明と部品リスト。このファイルをダウンロードするには、ここをクリックしてください。
補足図3:パーツ01-ウサギホルダーテーブルの図面。このファイルをダウンロードするには、ここをクリックしてください。
補足図4:パーツ02-前脚の図面。このファイルをダウンロードするには、ここをクリックしてください。
補足図5:パート03-メインレッグの図面。このファイルをダウンロードするには、ここをクリックしてください。
補足図6:パーツ04-Kワイヤーホルダーベースの図面。このファイルをダウンロードするには、ここをクリックしてください。
補足図7:部品05-スクリューヘッドKワイヤーホルダーの図面。このファイルをダウンロードするには、ここをクリックしてください。
補足図8:パーツ06-ポリエチレンプレートの図面。このファイルをダウンロードするには、ここをクリックしてください。
補足図9:パート07-プレートの図面。このファイルをダウンロードするには、ここをクリックしてください。
補足図10:部品11-トップホルダーの図面。このファイルをダウンロードするには、ここをクリックしてください。
補足図11:パート16-インパクタープレートの図面。このファイルをダウンロードするには、ここをクリックしてください。
補足図12:パート17-インパクタービームの図面。このファイルをダウンロードするには、ここをクリックしてください。
補足図13:パート20-インパクターチップの図面。このファイルをダウンロードするには、ここをクリックしてください。
補足図14:インパクター先端ヘッドの曲率の描画。このファイルをダウンロードするには、ここをクリックしてください。
補足コーディングファイル1: DropTestVIManual(1).vi.このファイルをダウンロードするには、ここをクリックしてください。
補足コーディングファイル2:ImpactAnalysis(1).m.このファイルをダウンロードするには、ここをクリックしてください。
ディスカッション
この外科的処置は、PTOAのモデルでウサギの内側大腿骨顆の体重を支える表面に一貫した軟骨損傷を引き起こすことを目的としています。この手順の利点は、膝への後方アプローチにより、完全な後内側大腿骨顆を直接視覚化でき、約37分で実行できることです(表2)。また、これは開放的な傷害モデルであり、滑膜および関節包への潜在的な損傷による衝撃だけでなく、急性炎症性変化をもたらす可能性があることにも注意すべきである17,44。このモデルの長所と短所を表 3 にまとめます。関節の安定性を確保するために、靭帯および半月板構造を損傷しないように注意が払われました。その結果、衝撃ゾーン外の関節区画(内側および外側脛骨プラトーおよび外側大腿骨顆)の対側対照肢と衝撃肢の間に差は検出されませんでした。
このプロトコルの最も重要な面は、大腿骨顆における孤立した軟骨病変の発生です。スタインマンピンの軌跡は、この方法の成功に大きく影響します。ワイヤーが関節面と平行でない場合、または内側大腿骨顆の中心に対して後方に配置されすぎると、大腿骨顆の骨軟骨骨折につながる可能性があります(図5)。外側上顆は、適切なピンの軌道に使用できる、一貫して触知可能なランドマークです。
軟骨下骨の骨折を伴う動物は、研究から除外する必要があります。現在の研究方法では、術中骨折に続発する失敗率は9.0%(手術67件中6件)でした。この破壊率は、28%の破壊率を誇ったMFCの最近のオープン振り子ベースの衝撃モデルよりも低い45。外科医と研究チームがアプローチと結果に満足するまで、死体標本でこの方法を試すことをお勧めします。この方法は、 in vivo 実験に先立って、後肢の死体標本とニュージーランド白ウサギ全体で試されました。
この方法は、以前に発表されたラパイン急性軟骨損傷生成法に匹敵します。この衝突モデルの荷重率は51.0±16.0MPa/msで、振り子(0.5-6MPa/ms程度)35,46,47、空気圧シリンダ(~0.4MPa/ms)36、バネ式衝撃装置(~530MPa/ms)37を用いた従来研究よりも高かった。現在の衝撃技術は、以前のモデルと比較して中程度の荷重をモデル化し、振り子、バネ式、および空気圧シリンダーによる負荷の以前のモデルと一致する12.3%のCVで81.9±10.1 MPaのピーク応力をもたらし、4つの以前のモデルが10.1〜169 MPaの応力を提供し、CVは0.85〜40.5%の範囲です36,37。45,46。
このモデルの1つの制限は、骨軟骨骨折を生じさせなかったため、臨床現場で見られる典型的な関節内骨折を完全に模倣しなかったことです17。また、衝突前の落錘塔キャリッジの平均加速度は6.4 ± 0.4 m/s 2であり、ボールベアリングの摩擦によるものと思われる重力自由落下加速度の9.8 m/s2よりも低いことも指摘された。それでも、この方法では、完全には理解されていないPTOA病因の影響を受けた軟骨を介した影響を分離することができます。
いくつかの説明された葡瓦礁モデルは軟骨損傷をもたらしますが、ドロップタワーモデルで膝への後方アプローチを利用することは、PTOAを生成するためのシンプルで効率的で臨床的に関連性のある方法として際立っており、その病因の研究と新しい治療法のテストを可能にします。全体として、ラパイン開放後内側大腿骨顆衝撃損傷モデルは、PTOAに関連する細胞および分子イベントを研究し、軟骨損傷を予防または軽減するための新しい治療標的48,49を特定するための有望なプラットフォームです。
開示事項
Roman Natoliは、AO Trauma North Americaで講演を行い、 Current Osteoporosis Reportsのセクションエディターであり、MorganとClaypoolから教科書の印税を受け取っています。トッド・マッキンリーはイノムドからロイヤリティを受け取る。残りの著者は何も開示していません。
謝辞
この研究は、米国陸軍医学研究取得活動の国防総省査読付き医学研究プログラム-医師主導研究賞W81XWH-20-1-0304、NIH NIAMS R01AR076477、およびNIH(AR065971)およびNIH NIAMS助成金R01 AR069657による包括的な筋骨格系T32トレーニングプログラムによって支援されました。著者らは、このプロジェクトに機械加工と製造の専門知識を提供してくれたKevin Carr氏と、組織学を支援してくれたDrew Brown氏とIndiana Center for Musculoskeletal Health Bone Histology Coreに感謝します。
資料
| Name | Company | Catalog Number | Comments |
| Flat head screw | McMaster-Carr | 92210A194 | Stainless steel hex drive flat head screw, 8-32, 1/2" |
| #15 scalpel blades | McKesson | 1029066 | Scalpel McKesson No. 15 Stainless Steel / Plastic Classic Grip Handle Sterile Disposable |
| 1/2”-20 threaded rod | McMaster-Carr | 99065A120 | 1/2”-20 threaded rod |
| 10 mL syringe | McKesson | 1031801 | For irrigation; General Purpose Syringe McKesson 10 mL Blister Pack Luer Lock Tip Without Safety |
| 3 mL syringe | McKesson | 1031804 | For lidocaine/bupiviacaine injection; General Purpose Syringe McKesson 3 mL Blister Pack Luer Lock Tip Without Safety. |
| 3-0 polysorb | Ethicon | J332H | 3-0 Vircryl, CT-2, 1/2 circle, 26 mm, tapered |
| 4-0 monosorb | Ethicon | Z397H | 4-0 PDS 2, FS-2, 3/8 circle, 19mm, cutting edge |
| 5-0 polysorb | Med Vet International | NC9335902 | Med Vet International 5-0 ETHICON COATED VICRYL C-3 |
| Accelerometer | Kistler | 8743A5 | Accelerometer |
| Adson-Browns Forceps | World precision tools | 500177 | Adson-Brown Forceps, 12 cm, Straight, TC Jaws, 7 x 7 Teeth |
| Alfaxalone | Jurox | 49480-002-01 | Alfaxan Multidose by Jurox : 10 mg/mL |
| Buprenorphine | Par Pharmaceuticals | 42023-0179-05 | Buprenorphine HCL injection: 0.3 mg/mL |
| Butorphanol | Zoetis | 54771-2033 | Butorphanol tartrate 10mg/ml by Zoetis |
| Chlorhexidine Hand Scrub | BD | 371073 | BD E-Z Scrub 107 Surgical Scrub Brush/Sponge, 4% CHG, Red |
| Collet | STRYKER | 14023 | Stryker 4100-62 wire Collet 0.28-0.71'' |
| Cordless Driver handpiece | STRYKER | OR-S4300 | Stryker 4300 CD3 Cordless Driver 3 handpiece |
| Cricket Retractors | Novosurgical | G3510 21 | 2x Heiss (Holzheimer) Cross Action Retractor |
| Dissector Scissors | Jorvet labs | J0662 | Aesculap AG, Metzenbaum, Scissors, Straight 5 3/4″ |
| Elizabethian Collar | ElizaSoft | 62054 | ElizaSoft Elizabethan Recovery Collar |
| Enrofloxacin | Custom Meds | Enrofloxacin compounded by Custom Meds | |
| Eye Ointment | Pivetal | 46066-753-55 | Pivetal Articifical Tears- recently recalled |
| Face-mount shaft collar | McMaster-Carr | 5631T11 | Face-mount shaft collar |
| Fast green | Millipore Sigma | F7258 | Fast green |
| Freer | Jorvet labs | J0226Q | Freer elevator |
| Head screw -1 | McMaster-Carr | 91251A197 | Black-oxide alloy steel socket head screw, 8-32, 3/4" |
| Head screw -2 | McMaster-Carr | 92196A194 | Stainless steel socket head screw, 8-32, 1/2" |
| Head screw -3 | McMaster-Carr | 92196A146 | Stainless steel socket head screw, 8-32, 1/2" |
| Head screw -4 | McMaster-Carr | 92196A151 | Stainless steel socket head screw, 6-32, 3/4" |
| Hematoxylin Solution, Gill No. 1 | Millipore Sigma | GHS132-1L | Hematoxylin Solution, Gill No. 1 |
| Hex nut | McMaster-Carr | 91841A007 | Stainless steel hex nut, 6-32 |
| Hold-down toggle clamp | McMaster-Carr | 5126A71 | Hold-down toggle clamp |
| Impact device | n/a | n/a | custom made |
| Impact platform | n/a | n/a | custom made |
| K-wires | Jorvet Labs | J0250A | JorVet Intramedullary Steinman Pins, Trocar-Trocar 1/16" x 7" |
| Lab View | National Instruments | n/a | n/a |
| Load cell | Kistler | 9712B5000 | Load cell |
| MATLAB | The MathWorks Inc. | n/a | n/a |
| Microscope | Leica | DMi-8 | Leica DMi8 microscope with LAS-X software |
| Midazolam | Almaject | 72611-749-10 | Midazolam Hydrochloride injection: 5mg/ml by Almaject |
| milling machine depth stops | McMaster-Carr | 2949A71 | Clamp-on milling machine depth stops |
| Mobile C-arm | Philips | 718095 | BV Pulsera, Mobile C-arm |
| Mounted linear ball bearing | McMaster-Carr | 9338T7 | Mounted linear ball bearing |
| Needle Driver | A2Z Scilab | A2ZTCIN39 | TC Webster Needle Holder Smooth Jaws 5", Premium |
| Pentobarbital | Vortech | 0298-9373-68 | Pentobarbital 390 mg/mL by Vortech |
| Safranin O | Millipore Sigma | HT90432 | Safranin O |
| Small Battery pack | STRYKER | NS014036 | 6212 Small Battery pack- 9.6 V |
| Steel rod, 2’ | McMaster-Carr | 89535K25 | Steel rod, 2’ |
| Sterile Saline | ICU Medical | 6139-22 | AquaLite Solution Pour Bottles, 250 mL |
| Stryker 6110-120 System 6 Battery Charger | STRYKER | OR-S6110-120 | |
| Surgical gloves | McKesson | 1044729 | Surgical Glove McKesson Perry Size 6.5 Sterile Pair Latex Extended Cuff Length Smooth Brown Not Chemo Approved |
| Surgical gown | McKesson | 1104452 | Non-Reinforced Surgical Gown with Towel McKesson Large Blue Sterile AAMI Level 3 Disposable |
| Suture scissors | Jorvet Labs | J0910SA | Super Cut Scissors, Mayo, Straight, 5 1/2″ |
| TUNEL staining kit | ABP Bioscience | A049 | TUNEL Chromogenic Apoptosis Detection Kit |
| Weitlaner Retractors | Fine Science Tools | 17012-11 | 2x Weitlaner-Locktite Retractors |
参考文献
- Thomas, A. C., Hubbard-Turner, T., Wikstrom, E. A., Palmieri-Smith, R. M. Epidemiology of posttraumatic osteoarthritis. Journal of Athletic Training. 52 (6), 491-496 (2017).
- Pasquale, M. K., et al. Healthcare Utilization and costs of knee or hip replacements versus pain-relief injections. American Health Drug Benefits. 8 (7), 384-394 (2015).
- Yao, J. J., et al. Direct Inpatient medical costs of operative treatment of periprosthetic hip and knee infections are twofold higher than those of aseptic revisions. Journal of Bone and Joint Surgery America. 103 (4), 312-318 (2021).
- Anatone, A. J., et al. Decreased implant survival is associated with younger patients undergoing total knee arthroplasty. HSS Journal. 18 (2), 290-296 (2022).
- Stone, B., Nugent, M., Young, S. W., Frampton, C., Hooper, G. J. The lifetime risk of revision following total knee arthroplasty : a New Zealand Joint Registry study. The Bone and Joint Journal. 104-B (2), 235-241 (2022).
- Chen, D., et al. Osteoarthritis: toward a comprehensive understanding of pathological mechanism. Bone Research. 5, 16044 (2017).
- Robinson, W. H., et al. Low-grade inflammation as a key mediator of the pathogenesis of osteoarthritis. Nature Review Rheumatology. 12 (10), 580-592 (2016).
- Perez-Garcia, S., et al. Profile of matrix-remodeling proteinases in osteoarthritis: impact of fibronectin. Cells. 9 (1), 40 (2019).
- Hashimoto, S., Ochs, R. L., Komiya, S., Lotz, M. Linkage of chondrocyte apoptosis and cartilage degradation in human osteoarthritis. Arthritis Rheumatology. 41 (9), 1632-1638 (1998).
- Natoli, R. M., Athanasiou, K. A. Traumatic loading of articular cartilage: Mechanical and biological responses and post-injury treatment. Biorheology. 46 (6), 451-485 (2009).
- Coleman, M. C., Brouillette, M. J., Andresen, N. S., Oberley-Deegan, R. E., Martin, J. M. Differential effects of superoxide dismutase mimetics after mechanical overload of articular cartilage. Antioxidants (Basel). 6 (4), 98 (2017).
- Goodwin, W., et al. Rotenone prevents impact-induced chondrocyte death. Journal of Orthopaedic Research. 28 (8), 1057-1063 (2010).
- Wolff, K. J., et al. Mechanical stress and ATP synthesis are coupled by mitochondrial oxidants in articular cartilage. Journal of Orthopaedic Research. 31 (2), 191-196 (2013).
- Delco, M. L., Bonnevie, E. D., Bonassar, L. J., Fortier, L. A. Mitochondrial dysfunction is an acute response of articular chondrocytes to mechanical injury. Journal of Orthopaedic Research. 36 (2), 739-750 (2018).
- Coleman, M. C., Ramakrishnan, P. S., Brouillette, M. J., Martin, J. A. Injurious loading of articular cartilage compromises chondrocyte respiratory function. Arthritis Rheumatology. 68 (3), 662-671 (2016).
- Bobinac, D., Spanjol, J., Zoricic, S., Maric, I. Changes in articular cartilage and subchondral bone histomorphometry in osteoarthritic knee joints in humans. Bone. 32 (3), 284-290 (2003).
- Coleman, M. C., et al. Targeting mitochondrial responses to intra-articular fracture to prevent posttraumatic osteoarthritis. Science Translational Medicine. 10 (427), eaan5372 (2018).
- Heraud, F., Heraud, A., Harmand, M. F. Apoptosis in normal and osteoarthritic human articular cartilage. Annals of Rheumatological Diseases. 59 (12), 959-965 (2000).
- Narez, G. E., Fischenich, K. M., Donahue, T. L. H. Experimental animal models of post-traumatic osteoarthritis of the knee. Orthopedic Reviews (Pavia). 12 (2), 8448 (2020).
- Fischenich, K. M., et al. Chronic changes in the articular cartilage and meniscus following traumatic impact to the lapine knee. Journal of Biomechanics. 48 (2), 246-253 (2015).
- Isaac, D. I., Meyer, E. G., Kopke, K. S., Haut, R. C. Chronic changes in the rabbit tibial plateau following blunt trauma to the tibiofemoral joint. Journal of Biomechanics. 43 (9), 1682-1688 (2010).
- Wei, F., et al. Post-traumatic osteoarthritis in rabbits following traumatic injury and surgical reconstruction of the knee. Annals of Biomedical Engineering. 50 (2), 169-182 (2022).
- Terracciano, R., et al. Quantitative high-resolution 7T MRI to assess longitudinal changes in articular cartilage after anterior cruciate ligament injury in a rabbit model of post-traumatic osteoarthritis. Osteoarthritis and Cartilage Open. 4 (2), 100259 (2022).
- Huang, K., Cai, H. L., Zhang, P. L., Wu, L. D. Comparison between two rabbit models of posttraumatic osteoarthritis: A longitudinal tear in the medial meniscus and anterior cruciate ligament transection. Journal of Orthopaedic Research. 38 (12), 2721-2730 (2020).
- Sun, Z. B., Peng, H. Experimental Study on the prevention of posttraumatic osteoarthritis in the rabbit knee using a hinged external fixator in combination with exercises. Journal of Investigative Surgery. 32 (6), 552-559 (2019).
- Gardner, M. J., et al. The incidence of soft tissue injury in operative tibial plateau fractures: a magnetic resonance imaging analysis of 103 patients. Journal of Orthopedic Trauma. 19 (2), 79-84 (2005).
- Dilley, J. E. B. . M. A., Roman, N., McKinley, T. O., Sankar, U. Post-traumatic osteoarthritis: A review of pathogenic mechanisms and novel targets for mitigation. Bone Reports. 18, 101658 (2023).
- Seol, D., et al. Effects of knockout of the receptor for advanced glycation end-products on bone mineral density and synovitis in mice with intra-articular fractures. Journal of Orthopedic Research. 36 (9), 2439-2449 (2018).
- Furman, B. D., et al. Joint degeneration following closed intraarticular fracture in the mouse knee: a model of posttraumatic arthritis. Journal of Orthopedic Research. 25 (5), 578-592 (2007).
- Glasson, S. S., Chambers, M. G., Van Den Berg, W. B., Little, C. B. The OARSI histopathology initiative - recommendations for histological assessments of osteoarthritis in the mouse. Osteoarthritis Cartilage. 18 Suppl 3, S17-S23 (2010).
- McCoy, A. M. Animal models of osteoarthritis: comparisons and key considerations. Veterinary Pathology. 52 (5), 803-818 (2015).
- Fening, S. D., Jones, M. H., Moutzouros, V., Downs, B., Miniaci, A. Method for Delivering a controlled impact to articular cartilage in the rabbit knee. Cartilage. 1 (3), 211-216 (2010).
- Leucht, F., et al. Development of a new biomechanically defined single impact rabbit cartilage trauma model for in vivo-studies. Journal of Investigative Surgery. 25 (4), 235-241 (2012).
- Vrahas, M. S., Smith, G. A., Rosler, D. M., Baratta, R. V. Method to impact in vivo rabbit femoral cartilage with blows of quantifiable stress. Journal of Orthopedic Research. 15 (2), 314-317 (1997).
- Borrelli, J., Burns, M. E., Ricci, W. M., Silva, M. J. A method for delivering variable impact stresses to the articular cartilage of rabbit knees. Journal of Orthopedic Trauma. 16 (3), 182-188 (2002).
- Milentijevic, D., Rubel, I. F., Liew, A. S., Helfet, D. L., Torzilli, P. A. An in vivo rabbit model for cartilage trauma: a preliminary study of the influence of impact stress magnitude on chondrocyte death and matrix damage. Journal of Orthopedic Trauma. 19 (7), 466-473 (2005).
- Alexander, P. G., et al. An In vivo lapine model for impact-induced injury and osteoarthritic degeneration of articular cartilage. Cartilage. 3 (4), 323-333 (2012).
- Bonitsky, C. M., et al. Genipin crosslinking decreases the mechanical wear and biochemical degradation of impacted cartilage in vitro. Journal of Orthopedic Research. 35 (3), 558-565 (2017).
- Bartley, K. A., Johnson, C. H. Human Infant pants for postoperative protection during social housing of new zealand white rabbits (Oryctolagus cuniculus). Journal of the American Association for Laboratory Animal Science. 58 (4), 510-516 (2019).
- Lillie, R. D., Fullmer, H. M. . Histopathologic technic and practical histochemistry. , (1976).
- Prophet, E., Mills, B., Arrington, J. B., Sobin, L. H. . Armed Forces Institute of Pathology: Laboratory Methods in Histotechnology. Washington DC: American Registry of Pathology. , (1992).
- Dilley, J. E., et al. CAMKK2 is upregulated in primary human osteoarthritis and its inhibition protects against chondrocyte apoptosis. Osteoarthritis and Cartilage. 31 (7), 908-918 (2023).
- Pritzker, K. P., et al. Osteoarthritis cartilage histopathology: grading and staging. Osteoarthritis Cartilage. 14 (1), 13-29 (2006).
- Christiansen, B. A., et al. Non-invasive mouse models of post-traumatic osteoarthritis. Osteoarthritis Cartilage. 23 (10), 1627-1638 (2015).
- Borrelli, J., Zaegel, M. A., Martinez, M. D., Silva, M. J. Diminished cartilage creep properties and increased trabecular bone density following a single, sub-fracture impact of the rabbit femoral condyle. Journal of Orthopaedic Research. 28 (10), 1307-1314 (2010).
- Borrelli, J., Silva, M. J., Zaegel, M. A., Franz, C., Sandell, L. J. Single high-energy impact load causes posttraumatic OA in young rabbits via a decrease in cellular metabolism. Journal of Orthopedic Research. 27 (3), 347-352 (2009).
- Borrelli, J., Zhu, Y., Burns, M., Sandell, L., Silva, M. J. Cartilage tolerates single impact loads of as much as half the joint fracture threshold. Clinical Orthopedics and Related Research. 426, 266-273 (2004).
- Karnik, S., et al. Decreased SIRT1 activity is involved in the acute injury response of chondrocytes to ex vivo injurious mechanical overload. International Journal of Molecular Sciences. 24 (7), 6521 (2023).
- Mevel, E., et al. Systemic inhibition or global deletion of CaMKK2 protects against post-traumatic osteoarthritis. Osteoarthritis Cartilage. 30 (1), 124-136 (2022).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved