Method Article
発達的心毒性の評価における強力なツールとしての鶏胚の使用
要約
鶏の胚は、古典的な発達モデルとして、様々な環境汚染物質への暴露後の発達的な心毒性を評価するために私たちの研究室で使用されています。この原稿には、露光法と形態・機能評価法が定められております。
要約
鶏の胚は、発達研究における古典的なモデルです。鶏胚の発達の間、心臓の発達の時間枠は明確に定義されており、複数の方法を用いて正確かつタイムリーな暴露を達成することは比較的容易である。さらに、鶏の胚の心臓の発達のプロセスは哺乳類に似ていて、4つの心臓を生じさせ、発達的心毒性の評価において貴重な代替モデルとなる。当研究室では、鶏胚モデルは、PFAS(PFAS)およびポリフルオロアルキル物質、粒子状物質(PM)、ディーゼル排気(DE)およびナノ材料を含む様々な環境汚染物質への暴露後の発達的心毒性の評価に日常的に使用されています。露光時間は、開発の開始(胚の日0、ED0)から孵化の前日まで、必要性に基づいて自由に選択することができる。主な暴露方法には、空気細胞注射、直接マイクロインジェクション、および空気細胞吸入(もともと私たちの研究室で開発された)が含まれ、現在利用可能なエンドポイントには、心機能(心電図)、形態(組織学的評価)および分子生物学的評価(免疫組織化学、qRT-PCR、ウェスタンブロッティングなど)が含まれます。もちろん、鶏胚モデルには、抗体の入手が限られているなど、独自の制限があります。それにもかかわらず、より多くの実験室がこのモデルを利用し始めると、それは発達的な心毒性の研究に大きな貢献をするために使用することができる。
概要
鶏の胚は、200年以上にわたって使用されてきた古典的な発達モデルです。鶏胚モデルは、従来のモデルと比較して様々な利点を有する。まず、70年以上前に、鶏胚の正常な発達は、鶏胚の発達中に合計46段階が正確な時間と形態学的特徴で定義され、異常な発達の検出を促進するハンブルガー・ハミルトンステージングガイド2で非常に明確に示されていた。さらに、鶏胚モデルは、比較的低コストで冗長な量、比較的正確な暴露量制御、シェル内の独立した閉じたシステム、発達中の胚の容易な操作など、強力な毒物学的評価モデルとして使用される可能性を保証する他の特徴を有する。
心毒性では、鶏の胚は哺乳類の心臓に似ているが、より厚い壁を有する4つのチャンバー心臓を特徴とし、形態学的評価を容易にする。さらに、鶏の胚は哺乳類モデルでは不可能な発達吸入暴露を可能にする:発達の後半段階では、鶏の胚は内部呼吸から外部呼吸(肺を介して酸素を得る)に移行する。後者は、胚がくちばしで空気細胞膜を貫通し、空気3を呼吸し始め、空気細胞をミニ吸入室にすることを要求する。この現象を利用して、心臓(および他の器官)に対するガス汚染物質の毒物学的影響は、専用の吸入室器具を必要とせずに評価され得る。
本稿では、いくつかの曝露/エンドポイント評価方法が記載されており、そのすべてが、環境汚染物質への暴露後の発達心毒性の評価において鶏胚を強力なツールにするのに役立つ。
プロトコル
記載されているすべての手順は、青島大学の施設動物のケアと使用委員会(IACUC)によって承認されました。私たちの研究室では、卵を2つのインキュベーターでインキュベーターでインキュベートしました。卵はインキュベーターで直立して保持され、無作為に棚に置かれました。卵のインキュベーション条件は次の通りであった:インキュベーション温度は37.9°Cで始まり、インキュベーションが進むにつれて徐々に37.1°Cに減少した。湿度は50%から始まり、徐々に70%に増加しました。
1. 露光方法
注:鶏の胚への環境汚染物質の暴露は、いくつかの方法で達成することができます。このセクションでは、3 つの日常的に使用されるメソッドについて詳しく説明します。
- 空気細胞の注入(図1)
注:これは、鶏の胚4、5、6に対する古典的な暴露方法であり、幅広い材料に適しており、開発の初めからハッチ(ED20)の前の日まで、非常に広い時間枠で行うことができる。●ひまわり油を車両として使用。これまでの研究では、ヒマワリ油を注入した未治療の胚と胚の間で死亡率、孵化性、または体重に有意な変化は観察されていないことが示されている。- 必要な試薬/ツールを準備する:75%エタノール、ティッシュペーパー、金属プローブ(任意の鋭い金属針/スティック/awlで代用することができます)、溶かしたパラフィン、ブラシ、ポビドネヨウ化液、ピペット、ピペットチップ、カリングランプ、混合剤を投与します。ヒマワリ油(推奨)4との混合を調製します。他の希釈剤を使用するには、車両制御(未治療の胚に対して)を行います。
- 卵の表面をポビドンヨウ化液(市販のポビドンヨウ化液1:5を脱イオン水で希釈)で洗浄し、卵殻をスクラブせずにティッシュペーパーで浸乾させます。スクラブは、シェルの外側にコーティング保護層を破ります。
- 暗い部屋で卵をろうそくに入れ、空気セルに鉛筆で印を付けます。殻に亀裂が入った卵を除外します。通常孵化する可能性が非常に低いため、鈍い先端の代わりに空気細胞を持つ卵を除外します。
- 75%エタノールで空気細胞面積を消毒し、次いで金属プローブで空気細胞領域の中心に小さな穴を開けます。プローブを空気細胞の奥深くに突き刺さないか、内部膜が損傷する可能性があり、代わりにプローブの先端でシェルを壊すだけです。穴が細かいピペットチップに収まるほど大きくない場合は、穴が10 μLピペットチップの挿入を可能にするほど大きくなるまで、既存の穴の近くでシェルを再び壊します。
- この混合剤を激しくボルテックスし、ピペットチップに溶液を直ちに引き出す。推奨される注入量は、10グラム当たり1μL(50グラム卵の場合は5μLの注入量)であり、より大きな注入量は、発達中の胚に対して低酸素または無酸素状態を生じる可能性がある。所望のmg/卵のkgの線量のための投与の溶液の濃度を計算する。
- ピペットチップを穴に差し込み、先端が内膜に触れます。徐々に混合剤を排出し、少なくとも10秒間保持し(粘性油を完全に分配させ)、先端を取り除きます。
- 穴をブラシと溶かしたパラフィンの滴で密封します。溶かしたパラフィンを内膜に滴り落とさないように注意してください。
- 密封したら、卵を目的の胚期に達するまでインキュベーターに入れます。既に発生している胚では、低い環境温度による潜在的な胚の損失を防ぐために、できるだけ早く全体のプロセスを実行します。
- マイクロインジェクション (図 2)
注:これは、より直接的な暴露方法であり、対象物質への決定的な暴露をもたらし、特に、古典的な空気細胞注入は化合物が内膜に浸透する時間を必要とするため、作用の短い持続時間を有する化合物(例えば、レンチウイルス)に適している。この方法は、空気細胞注入によって満足のいく結果が得られなければ試みることができる。この方法は、初期の胚(ED2まで)に最適ですが、古い胚(胚喪失のリスクが高い)にも対して行うことができます。- 必要な試薬/ツールを準備する:75%エタノール、ポビドネヨウ化物溶液、マイクロインジェクター(5 μL)、金属プローブ(任意の鋭い金属針/スティック/アウルで代用できる)、細かい鉗子、テープ。また、大幅に孵化に影響を与えることなく、注射制御として機能する滅菌生理食土との投与混合物を準備します。汚染された注射は劇的に死亡率を増加させるので、生理食前の無菌性を確保する。
- 1.1.2 の説明に従って卵をきれいにします。
- 1.1.3に記載されているように、卵をろうそく。
- 75%エタノールで空気細胞面積を消毒し、次いで金属プローブで空気細胞領域の中心に小さな穴を開けます。プローブを空気細胞の奥深くに突き刺さないか、内部膜が損傷する可能性があり、代わりにプローブの先端でシェルを壊すだけです。その後、細かい鉗子を使用して、直径が約2mmになるまで慎重に穴を拡大し、内膜の視覚的な確認を可能にします。
- マイクロインジェクターに溶液をロード(最大注入量:0.5 μL/10 gの卵。(例えば、50gの卵の場合は2.5 μL)、穴を通して約2〜3mmの内膜に針を慎重に挿入します。溶液をそっと分配し、針を取り除きます。針を膜に対してできるだけ垂直に保ちます。
- 小さなテープで穴を密封します。完全に、その後のインキュベーション中に胚の脱水と死を防ぐために穴を覆う。それにもかかわらず、低酸素症を防ぐために大きすぎるテープの破片を避けてください。
- 密封したら、卵を目的の胚期に達するまでインキュベーターに入れます。既に発生している胚では、環境温度の低さによる潜在的な胚の損失を防ぐために、できるだけ早く全プロセスを実行します。
- 空気細胞吸入(図3)
注:これは、後期鶏胚が空気を吸い始める空気細胞を利用した新しい吸入方法です。それはガスまたはエアロゾルの露出のために適し、非常に初期の吸入の露出を達成し、彼らは人生で初めて開くときに目標ガス/エアロゾルで肺を満たす可能性があります。- 次の必要な試薬/ツールを準備する:サンプリングバッグ(PVFバッグ、露出前のガス/エアロゾルサンプルの貯蔵用)、カテーテル針、注射器、金属プローブ(任意の鋭い金属針/スティック/アウルで代用可能)、テープ、ヒュームフード。
- 1.1.2に記載されているように卵をきれいにし、1.1.3(インキュベーション前に空気細胞をマークする必要はありません)に記載されているようにそれらをろうそくにし、ED17まで処理せずに卵をインキュベートします。
- 空気細胞領域をマークするためにED17で卵をろうそく。
- ED18では、インキュベーターから卵を取り出し、75%エタノールで空気細胞領域を消毒し、空気セルの両側に2つの小さな穴を慎重に掘削します。1つはガス/エアロゾルの注入用で、もう1つは空気の排出用です。注入穴のサイズがカテーテル針が挿入するのに十分になるように穴のサイズを慎重に制御し、排出穴の直径は少し大きい(約1mm)。。
- カテーテル針に取り付けられた注射器を用いて、注入穴から10mLのターゲットガス/エアロゾルを静かに注入します。吸入制御群に空気を注入し、負の対照群8に有意な差を持たないはずである。カテーテル針に対して圧力を加え(弾性針をシェルに押し付けることができる適切な圧力で)、注入穴からの漏れを最小限に抑えます。その後すぐに両方の穴をテープで密封し、卵をインキュベーターに戻します。
注:この手順は、オペレータによるガス/エアロゾルの吸入を防ぐために、ヒュームフードで行う必要があります。 - 1時間後に説明した手順を繰り返し、エアセル全体がターゲットガス/エアロゾルで満杯になっていることを確認します(オプション)。
- ED19で説明した手順を再度繰り返します(オプション)。露出を繰り返し、ハッチまで一貫した露出を確保するのに役立ちます。露出時間の概算値を示すハッチング時間を記録します。
- 所望の露出が行われ、密封されたら、孵化のために卵をインキュベーターに入れる。卵が培養器の外で過ごす時間を最小限に抑え、低い環境温度による死を防ぎます。
2. エンドポイント評価方法
注:開発中の胚に対する汚染物質の被曝後、心毒性を含むいくつかの毒性パラメータを評価することができる。このセクションでは、よく使用される 2 つの特定の方法について詳しく説明します。
- 心電図(図4)
注:羽根の存在により、鶏の孵化で非侵襲的な心電図を行うことは不可能です。したがって、電極の皮下移植が必須であり、麻酔を必要とする。実験室で使用される用量は、腹腔内注射を介して33mg / kgペントバルビタールです(一部の鶏は最大50%の用量増加を必要とするかもしれません)。この方法は、90%以上の動物の安定した心電図を生じ、心拍数の分析を可能にする。- 必要な試薬/工具を用意します:生理食音、注射器、電気バランス、ヒーター(必要に応じて)のペントバルビタール溶液1%、2チャネルの金属針電極付き心電図器(例えばBL-420E+)
- バランスで鶏の重量を量り、ペントバルビタール溶液の必要量を計算し、鶏を注入します。30gの鶏の場合は、ペントバルビタール溶液の0.1mLが必要です。黄身は真ん中にあり、注射が有効でない可能性があるため、腹部の側側に注射が行われていることを確認してください。
- 注入された鶏が麻酔されるまで待ちます(手に鶏を持って、首に緊張がなく、頭を自由に振ることができる場合は、麻酔で十分です)。操作テーブルに鶏を置きます(室温が20°C未満の場合はヒーターが必要です)。
- 腹部の両側から2つの針電極を皮下に挿入する。針が皮膚を少し持ち上げ、そこから針を挿入することによって腹腔に入らないようにしてください。挿入したら、胸腔の側面に届くまで針を慎重に前方に押し出します。針が体の奥深くまで入ったり、皮膚から突き出たりしないようにしてください。
- 心電図装置で測定を行います。心電図が可能な他の同様の器具を使用することができる。
- もし鶏が犠牲になる場合は、既に麻酔下にあるため、心電図後に安楽死を行う。鶏が生き残るためには、ケージに戻し、目を覚ますまで暖かくなります。それらをインキュベーターに戻すことは別の選択肢です。
- ヒストモルホトリー (図5)
注:心臓の横切り部で右心室壁の厚さを評価する特定の方法が開発されています。心エコーを介した右心室次元の形態学的評価は、右心室の不規則な形状のために100%正確ではなく、この方法は右心室の形態学的評価において良い補足として役立つ可能性がある。- 必要な試薬/ツールを準備します:4%リン酸緩衝ホルムアルデヒド、シャープブレード、リン酸緩衝生理食塩水、ペーパータオル、電気バランス、小さみはさみ、一般的な組織学的処理剤(グレードエタノール、キシレン、パラフィン)。
- 動物が犠牲になったら、水を使って羽を濡らします。これは、胸を開きながら羽を飛ばすことによって潜在的な汚染を最小限に抑えるためです。
- 胸腔を慎重に開け、心臓を傷つけることなく。小さいはさみを使って脈管を切り、心臓を胸腔からそっと取り除きます。心臓に取り付けられた小片(約1〜2mm)の血管を、心臓に損傷を与えることなく、心臓の後の取り扱いに便利な場合があります。
- 一度除去, 冷たいリン酸緩衝生理食塩液で心臓をすすいで血液を除去し、筋肉をリラックス.その後、正確な体重の読み取りのために重量を量る前にペーパータオルで心臓を乾燥させます。心臓を室温で24時間、10倍の体積固定液(4%リン酸緩衝ホルムアルデヒド)に入れます。固定組織は、その後パラフィンブロックに処理されるか、または4°Cで何年も保存される(免疫組織化学が計画されている場合は推奨されない)。
- 埋め込む前に、後で処理しやすくするために、頂点(図5A)から心臓を数える約60%の長さで組織を切断します。マイクロトームブレードは、迅速かつ垂直なクリーンカットをお勧めします。1日より古い鶏の場合は、パラフィンの浸透を容易にするために頂点から約25〜30%の長さで別のカットを行い、組織が組織カセットに収まるようにします。
- 以下の条件で組織を処理する(必要に応じて調整する):1時間で70%エタノール、1時間用80%エタノール、1時間x2の95%エタノール、 100%エタノールを30分間x2、キシレンを5分間x2、パラフィン(融点52~54°C)を1.5時間、パラフィン(融点62~64°C)を1時間、3:1のパラフィン(融点62-64°C)とパラフィン(融点52°C)に包み込む。
- 組織を6μmの厚さに切り離します。右心室の解剖学的ランドマーク(隔隔辺柱柱)の存在と大きさを確認することにより、断面の同一の相対位置を慎重に維持する。各セクションに適度な長さのランドマークを確認します(図5B、矢印)。
- ロゴ プログラマを使用して 2 つの電子ルーラーを作成する: Ruler 1 は、2 つの隣接するメジャー ラインの間に 22.5° の中間点にアタッチされた 7 半径の測定ラインを持つ直線です。ルーラー 2 は、T 図形の垂直な 2 本の線だけです (図 5B)。
- 2つのソフトウェアプログラムで測定:アドビフォトショップとイメージJ。
- Photoshop で、ルーラー 1 (再シェーピングなし) のサイズを変更して、定規の両端を自由な右心室壁の両端に配置し、定規 1 の 7 つの測定線がそれぞれ右心室壁の内側に合うようにします。次に、ルーラー2を使用して、内心室壁から外部心室壁までの垂直測定を行います(図5B)。
- ImageJ を使用して、各心臓の 7 つの測定を行います。
- 特定のニーズに応じて、1つの代表的な右心室壁厚さの7つの測定値または平均を分析します。特定の心室壁の厚さの変化のために心臓の重量全体に正規化します。
結果
露出結果
空気細胞の注入
空気細胞注射は、開発中の鶏胚を様々な薬剤に効果的に暴露することができ、その後、胚/孵化鶏の採取サンプル(血清、組織など)で検出される可能性があります。ここに、パーフルオロオクタン酸(PFOA)を空気細胞注入した例を挙げ、次いで、血清PFOA濃度を超高性能液体クロマトグラフィー質量分析法で測定した。血清濃度は、注射された用量に対応し、この手順の有効性を示す(図6)。
マイクロインジェクション
マイクロインジェクションは、現像する胚を、内膜に効果的に浸透しない可能性のある薬剤、またはレンチウイルスのような短期間の作用を伴って曝露する可能性がある。ここで、この方法で2日目にレンチウイルスを注射し、次いで胚15日目の胚の心臓に有意な緑色蛍光が認められた例を示し、レンチウイルストランスフェクションの有効性を示す(図7)。
空気細胞注入
空気細胞注入は、外部呼吸の開始段階で少量のガス/エアロゾル吸入暴露のために非常にうまく機能する新しい方法です。ここでは、胚18,19日目にディーゼル排気を空気細胞に注入した例であり、心臓および肺組織に有意な線維変化をもたらした(図8)。
エンドポイント評価結果
心電図の結果
2つの電極の制限により、3チャンネルの心電図のみが示され得る。しかし、それらはr波を区別するのに十分であり、したがって、機能評価に使用される可能性があります。実際の例では、ディーゼル排気にさらされた鶏の心電図は、R-R間隔を有意に短くし、機能的変化を示す(図9)。
組織病理学の結果
右心室壁厚評価の私達の方法は成功したいくつかの研究5、7、8、9、10、11、12で使用された。我々の以前の研究の1つでは、ディーゼル排気暴露は右心室壁を厚くした(図10)。

図1:空気細胞注入の実演 未発達の肥沃な卵子が写真に示されているが、すべての異なる段階で胚がこの方法で暴露されるかもしれない。 この図の大きなバージョンを表示するには、ここをクリックしてください。

図2:マイクロインジェクションのデモンストレーション 初期の胚は、この方法の好ましい露光時間ポイントである画像に示されていますが、他の時点も試みられる可能性があります。 この図の大きなバージョンを表示するには、ここをクリックしてください。

図3:空気細胞注入のデモンストレーション 内部ピッピングを受けている後期胚は、この方法の好ましい露光時間である画像に示されている。操作の4つの段階が示された。1:無傷の胚。2:2つの穴が作られました。3:注入が行われている。PVFサンプリングバッグも左下に表示されます。4:注入が終了し、テープで密閉された穴。 この図の大きなバージョンを表示するには、ここをクリックしてください。

図4: 心電図のデモンストレーション 左上のパネルは、孵化鶏が麻酔を受け、心電図測定を受けている様子を示した。右上パネルは、電極が取り付けられた心電図装置を示しています。下のパネルは鶏から取得した代表的な心電図を示す。 この図の大きなバージョンを表示するには、ここをクリックしてください。

図5:右心室壁厚の病理組織学的評価のデモンストレーション(ヘマトキシリンとエオシン染色)(A)埋め込む前の鶏の心臓の切断位置の実証(B)右心室壁厚の測定のデモンストレーション。スケールバーは1000 μmを表します。青い円は、右心室壁の7つの測定点を示しています。赤い円は、右心室壁の外側の測定点を示します。矢印は、適切な断面位置の解剖学的ランドマークを示しています。この図は江ら毒物学から修正されました。293 (1-3), 97-106 (2012)7.この図の大きなバージョンを表示するには、ここをクリックしてください。
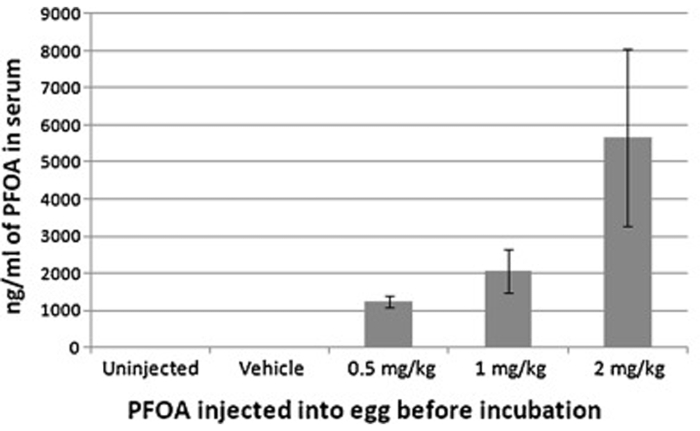
図6:インキュベーション前に0、0.5、1または2mg/卵kgパーフルオロオクタン酸を用いた空気細胞注射後の鶏の孵化によるパーフルオロオクタン酸の血清濃度。 得られた血清濃度は、注入された用量に対応し、空気細胞注入の有効性を示す。この図は江ら 毒物学から修正されました。 293 (1-3), 97-106 (2012)7. この図の大きなバージョンを表示するには、ここをクリックしてください。

図7:マイクロインジェクション暴露後のレンチウイルストランスフェクション効果の実証(クライオ切除後の直接観察) 左パネルは明視野画像を示し、右パネルは同じ組織切片に緑色の蛍光を示した。胚胚1日目に2羽の鶏胚をレンチウイルスまたは対照を注射し、その後胚15日目までインキュベートした。心臓を凍結切り離し、蛍光顕微鏡下で直接可視化した。(A)対照群は、ほとんど緑色蛍光が存在していた。(B)レンチウイルス暴露群は、有意な緑色蛍光が認められ、マイクロインジェクション後のレンチウイルストランスフェクションの有効性を示す。スケールバーは125 μmを表します。この図は、Zhaoらから変更されました . 環境毒性と薬理学. 56,136-144 (2017)11. この図の大きなバージョンを表示するには、ここをクリックしてください。

図8:空気細胞注入の有効性の実例 鶏の胚は18日目と19日目にディーゼル排気を注入し、次いで孵化した鶏を0、1または2週間保管し、その後犠牲にした。心臓組織は、線維性病変に対するマッソントリクローム染色で評価した。矢印は線維性病変(青色染色)を示した。*:対照と統計的に異なる(P<0.05分散分析と最も有意でない差検定)。スケールバーは150 μmを表します。この図は江ら環境 汚染から修正されました。264, 114718 (2020)8. この図の大きなバージョンを表示するには、ここをクリックしてください。

図9:心電図の有効性の実態を示す。 鶏の胚は、胚18、19日目にディーゼル排気を注入し、次いで孵化した鶏を0、1または2週間保持し、次いで心電図を行った。R-R間隔を有意に短くした鶏は、空気細胞注入を介してディーゼル排気にさらされた鶏において観察され、この方法の有効性を示す。*:対照と統計的に異なる(P<0.05分散分析と最も有意でない差検定)。この図は江ら環境 汚染から修正されました。264, 114718 (20208. この図の大きなバージョンを表示するには、ここをクリックしてください。
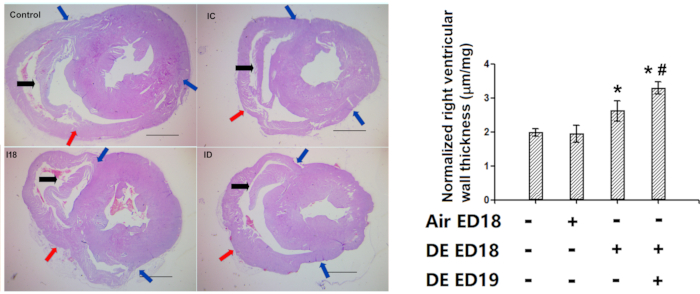
図10:右心室壁厚の測定(ヘマトキシリンとエオシン染色)の有効性の実証。 鶏の胚は、胚の日18と19でディーゼル排気を注入し、その後、孵化した鶏を1週間保持し、次に右心室壁の厚さの組織学的評価を行った。A:心臓断面の代表的な写真。すべての右心室に解剖学的マーカーが存在することに注意してください(古い鶏では、マーカーは所望の位置で少し長くなる傾向があり、測定の精度に影響を与えません)。B:最初に標準的なスライドで実際の長さに変換された右心室壁厚の定量化、そして心臓全体の重量で正規化されたum/ugの形で表した。青い矢印:自由な右心室壁の両端。赤い矢印: 右心室壁の中間点。黒い矢印:解剖学的マーカー。*:対照と統計的に異なる(P<0.05分散分析と最も有意でない差検定)。スケールバーは1000 μmを表します。この図は江ら環境 汚染から修正されました。264, 114718 (2020)8. この図の大きなバージョンを表示するには、ここをクリックしてください。
ディスカッション
鶏の胚は、200年の間、発達研究における古典的なモデルであった1.この原稿に記載されている我々の方法は、パーフルオロオクタン酸、粒子状物質、およびディーゼル排気を含むいくつかの環境汚染物質の評価に使用されており、成功した5、7、8、9、10、11、12。これらの方法により、発達的心毒性は費用対効果が高く、明確に示された。さらに、他の目的の化合物で鶏の胚を暴露し、潜在的な発達心毒性を評価することは困難ではありません。
空気細胞注入法は、多くの研究で以前に使用される古典的な方法です 13,14,15,これは便利で効果的です.げっ歯類モデル16、17、18などの他の発達暴露方法と比較して、それは母体の効果および多様な排泄による変動性を大幅に減少させる閉鎖的なシステムへの直接露出を特色にする。マイクロインジェクションは、空気細胞注入法の強化であり、初期胚の発達の上または近傍での決定的な暴露を確実にし、げっ歯類モデル19,20における子宮注射と同様の効果を達成する可能性がある。子宮注射と比較すると、我々の方法は比較的容易な操作ステップで注入の視覚確認を可能にし、正確な注入は、胚の実際の量および重量が容易に得られにくい子宮内注入では不可能である卵重量を制御することによって容易に達成される。輸液法は主に肺系の吸入剤の評価用であるが、心毒性と肺毒性がしばしば同時に起こる。この方法は、少量のガスまたはエアロゾルが注入されるエアセルを利用し、特定の吸入室を必要とせずにガス/エアロゾルを連続吸入することができます。対応するげっ歯類モデルは、比較的大量のガス/エアロゾルと大型の高価な吸入器21,22を使用する必要があります。
私たちの研究室で日常的にテストされた2つのエンドポイント、右心室壁の厚さの心電図および組織形態学的評価は、それぞれ毒性物質暴露後の機能的および形態学的変化を表す。右心室壁の厚さの評価は、右心室23の非対称かつ複雑な三日月形状のために、右心室の伝統的な心エコー検査ベースの評価は通常困難であり、非常に正確ではないため、右心室壁の包括的な理解を得る上で特定の利点を有する。我々の方法は、代表的な位置で右心室壁の厚さに関する追加情報を補完することによって、この不正確さを克服するのに役立つかもしれません。現在は全マニュアルですが、将来的には自動で測定が行われる可能性があり、測定点数が大幅に増加し、この方法の精度がさらに向上します。
鶏の胚ベースの発達モデルは、比較的正確な暴露量を提供する能力、シェル内の独立した暴露システム、および発達中の胚の容易な操作など、毒物学的研究でいくつかの利点を有する。心毒性に関しては、鶏は比較的大きな心臓と厚い心室壁を有し、容易に組織形態学的評価を可能にする。抗体/プライマーの入手可能性や、ハッチ後に鶏を飼育する場合のげっ歯類と比較して余分なケージスペース要件など、いくつかの欠点があります。それにもかかわらず、鶏の胚はまだ潜在的な発達心毒性評価に使用される良い代替毒物学的モデルです。
開示事項
著者らは利益相反を宣言しない。
謝辞
この研究は、中国国立自然科学財団(グラント・91643203、91543208、81502835)によって支援されました。
資料
| Name | Company | Catalog Number | Comments |
| 4% phosphate buffered formaldehydefixative | Biosharp, Hefei, China | REF: BL539A | |
| 75% ethanol | Guoyao,Shanghai,China | CAS:64-17-5 | |
| Biosignaling monitor BL-420E+ | Taimeng, Chengdu, China | BL-420E+ | |
| Candling lamp | Zhenwei, Dezhou, China | WZ-001 | |
| Disposable syringe | Zhiyu, Jiangsu, China | ||
| Egg incubator | Keyu,Dezhou, China | KFX | |
| Electrical balance | OHAUS, Shanghai, China | AR 224CN | |
| Electro-thermal incubator | Shenxian, Shanghai, China | DHP-9022 | |
| Ethanol absolute | Guoyao,Shanghai,China | CAS:64-17-5 | |
| Fertile chicken egg | Jianuo, Jining, China | ||
| Hematoxylin and Eosin Staining Kit | Beyotime, Bejing, China | C0105 | |
| Histology paraffin | Aladdin, Shanghai, China | P100928-500g | Melt point 52~54°C |
| Histology paraffin | Aladdin, Shanghai, China | P100936-500g | Melt point 62~64°C |
| IV catheter | KDL, Zhejiang, China | The catheters have to be soft, plastic ones. | |
| Lentivirus | Genechem, Shanghai, China | The lentivirus were individually designed/synthesized by Genechem. | |
| Masson's trichrome staining kit | Solarbio, Beijing, China | G1340 | |
| Metal probe | Jinuotai, Beijing, China | ||
| Microinjector (5 uL) | Anting,Shanghai, China | ||
| Microscope | CAIKON, Shanghai, China | XSP-500 | |
| Microtome | Leica, Germany | HistoCore BIOCUT | |
| Microtome blade | Leica,Germany | Leica 819 | |
| Pentobarbitual sodium | Yitai Technology Co. Ltd., Wuhan, China | CAS: 57-33-0 | |
| Pipetter(10ul) | Sartorius, Germany | ||
| Povidone iodide | Longyuquan, Taian, China | ||
| Scissor | Anqisheng,Suzhou, China | ||
| Sterile saline | Kelun,Chengdu, China | ||
| Sunflower oil | Mighty Jiage, Jiangsu, China | Any commerical sunflower oil for human consumption should work | |
| Tape | M&G, Shanghai, China | ||
| Tedlar PVF Bag (5L) | Delin, Dalian, China | ||
| Vortex mixer | SCILOGEX, Rocky Hill, CT, US | MX-F | |
| Xylene | Guoyao,Shanghai,China | CAS:1330-20-7 |
参考文献
- Kain, K. H., et al. The chick embryo as an expanding experimental model for cancer and cardiovascular research. Developmental Dynamics. 243 (2), 216-228 (2014).
- Menna, T. M., Mortola, J. P. Effects of posture on the respiratory mechanics of the chick embryo. Journal of Experimental Zoology. 293 (5), 450-455 (2002).
- Hamburger, V., Hamilton, H. L. A series of normal stages in the development of the chick embryo. Journal of Morphology. 88 (1), 49-92 (1951).
- Yamamoto, F. Y., Neto, F. F., Freitas, P. F., Oliveira Ribeiro, C. A., Ortolani-Machado, C. F. Cadmium effects on early development of chick embryos. Environmental Toxicology and Pharmacology. 34 (2), 548-555 (2012).
- Lv, N., et al. The roles of bone morphogenetic protein 2 in perfluorooctanoic acid induced developmental cardiotoxicity and l-carnitine mediated protection. Toxicology and Applied Pharmacology. 352, 68-76 (2018).
- Kmecick, M., Vieira da Costa, M. C., Oliveria Ribeiro, C. A., Ortolani-Machado, C. F. Morphological evidence of neurotoxic effects in chicken embryos after exposure to perfluorooctanoic acid (PFOA) and inorganic cadmium. Toxicology. 4227, 152286 (2019).
- Jiang, Q., Lust, R. M., Strynar, M. J., Dagnino, S., DeWitt, J. C. Perflurooctanoic acid induces developmental cardiotoxicity in chicken embryos and hatchlings. Toxicology. 293 (1-3), 97-106 (2012).
- Jiang, Q., et al. In ovo very early-in-life exposure to diesel exhaust induced cardiopulmonary toxicity in a hatchling chick model. Environmental Pollution. 264, 114718 (2020).
- Jiang, Q., Lust, R. M., DeWitt, J. C. Perfluorooctanoic acid induced-developmental cardiotoxicity: are peroxisome proliferator activated receptor alpha (PPARalpha) and bone morphorgenic protein 2 (BMP2) pathways involved. Journal of Toxicology and Environmental Health, Part A. 76 (11), 635-650 (2013).
- Jiang, Q., et al. Changes in the levels of l-carnitine, acetyl-l-carnitine and propionyl-l-carnitine are involved in perfluorooctanoic acid induced developmental cardiotoxicity in chicken embryo. Environmental Toxicology and Pharmacology. 48, 116-124 (2016).
- Zhao, M., et al. The role of PPAR alpha in perfluorooctanoic acid induced developmental cardiotoxicity and l-carnitine mediated protection-Results of in ovo gene silencing. Environmental Toxicology and Pharmacology. 56, 136-144 (2017).
- Jiang, Q., et al. Particulate Matter 2.5 Induced Developmental Cardiotoxicity in Chicken Embryo and Hatchling. Front Pharmacol. 11, 841 (2020).
- Molina, E. D., et al. Effects of air cell injection of perfluorooctane sulfonate before incubation on development of the white leghorn chicken (Gallus domesticus) embryo. Environmental Toxicology and Chemistry. 25 (1), 227-232 (2006).
- Crump, D., Chiu, S., Williams, K. L. Bis-(3-allyl-4-hydroxyphenyl) sulfone decreases embryonic viability and alters hepatic mRNA expression at two distinct developmental stages in chicken embryos exposed via egg injection. Environmental Toxicology and Chemistry. 37 (2), 530-537 (2018).
- Franci, C. D., et al. Potency of polycyclic aromatic hydrocarbons in chicken and Japanese quail embryos. Environmental Toxicology and Chemistry. 37 (6), 1556-1564 (2018).
- Rand, M. D., et al. Developmental exposure to methylmercury and resultant muscle mercury accumulation and adult motor deficits in mice. Neurotoxicology. 81, 1-10 (2020).
- Tanaka, T., Suzuki, T., Inomata, A., Moriyasu, T. Combined effects of maternal exposure to fungicides on behavioral development in F1 -generation mice: 2. Fixed-dose study of thiabendazole. Birth Defects Research. , (2020).
- Kofman, O., Lan, A., Raykin, E., Zega, K., Brodski, C. Developmental and social deficits and enhanced sensitivity to prenatal chlorpyrifos in PON1-/- mouse pups and adults. PLoS One. 15 (9), 0239738 (2020).
- Kischel, A., Audouard, C., Fawal, M. A., Davy, A. Ephrin-B2 paces neuronal production in the developing neocortex. BMC Developmental Biology. 20 (1), 12 (2020).
- Okolo, F., Zhang, G., Rhodes, J., Gittes, G. K., Potoka, D. A. Intra-Amniotic Sildenafil Treatment Promotes Lung Growth and Attenuates Vascular Remodeling in an Experimental Model of Congenital Diaphragmatic Hernia. Fetal Diagnosis and Therapy. , 1-13 (2020).
- Vyslouzil, J., et al. Subchronic continuous inhalation exposure to zinc oxide nanoparticles induces pulmonary cell response in mice. Journal of Trace Elements in Medicine and Biology. 61, 126511 (2020).
- Wahle, T., et al. Evaluation of neurological effects of cerium dioxide nanoparticles doped with different amounts of zirconium following inhalation exposure in mouse models of Alzheimer's and vascular disease. Neurochemistry International. 138, 104755 (2020).
- Tanabe, K. Three-Dimensional Echocardiography- Role in Clinical Practice and Future Directions. Circ J. 84 (7), 1047-1054 (2020).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved