Ozonolisi degli alcheni
Panoramica
Fonte: Vy M. Dong e Zhiwei Chen, Dipartimento di Chimica, Università della California, Irvine, CA
Questo esperimento dimostrerà un esempio di reazione di ozonolisi per sintetizzare la vanillina dall'isoeugenolo (Figura 1). L'ozonolisi degli alcheni, una reazione di ossidazione tra ozono e alchene, è un metodo comune per preparare aldeidi, chetoni e acidi carbossilici. Questo esperimento dimostra anche l'uso di un generatore di ozono e una reazione a bassa temperatura (-78 °C).

Figura 1. Diagramma che mostra l'ozonolisi dell'isoeugenolo alla vanillina.
Principi
La scissione ossidativa degli alcheni a due composti contenenti gruppi carbonilici è chiamata reazione di ozonolisi (Figura 2). Il meccanismo proposto (Figura 3) inizia con una cicloaddizione [3+2] tra alchene 1 con ozono per generare l'intermedio molozonide A. A è instabile e si riorganizza nell'ozonide C più stabile tramite lo zwitterion B. C si decompone in presenza di un riduttore come il solfuro di dimetile per fornire i due prodotti carbonilici (2, 3) e il dimetilsolfossido. Quando si utilizza un solvente nucleofilo(ad esempio,metanolo), il nucleofilo attacca l'intermedio B per formare un idroperossido E, che si decompone al prodotto 3 quando viene aggiunto solfuro di dimetile (Figura 4). La reazione viene tipicamente eseguita a -78 °C per prevenire reazioni collaterali e in presenza di un indicatore per determinare quando la reazione è completa. Sudan III è un indicatore comunemente usato. Inizialmente, la miscela di reazione è rossa e diventa viola / blu quando tutto l'alchene viene consumato. Quando tutto l'alchene ha reagito, l'indicatore, che ha un doppio legame N-N, reagisce con l'ozono dando così il cambiamento di colore.

Figura 2. Diagramma che mostra la reazione generale di ozonolisi di un alchene con un workup riduttivo.
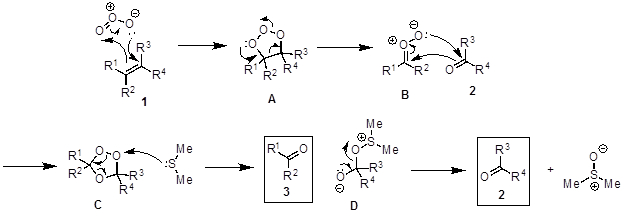
Figura 3. Diagramma che mostra il meccanismo generale dell'ozonolisi degli alcheni.

Figura 4. Diagramma che mostra la formazione di un idroperossido dall'intermedio B.
Procedura
- Aggiungere 200 mg di isoeugenolo, 15 ml di MeOH e ~ 2 mg di Sudan III a un pallone a fondo tondo da 50 mL a 3 colli dotato di una barra magnetica.
- Collegare il pallone di reazione a un serbatoio di ossigeno e a un gorgogliatore.
- Accendi il flusso di ossigeno.
- Raffreddare la miscela di reazione con un bagno di ghiaccio secco/acetone.
- Accendere il generatore di ozono, che converte l'ossigeno dal serbatoio in ozono che entra nel pallone di reazione. Il generatore si troverà tra il serbatoio di ossigeno e il pallone di reazione. Lasciare mescolare la miscela di reazione fino a quando il colore rosso cambia in viola / blu.
- Spegnere il generatore di ozono e consentire all'ossigeno di eliminare la miscela di reazione di ozono per 5 minuti.
- Rimuovere il bagno di raffreddamento e aggiungere 0,2 ml di solfuro di dimetile.
- Mescolare la miscela di reazione mentre si riscalda a temperatura ambiente per 1 ora.
- Rimuovere il solvente per evaporazione rotativa. Crea un tappo di silice posizionando il gel di silice in un imbuto Büchner. Sciogliere il residuo in acetato di etile al 10% in esani e far passare la soluzione attraverso il tappo di silice sotto vuoto per rimuovere le impurità. Lavare il tappo di silice altre 2 volte con il 10% di acetato di etile in esani. Raccogliere il filtrato e rimuovere il solvente per evaporazione rotativa per ottenere la vanillina come solido bianco.
- Calcola la resa percentuale di vanillina ottenuta e stabilisci la sua purezza e identità per punto di fusione (m.p.) e 1H NMR.
Risultati
La vanillina è stata ottenuta come solido bianco (150 mg, resa del 76%); m.p. 76-79 °C; 1 H NMR (400 MHz, CDCl3) δ 9,82 (br s, 1H), 7,43-7,41 (m, 2H), 7,04 (d, J = 8,8 Hz, 1H), 6,30 (s, 1H), 3,96 (s, 3H).
Applicazione e Riepilogo
In questo esperimento, abbiamo dimostrato la sintesi della vanillina dall'isoeugenolo usando la reazione di ozonolisi. Inoltre, è stato mostrato l'utilizzo di un generatore di ozono durante l'esecuzione di una reazione a bassa temperatura.
L'ozonolisi è una reazione utile per preparare aldeidi, chetoni e acidi carbossilici dagli alcheni. È stato applicato nella sintesi naturale del prodotto e nella preparazione su scala industriale di prodotti farmaceutici. L'artemisinina è un potente agente antimalarico ed è stato uno dei prodotti naturali riconosciuti nel Premio Nobel per la medicina 2015. In una sintesi in 10 fasi da (R) -(+) -pulegone, l'ozonolisi è stata utilizzata nell'ultima fase per realizzare il prodotto naturale (Figura 5). Ceftibuten e cefaclor sono antibiotici cefalosporinico prodotti su scala industriale. Una via commerciale utilizza l'ozonolisi per accedere a un intermedio chiave comune, che può essere elaborato per entrambi i composti (Figura 6).

Figura 5. Diagramma che mostra l'ozonolisi come l'ultimo passo in una sintesi di artemisinina.
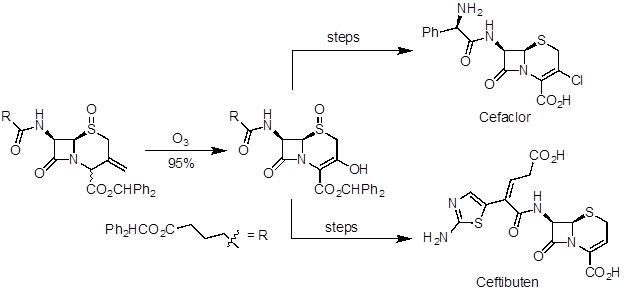
Figura 6. Diagramma che mostra l'ozonolisi per preparare un intermedio chiave nella sintesi divergente di cefaclor e ceftibuten.
Vai a...
Video da questa raccolta:

Now Playing
Ozonolisi degli alcheni
Organic Chemistry II
67.0K Visualizzazioni

Pulizia della vetreria
Organic Chemistry II
123.6K Visualizzazioni

Sostituzione nucleofila
Organic Chemistry II
99.6K Visualizzazioni

Agenti riducenti
Organic Chemistry II
43.1K Visualizzazioni

Reazione di Grignard
Organic Chemistry II
149.1K Visualizzazioni

Titolazione di n-butillitio
Organic Chemistry II
47.8K Visualizzazioni

Dispositivo di Dean Stark
Organic Chemistry II
100.3K Visualizzazioni

Organocatalisi
Organic Chemistry II
16.7K Visualizzazioni

Reazione di accoppiamento catalizzata da palladio
Organic Chemistry II
34.4K Visualizzazioni

Sintesi in fase solida
Organic Chemistry II
41.1K Visualizzazioni

Idrogenazione
Organic Chemistry II
49.6K Visualizzazioni

Polimerizzazione
Organic Chemistry II
94.1K Visualizzazioni

Punto di fusione
Organic Chemistry II
149.9K Visualizzazioni

Spettroscopia infrarossa
Organic Chemistry II
215.0K Visualizzazioni

Polarimetro
Organic Chemistry II
100.0K Visualizzazioni