Ozonólisis de alquenos
Visión general
Fuente: Vy M. Dong y Zhiwei Chen, Departamento de química, Universidad de California, Irvine, CA
Este experimento demuestra un ejemplo de una reacción de ozonólisis para sintetizar vainillina de isoeugenol (figura 1). Ozonólisis de alquenos, una reacción de oxidación entre el ozono y un alqueno, es un método común para preparar aldehídos, cetonas y ácidos carboxílicos. Este experimento también demuestra el uso de un generador de ozono y una reacción de baja temperatura (−78 ° C).

Figura 1. Diagrama que muestra la ozonólisis de isoeugenol a vainillina.
Principios
El clivaje oxidativo de alquenos a dos compuestos que contienen el grupo carbonilo se llama una reacción de ozonólisis (figura 2). El mecanismo propuesto (figura 3) comienza con una cicloadición [3 + 2] entre alkene 1 con ozono para generar el molozonide intermedio A. A es inestable y se reorganiza en la ozonida más estable C vía el zwitterion B. C se descompone en presencia de un reductor como el sulfuro de dimetilo para equipar los dos productos de carbonilo (2, 3) y dimetilsulfóxido. Cuando se utiliza un solvente nucleofílico (por ejemplo, metanol), el nucleófilo ataca intermedio B para formar un hidroperóxido E, que se descompone el producto 3 cuando sulfuro dimethyl se agrega (figura 4). La reacción se realiza generalmente a −78 ° C para evitar reacciones secundarias y en presencia de un indicador para determinar cuando la reacción es completa. Sudán III es un indicador comúnmente utilizado. Inicialmente, la mezcla de reacción es rojo y se convierte en púrpura/azul cuando todos el alkene se consume. Cuando ha reaccionado todo el alkene, el indicador, que tiene un enlace doble de N-N, reacciona con el ozono dando el cambio de color.

Figura 2. Diagrama que muestra la reacción general de la ozonólisis de un alqueno con un workup reductor.
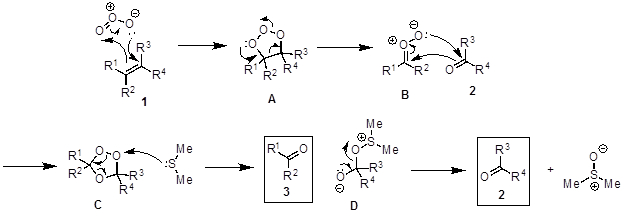
Figura 3. Diagrama que muestra el mecanismo general de ozonólisis alkene.

Figura 4. Diagrama que muestra la formación de un hidroperóxido de intermedio B.
Procedimiento
- Agregar 200 mg de isoeugenol, 15 mL de MeOH, y ~ 2 mg de Sudán III a un matraz de fondo redondo de 50 mL cuello 3 equipado con una barra de agitación magnética.
- Conectar el matraz de reacción a un tanque de oxígeno y un grifo.
- Encender el flujo de oxígeno.
- Enfríe la mezcla de reacción con un baño de hielo seco/acetona.
- Encienda el generador de ozono, que convierte el oxígeno en el tanque al ozono que va al matraz de reacción. El generador será entre el tanque de oxígeno y el matraz de reacción. Deje que la mezcla de reacción revolver hasta los cambios de color rojo a púrpura/azul.
- Apagar el generador de ozono y permita que el oxígeno purgar la mezcla de reacción de ozono durante 5 minutos.
- Retirar del baño de enfriamiento y añadir 0,2 mL de sulfuro dimethyl.
- Revuelva la mezcla de reacción al calentamiento a temperatura ambiente durante 1 h.
- Eliminar el disolvente por evaporación rotatoria. Hacer un sílice enchufe colocando gel de sílice en un embudo Büchner. Disolver el residuo en 10% acetato de etilo en hexanes y pasar la solución a través del tapón de silicona al vacío para eliminar las impurezas. Lavar el tapón de silicona 2 veces más con 10% de acetato de etilo en hexanes. Recoger el filtrado y eliminar el disolvente por evaporación rotatoria, para obtener vainillina como un sólido blanco.
- Calcule el rendimiento porcentual de vainillina obtenida y establecer su pureza e identidad de punto de fusión (m.p.) y 1H NMR.
Resultados
Vainillina fue obtenida como un sólido blanco (150 mg, rendimiento 76%); m.p. 76-79 ° C; 1 Δ H NMR (400 MHz, CDCl3) 9,82 (br s, 1 H), 7.43-7.41 (m, 2 H), 7.04 (d, J = 8,8 Hz, 1 H), 6.30 (s, 1 H), 3.96 (s, 3 H).
Aplicación y resumen
En este experimento, hemos demostrado la síntesis de la vainillina de isoeugenol usando la reacción de ozonólisis. También, utilizando un generador de ozono mientras que realizar una reacción de baja temperatura fue demostrado.
Ozonólisis es una reacción útil para preparar aldehídos, cetonas y ácidos carboxílicos de los alkenes. Se ha aplicado en la síntesis de productos naturales y preparación de escala industrial de productos farmacéuticos. La artemisinina es un potente agente antipalúdico y fue uno de los productos naturales reconocidos en el 2015 Premio Nobel en medicina. En una síntesis de 10 pasos de (R)-(+) - pulegona, ozonólisis se utilizan en el último paso para hacer el producto natural (figura 5). Ceftibuten y el cefaclor son antibióticos cefalosporina producidas en escala industrial. Una ruta comercial utiliza ozonólisis para acceder un intermedio clave común, que puede elaborarse a ambos compuestos (figura 6).

Figura 5 . Diagrama que muestra la ozonólisis como el último paso en una síntesis de la artemisinina.
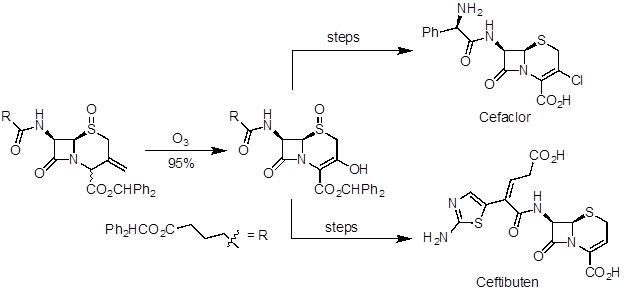
Figura 6 . Diagrama que muestra la ozonólisis para preparar una clave intermedia en la síntesis divergente de cefaclor y ceftibuten.
Tags
Saltar a...
Vídeos de esta colección:

Now Playing
Ozonólisis de alquenos
Organic Chemistry II
66.9K Vistas

Limpieza de cristalería
Organic Chemistry II
123.3K Vistas

Sustitución nucleófila
Organic Chemistry II
99.4K Vistas

Agentes de reducción
Organic Chemistry II
43.0K Vistas

Reacción de Grignard
Organic Chemistry II
148.9K Vistas

Titulación de n-butilitio
Organic Chemistry II
47.7K Vistas

Aparato de Dean-Stark
Organic Chemistry II
100.0K Vistas

Organocatálisis
Organic Chemistry II
16.6K Vistas

Acoplamiento cruzado catalizado por paladio
Organic Chemistry II
34.3K Vistas

Síntesis en fase sólida
Organic Chemistry II
40.9K Vistas

Hidrogenación
Organic Chemistry II
49.5K Vistas

Polimerización
Organic Chemistry II
93.7K Vistas

Punto de fusión
Organic Chemistry II
149.7K Vistas

Espectroscopia infrarroja
Organic Chemistry II
214.4K Vistas

Polarímetro
Organic Chemistry II
99.8K Vistas
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados