Ossigeno disciolto nelle acque superficiali
Panoramica
Fonte: Laboratori di Margaret Workman e Kimberly Frye - Depaul University
Le misurazioni dell'ossigeno disciolto (DO) calcolano la quantità di ossigeno gassoso disciolto nelle acque superficiali, che è importante per tutta la vita che respira ossigeno negli ecosistemi fluviali, comprese le specie ittiche preferite per il consumo umano(ad esempio bluegill e bass), nonché le specie decompositrici critiche per il riciclaggio dei materiali biogeochimici nel sistema.
L'ossigeno disciolto nei laghi, nei fiumi e negli oceani è cruciale per gli organismi e le creature che vivono in esso. Poiché la quantità di ossigeno disciolto scende al di sotto dei livelli normali nei corpi idrici, la qualità dell'acqua viene danneggiata e le creature iniziano a morire. In un processo chiamato eutrofizzazione, un corpo idrico può diventare ipossico e non sarà più in grado di sostenere gli organismi viventi, diventando essenzialmente una "zona morta".
L'eutrofizzazione si verifica quando i nutrienti in eccesso fanno crescere rapidamente le popolazioni di alghe in una fioritura algale. La fioritura algale forma dense stuoie sulla superficie dell'acqua bloccando due input essenziali di ossigeno per l'acqua: lo scambio di gas dall'atmosfera e la fotosintesi nell'acqua a causa della mancanza di luce sotto le stuoie. Man mano che i livelli di ossigeno disciolto diminuiscono sotto la superficie, gli organismi che respirano ossigeno muoiono in grandi quantità, creando un aumento della materia organica. L'eccesso di materia organica provoca un aumento delle popolazioni di decompositori che respirano ossigeno nella zona bentonica, che esaurisce ulteriormente i restanti livelli di ossigeno disciolto durante l'attività di decomposizione metabolica. Una volta che i livelli di ossigeno diventano così bassi, le specie mobili che respirano ossigeno(ad esempio i pesci) si allontaneranno, non lasciando vita aerobica nell'acqua e creando una zona morta.
Il metodo di titolazione Azide-Winkler utilizza la titolazione per determinare la concentrazione di un'incognita in un campione. In particolare, il tiosolfato di sodio viene utilizzato per titolare lo iodio, che può essere stechiometricamente correlato alla quantità di ossigeno disciolto in un campione.
Principi
Il metodo Azide-Winkler viene utilizzato per misurare il DO in loco, dove viene raccolta l'acqua superficiale. Il solfato di manganese (II) e l'idrossido di potassio vengono aggiunti al campione e l'ossigeno disciolto nel campione ossida il manganese e forma un precipitato marrone. L'azide viene aggiunto sotto forma di un reagente alcalino ioduro-azide acquistato per correggere la presenza di nitriti, che si trovano nei campioni di acque reflue e possono interferire con la procedura di ossidazione di Winkler.
MnSO4 + 2 KOH  Mn(OH)2 + K2SO4
Mn(OH)2 + K2SO4
4 Mn(OH)2 + O2 + 2 H2O  4 Mn(OH)3
4 Mn(OH)3
L'acido solforico viene quindi aggiunto per acidificare la soluzione e il precipitato si dissolve. In queste condizioni, lo ioduro del reagente alcalino ioduro-azide nella soluzione viene convertito in iodio.
2 Mn(OH)3 + 3 H2SO4  Mn2(SO4)3 + 6 H2O
Mn2(SO4)3 + 6 H2O
Mn2(SO4)3 + 2 KI  2 MnSO4 + K2SO4 + 2 I2
2 MnSO4 + K2SO4 + 2 I2
Il tiosolfato viene quindi utilizzato per titolare lo iodio in presenza di un indicatore di amido aggiunto.
4 Na2S2O3 + 2 I2  2 Na2S4O6 + 4 NaI
2 Na2S4O6 + 4 NaI
4 moli di S2O32-  1 mole di O2
1 mole di O2
Al termine di questa titolazione, la soluzione blu diventerà chiara. La quantità di ossigeno disciolto nel campione è quantificata in proporzione diretta alla quantità di tiosolfato necessaria per raggiungere l'endpoint.
X mL S2O3  X mg/L O:
X mg/L O:
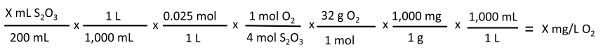
Procedura
1. Misurazione dell'ossigeno disciolto del campione
- Nel sito di raccolta dell'acqua, utilizzare una pipetta calibrata per aggiungere 2 ml di solfato manganoso a una bottiglia BOD trasparente da 300 mL riempita con l'acqua campione. Fare attenzione a non introdurre ossigeno nel campione inserendo la punta della pipetta sotto la superficie del campione e distribuendo con cura solfato manganoso. Ciò eviterà di creare bolle fino a quando il campione non sarà "fisso" e impedisce il cambiamento della concentrazione di ossigeno disciolto.
- Usando la stessa tecnica, aggiungere 2 ml di reagente alcalino ioduro-azide.
- Inserire immediatamente il tappo, inclinando leggermente la bottiglia e spingendo rapidamente il tappo in posizione in modo che nessuna bolla d'aria rimanga intrappolata nella bottiglia.
- Invertire con attenzione più volte (senza creare bolle d'aria) per mescolare. Un floccule (floc) si formerà da un'aggregazione precipitata di materiale con un aspetto nuvoloso (Figura 1).
- Attendere fino a quando il floc nella soluzione si è stabilizzato. Ancora una volta, invertire la bottiglia più volte e attendere che il floc si sia stabilizzato. Il campione è ora fissato per evitare cambiamenti nel contenuto di ossigeno disciolto e può essere trasportato in laboratorio e conservato per un massimo di 8 ore, se necessario, in condizioni fresche e buie.
- Se si conserva, i campioni devono essere sigillati utilizzando una piccola quantità di acqua deionizzata spruzzata attorno al tappo e il tappo deve essere avvolto in un foglio di alluminio, fissato con un elastico.
- Pipettare 2 mL di acido solforico concentrato nel campione tenendo la punta della pipetta appena sopra la superficie del campione. Invertire con attenzione più volte per sciogliere il floc (Figura 2).
- In un pallone di vetro, e utilizzando una pipetta calibrata, titolare 200 mL di acqua campione con 0,025 N tiosolfato di sodio standardizzato, vorticando e mescolando continuamente fino a formare un colore paglierino chiaro (Figura 3).
- Aggiungere 2 ml di soluzione di indicatore di amido con un contagocce e ruotare per mescolare. Una volta aggiunto l'indicatore dell'amido, la soluzione diventerà blu (Figura 4).
- Continuare la titolazione, aggiungendo una goccia alla volta fino a quando una goccia dissipa il blu, causando il punto finale incolore. Assicurati di aggiungere ogni goccia di titolante con attenzione e di mescolare uniformemente ogni goccia prima di aggiungere la successiva. Tenere il campione contro un pezzo di carta bianco può aiutare a migliorare la visualizzazione dell'endpoint.
- La concentrazione di DO è equivalente al volume (mL) del titolante utilizzato. Ogni millilitro di tiosolfato di sodio aggiunto al campione d'acqua equivale a 1 mg/L di ossigeno disciolto.

Figura 1. Un campione dopo che il reagente alcalino ioduro-azide è stato aggiunto e miscelato, mostrando la formazione di floc nella parte superiore del campione prima di depositarsi.

Figura 2. Un campione con floc disciolto dopo aggiunta di acido solforico.

Figura 3. Un campione dopo l'aggiunta di tiosolfato di sodio che mostra un colore paglierino chiaro.

Figura 4. Un campione che mostra il colore blu dopo l'aggiunta e la miscela dell'indicatore dell'amido.
Risultati
Un livello di ossigeno disciolto di 6 mg/L è sufficiente per la maggior parte delle specie acquatiche. I livelli di ossigeno disciolto inferiori a 4 mg / L sono stressanti per la maggior parte degli animali acquatici. Livelli di ossigeno disciolto inferiori a 2 mg/L non supportano la vita acquatica aerobica (Figura 5).
La quantità massima di ossigeno che può essere disciolta in acqua varia in base alla temperatura (Tabella 1).
Le misurazioni DO in mg/L vengono convertite in % di saturazione utilizzando la temperatura dell'acqua e la tabella di conversione riportata di seguito (Figura 6).
LIVELLI DI OSSIGENO DISCIOLTO (% SATURAZIONE)
Eccellente: 91 – 110
Buono: 71 – 90
Fiera: 51 – 70
Scarso: < 50
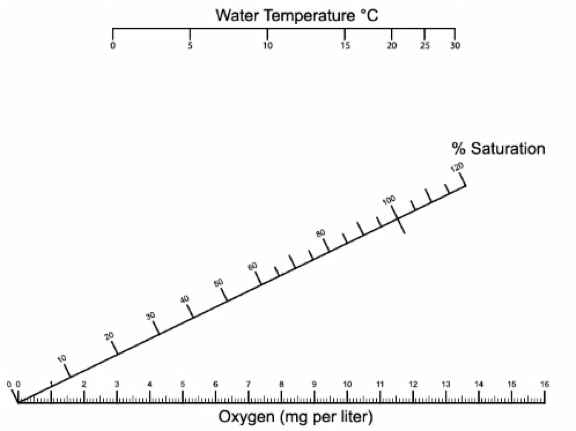
Figura 5. Le misurazioni DO vengono convertite in % di saturazione utilizzando la temperatura dell'acqua. La temperatura dell'acqua sull'asse orizzontale superiore e il valore DO misurato sull'asse orizzontale inferiore. Utilizzare un righello per disegnare una linea tra i due valori e registrare dove la linea incontra l'asse diagonale centrale per la saturazione percentuale.

Figura 6. Un livello di ossigeno disciolto di 6 mg/L è sufficiente per la maggior parte delle specie acquatiche. I livelli di ossigeno disciolto inferiori a 4 mg / L sono stressanti per la maggior parte degli animali acquatici. I livelli di ossigeno disciolto inferiori a 2 mg / L non supportano i pesci e inferiori a 1 mg / L non supportano la maggior parte delle specie.
| Temperatura (°C) | DO (mg/L) | Temperatura (°C) | DO (mg/L) | Temperatura(°C) | DO (mg/L) | Temperatura(°C) | DO (mg/L) |
| 0 | 14.60 | 11 | 11.01 | 22 | 8.72 | 33 | 7.16 |
| 1 | 14.19 | 12 | 10.76 | 23 | 8.56 | 34 | 7.16 |
| 2 | 13.81 | 13 | 10.52 | 24 | 8.40 | 35 | 6.93 |
| 3 | 13.44 | 14 | 10.29 | 25 | 8.24 | 36 | 6.82 |
| 4 | 13.09 | 15 | 10.07 | 26 | 8.09 | 37 | 6.71 |
| 5 | 12.75 | 16 | 9.85 | 27 | 7.95 | 38 | 6.61 |
| 6 | 12.43 | 17 | 9.65 | 28 | 7.81 | 39 | 6.51 |
| 7 | 12.12 | 18 | 9.45 | 29 | 7.67 | 40 | 6.41 |
| 8 | 11.83 | 19 | 9.26 | 30 | 7.54 | 41 | 6.41 |
| 9 | 11.55 | 20 | 9.07 | 31 | 7.41 | 42 | 6.22 |
| 10 | 11.27 | 21 | 8.90 | 32 | 7.28 | 43 | 6.13 |
Tabella 1. Quantità massime di ossigeno che possono essere sciolte in acqua dalla temperatura.
Applicazione e Riepilogo
I fiumi che si muovono lentamente sono particolarmente vulnerabili a bassi livelli di DO e, in casi estremi, questi livelli di DO possono portare a condizioni ipossica, creando "zone morte" in cui la vita aerobica non è più supportata da un corpo idrico (Figura 7). Una volta che le piante e gli animali muoiono, l'accumulo di sedimenti che si verifica può anche sollevare il letto del fiume, consentendo alle piante di colonizzare sopra l'acqua e potrebbe portare alla perdita del fiume tutti insieme (Figura 8). Le acque superficiali ad altitudini più elevate sono anche più vulnerabili a bassi livelli di DO, poiché la pressione atmosferica diminuisce con l'aumentare dell'altitudine e meno gas ossigeno viene sospeso nell'acqua.
Bassi livelli di DO supportano forme di vita considerate poco attraenti o inadatte all'uso umano, comprese sanguisughe e vermi acquatici (Oligochaeta).
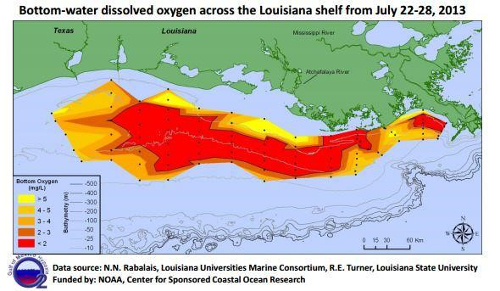
Figura 7. Mappa delle concentrazioni di ossigeno disciolto attraverso la piattaforma della Louisiana che mostra la regione della zona morta.

Figura 8. Fotografia del Mar Caspio che mostra una grave eutrofizzazione all'estremità nord.
Vai a...
Video da questa raccolta:

Now Playing
Ossigeno disciolto nelle acque superficiali
Environmental Science
55.7K Visualizzazioni

Identificazione degli alberi: come utilizzare una chiave dicotomica
Environmental Science
81.2K Visualizzazioni

Rilevamento degli alberi: metodo di campionamento a quarti centrati su un punto
Environmental Science
49.4K Visualizzazioni

Utilizzo di sistemi di geolocalizzazione (GIS) per lo studio della selvicoltura urbana
Environmental Science
12.6K Visualizzazioni

Cella a combustibile con membrana a scambio protonico
Environmental Science
22.1K Visualizzazioni

Biocarburanti: produzione di etanolo da materiali cellulosici
Environmental Science
53.1K Visualizzazioni

Test per alimenti geneticamente modificati
Environmental Science
89.7K Visualizzazioni

Torbidità e solidi totali nelle acque superficiali
Environmental Science
35.8K Visualizzazioni

Nutrienti negli ecosistemi acquatici
Environmental Science
38.8K Visualizzazioni

Misurazione dell'ozono troposferico
Environmental Science
26.4K Visualizzazioni

Determinazione degli ossidi di azoto (NO x) nei gas di scarico delle automobili tramite l'uso della spettroscopia UV-VIS
Environmental Science
30.1K Visualizzazioni

Analisi del piombo nel suolo mediante spettroscopia di assorbimento atomico
Environmental Science
125.4K Visualizzazioni

Analisi del carbonio e dell'azoto in campioni di matrici ambientali
Environmental Science
29.4K Visualizzazioni

Analisi dei nutrienti del suolo: azoto, fosforo e potassio
Environmental Science
215.8K Visualizzazioni

Analisi delle popolazioni di lombrichi nel suolo
Environmental Science
16.5K Visualizzazioni