שיטת התוספת הסטנדרטית
Overview
מקור: המעבדה של ד"ר פול באוור - אוניברסיטת פרדו
השיטה של תוספות סטנדרטיות היא שיטת ניתוח כמותית, אשר משמש לעתים קרובות כאשר המדגם של עניין יש רכיבים מרובים לגרום אפקטים מטריצה, שבו הרכיבים הנוספים עשויים גם להפחית או לשפר את אות ספיגת האנליטי. התוצאה היא טעויות משמעותיות בתוצאות הניתוח.
תוספות סטנדרטיות משמשות בדרך כלל כדי למנוע אפקטים מטריצה ממדידה, שכן ההנחה היא כי המטריצה משפיעה על כל הפתרונות באופן שווה. בנוסף, הוא משמש לתיקון הפרדות הפאזה הכימית המבוצעות בתהליך החילוץ.
השיטה מבוצעת על ידי קריאת עוצמת הניסיוני (במקרה זה פלואורסצנטי) של הפתרון הלא ידוע ולאחר מכן על ידי מדידת עוצמת הלא נודע עם כמויות שונות של תקן ידוע הוסיף. הנתונים מותווים כעוצמת פלואורסצנטיותלעומת כמות התקן שנוסף (הלא נודע עצמו, ללא תוספת סטנדרטית, מתוות על ציר ה- y). קו הריבועים הפחות מצטלב עם ציר ה-x בשלילי בריכוז הלא נודע, כפי שמוצג באיור 1.
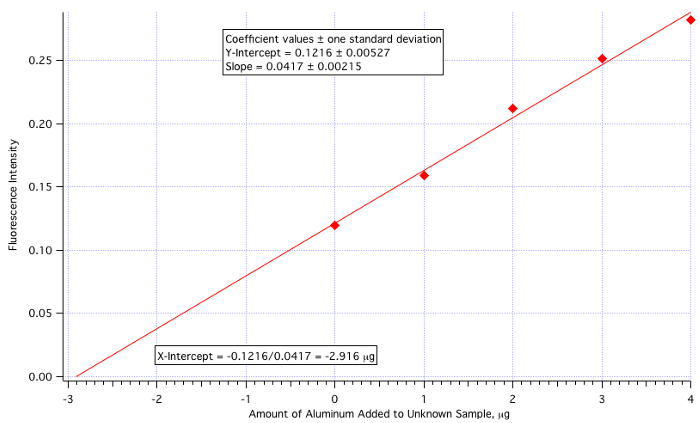
איור 1. ייצוג גרפי של שיטת התוספת הסטנדרטית.
Principles
בניסוי זה, השיטה של תוספות סטנדרטיות מוצגת ככלי אנליטי. השיטה היא הליך לניתוח כמותי של מין ללא יצירת עקומת כיול טיפוסית. ניתוח תוספת סטנדרטית מתבצע על ידי מדידת עוצמה ספקטרוסקופית לפני ואחרי התוספת של aliquots מדויק של פתרון סטנדרטי ידוע של האנליטה.
ניסוי זה חוקר מינים שאינם פלואורסצנטיים על ידי תגובה להם באופן כזה כדי ליצור קומפלקס פלואורסצנטי. גישה זו משמשת בדרך כלל בחקירה של יונים מתכת. יונים מאלומיניום (Al3+) ייקבעו על ידי יצירת קומפלקס עם 8-הידרוקסיקווינולין (8HQ). Al3+ הוא מזורז על ידי 8HQ מפתרון מימי ולאחר מכן מופק לתוך כלורופורם; הפלואורסצנטיות של פתרון הכלורופורם נמדדת וקשורה לריכוז של פתרון Al3+ המקורי. רגישות בטווח החלק למיליון (ppm או מיקרוגרם/מ"ל) צפויה לניסוי זה.
התגובה היא

כמות האלומיניום בכל מדגם במהלך ניסוי זה מחושבת כדלקמן:
| ריק | 0 | ||
| לא ידוע + תקן 0 מ"ל | Vלא ידוע(C לאידוע) = 25 מ"ל(C לאידוע) | ||
| לא ידוע + תקן 1 מ"ל | Vלא ידוע(C לאידוע)+תקןV (CStandard) = 25 מ"ל (Cלא ידוע)+ 1 מ"ל(1 מיקרוגרם/מ"ל) | ||
| לא ידוע + 2 מ"ל רגיל | Vלא ידוע(Cלאידוע)+ VStandard(CStandard) =25 מ"ל (Cלאידוע)+ 2 מ"ל(1 מיקרוגרם/מ"ל) | ||
| לא ידוע + 3 מ"ל רגיל | Vלא ידוע(Cלא ידוע)+תקןV(CStandard)= 25 מ"ל (Cלאידוע)+ 3 מ"ל(1 מיקרוגרם/מ"ל) | ||
| לא ידוע + תקן 4 מ"ל | Vלא ידוע(Cלא ידוע) +V Standard(CStandard) =25 מ"ל (Cלאידוע)+ 4 מ"ל(1 מיקרוגרם/מ"ל) | ||
Procedure
1. הכנת ריאגנטים
- פתרון Al3+ סטנדרטי ל-100 ppm: המיס 0.9151 גרם אלומיניום חנקתי (Al(NO3)3•9H2O) לבקבוק נפחי של 1-L עם מי DI.
- פתרון 8HQ בחומצה אצטית 1 M (2% wt/vol): הוסף 2.0 גרם של 8-הידרוקסיקווינולין לבקבוק נפחי של 100 מ"ל.
- בזהירות להוסיף 5.74 מ"ל חומצה אצטית קרחונית לבקבוק 100 מ"ל, ולאחר מכן לדלל לסימן עם מים DI. זה מאפשר 8-hydroxyquinoline להתמוסס בשלב מימי.
- 1 M NH4+/NH3 חוצץ (pH ~ 8): הוסף 20 גרם של אצטט אמוניום (NH4OAc) לבקבוק 100 מ"ל.
- הוסף 7 מ"ל של 30% אמוניום הידרוקסיד לבקבוק 100 מ"ל זה, ונדלל לסימן עם מי DI. זה עוזר לנטרל את החומצה בתמיסת 8HQ בשילוב.
- ריאגנטים אחרים כוללים נתרן גופרתי נטול מים (Na2SO4)וכלורופורם (ציון מפרט).
2. הכנת הדגימות
- הכן פתרון Al3+ סטנדרטי בגודל 1.00 ppm על-ידי הוספת 1.0 מ"ל מפתרון Al3+ של מלאי 100-ppm עם פיפטה לבקבוק נפחי של 100 מ"ל.
- הניחו שישה משפכים מפרידים בגודל 125 מ"ל על הטבעות שנמצאות על דוכן טבעת גדול הממוקם בשכונה. הם צריכים להיות מתויגים כדלקמן: BL, 0, 1, 2, 3, 4. ודא שכל כלי הזכוכית נקיים בקפידה, שכן קשה להשיג תוצאות כמותיות אם חרוזים קטנים של כלורופורם נדבקים לקירות כלי הזכוכית.
- הוסף 25.00 מ"ל של פתרון Al3+ הלא ידוע לחמשת משפכי ההפרדה המסומנים בתווית 0, 1, 2, 3 ו- 4. בדוגמה זו, הריכוז הלא ידוע הוא 0.110 עמודים לדקה.
- הוסף 0, 1.00, 2.00, 3.00 ו- 4.00 מ"ל של פתרון Al3+ סטנדרטי בגודל 1.00-ppm, בהתאמה, ל- 5 משפכים עם פיפטה של 1 מ"ל.
- הכן ריק על-ידי הוספת 25.00 מ"ל של מים מזוקקים למשפך המפריד המסומן BL.
- הוסף 1.0 מ"ל של פתרון 8-הידרוקסיקווינולין עם פיפטה לכל אחד מששת הפתרונות.
- הוסף 3.0 מ"ל של פתרון חיץ עם פיפטה לכל אחד מששת הפתרונות.
- לחלץ כל פתרון פעמיים עם 10 מ"ל של כלורופורם, רועד במרץ במשך 1 דקות בכל פעם. זכור מדי פעם לפרוק את המשפך המפריד כדי לשחרר הצטברות לחץ. (הערה: מיצוי טוב מתרחש רק כאשר יש הרבה מגע נוזלי נוזלי בין השלבים).
- לאסוף את הכלורופורם ב 100 מ"ל נקי, יבש תווית. לכלורופורם יש צפיפות של קרוב ל 1.5 גרם / ס"מ3, אז זה השכבה התחתונה. לא צריך להיות זכר של צבע צהוב עזב בשלב מימי לאחר החילוץ המלא.
- מעבירים את תמצית הכלורופורם המשולבת מכל כוב לבקבוקון נפחי בגודל 25 מ"ל ומדלדלים לסימן עם כלורופורם. הקפידו להניח פקקים בכל בקבוק נפחי כדי למנוע מכלורופורם להתאדות.
- הוסף ~ 1 גרם של נתרן גופרתי נטול מים (Na2SO4) לכל אחד מששת כוסות 100 מ"ל מהשלב 2.9. נתרן גופרתי מסייע להסיר כל עקבות של מים שעשויים להיות נוכחים בתמצית הכלורופורם.
- העבר את הפתרונות בחזרה למכסות המכובדות שלהם. מערבבים בזהירות כדי להקל על התייבשות של כל מים במדגם.
- דקאנט תמציות כלורופורם לתוך תא פלואורימטר קוורץ (הערה: כלורופורם יהיה להמיס תא פוליסטירן פלסטיק).
3. בחירת אורך הגל של העירור
קבעו את אורכי הגל של העירור והפליטה על-ידי הפעלת סריקות, ואז פשוט קראו ותעדו את עוצמת הפלואורסצנטיות של כל הדגימות בערכים אלה. רוחבי הפס של העירור והפליטה מוגדרים מראש ב- 5 ננומטר. המתחם נספג ב UV הקרוב, כך אורך גל העירור צריך להיות על 385 ננומטר. בתחילה, לפקח על פלואורסצנטיות ב 500 ננומטר בענף הפליטה.
- בפלורימטר, ודא כי מאווררי הקירור הפנימיים והחצונים בפלורימטר מופעלים לפני הפעלת מנורת הקסנון. מנורת הקסנון מתחממת מאוד, ודורשת קירור מתמשך.
- הפעל את המתח הגבוה (HV) לגלאי PMT ל- 400 V.
- פתח את שני התריסים.
- פתח את תוכנית רכישת הנתונים במחשב, כאן זה "100nmFluorScan".
- מקם את הפתרון "מדגם + 2 מ"ל הוסיף" (2) לתא קוורץ לשימוש לקביעת אורכי הגל העירור והפליטה הטובים ביותר.
- עם אורך גל הפליטה שנקבע בתחילה על 500 ננומטר, להפעיל סריקת עירור מ 335-435 ננומטר עם מהירות סריקה של 2 ננומטר / s.
- מתוך עלילת הפלואורסצנטיות המתקבלת, קבע את אורך הגל המרבי של עירור פלואורסצנטיות (EXλmax)והגדר את המכשיר לערך זה.
4. בחירת אורך גל הפליטה
- הגדר את אורך הגל פליטת פלואורימטר ל 450 ננומטר.
- הגדר את טווח אורך הגל של הפליטה כדי להפעיל סריקה של 100 ננומטר מ 450-550 ננומטר.
- כדי להתחיל את הסריקה, לחץ על כפתור "התחל ניסיון" בתוכנית באותו זמן של לחיצה על כפתור "START" בלוח הקדמי של הפלורימטר.
- מתוך עלילת הפלואורסצנטיות המתקבלת, קבעו את אורך הגל המרבי של פליטת פלואורסצנטיות(EMλmax)והגדירו את המכשיר לערך זה(איור 2).
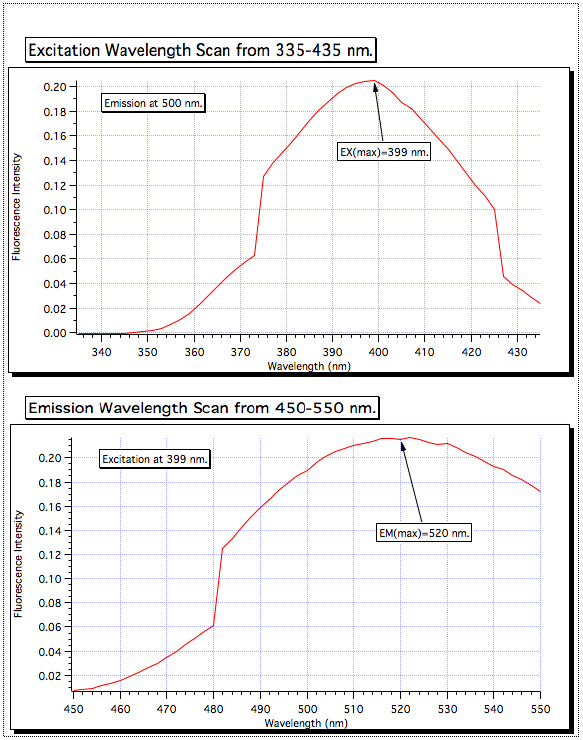
איור 2. קביעת EXλmax אופטימלי ו- EMλmax אורכי גל.
5. מדידת הפלואורסצנטיות של הדגימות
- כל הדגימות מופעלות ב- EMλmax וב- EXλmax. סריקות אינן נחוצות עבור כל מדגם, אלא רק את ערך הפלואורסצנטיות בתנאים אלה. החל מדגם מדלל ביותר (ריק), למקם בתא קוורץ ולאחר מכן בכלי. הקלט את עוצמת הפלואורסצנטיות במחשבון המעבדה.
- חזור על הפעולה עבור כל הדגימות האחרות.
- זכור שיש להפחית את העוצמה היחסית הריקה מהעוצמה היחסית של כל פתרון לפני יצירת תרשים הכיול.
6. יצירת עלילת התוספת הסטנדרטית
- התווה את עוצמת הפלואורסצנטיות לעומת מיקרוגרם של Al3+ הוסיף.
- קבע את הערך הפחות ריבועי של התוויית התוצאה, ורשום הן את השיפוע והן את היירוט.
- קבע את הμg של Al3+ במדגם הלא ידוע מהמשוואה מיקרוגרם של Al3+ = -b/m
- בידיעה כי אלומיניום לא ידוע היה נפח של 25.0 מ"ל הוסיף לכל מדגם, לקבוע את הריכוז של אלומיניום לא ידוע.
Results
סריקה של אורך גל העירור בין 335-435 הראתה את הספיגה הגבוהה ביותר ב-399 ננומטר, כך שמונוכרומט העירור נקבע לערך זה. לאחר מכן בוצעה סריקת הפליטה בין 450 ל-550 ננומטר, והאות החזק ביותר נמצא ב-520 ננומטר. אלה הם אורכי הגל המשמשים לכל הדגימות.
| לדוגמה | עוצמת פלואורסצנטיות | עוצמת פלואורסצנטיות מתוקנת |
| ריק | 0.008 | 0.000 |
| לדוגמה | 0.128 | 0.120 |
| דוגמה + 1 מ"ל | 0.167 | 0.159 |
| דוגמה + 2 מ"ל | 0.220 | 0.212 |
| דוגמה + 3 מ"ל | 0.260 | 0.252 |
| דוגמה + 4 מ"ל | 0.290 | 0.282 |
חלקה של פלואורסצנטיות (איור 3) לעומת מיקרוגרם של Al3 + הוסיף (איור 4) הניב קו ריבועי פחות של:
עוצמת פלואורסצנטיות = 0.0417 x (מיקרוגרם של Al3+ הוסיף) + 0.1216
כמות Al3+ = -(Y-Int)/שיפוע = -0.1216/0.0417 = -2.916 מיקרוגרם /מ"ל
מאז כמות לא ידוע הוסיף היה 25 מ"ל, אז ערך 2.916 מיקרוגרם / מ"ל צריך להיות מחולק על ידי 25.
ריכוז אלומיניום לא ידוע = 2.916 מיקרוגרם / מ"ל / 25.0 מ"ל = 0.117 מיקרוגרם / מ"ל = 0.117 ppm
שהוא די קרוב לערך בפועל של 0.110 ppm (6.4% שגיאה).

איור 3. פלואורסצנטיות של הדגימות.
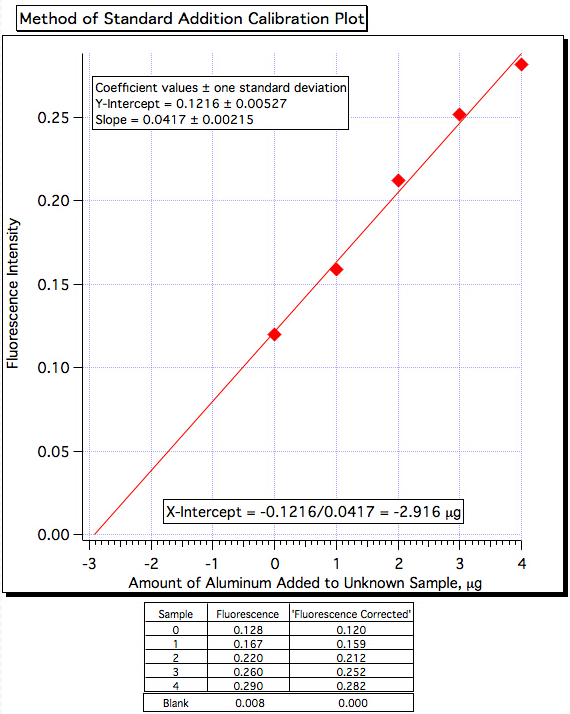
איור 4. התוויית הכיול של התוספת הסטנדרטית.
Application and Summary
השיטה של תוספות סטנדרטיות היא לעתים קרובות הטכניקה המשמשת כאשר נדרשות תוצאות כמותיות מדויקות, המשמשת בניתוח אנליטי כגון ספיגה אטומית, ספקטרוסקופיית פלואורסצנטיות, ICP-OES וכרומטוגרפיה של גז. זה משמש לעתים קרובות כאשר ישנם רכיבים אחרים במדגם של עניין שגורם גם הפחתה או שיפור של הספיגה הרצויה לתוצאות כמותיות. כאשר זה המקרה, אי אפשר פשוט להשוות את אות הניתוחים לסטנדרטים באמצעות הגישה המסורתית של עקומת הכיול. למעשה, הערכת אפקט מטריצה צריכה להיות חלק הכרחי של הליך האימות.
דוגמה נוספת שבה ניתן להשתמש בנתוספות סטנדרטיות היא בעת חילוץ כסף מפסולת צילום ישנה. הפסולת מכילה חלידים כסופים, וניתן לחלץ אותה כך שניתן יהיה להחזיר את הכסף. על ידי ספייק "פסולת" לא ידוע עם כמויות ידועות של כסף, שיטה זו יכולה לחזות את כמות הכסף המתקבלת מסרט הצילום.
עובדים החשופים למפעלי ייצור בנזן נבדקים לעתים קרובות כדי לוודא שהם נמצאים בבטחה מתחת לרמות המקובלות של בנזן. השתן שלהם נבדק לכימיקל, וזו המטריצה הביולוגית. כמו כן, כמות דיכוי הניתוח משתנה עבור אנשים שונים, כך שערכת כיול אחת לא תעבוד. בשיטת התוספת הסטנדרטית, כל עובד יכול להיבדק ולהעריך במדויק.
Tags
Skip to...
Videos from this collection:

Now Playing
שיטת התוספת הסטנדרטית
Analytical Chemistry
320.0K Views

הכנה לדוגמה לאפיון אנליטי
Analytical Chemistry
84.6K Views

תקנים פנימיים
Analytical Chemistry
204.7K Views

עקומות כיול
Analytical Chemistry
796.5K Views

ספקטרוסקופיה אולטרה סגולה (UV-Vis)
Analytical Chemistry
623.3K Views

רמאן ספקטרוסקופיה לניתוח כימי
Analytical Chemistry
51.2K Views

פלואורסצנטיות של קרני רנטגן (XRF)
Analytical Chemistry
25.4K Views

כרומטוגרפיה של גז (GC) עם גילוי יינון להבה
Analytical Chemistry
281.9K Views

כרומטוגרפיה נוזלית בעלת ביצועים גבוהים (HPLC)
Analytical Chemistry
384.3K Views

כרומטוגרפיה של חילופי יונג
Analytical Chemistry
264.4K Views

אלקטרופורזה נימית (CE)
Analytical Chemistry
93.8K Views

מבוא לספקטרומטריית מסה
Analytical Chemistry
112.2K Views

סריקת מיקרוסקופיית אלקטרונים (SEM)
Analytical Chemistry
87.1K Views

מדידות אלקטרוכימיות של זרזים נתמכים באמצעות פוטנציוסטט /גלוונוסטאט
Analytical Chemistry
51.4K Views

וולטמטריה מחזורית (קורות)
Analytical Chemistry
125.1K Views
Copyright © 2025 MyJoVE Corporation. All rights reserved