Method Article
טיהור של האדם S100A12 ואת היונים שלה הנגרמת Oligomers עבור גירוי תא החיסון
In This Article
Summary
פרוטוקול זה מתאר שיטת טיהור ל-רקומביננטי הסידן מחייב חלבון בחינם S100A12 והוא המושרה היונים שלה עבור גירוי מונוציט אנושי.
Abstract
בפרוטוקול זה, אנו מתארים שיטה כדי לטהר את החלבון האנושי מחייב S100A12 החלבונים ואת oligomers המושרה שלה מפני es, המנוכיה קולי התרבות לגירוי התא החיסונית. פרוטוקול זה מבוסס על אסטרטגיה בעלת שני שלבים כרומטוגרפיה, הכוללת את החלבון הטרום-טיהור בטור כרומטוגרפיה של anion-exchange וצעד נוסף ליטוש בטור של אינטראקציה הידרופובי. אסטרטגיה זו מייצרת חלבון S100A12 של טוהר גבוהה ותשואה על עלויות לניהול. עבור מוסר פונקציונלי על התאים החיסוניים בסופו של דבר שארית זיהום אנדוטוקסין דורש ניטור זהיר ועוד לנקות את הצעדים כדי להשיג חלבון אנדוטוקסין ללא. רוב זהום אנדוטוקסין יכול להיות מנשלל על ידי האניב-exchange כרומטוגרפיה. כדי לרוקן זהום שיורית, פרוטוקול זה מתאר שלב ההסרה עם מסננים צנטריפוגליים. בהתאם לS100A12 של כוח היון הזמין יכול לארגן הומוגוטיימרים שונים. כדי לחקור את הקשר בין מבנה לפונקציה, פרוטוקול זה מתאר עוד את יון-הטיפול של חלבון S100A12 ואחריו כימיים המקשרים לייצב S100A12 oligomers והפרדה הבאים שלהם לפי גודל-להדרה כרומטוגרפיה. לבסוף, אנו מתארים שיטת תא המאשרת את הפעילות הביולוגית של החלבון הטהור ומאשרת הכנה ל-LPS ללא תשלום.
Introduction
S100A12 הוא חלבון מחייב סידן אשר מופק בעיקר על ידי האדם גרנולוציטים. החלבון הוא ביטוי מוגזם במהלך (מערכתי) דלקת רמות הסרום שלה, במיוחד (אוטומטי) מחלות דלקתיות כגון דלקת מפרקים אידיופטית מערכתית (sJIA), קדחת ים תיכונית משפחתית (FMF) או מחלת קווסאקי (KD) יכול להודיע על פעילות מחלה ותגובה לטיפול. בהתאם לקולטני זיהוי תבניות (PRRs) כגון קולטנים למספרי חיוג (TLRs), מערכת החיסון הטבועה יכולה להיות מופעלת על-ידי תבניות מולקולריות הקשורות לפתוגן (PAMPs) כמו ליפופולפידים (LPS) או נזק דפוסי מולקולרי הקשורים (DAMPs; נקרא גם ' מדאיג '. DAMPs הם מולקולות אנדוגני כגון חלבונים סלולריים, שומנים או חומצות גרעין1. לח-פונקציות מתוארות היטב עבור חברי משפחת החלבון calgranulin, S100A8/A9 ו S100A122, אשר מדווחים גם לפעול כמו מתכת יון-הכלג1 פפטידים מיקרוביאלית3,4, 5,6. בהתאם ל-ion הזמין S100A12 יכול, כמו חברים אחרים של משפחת S100, לסדר לתוך הומומרים שונים עד לאחרונה ההשפעה של S100A12-oligomerisation התאמה על PRR-אינטראקציה, במיוחד TLR4, לא היה ידוע.
טופס monomeric של חלבון (92 חומצות אמינו, 10.2 kDa) מורכב משני מבנים EF-לולאה-סליל הסליל מחובר על ידי מקשר גמיש. C-טרמינל ef-יד מכיל את המוטיב הקלאסי של Ca2 +-מחייב בעוד N-טרמינל ef-יד המוצגים S100 חלבון-מבנה ספציפי לולאה מורחבת ("פסאודו-EF-יד") ומגלה Ca מופחת2 +-אהדה. Ca2 +-קשירה על ידי S100A12 יכול לגרום לשינוי הגדול ביותר של החלבונים ' C-הטרמינוס, אשר גורמת לחשיפה של תיקון הידרופובי על כל מונומר וצורות ממשק dimerization. כך, בתנאים פיסיולוגיים, המבנה הרבעוני הקטן ביותר שנוצר על ידי S100A12 הוא דיימר לא-חד-ממדי (כ -21 kda) שבו מונמרים בודדים נמצאים בכיוון אנטי מקבילי. כאשר מסודרים כמו dimer, S100A12 מדווחת Zn 2 + כמו גם יוני מתכתדיאטתיים אחרים, למשל, Cu2 + עם אהדה גבוהה7. היונים הללו מתואמים בממשק S100A12 דימר על ידי חומצות אמינו H15 וD25 של יחידת משנה אחת וH85, כמו גם H89 של משנה אנטי מקבילים השני8,9,10. בעוד מחקרים מוקדם יותר להציע zn2 +-טעון S100A12 עשוי לגרום לארגון של חלבון לתוך הומו-טטרמרס (44 kda) וכתוצאה מכך מוגברת Ca2 +-אהדה11,12, טיטור מתכת לאחרונה מחקרים6 מציעים Ca2 +-מחייב על ידי S100A12 כדי להגביר את הזיקה של חלבון zn2 +. לאחר S100A12 EF-הידיים מאוכלס באופן מלא על ידי Ca2 +, ca נוסף2 + הוא חשב לאגד בין dimers, מפעיל היווצרות הבוחנים (כ 63 kda). הארכיטקטורה של המבנה האפארי של ההקאמארה שונה בבירור מזו של הטטרמר. הוא הציע כי ממשק הטטרמר משתבש כדי לתת עלייה ממשקי dimer החדש, אשר מועילה היווצרות הבוחנים10. S100A12 מתבטא כמעט באופן בלעדי על ידי הגרנולוציטים האדם שבו הוא מהווה כ 5% חלבון ציטוסולג13. בפונקציה לח שלה S100A12 היה מתואר היסטורית כמו אגוניסט של multi-ליגציה עבור גליקטיון מתקדם מוצרי הקצה (זעם), ולאחר מכן כינה מוצרים שזוהו לאחרונה חלבון כריכת זעם (EN-זעם)14. אף על פי שדווחו קודם לכן כS100A12 ביוכימיים לזעם ולTLR415, הדגמנו לאחרונה מונוציטים אנושיים כדי להגיב לגירוי S100A12באופןהתלוי בTLR4. זה דורש הסדר של S100A12 לתוך Ca שלה2 +/zn2 +-המושרה מבנה הקסעון הרבע16.
כאן אנו מתארים הליך טיהור עבור רקומביננטי S100A12 האנושי ואת oligomers יון המושרה שלה לגירוי תא החיסון16,17. זה מבוסס על אסטרטגיה בעלת שני שלבים כרומטוגרפיה, אשר כוללת בתחילה טור anion-exchange כדי לבודד ולרכז את החלבון ולהסיר זהום בצובר (למשל, אנטוקסינים/ליפופוליסכרידים)18. לחילופין, כרומטוגרפיה שרפים חלבונים נפרדים על בסיס של חיובים שונים של פני השטח נטו. עבור חלבונים חומציים כמו S100A12 (נקודת איזואלקטריים של 5.81), מערכת מאגר עם pH של 8.5 ו שרף anion-exchange חזק מוביל הפרדה טובה. חלבונים מאוגדים הובלו עם מעבר מבריק של מאגר מלח גבוה. עם עלייה של יוני יוני שלילי החוזק במאגר להתחרות עם חלבונים עבור חיובים על פני השטח של שרף. חלבונים בנפרד elute בהתאם לחיוב הנטו שלהם וכתוצאה מכך, המאגרים המתוארים כאן מאפשרים לבודד ולרכז את החלבון S100A12 ביטוי יתר. בשל קבוצות טעונה שלילית ליפופוליסכדים, מולקולות אלה גם לאגד anion-exchange שרפים. עם זאת, החיוב הנטו הגבוה יותר שלהם מביא להאצלת מאוחר יותר את מעבר הצבע הגבוה של המלח. השלב השני של תהליך הטיהור הוצג לצורך הליטוש. זה עושה שימוש ביכולת כריכת הסידן של S100A12 ומסיר את הנותרים זיהומים על העמוד אינטראקציה הידרופובי. כריכת סידן של S100A12 מוביל לשינוי הקונפורמציה וחשיפה של טלאים הידרופובי על פני השטח של החלבון. במצב זה, S100A12 מקיים אינטראקציה עם משטח ההידרופובי של השרף. על ידי הסידן-מכלפת על ידי EDTA, אינטראקציה זו היא הפוכה. בנוכחות יונים, במיוחד סידן ואבץ, S100A12 מארגן לתוך הומומרים oligomers. כדי לחקור את מבנה היחסים בתפקוד של oligomers שונים, אנו התייצב dimeric, tetrameric ו hexameric רקומביננטי S100A12 עם מקשר כימי והפרידו את התסביכים על עמוד בגודל כרומטוגרפיה הדרה. לבסוף, כדי לנתח את הפונקציונליות ואת הפעילות הביולוגית של החלבון מטוהרים ואת oligomers המושרה היונים שלה, שחרור cy, S100A12 ו-LPS גירוי מונוציט ניתן להשוות.
שיטות שונות לטיהור S100A12 תוארו עד כה. ג'קסון ואח '19, למשל, פרסם פרוטוקול עם טיהור באמצעות עמודת anion-exchange וכרומטוגרפיה שלאחר הרחקה מהגודל. הליטוש טיהור על עמודה בעלת הגבלת גודל מוביל לתוצאות טובות, אך-בגלל לדוגמה לאמצעי אחסון מוגבלים בטעינה-הוא גמיש פחות במדרגיות. גישה שונה, שפורסם על ידי נשיקה ואח '20, מתאר טיהור של חלבון מתויג דרך Ni2 + טור אהדה כצעד הטיהור הראשון, ואחריו מחשוף אנזימטי כדי להסיר את התג ועוד שלבי הטיהור. בניגוד למחקרים שנערכו במהלך הלימודים19,20, החלבון המיוצר כפי שמתואר בפרוטוקול זה נקבע לניסויים על תאים חיסוניים. לכן, שארית זיהום אנטוקסין מהתרבות החיידקית היא אתגר. למרות שגישות שונות להסרת שורש הסרת רעלן כבר תוארו עד כה, אין שיטה אחידה הפועלת באותה מידה גם עבור כל פתרון חלבון נתון21,22.
לסיכום, הפרוטוקול שלנו משלב את היתרונות של ביטוי ללא תגית במערכת חיידקית עם הסרת אנטוקסין יעיל ותשואה גבוהה של חלבון טהור.
Protocol
הערה: עיין בטבלה משלימה 1 להכנת מאגרים ופתרונות מניות.
1. ביטוי חלבון ב E. coli
-
שיבוט
- S100A12 האדם ללא תגית (רצף הפניות NCBI ק: NP_ 005612.1) לתוך הביטוי בקטריאלי וקטורי pET11b. כדי לבטא את החלבון, להפוך את המבנה לתוך E. coli BL21 (DE3).
-
תרבות
- הכינו תרבות התחלתית על ידי הצרת מושבה אחת ב 5 מ ל של גידול בינוני (ליברות ציר עם 100 μg/mL אמפיצילין) בתוך הצינור 14 mL עגול-תחתון. דגירה לילה ב 37 ° c עם טלטול ב 220 סל ד. העברה 2-4 מ ל של תרבות לילה לתוך 400 mL של מדיום צמיחה ב 2 L ' Erlenmayer בקבוקון ו מודדים את התרבות ב 37 ° c עם טלטול ב 220 rpm.
הערה: הצפיפות הראשונית של התרבות העיקרית צריכה להיות צפיפות אופטית ב 600 ננומטר (OD600) = 0.1. - נטר את ה-OD600 במהלך הצמיחה. לגרום חלבון ביטוי על-ידי תוספת של 1 M איזופרופיל-מו-D-האיויוגלטותוסיד (IPTG) לריכוז הסופי של 1 מ"מ ב OD600 = 0.5-0.6. מודטה ב 37 ° צ' ו 220 rpm עבור נוספים 4 h.
הערה: באופן כללי,ה600 לאחר 1.5 עד 2.5 0.6 שעות בשעה 37 ° c. - הכינו 50 mL sonication מאגר על ידי המסת 50 mM טריס, 50 mM הנאקל ו 1 מ"מ החומצה הטאצלואמין הטאדוב (EDTA) בשנת 40 mL של מים מיוהים. להתאים את ה-pH ל 8.0 ולפצות עד 50 mL. הוסף מעכב פרוטאז (1 טבליה לפתרון 50 mL) ומשווה את המאגר ל -4 ° c.
- להעביר את התרבות החיידקית לתוך בקבוקי צנטריפוגה מתאים ולקצור את התאים ב 3,200 x g עבור 30 דקות ב 4 ° c. השמט את הסופרנטאנט והשהה מחדש את הגלולה ב -25 מ ל של מאגר sonication קר קרח. . מעתה והלאה, התאים בקרח
הערה: ניתן לאחסן תאים מושהים ב-20 ° c לטווח קצר וב-80 ° c לטווח ארוך.
- הכינו תרבות התחלתית על ידי הצרת מושבה אחת ב 5 מ ל של גידול בינוני (ליברות ציר עם 100 μg/mL אמפיצילין) בתוך הצינור 14 mL עגול-תחתון. דגירה לילה ב 37 ° c עם טלטול ב 220 סל ד. העברה 2-4 מ ל של תרבות לילה לתוך 400 mL של מדיום צמיחה ב 2 L ' Erlenmayer בקבוקון ו מודדים את התרבות ב 37 ° c עם טלטול ב 220 rpm.
-
Sonication/לוליזיס
- Sonicate התאים עבור 6 מחזורים של 30 על הקרח. לאחר כל מחזור, תאי מנוחה עבור 30-60 למעלה כדי להגן על התאים מפני התחממות יתר.
- העבר את ההשעיה התא כדי מקורר 50 mL מהירות גבוהה צנטריפוגה tube ו צנטריפוגה ברוטור זווית קבועה ב 15,000 x g עבור 30 דקות ב 4 ° c. Decant את ליפוסט נקי אשר מכיל את החלבונים מסיסים ציטוסולוליג לתוך שפופרת טריים 50 mL ולהשליך את הגלולה.
2. טיהור חלבון
- כרומטוגרפיה של אניב
- דיאליזה
- הכנת anion-exchange כרומטוגרפיה (AIEX) מאגר על ידי המסת 20 מ"מ טריס, 1 מ"מ EDTA ו 1 מ"מ אתילן גליקול-bis (2-עמינח)-N, N, N '-חומצה טטראצטט (EGTA) במים מיולים ולהתאים את ה-pH כדי 8.5 עם HCl. עבור דיאליזה להכין 2 x 5 L ו עבור כרומטוגרפיה 2x 1 L של מאגר AIEX.
הערה: נפח דיאליפוסט צריך להיות בערך 100 פעמים את נפח המדגם. כל המאגרים המשמשים כרומטוגרפיה צריך להיות מסוננים (0.45 יקרומטר או קטן יותר) ומדתחת (למשל, על ידי אמבטיה אולטרה סאונד או ואקום). - גזור אבובים דיאליזה (משקל מולקולרי לגזור [MWCO]: 3.5 kDa) לאורך מתאים עם שטח נוסף לאוויר כדי להבטיח לדוגמה לציפה מעל בר מסתובב מסתובבת.
הערה: גליצרול שומרת על הקרום ויש להסירו לפני השימוש. - כדי להקטין את צמיגות של פתרון חלבון נקי משלב 1.3.2, לדלל את הפתרון עם 25 מ ל של AIEX מאגר A כדי להקל על היישום הבא לטור כרומטוגרפיה. לחבר את הסגר הראשון על אבובים, לטעון את המדגם לתוך הקרום ולצרף את הסגר השני לפחות 1 ס מ מהקצה העליון של אבובים.
- מניחים את מיכל 5 L עם מאגר AIEX A על צלחת מהומה, להוסיף בר מהומה הקרום מלא בתמיסה חלבון. להתאים את המהירות כדי לסובב את המדגם על ידי הימנעות הפרעות עם מסתובב-בר. Dialyze עבור 12 עד 24 שעות ב -4 ° c, לאחר מכן להחליף את המאגר dialyze פוסט (AIEX מאגר A) על ידי הכנה מקורר מחדש ולהמשיך לפחות 4 שעתיים נוספות. העבר את פתרון חלבון דיאליזה לצינור 50 mL ולסנן דרך יחידת מסנן יקרומטר 0.45.
הערה: . האחסון אפשרי
- הכנת anion-exchange כרומטוגרפיה (AIEX) מאגר על ידי המסת 20 מ"מ טריס, 1 מ"מ EDTA ו 1 מ"מ אתילן גליקול-bis (2-עמינח)-N, N, N '-חומצה טטראצטט (EGTA) במים מיולים ולהתאים את ה-pH כדי 8.5 עם HCl. עבור דיאליזה להכין 2 x 5 L ו עבור כרומטוגרפיה 2x 1 L של מאגר AIEX.
- כרומטוגרפיה
- הפעל את מערכת כרומטוגרפיה נוזלית (FPLC) עם תחזוקה כללית, לחבר מאגרי העמודות AIEX A ו-AIEX B (מאגר AIEX A עם 1 M הנאל) ואת שרף anion-exchange המכיל טור. עיין בטבלה 1 עבור פרמטרי כרומטוגרפיים כלליים.
הערה: לפני תחילת ההפעלה (עיין בפרמטרים של כרומטוגרפיים בטבלה 1, בטבלה 2, בטבלה 3, בטבלה 4 ובטבלה 5). - משקל העמודה עם מאגר AIEX A, לאחר מכן לטעון את המדגם על העמודה ולאחר מכן את החלבונים עם מעבר ליניארי מ 0% עד 100% גבוהה מאגר מלח (AIEX B). עיין בטבלה 2 עבור פרוטוקול שיטה מפורט.
- לאסוף 2 מ"ל שברים במהלך הימנעות ולנתח 10 μL של כל שבר על Coomassie מוכתם 15% נתרן dodecyl סולפט פוליאקרילמיד ג'ל אלקטרופורזה (SDS-עמוד). מאגר השברים המכילים חלבון S100A12 עבור דיאליזה.
הערה: המשקל המולקולרי של S100A12 הוא 10,575 Da.
- דיאליזה
- הידרופובי תלוי סידן כרומטוגרפיה (HIC)
- דיאליזה
- Dialyze הפתרון החלבון נגד מילימטר 20 מ"מ, 140 מ"מ הנאל, pH 7.5 בעקבות ההליך המתואר בסעיף 2.1.1.
- כרומטוגרפיה
- להכין 1 L של כרומטוגרפיה מאגר HIC A על ידי המסת 20 מ"מ טריס, 140 mM הנאקל ו 25 מ"מ CaCl2 במים מוהים ולהתאים את ה-pH כדי 7.5. עבור מאגר HIC B, לפזר 20 מ"מ מ טריס, 140 מ"מ הנאל ו 50 מ"מ EDTA. להתאים את ה-pH ל 7.0 ולסנן ולדגה את המאגרים. הוסף CaCl2 למדגם לריכוז סופי של 25 מ"מ ולסנן דרך 0.45 μm. מאגרי hic המתכלה ומדגם עד 4 ° צ' (טמפרטורת עמודה).
- הפעל את מערכת כרומטוגרפיה נוזלית עם תחזוקה כללית, חבר את מאגרי העמודות HIC A ו-B ואת העמודה. עיין בטבלה 3 עבור פרמטרים כרומטוגרפיים נוספים.
- להוריד את העמודה, לטעון את המדגם ולהאריך ' לשטוף את המדגם לא מאוגד ' לחסום עד אות UV מגיע לרמה בסיסית שוב. לאחר מכן להתחיל להתחמק עם כלקטור סידן המכיל מאגר (EDTA). עיין בטבלה 4 עבור פרוטוקול שיטה מפורט.
הערה: ניסויים קודמים הראו כי עודף של סידן נראה מועיל עבור קשירה של S100A12 כרומטוגרפיה שרף. - לאסוף שברי שיא של 2 מ ל ולנתח 10 μL של כל שבר על Coomassie מוכתם 15% SDS-עמוד. הבריכה טהור S100A12 שברים ו dialyze נגד Hepes-מלוחים באגירה (HBS; 20 מ"מ Hepes, 140 מ"מ הייגל, pH 7.0) כמתואר בסעיף 2.1.1.
הערה: מקדם הכחדה של monomeric S100A12 הוא 2980 M-1 ס מ-1.
- דיאליזה
3. איתור והסרה של אנדוטוקסין
-
זיהוי אנדוטוקסין
- כדי לקבוע את זיהום אנדוטוקסין, למדוד ריכוזי חלבון מדולל משלב 2.2.2.4. (למשל, 1:10 ו 1:100 ב HBS) באמצעות האנזים מקושר אנזימים (מבוסס על-ידי משתמשים בשיטה מבוססת-בדיקות פלורסצנט) (שולחן חומרים). בצע את השיטת הפעולה על-ידי ביצוע פרוטוקול היצרן.
הערה: השתמש בפתרונות hbs טריים המומסים מומס במים המוהים ביותר באלקטרופורזה כדי למנוע (חדש) זיהום אנדוטוקסין על ידי המאגר.
- כדי לקבוע את זיהום אנדוטוקסין, למדוד ריכוזי חלבון מדולל משלב 2.2.2.4. (למשל, 1:10 ו 1:100 ב HBS) באמצעות האנזים מקושר אנזימים (מבוסס על-ידי משתמשים בשיטה מבוססת-בדיקות פלורסצנט) (שולחן חומרים). בצע את השיטת הפעולה על-ידי ביצוע פרוטוקול היצרן.
-
הסרת אנדוטוקסין וריכוז חלבונים
- טען 15 mL של מדגם אל 50 kDa מסנן צנטריפוגלי יחידת צנטריפוגה ב 3,200 x g ו 10 ° c עבור כ 10 דקות. להעביר את הזרימה-דרך לתוך כלי חדש (על הקרח) ומילוי מחדש ו צנטריפוגה את שפופרת מסנן kda ה50 לעתים קרובות ככל הנדרש. לשטוף את הממברנה מסנן פעמיים עם HBS כדי לשחזר חלבון רב ככל האפשר לאחר כל שלב.
- רכזו את הזרימה המכילה את S100A12-through באמצעות מסנן של 3 kDa צנטריפוגלי עד שעוצמת הקול מצטמצמת לחמישית עד לעשירית מנפח הטעינה הראשוני (צנטריפוגה ב-3,200 x g, 10 ° c עבור כ -30 דקות). למלא את המסנן לעתים קרובות ככל הצורך, לשטוף את הקרום ולהעביר את הפתרון מרוכז צינור חדש לאחר כל מילוי. התעלם מהזרימה. מסנן שוב באמצעות 50 kDa כמתואר לעיל.
הערה: במהלך הליך זה, אובדן החלבון הוא יוצא מן הכלל (עד 50%), אך הכנת החלבון הנותר מרוקנת לחלוטין מ-LPS. שיטה זו מניבה כ-10/15 מ ג חלבון מתרבות 400 mL. - כוונן את פתרון החלבון ל-1 מ"ג/mL עם HBS ללא שינוי ולמדוד את התוכן LPS כמתואר בשלב 3.1.1. במקרה של פתרון חלבון עדיין לא נבדק כמו LPS-free (< 0.1 האיחוד האירופי/mL), לחסל שארית זהום באמצעות שרף להסרת אנדוטוקסין.
הערה: עם ריכוז חלבון של 1 מ"ג/mL, זיהום של 0.1 האיחוד האירופי/mL LPS שווה כ 0.01 pg LPS/μg חלבון.
4. קשר כימי והפרדת האוליעומר
-
התחברות כימית
- הכינו פתרונות מניות טהורים במיוחד (אנדוטוקסין-free) של 1מטרים ו- 100 מ"מ2 במים בעלי מיים בעלי בדיקת אולטרה-טהורות (טבלת חומרים). השתמש במאגר זה, שנעשה טרי, לשלב הבא.
- מודטה 10 מ ל של מטוהרים אנדוטוקסין S100A12 חינם (ריכוז 1 מ"ג/mL ב HBS) עבור 30 דקות בטמפרטורת החדר (RT) עם 25 מ"מ CaCl2 עבור dimeric/tetrameric, או 25 מ"מ cacl2 ו-1 מ"מ הלאניק2 עבור hexameric/tetrameric S100A12 . לפני שנים
- להכין crosslinker קשר על ידי המסת 8 מ ג BS3 ב 500 μl של המים אנדוטוקסין בחינם ישירות לפני השימוש (8 מ"ג crosslinker קשר עבור 10 mL מחודדים הפתרון חלבון שווה ריכוז סופי של 1.4 mM). מערבבים crosslinker קשר ולדוגמה על ידי ליטוף ו דגירה עבור 30 דקות נוספות ב RT. כיבוי התגובה על ידי הוספת 1 מ טריס-HCl, pH 7.5 לריכוז הסופי של 50 מ"מ ולסנן דרך 0.45 μm.
-
כרומטוגרפיה של החרגת מהגודל
- שיטה זו מדגימה את הדגם המקושר ל-12 עד 15 ° צ' (טמפרטורת טור) ומפעיל את מערכת הכרומטוגרפיה הנוזלית בתחזוקה כללית. חבר את מאגר העמודות (HBS) ואת עמודת ההדרה של הגודל. עיין בטבלה 5 לקבלת מידע מפורט.
- באמצעות העמודה HBS, לטעון לדוגמה לאסוף שברים שיא (1-2-mL) במהלך הריצה. לנתח שברים אלה על 4 למעלה-20% SDS הדרגתי-עמוד ושברים הבריכה עם להקות גדולות של קומפלקס החלבון הרצוי.
הערה: הידרוליזה של מרבית הריאגנטים כגון BS3 בפתרונות מימית מביא לספיגה חזקה ב 280 ננומטר. Crosslinker קשר לא מאוגד (משקל מולקולרי: 572 g/מול) חומק בסוף הריצה ותוצאות בשיא חזק. - רכזו את הפתרונות באמצעות יחידות סינון צנטריפוגלי עם MWCOs של 10 קק (dimer), 30 קודה (טטרמר) או 50 kDa (הבוחנים). לקבוע את זיהום אנדוטוקסין כפי שמתואר בסעיף 3.1. אם יש צורך, להסיר את LPS הנותרים עם שרף להסרת אנדוטוקסין בעקבות המלצות היצרן (טבלת חומרים).
5. בדיקות פונקציונליות במונולוציטים
- הכנת המונולוציטים
- בידוד מונוציטים ממעילים באפי האדם על ידי צפיפות צנטריפוגה הדרגתי והעשרה מונוציט הבאים באמצעות ערכת הפרדת חרוזים מגנטית (טבלת חומרים).
הערה: פרוטוקול זה יביא בקירוב כ-5-7 x 107 מונוציטים (מעיל באפי אחד) עם טוהר של 83-95%. מאחר שהמספר, אך גם ההיענות של התאים תלויה באופן חזק בתורם, ייתכן שיהיה צורך לשנות את הפרוטוקול (בהתאם לספירת התאים הדרושה). - עבור צפיפות צנטריפוגה, באמצעות הפתרון ההפרדה (צפיפות = 1.077 g/mL) כדי RT ולהעביר 20 מ ל לתוך 50 מ"ל צינורות צנטריפוגה (2 צינורות לכל מעיל באפי). לדלל דם ממעיל באפי האנושי עם פתרון המלח באגירה של האנק (HBSS) לנפח כולל של 60 mL ושכבה 30 מ ל של תערובת זו בזהירות על גבי מדיום ההפרדה. צנטריפוגה ב 550 x g עבור 35 דקות ב RT. להשבית את בלם הצנטריפוגה.
- לאחר צנטריפוגה, תאי הדם ההיקפיים היקפיים (PBMCs) ממוקמים ישירות על גבי מדיום ההפרדה. העברת תאים אלה לתוך שפופרת חדש של צנטריפוגה 50 mL, לפצות על 50 mL עם HBSS, ו צנטריפוגה ב 170 x g עבור 10 דקות. ולאחר מכן להשעות את הגלולה תא בנפח קטן של hbss על ידי ליטוף.
- למלא את הצינור עד 50 mL ו צנטריפוגה ב 290 x g עבור 10 דקות. ומלא את הסופרנטאנט שוב, להשעות מחדש את התאים ב-HBSS (50 mL) ו צנטריפוגה ב 170 x g עבור 10 דקות. לספור את התאים ולהשעות אותם במאגר הפרדת תאים (טבלת חומרים < /c9 >) לריכוז של 5 x 107 תאים/mL.
הערה: במקום HBSS, מלוחים באגירה פוספט (PBS) ניתן להשתמש כדי לשטוף את התאים. - עבור בידוד מונוציט מ-PBMCs, השתמש בערכת בידוד תא מגנטית שלילית ועקוב אחר פרוטוקול היצרן. הרוזן מונוציטים ולהשעות מחדש בינונית-מונוציט (RPMI 1640, 15% חום-מופעל סרום עגל העוברי [FCS], 4 מ"מ L-גלוטמין, 100 U/mL פניצילין/סטרפטומיצין) לריכוז של 2 x 106 תאים/mL.
- לתרבות מונוציטים, מנות תרבות הפרווה (לדוגמה, 100 מ"מ) עם הידרופובי, סרט חדיר גז, מתאים לתאיההשעיה (שולחן חומרים). לחטא את הצלחות באמצעות אור UV במשך כ 30 דקות. העבר את התאים ללוחות התרבות האלה ותן להם לנוח לאורך הלילה ב 37 ° c ו-5% CO2.
הערה: השתמש ב-15 עד 25 מ ל של השעיית תאים לכל מנה מצופה.
- בידוד מונוציטים ממעילים באפי האדם על ידי צפיפות צנטריפוגה הדרגתי והעשרה מונוציט הבאים באמצעות ערכת הפרדת חרוזים מגנטית (טבלת חומרים).
- גירוי מונוציט
- גירוי בS100A12 (מסוג wildtype
הערה: כדי להבדיל S100A12 (מוצר קצה ממקטע 2.2.2) מחלבון מקושר, S100A12 בהלן נקרא ' wildtype '.- העבר את התאים נח לתוך צינור צנטריפוגלי 50 mL ו צנטריפוגה ב 350 x g עבור 10 דקות. ומלא את הסופרנטאנט ולהשעות מחדש את הגלולה התא במדיום גירוי (RPMI 1640, 5% חום-inactivated, 4 מ"מ L-גלוטמין, 100 U/mL פניצילין/ סטרפטומיצין) בריכוז של 2 x 106 תאים/mL.
- עבור גירוי, השתמש 24 לוחות הבולם היטב ולהוסיף 250 μL של התא ההשעיה לכל טוב (0.5 x 106 תאים/טוב). הוסף 50 μg/mL polymyxin B כדי הבארות מיועד, ואחריו LPS בריכוזים שונים (25, 50, 100 ו-200 pg/mL) או wildtype S100A12 (10, 20, 40, 60 μg/mL). יתר על כן, להחיל את החלבון או מטופל או חום הלחץ (99 ° צ', 10 דקות) בריכוזים שונים לתאים.
הערה: טיפול בחום קצר מS100A12 חלבון, אך יש לו פחות השפעה על LPS. - הצלחות דגירה עבור 4 h ב 37 ° צ' ו 5% CO2. לקצור את התאים על ידי העברת השעיית התא של כל טוב כדי 1.5 mL התגובה צינורות. צנטריפוגה ב 500 x g עבור 10 דקות. להעביר את supernatants צינורות טריים ולמדוד tnfα לשחרר בדיעות שונות (g., 1:2, 1:5, 1:10) עם ערכת האדם TNFα אליסה בעקבות המלצות היצרן.
- גירוי בS100A12 אולימרים
- הכן והזרע החוצה מונוציטים ב -24 לוחיות ההשעיה היטב כמתואר לעיל. לעורר את התאים על ידי הוספת S100A12 oligomers משלב 4.2.3. בריכוזים שונים של מולרי (125 nM, 250 nM, 500 nM, 1000 nM).
הערה: על מנת להשוות את היכולות של oligomers שונים כדי לעורר מונוציטים, oligomers הוחלו על התאים בריכוזים של מולרי המקבילה. - דגירה עבור 4 h ב 37 ° צ' ו 5% CO2, לקצור את התאים ולמדוד TNFα לשחרר את סופרנטנמלים כפי שמתואר לעיל.
- הכן והזרע החוצה מונוציטים ב -24 לוחיות ההשעיה היטב כמתואר לעיל. לעורר את התאים על ידי הוספת S100A12 oligomers משלב 4.2.3. בריכוזים שונים של מולרי (125 nM, 250 nM, 500 nM, 1000 nM).
- גירוי בS100A12 (מסוג wildtype
תוצאות
בעקבות טיהור מראש בעמודת AIEX (איור 1א-ג) והבאים התלויים בסידן hic (איור 2א, ב), חלבון טהור מאוד הושג (איור 2c). בנוסף, מדידות של אנדוטוקסין חשף הסרת LPS מוצלחת. תוכן ה-LPS שלאחר AIEX נמדד בדילול 1:10 מעל למגבלת זיהוי ה, כלומר, מעל 500 האיחוד האירופי/mL. לאחר הסינון הראשון באמצעות יחידת סינון kDa 50, התוכן LPS הופחת ל-1 EU/mL. בעקבות ריכוז 3 kDa מסנן יחידת סינון נוסף דרך 50 kDa, זיהום LPS נמדד היה 0.08 EU/mL.
כפקד נוסף, מונוציטים האדם היו מגורה עם חלבון מסוג wildtype (איור 3A, B). Polymyxin B טיפול באברושערים משחרר מסוג LPS-מוולוציטים, אשר לא ניתן להבחין עם S100A12. מצד שני, טיפול בחום של LPS ו S100A12 מבטל את יכולת החלבון לגרות את התאים, בעוד זה לא משפיע על התגובה התאית ל-LPS-גירוי.
חשיפת חלבונים ליונים שונים יוצרת הסדר של S100A12 oligomers שונים (איור 4A). הקשר הכימי מאפשר ללכוד מתחמים מוגדרים כגון דימרס, טטרמרס, ו הבוחנים, כמו גם מצבי מעבר (למשל, ' טרימרס ', להקה בערך 30 kDa). על מנת לגרום לשינוי בולט של מאזן האולייומר לפני החיבור, הוחל עודף יונים (איור 4B).
Oligomers מבודדים בריכוזים שווים של הטוחנת (איור 5א-ג) היו לאחר מכן גירוי מונוציט כדי להשוות את היכולות איתות באמצעות Prrs. מונוציט גירוי עם hexameric S100A12 הביא ביטוי tnfα שחרור (איור 6 ). שארית ציטוקינים שחרור ניתן להבחין בין תאים מגורה עם tetrameric S100A12, בעוד הטיפול עם dimeric חלבון אינו לגרום tnfα לשחרר.

איור 1: תוצאות כרומטוגרפיה של אניב-exchange. (א) כרומאטוגרם עם ספיגת ב280 ננומטר (a280) ואחוז מאגר האלוטור B (קו מקווקו). בלוקים של שיטות מצוינים עם A = לשטוף מדגם לא מאוגד, B = מעבר ליניארי עם מאגר משחררי (מאגר B), C = לשטוף עם מאגר B, ו-D = שינוי מחדש במאגר A. (ב) להתמקד בפסגות הרלוונטיות עם מספרים שפופרת שבר באדום. (ג) שברים נבחרים נותחו ב-15% coomassie ויטראז '-עמוד. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 2: תוצאות כרומטוגרפיה של הידרופובי-אינטראקציה. (א) כרומאטוגרם עם ספיגת ב280 ננומטר (a280) ואחוז מאגר האלוטור B (קו מקווקו). בלוקים של שיטות מצוינים עם A = לשטוף מדגם לא מאוגד, B = הימנעות עם מאגר B, ו-C = מחדש השפה במאגר A. (ב) להתמקד בפסגות הרלוונטיות עם מספרי צינור שבר באדום. (ג) שברים שנותחו ב-15% coomassie המוכתמת-עמוד. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 3: מונוציטים האדם העיקרי היו מגורה בריכוזים שצוין. LPS (A) או S100A12 (מסוגWildtype B) נותרו ללא טיפול או חום-מודגש (99 ° c, 10 דקות). שני התנאים נבדקו בנוכחות והעדר של polymyxin B. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
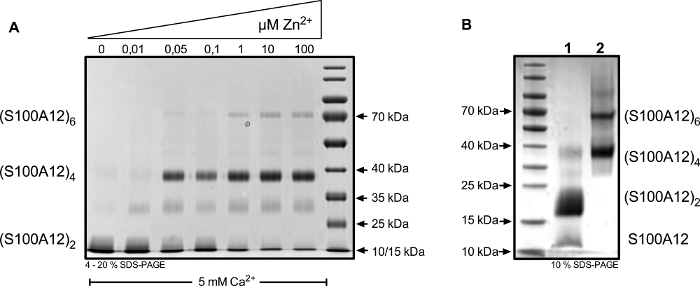
איור 4: חלבון S100A12 היה מקושר עם BS3 לאחר דגירה במאגר hbs המכיל 5 מ"מ Ca2 + והצביעו zn2 + ריכוזים. (א) הגדלת zn2 + ריכוזים לגרום הסדר של S100A12 לתוך הטטרמרים והבוחנים על הפרדה על 4 למעלה 20% COOMASSIE מוכתם sds-עמוד. (ב) כתוצאה מייצוג של oligomers מקושרים עם תנאים המשמשים להפרדה בעמודה החרגה מהגודל. S100A12 היה מקושר בנוכחות של 25 מ"מ Ca2 + (ליין 1) או 25 מ"מ ca2 + ו 1 מ"מ zn2 + (ליין 2). (S100A12) 2 = דיימר; (S100A12) 4 = טטרמר; (S100A12) 6 = החודש . אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 5: S100A12 oligomers הופרדו על עמודה הדרה גודל. (א) כרומואטוגרמה של הפרדת ההקשמר/טטראמר לאחר הקישור במאגר hbs עם 25 מ"מ cacl2 ו 1 מ"מ לאחד2. (ב) כרומטוגרמה עבור הפרדת הטטרמר במאגר hbs עם 25 מ"מ cacl2. (ג) דוגמה לאויגמרים במאגר ומרוכז לאחר הפרדה על מפרידי מערכות הדרגתיות 4-15% SDS-עמוד. ליין 1 = dimer; ליין 2 = טטרמר; ליין 3 = הג. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 6: גירוי של מונוציטים עם S100A12 oligomers מטוהרים. TNFα-שחרור לאחר 4 h דגירה היה כימות על ידי אליסה. הנתונים מציגים את הערך הממוצע משני ניסויים עצמאיים. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
| נפח מיטה (CV) | 75 מ ל |
| הצג | ספיגת ב280 nM |
| מקסימום לחץ | 3 בר |
| מאגר עמודות A | 20 מ"מ Tris-HCl, 1 מ"מ EDTA, 1 מ"מ EGTA, pH 8.5 |
| מאגר עמודות B | 20 מ"מ Tris-HCl, 1 מ"מ EDTA, 1 מ"מ EGTA, 1 M הנאגל, pH 8.5 |
| נפח לדוגמה | שתנה |
| קצב זרימה | 1-2 מ ל/דקה |
| טמפרטורה | 4 מעלות צלזיוס |
טבלה 1: מידע מפורט על הפרמטרים המוחלים של כרומטוגרפיה של anion-exchange.
| חסום | אמצעי אחסון | אגר | שקע |
| שיווציה | 1 שני אמצעי אחסון לעמודות (קורות חיים) | קצת | פסולת |
| מטען לדוגמה | n/a | קצת | פסולת |
| שטוף מדגם לא מאוגד | 1 קורות חיים | קצת | שקע בנפח גבוה |
| שינוי הדרגתי – הללויה | 0 כ 100% מאגר B ב 1 קורות חיים | א-ב | אספן שבר |
| התרחץ – מאגר B | 1 קורות חיים | B | פסולת |
| מחדש באקוויציה | 2 קורות חיים | קצת | פסולת |
טבלה 2: מידע מפורט על השיטה הנמצאת בשימוש של כרומטוגרפיה של anion-exchange.
| נפח מיטה (CV) | 125 מ ל |
| הצג | ספיגת ב280 nM |
| מקסימום לחץ | 4 בר |
| מאגר עמודות A | 20 מ"מ טריס, 140 מ"מ הנאקל, 25 מ"מ CaCl2, pH 7.5 |
| מאגר עמודות B | 20 מ"מ טריס, 140 מ"מ היום, 50 mM EDTA, pH 7.5 |
| נפח לדוגמה | שתנה |
| קצב זרימה | 1-2 מ ל/דקה |
| טמפרטורה | 4 מעלות צלזיוס |
טבלה 3: מידע מפורט על הפרמטרים המוחלים של כרומטוגרפיה הידרופובי-אינטראקציה.
| חסום | אמצעי אחסון | אגר | שקע |
| שיווציה | 1 שני אמצעי אחסון לעמודות (קורות חיים) | קצת | פסולת |
| מטען לדוגמה | n/a | קצת | פסולת |
| שטוף מדגם לא מאוגד | 1-2 קורות חיים | קצת | שקע בנפח גבוה |
| אלוציה | 100% מאגר B | B | אספן שבר |
| התרחץ – מאגר B | 1 קורות חיים | B | פסולת |
| מחדש באקוויציה | 2 קורות חיים | קצת | פסולת |
שולחן 4: מידע מפורט על השיטה המשמשת כרומטוגרפיה לאינטראקציה הידרופובי.
| נפח מיטה (CV) | 320 מ ל |
| הצג | ספיגה ב280 ננומטר |
| מקסימום לחץ | 3 בר |
| מאגר עמודות A | 20 מ"מ Hepes, 140 מ"מ הייקל, pH 7.2 |
| נפח לדוגמה | עד 13 מל ' |
| קצב זרימה | 1-1.5 מ"ל לדקה |
| טמפרטורה | 12 עד 15 ° צ' |
טבלה 5: מידע מפורט על הפרמטרים המוחלים של כרומטוגרפיה של אי-הכללה בגודל.
טבלה משלימה 1: הכנת מאגרים ופתרונות מניות. אנא לחץ כאן כדי להוריד קובץ זה.
Discussion
בפרוטוקול זה, אנו מתארים ביטוי בקטריאלי ללא תג של S100A12 האדם ואת הטיהור שלה, כמו גם הפרדה לתוך שונים המושרה יון oligomers הנגרמת על ידי גירוי תא החיסון. בהשוואה לספרות שפורסמה על טיהור חלבון S100A128,23,24, השימוש גבוה cacl2 (25 מ"מ) ב הידרופובי-אינטראקציה כרומטוגרפיה היא לידע שלנו ייחודי. פרוטוקולים מספר החלת ריכוזים מ 1 עד 5 מ"מ לייצר חלבון טהור, ובכל זאת הבחנו בתשואה גבוהה מספר פעמים בעקבות הגישה שלנו באמצעות ה-25 מ"מ CaCl2 במקום. זה יכול להיות מוסבר על ידי היררכיה של אינטראקציה עם החומר בעמודה: S100A12 יכול לאגד ישירות לחומר העמודה, אך עודף Ca2 + עשוי גם להקל על כריכה עקיפה של S100A12-dimers לחלבון מאוגד העמודה כבר 8. Thus, גבוהה Ca2 + ריכוזים עשויים להגדיל את פני השטח זמין עבור טיהור S100A12. הללויה (באמצעות מעבר ליניארי) של S100A12 מ HIC כאחד מוקדם (כרוך בעקיפין S100A12) ושיא אחד מאוחר מאוד (חלבון מאוגד חומר העמודה) עשוי לתמוך ספקולציות זה (נתונים לא מוצגים).
לייצור של רקומביננטי S100A12 (כמו גם חלבונים אחרים) ב תשואה גבוהה ועלויות לניהול, חלבון ביטוי E. coli הוא עדיין שיטת הבחירה. עם זאת, זיהום בלתי נמנע עם האנדוטוקסינים החיידק נשאר בעיה, כאשר חלבונים נקבעים על ניסויים בתרבות התא, במיוחד במחקרים הכרוכים בתאים חיסוניים מולדים. לניסיוננו, אפילו חלבונים זמינים מסחרית הכריז במפורש עבור שימוש בתרבות התא יכול להכיל אנדוטוקסין זהום עד 1 חלבון EU/μg, אשר ניתן להטות באופן משמעותי. לכן, הסרת רעלים מוחלטת היא חובה. ונומרים אנדוטוקסין בטווח הפתרון מתוך משקולות מולקולריות של 10 עד 20 kda, אבל הם יכולים ליצור מיקרולים ומבנים עם משקולות מולקולרי גבוה יותר. היווצרות מבנים גדולים מאוד הוא, למשל, מקודם דרך יוני ביונטי21,25.
על פי הפרוטוקול שלנו, אנו מאמתים את הייצור האנדוטוקסין ללא הS100A12 חלבון באמצעות שילוב של מדידות אנדוטוקסין ברגישות גבוהה באמצעות גירוי מונואלי. אנו רואים שילוב כזה משמעותי במיוחד כמו a) זיהום אנדוטוקסין ברמה נמוכה עשוי להיות קשה להעריך בהתאם לרגישות של המיקום ו-b) השימוש polymyxin B כמו מעכב LPS על מונוציטים עלול לגרום קשה לפענח נתונים בשל לאפקטי polymyxin B בלעדיים על תאים26,27. Polymyxin B, כמו גם פפטידים אחרים האחרים דיווחו לאגד LPS באמצעות שלילית טעונה שומנים מסוג A28. כמו המשטח חשוף הממס של S100A12 מכיל גם טלאים גדולים שלילית טעונה הפחתת הנצפה של TNFα-שחרור מ-S100A12 מגורה מונוציטים האדם בנוכחות polymyxin B (איור 3B) יכול להיות בשל a) מחייב ישירה לא ספציפי של polymyxin B כדי S100A12 ו/או B) השפעות ישירות של polymyxin b על תאים ממריצים26,27. בשל מגבלות ידועות הן זיהוי של זיהום אנדוטוקסין ברמה נמוכה כמו גם השפעות polymyxin B לא ספציפי, הפרוטוקול שלנו עוד מכיל צעד הפעלה בחום כדי להבדיל בבירור בין LPS-חלבון-תיווך TLR4-איתות.
שימוש ב-LPS-free S100A12 לייצור וטיהור של oligomers המושרה הגדיר היא קריטית ותשומת לב נוספת צריך להיות משולם לטיהור הבאים שלהם כדי למנוע בסופו של דבר הקדמה של אנדוטוקסין דרך מאגרים או חומר העמודה וכך חלבון נוסף בדרישה LPS-דלדול דרך הסרת שרפים אנטוקסין.
הרלוונטיות של oligomerization עבור הפונקציה הביולוגית של חלבונים ניתן להעריך באמצעים שונים. במקרה של S100A12, השתמשנו בתהודה משטח, כמו גם לחילופי חומצות אמינו ממוקדות באתרים כריכת יון ו--להגדיר בדיוק את חלבון מורכב מסוגל לאגד ולאותת דרך TLR4-אנו מועסקים החוצה כימית המקשר של Ca2 +/Zn2 + -פעמו רקומביננטי S100A1216. מעבר כימי של S100A12 בתנאים יוניים שונים snap-קופא מדינה רגעית כולל צורות oligomeric מספר כי הם במעבר. מתוך ניסויי יון טיטור, הגדרתם מצבים שבהם dimeric, tetrameric או הקסאמנרס, ניתן לקבוע כ-oligomers השולט16. בנוסף, ניסויים קודמים הראו כי עודף יונים הוא מועיל עבור המקבילה, מעבר יציב וטיהור לאחר מכן, למרות oligomerization יכול להיגרם גם בריכוזים נמוכים משמעותית של יון. עם זאת, טיהור האויגמרים האלה באמצעות כרומטוגרפיה של הוצאה מהכלל מביא לתוצאה טובה, אך לא הפרדה מוחלטת. ובכל זאת, העשרת האולימרים הסלקטיביים. מאפשרים ניתוח מהימן במורד הזרם
לסיכום, פרוטוקול זה מספק שיטה לטיהור של LPS-free S100A12 אנושי או הקשורים חלבונים כריכת סידן. כדי לתקן שינויים המושרה יון, מרובי כימיים והפרדה מורכבת לאחר מכן על ידי הוצאת גודל כרומטוגרפיה הוא כלי שימושי כדי להבין את הרלוונטיות של oligomerization חלבונים עבור תהליכים ביולוגיים במורד.
Disclosures
. למחברים אין מה לגלות
Acknowledgements
מחקר זה היה נתמך על ידי מענקים מתוך תוכנית המחקר הרפואי חדשני של אוניברסיטת Muenster הפקולטה לרפואה (KE121201 ל-ק. ק.) וקרן המחקר הגרמני (DFG, Fo354/3-1 כדי D.F.).
Materials
| Name | Company | Catalog Number | Comments |
| pET11b vector | Novagen | ||
| BL21(DE3) competent E. coli | New England Biolabs | C2527 | |
| 100x Non-essential amino acids | Merck | K 0293 | |
| 25% HCl | Carl Roth | X897.1 | |
| 4−20% Mini-PROTEAN TGX Protein Gels | BioRad | 4561093 | |
| Ampicillin sodium salt | Carl Roth | HP62.1 | |
| BS3 (bis(sulfosuccinimidyl)suberate) - 50 mg | ThermoFisher Scientific | 21580 | |
| Calciumchlorid Dihydrat | Carl Roth | 5239.1 | |
| Coomassie Briliant Blue R250 Destaining Solution | BioRad | 1610438 | |
| Coomassie Briliant Blue R250 Staining Solution | BioRad | 1610436 | |
| EasySep Human Monocyte Enrichment Kit | Stemcell | 19059 | Magnetic negative cell isolation kit |
| EDTA disodium salt dihydrate | Carl Roth | 8043.1 | |
| EGTA | Carl Roth | 3054.3 | |
| EndoLISA | Hyglos | 609033 | Endotoxin detection assay |
| Endotoxin-Free Ultra Pure Water | Sigma-Aldrich | TMS-011-A | Ultrapure water for preparation of endotoxin-free buffers |
| EndoTrap red | Hyglos | 321063 | Endotoxin removal resin |
| FBS (heat-inactivated) | Gibco | 10270 | |
| HBSS, no calcium, no magnesium | ThermoFisher Scientific | 14175053 | |
| Hepes | Carl Roth | 9105 | |
| Hepes (high quality, endotoxin testet) | Sigma-Aldrich | H4034 | |
| hTNF-alpha - OptEia ELISA Set | BD | 555212 | |
| IPTG (isopropyl-ß-D-thiogalactopyranosid) | Carl Roth | CN08.1 | |
| L-Glutamine (200 mM) | Merck | K 0282 | |
| LB-Medium | Carl Roth | X968.1 | |
| Lipopolysaccharides from E. coli O55:B5 | Merck | L6529 | |
| Pancoll, human | PAN Biotech | P04-60500 | Separation solution (density gradient centrifugation) |
| Penicillin/Streptomycin (10.000 U/mL) | Merck | A 2212 | |
| Phenyl Sepharose High Performance | GE Healthcare | 17-1082-01 | Resin for hydrophobic interaction chromatography |
| Polymyxin B | Invivogen | tlrl-pmb | |
| Protease inhibitor tablets | Roche | 11873580001 | |
| Q Sepharose Fast Flow | GE Healthcare | 17-0510-01 | Resin for anion-exchange chromatography |
| RoboSep buffer | Stemcell | 20104 | Cell separation buffer (section 5.1.4) |
| RPMI 1640 Medium | Merck | F 1215 | |
| Sodium chloride (NaCl) | Carl Roth | 3957.2 | |
| Sodium hydroxide | Carl Roth | P031.1 | |
| Tris Base | Carl Roth | 4855.3 | |
| Zinc chloride | Carl Roth | T887 | |
| Labware | |||
| 0,45 µm syringe filter | Merck | SLHA033SS | |
| 14 mL roundbottom tubes | BD | 352059 | |
| 2 L Erlenmyer flask | Carl Roth | LY98.1 | |
| 24 well suspension plates | Greiner | 662102 | |
| 5 L measuring beaker | Carl Roth | CKN3.1 | |
| 50 mL conical centrifuge tubes | Corning | 430829 | |
| 50 mL high-speed centrifuge tubes | Eppendorf | 3,01,22,178 | |
| Amicon Ultra-15 Centrifugal Filter Unit MWCO 3 kDa | Merck | UFC900324 | |
| Amicon Ultra-15 Centrifugal Filter Unit MWCO 50 kDa | Merck | UFC905024 | |
| Culture dish (100 mm) | Sarstedt | 83.3902 | |
| Dialysis Tubing Closures | Spectrum | 132738 | |
| EasySep magnet 'The Big Easy` | Stemcell | 18001 | |
| Fraction collector tubes 5 mL | Greiner | 115101 | |
| Lumox film, 25 µm, 305 mm x 40 m | Sarstedt | 94,60,77,316 | Film for monocyte culture plates |
| Spectra/Por Dialysis Membrane (3.5 kDa) | Spectrum | 132724 | |
| Steritop filter unit | Merck | SCGPT01RE | |
| Equipment | |||
| 37 °C Incubator (with shaking) | New Brunswick Scientific | Innova 42 | |
| ÄKTA purifier UPC 10 | GE Healthcare | FPLC System | |
| Fraction collector | GE Healthcare | Frac-920 | |
| Centrifuge (with rotor A-4-81) | Eppendorf | 5810R | |
| Fixed angle rotor | Eppendorf | F-34-6-38 | |
| Mini Protean Tetra Cell | BioRad | 1658000EDU | |
| NanoPhotometer | Implen | P330 | |
| Sonicator | Brandelin | UW2070 | |
| Fluorescence reader | Tecan | infinite M200PRO | |
| pH meter | Knick | 765 |
References
- Liston, A., Masters, S. L. Homeostasis-altering molecular processes as mechanisms of inflammasome activation. Nature Reviews Immunology. 17 (3), 208-214 (2017).
- Kessel, C., Holzinger, D., Foell, D. Phagocyte-derived S100 proteins in autoinflammation: putative role in pathogenesis and usefulness as biomarkers. Clinical Immunology. 147 (3), 229-241 (2013).
- Baker, T. M., Nakashige, T. G., Nolan, E. M., Neidig, M. L. Magnetic circular dichroism studies of iron(ii) binding to human calprotectin. Chemical Science. 8 (2), 1369-1377 (2017).
- Nakashige, T. G., Zhang, B., Krebs, C., Nolan, E. M. Human calprotectin is an iron-sequestering host-defense protein. Nature Chemical Biology. 11 (10), 765-771 (2015).
- Nakashige, T. G., Zygiel, E. M., Drennan, C. L., Nolan, E. M. Nickel Sequestration by the Host-Defense Protein Human Calprotectin. Journal of the American Chemical Society. 139 (26), 8828-8836 (2017).
- Cunden, L. S., Gaillard, A., Nolan, E. M. Calcium Ions Tune the Zinc-Sequestering Properties and Antimicrobial Activity of Human S100A12. Chemical Science. 7 (2), 1338-1348 (2016).
- Moroz, O. V., et al. Structure of the human S100A12-copper complex: implications for host-parasite defence. Acta Crystallographica Section D, Biological Crystallography. 59 (Pt 5), 859-867 (2003).
- Moroz, O. V., Blagova, E. V., Wilkinson, A. J., Wilson, K. S., Bronstein, I. B. The crystal structures of human S100A12 in apo form and in complex with zinc: new insights into S100A12 oligomerisation. Journal of Molecular Biology. 391 (3), 536-551 (2009).
- Korndorfer, I. P., Brueckner, F., Skerra, A. The crystal structure of the human (S100A8/S100A9)2 heterotetramer, calprotectin, illustrates how conformational changes of interacting alpha-helices can determine specific association of two EF-hand proteins. Journal of Molecular Biology. 370 (5), 887-898 (2007).
- Moroz, O. V., et al. Both Ca2+ and Zn2+ are essential for S100A12 protein oligomerization and function. BMC Biochemistry. 10, 11(2009).
- Baudier, J., Glasser, N., Gerard, D. Ions binding to S100 proteins. I. Calcium- and zinc-binding properties of bovine brain S100 alpha alpha, S100a (alpha beta), and S100b (beta beta) protein: Zn2+ regulates Ca2+ binding on S100b protein. Journal of Biological Chemistry. 261 (18), 8192-8203 (1986).
- Dell’Angelica, E. C., Schleicher, C. H., Santome, J. A. Primary structure and binding properties of calgranulin C, a novel S100-like calcium-binding protein from pig granulocytes. Journal of Biological Chemistry. 269 (46), 28929-28936 (1994).
- Vogl, T., et al. S100A12 is expressed exclusively by granulocytes and acts independently from MRP8 and MRP14. Journal of Biological Chemistry. 274 (36), 25291-25296 (1999).
- Hofmann, M. A., et al. RAGE mediates a novel proinflammatory axis: a central cell surface receptor for S100/calgranulin polypeptides. Cell. 97 (7), 889-901 (1999).
- Foell, D., et al. Proinflammatory S100A12 Can Activate Human Monocytes via Toll-like Receptor 4. American Journal of Respiratory and Critical Care Medicine. 187 (12), 1324-1334 (2013).
- Kessel, C., et al. Calcium and zinc tune autoinflammatory Toll-like receptor 4 signaling by S100A12. Journal of Allergy and Clinical Immunology. 142 (4), 1370-1373 (2018).
- Armaroli, G., et al. Monocyte-Derived Interleukin-1beta As the Driver of S100A12-Induced Sterile Inflammatory Activation of Human Coronary Artery Endothelial Cells: Implications for the Pathogenesis of Kawasaki Disease. Arthritis & Rheumatology. 71 (5), 792-804 (2019).
- GE Healthcare. Strategies for Protein Purification. Handbook. , Freiburg, Germany. (2010).
- Jackson, E., Little, S., Franklin, D. S., Gaddy, J. A., Damo, S. M. Expression, Purification, and Antimicrobial Activity of S100A12. Journal of Visualized Experiments. (123), (2017).
- Kiss, B., Ecsedi, P., Simon, M., Nyitray, L. Isolation and Characterization of S100 Protein-Protein Complexes. Methods in Molecular Biology. 1929, 325-338 (2019).
- Magalhaes, P. O., et al. Methods of endotoxin removal from biological preparations: a review. Journal of Pharmacy and Pharmaceutical Sciences. 10 (3), 388-404 (2007).
- Petsch, D., Anspach, F. B. Endotoxin removal from protein solutions. Journal of Biotechnology. 76 (2-3), 97-119 (2000).
- Heilmann, R. M., Suchodolski, J. S., Steiner, J. M. Purification and partial characterization of canine S100A12. Biochimie. 92 (12), 1914-1922 (2010).
- Hung, K. W., Hsu, C. C., Yu, C. Solution structure of human Ca2+-bound S100A12. Journal of Biomolecular NMR. 57 (3), 313-318 (2013).
- Endotoxin Removal. Application Note - Sartorius Stedim Biotech. , (2010).
- Hogasen, A. K. M., Abrahamsen, T. G. Polymyxin-B Stimulates Production of Complement Components and Cytokines in Human Monocytes. Antimicrobial Agents and Chemotherapy. 39 (2), 529-532 (1995).
- Valentinis, B., et al. Direct effects of polymyxin B on human dendritic cells maturation - The role of I kappa B-alpha/NF-kappa B and ERK1/2 pathways and adhesion. Journal of Biological Chemistry. 280 (14), 14264-14271 (2005).
- Teuber, M., Miller, I. R. Selective Binding of Polymyxin-B to Negatively Charged Lipid Monolayers. Biochimica Et Biophysica Acta. 467 (3), 280-289 (1977).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved