Method Article
Une nouvelle méthode pour l’analyse de pentosane présente dans la biomasse Jute et sa transformation en monomères de sucre à l’aide d’acide liquide ionique
Dans cet article
Résumé
Nous présentons un protocole pour la synthèse de sucres C5 (xylose et l’arabinose) d’une renouvelable biomasse ligno-cellulosique non comestibles (c.-à-d., jute) avec la présence de liquides ioniques acides de Brønsted (BAILs) le rôle de catalyseur dans l’eau. Le catalyseur de ballots expose mieux rendement catalytique que catalyseurs acides minéraux classiques (H2SO4 et HCl).
Résumé
Récemment, des liquides ioniques (ILs) sont utilisés pour la valorisation de la biomasse en produits chimiques produits précieux en raison de leurs propriétés remarquables comme stabilité thermique, pression de vapeur inférieure, ininflammabilité, capacité de chaleur plus élevée et solubilité accordable et acidité. Ici, nous démontrons une méthode pour la synthèse de sucres C5 (xylose et l’arabinose) depuis le pentosane présente dans la biomasse de jute dans un processus d’un pot en utilisant une quantité catalytique de sulfate d’hydrogène 1-methyl-3-(3-sulfopropyl)-imidazolium acides de Brønsted IL. L’acide IL est synthétisé en laboratoire et caractérisées à l’aide de techniques de spectroscopie RMN pour comprendre sa pureté. Les différentes propriétés d’un cautionnement sont mesurées comme la force de l’acide, stabilité thermique et hydrothermale, ce qui montre que le catalyseur est stable à une température plus élevée (250 ° C) et possède de très grande force de l’acide (Ho 1,57). L’acide IL convertit plus de 90 % de pentosane dans les sucres et le furfural. Par conséquent, la méthode de présentation dans cette étude peut également être utilisée pour l’évaluation de la concentration de pentosane dans d’autres types de biomasse ligno-cellulosique.
Introduction
La biomasse a un grand potentiel comme une énergie renouvelable et la source chimique parce qu’il est durable, peu coûteux et tout aussi distribués à la différence des ressources fossiles, ce qui en fait l’un des candidats prometteurs pour remplacer les matières premières fossiles. La production estimée de biomasse ligno-cellulosique est 146 milliards de tonnes / année1. La biomasse lignocellulosique est principalement composée de lignine, cellulose et hémicellulose comme ses trois principaux constituants. La lignine est un polymère aromatique issu d’unités phénylpropanoïdes ; en revanche, cellulose et l’hémicellulose sont les parties de polysaccharide de la biomasse lignocellulosique. Cellulose est composé d’unités de glucose reliées par β(1→4) lien glycosidique, tandis que les hémicelluloses se compose de sucres C5, C6 sucres et acides de sucre reliés entre eux par β (1→4), β (1→3) et β (1→6) liaisons glycosidiques2,3. Ainsi que divers biomasse ligno-cellulosiques (bagasse, cosse de riz, paille de blé, etc.), la biomasse lignocellulosique de jute est aussi produite en très grande quantité (environ 98 % en 2014) en Asie par rapport à la production de jute total dans le monde. L’Inde produit 1,96 x 106 tonnes de biomasse de jute tandis que Bangladesh produit 1,34 x 106 tonnes de biomasse de jute par rapport à la production totale de biomasse de jute dans le monde (3,39 x 106 tonnes) en 20144. L’utilisation de cette biomasse non comestible n’entrera en conflit avec la demande alimentaire. Par conséquent, il est bénéfique pour l’utiliser comme un stock pour la synthèse d’une variété de valeur ajoutée produits chimiques (xylose, arabinose, furfural, 5-hydroxyméthylfurfural (HMF), etc.). Selon l’US Department of Energy, furfural et HMF sont considérés comme certains des produits chimiques top 30 bloc de construction provenant de la biomasse5. Furfural est obtenu à partir du xylose ou directement à partir de hémicellulose et peut être converti en nombre important de produits chimiques. Alcool furfurylique, furane de méthyle et le tétrahydrofurane sont importants produits chimiques obtenus à partir de furfural6. Conversion de la biomasse lignocellulosique telles que la biomasse de jute en sucres C5 et autres produits chimiques importants est donc un sujet important.
Extensive des rapports sont disponibles sur les différentes méthodes catalytiques pour la conversion de la biomasse lignocellulosique en valeur ajoutée produits chimiques. Les acides minéraux (HCl et H2SO4) et de catalyseurs hétérogènes (Amberlyst, HMOR, Jean-Louis, SAPO-44, etc.) ont été significativement utilisées pour la conversion d’hémicellulose et de la biomasse lignocellulosique en sucres (sucres pentoses et des hexoses) et furannes (furfural et HMF)7,8. La réutilisabilité et l’action corrosive de l’acide minéral est un enjeu majeur. Cependant, avec le catalyseur acide solide, température et des pressions plus élevées sont nécessaires parce que la réaction se produit à la surface du catalyseur. Pour surmonter ces problèmes, récemment ILs sont signalés pour la valorisation de la biomasse comme un catalyseur ou un solvant9,10,11,12,13,14. L’utilisation de IL comme solvant n’est pas une meilleure méthode en raison de son coût plus élevé et la pression de vapeur inférieure d’ILs qui crée des difficultés dans la séparation de produits. Par conséquent, il est impératif d’utiliser IL recyclable comme catalyseur (en petites quantités) dans un système de solvants de l’eau pour la conversion de la biomasse à valeur ajoutée produits chimiques.
Nous présentons ici une méthode pour utiliser 1-methyl-3-(3-sulfopropyl) imidazolium hydrogène sulfate acide IL comme catalyseur pour la conversion directe de pentosane présente dans la biomasse jute en monomères de sucre sans aucun prétraitement. Souvent, ILs sont signalés pour le prétraitement de la biomasse lignocellulosique10,15,16,17 alors que la très grande quantité de l’ILs est utilisée pour le prétraitement de la biomasse. Par conséquent, il est toujours avantageux d’utiliser IL comme catalyseur et pour convertir la biomasse lignocellulosique en produits chimiques sans traitement supplémentaire. En outre, dans le présent travail, la teneur en lignine présentée en biomasse de jute calculée selon méthode Klason qui pourrait se transformer en différents monomères aromatiques18.
Protocole
Plusieurs substances chimiques utilisées dans les travaux de présentation sont toxiques et cancérigènes. Copiez toutes les pratiques de sécurité qui s’imposent lorsque vous effectuez la synthèse de l’IL et la transformation de la biomasse.
1. préparation des acide IL
- Ajouter 7,625 mmol de 1, 3-propane sultone dans un 50 mL ballon à fond rond, puis fermez le ballon avec un septum en caoutchouc.
- Ajouter 7,625 mmol de 1-méthylimidazole dans 7,625 mmol de 1, 3-propanesultone lentement (10 min) à 0 ° C à l’aide d’une seringue (1 mL).
- Après l’addition complète de 1-méthylimidazole et 1, 3-propanesultone, ajouter 15 mL de toluène sec et reflux le mélange pendant 16 h à 120 ° C pour obtenir le zwitterion solid.
- Séparer le zwitterion de toluène à l’aide de filtration et laver le zwitterion avec 40 mL de toluène. Pour sécher le zwitterion, régler la température du four à 80 ° C. Une fois que la température du four atteint 80 ° C, conserver l’échantillon dans le four pendant 4 h et ensuite utiliser le zwitterion séché à l’étape suivante.
- Ajouter de l’acide sulfurique dans le ballon contenant le zwitterion (moles égales de zwitterion et d’acide sulfurique) à l’aide d’une micropipette 1 000 µL. Puis connecter le ballon d’un réfrigérant à reflux. Faire chauffer et remuer le mélange à 110 ° C pendant 12 h obtenir l’IL désiré.
NOTE : La réaction entre l’acide sulfurique et zwitterion s’effectue sans aucun solvant. - Après la synthèse des acide IL, caractériser à l’aide de 13C RMN du 1H et.
2. détermination de l’acidité de Hammett (Ho)
- Ajouter 10 mg de la p- nitroaniline indicateur dans une fiole jaugée de 1 L et ensuite ajouter l’eau distillée pour préparer une solution de 1 L. Agiter la solution bien à la main pendant 2 min et laissez la solution pendant 1 h à mélanger la p- nitroaniline dans l’eau (solution à blanc).
- Ajouter 1,59 mmol d’ions H+ du catalyseur acide (HCl/H2SO4/ acides IL) à 50 mL de solution d’indicateur p- nitroaniline et agiter la solution à la main pour le mélange (solution de l’échantillon).
Notez tous les catalyseurs acides utilisés dans le présent travail (HCl, H2SO4et IL acide) sont ajoutés individuellement dans la solution d’indicateur de 50 mL (tableau 1) pour la détermination de l’acidité de Hammett (Ho). - Effectuer la mesure UV de la solution témoin (p- nitroaniline solution) et la solution d’échantillon (catalyseur contenant une solution de p- nitroaniline) et déterminer l’arrêt Amax de p- nitroaniline.
- Enfin, calculer les concentrations molaires des protonées [I] et des solutions d’indicateur protoné [IH+] en utilisant la valeur Amax de p- nitroaniline et échantillon de solutions. Puis calculer Ho à l’aide de l’équation ci-dessous2
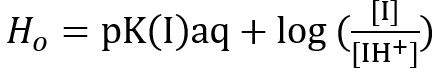 Équation 1
Équation 1
où pK(I)aq est le pKun de la p- nitroaniline indicateur dans l’eau (pKa = 0,99) et [I] et [IH+] sont les concentrations molaires des protonées et protoné solutions indicateur, respectivement.
3. analyse de la biomasse de Jute
-
Analyse de pentosane
Remarque : La biomasse de jute est four séché à 105 ° C pendant 16 h dans le four.- Ajouter 3 g de biomasse de jute four séché dans un 1 L ballon à fond rond et puis ajouter 100 mL de solution de HCl N 3,85 dedans.
- Raccorder le ballon à l’appareil à distiller et commencer l’agitation et le chauffage afin que la solution commence à bouillir.
- Ajouter 250 mL de 3,85 N HCl, goutte à goutte à l’aide d’un entonnoir pour le ballon contenant la solution de HCl et de la biomasse de jute.
- Maintenir un volume constant (100 mL) dans le ballon lors de la distillation en ajoutant 3.85 N HCl solution goutte à goutte.
- Arrêter l’expérience quand 220 mL de distillat est collectée. Diluer le distillat recueilli dans 500 mL d’eau distillée.
- Analyser l’échantillon à l’aide du spectromètre UV-visible et mesurer l’absorbance à 280 nm.
- Déterminer le % de pentosane selon la formule suivante à l’aide de la valeur de l’absorbance et la dilution :
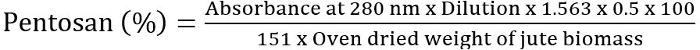 Équation 2
Équation 2
Remarque : Cette méthode est appelée l’Association technique de la méthode Pulp and Paper Industry (TAPPI) pour analyse de pentosane9,19. Répéter l’expérience de deux à trois fois et prendre la valeur moyenne de pentosane %. Si nécessaire, diluer le distillat recueilli pour obtenir l’absorbance à la limite optimale.
-
Analyse de la lignine
Remarque : Retirez l’humidité contenue dans la biomasse de jute avant de l’utiliser pour l’analyse de la lignine. Maintenir la biomasse de jute dans une étuve à 105 ° C pendant 16 h enlever l’humidité.- Ajouter 1 g de biomasse de jute dans un flacon de 50 mL et puis ajouter 15 mL de 72 wt% H2SO4 dans le flacon contenant la biomasse de jute. Incorporer le mélange à l’aide d’une plaque chauffante avec agitateurs installation à 30 ° C pendant 2 h.
- Ajoutez 150 mL d’eau distillée dans un 1 L ballon à fond rond et transférer l’échantillon digéré la biomasse (présent dans le flacon) dans le ballon.
- Laver la fiole avec 195 mL d’eau et transvaser le liquide de lavage dans un 1 L contenant la biomasse digérée ballon à fond rond.
- La solution pour 4 h de reflux et refroidir le ballon à la température ambiante. Attendre 12 h pour la lignine insoluble et les cendres se sédentariser.
- Filtrer la solution à l’aide d’un creuset G2 pour obtenir la lignine insoluble avec de la cendre. Puis laver le solide insoluble avec 150 mL d’eau chaude pour le rendre non acide.
- Sécher le solide (la lignine + ash) à 60 ° C pendant 16 h dans le four et la sécher encore 105 ° C pendant 1 h dans le four.
- Conserver l’échantillon dans le dessiccateur et prendre du poids lorsque l’échantillon est refroidi. La lignine obtenue à ce stade contient des cendres et par conséquent s’appelle non corrigée de la lignine.
- Effectuer une correction de cendres en chauffant l’échantillon obtenu à 650 ° C pendant 5 h, en présence d’air. Déterminer la correction de cendres à l’aide de la formule ci-dessous :
 Équation 3
Équation 3
4. conversion de pentosane du Jute biomasse en sucres
- Ajouter 2 g de biomasse de jute four séché à une haute pression et le réacteur discontinu de haute température (réacteur de Parr de 160 mL). Ajouter 60 mL d’eau et 0,24 g d’acide IL et augmentez la température à 160 ° C.
- Définir la vitesse d’agitation à 200 tr/min tandis que le réacteur est réchauffées jusqu'à 160 ° C. Après avoir atteint la température de 160 ° C, augmenter la vitesse d’agitation à 600 tr/min.
- Continuer la réaction pendant 1 h. Ensuite, diminuer la vitesse d’agitation à 200 tr/min et arrêter le chauffage.
- Permettre le réacteur refroidir à température ambiante. Arrêter l’agitation, ouvrir le réacteur et de séparer le solide du mélange réactionnel. Effectuer l’analyse du mélange réactionnel par CLHP.
Résultats
La quantité exacte de pentosane et lignine extraite de la biomasse dépend du type de biomasse ligno-cellulosique. Types de biomasse ligno-cellulosique prélevés à différents endroits similaires peuvent avoir différente concentration de pentosane et de lignine. La biomasse de jute utilisée dans cette étude contient 20 % de wtpentosane et 14 wt% de lignine.
La figure 1 montre la comparaison de l’activité catalytique des acides minéraux (H2SO4 et HCl) et acide IL pour la conversion de la biomasse de jute en sucres C5. Les réactions ont été effectuées dans l’eau à 160 ° C (1 h) à l’aide de la même quantité d’acide des catalyseurs acides (c'est-à-dire, 1,59 mmol de H+). La non acide et IL acide sont utilisés à une concentration molaire similaire (0.79 mmol). En outre, l’activité catalytique est comparée avec un IL sans aucune acidité de Brønsted (chlorure de 1-butyl-3-méthylimidazolium).
La figure 2 illustre le 1H et 13caractérisation RMN du 13C de l’acide IL utilisé dans cette étude. Les spectres de RMN (1H et 13C) de l’acide IL ne montre aucun pics supplémentaires autres que l’acide IL ; Cela confirme que l’acide IL synthétisé est pur. La figure 3 montre la DRX de la biomasse de jute avant la séparation de la lignine et la DRX de la lignine séparée de la biomasse de jute.
Le tableau 1 présente l’analyse de fonction (Ho) acidité de Hammett des tous les catalyseurs. L’analyse a été réalisée à l’aide de l’indicateur - nitroaniline pqui fournit les informations sur la force de l’acide.

Figure 1 : Conversion de pentosane présente dans la biomasse jute en sucres C5 et le furfural. Condition de réaction : Jute biomasse 2 g, catalyseur 1,59 mmol de H+ (l’émission et acide IL sont utilisés avec même taupe c'est-à-dire, 0.79 mmol), 60 mL d’eau, 160 ° C, 1 h. s’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
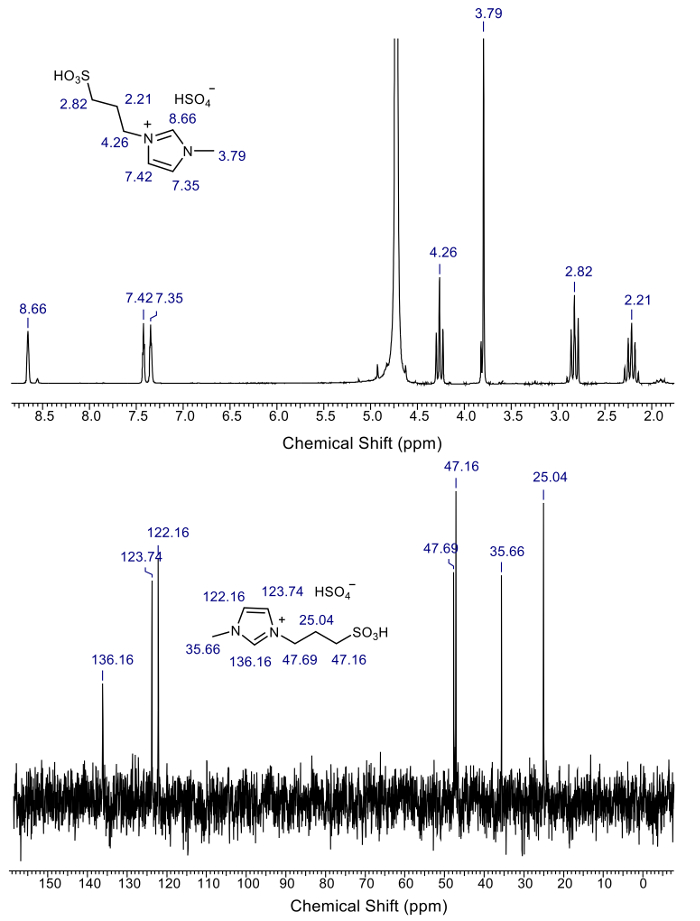
Figure 2 : 1H et 13RMN du 13C des acide IL (sulfate d’hydrogène 1-methyl-3-(3-sulfopropyl)-imidazolium). S’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
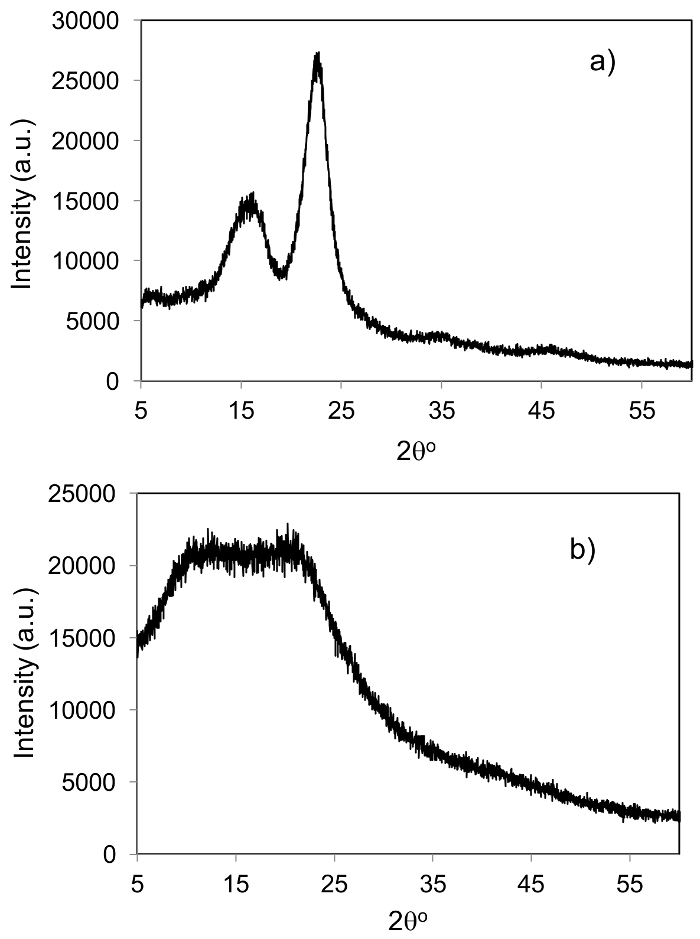
Figure 3 : Diffraction des rayons x. (un) XRD de biomasse de jute et (b) XRD de lignine extraite de la biomasse de jute. S’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
| Catalyseur | Unmax | [I] % | % [IH+] | H0 |
| Vide | 0,991 | 100 | 0 | -- |
| HCl | 0,753 | 76 | 24 | 1.5 |
| H2SO4 | 0,8 | 80,72 | 19.28 | 1,62 |
| IL acide | 0,787 | 79,4 | 20,6 | 1.57 |
| IL non acides | 0,991 | 100 | -- | -- |
Tableau 1 : détermination de la fonction d’acidité de Hammett (Ho) de divers catalyseurs. Dans toutes les mesures, le catalyseur (1,59 mmol H+) est mélangé avec 50 mL de solution - nitroaniline pdans l’eau (10 mg de p- nitroaniline a été ajouté dans 1 L d’eau, le pKa de la p- nitroaniline = 0,99).
Discussion
Le pentosane présente dans la conversion de la biomasse de jute en C5 sucre monomères est démontrée à l’aide de divers catalyseurs acides de Brønsted homogènes tels que H2SO4, HCl et IL acide. En outre, le résultat catalytique de l’acide IL était comparé à l’IL sans acidité (chlorure de 1-butyl-3-méthylimidazolium). Toutes les réactions ont été effectuées dans un autoclave de Parr à 160 ° C dans l’eau. L’utilisation d’acide IL a montré la conversion de pentosane plus élevée par rapport aux acides homogènes utilisés dans ce travail (acides minéraux H2SO4 et HCl). Les résultats indiquent que les acide IL présente rendement en sucre C5 plus élevé (76 %) alors que les acides minéraux montrent des rendements plus faibles (HCl 49 % et H2donc4 57 % de C5 sucre rendement) pour la conversion de pentosane en sucres. Le catalyseur acide minéral et acide IL servent à des quantités semblables acides (1,59 mmol de H+) pour éviter les conséquences de l’acidité de catalyseur dissemblables. La réaction effectuée en utilisant IL non acide et sans catalyseur a montré de très faibles rendements de sucre C5. Cela implique que les acide IL est le meilleur catalyseur pour la conversion de pentosane en monomères de sucre par rapport aux acides minéraux. De plus, l’acidité du IL est essentielle pour cette réaction parce qu’un tel type de non acides IL n’est pas actif dans cette réaction.
L’acide IL peut également être utilisé pour l’analyse de pentosane présente dans la biomasse lignocellulosique parce qu’elle produit un rendement très élevé de monomères de sucre C5 (76 %) et le furfural (12 %). Cette méthode est plus supérieure par rapport à la méthode décrite à la section 3.1 qui utilise 3.85 N HCl et un temps de réaction plus long (environ 24h). Les sucres obtenus à l’aide d’acide IL peuvent être convertis en furanes (furfural et divers dérivés furaniques) ou hydrogénés dans xylitol ou arabitol. Plus important encore, à l’aide de cette méthode il est possible de récupérer les sucres C5 comme produits d’hydrolyse de pentosane. Cependant, récupération de pentosane n’est pas possible de la méthode décrite à la section 3.1 car pentosane se dégrade en furanes dans l’HCl concentré19. L’ILs ont la plus faible pression de vapeur et c’est pourquoi, il y a une possibilité une diminution de l’évaporation IL durant le processus, ce qui rend ce processus plus respectueux de l’environnement sécuritaire. En outre, la corrosivité et la recyclabilité des HCl est le problème majeur avec le HCl prétraitement20,21. En revanche, l’utilisation d’une quantité catalytique d’acide IL dans le processus de conversion de pentosane peut être recyclée.
Les résultats de l’acidité (Ho) Hammett ont montré que l’acide IL a la force plus élevée de l’acide (Ho = 1,57) par rapport à H2SO4 (Ho = 1,62) ; par conséquent, il exécute mieux que le H2catalyseur4 SO. Cependant, l’acide IL a une force acide plus faible par rapport à HCl. Néanmoins, ses performances sont supérieures que le catalyseur de HCl parce que c’est bénéfique pour une meilleure interaction ion-dipôle de polysaccharides présents dans la biomasse lignocellulosique2. En outre, l’acide IL utilisé dans le présent travail est stable à la chaleur sous une température de 300 ° C (analysée à l’aide de l’analyse thermogravimétrique) bien qu’il soit hydrothermique stable sous température de 180 ° C (0,6 g acide IL chauffé dans 60 mL d’eau à 180 ° C pendant 3 h)2 .
En outre, la séparation de la lignine de la biomasse de jute est effectuée à l’aide de la méthode Klason (section 3.2). La biomasse de jute utilisée dans le présent ouvrage contient 14 wt% de lignine. La lignine, séparée de la biomasse de jute est pure et contient beaucoup moins de cendres (< 1 %), qui pourrait également être convertie en monomères aromatiques.
Analyse de la concentration de pentosane et lignine s’effectue à l’aide d’acide minéral (HCl et H2SO4). En outre, IL acide utilisé pour la conversion de pentosane présente dans la biomasse de jute a montré un excellent rendement de sucres C5 (76 %) et le furfural (12 %) ainsi que des oligomères de 5 à 10 % et la réaction a été réalisée dans l’eau à l’aide d’une petite quantité d’acide IL sans aucun externe pression et un prétraitement. En outre, l’acide IL expose plus 90 % conversion de pentosane (la conversion de pentosane a été calculée à l’aide des rendements en sucres C5, furfural et oligomères).
Nous avons développé la méthode de conversion de pentosane présente dans la biomasse jute en sucres C5, mais cette méthode pourrait également être appliquée pour la détermination de la concentration de pentosane présente dans la biomasse de jute. En outre, la concentration de pentosane présente dans autres divers de la biomasse lignocellulosique peut être déterminée à l’aide de la méthode actuelle.
Déclarations de divulgation
Nous n’avons rien à divulguer.
Remerciements
Nous tenons à remercier le ministère de la Science et la technologie (MOST) de Taïwan (104-2628-E-002-008-MY3 105-2218-E-155-007 ; 105-2221-E-002-003-MY3 ; 105-2221-E-002-227-MY3 ; 105-2622-E-155-003-CC2) et le but pour projet universitaire supérieur au National Taiwan Université (105R7706) pour le soutien financier. Nous sommes reconnaissants à la Banque mondiale pour le financement partiel de ce travail à travers un sous-projet de l’enseignement supérieur qualité Enhancement Project (HEQEP), complète proposition #2071. Ce travail a été également partiellement soutenu par AIIM de l’Université de Wollongong (financement d’or).
matériels
| Name | Company | Catalog Number | Comments |
| 1-Methylimidazole | Sigma Aldrich | M50834 | |
| 1,3-Propanesultone | Sigma Aldrich | P50706 | Moisture sensitive |
| p-nitroaniline | Sigma Aldrich | 185310 | |
| Toluene | J. T. Baker | 9460-03 | |
| Sulfuric acid | Honeywell-Fluka | 30743 | Highly corrosive |
| Hydrochloric acid | Honeywell-Fluka | 30719 | Highly corrosive |
| 1-butyl-3-methylimidazolium chloride | Sigma Aldrich | 900856 | Highly hygroscopic |
| D(+)-Xylose | Acros Organics | 141001000 | |
| L(+)-Arabinose | Acros Organics | 104981000 | |
| UV-Spectrometer | JASCO | V-670 | |
| Parr reactor | Parr USA | Seriese 4560 | |
| Parr reactor controller | Parr USA | Seriese 4848 | |
| High pressure liquid chromatography (HPLC) | JASCO | Seriese LC-2000 | |
| Digital hot plate stirrer | Thermo Scientific | SP142020-33Q Cimarec | |
| Oven furnace | Thermal Scientific | FB1400 Thermolyne blast oven furnace |
Références
- Demirbaş, A. Biomass resource facilities and biomass conversion processing for fuels and chemicals. Energy Convers. Manage. 42 (11), 1357-1378 (2001).
- Matsagar, B. M., Dhepe, P. L. Brönsted acidic ionic liquid-catalyzed conversion of hemicellulose into sugars. Catal. Sci. Technol. 5 (1), 531-539 (2015).
- Matsagar, B. M., Dhepe, P. L. Effects of cations, anions and H+ concentration of acidic ionic liquids on the valorization of polysaccharides into furfural. New J Chem. 41 (14), 6137-6144 (2017).
- Food and Agriculture Organization of the United Nations. , Available from: http://faostat3.fao.org/download/Q/QC/E (2014).
- Costa Lopes, A. M., Morais, A. R. C., Łukasik, R. M. Sustainable Catalytic Strategies for C5-Sugars and Biomass Hemicellulose Conversion Towards Furfural Production. Production of Platform Chemicals from Sustainable Resources. , Springer Singapore. 45-80 (2017).
- Matsagar, B. M., Munshi, M. K., Kelkar, A. A., Dhepe, P. L. Conversion of concentrated sugar solutions into 5-hydroxymethyl furfural and furfural using Bronsted acidic ionic liquids. Catal. Sci. Technol. 5 (12), 5086-5090 (2015).
- Gürbüz, E. I., et al. Conversion of Hemicellulose into Furfural Using Solid Acid Catalysts in γ-Valerolactone. Angew Chem Int Ed. 52 (4), 1270-1274 (2013).
- Filiciotto, L., Balu, A. M., Van der Waal, J. C., Luque, R. Catalytic insights into the production of biomass-derived side products methyl levulinate, furfural and humins. Catal Today. 302, 2-15 (2017).
- Matsagar, B. M., et al. Direct Production of Furfural in One-pot Fashion from Raw Biomass Using Brønsted Acidic Ionic Liquids. Sci. Rep. 7 (1), 13508(2017).
- Gschwend, F. J. V., et al. Pretreatment of Lignocellulosic Biomass with Low-cost Ionic Liquids. J Vis Exp. (114), e54246(2016).
- Xu, F., et al. Transforming biomass conversion with ionic liquids: process intensification and the development of a high-gravity, one-pot process for the production of cellulosic ethanol. Energy Environ. Sci. 9 (3), 1042-1049 (2016).
- Sun, J., et al. One-pot integrated biofuel production using low-cost biocompatible protic ionic liquids. Green Chem. 19 (13), 3152-3163 (2017).
- Nguyen, C. V., et al. Combined treatments for producing 5-hydroxymethylfurfural (HMF) from lignocellulosic biomass. Catal Today. 278 (Part 2), 344-349 (2016).
- Yan, N., Yuan, Y., Dykeman, R., Kou, Y., Dyson, P. J. Hydrodeoxygenation of Lignin-Derived Phenols into Alkanes by Using Nanoparticle Catalysts Combined with Brønsted Acidic Ionic Liquids. Angew Chem Int Ed. 49 (32), 5549-5553 (2010).
- Weerachanchai, P., Lee, J. -M. Recyclability of an ionic liquid for biomass pretreatment. Bioresour. Technol. 169 (Supplement C), 336-343 (2014).
- Shill, K., et al. Ionic liquid pretreatment of cellulosic biomass: Enzymatic hydrolysis and ionic liquid recycle. Biotechnol Bioeng. 108 (3), 511-520 (2011).
- Tadesse, H., Luque, R. Advances on biomass pretreatment using ionic liquids: An overview. Energy Environ. Sci. 4 (10), 3913-3929 (2011).
- Agirrezabal-Telleria, I., Gandarias, I., Arias, P. L. Production of furfural from pentosan-rich biomass: Analysis of process parameters during simultaneous furfural stripping. Bioresour. Technol. 143 (Supplement C), 258-264 (2013).
- Yingying, L., et al. An Improved Method for Determination of Pentosans in Pulps using Dual-Wavelength Spectroscopy. BioResources. 11 (3), 6801-6807 (2016).
- Kumar, A. K., Sharma, S. Recent updates on different methods of pretreatment of lignocellulosic feedstocks: a review. Bioresour. Bioprocess. 4 (1), 7(2017).
- Kumar, P., Barrett, D. M., Delwiche, M. J., Stroeve, P. Methods for Pretreatment of Lignocellulosic Biomass for Efficient Hydrolysis and Biofuel Production. Ind. Eng. Chem. Res. 48 (8), 3713-3729 (2009).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon