Method Article
Preparación y cría de insectos axénicos con plántulas cultivadas en tejidos para estudios de interacción entre la microbiota huésped-intestino del escarabajo de la hoja
En este artículo
Resumen
Para obtener un insecto axénico, se esteriliza la superficie de su huevo y la larva eclosionada se cría posteriormente con hojas axiénicas. Este método proporciona una forma eficiente para la preparación de insectos axénicos sin administrar antibióticos o desarrollar una dieta artificial, que también se puede aplicar a otros insectos que comen hojas.
Resumen
Los intestinos de los insectos son colonizados por diversas bacterias que pueden afectar profundamente los rasgos fisiológicos del huésped. La introducción de una cepa bacteriana particular en un insecto axénico es un método poderoso para verificar la función microbiana intestinal y dilucidar los mecanismos subyacentes a las interacciones entre microbios intestinales y huéspedes. La administración de antibióticos o la esterilización de las superficies de los huevos son dos métodos comúnmente utilizados para eliminar las bacterias intestinales de los insectos. Sin embargo, además de los posibles efectos adversos de los antibióticos en los insectos, estudios previos indicaron que la alimentación con antibióticos no podía eliminar las bacterias intestinales. Por lo tanto, las dietas artificiales libres de gérmenes generalmente se emplean para mantener los insectos axénicos, que es un proceso tedioso y laborioso que no puede parecerse completamente a los componentes nutricionales de los alimentos naturales. Aquí se describe un protocolo eficiente y simple para preparar y mantener larvas axénicas de un escarabajo de la hoja (Plagiodera versicolora). Específicamente, las superficies de los huevos de escarabajo fueron esterilizadas, después de lo cual se utilizaron hojas de álamo libres de gérmenes para criar larvas axénicas. El estado axénico de los insectos se confirmó aún más a través de ensayos dependientes del cultivo e independientes del cultivo. Colectivamente, al combinar la desinfección de huevos y el cultivo libre de gérmenes, se desarrolló un método eficiente y conveniente para obtener P. versicolora axénico, proporcionando una herramienta fácilmente transferible para otros insectos que comen hojas.
Introducción
Similar a los mamíferos, el tracto digestivo de los insectos es una cavidad para la digestión y absorción de los alimentos. La mayoría de los insectos albergan diversas bacterias comensales que prosperan en sus intestinos y viven de la nutrición suministrada por los huéspedes1. La comunidad comensal intestinal tiene un profundo impacto en múltiples procesos fisiológicos en insectos, incluyendo la digestión y desintoxicación de alimentos 2,3,4, nutrición y desarrollo 5,6,7, defensa contra patógenos y parásitos 8,9,10,11, comunicación química 12,13 y comportamientos14 ,15. Curiosamente, parte de la microbiota intestinal puede ser facultativamente patógena o ser manipulada por patógenos invasores para agravar la infección, lo que indica que las bacterias intestinales pueden ser dañinas en algunos casos 16,17,18. Las bacterias intestinales también pueden servir como un recurso microbiano para aplicaciones biotécnicas y manejo de plagas. Por ejemplo, se utilizaron bacterias que digieren la lignocelulosa de insectos fitófagos y xilófagos para digerir células vegetales para desarrollar biocombustibles19. La dispersión de simbiontes intestinales modificados que expresan moléculas bioactivas es una táctica novedosa y prometedora para controlar las plagas agrícolas y forestales y los mosquitos transmisores de enfermedades infecciosas 19,20,21, que también se puede utilizar para mejorar la aptitud de los insectos beneficiosos22. Por lo tanto, ilustrar cómo se comporta una bacteria intestinal in vivo se considera una prioridad para aprovechar al máximo su función y explotarla aún más para diversas aplicaciones.
Los animales pueden albergar de 1 a >1000 especies microbianas simbióticas en el intestino1. Como resultado, es difícil verificar con precisión cómo funcionan los taxones bacterianos individuales o su ensamblaje dentro de un animal, y si el huésped o sus socios microbianos impulsan una función específica. Por lo tanto, la preparación de larvas axénicas para obtener insectos gnotobióticos por colonización mono o multiespecie es necesaria para investigar la función bacteriana y la interacción con los insectos23. En la actualidad, la administración de cócteles antibióticos y la esterilización de la superficie de los huevos de insectos son métodos comunes para eliminar las bacterias intestinales 14,24,25,26. Sin embargo, las dietas antibióticas no pueden eliminar las bacterias intestinales por completo y tienen un efecto negativo en la fisiología del insecto huésped27,28. En consecuencia, el uso de insectos tratados con antibióticos puede oscurecer las verdaderas capacidades de algunas bacterias intestinales. Afortunadamente, la esterilización superficial de los huevos puede negar este problema23,29, que tiene efectos nulos o insignificantes en los insectos experimentales. Además, las dietas artificiales no pueden parecerse completamente a los alimentos naturales para insectos, y desarrollar una dieta artificial es un proceso costoso y que consume mano de obra30,31.
El escarabajo de la hoja de sauce, Plagiodera versicolora (Laicharting) (Coleoptera: Chrysomelidae), es una plaga herbácea generalizada que se alimenta principalmente de árboles salicáceos, como sauces (Salix) y álamos (Populus L.) 32,33. Aquí, el escarabajo de la hoja de sauce se utilizó como un insecto representativo que come hojas para desarrollar un protocolo para preparar y criar un insecto libre de gérmenes. Explotamos el cultivo de tejido vegetal para obtener hojas de álamo libres de gérmenes para criar larvas axénicas de P. versicolora a partir de huevos esterilizados. El estado axénico de las larvas de P. versicolora se verificó mediante ensayos dependientes del cultivo e independientes del cultivo. Este protocolo puede mantener insectos axénicos que imitan mejor la condición silvestre que la cría de insectos con una dieta artificial. Más importante aún, este método es conveniente a un costo muy bajo, lo que aumenta la viabilidad de obtener insectos axénicos para futuros estudios de interacción insecto-microbiota intestinal, especialmente para insectos no modelo sin dietas artificiales bien desarrolladas.
Protocolo
1. Cría de insectos
- Mantener la población de P. versicolora en una cámara de crecimiento en la condición de 27 °C y 70 ± 5% de humedad relativa con un fotoperíodo de 16 h de luz/8 h de oscuridad. Colóquelos en cajas de plástico perforadas con papel absorbente húmedo alicatado y aliméntelos con ramas de álamo frescas. Rocíe agua limpia sobre el papel absorbente para mantener la humedad y cambie las ramas cada dos días.
- Aislar a los adultos para la oviposición después de la pupación. Aliméntelos con hojas tiernas para obtener más huevos.
- Recoger los huevos recién puestos (en un plazo de 24 h). Coloque los huevos sobre papel absorbente húmedo durante 60 h para preparar las larvas axiénicas.
NOTA: Los huevos recién puestos eclosionarán después de ~ 72 h. El mejor momento para esterilizar las superficies de los huevos es el día antes de la eclosión; de lo contrario, el número de huevos eclosionados con éxito disminuirá.
2. Cultivo de álamos sin gérmenes
- Preparar soluciones madre de Murashige y Skoog (MS) medio y 1 mg/ml de ácido acético α-naftaleno (NAA) (consulte la Tabla de Materiales).
- En una campana de bioseguridad, agregue 50 μL de solución madre de NAA de 1 mg / ml a 500 ml de medio de EM, agite para mezclar bien y vierta ~ 50 ml por recipiente de cultivo de tejidos y espere la solidificación.
- Prepare bisturíes, lámpara de alcohol y fórceps; esterilizar los bisturíes y fórceps en la llama de la lámpara de alcohol en la campana de bioseguridad.
- Corte los segmentos de tallo de 3-4 cm con brotes apicales o brotes laterales de plántulas de álamo a ~ 1 mes de crecimiento (plántulas cultivadas con tejido libre de gérmenes) e insértelos en el medio de cultivo, uno o dos segmentos de tallo por contenedor.
- Incubar estos segmentos del tallo en una cámara de crecimiento a 25 °C y 50 ± 10 cd de intensidad de luz con un fotoperíodo de 16 h de luz/8 h de oscuridad durante aproximadamente 30 días. Use las hojas libres de gérmenes para alimentar a las larvas axénicas.
3. Esterilización de la superficie del huevo y cría de larvas axénicas
- Placas de Petri en autoclave, pinceles, papel de filtro, agua destilada y una placa de Petri que contiene medio de agar LB (Luria-Bertani).
- Coloque las hojas con huevos adherentes en una placa de Petri, retire cuidadosamente los huevos de las hojas con fórceps y transfiéralos a otra placa de Petri.
NOTA: Este paso debe realizarse con mucho cuidado porque los huevos son adherentes a las hojas. - Lave estos huevos con etanol al 75% durante 8 minutos y repita el lavado cuatro veces con agua estéril.
- Transfiera los huevos al medio de agar LB para preservar la humedad para la eclosión.
NOTA: El uso de medio de agar LB puede ayudar a verificar si el huevo desinfectado está libre de gérmenes. - Coloque la placa de Petri en una cámara de crecimiento y espere a que los huevos eclosionen dentro de las 24 h.
- En una campana de bioseguridad, azulee tres trozos de papel de filtro húmedo en una placa de Petri, coloque hojas de álamo libres de gérmenes en el papel, recoja las larvas y colóquelas en las hojas, selle la placa de Petri con parafilm y cúbralas en una cámara de crecimiento a 27 ° C y 70 ± 5% de humedad relativa con un fotoperíodo de 16 h de luz / 8 h de oscuridad.
NOTA: Las hojas cultivadas con tejido son delicadas y pueden perder agua rápidamente. Por lo tanto, es necesario usar papel de filtro húmedo al transferir las hojas a la placa de Petri. - Cambie las hojas cada dos días.
- Para los grupos criados convencionalmente, transfiera los huevos de las hojas a una placa de Petri que contenga papel de filtro húmedo y alimente a estas larvas con hojas de álamo libres de gérmenes.
4. Verificación de larvas axénicas con ensayos dependientes del cultivo
- Seleccione al azar tres larvas de1º,2º y3º instar de los grupos libres de gérmenes y criados convencionalmente.
- Diseccionar las larvas de3º instar con tijeras y fórceps estériles bajo un estereomicroscopio y recoger sus tripas en tubos de microcentrífuga. Recolectar larvasintactas de 1º y2º instar en tubos.
NOTA: Recolecte larvas enteras de1º y2º instar, ya que son demasiado pequeñas para diseccionar, y mantenga sus intestinos intactos. - Agregue 100 μL de solución salina tamponada con fosfato y tres bolas de acero a los tubos de 1,5 ml y muela los tejidos en homogeneizados utilizando un homogeneizador de perlas.
- Agregue 100 μL del homogeneizado al medio y placa de agar LB usando una varilla de vidrio estéril.
- Coloque las placas a 37 °C durante 24 h y observe las colonias bacterianas.
5. Verificación de individuos axénicos con ensayos independientes de la cultura
- Extraer el ADN total de los tejidos (obtenido en la sección 4) mediante un kit de extracción de ADN.
- Mida la concentración de ADN utilizando un espectrofotómetro a 260 nm.
- Amplificar el gen bacteriano 16S rRNA utilizando cebadores universales de ARNr 16S con PCR. Configure el sistema de reacción con 18 μL de mezcla maestra de PCR 1.1x (consulte la Tabla de Materiales), 0.5 μL de imprimación 27F (5'-ACGGATACCTTGTTACGAC-3'), 0.5 μL de imprimación 1495R (5'-ACGGATACCTTGTTACGAC-3') y 100 ng de PLANTILLA de ADN. Establecer las condiciones de PCR a 95 °C durante 3 min; 28 ciclos de 95 °C durante 30 s, 55 °C durante 1 min y 72 °C durante 1 min; seguido de 72 °C durante 10 min. Conservar los productos de PCR a 4 °C hasta un análisis adicional.
- Mezcle los productos de PCR con colorante de ácido nucleico y analícelos mediante electroforesis en un gel de agarosa al 1% en 1x tampón TAE. Utilice 10 μL de un marcador de ADN como referencia.
- Observe el gel con un transiluminador UV y busque el fragmento objetivo alrededor de 1.500 pb.
Resultados
Las etapas de la vida de P. versicolora se muestran en la Figura 1. El macho adulto es más pequeño que la hembra adulta (Figura 1A). En el campo, el escarabajo agrupa sus huevos en una hoja; aquí, cuatro huevos se separaron de una hoja (Figura 1B). Los segmentos del tallo del álamo y las plántulas utilizadas para la cría de insectos axénicos se muestran en la Figura 2. El intestino de una larva de3ª instar se muestra en la Figura 3, y los segmentos intestinales están marcados con corchetes blancos.
Aunque no se observaron colonias bacterianas en ningún grupo libre de gérmenes, se observaron en todos los grupos criados convencionalmente (Figura 4), lo que indica que las larvas de huevos esterilizados que fueron alimentados con hojas de álamo cultivadas con tejidos no contienen bacterias. Las bandas de PCR de ~1.500 pb aparecieron en todos los grupos criados convencionalmente. En contraste, no se observó ninguna banda en los grupos libres de gérmenes o el control negativo (Figura 5), lo que implica que no existían bacterias intestinales en las larvas axénicas. No hubo diferencias en el tiempo de desarrollo larval, la tasa de supervivencia o la apariencia entre las larvas de P. versicolora libres de gérmenes y criadas convencionalmente. Sin embargo, la masa corporal de las larvas libres de gérmenes fue ligeramente mayor que la de las larvas criadas convencionalmente enel día 5 , aunque las masas se volverán similares antes de la pupación16. Estos resultados confirmaron la viabilidad de este protocolo para preparar y criar larvas axénicas.

Figura 1: Etapas de la vida del escarabajo de la hoja de sauce, Plagiodera versicolora. (A) Adultos hembras y machos; B) huevos; (C)1ª larva instar; (D)2ª larva instar; (E)3ª larva instar; y (F) pupa. Barras de escala = 1 mm. Haga clic aquí para ver una versión más grande de esta figura.

Figura 2: Segmentos de tallo de álamo y plántulas. (A) Segmentos de tallo con brotes apicales; (B) los segmentos del tallo crecieron raíces después de 10 días; (C) una plántula de un mes de edad. Barras de escala = 1 cm. Haga clic aquí para ver una versión más grande de esta figura.

Figura 3: El intestino de una larva de tercera estrella. El intestino anterior, el intestino medio y el intestino posterior están etiquetados con corchetes. Barra de escala = 1 mm. Haga clic aquí para ver una versión más grande de esta figura.

Figura 4: Confirmación de la eficacia de la eliminación de bacterias intestinales mediante el cultivo de homogeneizados intestinales o de insectos enteros en placas de agar LB. No se observaron bacterias en larvas alimentadas con hojas de álamo libres de gérmenes, mientras que se observaron bacterias en grupos criados convencionalmente. Para el ensayo se utilizaron larvas de1ª,2ª y 3ª instar. Tres larvas fueron seleccionadas al azar en cada grupo. Abreviaturas: GF = larvas libres de gérmenes; CR = larvas criadas convencionalmente. Haga clic aquí para ver una versión más grande de esta figura.
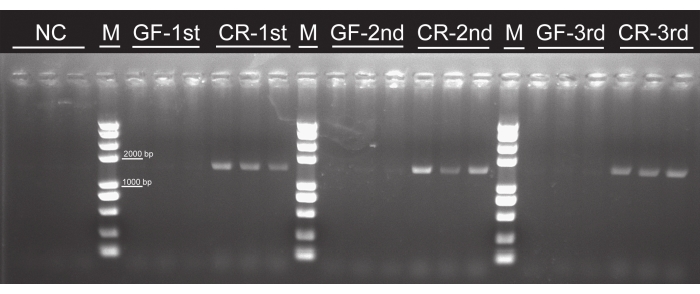
Figura 5: Confirmación de la eficacia de la eliminación de bacterias intestinales mediante ensayo de PCR utilizando cebadores universales del gen 16S rRNA. La banda objetivo del gen 16S rRNA es ~ 1,500 bp. Se utilizaron larvas de 1st, 2nd y 3rd instar para el ensayo. No se observó banda objetivo en los grupos de GF. Abreviaturas: NC = control negativo; GF = libre de gérmenes; CR = criado convencionalmente. Haga clic aquí para ver una versión más grande de esta figura.
Discusión
La preparación de larvas libres de gérmenes y la obtención de larvas gnotobióticas mediante la reintroducción de cepas bacterianas específicas son métodos poderosos para dilucidar los mecanismos subyacentes a las interacciones huésped-microbio. Las larvas recién nacidas obtienen la microbiota intestinal de dos maneras principales: transmisión vertical de la madre a la descendencia o adquisición horizontal de los hermanos y el medio ambiente34. El primero puede cumplirse mediante la transferencia parental a la descendencia a través de la contaminación de la superficie del huevo35. Por lo tanto, es altamente factible obtener larvas axénicasesterilizando las superficies de huevos de insectos 27,28,29. La administración de un cóctel de varios antibióticos es otra forma de desarrollar insectos axénicos pero tiene varias desventajas28. En contraste, la esterilización de la superficie del huevo seguida de una dieta axénica es mejor para el desarrollo de insectos axénicos 23,28,29.
Los huevos de la mayoría de los escarabajos que consumen hojas son visibles, fáciles de adquirir y fáciles de desinfectar. Esta es la razón principal por la que se utilizó un reactivo simple (75% de etanol) y un tiempo más corto (8 min) para la desinfección en comparación con estudios similares (por ejemplo, 40 min de desinfección de huevos para la chinche Apestosa stali con 75% de etanol y formaldehído para obtener insectos axénicos; 6 min de esterilización de la superficie del huevo de Drosophila con 1% de cloro activo y 75% de etanol; y 10 min de esterilización de la superficie del huevo del gorgojo rojo de la palma Rhynchophorus ferrugineus con 10% de hipoclorito de sodio solución)23,29,36. Para las especies de insectos con huevos pequeños, el uso de desinfectantes y la duración de la esterilización deben optimizarse, ya que el tratamiento puede afectar significativamente los resultados.
En algunos casos, se emplean dietas artificiales libres de gérmenes para la cría de insectos axénicos después de la esterilización de la superficie del huevo29,37. Sin embargo, desarrollar una dieta artificial adecuada para insectos es un proceso tedioso y que consume mano de obra. Los nutrientes en la dieta influyen ampliamente en la fisiología de los insectos (por ejemplo, el tiempo de desarrollo, la inmunidad) y la microbiota intestinal 6,35. Por lo tanto, una dieta artificial calificada para un insecto debe contener una composición nutricional similar a la de los alimentos naturales, lo cual es difícil de lograr, especialmente para los insectos fitófagos. En este protocolo, alimentamos a los insectos con plantas huésped axénicas, lo que supera las deficiencias de una dieta artificial. Es importante destacar que, al igual que con la planta de álamo utilizada aquí, tampoco es difícil obtener plántulas cultivadas en tejidos de muchos cultivos económicamente importantes como el tabaco, la papa, el tomate, el trigo y el arroz mediante la esterilización de la superficie de la semilla o la desinfección de la sección del tallo38. Cabe destacar que los endófitos en las plantas pueden existir en plántulas cultivadas en tejidos39 y pueden eliminarse mediante la tecnología de cultivo de meristemo en punta de brote40. En conclusión, este protocolo proporciona un nuevo método para mantener insectos libres de gérmenes, que es una herramienta útil para facilitar los estudios de interacción insecto-bacteria intestinal.
Divulgaciones
Los autores no tienen conflictos de intereses que revelar.
Agradecimientos
Este trabajo fue financiado por la Fundación Nacional de Ciencias Naturales de China (31971663) y el Programa de Patrocinio de Jóvenes Científicos de Élite por CAST (2020QNRC001).
Materiales
| Name | Company | Catalog Number | Comments |
| 0.22 µm syringe filters | Millipore | SLGP033RB | |
| 1 mg/mL NAA stock solution | a. Prepare 0.1 M NaOH solution (dissolve 0.8 g NaOH in 200 mL of distilled water). b. Add 0.2 g NAA in a 250 mL beaker, add little 0.1 M NaOH solution until NAA dissolved, and adjust the final volume to 200 mL with distilled water. c. Filter the solution to remove bacteria with a 0.22 µm syringe filter and a 50 mL sterile syringe, subpackage the solution in 1.5 mL centrifuge tubes and restore at -20 °C. | ||
| 1.5 mL microcentrifuge tubes | Sangon Biotech | F600620 | |
| 10x PBS stock solution | Biosharp Life Sciences | BL302A | |
| 2 M KOH solution | Dissolve 22.44 g KOH (molecular weight: 56.1) in 200 mL of distilled water and autoclave it for 20 min at 121 °C. | ||
| 250 mL and 2,000 mL beakers | Shubo | sb16455 | |
| 50 mL sterile syringes | Jinta | JT0125789 | |
| 500 mL measuring cylinder | Shubo | sb1601 | |
| 50x TAE stock solution | a. Dissolve 242 g Tris and 18.612 g EDTA in 700 mL of distilled water. b. Adjust pH to 7.8 with about 57.1 mL of acetic acid. c. Adjust the final volume to 1,000 mL. d. The stock solution was diluted to 1x TAE buffer when used. | ||
| 75% ethanol | Xingheda trade | ||
| α-naphthalene acetic acid (NAA) | Solarbio Life Sciences | 86-87-3 | |
| Absorbing paper | 22.3 cm x 15.3 cm x 9 cm | ||
| Acetic acid | Sinopharm Chemical Reagent Co. Ltd | ||
| Agar | Coolaber | 9002-18-0 | |
| Agarose | Biowest | 111860 | |
| Autoclave | Panasonic | MLS-3781L-PC | |
| Bead-beating homogenizer | Jing Xin | XM-GTL64 | |
| DNA extraction kit | MP Biomedicals | 116560200 | |
| EDTA | Saiguo Biotech | 1340 | |
| Filter paper | Jiaojie | 70 mm diameter | |
| Gel electrophoresis unit | Bio-rad | 164-5052 | |
| Gel Signal Green nucleic acid dye | TsingKe | TSJ003 | |
| Germ-free poplar seedlings | Shan Xin poplar from Ludong University in Shandong Province | ||
| Golden Star Super PCR Master Mix (1.1×) | TsingKe | TSE101 | |
| Growth chamber | Ruihua | HP400GS-C | |
| LB agar medium | a. Dissolve 5 g tryptone, 5 g NaCl, 2.5 g yeast extract in 300 mL of distilled water. b. Adjust the final volume to 500 mL, transfer the solution to a 1,000 mL conical flask, and add 7.5 g agar. c. Autoclave the medium for 20 min at 121 °C. | ||
| Mini centrifuge | DRAGONLAB | D1008 | |
| MS basic medium | Coolaber | PM1121-50L | M0245 |
| MS solid medium for germ-free poplar seedling culture | a. Dissolve 4.43 g MS basic medium powder and 30 g sucrose in 800 mL of distilled water. b. Adjust the pH to about 5.8 with 2 M KOH by a pH meter. c. Adjust the final volume to 1,000 mL, separate into two parts, transfer into two 1,000 mL conical flasks, and add 2.6 g agar per 500 mL. d. Autoclave for 20 min at 121 °C. | ||
| NanoDrop 1000 spectrophotometer | Thermo Fisher Scientific | ||
| Paintbrush | 1 cm width, used to collect the eggs | ||
| Parafilm | Bemis | PM-996 | |
| PCR Thermal Cyclers | Eppendorf | 6331000076 | |
| Petri dishes | Supin | 90 mm diameter | |
| pH meter | METTLER TOLEDO | FE20 | |
| Pipettes 0.2-2 µL | Gilson | ECS000699 | |
| Pipettes 100-1,000 µL | Eppendorf | 3120000267 | |
| Pipettes 20-200 µL | Eppendorf | 3120000259 | |
| Pipettes 2-20 µL | Eppendorf | 3120000232 | |
| Plant tissue culture container | Chembase | ZP21 | 240 mL |
| Plastic box | 2.35 L | ||
| Potassium hydroxide (KOH) | Sinopharm Chemical Reagent Co. Ltd | ||
| Primers for amplifying the bacterial 16S rRNA gene | Sangon Biotech | 27-F: 5’-ACGGATACCTTGTTACGAC-3’, 1492R: 5’-ACGGATACCTTGTTACGAC-3’ | |
| Sodium chloride (NaCl) | Sinopharm Chemical Reagent Co. Ltd | ||
| Sodium hydroxide (NaOH) | Sinopharm Chemical Reagent Co. Ltd | ||
| Steel balls | 0.25 mm | used to grind tissues | |
| Stereomicroscope | OLYMPUS | SZ61 | |
| Sucrose | Sinopharm Chemical Reagent Co. Ltd | ||
| Trans2K plus II DNA marker | Transgene Biotech | BM121-01 | |
| Tris base | Biosharp Life Sciences | 1115 | |
| Tryptone | Thermo Fisher Scientific | LP0037 | |
| UV transilluminator | Monad Biotech | QuickGel 6100 | |
| Vortexer | Scilogex | MX-S | |
| Willow branches | Sha Lake Park, Wuhan, China | ||
| Willow leaf beetle | Huazhong Agricultural University, Wuhan, China | ||
| Yeast extract | Thermo Fisher Scientific | LP0021 |
Referencias
- Moran, N. A., Ochman, H., Hammer, T. J. Evolutionary and ecological consequences of gut microbial communities. Annual Review of Ecology, Evolution, and Systematics. 50 (1), 451-475 (2019).
- Warnecke, F., et al. Metagenomic and functional analysis of hindgut microbiota of a wood-feeding higher termite. Nature. 450 (7169), 560-565 (2007).
- Tokuda, G., et al. Fiber-associated spirochetes are major agents of hemicellulose degradation in the hindgut of wood-feeding higher termites. Proceedings of the National Academy of Sciences of the United States of America. 115 (51), 11996-12004 (2018).
- Wang, G. H., et al. Changes in microbiome confer multigenerational host resistance after sub-toxic pesticide exposure. Cell Host & Microbe. 27 (2), 213-224 (2020).
- Shin, S. C., et al. Drosophila microbiome modulates host developmental and metabolic homeostasis via insulin signaling. Science. 334 (6056), 670-674 (2011).
- Storelli, G., et al. Lactobacillus plantarum promotes Drosophila systemic growth by modulating hormonal signals through TOR-dependent nutrient sensing. Cell Metabolism. 14 (3), 403-414 (2011).
- Salem, H., et al. Vitamin supplementation by gut symbionts ensures metabolic homeostasis in an insect host. Proceedings. Biological Sciences. 281 (1796), 20141838 (2014).
- Koch, H., Schmid-Hempel, P. Socially transmitted gut microbiota protect bumble bees against an intestinal parasite. Proceedings of the National Academy of Sciences of the United States of America. 108 (48), 19288-19292 (2011).
- Cirimotich, C. M., et al. Natural microbe-mediated refractoriness to Plasmodium infection in Anopheles gambiae. Science. 332 (6031), 855-858 (2011).
- Kaltenpoth, M., Gottler, W., Herzner, G., Strohm, E. Symbiotic bacteria protect wasp larvae from fungal infestation. Current Biology. 15 (5), 475-479 (2005).
- Yuan, C., Xing, L., Wang, M., Hu, Z., Zou, Z. Microbiota modulates gut immunity and promotes baculovirus infection in Helicoverpa armigera. Insect Science. , (2021).
- Dillon, R. J., Vennard, C. T., Charnley, A. K. Pheromones - Exploitation of gut bacteria in the locust. Nature. 403 (6772), 851 (2000).
- Xu, L. T., Lou, Q. Z., Cheng, C. H., Lu, M., Sun, J. H. Gut-associated bacteria of Dendroctonus valens and their involvement in verbenone production. Microbial Ecology. 70 (4), 1012-1023 (2015).
- Schretter, C. E., et al. A gut microbial factor modulates locomotor behaviour in Drosophila. Nature. 563 (7731), 402-406 (2018).
- Jia, Y., et al. Gut microbiome modulates Drosophila aggression through octopamine signaling. Nature Communications. 12 (1), 2698 (2021).
- Ma, M., et al. Metabolic and immunological effects of gut microbiota in leaf beetles at the local and systemic levels. Integrative Zoology. 16 (3), 313-323 (2021).
- Xu, L., et al. Synergistic action of the gut microbiota in environmental RNA interference in a leaf beetle. Microbiome. 9 (1), 98 (2021).
- Xu, L., et al. Gut microbiota in an invasive bark beetle infected by a pathogenic fungus accelerates beetle mortality. Journal of Pest Science. 92, 343-351 (2019).
- Berasategui, A., Shukla, S., Salem, H., Kaltenpoth, M. Potential applications of insect symbionts in biotechnology. Applied Microbiology and Biotechnology. 100 (4), 1567-1577 (2016).
- Tikhe, C. V., Martin, T. M., Howells, A., Delatte, J., Husseneder, C. Assessment of genetically engineered Trabulsiella odontotermitis as a 'Trojan Horse' for paratransgenesis in termites. BMC Microbiology. 16 (1), 202 (2016).
- Wang, S., et al. Fighting malaria with engineered symbiotic bacteria from vector mosquitoes. Proceedings of the National Academy of Sciences of the United States of America. 109 (31), 12734-12739 (2012).
- Leonard, S. P., et al. Engineered symbionts activate honey bee immunity and limit pathogens. Science. 367 (6477), 573-576 (2020).
- Kietz, C., Pollari, V., Meinander, A. Generating germ-free Drosophila to study gut-microbe interactions: protocol to rear Drosophila under axenic conditions. Current Protocols in Toxicology. 77 (1), 52 (2018).
- Brummel, T., Ching, A., Seroude, L., Simon, A. F., Benzer, S. Drosophila lifespan enhancement by exogenous bacteria. Proceedings of the National Academy of Sciences of the United States of America. 101 (35), 12974-12979 (2004).
- Correa, M. A., Matusovsky, B., Brackney, D. E., Steven, B. Generation of axenic Aedes aegypti demonstrate live bacteria are not required for mosquito development. Nature Communications. 9 (1), 4464 (2018).
- Romoli, O., Schonbeck, J. C., Hapfelmeier, S., Gendrin, M. Production of germ-free mosquitoes via transient colonisation allows stage-specific investigation of host-microbiota interactions. Nature Communications. 12 (1), 942 (2021).
- Berasategui, A., et al. Gut microbiota of the pine weevil degrades conifer diterpenes and increases insect fitness. Molecular Ecology. 26 (15), 4099-4110 (2017).
- Lin, X. L., Kang, Z. W., Pan, Q. J., Liu, T. X. Evaluation of five antibiotics on larval gut bacterial diversity of Plutella xylostella (Lepidoptera: Plutellidae). Insect Science. 22 (5), 619-628 (2015).
- Muhammad, A., Habineza, P., Hou, Y., Shi, Z. Preparation of red palm weevil Rhynchophorus Ferrugineus (Olivier) (Coleoptera: Dryophthoridae) germ-free larvae for host-gut microbes interaction studies. Bio-protocol. 9 (24), 3456 (2019).
- Gelman, D. B., Bell, R. A., Liska, L. J., Hu, J. S. Artificial diets for rearing the Colorado potato beetle, Leptinotarsa decemlineata. Journal of Insect Science. 1, 7 (2001).
- Bengtson, D. A. A comprehensive program for the evaluation of artificial diets. Journal of the World Aquaculture Society. 24 (2), 285-293 (2007).
- Utsumi, S., Ando, Y., Ohgushi, T. Evolution of feeding preference in a leaf beetle: the importance of phenotypic plasticity of a host plant. Ecology Letters. 12 (9), 920-929 (2009).
- Ishihara, M., Ohgushi, T. Reproductive inactivity and prolonged developmental time induced by seasonal decline in host plant quality in the willow leaf beetle Plagiodera versicolora (Coleoptera: Chrysomelidae). Environmental Entomology. 35 (2), 524-530 (2006).
- Bright, M., Bulgheresi, S. A complex journey: transmission of microbial symbionts. Nature Reviews: Microbiology. 8 (3), 218-230 (2010).
- Hassan, B., Siddiqui, J. A., Xu, Y. Vertically transmitted gut bacteria and nutrition influence the immunity and fitness of Bactrocera dorsalis larvae. Frontiers in Microbiology. 11, 596352 (2020).
- Hosokawa, T., et al. Obligate bacterial mutualists evolving from environmental bacteria in natural insect populations. Nature Microbiology. 1, 15011 (2016).
- Habineza, P., et al. The promoting effect of gut microbiota on growth and development of red palm weevil, Rhynchophorus ferrugineus (Olivier) (Coleoptera: Dryophthoridae) by modulating its nutritional metabolism. Frontiers in Microbiology. 10, 1212 (2019).
- Meilan, R., Ma, C. Poplar (Populus spp.). Methods in Molecular Biology. 344, 143-151 (2006).
- Wani, Z. A., Ashraf, N., Mohiuddin, T., Riyaz-Ul-Hassan, S. Plant-endophyte symbiosis, an ecological perspective. Applied Microbiology and Biotechnology. 99 (7), 2955-2965 (2015).
- Grout, B. W. Meristem-tip culture. Methods in Molecular Biology. 6, 81-91 (1990).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados