Method Article
El modelo de conejo de ateroesclerosis acelerada: una perspectiva metodológica de la lesión de globo de la arteria ilíaca
* Estos autores han contribuido por igual
En este artículo
Resumen
Modelos animales de aterosclerosis son esenciales para comprender el mecanismo e investigar nuevos enfoques para prevenir el desarrollo de la placa o ruptura, una causa principal de muerte en el mundo industrializado. Este protocolo utiliza una combinación de lesión de globo y dieta rica en colesterol para inducir a las placas ateroscleróticas en arteria ilíaca de conejo.
Resumen
Síndrome coronario agudo resultante de la obstrucción coronaria después de la ruptura y desarrollo de la placa aterosclerótica es la causa principal de muerte en el mundo industrializado. Conejos Nueva Zelanda blanco (NZB) son ampliamente utilizados como modelo animal para el estudio de la aterosclerosis. Desarrollan lesiones espontáneas cuando alimentados con la dieta aterogénico; sin embargo, esto requiere mucho tiempo de 4 a 8 meses. Para mejorar y acelerar la aterogénesis, se emplea a menudo una combinación de dieta aterogénico y lesión endotelial mecánica. El procedimiento presentado en la inducción de las placas ateroscleróticas en conejos utiliza un catéter con balón para alterar el endotelio en la arteria ilíaca izquierda de NZB conejos alimentados con la dieta aterogénico. Daño mecánico causado por el catéter con balón induce una cadena de reacciones inflamatorias iniciar neointimal acumulación del lípido en una manera dependiente del tiempo. Placa aterosclerótica después de espesamiento de neointimal de mostrar globo lesiones con infiltración extensa de lípidos, contenido de la celda alta del músculo liso y presencia de macrófagos derivados de células de la espuma. Esta técnica es simple, reproducible y produce la placa de longitud controlada dentro de la arteria ilíaca. Todo el procedimiento se completa dentro de 20-30 minutos. El procedimiento es seguro con baja mortalidad y ofrece también gran éxito en la obtención de importantes lesiones intimales. El procedimiento del catéter de balón indujo resultados de lesión arterial en la aterosclerosis dentro de dos semanas. Este modelo puede utilizarse para investigar la patología de la enfermedad, diagnóstico por imágenes y evaluar nuevas estrategias terapéuticas.
Introducción
La ruptura de las placas ateroscleróticas vulnerables es una de las principales causas de muerte en los países industrializados1. Aunque la investigación en las últimas décadas ha desarrollado varios mecanismos moleculares y celulares implicados en la progresión de la placa, continuó todavía se necesitan esfuerzos no sólo para desentrañar el complejo mecanismo de progresión de la enfermedad sino también para probar nuevas terapéuticas se acerca. Se han propuesto varios modelos animales para el estudio de la aterosclerosis. Manipulación genética, lesión de endotelio de alimentación o mecánico de colesterol son las estrategias estándar compartidas por modelos más animales de la aterosclerosis, incluyendo ratones, conejos o minipigs. Entre éstos, NZB los conejos son sensibles a la dieta de colesterol mientras que los ratones y las ratas normales no absorben mucho colesterol de la dieta2,3,4. Conejos desarrollan espontáneamente las lesiones aórticas ricas en macrófagos con algún componente fibroso cuando alimentados con colesterol dieta rica5,6. Sin embargo, el tiempo largo preparatorio de 4 a 8 meses para inducir la aterosclerótica plaquesby alimentación colesterol dieta solo6,7 es un gran inconveniente para la mayoría de los ajustes experimentales. En búsqueda para inducir lesiones en relativamente poco tiempo, una combinación de colesterol alto dieta y balón la lesión ha sido desarrollada por Baumgarter y Studer8. El objetivo general de esta técnica es inducir a las placas ateroscleróticas compuestas de células espumosas (similares a la estría grasa en los seres humanos) en conejos hipercolesterolémicos dentro de 2 semanas. La presente técnica describe el procedimiento de lesión de la pared arterial basado en método de Baumgarter utilizando un catéter con balón en la arteria ilíaca de conejos hipercolesterolémicos NZB.
Junto con una dieta rica en colesterol, lesiones resultantes de globo inducido la endotelialización conducirá a la aterosclerosis. Lesión de globo acelera la formación de lesiones ateroscleróticas y produce placa de tamaño uniforme y distribución. Engrosamiento intimal aumenta durante un período de tiempo y célula intimal infiltración comienza en pocos días después de lesión. Grasos con macrófagos importantes comienzan a aparecer después de 7-10 días de lesión de globo y están representados como lesión tipo II según la clasificación de la Asociación Americana del corazón. Lesión de globo en conejo se realiza con frecuencia en la aorta para estudiar la composición de la placa. El endotelio neointimal expresa altos niveles de la molécula de adhesión intercelular. Las placas se asocian a disección medial y cambios adventicial. Las lesiones ateroscleróticas están compuestos por lípidos, proliferación las células musculares lisas (SMCs), fibras de colágeno y células inflamatorias que se acumulan en el endotelio regenerado y son principalmente de tipo II en la naturaleza. La distribución topológica de las placas de conejo fue similar al reportado en aortas humanas 9,10 , en principio, la aorta es más grande en tamaño en comparación con las arterias ilíacas y produciría la placa de mayor longitud. Sin embargo, la gran ventaja de la utilización de la arteria ilíaca como el sitio de la aterosclerosis en conejos es su accesibilidad, su similitud en el contenido muscular de la arteria coronaria humana11, lesión uniforme desarrollo12, factor tisular alta actividad13 y recipiente consistente dimensión comparable a la coronaria humana permitiendo la evaluación de dispositivos comercialmente manufacturados morfométricas y criterios de valoración angiográficas. Se han investigado métodos invasivos y no invasivos para analizar las placas en las arterias ilíacas de conejo en el animal vivo. Informes anteriores describen el uso de resonancia magnética (MRI) con la ayuda de un Señor de 2,35-tesla sistema 14 además, el ultrasonido intravascular (IVUS) o catéteres de tomografía de coherencia óptica pueden ser adecuadamente aplicada a la imagen placas ateroscleróticas en las arterias ilíacas conejo. La arteria ilíaca es accesible para la proyección de imagen de ultrasonido cuando se usa una ecografía de alta resolución y la aorta puede estudiarse también con esta técnica.
En la última década, este modelo de conejo de lesión de globo ha ayudado a comprender aún más los mecanismos de progresión de placa15y regresión de placa16. Además, el modelo se ha utilizado para estudiar la influencia de nuevos agentes terapéuticos tales como las estatinas, antiagregantes estándar, antioxidante agentes17,18 y stents liberadores de fármacos como everolimus o liberador de zotarolimus stent19,20 en engrosamiento neointimal. Este modelo también se ha utilizado para investigar la proyección de imagen intravascular del catéter21la proyección de imagen de la fluorescencia del infrarrojo cercano.
Protocolo
este protocolo experimental ha sido aprobado por la Oficina veterinaria Cantonal, Fribourg y el suizo Federal veterinario oficina, Suiza (FR 2015/58).
Nota: se utilizaron conejos macho NZB entre 2.8 a 3.2 kg. Los animales fueron alojados bajo condiciones convencionales (12 h de luz y oscuro ciclo, proporcionada alimento y agua ad libitum). Antes de denudación del globo, los animales se aclimataron durante 1 semana durante la cual fueron alimentados con dieta normal chow. Después de una semana de aclimatación, conejos fueron cambiados a aterogénico dieta consistente en grasas (8.6%) y saturan ácidos grasos con 205 mg/kg dieta de colesterol (1%) para la duración del estudio entero. Lesión de globo en la arteria ilíaca izquierda se realizó 1 semana después de la iniciación de la dieta y los animales fueron sacrificados después de 2 semanas o 4 semanas de lesión de globo.
1. procedimientos preoperatorios
- esterilizar todos los instrumentos quirúrgicos antes de usar con un esterilizador de bolas de vidrio u otro instrumento adecuado.
- Preparar y comprobar el conjunto de catéter balón.
- Coloque una cerradura de luer 1 mL jeringa llena con solución salina normal a la parte de la cerradura del luer del catéter con balón. Vigilar cuidadosamente por ausencia de aire atrapado. Compruebe las fugas y garantizar la inflación adecuada globo presionando el émbolo de la jeringa de.
- Pesan el conejo y encienda el thermopad a 37 ° C.
- Utilizar una solución de buprenorfina a una concentración de 0,3 mg / ml. inyectar por vía subcutánea una dosis de 0,01 mg/kg.
- Anesthetize el conejo con 5% isoflurano y 5 L/min O 2 en una cámara de inducción de 10-15 min.
- Poner el conejo anestesiado en la almohada en la plataforma quirúrgica. Coloque el parche y clips para monitorear la temperatura, respiración y electrocardiograma.
- Colocar el hocico del conejo a una mascarilla conectada a una máquina de anestesia adecuada. Mantener la anestesia con isoflurano (4.0% con 2,5 L/min O 2). Confirmar la anestesia apropiada (indicada por la falta de tono muscular y pérdida de los reflejos nauseoso y pinnae).
- Aplique pomada oftálmica en ambos ojos para evitar que la córnea se seque. Cuelgue el conejo con una hoja quirúrgica estéril con sólo el miembro inferior expuesto.
2. Protocolo quirúrgico
- eliminar el pelo de la zona ventral justo debajo de las articulaciones de rodilla con cortapelos animales.
- Limpiar el área con desinfectante adecuado para limpiar la piel y quitar el pelo flojo.
- Localizar la arteria safena y haga una incisión de piel pequeña de unos 1,5 cm de longitud con un bisturí.
- Exponer una pequeña porción de la arteria safena con pinzas curvas pequeñas, sin dañar la vena femoral y nervio femoral.
- Coloque dos lazos de ligadura suelta (5-0 seda) debajo de la arteria safena y ATA una ligadura hacia el extremo distal de la arteria. Colocar un clamp microvascular por encima de la ligadura para detener el flujo de sangre desde la arteria ilíaca.
- Por vía tópica se aplica una gota de la papaverina para dilatar la arteria y evitar vasoespasmo.
- Levante la arteria safena con la ayuda de la ligadura atada y hacer una incisión pequeña arteriotomía utilizando 24 aguja g.
- Elevar las aletas de la incisión con unas pinzas finas y lentamente introducir una selección de vena o una aguja guía en el lumen de la arteria.
- Insertar un catéter de embolectomía arterial de Fogarty francés 2 dentro de la arteria safena. Quite la selección de la vena y pinzas microvasculares.
- Haga avanzar el catéter hasta la sexta marca (20-25 cm) correspondiente a una posición aproximadamente 2-5 cm por encima de la bifurcación ilíaca.
- Inflar el balón con solución salina normal 0,1 mL usando una jeringa de 1 mL o a una presión nominal de 6 atm con un inflador manual regulada tal como se describe en el 16 , 22.
- Mantenga el catéter de balón con pinzas y arrastre por 6 cm a través de la arterytoward ilíaca el punto de inserción, mientras gira el catéter.
- Desinflar el balón tirando hacia atrás el émbolo de la jeringa de.
- Repita 2.10 a 2.13 tres veces para asegurar la completa denudación endotelial.
- Retirar el catéter e inmediatamente atar el lazo de la ligadura por encima del sitio de arteriotomía para detener el sangrado.
- Aplique todo antiséptico adecuado alrededor de la periferia de la herida y limpiar lejos los coágulos de sangre. Cerrar la incisión de la piel con una sutura 5-0 y desinfectar el sitio de la cirugía con solución de povidona-yodo.
- Repita 2.1 a 2.16 en el contralateral ilíaca usando un catéter nuevo.
- Esponja el ungüento oftálmico de ojos.
3. Cuidados postoperatorios
- administrar sulfadoxina 40 mg/kg y el trimethoprim 8 mg/kg o cualquier otro antibiótico adecuado inmediatamente después del procedimiento quirúrgico.
- Durante el período de recuperación anestésica, mantener el conejo sobre una almohadilla de calor colocada en una jaula limpia esterilizada.
- Quitar el parche monitoreo y clips de.
- Después de la recuperación, regresar los conejos en sus jaulas hogar. Inyectar en forma subcutánea buprenorfina 0.05 - 0.1 mg/kg post - operativamente cada 6-12 h para 48 h. continuar dieta aterogénico por otro dos semanas o cuatro semanas.
4. La cosecha de tejido y análisis de composición de la placa
- después de dos semanas (para la placa delgada temprano) o de tres semanas de lesión de globo, anestesiar al conejo con isoflurano en una manera similar como se describe arriba.
- Abrir la cavidad torácica y eutanasia a los conejos por intracardial exsanguination.
- Aislar las arterias ilíacas, como se describe en el 23.
- Brevemente, abrir el abdomen y exponer el retroperitoneum. Seguimiento de la aorta hacia la bifurcación ilíaca y atarla por encima de la bifurcación. Retire con cuidado los tejidos circundantes para denunciar y aislar ambas arterias ilíacas.
- Diseque hacia fuera ambas arterias ilíacas y sumergirlos en solución salina amortiguada de fosfatos helada. Eliminar los coágulos con la ayuda de fórceps. Cada arteria ilíaca se dividen en segmentos de 4 a 6 para caracterizar el espesor de la placa a lo largo de la arteria.
- Inmediatamente incrustar los segmentos arteriales en un molde con temperatura óptima de corte compuesto, snap-congelación con nitrógeno líquido y guardar a-70 ° C. preparar 5 μm secciones de espesor con un criostato como se describe en 24.
- Realizar histología, la inmunofluorescencia o la coloración immunohistochemical para morfometría, placa lípidos y contenido celular como se describe en 10 , 25.
Nota: Brevemente, enjuagar las secciones arteriales con tampón fosfato salino (PBS) y permeabilizar utilizando 0,2% Tritón. Enjuague las secciones con PBS y bloquear sitios no específicos con seroalbúmina bovina al 2% durante 30 minutos incubar las secciones por 1 h a 37 ° C con anti actina α-SM (1: 200) o RAM11 anticuerpo (1: 200). Enjuague las secciones con PBS e incubar con el anticuerpo secundario apropiado durante 30 min a 37 ° C. lavado nuevamente con PBS y añadir Hoechst (5 μg/mL) durante 10 min detectar núcleos.
Resultados
Lesiones del globo de la arteria ilíaca fue realizada con éxito sin complicaciones (figura 1). El tiempo quirúrgico total varió de 20 a 30 min de lesiones realizado en sólo una arteria ilíaca y 35 a 45 min para las lesiones en ambas arterias. El conejo se recuperó dentro de 1 h después de lesión de globo. Todos los animales aparecieron sanos sin pérdida significativa de peso. Se ha encontrado ninguna infección, edema o trombosis arterial. El área de la herida era normal además algunas fibrosis leve en el sitio de sutura. Después de 4 semanas de dieta aterogénico alimentación, conejos exhibieron hipercolesterolemia de 44 ± 18 mM/l.
Figuras 2A, Figura 2Ey mostrar figura 2I la derecha ileso de la arteria ilíaca (no sometida a lesiones del globo) con una apariencia normal. Una combinación de globo dietresulted de lesión y el colesterol en los cambios estructurales de la pared del vaso hacia el desarrollo de placas ateroscleróticas en dos semanas (figura 2 y figura 3). Las arterias ilíacas lesionadas ileso y globo para fueron aisladas de los mismos animales. La respuesta proliferativa vascular lesión de globo como un hecho desencadenante resultó en lípidos extensa infiltración (8,7 ± 1.7% lípidos del área) (figura 2 y figura 3), músculo liso migración celular y la proliferación (figura 4), así reclutamiento de macrófagos (figura 4) conduce a un aumento en cociente del espesor íntima-media (1,5 ± 0,2) y área de placa (0,8 ± 0,2 mm2) con una concomitante disminución en el área de lumen (1,4 ± 0,2 mm2) (figura 3) observar 2 semanas después de lesión del globo. RAM-11 es un anticuerpo monoclonal que es específicamente dirigido contra el citoplasma de macrófagos de conejo. Actina α-SM identifica la actinia del músculo y reacciona con las células de músculo liso vascular en los vasos sanguíneos. Estos anticuerpos se han utilizado anteriormente para el estudio de macrófagos y células de músculo liso en las lesiones de la íntimas del conejo. Estos cambios continúan evolucionando con el tiempo y un mayor aumento en el cociente del espesor íntima/media (2,6 ± 0,2) y luminal estrechamiento (0,7 ± 0,1 mm2) (figura 2 y figura 3) se observó 4 semanas después de lesión de globo. Esta técnica conduce al robusto desarrollo de placas ateroscleróticas que desarrolla con el tiempo y se estudió después de 2 a 4 semanas.
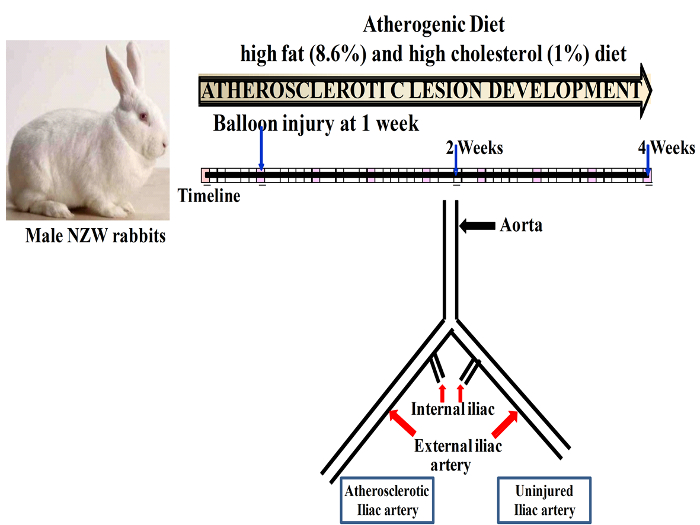
Figura 1: representación esquemática que ilustra la línea de tiempo de progresión de la placa después de lesión de globo. Haga clic aquí para ver una versión más grande de esta figura.

Figura 2: lesiones de globo inducida por aterosclerosis de arteria ilíaca conejo. Imágenes representativas de Movat pentachrome (A-d), hematoxilina-eosina (H E) y aceite rojo O (-L) secciones de los heridos no manchadas (A, E, I), 2 semanas post lesión de globo (B, F, J) (n = 5) y 4 semanas post lesión de globo (C, G, K) (n = 3) segmentos de arteria ilíaca de dieta aterogénico alimentan NZB conejos. Escala bar D, H y L es 100 μm. escala para las otras imágenes = 500 μm. etiqueta en la imagen B es la luz, íntima, IEL (lámina elástica interna) y anguila (lámina elástica externa). Los medios de comunicación son el área entre IEL y anguila. Haga clic aquí para ver una versión más grande de esta figura.
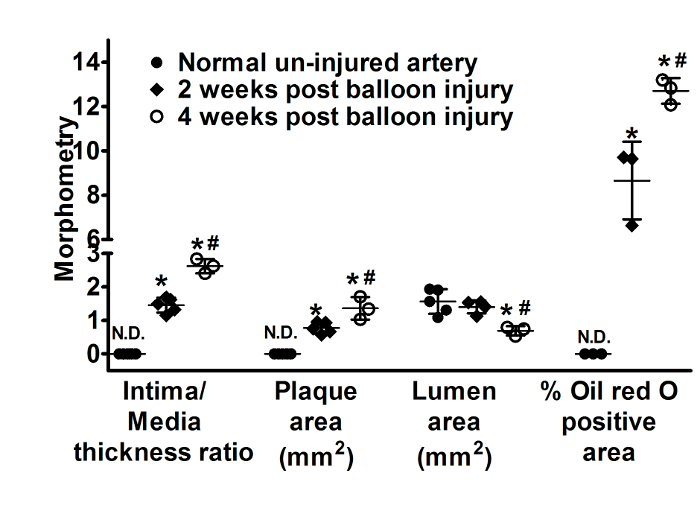
Figura 3: análisis morfométrico de la placa. La dispersión parcela muestra íntima/media relación de grosor, área de placa, área de lumen y % aceite rojo O positivo del área en secciones de la arteria ilíaca de control sin lesionados, globo lesiona arteria en 2 (n = 5) y 4 semanas (n = 3). Datos se muestran como media ± SD. * p < 0,05 vs arteria sin lesionados, #p < 0.05 vs 4 semanas post lesión de globo. N.D. denota no detectado. Zona de placa se calcula restando el área del lumen de la zona de la IEL al aceite rojo O área positiva representa % de la superficie de la pared de nave transversal total. Haga clic aquí para ver una versión más grande de esta figura.
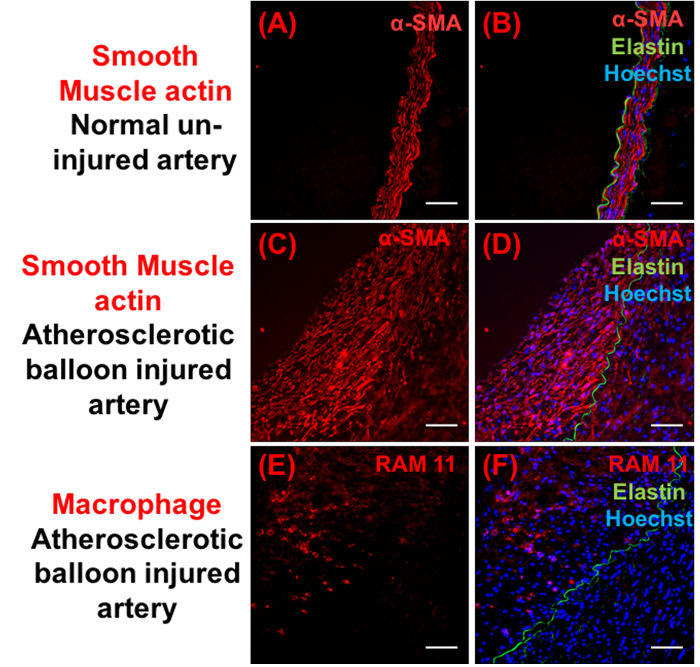
Figura 4: el análisis de Immunohistochemical de la composición de la placa. Imágenes representativas que muestran músculo liso α actina (rojo) (A-D) y macrófagos células positivas (RAM 11) (rojo) (E-F). Paneles de la derecha muestran las respectivas imágenes combinadas con Hoechst (azul) y elastina (verde). Barra de escala = 100 μm. haga clic aquí para ver una versión más grande de esta figura.
Discusión
El modelo de aterosclerosis de la arteria ilíaca de conejo es ampliamente utilizado en la investigación de la aterosclerosis. Con este protocolo los conejos desarrollaron rápidamente las placas más severas y avanzadas en comparación con las lesiones espontáneas convertidas sólo dieta de colesterol. Lo importante, animales recuperan rápidamente de la cirugía.
El principal estímulo de la aterogénesis es el daño mecánico causado por el catéter de balón que lesiona el endotelio y el buque de pared26de dilata. Este procedimiento induce una respuesta de remodelación caracterizada por una inflamación con macrófagos captación y acumulación de lípidos cuando se asocia con la dieta hypercholestorolemic, migración de células de músculo liso vascular y proliferación, matriz mejorada síntesis y el establecimiento de una neoíntima invasivo en un tiempo moda dependiente15,16. Insertar el catéter con balón es la parte más crítica del procedimiento. Debe tener cuidado para evitar introducir con fuerza el balón. Del uso de arterias periféricas safena a la arteria ilíaca común simplifica la técnica. Arteria ilíaca puede accederse también a través de la arteria carótida cut-down como se describió anteriormente27,28. Sin embargo, evaluar la arteria ilíaca a través de la arteria carótida requiere un grado alto de experiencia quirúrgica y equipo adicional como una unidad de angiografía. También se asocia con complicaciones procedimiento-relacionadas como lesión a la vena yugular a hemorragia fatal29. Uso de tópicos vasodilatadores como papaverina ayuda a dilatar el vaso y reducir la resistencia de la pared arterial contra el globo catéter30. El tamaño de la presión y el globo de inflación debe ser considerado cuidadosamente ya que estos tienen una asociación directa de formación neointimal31. Excesiva distensión del balón para un grado más alto que los niveles deseados podría conducir a la ruptura de la pared del vaso. Esto podría producir pérdidas de sangre y formación de trombo robusto en el lumen y el superficie exterior26.
Los animales deben ser alimentados una dieta rica para 1 o 2 semanas antes de lesión de globo para lesión endotelial se produce en un entorno hipercolesterolémicos de lípidos. También ayuda a los animales para adaptarse a la nueva dieta. Aunque esta técnica provoca placas avanzadas en conejos, la morfología de las placas difiere de aquel observado en los seres humanos. Las lesiones humanas espontáneas están restringidas a la región sub-endotelial con una capa elástica interna intacta32. Aquí, los estudios efectuados hasta 4 semanas no demostró corazones fibróticos. La lesión aterosclerótica sigue siendo similar a grasa racha con infiltración de macrófagos substancial.
Muchos modelos de animales grandes y pequeños se han utilizado para la comprensión de aterogénesis6. El modelo de lesión de globo conejo arteria ilíaca se ha utilizado para estudiar el efecto de nuevos agentes terapéuticos, sistemas de administración de fármaco nuevo, placa evolución y proyección de imagen de32,10,33. Único o múltiples injurieshave de globo se han realizado en la arteria ilíaca34,35,36,de la arteria carótida37y aorta10,38. Las ventajas del método actual son el desarrollo del volumen de la placa grande y grueso en comparación al uso de la arteria carótida. Además, la can ilíaca contralateral puede usarse como un control y por lo tanto reduce la variabilidad entre animales29. La lesión de globo en las arterias ilíacas conejo puede realizarse con seguridad y fácilmente usando el método descrito aquí. Placa se convierte en una manera dependiente del tiempo y es homogénea a lo largo de la longitud de la arteria. También han desarrollado otros modelos de conejo aterosclerótica como el Watanabe hereditarios hiperlipidémicos (WHHL) modelo un modelo de animales modificado genéticamente con deficiencia del receptor de la lipoproteína de baja densidad. El modelo de lesión de globo puede aplicarse también al conejo WHLL para producir las lesiones en un sitio definido.
Hay diferencias entre la arteria ilíaca de conejo y humanas placas coronarias. De hecho, se han establecido varios procedimientos alternativos en un intento para el desarrollo de lesiones ateroscleróticas avanzadas y crear un modelo de ruptura de placa, como se observa en los seres humanos39. Por ejemplo, la formación de placa inestable fue inducida mediante la eliminación de la dieta de colesterol después de 8 semanas en conejos que sufrió lesiones de globo16. Otros procedimientos modificados utilizan desencadenantes farmacológicos como veneno de víbora de Russell10 y posterior globo repetidas lesiones40para evaluar el mecanismo de ruptura de placa, crecimiento trombogénesis y trombo aterosclerótico vasos. El veneno de víbora de Russell contiene proteasas que activan la cascada de la coagulación llevando a trombosis. Resultados de lesión de globo repetidas en la generación de trombina por placa tejido factor40. Cabe señalar que los resultados de modelos animales incluyendo el modelo de conejo no se pueden extrapolar perfectamente a los seres humanos. Sin embargo, estos modelos pueden ser una herramienta útil para evaluar y comparar la eficacia de nuevas intervenciones farmacológicas. Cuidado de extrapolaciones deben hacerse en relación con el grado de hipercolesterolemia y placa composición para ampliar los conocimientos sobre la etiología, Fisiopatología y tratamiento de la aterosclerosis humana. El modelo presentado aquí ayuda a estudiar los mecanismos implicados en la evolución de la placa y a investigar el efecto de nuevas terapias anti-ateroscleróticas dirigida hacia la estabilización o regresión de la placa.
Divulgaciones
Los autores no declaran a intereses financieros en competencia.
Agradecimientos
Este trabajo fue apoyado por el suizo nacional ciencia Fundación beca 150271.
Materiales
| Name | Company | Catalog Number | Comments |
| New Zealand White rabbits | Charles River laboratories,France | Cre:KBL(NZW) | |
| Cholesterol rich diet | Ssniff spezialdiäten | Ssniff EF K High Fat and Cholesterol | |
| Glass bead sterilizer-Germinator 500 | VWR, Leicestershire, UK | 101326-488 | |
| Fogarty balloon embolectomy catheters, 2 French | Edwards Lifesciences, Switzerland | 120602F | For single use only |
| Luer Lock Syringe | Becton, Dickinson and Company, USA | 309628 | |
| Thermopad Type 226 | Solis, Switzerland AG | 397387 | |
| Buprenorphine- Temgesic | Reckitt Benckiser AG, Switzerland | 7.68042E+12 | |
| Isoflurane | Piramal Critical Care, Inc, Bethlehem, PA 18017 | 2667-46-7 | |
| Anaesthesia machine-combi-vet Base Anesthesia System | Rothacher Medical GmbH, Switzerland | CV 30-301-A | |
| Cardell touch veterinary vital signs monitor | Midmark, Ohio, USA | 8013-001 | |
| Ophthalmic ointment-Humigel | Virbac, France | ||
| Animal hair clippers | Aesculap AG, Germany | GT420 | |
| Disinfectant-Betadine solution | MundipharmaMedicalCompany, Switzerland | 14671-1203 | |
| Dumont #7 Forceps | FST Germany | 11274-20 | |
| Medium and small microscissors | Medline International Switzerland Sàrl | UC4337 | |
| Microvascular clamps | FST, Germany | 18051-28 | |
| Papaverine | ESCA chemicals, Switzerland | RE 356 803 | |
| Vein Pick | Harvard Apparatus, Cambridge, UK | 72-4169 | For single use only |
| Saline | Laboratorium Dr. G. Bichsel AG, , Switzerland | 1330055 | |
| Polysorb 5-0 suture | Covidien AG, Switzerland | UL 202 | Monofilament |
| Sulfadoxine and Trimethoprim-Trimethazol | Werner Stricker AG, Switzerland | Swissmedic Nr. 50'361 | |
| Antiseptic- Octenisept | Schülke & Mayr AG, Switzerland | GTIN: 4032651214068 | |
| Phosphate Buffered Saline | Roth | 1058.1 | |
| Isobutanol-2-Methylbutane | Sigma-Aldrich, Switzerland | M32631-1L | |
| Optimum Cutting Temperature compound-Tissue-Tek | VWR Chemicals, Belgium | 25608-930 | |
| Cryostat | Leica, Glattbrugg, Switzerland | Leica CM1860 UV | |
| Glass slide- Superfrost Plus | Thermo Scientific | 4951PLUS4 | |
| Mayer's Haematoxylin | Sigma-Aldrich, Switzerland | MHS32-1L | |
| Eosin 0.5% aq. | Sigma-Aldrich, Switzerland | HT110232-1L | |
| Oil Red O | Sigma-Aldrich, Switzerland | O0625-25G | |
| α-smooth muscle actin antibody | Abcam, UK. | ab7817 | |
| Macrophage Clone RAM11 antibody | DAKO, Switzerland | M063301 | |
| Hoechst | Abcam, UK. | ab145596 | |
| Goat polyclonal Secondary Antibody (Chromeo 546) | Abcam, UK. | ab60316 | |
| Alexa Fluor 488/547 | Abcam, UK. | ||
| Glycergel Mounting Medium, Aqueous | DAKO, Switzerland | C056330 | |
| Hematoxylin for Movat pentachrome staining | Sigma-Aldrich, Switzerland | H3136-25G | |
| Ferric chloride for Movat pentachrome staining | Sigma-Aldrich, Switzerland | 157740-100G | |
| Iodine for Movat staining | Sigma-Aldrich, Switzerland | 207772-100G | |
| Potassium iodide for Movat pentachrome staining | Sigma-Aldrich, Switzerland | 60400-100G-F | |
| Alcian blue for Movat staining | Sigma-Aldrich, Switzerland | A5268-10G | |
| Strong Ammonia for Movat pentachrome staining | Sigma-Aldrich, Switzerland | 320145-500ML | |
| Brilliant crocein MOO for Movat pentachrome staining | Sigma-Aldrich, Switzerland | 210757-50G | |
| Acid Fuchsin for Movat pentachrome staining | Sigma-Aldrich, Switzerland | F8129-50G | |
| Sodium Thiosulfate for Movat pentachrome staining | Sigma-Aldrich, Switzerland | 72049-250G | |
| Phosphotungstic acid for Movat pentachrome staining | Sigma-Aldrich, Switzerland | 79690-100G | |
| Crocin for Movat pentachrome staining | Sigma-Aldrich, Switzerland | 17304-5G | |
| EUKITT for Movat pentachrome staining | Sigma-Aldrich, Switzerland | 03989-100ML |
Referencias
- Mozaffarian, D., et al. Heart disease and stroke statistics--2015 update: a report from the American Heart Association. Circulation. 131, e29-e322 (2015).
- Boone, L. R., Brooks, P. A., Niesen, M. I., Ness, G. C. Mechanism of resistance to dietary cholesterol. J Lipids. 2011, 101242(2011).
- Kapourchali, F. R., et al. Animal models of atherosclerosis. World J Clin Cases. 2, 126-132 (2014).
- Carter, C. P., Howles, P. N., Hui, D. Y. Genetic variation in cholesterol absorption efficiency among inbred strains of mice. J Nutr. 127, 1344-1348 (1997).
- Kolodgie, F. D., et al. Hypercholesterolemia in the rabbit induced by feeding graded amounts of low-level cholesterol. Methodological considerations regarding individual variability in response to dietary cholesterol and development of lesion type. Arterioscler Thromb Vasc Biol. 16, 1454-1464 (1996).
- Singh, V., Tiwari, R. L., Dikshit, M., Barthwal, M. K. Models to study atherosclerosis: a mechanistic insight. Curr Vasc Pharmacol. 7, 75-109 (2009).
- Dornas, W. C., Oliveira, T. T., Augusto, L. E., Nagem, T. J. Experimental atherosclerosis in rabbits. Arq Bras Cardiol. 95, 272-278 (2010).
- Baumgartner, H. R., Studer, A. [Effects of vascular catheterization in normo- and hypercholesteremic rabbits]. Pathol Microbiol (Basel). 29, 393-405 (1966).
- Tanaka, H., et al. Sustained activation of vascular cells and leukocytes in the rabbit aorta after balloon injury. Circulation. 88, 1788-1803 (1993).
- Phinikaridou, A., Hallock, K. J., Qiao, Y., Hamilton, J. A. A robust rabbit model of human atherosclerosis and atherothrombosis. J Lipid Res. 50, 787-797 (2009).
- Nakazawa, G., et al. Drug-eluting stent safety: findings from preclinical studies. Expert Rev Cardiovasc Ther. 6, 1379-1391 (2008).
- Aikawa, M., et al. Lipid lowering by diet reduces matrix metalloproteinase activity and increases collagen content of rabbit atheroma: a potential mechanism of lesion stabilization. Circulation. 97, 2433-2444 (1998).
- Jeanpierre, E., et al. Dietary lipid lowering modifies plaque phenotype in rabbit atheroma after angioplasty: a potential role of tissue factor. Circulation. 108, 1740-1745 (2003).
- Durand, E., et al. Magnetic resonance imaging of ruptured plaques in the rabbit with ultrasmall superparamagnetic particles of iron oxide. J Vasc Res. 44, 119-128 (2007).
- Stadius, M. L., et al. Time course and cellular characteristics of the iliac artery response to acute balloon injury. An angiographic, morphometric, and immunocytochemical analysis in the cholesterol-fed New Zealand white rabbit. Arterioscler Thromb. 12, 1267-1273 (1992).
- Khanna, V., et al. Cholesterol diet withdrawal leads to an initial plaque instability and subsequent regression of accelerated iliac artery atherosclerosis in rabbits. PLoS One. 8, e77037(2013).
- Zou, J., et al. Effect of resveratrol on intimal hyperplasia after endothelial denudation in an experimental rabbit model. Life Sci. 68, 153-163 (2000).
- Li, M., Zhang, Y., Ren, H., Zhang, Y., Zhu, X. Effect of clopidogrel on the inflammatory progression of early atherosclerosis in rabbits model. Atherosclerosis. 194, 348-356 (2007).
- Nakazawa, G., et al. Evaluation of polymer-based comparator drug-eluting stents using a rabbit model of iliac artery atherosclerosis. Circ Cardiovasc Interv. 4, 38-46 (2011).
- Van Dyck, C. J., et al. Resolute and Xience V polymer-based drug-eluting stents compared in an atherosclerotic rabbit double injury model. Catheter Cardiovasc Interv. 81, E259-E268 (2013).
- Abran, M., et al. Validating a bimodal intravascular ultrasound (IVUS) and near-infrared fluorescence (NIRF) catheter for atherosclerotic plaque detection in rabbits. Biomed Opt Express. 6, 3989-3999 (2015).
- Kanamasa, K., et al. Recombinant tissue plasminogen activator prevents intimal hyperplasia after balloon angioplasty in hypercholesterolemic rabbits. Jpn Circ J. 60, 889-894 (1996).
- Pai, M., et al. Inhibition of in-stent restenosis in rabbit iliac arteries with photodynamic therapy. Eur J Vasc Endovasc Surg. 30, 573-581 (2005).
- Fischer, A. H., Jacobson, K. A., Rose, J., Zeller, R. Cryosectioning tissues. CSH Protoc. 2008, (2008).
- Chaytor, A. T., Bakker, L. M., Edwards, D. H., Griffith, T. M. Connexin-mimetic peptides dissociate electrotonic EDHF-type signalling via myoendothelial and smooth muscle gap junctions in the rabbit iliac artery. Br J Pharmacol. 144, 108-114 (2005).
- Zhang, W., Trebak, M. Vascular balloon injury and intraluminal administration in rat carotid artery. J Vis Exp. (94), (2014).
- Maillard, L., et al. Effect of percutaneous adenovirus-mediated Gax gene delivery to the arterial wall in double-injured atheromatous stented rabbit iliac arteries. Gene Ther. 7, 1353-1361 (2000).
- Sharif, F., et al. Gene-eluting stents: adenovirus-mediated delivery of eNOS to the blood vessel wall accelerates re-endothelialization and inhibits restenosis. Mol Ther. 16, 1674-1680 (2008).
- Lee, J. M., et al. Development of a rabbit model for a preclinical comparison of coronary stent types in-vivo. Korean Circ J. 43, 713-722 (2013).
- Tulis, D. A. Rat carotid artery balloon injury model. Methods Mol Med. 139, 1-30 (2007).
- Asada, Y., et al. Effects of inflation pressure of balloon catheter on vascular injuries and subsequent development of intimal hyperplasia in rabbit aorta. Atherosclerosis. 121, 45-53 (1996).
- Dornas, W. C., Oliveira, T. T., Augusto, L. E., Nagem, T. J. Experimental atherosclerosis in rabbits. Arq Bras Cardiol. 95, 272-278 (2010).
- Waksman, R., et al. PhotoPoint photodynamic therapy promotes stabilization of atherosclerotic plaques and inhibits plaque progression. J Am Coll Cardiol. 52, 1024-1032 (2008).
- Fernandez-Parra, R., et al. Pharmacokinetic Study of Paclitaxel Concentration after Drug-Eluting Balloon Angioplasty in the Iliac Artery of Healthy and Atherosclerotic Rabbit Models. J Vasc Interv Radiol. 26, 1380-1387 (2015).
- Dussault, S., Dhahri, W., Desjarlais, M., Mathieu, R., Rivard, A. Elsibucol inhibits atherosclerosis following arterial injury: multifunctional effects on cholesterol levels, oxidative stress and inflammation. Atherosclerosis. 237, 194-199 (2014).
- Manderson, J. A., Mosse, P. R., Safstrom, J. A., Young, S. B., Campbell, G. R. Balloon catheter injury to rabbit carotid artery. I. Changes in smooth muscle phenotype. Arteriosclerosis. 9, 289-298 (1989).
- Miyake, T., et al. Prevention of neointimal formation after angioplasty using nuclear factor-kappaB decoy oligodeoxynucleotide-coated balloon catheter in rabbit model. Circ Cardiovasc Interv. 7, 787-796 (2014).
- Fulcher, J., Patel, S., Nicholls, S. J., Bao, S., Celermajer, D. Optical coherence tomography for serial in vivo imaging of aortic plaque in the rabbit: a preliminary experience. Open Heart. 2, e000314(2015).
- Abela, O. G., et al. Plaque Rupture and Thrombosis: the Value of the Atherosclerotic Rabbit Model in Defining the Mechanism. Curr Atheroscler Rep. 18, 29(2016).
- Yamashita, A., Asada, Y. A rabbit model of thrombosis on atherosclerotic lesions. J Biomed Biotechnol. 2011, 424929(2011).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados