Method Article
Zellfreie Produktion von Proteoliposomen für die funktionelle Analyse und Antikörperentwicklung gegen Membranproteine
In diesem Artikel
Zusammenfassung
Dieses Protokoll beschreibt ein effizientes zellfreies Verfahren zur Herstellung von hochwertigem Proteoliposom mittels Doppelschichtdialysemethode unter Verwendung eines weizenzellenfreien Systems und Liposomen. Diese Methode bietet geeignete Mittel für die funktionelle Analyse von Membranproteinen, das Screening von Wirkstoffzielen und die Entwicklung von Antikörpern.
Zusammenfassung
Membranproteine spielen eine wesentliche Rolle in einer Vielzahl von zellulären Prozessen und erfüllen lebenswichtige Funktionen. Membranproteine sind in der Wirkstoffforschung von medizinischer Bedeutung, da sie das Ziel von mehr als der Hälfte aller Medikamente sind. Ein Hindernis für die Durchführung biochemischer, biophysikalischer und struktureller Studien von Membranproteinen sowie für die Antikörperentwicklung war die Schwierigkeit, große Mengen an hochwertigem Membranprotein mit korrekter Konformation und Aktivität herzustellen. Hier beschreiben wir eine "Bilayer-Dialysemethode" mit einem weizenkeimzellfreien System, Liposomen und Dialysebechern, um Membranproteine effizient zu synthetisieren und gereinigte Proteoliposomen in kurzer Zeit mit einer hohen Erfolgsrate herzustellen. Membranproteine können ebenso hergestellt werden wie in mehreren Milligramm, wie GPCRs, Ionenkanälen, Transportern und Tetraspaninen. Diese zellfreie Methode trägt dazu bei, Zeit, Kosten und Aufwand für die Herstellung hochwertiger Proteoliposomen zu reduzieren und bietet geeignete Mittel für die funktionelle Analyse von Membranproteinen, das Screening von Wirkstoffzielen und die Antikörperentwicklung.
Einleitung
Membranproteine sind eines der wichtigsten Wirkstoffziele in Diagnose und Therapie. Tatsächlich sind die Hälfte der kleinen Wirkstoffe Membranproteine wie G-Protein-gekoppelte Rezeptoren (GPCRs) und Ionenkanäle1. Im Laufe der Jahre haben Forscher an biochemischen, biophysikalischen und strukturellen Studien von Membranproteinen gearbeitet, um ihre Struktur und Funktion aufzuklären 2,3. Die Entwicklung monoklonaler Antikörper gegen Membranproteine wird ebenfalls aktiv durchgeführt, um funktionelle und strukturelle Studien zu beschleunigen und therapeutische und diagnostische Anwendungen zu entwickeln 4,5,6,7,8,9. Alle diese Studien erfordern eine große Menge an hochwertigen Membranproteinen10. So werden beispielsweise mehrere Milligramm gereinigte Membranproteine mit natürlicher Konformation für die Antikörperentwicklung benötigt. Für die Röntgenkristallographie wird eine viel größere Menge an hochgereinigten Membranproteinen benötigt. Die Massenproduktion von Membranproteinen bleibt jedoch ein Engpass in der Membranproteinforschung11. Membranproteine haben komplizierte Strukturen mit einer oder mehreren Transmembranhelices und spielen eine wichtige Rolle bei der Zellhomöostase. Die heterologe Überexpression von Membranproteinen führt zu mehreren Hindernissen wie der Aggregation von Membranproteinen, die sich in hohen lokalen Konzentrationen ansammeln, oder der Störung zellulärer Signalwege. Selbst wenn die Expression erfolgreich ist, stoßen auch nachfolgende Schritte der Probenvorbereitung auf Schwierigkeiten. Zum Beispiel erfordert die Herstellung von Proteoliposom hohe Fähigkeiten und Berufserfahrung in der Solubilisierung, Reinigung und Stabilisierung von Membranproteinen und kostet viel Aufwand und Zeit12,13.
Auf der anderen Seite sind in den letzten Jahrzehnten einige fortschrittliche Technologien entstanden, um Proteine ohne die Verwendung lebender Zellen herzustellen 14,15,16,17,18. Die zellfreie Proteinsynthesetechnologie rekonstruiert die Translationsreaktion in einem Reagenzglas. Da es keine Einschränkungen gibt, die das zelluläre Expressionssystem hat, haben zellfreie Systeme das Potenzial, eine Vielzahl von Proteinen zu synthetisieren, die schwer zu exprimieren sind oder Toxizität in Zellen zeigen. Gereinigter Zellextrakt oder rekonstituierte translationale Maschinerie wird mit Template-mRNAs, Aminosäuren und Energiequellen gemischt, und rekombinante Proteine werden in kurzer Zeit synthetisiert. In Bezug auf die Membranproteinsynthese werden einige Arten von Gerüsten, die aus Lipiden oder Amphiphilen bestehen, wie Liposomen, Bizellen, Nanoscheiben oder Copolymere, zur zellfreien Reaktion 19,20,21,22,23,24 hinzugefügt. Synthetisierte Membranproteine interagieren mit den Gerüsten und können in Wasser stabilisiert werden. Zellfreie synthetisierte Membranproteine werden häufig in funktionellen Studien und der Antikörperproduktion verwendet 25,26,27,28,29,30,31.
In diesem Protokoll beschreiben wir eine effiziente zellfreie Methode der Proteoliposomenproduktion unter Verwendung eines weizenzellenfreien Systems und Liposomen. Weizenzellfreies Proteinsynthesesystem ist ein leistungsfähiges In-vitro-Translationssystem mit Extrakt aus Weizenkeimen 15,32,33. Weizenkeime enthalten eine große Menge an translationalen Maschinen und wenige Translationshemmer. Die translationale Maschinerie in Weizen, einem Mitglied der Eukaryoten, eignet sich für die Translation eukaryotischer Proteine, und seine Translationseffizienz wird durch die Codonverwendung der Template-mRNA kaum beeinflusst. Unter Verwendung des weizenzellfreien Systems haben wir eine Vielzahl von Proteinen synthetisiert, darunter Proteinkinasen34,35, Ubiquitin-Ligasen36, Transkriptionsfaktoren37 und Membranproteine mit hohen Erfolgsraten. Für die Membranproteinproduktion fügen wir Lipidvesikelliposom als Gerüst19,38 in die Translationsmischung ein. Hydrophobe Domänen des Membranproteins interagieren mit der Lipiddoppelschicht und sind spontan in das Liposom integriert. Die Dichtegradientenzentrifugation wird verwendet, um Proteoliposom von endogenen Weizenproteinen strikt zu trennen, obwohl eine gemeinsame Zentrifugation des Translationsreaktionsgemisches für eine einfache Reinigung von Proteoliposom20 ausreicht. Viele Arten von integralen Membranproteinen wurden mit einem weizenzellenfreien System synthetisiert und für verschiedene Forschungen und Entwicklungen 25,38,39,40,41,42,43,44 angewendet. Darüber hinaus haben wir das "Bilayer-Dialyse-Verfahren" für die Großserienproduktion45,46 entwickelt. Bei diesem Verfahren wird ein Becherdialysegerät in den Substratzufuhrpuffer eingetaucht, und es werden zwei Schichten Translationsreaktionsgemisch und Substratzuführpuffer im Becher gebildet, wie in Abbildung 1 gezeigt. Die kontinuierliche Zuführung von Substraten und die Entfernung des Nebenprodukts kann sowohl oben als auch unten des Reaktionsgemisches über einen langen Zeitraum effizient durchgeführt werden, was zu einer hervorragenden Translationseffizienz führt (Abbildung 2A und Abbildung 2B)45.
Protokoll
1. Herstellung von pEU-Expressionsplasmid
HINWEIS: Das pEU-Expressionsplasmid sollte Startcodon, offenen Leserahmen des Zielmembranproteins und Stopcodon im Fragment enthalten (siehe Abbildung 1). Fügen Sie bei Bedarf Erkennungs-/Reinigungs-Tag-Sequenz(en) an der entsprechenden Position hinzu. Für das Subklonen ist entweder die Restriktionsenzymverdauung oder das nahtlose Klonen anwendbar. Hier beschreiben wir ein Protokoll, das eine nahtlose Klonmethode verwendet.
- Bereiten Sie das DNA-Fragment vor.
- Amplifizieren Sie das interessierende Gen durch PCR unter Verwendung der cDNA-Vorlage, Primer 1 und Primer 2. Primer 1 und Primer 2 enthalten 15 bp Überlappungen für nahtloses Klonen (siehe Materialtabelle).
HINWEIS: Fügen Sie keine Sequenzen hinzu, die verarbeitet und aus reifem Protein in den Zellen entfernt werden sollen (z. B. Signalsequenz). Die Verarbeitung von synthetisiertem Protein wird nicht im weizenzellenfreien System durchgeführt. Fügen Sie keine Kozak-Sequenz hinzu. Der pEU-E01-MCS-Vektor hat einen E01-Translationsverstärker. - Fügen Sie dem PCR-Produkt 1/25 Volumen des DpnI-Restriktionsenzyms hinzu, um die Template-Plasmid-DNA zu entfernen. 30 min bei 37 °C inkubieren.
- Verwenden Sie ein PCR-Reinigungskit, um das PCR-Produkt zu reinigen und die Konzentration bei 20-50 ng / μl einzustellen.
- Amplifizieren Sie das interessierende Gen durch PCR unter Verwendung der cDNA-Vorlage, Primer 1 und Primer 2. Primer 1 und Primer 2 enthalten 15 bp Überlappungen für nahtloses Klonen (siehe Materialtabelle).
- Linearisieren Sie den pEU-E01-MCS-Vektor.
- Führen Sie eine inverse PCR mit pEU-E01-MCS, Primer 3 und Primer 4 durch.
- Fügen Sie dem inversen PCR-Produkt 1/25 Volumen des DpnI-Restriktionsenzyms hinzu. 30 min bei 37 °C inkubieren.
- Verwenden Sie ein PCR-Reinigungskit, um das PCR-Produkt gemäß der Empfehlung des Herstellers zu reinigen. Stellen Sie die Konzentration auf 20–50 ng/μL ein.
- Mischen Sie 2 μL DNA-Fragment, 2 μL linearisierten Vektor und 4 μL 2x nahtlose Klonenzymmischung.
- Transformieren Sie den Escherichia coli-Stamm JM109 mit dem nahtlosen Klonprodukt. Verteilen Sie die Bakteriensuspension mit einem Streuer auf einer LB-Ampicillin-Agarplatte.
HINWEIS: pEU-Vektor hat einen Ampicillin-Widerstandsmarker. - Bestätigen Sie die Sequenz des Expressionsplasmids, das unter Verwendung von Primer 5 und Primer 6 von der 5'- bzw. 3'-Seite von MCS im pEU-Plasmid konstruiert wurde.
- Amplifizieren und reinigen Sie die Expressionsplasmide.
- Kultur des plasmidtransformierten E . coli-Stammes JM109 in 150 ml LB-Ampicillin-Medium bei 37 °C und 125 Hüben pro Minute unter Schütteln über Nacht.
- Extrahieren und reinigen Sie die Plasmide mit handelsüblichen Plasmid-Prep-Midi-Kits. Plasmide werden in 500 μL TE-Puffer gelöst.
VORSICHT: Verwenden Sie kein Mini-Vorbereitungskit für die Plasmidextraktion. Es bietet keine ausreichende Qualität und Quantität des Plasmids. - Fügen Sie 500 μL Phenol/Chloroform/Isoamylalkohol hinzu (25:24:1). 5 min kräftig mischen und 5 min bei 17.800 x g Raumtemperatur zentrifugieren. Die obere Plasmidlösung in ein neues Röhrchen überführen.
ACHTUNG: Tragen Sie Einweghandschuhe, um die Haut vor Phenol und Chloroform zu schützen.
HINWEIS: Um die Kontamination von RNase aus dem Plasmidextraktionskit zu entfernen, reinigen Sie die Plasmide mit Phenol-Chloroform-Reinigung. - Fügen Sie 500 μL Chloroform hinzu, um Phenol vollständig zu entfernen. 5 min kräftig mischen und 5 min bei 17.800 x g Raumtemperatur zentrifugieren. Die obere Plasmidlösung in ein neues Röhrchen überführen.
- 2,5 Volumen Ethanol und 1/8 Volumen 7,5 M Ammoniumacetat zugeben und bei -30 °C 1 h lagern.
- Zentrifugieren bei 17.800 x g bei 4 °C für 10 min. Waschen Sie das Pellet mit 500 μL 70% Ethanol. Entfernen Sie den Überstand vorsichtig und lassen Sie das Pellet 5 min trocknen.
- Lösen Sie die Expressionsplasmide vollständig in 100 μL Reinstwasser auf. Messen Sie die Konzentration von Plasmiden mit Absorption bei 260 nm. Stellen Sie die Konzentration auf 1 mg/ml ein.
2. In-vitro-Transkription
VORSICHT: Verwenden Sie DNase- und nukleasefreie Kunststoffröhrchen und -spitzen in Schritten der Transkription und Translation. Vermeiden Sie das Autoklavieren von Kunststoffwaren, um eine Kontamination zu vermeiden.
- Ernten Sie Reinstwasser in einem neuen Kunststoffrohr.
VORSICHT: Verwenden Sie kein DEPC-behandeltes Wasser, da Rest-DEPC die Reaktion stark hemmt. Verwenden Sie frisch gereinigtes Reinstwasser für die Transkription und Übersetzung. - Herstellen einer Transkriptionsreaktionsmischung durch Mischen von 115,2 μL Reinstwasser, 40 μL Transkriptionspuffer LM, 20 μL NTP-Mischung, 2,4 μL 80 U/μL RNase-Inhibitor, 2,4 μL 80 U/μL SP6-Polymerase und 20 μL 1 mg/ml pEU-Expressionsplasmiden. Mischen Sie die Reagenzien vorsichtig durch Umdrehen. Führen Sie eine schnelle Drehung durch.
- Die Transkriptionsreaktion wird bei 37 °C für 6 h inkubiert.
- Mischen Sie die Reaktion vorsichtig, indem Sie sie umkehren und schnell herunterdrehen. Verwenden Sie es sofort für die Übersetzung, ansonsten einfrieren und bei -80 °C lagern.
- Bestätigen Sie das Transkriptionsprodukt durch Elektrophorese.
- Mischen Sie 100 ml 1x TAE-Puffer und 1 g Agarose. Erhitzen Sie die Suspension in einer Mikrowelle, um 1% Agarose TAE-Gel herzustellen.
- Man nimmt 1 μL Transkriptionsreaktion und mischt mit 3 μL Wasser und 4 μL 2x Ladenfarbstoff.
HINWEIS: Eine Denaturierung der RNA ist nicht erforderlich. - Laden Sie 4 μL der Mischung und 2 μL DNA-Leitermarker in das Agarose-TAE-Gel.
- Elektrophorese bei 100 V für 20 min.
- Färben Sie das Gel in Ethidiumbromid für 30 min. Überprüfen Sie das Leiterbandmuster der mRNA mit UV-Transilluminator und Gel-Imager.
HINWEIS: Wenn eine verschmierte Bande von weniger als 500 bp beobachtet wird, wird ein mRNA-Abbau vermutet.
3. Vorbereitung der Materialien für die Übersetzung
- Bereiten Sie den Übersetzungspuffer vor.
- Mischen Sie 27 ml frisch zubereitetes Reinstwasser und 0,75 ml jeder 40-fachen Stammlösung für S1, S2, S3 und S4 in einem 50-ml-Röhrchen.
HINWEIS: Modulieren Sie die Materialmengen entsprechend der endgültigen erforderlichen Menge an 1x Übersetzungspuffer.
ACHTUNG: Lagern oder frieren Sie den überschüssigen 1x-Übersetzungspuffer nach Gebrauch nicht wieder ein.
- Mischen Sie 27 ml frisch zubereitetes Reinstwasser und 0,75 ml jeder 40-fachen Stammlösung für S1, S2, S3 und S4 in einem 50-ml-Röhrchen.
- Kreatinkinase-Stammlösung vorbereiten. Lyophilisierte Kreatinkinase in Reinstwasser auf eine Endkonzentration von 20 mg/ml auflösen. Die Lösung wird in kleinen Mengen (jeweils 10 bis 50 μL) in 0,2 ml 8-Streifen-PCR-Röhrchen verabreicht. Die Röhrchen in flüssigem Stickstoff einfrieren und bei -80 °C lagern.
ACHTUNG: Kreatinkinaselösung nach dem Auftauen nicht wieder einfrieren. - Waschen Sie Dialysebecher (Größe 0,1 ml), um Glycerin aus der Dialysemembran zu entfernen.
HINWEIS: Es gibt mehrere Dialysebecher unterschiedlicher Größe. Kleine Becher (0,1 ml) werden für Tests in kleinem Maßstab (Abschnitt 5.4) bzw. großformatige Becher (2 ml) für die Großproduktion (Abschnitt 5.5) verwendet. Der Waschschritt der Dialysemembran von großformatigen Bechern ist vermeidbar.- Geben Sie 1 ml Reinstwasser in ein neues 1,5-ml-Röhrchen. Führen Sie einen kleinen Dialysebecher (0,1 ml) in das Röhrchen ein. Fügen Sie 0,5 ml Reinstwasser in die Tasse hinzu.
- Inkubieren Sie länger als 30 min bei Raumtemperatur.
4. Herstellung von Liposomen
HINWEIS: Hier beschreiben wir zwei Protokolle zur Herstellung von Liposomen. Einer verwendet gebrauchsfertige lyophilisierte Liposomen (Abschnitt 4.1), während der andere Liposomen durch Hydratisieren eines dünnen Lipidfilms produziert (Abschnitt 4.2).
- Bereiten Sie Liposomen mit lyophilisierten Liposomen vor.
HINWEIS: Ein einfacherer Weg, Proteoliposom zu produzieren, ist die Verwendung von kommerziell erhältlichem Asolectin-Liposom. Asolectin ist eine Art natürliches Lipid, das aus Sojabohnen gewonnen wird.- Öffnen Sie die Durchstechflasche mit 10 mg lyophilisierten Asolectin-Liposomen (siehe Materialtabelle) und geben Sie 200 μl Translationspuffer (Abschnitt 3.1) auf den Boden der Durchstechflasche. Die Durchstechflasche verschließen und 10 min inkubieren.
- Mischen Sie kräftig, indem Sie die Durchstechflasche für 1 min auf den Vortex-Mixer legen.
- Führen Sie die Durchstechflasche in ein 50-ml-Röhrchen ein. Schleudern Sie das Röhrchen durch Zentrifugieren mit 500 x g für 1 min.
- Die Asolectin-Liposomensuspension (50 mg Lipid/ml) wird mit einer Pipette in ein neues 1,5-ml-Röhrchen überführt. Liposom sofort zur Translation verwenden, ansonsten in flüssigem Stickstoff einfrieren und bei -80 °C lagern.
- Bereiten Sie Liposomen vor, indem Sie einen dünnen Lipidfilm hydratisieren.
- Wenn ein Lipid in Pulverform verkauft wird, lösen Sie es in Chloroform oder einem geeigneten organischen Lösungsmittel auf eine Konzentration von 10-100 mg / ml.
HINWEIS: Ein dünner Lipidfilm kann unter Verwendung gereinigter und/oder synthetisierter amphiphiler Lipide hergestellt werden. Das Reinigungsverfahren von Asolectin ist bereits beschrieben38. Funktionell modifizierte Lipide, wie biotinylierte Lipide, fluoreszierende Lipide und adjuvante Lipide, können den Basallipiden zugesetzt werden, um funktionelle Liposomen zu erzeugen. - Die Lipidlösung, die 50 mg Lipid(e) enthält, wird in einen Verdampfungskolben überführt.
- Verdampfen Sie das Lösungsmittel mit einem Rotationsverdampfer und verteilen Sie das Lipid gleichmäßig auf der Wand des Kolbenbodens, um einen dünnen Lipidfilm zu bilden.
- Der Kolben wird in einen Vakuum-Exsikkator gegeben und über Nacht unter Unterdruck stehen gelassen, um das Lösungsmittel vollständig zu entfernen.
- 1 ml Translationspuffer in den Verdampfungskolben geben. Drehen Sie den Kolben, um den Puffer über den dünnen Lipidfilm zu verteilen. 5 min inkubieren, um den Film mit Feuchtigkeit zu versorgen.
- Beschallen Sie den Kolben mit einem Ultraschallhomogenisator oder Ultraschallreiniger. Ändern Sie gelegentlich den Winkel des Kolbens, damit die Lösung den Film gründlich berühren kann. Stellen Sie sicher, dass der dünne Lipidfilm von unten abgezogen und vollständig und homogen emulgiert wird.
HINWEIS: Die elektronenmikroskopische Aufnahme von biotinylierten Lipiden, die Liposomen enthalten, ist in Abbildung 1 dargestellt. - Die Liposomensuspension (50 mg Lipide/ml) wird in ein neues 1,5 ml Röhrchen überführt. Wenn es nicht sofort verwendet werden soll, frieren Sie die Liposomen in flüssigem Stickstoff ein und lagern Sie sie bei -80 °C.
- Wenn ein Lipid in Pulverform verkauft wird, lösen Sie es in Chloroform oder einem geeigneten organischen Lösungsmittel auf eine Konzentration von 10-100 mg / ml.
5. In-vitro-Übersetzung
- Tauen Sie den Weizenkeimextrakt schnell auf, indem Sie die Röhrchen einige Minuten auf Wasser bei Raumtemperatur schwimmen lassen. Nach dem Auftauen sofort vorsichtig mischen, indem Sie die Röhrchen umdrehen, herunterdrehen und bis zum Gebrauch auf Eis kühlen.
HINWEIS: Weizenkeimextrakt nach Gebrauch in flüssigem Stickstoff einfrieren und bei -80 °C lagern. Es übersteht mehrere Gefrier-/Tauzyklen. - 20 mg/ml Kreatinkinase-Stammlösung auftauen. Mischen Sie 5 μL Stammlösung und 45 μL Translationspuffer, um 2 mg/ml Kreatinkinase-Arbeitslösung herzustellen.
ACHTUNG: Das erneute Einfrieren der Kreatinkinase wird nicht empfohlen. - Liposomen oder mRNAs bei Bedarf auftauen.
- Führen Sie eine Proteinübersetzung in kleinem Maßstab durch.
- Wasser aus dem Röhrchen und dem Dialysebecher (0,1 ml) entfernen, wie in Schritt 3.3.2 vorbereitet.
- Injizieren Sie 1 ml bzw. 300 μL Translationspuffer in das Röhrchen bzw. den Dialysebecher.
VORSICHT: Falls der Boden des Dialysebechers die Oberfläche des Translationspuffers im 1,5-ml-Röhrchen nicht erreicht, injizieren Sie zusätzliche 50-100 μL Puffer in den Schlauch. - Präparation der Translationsreaktionsmischung durch Mischen von 15,6 μL Translationspuffer, 2,4 μL 2 mg/ml Kreatinkinase, 12 μL 50 mg/ml Liposomen, 15 μL Weizenkeimextrakt und 15 μL mRNA. Mischen Sie vorsichtig, indem Sie die Röhrchen umdrehen, und drehen Sie sie nach unten.
- 60 μL des Translationsreaktionsgemisches werden mit einer 200 μL Pipette abgesaugt.
- Führen Sie die Pipettenspitze in die Unterseite des Translationspuffers im Dialysebecher ein. Pipetten Sie das Reaktionsgemisch langsam und vorsichtig heraus. Decken Sie den Dialysebecher mit einem Deckel ab, um eine Verdunstung zu verhindern.
HINWEIS: Das Reaktionsgemisch sinkt auf natürliche Weise auf den Boden des Bechers und bildet eine Doppelschicht. Stören Sie die Doppelschicht nicht, indem Sie die Tasse mischen oder schütteln.
- Führen Sie eine umfangreiche Übersetzung durch (Abbildung 1).
- Gießen Sie 22 mL Translationspuffer in ein 25 ml Röhrchen. Führen Sie einen großen Dialysebecher (2 ml) in das Röhrchen ein und geben Sie 2 ml Translationspuffer in den Becher.
- Präparation einer Translationsreaktionsmischung durch Mischen von 130 μL Translationspuffer, 20 μL 2 mg/ml Kreatinkinase, 100 μL 50 mg/ml Liposom, 125 μL Weizenkeimextrakt und 125 μL mRNA. Durch Pipettieren vorsichtig mischen.
- Das gesamte Translationsreaktionsgemisch (500 μL) wird mit einer 1.000 μL Pipette abgesaugt. Das Translationsreaktionsgemisch wird wie in Schritt 5.4.5 beschrieben in den Dialysebecher injiziert. Decken Sie den Dialysebecher mit einem Deckel ab, um eine Verdunstung zu verhindern.
- Die Reaktionen werden bei 15 °C für 24 h inkubiert.
- Mischen Sie die Reaktion gut im Dialysebecher durch Pipettieren. Übertragen Sie die rohe Proteoliposomensuspension in ein neues Röhrchen.
HINWEIS: Ein 1,5-ml-Röhrchen mit flachem Boden wird empfohlen, um das Proteoliposom aus der kleinskaligen Translation zu sammeln. Nach der Zentrifugation bilden Liposomen ein kompaktes und gut sichtbares Pellet an der unteren Ecke des Röhrchens.
6. Reinigung von Proteoliposomen
- Zentrifugieren Sie das Röhrchen mit der rohen Proteoliposomensuspension bei 17.800 x g bei 4 °C für 10 min.
- Entfernen Sie den Überstand. Suspendieren Sie das Proteoliposomenpellet in PBS (kleiner Maßstab: 1 ml, großer Maßstab: 10 ml) durch Pipettieren.
- Wiederholen Sie die Zentrifugation und das Waschen von Proteoliposomen für weitere zwei Kreise.
- Fügen Sie nach dem Waschen eine kleine Menge PBS hinzu und suspendieren Sie das Proteoliposomenpellet gut durch Pipettieren. Messen Sie das Volumen der Suspension mit einer Mikropipette. Fügen Sie PBS hinzu, um das Volumen auf 60 μL (kleiner Maßstab) oder 500 μL (großer Bereich) einzustellen. Die Suspension wird in ein neues 1,5-ml-Röhrchen überführt.
- Übertragen Sie 10 μL Proteoliposom-Suspension in ein neues PCR-Röhrchen für SDS-PAGE. Teilen Sie den Rest der Proben in kleinere Portionen, um sie bei Bedarf zu verwenden. In flüssigem Stickstoff einfrieren und bei -80 °C lagern.
7. SDS-PAGE und CBB-Färbung
- Fügen Sie 70 μL Wasser und 40 μL 3x SDS-PAGE Probenpuffer zu 10 μL Proteoliposomensuspension hinzu.
ACHTUNG: Kochen Sie die SDS-PAGE-Probe nicht, da Membranproteine aggregieren und bei der Elektrophorese kaum in das Acrylamidgel eindringen. Fügen Sie außerdem genügend Reduktionsmittel zum SDS-PAGE-Probenpuffer hinzu (z. B. 2-Mercaptoethanol bei 3% Endkonzentration), um eine Oxidation zu verhindern. - Legen Sie ein SDS-PAGE-Gel mit einem Farbverlauf von 5 % bis 20 % in eine Elektrophoresekammer. Laden Sie 3 μL, 6 μL, 12 μL Proteoliposomenproben, 2 μL Proteingrößenmarker und BSA-Standardserien.
- Elektrophorese bei 52 mA, 400 V für 30 min.
- Färben Sie das Gel mit CBB-Farbstoff für 1 h. In heißem Wasser entfärben und das Gelbild scannen.
- Quantifizieren Sie mithilfe der NIH Image J-Software (https://imagej.nih.gov/ij/) die Bandenintensität des Membranproteins in jeder Bahn. Schätzen Sie die Menge der synthetisierten Membranproteine mit BSA-Standardreihen.
Ergebnisse
Mit diesem Protokoll können teilweise gereinigte Proteoliposomen in kurzer Zeit erhalten werden. Repräsentative Ergebnisse sind in Abbildung 2A dargestellt. Fünfundzwanzig GPCRs der Klassen A, B und C wurden erfolgreich mit der Doppelschichtdialysemethode (kleiner Maßstab) synthetisiert und teilweise durch Zentrifugation und Pufferwäsche gereinigt. Obwohl die Menge der synthetisierten Proteine je nach Proteintyp variiert, können bei Verwendung großer Dialysebecher in der Regel 50 bis 400 μg Membranproteine pro Reaktion synthetisiert werden. Mehrere Milligramm Membranproteine können aufgrund der hohen Skalierbarkeit des weizenzellenfreien Systems leicht hergestellt werden, indem die Anzahl der Reaktionen erhöht wird. Ein Vortest mit einem kleinen Dialysebecher reicht aus, um die Produktionswirksamkeit des Zielproteins im Doppelschichtdialyseverfahren zu bestimmen. Entsprechend der erzielten Produktivität kann die Menge des Zielproteins, die mit großen Dialysebechern hergestellt werden soll, abgeschätzt werden.
Dieses Protokoll eignet sich für die Expression von Membranproteinen, insbesondere für solche mit multiplen Transmembranhelices. In den meisten Fällen werden Membranproteine mit drei oder mehr Transmembranhelices nach der Synthese leicht in Proteoliposomen eingebaut (Abbildung 2B), was eine gute Produktivität der Proteoliposomen ausmacht. Single-Transmembran-Helix-Proteine werden normalerweise reibungslos synthetisiert; Allerdings integrieren sie sich aufgrund der kleinen hydrophoben Region kaum in Liposomen. Bei Proteinen mit zwei Transmembranhelices hängt es davon ab, wie ihre Transmembranhelices exponiert sind, ob sie an Liposomen verankert sind oder nicht.
Synthetisierte Proteoliposomen werden durch einfache Zentrifugation gesammelt und teilweise mit einem Waschpuffer gereinigt, was den Reinigungsprozess von Membranproteinen stark verkürzt. Obwohl sowohl biologische Membranen als auch Membranproteine zuvor aus Weizenkeimextrakten entfernt wurden, werden manchmal kleine Mengen von Weizenproteinen durch Bindung an Liposomen oder synthetisierte Membranproteine mitpräzipitiert (Abbildung 2A). Solche Proteinverunreinigungen lassen sich durch einfaches Zentrifugieren und Pufferwaschen nur schwer entfernen. Wenn ein hochgereinigtes Membranprotein benötigt wird, ist es notwendig, die teilgereinigten Proteoliposomen mit einem Tensid zu solubilisieren und durch Säulenchromatographie zu reinigen.

Abbildung 1: Schema der zellfreien Proteoliposomenproduktion. SP6, SP6-Promotorsequenz; E01, E01 Translation Enhancer Sequenz; Ampr, Ampicillinresistenzgen; DTT, Dithiothreitol. Elektronenmikroskopische Aufnahme zeigt Immunogold-Markierung von biotinyliertem Lipid enthaltendem Liposom. Bar, 0,2 μm. Dieses elektronenmikroskopische Bild stammt aus Abbildung 1D in Takeda et al., 201545. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
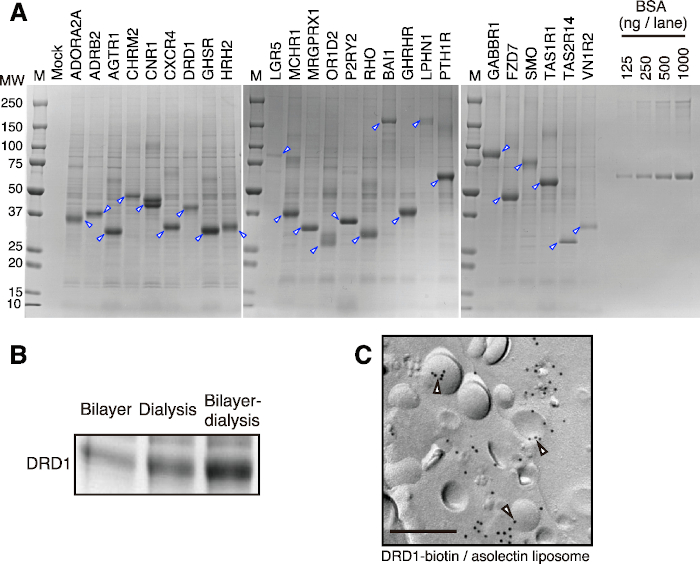
Abbildung 2: Repräsentative Ergebnisse der Proteoliposomenproduktion mittels Doppelschichtdialysemethode. (A) SDS-PAGE Bild von zellfrei synthetisierten GPCRs. Fünfundzwanzig ausgewählte GPCRs wurden mittels der Zweischichtdialysemethode synthetisiert. Proteoliposomen wurden teilweise gereinigt und auf SDS-PAGE und CBB-Färbung aufgetragen. Pfeilspitzen zeigen Ziel-GPCRs an. (B) Vergleich der Membranproteinproduktion zwischen verschiedenen Translationsmethoden. Das Dopaminrezeptor D1 (DRD1) -Protein wurde nach jeder Methode im gleichen Verhältnis von Weizenkeimextrakt, Liposomen und mRNA synthetisiert. Das DRD1-Proteoliposom wurde teilweise durch Zentrifugation gereinigt und einer SDS-PAGE- und CBB-Färbung unterzogen. (C) Immunogold-Markierung des DRD1-Biotin/Liposom-Komplexes. DRD1 wurde enzymatisch durch BirA-Biotin-Ligase biotinyliert. Bar, 0,2 μm. Leere Pfeilspitzen zeigen DRD1-Biotin auf Liposomen an. Diese Abbildung wurde von Abbildung 1 in Takeda et al., 201545 modifiziert. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
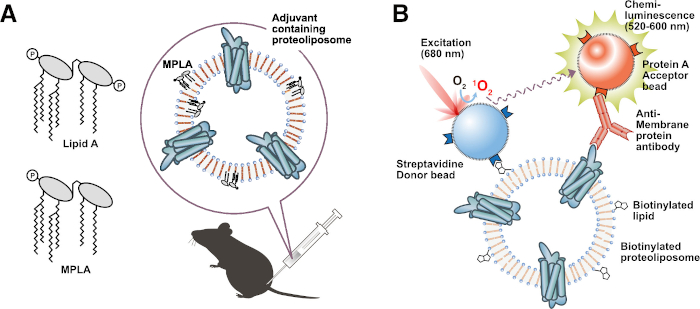
Abbildung 3: Anwendung funktioneller Proteoliposomen. (A) Immunisierung von adjuvanten lipidhaltigen Proteoliposomen. (B) Biotinylierter Liposom-basierter Interaktionstest (BiLIA). Die Interaktion zwischen Membranprotein und Anti-Membranprotein-Antikörper wurde von AlphaScreen nachgewiesen. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
Diskussion
Das vorgestellte Protokoll bietet eine Methode zur Herstellung von Membranproteinen mit einer hohen Erfolgsrate. Dieses Protokoll ist einfach, hochgradig reproduzierbar und leicht zu skalieren. Es hat auch das Potenzial, den Zeit- und Kostenaufwand für Experimente zu reduzieren, die eine große Menge an Membranproteinen verbrauchen. Die Zweischichtdialysemethode verbessert die Produktivität um das 4- bis 10-fache im Vergleich zur Doppelschichtmethode oder Dialysemethode (Abbildung 2B)45. Im Extremfall erhöhte sich die Ausbeute eines Ionenkanals und eines Transporters bei der Bilayer-Dialysemethode um das 30- bzw. 20-fache als bei der Doppelschicht-Methode (Daten nicht gezeigt). Die hohe Produktivität dieses Protokolls ist ein Vorteil bei der Antigenproduktion für die Immunisierung. Proteoliposomen werden häufig als immunisierende Antigene für die Entwicklung von Anti-Membran-Protein-Antikörpern verwendet. Hochkonzentrierte und gereinigte Membranproteine, die in Proteoliposomen eingebettet sind, stimulieren effektiv die Immunantwort und induzieren Antikörper41,47. Mit dieser Doppelschicht-Dialysemethode können Proteoliposomen, die mehrere Milligramm Membranproteine für Immunisierungszwecke tragen, in wenigen Tagen leicht hergestellt werden. Tatsächlich hat unsere Gruppe GPCRs, Ionenkanäle und Claudine unter Verwendung dieses Protokolls synthetisiert und Mäuse mit den Produkten immunisiert, um monoklonale Antikörper gegen sie zu erhalten31,41,45. Einige der erhaltenen monoklonalen Antikörper wurden als funktionelle Antikörper verifiziert, wie z. B. hochaffine Antikörper, konformationssensitive Antikörper, durchflusszytometrisch anwendbare Antikörper und inhibitorische Antikörper, was darauf hindeutet, dass dieses Protokoll in der Lage ist, Membranproteine mit funktionell korrekten Konformationen herzustellen.
Ein weiterer attraktiver Vorteil dieses Protokolls besteht darin, die Produktion von Proteoliposomen zu ermöglichen, denen bestimmte Funktionen unter Verwendung modifizierter Lipide zugewiesen werden, wie biotinylierte Lipide, fluoreszierende Lipide oder adjuvante Lipide. Vorbereitete Proteoliposomen mit spezifischen Funktionen sind nützlich und für eine Vielzahl von Experimenten anwendbar. Zum Beispiel sind adjuvante lipidhaltige Proteoliposomen, wie Lipid A48 oder Monophosphoryllipid A (MPLA)49, bequeme Immunisierungsantigene, da sie direkt verabreicht werden können, um Mäuse ohne Emulsion zu immunisieren. Adjuvante Lipide stimulieren effektiv die Immunantwort bei Wirtstieren und induzieren Antikörper gegen Zielmembranproteine (Abbildung 3A). Tatsächlich haben wir erfolgreich durchflusszytometrische Antikörper induziert, indem wir Mäuse mit MPLA-haltigem Proteoliposom31 immunisiert haben. Auch Proteoliposomen, die aus biotinylierten Lipiden hergestellt werden, sind ideale Sonden für Screening-Assays. Wir entwickelten eine Hochdurchsatz-Screening-Methode zur Auswahl von Anti-Membran-Protein-Antikörpern unter Verwendung biotinylierter Proteoliposomen und AlphaScreen (BiLIA-Methode) (Abbildung 3B)45. Sandwich-ELISA kann auch leicht mit biotinylierten Proteoliposomen und Streptavidin-beschichteten Platten konstruiert werden.
Schließlich gibt es zwei wichtige Vorbehalte, die bei der Verwendung dieser Methode berücksichtigt werden sollten. Erstens kann die Bildung von Disulfidbindungen aufgrund der hohen Konzentrationen von DTT im Translationspuffer, die möglicherweise die Struktur einiger Arten von Membranproteinen beeinflussen15, unzureichend sein. Obwohl sich Disulfidbindungen bilden können, nachdem das Reduktionsmittel während des Reinigungsprozesses entfernt wurde, bilden sie sich möglicherweise in einem anderen Typ als den natürlichen. Die andere ist, dass Membranproteine nicht glykosyliert sind. Die für die Glykosylierung benötigten Enzyme fehlen theoretisch im zellfreien System, da während des Prozesses der Herstellung von Weizenkeimextrakt Biomembranen, einschließlich Golgi und ER, entfernt wurden. Da das Fehlen von Disulfidbindungen und Glykosylierung zu unterschiedlichen Konformationen führen kann, sollte das experimentelle Design sorgfältig geprüft und bewertet werden, insbesondere wenn posttranslationale Modifikationen für die funktionelle Expression von Proteinen gemäß den experimentellen Zwecken entscheidend sind.
Offenlegungen
Die Autoren haben nichts offenzulegen.
Danksagungen
Diese Forschung wurde vom Platform Project for Supporting Drug Discovery and Life Science Research (Basis for Supporting Innovative Drug Discovery and Life Science Research (BINDS)) von AMED unter der Fördernummer JP20am0101077 unterstützt. Diese Arbeit wurde auch teilweise durch JSPS KAKENHI Grant Number 20K05709 unterstützt.
Materialien
| Name | Company | Catalog Number | Comments |
| ×3 SDS-PAGE sample buffer | Containing 10% 2-mercaptoethanol | ||
| 5-20% gradient SDS-PAGE gel | ATTO | E-D520L | |
| 70% ethanol | Diluted ethanol by ultrapure water. | ||
| Agarose | Takara Bio | ||
| Ammonium acetate | Nakalai tesque | 02406-95 | As this reagent is deliquescent, dissolve all of it in water once opened and store it at -30°C. |
| Ampicillin Sodium | Nakalai tesque | 02739-74 | |
| Asolectin Liposome, lyophilized | CellFree Sciences | CFS-PLE-ASL | A vial contains 10 mg of lyophilized liposomes. |
| BSA standard | 1000 ng, 500 ng, 250 ng, 125 ng BSA / 10 µL ×1 SDS-PAGE sample buffer | ||
| CBB gel stain | |||
| cDNA clone of interest | Plasmid harboring cDNA clone or synthetic DNA fragment | ||
| Chloroform | Nakalai tesque | 08402-84 | |
| Cooled incubator | Temperature ranging from 0 to 40 °C or wider. | ||
| Creatine kinase | Roche Diagnostics | 04524977190 | |
| Dialysis cup (0.1 mL) | Thermo Fisher Scientific | 69570 | Slide-A-Lyzer MINI Dialysis Device, 10K MWCO, 0.1 mL |
| Dialysis cup (2 mL) | Thermo Fisher Scientific | 88404 | Slide-A-Lyzer MINI Dialysis Device, 10K MWCO, 2 mL |
| DNA ladder marker | Thermo Fisher Scientific | SM0311 | GeneRuler 1 kb DNA Ladder |
| DpnI | Thermo Fisher Scientific | FD1703 | FastDigest DpnI |
| E. coli strain JM109 | |||
| Electrophoresis chamber | ATTO | ||
| Ethanol (99.5%) | Nakalai tesque | 14713-95 | |
| Ethidium bromide | |||
| Evaporation flask, 100 mL | |||
| Gel imager | |||
| Gel scanner | We use document scanner and LED immuninator as a substitute. | ||
| LB broth | |||
| Lipids of interest | Avanti Polar Lipids | ||
| Micro centrifuge | TOMY | MX-307 | |
| NTP mix | CellFree Sciences | CFS-TSC-NTP | Mixture of ATP, GTP, CTP, UTP, at 25 mM each |
| Nuclease-free 25 mL tube | IWAKI | 362-025-MYP | |
| Nucrease-free plastic tubes | Watson bio labs | Do not autoclave. Use them separately from other experiments. | |
| Nucrease-free tips | Watson bio labs | Do not autoclave. Use them separately from other experiments. | |
| PBS buffer | |||
| PCR purification kit | MACHEREY-NAGEL | 740609 | NucleoSpin Gel and PCR Clean-up |
| pEU-E01-MCS vector | CellFree Sciences | CFS-11 | |
| Phenol/chloroform/isoamyl alcohol (25:24:1) | Nippon Gene | 311-90151 | |
| Plasmid prep Midi kit | MACHEREY-NAGEL | 740410 | NucleoBond Xtra Midi |
| Primer 1 | Thermo Fisher Scientific | Custom oligo synthesis | 5’-CCAAGATATCACTAGnnnnnnnnnnnnnnnnnnnnnnnn-3’ Gene specific primer, forward. Upper case shows overlap sequence to be added for seamless cloning. Lower case nnnn…. (20-30 bp) shows gene specific sequence. |
| Primer 2 | Thermo Fisher Scientific | Custom oligo synthesis | 5'-CCATGGGACGTCGACnnnnnnnnnnnnnnnnnnnnnnnn-3’ Gene specific primer, reverse. Upper case shows overlap sequence to be added for seamless cloning. Lower case nnnn…. (20-30 bp) shows gene specific sequence. |
| Primer 3 | Thermo Fisher Scientific | Custom oligo synthesis | 5'-GTCGACGTCCCATGGTTTTGTATAGAAT-3' Forward primer for vector linearization. Underline works as overlap in seamless cloning. |
| Primer 4 | Thermo Fisher Scientific | Custom oligo synthesis | 5'-CTAGTGATATCTTGGTGATGTAGATAGGTG-3' Reverse primer for vector linearization. Underline works as overlap in seamless cloning. |
| Primer 5 | Thermo Fisher Scientific | Custom oligo synthesis | 5’-CAGTAAGCCAGATGCTACAC-3’ Sequencing primer, forward |
| Primer 6 | Thermo Fisher Scientific | Custom oligo synthesis | 5’- CCTGCGCTGGGAAGATAAAC-3’ Sequencing primer, reverse |
| Protein size marker | Bio-Rad | 1610394 | Precision Plus Protein Standard |
| Rotary evaporator | |||
| seamless cloning enzyme mixture | New England BioLabs | E2611L | Gibson Assembly Master Mix Other seamless cloning reagents are also avairable. |
| SP6 RNA Polymerase & RNase Inhibitor | CellFree Sciences | CFS-TSC-ENZ | |
| Submarine Electrophoresis system | |||
| TAE buffer | |||
| Transcription Buffer LM | CellFree Sciences | CFS-TSC-5TB-LM | |
| Translation buffer | CellFree Sciences | CFS-SUB-SGC | SUB-AMIX SGC (×40) stock solution (S1, S2, S3, S4). Prepare ×1 translation buffer before use by mixing stock S1, S2, S3, S4 stock and ultrapure water. |
| Ultrapure water | We recommend to prepare ultrapure water by using ultrapure water production system every time you do experiment. Do not autoclave. We preparaed ultrapure water by using Milli-Q Reference and Elix10 system. Commercially available nuclease-free water (not DEPC-treated water) can be used as a substitute. Take care of contamination after open the bottle. | ||
| Ultrasonic homogenizer | Branson | SONIFIER model 450D-Advanced | Ultrasonic cleaner can be used as a substitute. |
| UV transilluminator | |||
| Vacuum desiccator | |||
| Wheat germ extract | CellFree Sciences | CFS-WGE-7240 | WEPRO7240 |
Referenzen
- Santos, R., et al. A comprehensive map of molecular drug targets. Nature Reviews. Drug Discovery. 16 (1), 19-34 (2017).
- Gusach, A., et al. Beyond structure: emerging approaches to study GPCR dynamics. Current Opinion in Structural Biology. 63, 18-25 (2020).
- Congreve, M., de Graaf, C., Swain, N. A., Tate, C. G. Impact of GPCR Structures on Drug Discovery. Cell. 181 (1), 81-91 (2020).
- Wilkinson, T. C. I. Discovery of functional monoclonal antibodies targeting G-protein-coupled receptors and ion channels. Biochemical Society Transactions. 44 (3), 831-837 (2016).
- Hino, T., Iwata, S., Murata, T. Generation of functional antibodies for mammalian membrane protein crystallography. Current Opinion in Structural Biology. 23 (4), 563-568 (2013).
- Webb, D. R., Handel, T. M., Kretz-Rommel, A., Stevens, R. C. Opportunities for functional selectivity in GPCR antibodies. Biochemical Pharmacology. 85 (2), 147-152 (2013).
- Douthwaite, J. A., Finch, D. K., Mustelin, T., Wilkinson, T. C. I. Development of therapeutic antibodies to G-protein coupled receptors and ion channels: Opportunities, challenges and their therapeutic potential in respiratory diseases. Pharmacology and Therapeutics. 169, 113-123 (2016).
- Hashimoto, Y., Yagi, K., Kondoh, M. Current progress in a second-generation claudin binder, anti-claudin antibody, for clinical applications. Drug Discovery Today. 21 (10), 1711-1718 (2016).
- Hutchings, C. J., Colussi, P., Clark, T. G. Ion channels as therapeutic antibody targets. mAbs. 11 (2), 265-296 (2019).
- Errey, J. C., Fiez-Vandal, C. Production of membrane proteins in industry: The example of GPCRs. Protein Expression and Purification. 169, 105569 (2020).
- Pandey, A., Shin, K., Patterson, R. E., Liu, X. Q., Rainey, J. K. Current strategies for protein production and purification enabling membrane protein structural biology. Biochemistry and Cell Biology. 94 (6), 507-527 (2016).
- Wiseman, D. N., et al. Expression and purification of recombinant G protein-coupled receptors: a review. Protein Expression and Purification. 167, 105524 (2020).
- Jeffery, C. J. Expression, Solubilization, and Purification of Bacterial Membrane Proteins. Current Protocols in Protein Science. 83 (1), 1-15 (2016).
- Spirin, A. S., Baranov, V. I., Ryabova, L. A., Ovodov, S. Y., Alakhov, Y. B. A continuous cell-free translation system capable of producing polypeptides in high yield. Science. 242 (4882), 1162-1164 (1988).
- Takai, K., Sawasaki, T., Endo, Y. Practical cell-free protein synthesis system using purified wheat embryos. Nature Protocols. 5 (2), 227-238 (2010).
- Endo, Y., Sawasaki, T. Cell-free expression systems for eukaryotic protein production. Current Opinion in Biotechnology. 17 (4), 373-380 (2006).
- Shimizu, Y., Kuruma, Y., Ying, B. W., Umekage, S., Ueda, T. Cell-free translation systems for protein engineering. The FEBS Journal. 273 (18), 4133-4140 (2006).
- Klammt, C., et al. Cell-free expression as an emerging technique for the large scale production of integral membrane protein. The FEBS Journal. 273 (18), 4141-4153 (2006).
- Nozawa, A., et al. A cell-free translation and proteoliposome reconstitution system for functional analysis of plant solute transporters. Plant and Cell Physiology. 48 (12), 1815-1820 (2007).
- Nozawa, A., et al. Production and partial purification of membrane proteins using a liposome-supplemented wheat cell-free translation system. BMC Biotechnology. 11 (1), 35-45 (2011).
- Henrich, E., Hein, C., Dotsch, V., Bernhard, F. Membrane protein production in Escherichia coli cell-free lysates. FEBS Letters. 589 (15), 1713-1722 (2015).
- Henrich, E., Peetz, O., et al. Analyzing native membrane protein assembly in nanodiscs by combined non-covalent mass spectrometry and synthetic biology. eLife. 6, 243 (2017).
- Shelby, M. L., He, W., Dang, A. T., Kuhl, T. L., Coleman, M. A. cell-free co-translational approaches for producing mammalian receptors: expanding the cell-free expression toolbox using nanolipoproteins. Frontiers in Pharmacology. 10, 744 (2019).
- Jacobs, M. L., Boyd, M. A., Kamat, N. P. Diblock copolymers enhance folding of a mechanosensitive membrane protein during cell-free expression. Proceedings of the National Academy of Sciences of the United States of America. 116 (10), 4031-4036 (2019).
- Sackin, H., Nanazashvili, M., Makino, S. I. Direct injection of cell-free Kir1.1 protein into Xenopus oocytes replicates single-channel currents derived from Kir1.1 mRNA. Channels. 9 (4), 196-199 (2015).
- Zemella, A., Richter, T., Thoring, L., Kubick, S. A combined cell-free protein synthesis and fluorescence-based approach to investigate GPCR binding properties. Methods in Molecular Biology. 1947 (10), 57-77 (2019).
- Vaish, A., Guo, S., Murray, R. M., Grandsard, P. J., Chen, Q. On-chip membrane protein cell-free expression enables development of a direct binding assay: A curious case of potassium channel KcsA-Kv1.3. Analytical Biochemistry. 556, 70-77 (2018).
- Suzuki, Y., et al. Functional G-Protein-Coupled Receptor (GPCR) synthesis: the pharmacological analysis of Human Histamine H1 Receptor (HRH1) synthesized by a wheat germ cell-free protein synthesis system combined with asolectin glycerosomes. Frontiers in Pharmacology. 9, 38 (2018).
- Cortes, S., Barette, C., Beroud, R., De Waard, M., Schaack, B. Functional characterization of cell-free expressed Kv1.3 channel using a voltage-sensitive fluorescent dye. Protein Expression and Purification. 145, 94-99 (2018).
- Woznicka-Misaila, A., Juillan-Binard, C., Baud, D., Pebay-Peyroula, E., Ravaud, S. Cell-free production, purification and characterization of human mitochondrial ADP/ATP carriers. Protein Expression and Purification. 144, 46-54 (2018).
- Hashimoto, Y., et al. Engineered membrane protein antigens successfully induce antibodies against extracellular regions of claudin-5. Scientific Reports. 8 (1), 8383 (2018).
- Sawasaki, T., et al. A bilayer cell-free protein synthesis system for high-throughput screening of gene products. FEBS Letters. 514 (1), 102-105 (2002).
- Goshima, N., et al. Human protein factory for converting the transcriptome into an in vitro-expressed proteome. Nature Methods. 5 (12), 1011-1017 (2008).
- Nemoto, K., Takemori, N., Seki, M., Shinozaki, K., Sawasaki, T. Members of the plant CRK superfamily are capable of trans- and autophosphorylation of tyrosine residues. The Journal of Biological Chemistry. 290 (27), 16665-16677 (2015).
- Takeda, H., et al. Comparative analysis of human src-family kinase substrate specificity in vitro. Journal of Proteome Research. 9 (11), 5982-5993 (2010).
- Takahashi, H., et al. Establishment of a wheat cell-free synthesized protein array containing 250 human and mouse E3 ubiquitin ligases to identify novel interaction between E3 ligases and substrate proteins. PLoS One. 11 (6), 0156718 (2016).
- Nozawa, A., et al. Construction of a protein library of Arabidopsis transcription factors using a wheat cell-free protein production system and its application for DNA binding analysis. Bioscience, Biotechnology, and Biochemistry. 73 (7), 1661-1664 (2009).
- Goren, M. A., Nozawa, A., Makino, S. I., Wrobel, R. L., Fox, B. G. Cell-free translation of integral membrane proteins into unilamelar liposomes. Methods in Enzymology. 463, 647-673 (2009).
- Nozawa, A., et al. Production and partial purification of membrane proteins using a liposome-supplemented wheat cell-free translation system. BMC Biotechnology. 11 (1), 35 (2011).
- Renauld, S., et al. Functional reconstitution of cell-free synthesized purified Kv channels. Biochimica Et Biophysica Acta. Biomembranes. 1859 (12), 2373-2380 (2017).
- Liu, S., et al. Efficiency and Safety of CRAC Inhibitors in Human Rheumatoid Arthritis Xenograft Models. Journal of Immunology. 199 (5), 1584-1595 (2017).
- Jarecki, B. W., Makino, S. I., Beebe, E. T., Fox, B. G., Chanda, B. Function of shaker potassium channels produced by cell-free translation upon injection into xenopus oocytes. Scientific Reports. 3, 1-7 (2013).
- David, G., et al. Phosphorylation and alternative translation on wheat germ cell-free protein synthesis of the DHBV large envelope protein. Frontiers in Molecular Biosciences. 6, 138 (2019).
- Jirasko, V., et al. Proton-detected solid-state NMR of the cell-free synthesized α-helical transmembrane protein NS4B from hepatitis C virus. Chembiochem: A European Journal of Chemical Biology. 21 (10), 1453-1460 (2020).
- Takeda, H., et al. Production of monoclonal antibodies against GPCR using cell-free synthesized GPCR antigen and biotinylated liposome-based interaction assay. Scientific Reports. 5, 11333 (2015).
- Zhou, W., Takeda, H. Production of immunizing antigen proteoliposome using cell-free protein synthesis system. Methods in Molecular Biology. 1868, 49-67 (2018).
- Hutchings, C. J., Koglin, M., Marshall, F. H. Therapeutic antibodies directed at G protein-coupled receptors. mAbs. 2 (6), 594-606 (2010).
- Raetz, C. R. H., et al. Discovery of new biosynthetic pathways: the lipid A story. Journal of Lipid Research. 50, 103-108 (2009).
- Baldridge, J. R., Crane, R. T. Monophosphoryl lipid A (MPL) formulations for the next generation of vaccines. Methods. 19 (1), 103-107 (1999).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten