Method Article
Клиническое применение трехпортовой лапароскопической резекции при колоректальном раке с экстракцией образцов из естественного отверстия
В этой статье
Резюме
Здесь мы представляем протокол успешного выполнения однохирургической трехпортовой лапароскопической резекции колоректального рака с извлечением образца из естественного отверстия.
Аннотация
Лапароскопическая хирургия с редуцированными портами (RPLS) широко используется для радикальной резекции опухолей желудочно-кишечного тракта. Однохирургическая, трехпортовая, лапароскопическая радикальная резекция при раке сигмовидной кишки или высокой прямой кишки с операцией по извлечению образцов из естественного отверстия (NOSES) имеет преимущество небольшого разреза, быстрого послеоперационного восстановления и короткого пребывания в больнице. Тем не менее, до сих пор существует лишь несколько сообщений о NOSES. В данной статье описаны показания, предоперационная подготовка, хирургические этапы и меры предосторожности при однохирургической, трехпортовой, лапароскопической радикальной резекции сигмовидной кишки и рака прямой кишки, а также интраоперационном сборе образцов через естественное отверстие.
Протокол фокусируется на этапах радикальной диссекции и основных технических моментах резекции и реконструкции. В то же время была творчески усовершенствована процедура фиксации сиденья наковальни путем самовытяжения экстракорпоральной шелковой нити, используемой для фиксации кисетного шва после помещения проксимальной наковальни в брюшную полость. Эта операция позволяет эффективно избежать таких проблем, как недостаточная проксимальная кишечная трубка, стряхивание седла наковальни и слабый кисетный шов во время одной операции. Хирургическое лечение было менее вариативным и простым в выполнении, что позволило эффективно избежать послеоперационного подтекания анастомоза и кровотечения из-за избыточного количества интраоперационной анастомотической ткани. Эта операция может широко пропагандироваться в больницах первичного звена.
Введение
Операция по извлечению образцов с естественным отверстием (NOSES) представляет собой модифицированный подход к открытой хирургии и традиционной лапароскопической хирургии, который основан на лапароскопических или роботизированных методах. К его основным преимуществам относятся более короткая продолжительность пребывания в стационаре, снижение раневых осложнений и послеоперационных болей, более быстрое восстановление функции кишечника, а также лучший косметический и психологический эффект. Во время NOSES операционный образец извлекается из естественного отверстия (прямой кишки или влагалища) без необходимости выполнения вспомогательного разреза в брюшной стенке1. «Экспертный консенсус по NOSES для колоректальных опухолей (издание 2019 г.)» рекомендует NOSES с пятипортовой техникой 2,3.
Omori et al.4 впервые применили лапароскопическую хирургию с редуцированными портами (RPLS) для лечения рака желудка. В 2016 году Kim et al. предположили, что лапароскопическая операция по уменьшению пористости технически осуществима и безопасна для лечения колоректального рака и сопоставима с обычной многопортовой лапароскопической хирургией (ХМЛС) с точки зрения послеоперационной боли5. Oh et al., 2 года спустя, обсудили периоперационные клинические исходы у пациентов с раком сигмовидной кишки, перенесших RPLS и традиционную многопортовую лапароскопическую хирургию (MPLS); Результаты свидетельствуют о том, что однохирургическая, трехпортовая, лапароскопическая радикальная сигмоидэктомия является осуществимым и безопасным хирургическим вариантом для пациентов с благоприятными характеристиками опухоли6. Тем не менее, операции по поводу рака сигмовидной кишки или высокой степени прямой кишки и извлечение образцов с помощью NOSES в основном выполнялись одним главным хирургом без помощи других ассистентов во время интраоперационного разделения.
В настоящее время по NOSES по-прежнему существует всего несколько отчетов. При NOSES размещение и фиксация опорного места, которая в основном зависит от расположения опухоли, метода забора образца и способностей хирурга, может быть сложной задачей. В настоящее время предложен ряд методов фиксации наковальни, в том числе метод фиксированной экструзии, метод обратного прокола, метод перевязки малого барабана и метод ручного шва кисетной нитью. Каждый способ имеет свои уникальные преимущества и недостатки. В этом исследовании ретроспективно проанализированы клинические данные 10 пациентов, перенесших однохирургическую, трехпортовую, лапароскопическую операцию по поводу рака сигмовидной кишки или высокого уровня прямой кишки с помощью NOSES, чтобы изучить безопасность и целесообразность этой операции. Творчески усовершенствован метод самовытягивания и фиксации наружного опорного сиденья, который может быть использован для ручной фиксации кисетного шовного материала после установки седла наковальни. Следуя принципу безопухолевой асептики, можно эффективно избежать риска утечки анастомоза и кровотечения, и эта хирургическая процедура может широко пропагандироваться в больницах первичного звена.
протокол
Все лапароскопические хирургические процедуры и послеоперационное лечение в этом исследовании выполнялись в соответствии с рекомендациями, установленными Комитетом по этике лапароскопических операций Первой филиальной больницы Университета Сунь Ятсена, Китай. Протокол и содержание исследования были разъяснены всем пациентам, и было получено информированное согласие. Данное исследование проводилось под руководством этического комитета больницы.
1. Критерии включения в кейс
- В исследование включены пациенты, у которых была диагностирована аденокарцинома сигмовидной кишки или высокая аденокарцинома прямой кишки (10-15 см от заднего прохода), которым была проведена однохирургическая трехпортовая лапароскопия с NOSES. Примите следующие критерии включения:
- Обеспечьте диагностику сигмовидной кишки или аденокарциномы высокой прямой кишки с помощью предоперационной колоноскопии и патологоанатомических исследований.
- Убедитесь, что расширенная компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) не выявили инвазию опухоли в окружающие ткани или кишечную непроходимость из-за отдаленных метастазов.
- Следите за тем, чтобы окружность опухоли составляла <5 см.
- Убедитесь, что ступень Т имеет значение ≤T4a.
- Убедиться в том, что у пациентов нет серьезных заболеваний органов и они могут переносить хирургическое лечение.
- Убедиться в том, что у пациентов нет чрезмерного ожирения или гипертрофии брыжейки (ИМТ < 35 кг/м2).
- Убедитесь, что пациенты ранее не подвергались операциям на брюшной полости и не имеют спаек тазового дна.
2. Подготовка к операции
- За 3 дня до операции назначают пероральные слабительные и бесшлаковые полужидкие или жидкие пищевые продукты, а также порошок электролита полиэтиленгликоля (137,12 г) для подготовки пациентов к операции на кишечнике.
- Сделайте клизму накануне вечером и рано утром в день операции.
- Поместите пациента в модифицированное положение для литотомии, опустив голову на 15°-20° и наклонив тело на 15° с правой стороны.
3. Хирургическое вмешательство
- Чтобы выполнить введение троакара с тремя отверстиями, сделайте разрез на 10 мм ниже пупка и вставьте 10-миллиметровый троакар. Введите троакар диаметром 12 мм в разрез диаметром 12 мм над линией, соединяющей правый пупок и переднюю верхнюю подвздошную кость. Затем введите 5-миллиметровый троакар в разрез 5 мм над правым плоским пупком. Последние два отверстия считаются рабочими.
- После планового осмотра брюшной полости осмотрите верхнюю брюшную полость печени и диафрагмальную брюшину и проверьте брюшную полость против часовой стрелки. Зондируют локализацию опухоли и прилегающих структур. Используйте иглы для анастомоза, чтобы подвешивать матку (у пациенток) к передней части брюшной стенки, чтобы расширить операционное поле, облегчить операцию одного хирурга и облегчить извлечение образцов через влагалище и введение седла степлера.
- Диссоциируют сигмовидную кишку и ее брыжейку, обычно это делается путем освобождения левой латеральной стороны вперед, или используют медиальную диссоциацию, чтобы обнажить плоскость рассечения между фасциями Тольдта и Героты.
ПРИМЕЧАНИЕ: Однако из-за мезангиальной гипертрофии или отсутствия помощи ассистента полное обнажение операционного поля может быть сложной задачей. Таким образом, в данном исследовании предпочтение отдавалось подходу с латеральным разделением. - Увеличить головное пространство Тольдта и перевязать нижнюю брыжеечную артерию и вену. После освобождения латеральной стороны сигмовидной мезоколоны примите медиальный доступ. Далее брыжейку приподнимают желудочными щипцами, чтобы обнажить брыжеечное соединение, диссоциируя его снизу вверх до тех пор, пока не будет достигнут горизонтальный сегмент двенадцатиперстной кишки, включая диссекцию лимфатических узлов в 253 и 216 группах. Обнажив нижнюю брыжеечную артерию, перевязайте сосуды, чтобы расширить пространство Тольдта до тех пор, пока не дойдете до нижней части поджелудочной железы, а затем перевязайте нижнюю брыжеечную вену в верхнем положении.
- Расширьте пространство Тольдта каудально и свободно вытяните нижний мезангиум вверх. Обратите внимание на движения левой руки: выполните микронаружное вращение кишечных щипцов и потяните проксимальный отдел толстой кишки назад и вверх. Обнажайте гипогастральный нерв, защищая его при соответствующем натяжении. После адекватного отделения брыжейки, в зависимости от расстояния от места опухоли, отделяют брыжейку ниже прямой кишки для иссечения, в результате чего получается голая кишка.
ПРИМЕЧАНИЕ: Поскольку сначала диссоциирует латеральная брыжейка, когда нижняя брыжейка освобождается, сигмовидную кишку можно плавно поднять с помощью желудочных щипцов, правильно обнажив, чтобы показать напряжение. - Чтобы определить степень резекции кишечника, сначала подготовьте шелковую нить длиной 8-10 см in vitro и отметьте положение проксимальной резекции кишечной трубки шелковой нитью по верхнему краю опухоли. Диссоциируют проксимальный отдел кишечника и обнажают его с помощью ультразвукового скальпеля. Используйте эндоскопический степлер для линейного разреза, чтобы последовательно пересечь проксимальный и дистальный концы обнаженной кишечной трубки.
- Установка седла наковальни степлера и извлечение образца
- Убедитесь, что дистальная культя прямой кишки промыта при извлечении образца из прямой кишки. Сделайте надрез дистальной культи прямой кишки и наложите под нее чистую эндоскопическую марлю, чтобы предотвратить загрязнение операционного поля.
- Когда образец будет извлечен из влагалища, попросите ассистента орошать влагалище, а затем ввести кишечную прижимную пластину. Далее делают разрез во влагалище 3-4 см под руководством кишечной прижимной пластины. Многократно дезинфицируйте прямую кишку или влагалище йодофорной марлей.
- Вставьте пакет для образцов в брюшную полость через 12-миллиметровый троакар в качестве защиты во время забора образца, чтобы предотвратить засеивание опухоли или загрязнение прямой кишки или влагалища. Во время этого процесса сначала поместите наковальню скобы, а затем выньте образец, чтобы избежать возможного загрязнения наковальни.
- Наложение швов на стенку влагалища и культю прямой кишки
- Зашить стенку влагалища непосредственно антибактериальным полидиоксаноном 3-0. После того, как культя прямой кишки будет ушита, поднимите нить и снова закройте культю прямой кишки с помощью эндолюминального режущего и закрывающего устройства, чтобы избежать возможности загрязнения и подтекания анастомоза.
- Установка седла степлера в проксимальный отдел кишечника
- Разрежьте проксимальный отдел кишечного канала, увеличьте разрез на 2-3 см и регулярно стерилизуйте его йодофорной марлей. Поместите наковальню и зашить кишечный канал без узлов полиглактином 3-0.
- Кишечный анастомоз и усиленные швы
- Выполняйте рутинный сквозной анастомоз кишечника через задний проход. Введите ручку спускового крючка кольцевого степлера через анальное отверстие, проткните центральное прокалывающее устройство рукоятки спускового крючка степлера, соедините центральный стержень проксимального степлера с ногтевым седлом и поверните стенку кишечника возле проксимального и дистального концов.
- Плотно прижмите гаечный ключ для анастомоза, чтобы завершить разрез и анастомоз.
- Сшить всю окружность анастомоза без узлов 4-0.
- Промойте брюшную полость, установите дренажную трубку и поместите резиновую трубку с левой или правой стороны таза.
Результаты
Ни у одного пациента не было дистальной подвздошной профилактической стомы. Образцы шести пациентов были взяты из прямой кишки, а у четырех – из влагалища. Среднее время операции составило 169,5 ± 35,6 мин, средний объем кровотечения – 40 ± 13,3 мл, среднее время послеоперационного истощения – 43,2 ± 22,1 ч, среднее количество рассеченных лимфатических узлов – 13,1 ± 8,6, среднее время пребывания в стационаре – 13,2 ± 3,6 дня. После операции не возникало подтекания анастомоза или легочных/абдоминальных инфекций. Всего было вскрыто 5,0 ± 4,0 лимфатических узлов в центральной группе и 3,8 ± 2,9 лимфатических узлов в средней группе. Было девять случаев с умеренно дифференцированной аденокарциномой, и ни одного пациента с низкодифференцированной аденокарциномой. Средний размер опухоли составил 3,6 ± 1,3 см (табл. 1).
В этом исследовании введение троакаров при однохирургической трехпортовой лапароскопии было относительно фиксированным, но чрезвычайно важным. Когда расстояние между троакарами было слишком большим, операцию было трудно выполнить (рис. 1А). Для наблюдательного отверстия был выбран 10-миллиметровый троакар, который помещался на пупок или ниже для наблюдения. Размер основного рабочего отверстия составлял 12 мм, а вспомогательного — 5 мм, при этом расстояние между двумя отверстиями в идеале должно было равняться размеру кулака. Главный хирург стоял с правой стороны пациента, держатель зеркала — с правой стороны головы пациента, а медсестра с инструментальной медсестрой — с левой стороны пациента (рис. 1B).
Учитывая ограничения лапароскопической операции с одним хирургом, тремя портами и радикализм лечения, основной спор заключается в том, может ли оно соответствовать требованиям радикального лечения. Адекватная резекция кишечника и полное удаление лимфатических узлов являются основными требованиями для радикальной операции (рис. 2А, Б); Мы считаем, что диссекция лимфатических узлов не представляет сложности при однохирургической, трехпортовой, лапароскопической радикальной резекции при раке сигмовидной кишки или высокой степени прямой кишки. Основываясь на изображениях и видео, мы пришли к следующему выводу: (1) диссекция лимфатических узлов была технически осуществима, и хирурги, владеющие лапароскопическими методами, могли легко рассекать лимфатические узлы в анатомических группах 216 и 253, даже на поверхности важных кровеносных сосудов. Рисунок 3 также говорит о том, что эта лапароскопическая процедура соответствовала критериям диссекции лимфатических узлов; (2) Лимфатические узлы в группах 216 и 253 были рассечены над брюшной аортой. С помощью миорелаксантов, правильного положения тела и использования марли они подвергались воздействию даже при однократной манипулятивной процедуре.
Однохирургическая, трехпортовая, лапароскопическая процедура имеет некоторые ограничения, в том числе отсутствие ассистентов и напряжение. Кроме того, неясно, может ли он обеспечить приоритизацию анатомического слоя мембраны или защитить функцию нерва. Хирург в этом исследовании следовал принципу приоритета слоев в обычной многопортовой лапароскопической хирургии (ХМЛС) и проводил операцию с помощью ассистентов. Однако из-за отсутствия помощи ассистентов и недостаточной натяжения при однохирургической, трехпортовой, лапароскопической операции приоритет был отдан латеральному (левому) доступу. Соединение между левой брыжейкой и брюшной стенкой сигмовидной кишки сначала отделяли, а марлю помещали на внешнюю сторону мочеточника в качестве ориентира после ее обнажения (рис. 3А). После этого медиальный и латеральный доступы были использованы для открытия пространства Тольдта и обнажения мочеточника (рис. 3B). Во время этого процесса адгезия или соединение между сигмовидной кишкой и тазовой боковой стенкой преимущественно высвобождались, что снижало трудность распознавания сигмовидной брыжейки, особенно у пациентов с ожирением. При использовании медиального доступа избыточный мезоколон сигмовидной кишки может опускаться, что затрудняет манипуляции со слоями.
Защита нервной функции находится в центре внимания хирургических операций при лечении пациентов с раком сигмовидной кишки или прямой кишки (рис. 4A). Под четким лапароскопическим обзором оператор поднимает проксимальную кишечную трубку как можно выше, чтобы расширить натяжение, рационально используя левосторонние лапароскопические кишечные щипцы, тем самым защищая гипогастральный нерв.
Армирование анастомоза является ключевым шагом в уменьшении утечки анастомоза. При традиционной пятипортовой лапароскопической хирургии хирурги выполняли только профилактические свищи у пациентов с низким и сверхнизким уровнем рака прямой кишки. Анастомозная стома, как правило, усиливалась у пациентов с раком сигмовидной кишки и высокой степенью рака прямой кишки (рис. 4B). «Рог» правого дистального отдела кишечника мог быть внедрен при наложении переднего анастомоза. Основное подтекание анастомоза в основном происходило за анастомотической стомой. Операция с тремя отверстиями, выполненная одним хирургом, также включала в себя усиление швов на передней и задней сторонах анастомотической стомы, что эффективно предотвращало утечку анастомоза (Рисунок 5).
Размещение и фиксация опорного места было самым сложным моментом в этой лапароскопической операции. Традиционные методы установки и фиксации включают фиксированную экструзию, обратную пункцию, перевязку малого барабана и ручной кисетный шов. Метод обратной пункции был относительно прост в обычной лапароскопической операции с пятью отверстиями, но также было возможно, что седло наковальни соскользнет в проксимальный отдел кишечной трубки, и будет трудно отодвинуть прокол назад. То же самое происходило и при операции с тремя отверстиями, проводимой одним хирургом, поэтому хирург выполнял ручной кисетный шв. Однако, поскольку проксимальный отдел кишечной трубки легко поворачивался после разрезания, было трудно сшить и зафиксировать его после установки опорного места. Раньше эта операция занимала много времени. Тем не менее, мы творчески усовершенствовали метод самовытяжения и фиксации наковальни in vitro , который использовался для фиксации швов после установки проксимальной наковальни (рис. 6A, B).
После операции пациент быстро выздоровел, и не было никаких различий в прохождении газов или времени дефекации по сравнению с традиционной процедурой с пятью отверстиями. Во время операции соблюдался принцип бесопухолевой стерильности, и явного увеличения инфекции брюшной полости после операции не наблюдалось. У пациента были только послеоперационные раны брюшной полости на трех отверстиях, как показано на рисунке 7. Поэтому это хирургическое лечение было действительно малоинвазивным.
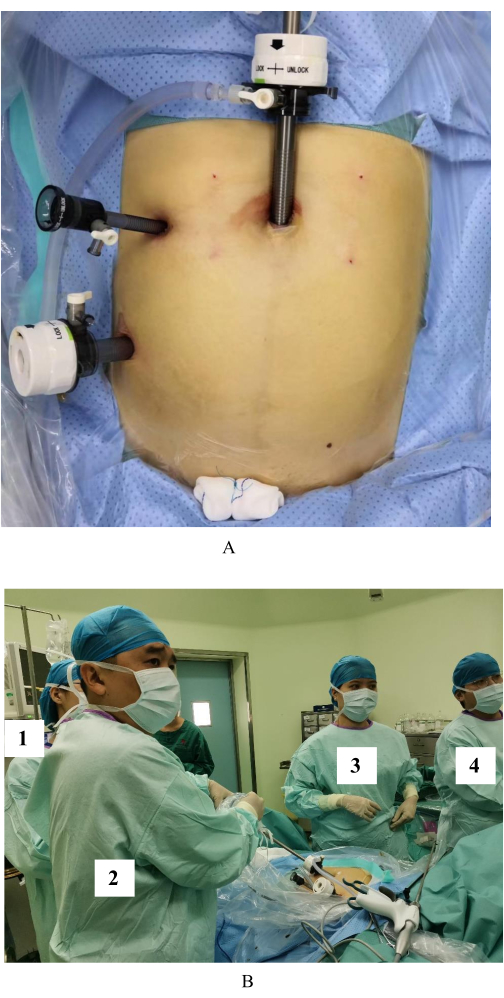
Рисунок 1: Введение троакара с тремя отверстиями и позиции хирургов. (A) Введение троакара с тремя отверстиями. (B) Должности держателя зеркала (1), главного хирурга (2), ассистента и инструментальных медсестер (3, 4). Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.
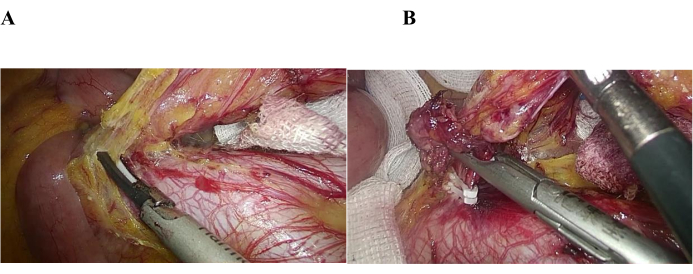
Рисунок 2: Резекция кишечника и лимфатические узлы. А) Диссекция лимфатических узлов в 216 группах. (Б) Перевязка нижней брыжеечной артерии. Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.

Рисунок 3: Расширение пространства Тольдта. (А) Приоритет отдавался латеральному доступу, и мочеточник обнажался. (Б) Медиальные доступы использовались для того, чтобы открыть пространство Тольдта и обнажить мочеточник. Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.

Рисунок 4: Защита нервов и укрепление анастомотической стомы. (А) Защита нервов. (Б) Может быть установлено усиление анастомотической стомы и «рога» правого дистального отдела кишечника. Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.
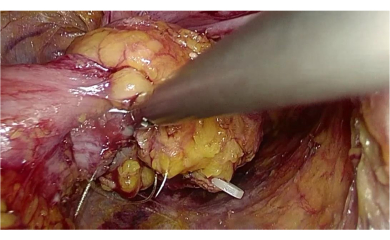
Иллюстрация 5: Армирующий шов на тыльной стороне анастомотической стомы. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
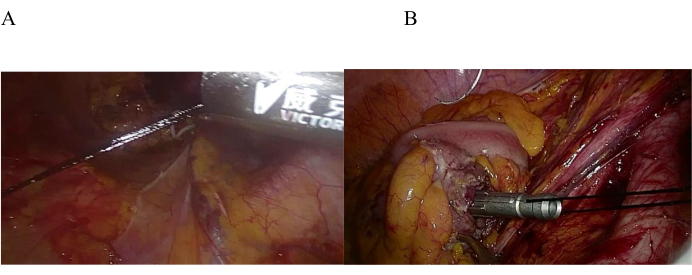
Рисунок 6: Самовытяжение и фиксация наковальни in vitro . (А) Шелковая нить вытягивается через 12-миллиметровый троакар, а проксимальный кишечный канал стабилизируется наружным вытяжением. (B) Шнурок для фиксации седла наковальни после наружного вытяжения шелковой нити in vitro . Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.

Рисунок 7: Рана пациента после операции. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
| Терпеливый | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | ||
| Возраст (год) | 55 | 56 | 69 | 54 | 59 | 59 | 61 | 63 | 60 | 66 | ||
| Пол (ж/м) | F | F | M | F | F | F | F | F | M | F | ||
| Время работы (мин) | 115 | 180 | 150 | 180 | 155 | 250 | 157 | 175 | 145 | 188 | ||
| Пребывание в больнице (дней) | 17 | 15 | 15 | 19 | 8 | 11 | 9 | 13 | 10 | 15 | ||
| Послеоперационное время вытяжки (дней) | 48 | 24 | 24 | 96 | 24 | 24 | 48 | 48 | 48 | 48 | ||
| Объем кровотечения (мл) | 50 | 50 | 50 | 30 | 50 | 20 | 50 | 50 | 20 | 30 | ||
| Подтекание анастомоза | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | ||
| Профилактическая стома подвздошной кишки | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | ||
| Легочные инфекции | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | ||
| Инфекции брюшной полости | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | ||
| лимфатические узлы | 2 | 10 | 5 | 19 | 5 | 29 | 20 | 19 | 8 | 14 | ||
| Центральная группа | 0 | 8 | 0 | 9 | 3 | 10 | 10 | 4 | 5 | 1 | ||
| средняя группа | 1 | 2 | 4 | 4 | 1 | 6 | 6 | 3 | 1 | 10 | ||
| Этап Т | 1 | 2 | 2 | 2 | - | 3 | 3 | 3 | 1 | 3 | ||
| Этап N | 0 | 1 | 0 | 0 | - | 2 | 0 | 0 | 0 | 0 | ||
| Положительная маржа | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | Нет | ||
| Дифференцированная степень | M | M | M | M | W | M | M | M | M | M | ||
| Размер опухоли (см) | - | - | 2 | 3.8 | 3 | 4.4 | 4 | 5 | 1.5 | 4.8 | ||
| Извлечение образцов (R/V) | R | R | R | R | R | V | V | V | R | V | ||
| Локализация опухоли (S/R) | S | R | R | S | S | S | S | S | R | R | ||
Таблица 1: Клинико-патологоанатомические данные пациентов. Сокращения: F = женский; M = мужчина; Дифференцированная степень: W = хорошо дифференцированная; M = умеренно дифференцированный; P = слабо дифференцированный; Извлечение образца: R = прямая кишка; V = влагалище; Локализация опухоли: S = сигмовидная кишка; R = прямая кишка.
Обсуждение
С улучшением хирургических навыков и развитием хирургического оборудования, особенно с развитием устройств визуализации, роботизированная хирургия часто считается разумным выбором для сложных процедур, таких как диссекция латеральных тазовых лимфатических узлов7. Лапароскопическая хирургия с уменьшением портов является новой процедурой, характеризующейся уменьшением количества и размера разрезов, что делает операцию менее инвазивной, чем традиционная лапароскопическая хирургия8. В 2016 году Инаки9 предположил, что гастрэктомия может быть завершена лапароскопической операцией по уменьшению пористости. В связи с отсутствием длительного радикального лечебного эффекта при раке желудка, лапароскопическая процедура должна быть тщательно подобрана. Необходимо провести проспективные многоцентровые исследования, чтобы установить, что лапароскопическая операция по уменьшению пористости является настоящей научно обоснованной практикой, которая не только решает косметические проблемы, но и обеспечивает правильный баланс между минимальной инвазивностью и радикальным излечением. Takemasa10 проспективно проанализировала возможность проведения лапароскопии с сужением пор в сочетании с трансвагинальным забором образцов. Предыдущие ретроспективные и проспективные исследования подтвердили, что лапароскопическая операция по уменьшению пористости с улучшенными минимально инвазивными хирургическими навыками осуществима при радикальной резекции опухолей желудочно-кишечного тракта. В настоящем исследовании статистический анализ 10 пациенток (табл. 1) показал, что трансвагинальная экстракция образцов (TVSE) в сочетании с редуцированной порт-хирургией (RPS) при колоректальном раке была осуществима с меньшей послеоперационной болью.
Благодаря относительно фиксированным анатомическим характеристикам сигмовидной кишки и высокой прямой кишки, радикальная операция при опухолях в этих местах может сочетаться с лапароскопической хирургией по уменьшению пористости и забором образцов из естественного отверстия, эффективно избегая дополнительных разрезов брюшной полости. Минимально инвазивная лапароскопическая хирургия может эффективно уменьшить послеоперационную боль и инфекцию, как показано в таблице 1. Пациенты могут быстрее выздоравливать, а функция желудочно-кишечного тракта быстро восстанавливается, тем самым сокращая время пребывания в больнице. Тем не менее, лапароскопическая операция с одним хирургом, трехпортовая, при раке сигмовидной кишки или высокой прямой кишки с NOSES связана с увеличением времени операции и сложностью операции для одного хирурга. Поэтому до сих пор ведутся споры в развитии этой технологии. В настоящее время имеется мало отчетов по этой процедуре; Несмотря на наличие соответствующих видеоматериалов, анализ данных не проводился11. Некоторые специалисты считают, что добавление еще одного-двух троакаров может сформировать хорошее натяжение с помощью помощников, что помогает завершить операцию быстрее, эффективнее и безопаснее. По сравнению с традиционной лапароскопической операцией с пятью портами, время операции и длина разреза при лапароскопической операции по уменьшению пористости короче6.
До сих пор существуют разные мнения относительно этой операции. Во-первых, выбор хирургического подхода зависит от того, ориентирован ли он на приоритет слоя или приоритета кровеносных сосудов, а также от того, использует ли он медиальный или латеральный доступ или комбинацию этих двух подходов. В этом исследовании хирург сначала использовал латеральный (левый) доступ, чтобы облегчить расширение заднего пространства Тольдта при операции одним человеком, отдавая предпочтение хирургической идее с приоритетом слоев.
Из-за ограничений операции с тремя отверстиями, проводимой одним хирургом, остается неясным, была ли радикальная резекция и диссекция лимфатических узлов достаточными. Мы обнаружили, что для успешного рассечения лимфатических узлов может потребоваться применение миорелаксантов и лапароскопических щипцов кишечника с большим отверстием и умелое использование марли.
Поскольку операция подходила для лечения рака сигмовидной кишки и высокой степени рака прямой кишки, остается неясным, есть ли необходимость в рутинном армировании и наложении швов после анастомоза. Мы считаем, что все анастомозы должны быть усилены. Таким образом, мы предлагаем перенять навыки принуждения, в том числе применить лапароскопическое зеркало и выполнить армирование справа налево. Армирование и наложение швов после анастомоза было предложено многими специалистами. Сложность этой операции заключается в обработке левого «рога» и заднего усиления и сшивания. Наш принцип заключался в том, чтобы шить серозу или брыжейку, насколько это возможно, поэтому не было необходимости накладывать швы на серозу. Этот опыт выдержал испытание и в клинической практике.
Принцип безопухолевой асептики был в центре споров, когда продвигалась операция NOSES. Основываясь на нашем опыте, мы предлагаем следующее: (1) предоперационная подготовка должна быть достаточной для уменьшения остаточного содержимого кишечника; (2) лучше увеличить частоту использования линейных режущих и укупорочных устройств и уменьшить количество обнажений кишечника; (3) строгие хирургические показания, особенно для пациентов со слишком большими опухолями и гипертрофическим мезангием, когда взятие образцов может легко привести к имплантации опухоли.
Постановка и фиксация скоб наковальни являются сложными процедурами и спорными моментами этой операции, так как не было помощника, который помог бы зафиксировать кишечник. Кроме того, операции могут легко вызвать внутрибрюшное загрязнение после проксимального разреза кишечника.
Кроме того, когда наковальня для скоб была помещена в брюшную полость, поворот наковальни мог легко привести к плохому шву или неполному обнажению наковальни, чрезмерному содержимому скобы во время анастомоза, кровотечению и даже свищу. В ранней практике использование метода обратной пункции для размещения кишечника могло привести к возможности соскальзывания седла наковальни в проксимальный отдел кишечника, и было нелегко вытолкнуть седло наковальни за одну операцию. Кроме того, одному человеку было сложно управлять и фиксировать наковальню при одновременной резке. Изучив литературу и изучив видеоролики, на которых показаны операции других специалистов, мы внесли некоторые улучшения, привязав шелковую нить No 4 к головному концу наковальни, прежде чем поместить ее в брюшную полость. При наложении швов кишечника нить должна была быть выдернута из 12-миллиметрового троакара и поднята ассистентом, чтобы зафиксировать место наковальни и кишечник, что было полезно для ушивания кишечника. Следует выполнить шов кисета на всю толщину вокруг скобовой наковальни. Несмотря на то, что этот метод редко применяется в современных клинических операциях, он не сложен в исполнении и может широко пропагандироваться в больницах первичного звена.
Эта операция также имеет определенные ограничения. Пациентам с ожирением, избыточной брыжейкой, отеком кишечника, большой опухолью и наружной опухолевой инвазией эта операция не подходит. Кроме того, как упоминалосьранее, до сих пор существуют такие проблемы, как хирургическая целесообразность, эффективность опухоли, а также подготовка и образование в области лапароскопической хирургии по уменьшению пористости при злокачественных опухолях. Как и в случае с роботизированной панкреатодуоденэктомией (РПД), наиболее сложной панкреатодуоденэктомией, требуется построение кривой обучения и установление подробных правил12. Таким образом, выполнение однохирургической, трехпортовой, лапароскопической операции с помощью NOSES требует подготовки.
Подводя итог, можно сказать, что после правильного отбора пациентов и завершения длительного обучения, для проведения этой операции подходят хирурги с независимыми лапароскопическими навыками. Этот вид операции позволяет уменьшить травматичность и достичь более малоинвазивного эффекта хирургического лечения. Кроме того, фиксация скоб наковальни путем самовытяжения внешней шелковой нити проста и практична, и может широко применяться в больницах первичного звена.
Раскрытие информации
Авторы не имеют конфликта интересов или финансовых отношений, которые необходимо раскрывать.
Благодарности
Данное исследование проводилось при поддержке Программы исследований и применения ключевых технологий в области медицины и здравоохранения в Гуанчжоу, Китай (Проект No 202206010104).
Материалы
| Name | Company | Catalog Number | Comments |
| antibacterial polydioxanone | Johnson & Johnson | 8622H,SXPP1A403 | |
| Laparoscopic system | STORZ | 26003BA | |
| Ring stapler | Johnson & Johnson | CDH29A | |
| Straight cut closure | Johnson & Johnson | EC45A | |
| Trocar | Johnson & Johnson | B5LT,B11LT,B12LT |
Ссылки
- Wang, X. S. Natural Orifice Specimen Extraction Surgery: Colorectal. , Springer. Berlin. (2018).
- Jiang, Z., Chen, Y., Wang, X. Laparoscopic radical resection of lower rectal cancer through transrectal valgus resection without abdominal incisions. Chinese Journal of Gastrointestinal Surgery. 17 (5), 499-501 (2014).
- Liu, Z., Wang, G., Wang, X. Laparoscopic median radical resection for rectal cancer through the rectum to pull the specimen out of the anus without abdominal incision. Chinese Journal of Colorectal Diseases. 2 (6), 331-332 (2013).
- Omori, T., et al. Transumbilical single-incision laparoscopic distal gastrectomy for early gastric cancer. Surgical Endoscopy. 25 (7), 2400-2404 (2011).
- Song, J. M., et al. Reduced port laparoscopic surgery for colon cancer is safe and feasible in terms of short-term outcomes: comparative study with conventional multiport laparoscopic surgery. Annals of Surgical Treatment and Research. 91 (4), 195-201 (2016).
- Oh, J. R., et al. Clinical outcomes of reduced-port laparoscopic surgery for patients with sigmoid colon cancer: surgery with 1 surgeon and 1 camera operator. Annals of Coloproctology. 34 (6), 292-298 (2018).
- Hu, C., et al. Robot-assisted total mesorectal excision and lateral pelvic lymph node dissection for locally advanced middle-low rectal cancer. Journal of Visualized Experiments. (180), e62919(2022).
- Curcillo, P. G., Podolsky, E. R., King, S. A. The road to reduced port surgery: from single big incisions to single small incisions, and beyond. World Journal of Surgery. 35 (7), 1526-1531 (2011).
- Inaki, N., et al. Reduced port laparoscopic gastrectomy for gastric cancer. Translational Gastroenterology and Hepatology. 1, 38(2016).
- Takahashi, H., et al. Prospective multicenter study of reduced port surgery combined with transvaginal specimen extraction for colorectal cancer resection. Surgery Today. 50 (7), 734-742 (2020).
- Zhou, H., Xu, K., Sun, Q., Wang, Z., Ruan, C. Three-port laparoscopic sigmoidectomy with natural orifice specimen extraction-a video vignette. Colorectal Disease. 22 (11), 1782-1783 (2020).
- Kim, A. C., Rist, R. C., Zureikat, A. H. Technical detail for robot assisted pancreaticoduodenectomy. Journal of Visualized Experiments. (151), e60261(2019).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены