Method Article
单外科医生、三孔腹腔镜切除术自然孔口标本提取治疗结直肠癌的临床应用
摘要
在这里,我们提出了一种通过自然孔口标本提取成功对结直肠癌进行单外科医生、三端口腹腔镜切除术的方案。
摘要
腹腔镜手术(RPLS)已被广泛用于胃肠道肿瘤的根治性切除术。乙状结肠或高位直肠癌采用自然孔口标本提取手术(NOSES)的单外科医生、三孔腹腔镜根治性切除术具有切口小、术后恢复快、住院时间短等优点。然而,关于NOSES的报道仍然很少。本文介绍了乙状结肠和高位直肠癌单外科医生、三孔腹腔镜根治性切除术以及通过自然孔采集术中标本的适应证、术前准备、手术步骤和注意事项。
该协议侧重于根治性解剖的步骤以及切除和重建的主要技术要点。同时,创造性地改进了将近端砧座放入腹腔后,通过体外丝线自牵固定砧座的程序,用于钱包线缝合固定。该手术可有效避免单次手术中近端肠管不足、砧座抖落、钱包缝合不力等问题。手术护理可变性小,易于执行,有效避免了术后吻合口瘘和术中吻合口组织过多导致的出血。这种手术可以在初级医院广泛推广。
引言
自然孔道标本提取手术 (NOSES) 是开放手术和传统腹腔镜手术的改良方法,它依赖于腹腔镜或机器人技术。它的主要优点包括住院时间短、伤口并发症和术后疼痛减少、肠道功能恢复更快以及更好的美容和心理效果。在 NOSES 期间,手术标本从自然孔(直肠或阴道)中取出,而无需在腹壁上进行辅助切口1。《结直肠肿瘤 NOSES 专家共识(2019 年版)》推荐采用五端口技术的 NOSES 2,3。
Omori 等[4 ]首次应用腹腔镜小孔手术 (RPLS) 治疗胃癌。2016 年,Kim 等人提出,缩小孔隙腹腔镜手术治疗结直肠癌在技术上可行且安全,在术后疼痛方面可与传统的多端口腹腔镜手术 (CMLS) 相当5。2 年后,Oh 等人讨论了接受 RPLS 和传统多端口腹腔镜手术 (MPLS) 的乙状结肠癌患者的围手术期临床结果;结果表明,对于肿瘤特征良好的患者,单外科医生、三孔腹腔镜根治性乙状结肠切除术是一种可行且安全的手术选择6。然而,乙状结肠癌或高位直肠癌的手术和通过NOSES提取标本主要由一名主刀医生在术中分离期间进行,没有其他助手的帮助。
目前,关于NOSES的报道仍然很少。在 NOSES 中,砧座的放置和固定主要取决于肿瘤的位置、标本采集方法和外科医生的能力,可能具有挑战性。目前已经提出了多种砧座固定方法,包括固定挤压法、反向穿刺法、圈套结扎法和手动钱包线缝合法。每种方法都有其独特的优点和缺点。本研究回顾性分析了10例接受单外科医生、三孔腹腔镜手术治疗乙状结肠癌或高位直肠癌NOSES的患者的临床资料,探讨该手术的安全性和可行性。创造性地改进了外砧座自牵固定方法,可用于砧座放置后手动进行钱包-绳缝合固定。遵循无肿瘤无菌原理,可以有效避免吻合口瘘和出血的风险,这种手术程序可以在初级医院广泛推广。
研究方案
本研究中的所有腹腔镜手术程序和术后治疗均按照中国中山大学第一附属医院腹腔镜手术伦理委员会制定的指南进行。向所有患者解释研究方案和内容,并获得知情同意。这项研究是在医院伦理委员会的指导下进行的。
1. 案例纳入标准
- 包括被诊断患有乙状结肠或高位直肠腺癌(距肛门 10-15 厘米)的患者,他们在研究中接受了单外科医生、三孔腹腔镜检查和 NOSES。采用以下纳入标准:
- 确保通过术前结肠镜检查和病理检查诊断乙状结肠或高位直肠腺癌。
- 确保增强型计算机断层扫描 (CT) 和磁共振成像 (MRI) 检查不会发现任何肿瘤侵袭周围组织,或由于远处转移导致的肠梗阻。
- 确保肿瘤周长为<5厘米。
- 确保 T 阶段为 ≤T4a。
- 确保患者无重大器官疾病,能耐受手术治疗。
- 确保患者没有过度肥胖或肠系膜肥大(BMI < 35 kg/m2)。
- 确保患者以前没有接受过任何腹部手术,也没有盆底粘连。
2. 手术准备
- 术前3天给予口服泻药和无渣半液体或液体食品和口服复合聚乙二醇电解质粉(137.12g),为患者做好肠道手术准备。
- 在手术前一天晚上和清晨进行灌肠。
- 将患者置于改良的截石姿势,头部降低 15°-20°,身体向右侧倾斜 15°。
3. 外科手术
- 要进行三孔套管针插入,请在脐部下方切一个 10 毫米的切口并插入一个 10 毫米的套管针。将 12 毫米套管针插入连接右脐和髂前上棘的线上方的 12 毫米切口中。接下来,将 5 毫米套管针插入右扁平脐上方的 5 毫米切口中。后两个孔被认为是操作孔。
- 对腹腔进行例行检查后,检查上腹肝和膈肌腹膜,逆时针检查腹腔。探测肿瘤和邻近结构的位置。使用吻合针将子宫(女性患者)悬浮到腹壁前部,以扩大手术范围,辅助单人手术,并便于通过阴道取出标本并插入吻合器座。
- 分离乙状结肠及其肠系膜,通常先松开左侧外侧,或使用内侧解离方法,暴露 Toldt 和 Gerota 筋膜之间的夹层平面。
注意:然而,由于系膜肥大或缺乏助手的帮助,完全暴露手术区域可能具有挑战性。因此,本研究首选横向分离方法。 - 扩大 Toldt 的头腔并结扎肠系膜下动脉和静脉。松开乙状结肠系膜的外侧后,采用内侧入路。接下来,用胃镊抬起肠系膜以暴露肠系膜交界处,将其从下到上解离,直到达到十二指肠的水平段,包括253和216组淋巴结的解剖。暴露肠系膜下动脉后,结扎血管以扩大 Toldt 间隙,直到到达胰腺下部,然后在高位结扎肠系膜下静脉。
- 向尾部扩展 Toldt 的空间,并自由地向上拉下系膜。注意左手的动作:对肠镊进行微外旋,将近端结肠向后和向上拉动。暴露下腹神经,同时在适当的张力下保护它。肠系膜充分分离后,根据与肿瘤部位的距离,将直肠下方的肠系膜分离进行切除,从而形成裸肠。
注意:由于肠系膜外侧首先分离,因此当下肠系膜松开时,可以使用胃镊平稳地提起乙状结肠,适当地暴露以显示张力。 - 要确定肠切除的程度,首先 在体外准备一根8-10厘米长的丝线,并用丝线在肿瘤的上边缘标记肠管近端切除的位置。解离近端肠管并使用超声手术刀将其暴露。使用内窥镜线性切割吻合器依次横切裸肠管的近端和远端。
- 插入订书机砧座并取出试样
- 从直肠中取出标本时,确保冲洗直肠远端残端。切开直肠远端残端,并在其下方放置干净的内窥镜纱布,以防止污染手术区域。
- 当标本从阴道中取出时,让助手冲洗阴道,然后插入肠压板。接下来,在肠压板的引导下,在阴道做一个3-4厘米的切口。用碘磷纱布反复消毒直肠或阴道。
- 通过 12 毫米套管针将标本袋插入腹腔,作为标本取出过程中的保护,以防止肿瘤播种或直肠或阴道污染。在此过程中,先放置订书钉砧,然后取出试样,以免可能污染订书钉砧。
- 阴道壁和直肠残端的缝合
- 用3-0抗菌聚二恶烷酮直接缝合阴道壁。直肠残端缝合后,抬起线,用腔内切割和闭合装置再次闭合直肠残端,以避免污染和吻合口渗漏的可能性。
- 将吻合器座放入近端肠
- 切开近端肠管,扩大2-3厘米的切口,并常规用碘磷纱布消毒。放置一个铁砧,用3-0聚乳糖蛋白缝合肠管,不打结。
- 肠吻合术和加固缝合
- 通过肛门进行常规的端到端肠道吻合术。将环形订书机扳机手柄插入肛门,刺穿订书机扳机手柄的中心穿刺装置,将近端订书机的中心杆连接到钉座上,并在近端和远端附近旋转肠壁。
- 紧紧按吻合口扳手以完成切割和吻合。
- 以 4-0 节的无结模式缝合吻合口的整个圆周。
- 冲洗腹腔,放置引流管,并在骨盆左侧或右侧放置橡胶管。
结果
没有患者有任何远端回肠预防性造口。6例标本取自直肠,4例标本取自阴道。平均手术时间为169.5±35.6 min,平均出血量为40±13.3 mL,术后平均排气时间为43.2±22.1 h,平均淋巴结清扫数为13.1±8.6,平均住院时间为13.2±3.6 d。术后未发生吻合口瘘或肺部/腹部感染。共解剖中央组5.0±4.0淋巴结,中间组3.8±2.9淋巴结。中分化腺癌9例,无低分化腺癌患者。平均肿瘤大小为3.6±1.3厘米(表1)。
在这项研究中,单外科医生三孔腹腔镜检查的套管针的插入相对固定但极其重要。当套管针之间的距离太近时,操作难以执行(图1A)。选择10毫米套管针作为观察孔,并放置在脐部或脐部下方进行观察。主操作孔的尺寸为12 mm,辅助操作孔的尺寸为5 mm,两个孔之间的距离理想为拳头大小。主刀医生站在患者的右侧,镜架站在患者头部的右侧,器械护士站在患者的最左侧(图1B)。
鉴于单外科医生、三孔腹腔镜手术的局限性和治疗的激进性,主要争议在于它是否能满足根治性治疗的要求。充分的肠切除术和完全淋巴结清扫术是根治性手术的基本要求(图2A,B);我们认为,在乙状结肠癌或高位直肠癌的单外科医生、三孔腹腔镜根治性切除术中,淋巴结清扫术并不困难。根据图像和视频,我们得出以下结论:(1)淋巴结清扫术在技术上是可行的,熟练掌握腹腔镜技术的外科医生可以很容易地解剖解剖组216和253的淋巴结,甚至在重要血管的表面。图 3 还表明该腹腔镜手术符合淋巴结清扫标准;(2)第216组和第253组的淋巴结在腹主动脉上方进行解剖。在肌肉松弛剂、适当的身体姿势和纱布使用的帮助下,即使通过一次手法操作,它们也会暴露出来。
单外科医生、三端口腹腔镜手术有一些局限性,包括缺乏助手和紧张。此外,目前尚不清楚它是否能实现膜解剖层的优先化或保护神经功能。本研究中的外科医生遵循传统多端口腹腔镜手术 (CMLS) 中的层优先原则,并在助手的帮助下进行手术。然而,由于缺乏助手的帮助,并且在单外科医生、三孔腹腔镜手术中张力不足,因此优先考虑侧(左)入路。首先分离左侧肠系膜与乙状结肠腹壁之间的连接,并在暴露输尿管后将纱布放置在输尿管外侧作为引导(图3A)。之后,使用内侧和外侧入路打开 Toldt 空间并暴露输尿管(图 3B)。在此过程中,乙状结肠与盆腔侧壁之间的粘连或连接优先释放,降低了识别乙状结肠系膜的难度,尤其是肥胖患者。当使用内侧入路时,过多的乙状结肠系膜可能会下沉,使层操作变得困难。
在治疗乙状结肠癌或直肠癌患者时,保护神经功能是手术的重点(图4A)。在清晰的腹腔镜视野下,操作者合理使用左腹腔镜肠钳,将近端肠管抬得尽可能高,以扩大张力,从而保护下腹神经。
吻合口加固是减少吻合口瘘的关键步骤。在传统的五孔腹腔镜手术中,外科医生只对低位和超低位直肠癌患者进行预防性瘘管治疗。吻合口造口通常在乙状结肠和高位直肠癌患者中得到加强(图4B)。当缝合前吻合口时,右远端肠的"角"可以嵌入。主要吻合口瘘多发生在吻合口造口后方。单外科医生的三孔手术还涉及吻合口前后两侧的加固缝合线,有效防止了吻合口渗漏(图5)。
砧座的放置和固定是这次腹腔镜手术中最困难的一点。传统的放置和固定方法包括固定挤压、反向穿刺、圈套结扎和手动钱包线缝合。在常规的双人五孔腹腔镜手术中,反向穿刺方法相对容易,但也有可能砧座滑入近端肠管,难以将穿刺推回。同样的情况也发生在单外科医生的三孔手术中,因此外科医生进行了手动钱包线缝合。但是,由于近端肠管在切割后容易摆动,因此放置砧座后很难缝合和固定。以前,此操作需要花费大量时间。然而,我们创造性地改进了一种体外砧砧自牵和固定方法,该方法用于放置近端砧后的缝合固定(图6A,B)。
手术后,患者恢复迅速,与传统的五孔手术相比,排气或排便时间没有差异。术中遵循无肿瘤无菌原则,术后腹部感染无明显增加。患者术后3个孔仅腹部有伤口,如 图7所示。因此,这种手术治疗确实是微创的。
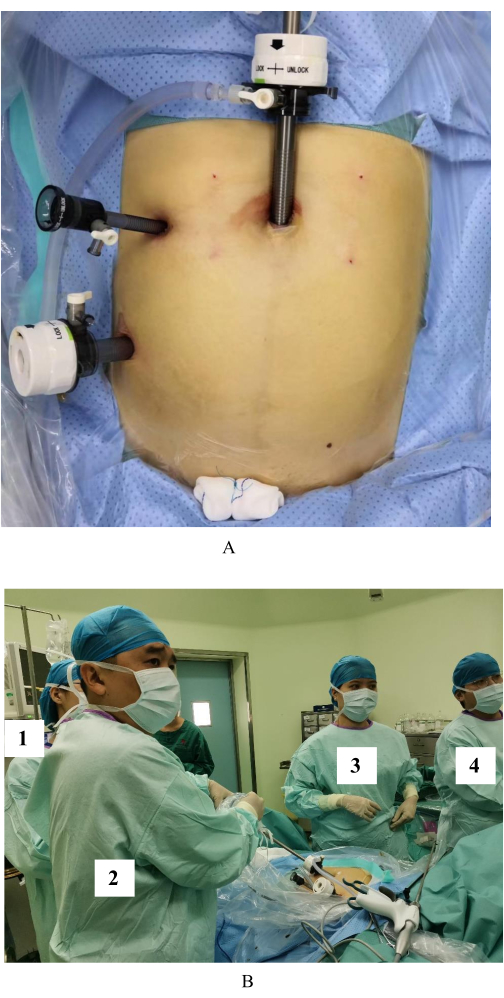
图1:三孔套管针插入和外科医生的位置。 (A) 三孔套管针插入。(B) 镜架 (1)、主刀师 (2)、助理和器械护士 (3、4) 的位置。 请点击这里查看此图的较大版本.
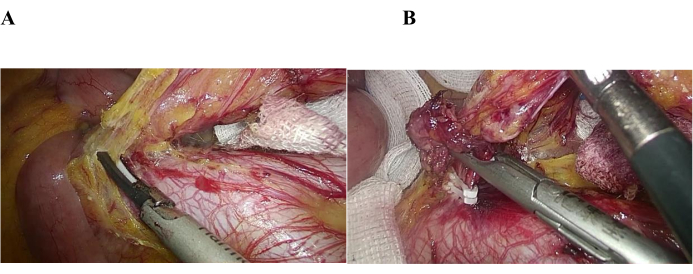
图2:肠切除术和淋巴结清扫术。 (A)淋巴结清扫216组。(B) 肠系膜下动脉结扎术。 请点击这里查看此图的较大版本.

图3:托尔特空间的扩展。 (A) 优先侧向入路,输尿管暴露。(B) 使用内侧入路打开 Toldt 间隙并暴露输尿管。 请点击这里查看此图的较大版本.

图4:吻合口造口的神经保护和强化。 (A) 神经保护。(B) 可以嵌入吻合口和右远端肠的"角"的加固。 请点击这里查看此图的较大版本.
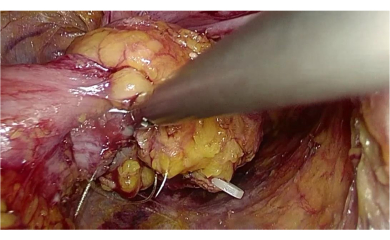
图 5:吻合口造口后侧的加固缝合线。 请点击这里查看此图的较大版本.
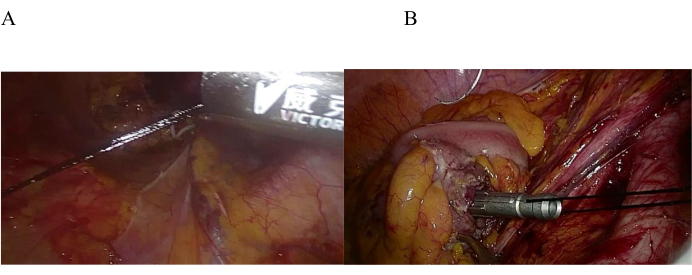
图6: 体外 砧的自牵和固定。 (A)通过12毫米套管针拉出丝线,通过外部牵引稳定近端肠管。(B) 体 外 丝线外牵引后固定砧座的钱包绳。 请点击这里查看此图的较大版本.

图7:患者手术后的伤口。 请点击这里查看此图的较大版本.
| 病人 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | ||
| 年龄(岁) | 55 | 56 | 69 | 54 | 59 | 59 | 61 | 63 | 60 | 66 | ||
| 性别 (F/M) | F | F | M | F | F | F | F | F | M | F | ||
| 操作时间(分钟) | 115 | 180 | 150 | 180 | 155 | 250 | 157 | 175 | 145 | 188 | ||
| 住院时间(天) | 17 | 15 | 15 | 19 | 8 | 11 | 9 | 13 | 10 | 15 | ||
| 术后排气时间(天) | 48 | 24 | 24 | 96 | 24 | 24 | 48 | 48 | 48 | 48 | ||
| 出血量 (mL) | 50 | 50 | 50 | 30 | 50 | 20 | 50 | 50 | 20 | 30 | ||
| 吻合口瘘 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | ||
| 回肠预防性造口 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | ||
| 肺部感染 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | ||
| 腹部感染 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | ||
| 淋巴结 | 2 | 10 | 5 | 19 | 5 | 29 | 20 | 19 | 8 | 14 | ||
| 中央集团 | 0 | 8 | 0 | 9 | 3 | 10 | 10 | 4 | 5 | 1 | ||
| 中间组 | 1 | 2 | 4 | 4 | 1 | 6 | 6 | 3 | 1 | 10 | ||
| T期 | 1 | 2 | 2 | 2 | - | 3 | 3 | 3 | 1 | 3 | ||
| N级 | 0 | 1 | 0 | 0 | - | 2 | 0 | 0 | 0 | 0 | ||
| 正保证金 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | 不 | ||
| 分化程度 | M | M | M | M | W | M | M | M | M | M | ||
| 肿瘤大小(cm) | - | - | 2 | 3.8 | 3 | 4.4 | 4 | 5 | 1.5 | 4.8 | ||
| 标本提取 (R/V) | R | R | R | R | R | V | V | V | R | V | ||
| 肿瘤位置 (S/R) | S | R | R | S | S | S | S | S | R | R | ||
表1:患者的临床病理数据。 缩写:F = 女性;M = 男性;分化程度:W =分化良好;M = 中度分化;P = 低分化;标本提取:R = 直肠;V = 阴道;肿瘤位置:S = 乙状结肠;R = 直肠。
讨论
随着手术技术的提高和手术设备的进步,特别是可视化设备的发展,机器人手术通常被认为是复杂手术的合理选择,例如盆腔外侧淋巴结清扫术7。腹腔镜手术是一种新兴的手术,其特点是切口数量和尺寸减少,使手术比传统的腹腔镜手术侵入性更小8。2016 年,Inaki9 提出胃切除术可以通过减少孔隙率的腹腔镜手术完成。由于缺乏对胃癌的长期根治效果,腹腔镜手术应慎重选择。应进行前瞻性多中心研究,将减少孔隙率腹腔镜手术确立为一种真正的循证实践,这不仅可以解决美容问题,还可以在微创和根治性之间取得适当的平衡。Takemasa10 前瞻性分析了缩孔腹腔镜结合经阴道标本采集的可行性。先前的回顾性和前瞻性研究已经证实,具有改进的微创手术技能的孔隙缩小腹腔镜手术在胃肠道肿瘤的根治性切除中是可行的。在本研究中,对 10 例患者的统计分析(表 1)表明,经阴道标本提取 (TVSE) 联合减少输液港手术 (RPS) 治疗结直肠癌是可行的,术后疼痛较小。
由于乙状结肠和高位直肠的解剖学特征相对固定,因此可以结合孔隙缩小腹腔镜手术和自然孔口标本采集对这些部位肿瘤进行根治性手术,有效避免额外的腹部切口。微创腹腔镜手术可有效减轻术后疼痛和感染,如 表1所示。患者可以更快地康复,胃肠功能迅速恢复,从而缩短住院时间。然而,单外科医生、三孔腹腔镜手术治疗乙状结肠或高位直肠癌伴 NOSES 与手术时间增加和单外科医生手术难度有关。因此,这项技术的发展仍然存在争议。目前关于这一程序的报告很少;虽然有相关视频,但没有提供数据分析11.有专家认为,在助手的帮助下,多加一两个套管针可以形成良好的张力,有助于更快、更有效、更安全地完成操作。与传统的五孔腹腔镜手术相比,孔隙缩小腹腔镜手术的手术时间和切口长度更短6。
对于这次行动,目前还存在不同意见。首先,手术方法的选择取决于它是侧重于层优先还是血管优先,以及是否采用内侧或外侧方法或这两种方法的组合。在这项研究中,外科医生首先使用侧(左)方法,以促进由一个人操作时后部 Toldt 空间的扩展,支持层优先手术思想。
由于单外科医生三孔手术的局限性,根治性切除术和淋巴结清扫术是否足够尚不清楚。我们发现,成功解剖淋巴结可能需要使用肌肉松弛剂和腹腔镜肠钳,开口大,并熟练使用纱布。
由于该手术适用于乙状结肠癌和高位直肠癌,因此尚不清楚吻合后是否需要常规加固和缝合。我们认为,必须加强所有吻合口。因此,我们建议采用强制技能,包括应用腹腔镜镜和从右侧到左侧进行强化。许多专家已经提出了吻合后的加固和缝合。该手术的难点在于处理左"角"和后部加固和缝合。我们的原则是尽可能缝合浆膜或肠系膜,因此没有必要缝合浆膜。这种经验在临床实践中也经受住了考验。
无肿瘤无菌原则是推广NOSES手术时争议的焦点。根据我们的经验,我们提出以下建议:(1)术前准备应充分减少残留肠内容物;(2)最好增加线性切割闭合装置的使用频率,减少肠道暴露次数;(3)严格的手术指征,特别是对于肿瘤过大、系膜肥厚的患者,采集标本时容易导致肿瘤着床。
订书钉砧的放置和固定是该手术的困难程序和争议点,因为没有助手可以帮助固定肠道。此外,在近端肠切口后,手术很容易造成腹腔内污染。
此外,当将钉砧放置在腹腔中时,钉砧的摆动很容易导致缝合不良或钉砧暴露不完全、吻合时切割内容过多、出血甚至瘘管。在早期的实践中,使用反向穿刺方法放置肠道可能会导致砧座滑入近端肠的可能性,并且不容易通过一次手术将砧座推出。此外,一个人在同时切割铁砧时很难操作和固定。在查阅了文献并研究了其他专家的操作视频后,我们做了一些改进,将 4 号丝线绑在铁砧的头端,然后再将其放入腹腔。缝合肠道时,必须将线从12毫米套管针中拉出,并由助手提起以固定砧座和肠道,这有利于缝合肠道。应在订书钉砧周围进行全层钱包线缝合。虽然这种方法在目前的临床操作中很少应用,但执行起来并不复杂,可以在基层医院广泛推广。
此操作还具有某些限制。肥胖、肠系膜过多、肠水肿、肿瘤大、肿瘤外润的患者不适合本手术。此外,如前所述6,在恶性肿瘤腹腔镜手术的手术可行性、肿瘤有效性、培训和教育方面仍然存在问题。与机器人胰十二指肠切除术 (RPD) 类似,最困难的胰十二指肠切除术需要绘制学习曲线并建立详细的规则12.因此,使用 NOSES 进行单外科医生、三端口腹腔镜手术需要培训。
总之,经过对患者的适当选择和长期学习的完成,具有独立腹腔镜技能的外科医生适合进行这种手术。这种手术可以减少创伤,达到更微创的手术治疗效果。此外,通过外丝线自牵固定订书钉砧,简单实用,可在基层医院广泛开展。
披露声明
作者没有利益冲突或财务关系需要披露。
致谢
该研究得到了中国广州医疗健康关键技术研究与应用计划重点研发项目(项目编号202206010104)的支持。
材料
| Name | Company | Catalog Number | Comments |
| antibacterial polydioxanone | Johnson & Johnson | 8622H,SXPP1A403 | |
| Laparoscopic system | STORZ | 26003BA | |
| Ring stapler | Johnson & Johnson | CDH29A | |
| Straight cut closure | Johnson & Johnson | EC45A | |
| Trocar | Johnson & Johnson | B5LT,B11LT,B12LT |
参考文献
- Wang, X. S. Natural Orifice Specimen Extraction Surgery: Colorectal. , Springer. Berlin. (2018).
- Jiang, Z., Chen, Y., Wang, X. Laparoscopic radical resection of lower rectal cancer through transrectal valgus resection without abdominal incisions. Chinese Journal of Gastrointestinal Surgery. 17 (5), 499-501 (2014).
- Liu, Z., Wang, G., Wang, X. Laparoscopic median radical resection for rectal cancer through the rectum to pull the specimen out of the anus without abdominal incision. Chinese Journal of Colorectal Diseases. 2 (6), 331-332 (2013).
- Omori, T., et al. Transumbilical single-incision laparoscopic distal gastrectomy for early gastric cancer. Surgical Endoscopy. 25 (7), 2400-2404 (2011).
- Song, J. M., et al. Reduced port laparoscopic surgery for colon cancer is safe and feasible in terms of short-term outcomes: comparative study with conventional multiport laparoscopic surgery. Annals of Surgical Treatment and Research. 91 (4), 195-201 (2016).
- Oh, J. R., et al. Clinical outcomes of reduced-port laparoscopic surgery for patients with sigmoid colon cancer: surgery with 1 surgeon and 1 camera operator. Annals of Coloproctology. 34 (6), 292-298 (2018).
- Hu, C., et al. Robot-assisted total mesorectal excision and lateral pelvic lymph node dissection for locally advanced middle-low rectal cancer. Journal of Visualized Experiments. (180), e62919(2022).
- Curcillo, P. G., Podolsky, E. R., King, S. A. The road to reduced port surgery: from single big incisions to single small incisions, and beyond. World Journal of Surgery. 35 (7), 1526-1531 (2011).
- Inaki, N., et al. Reduced port laparoscopic gastrectomy for gastric cancer. Translational Gastroenterology and Hepatology. 1, 38(2016).
- Takahashi, H., et al. Prospective multicenter study of reduced port surgery combined with transvaginal specimen extraction for colorectal cancer resection. Surgery Today. 50 (7), 734-742 (2020).
- Zhou, H., Xu, K., Sun, Q., Wang, Z., Ruan, C. Three-port laparoscopic sigmoidectomy with natural orifice specimen extraction-a video vignette. Colorectal Disease. 22 (11), 1782-1783 (2020).
- Kim, A. C., Rist, R. C., Zureikat, A. H. Technical detail for robot assisted pancreaticoduodenectomy. Journal of Visualized Experiments. (151), e60261(2019).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。