Method Article
Количественная оценка гистонов на глобальном уровне посттрансляционных модификаций в 3D-модели клеточной культуры печеночной ткани
В этой статье
Резюме
Этот протокол описывает, как трехмерная система клеточных культур может быть использована для моделирования, обработки и анализа модификаций хроматина в почти физиологическом состоянии.
Аннотация
Плоские культуры клеток млекопитающих являются широко используемым подходом in vitro для понимания физиологии клеток, но эта система ограничена в моделировании твердых тканей из-за неестественно быстрой репликации клеток. Это особенно сложно при моделировании зрелого хроматина, поскольку быстро реплицирующиеся клетки часто участвуют в репликации ДНК и имеют гетерогенную полиплоидную популяцию. Ниже представлен рабочий процесс для моделирования, обработки и анализа модификаций покоящегося хроматина с использованием трехмерной (3D) системы клеточных культур. Используя этот протокол, клеточные линии гепатоцеллюлярной карциномы выращиваются в виде воспроизводимых 3D-сфероидов в инкубаторе, обеспечивающих активную диффузию питательных веществ и низкие силы сдвига. Лечение бутиратом натрия и сукцинатом натрия индуцировало увеличение ацетилирования гистонов и сукцинилирования соответственно. Повышение уровней ацетилирования гистонов и сукцинилирования связано с более открытым состоянием хроматина. Сфероиды затем собираются для выделения клеточных ядер, из которых извлекаются гистоновые белки для анализа их посттрансляционных модификаций. Анализ гистонов выполняется с помощью жидкостной хроматографии в сочетании с тандемной масс-спектрометрией, за которой следует собственный вычислительный конвейер. Наконец, приведены примеры представления данных для исследования частоты и возникновения комбинаторных гистоновых меток.
Введение
С конца 19века системы клеточных культур использовались в качестве модели для изучения роста и развития клеток вне человеческого организма 1,2. Их использование также было расширено для изучения того, как ткани и органы функционируют как в здоровом, так и в больном контексте 1,3. Суспензионные клетки (например, клетки крови) растут в чашках или колбах Петри плавно и взаимозаменяемо, поскольку они не собираются в трехмерные (3D) структуры in vivo. Клетки, полученные из твердых органов, могут расти как в двумерных (2D), так и в 3D-системах культур. В 2D культуре клетки выращиваются в монослое, который прилипает к плоской поверхности 2,4. Системы 2D-культур клеток характеризуются экспоненциальным ростом и быстрым временем удвоения, обычно от 24 ч до нескольких дней5. Клетки в 3D-системах растут, образуя сложные клеточные взаимодействия, моделирующие тканеподобные конгломераты более тесно, и они характеризуются своей способностью достигать динамического равновесия, где их время удвоения может достигать 1 месяца или дольше5.
В этой статье представлена инновационная методология выращивания 3D-сфероидов во вращающихся системах клеточных культур, которые имитируют пониженную гравитацию6. Это упрощенная производная системы клеточных культур, введенная НАСА в 1990-хгодах 7. Этот подход сводит к минимуму силы сдвига, которые возникают в существующих методах, таких как вращающиеся колбы, и увеличивает сфероидную воспроизводимость6. Кроме того, вращающийся биореактор увеличивает активную диффузию питательных веществ, сводя к минимуму некротическое образование, которое происходит в таких системах, как висячая культура капельных клеток, где обмен средой непрактичен6. Таким образом, клетки растут в основном без помех, что позволяет формировать структурные и физиологические характеристики, связанные с клетками, растущими в ткани. Гепатоциты C3A (HepG2/C3A), культивируемые таким образом, не только имели ультраструктурные органеллы, но и продуцировали количества АТФ, аденилаткиназы, мочевины и холестерина, сопоставимые с уровнями, наблюдаемыми in vivo 1,2. Кроме того, клетки, выращенные в системах 2D и .3D клеточных культур, демонстрируют различные паттерны экспрессии генов8. Анализ экспрессии генов гепатоцитов C3A, выращенных в виде 3D-сфероидов, показал, что эти клетки экспрессируют широкий спектр специфических для печени белков, а также генов, участвующих в ключевых путях, которые регулируют функцию печени8. Предыдущие публикации продемонстрировали различия между протеомами экспоненциально растущих клеток в 2D-культуре и клетками в динамическом равновесии в 3D-сфероидных культурах5. Эти различия включают клеточный метаболизм, который, в свою очередь, влияет на структуру, функцию и физиологию клетки5. Протеом клеток, выращенных в 2D-культуре, был более обогащен белками, участвующими в репликации клеток, в то время как протеом 3D-сфероидов был более обогащен функциональностью печени5.
Более медленная скорость репликации клеток, выращенных в виде 3D-сфероидов, более точно моделирует конкретные явления, связанные с состоянием хроматина и модификациями (например, отсечение гистонов9). Гистоновое обрезание является необратимой посттрансляционной модификацией гистона (PTM), которая вызывает протеолитическое расщепление части N-концевого хвоста гистона. Хотя его биологическая функция все еще обсуждается 10,11,12,13, ясно, что его присутствие в первичных клетках и ткани печени моделируется клетками HepG2 / C3A, выращенными как сфероиды, но не как плоские клетки 9. Это имеет решающее значение, поскольку состояние хроматина и его модификации регулируют считывание ДНК в основном путем модуляции доступности генов и, следовательно, их экспрессии14. Гистоновые ПТМ либо влияют на состояние хроматина напрямую, воздействуя на чистый заряд нуклеосом, где собраны гистоны, либо косвенно, привлекая хроматиновых писателей, читателей и ластиков14. Сотни гистоновых ПТМ были идентифицированы на сегодняшний день15, что подтверждает гипотезу о том, что хроматин содержит «гистоновый код», используемый клеткой для интерпретации ДНК16. Однако идентификация множества комбинацийPTM 15 и открытие того, что комбинации гистоновых PTM часто имеют различные биологические функции от PTM, присутствующих изолированно (например, Fischle, et al.17), подчеркивает, что для расшифровки «гистонового кода» требуется больше работы.
В настоящее время анализ Гистонового ПТМ основан либо на методах, использующих антитела (например, западные блоты, иммунофлуоресценцию или иммунопреципитацию хроматина с последующим секвенированием [ChIP-seq]), либо масс-спектрометрию (МС). Методы, основанные на антителах, обладают высокой чувствительностью и могут предоставить подробную информацию о общегеномной локализации гистоновых меток, но часто ограничены в изучении редких ПТМ или ПТМ, присутствующих в комбинациях 18,19,20. MS больше подходит для высокопроизводительной и непредвзятой идентификации и количественной оценки одиночных и сосуществующих модификаций белков, в частности гистоновых белков 18,19,20. По этим причинам эта и несколько других лабораторий оптимизировали конвейер MS для анализа гистоновых пептидов (снизу вверх MS), интактных гистоновых хвостов (middle-down MS) и полноразмерных гистоновых белков (сверху вниз MS)21,22,23.
Ниже подробно описан рабочий процесс выращивания сфероидов HepG2 / C3A и подготовки их к анализу гистоновых пептидов (снизу вверх MS) с помощью наножидкой хроматографии в сочетании с тандемной масс-спектрометрией (nLC-MS / MS). Выращивали 2D-культуру клеток, и клетки собирали и передавали в биореактор, где они начинали образовывать сфероиды (рисунок 1). После 18 дней в культуре сфероиды обрабатывали бутиратом натрия или сукцинатом натрия для увеличения относительного обилия ацетилирования и сукцинилирования гистонов. Примечательно, что 3D-культуры могут быть обработаны генотоксическими соединениями так же, как и их эквиваленты плоских культур; фактически, последние публикации подчеркивают, что токсикологический ответ клеток в 3D-культуре больше похож на первичные ткани, чем на те, которые находятся в 2D плоской культуре24,25. Затем клетки собирали в определенные моменты времени и проводили ядерную изоляцию. Затем гистоны экстрагировали и дериватизировали пропионовым ангидридом до и после переваривания трипсина в соответствии с протоколом, впервые разработанным Garcia et al.26. Эта процедура генерирует пептиды соответствующего размера для онлайн-разделения с помощью обратнофазной хроматографии (C18) и обнаружения при РС. Наконец, гистоновые пептиды были идентифицированы и количественно определены, а полученные данные были представлены несколькими способами для более полной биологической интерпретации.
протокол
1. Подготовка буферов и реагентов
- Среда роста клеток (для клеток HepG2 / C3A): Добавьте фетальную бычью сыворотку (FBS) (10% v / v), заменимые аминокислоты (1% v / v), добавку L-глутамина (1% v / v) и пенициллин / стрептомицин (0,5% v / v) в модифицированную среду Dulbecco Eagle 's Medium (DMEM, содержащую 4,5 г / л глюкозы). Питательные среды хранят при 4 °C в течение максимум 2 недель.
- 200 мМ раствор бутирата натрия (NaBut): Для приготовления 10 мл повторно суспендируют 220,18 мг NaBut в 10 мл ddH2O. Хранить 1 мл аликвоты при -20 °C. Перед обработкой клеток фильтруют раствор с помощью шприцевого фильтра 0,45 мм и добавляют 1 мл фильтрованного раствора в 9 мл клеточной среды для роста для рабочей концентрации 20 мМ.
- 100 мМ раствор сукцината натрия (NaSuc): Для приготовления 10 мл повторно суспендировать 162,05 мг NaSuc в 10 мл ddH2O. Хранить 1 мл аликвоты при -20 °C. Перед обработкой клеток фильтруют раствор с помощью шприцевого фильтра 0,45 мм и добавляют 1 мл фильтрованного раствора в 9 мл клеточной среды для роста для рабочей концентрации 10 мМ.
- Холодный 0,2 M H2SO4: Для приготовления 1 л добавьте 10 мл концентрированного H2SO4 до 990 мл воды класса ВЭЖХ. Хранить при температуре 4 °C.
- Холодный ацетон + 0,1% соляной кислоты (HCl): Добавьте концентрированный HCl (0,1% v/v) к ацетону. Хранить при температуре 4 °C.
- 100 мМ NH4HCO3 раствор, рН 8,0: Для приготовления 1 л повторно суспендировать 7,91 г NH4HCO3 в 1 л воды класса ВЭЖХ. Хранить 50 мл аликвот при -20 °C.
- 0,1% раствор трифторуксусной кислоты (TFA): Добавьте концентрированный TFA (0,1% v/v) в воду класса HPLC. Хранить при температуре 4 °C.
- 60% ацетонитрил/0,1% раствор TFA: Добавьте ацетонитрил класса ВЭЖХ (60% v/v) в воду класса HPLC. Затем добавьте к этому раствору концентрированный TFA (0,1% v/v). Хранить при температуре 4 °C.
- 2% ацетонитрила класса ВЭЖХ + 0,1% муравьиной кислоты: Добавьте ацетонитрил класса ВЭЖХ (2% v/v) в воду класса HPLC. Затем к этому раствору добавляют концентрированную муравьиную кислоту (0,1% v/v).
- 80% ацетонитрила класса ВЭЖХ + 0,1% муравьиной кислоты: Добавьте ацетонитрил класса ВЭЖХ (80% v/v) в воду класса HPLC. Затем к этому раствору добавляют концентрированную муравьиную кислоту (0,1% v/v).
2. Подготовка системы 3D культуры
ПРИМЕЧАНИЕ: Разные клетки, первичные или увековеченные, обладают разными культуральными свойствами, поэтому образование сфероидов может отличаться в зависимости от типов клеток. Этот протокол был создан для формирования сфероидов HepG2/C3A с использованием биореакторов и инновационной системы 3D-культур клеток.
- Используя стандартные питательные среды, выращивайте клетки в виде монослоя до тех пор, пока они не станут на 80% сливающимися.
- Промыть клетки HBSS (5 мл для колбы 75см2 ) и инкубировать клетки с 5 мл 0,05% трипсина-ЭДТА, разведенными в HBSS (разведение 1:2) в течение 5 мин при 37oCс 5% CO2.
- Проверьте отслоение клеток под микроскопом и нейтрализуйте трипсин, добавив 3 мл фетальной бычьей сыворотки (FBS) или питательных сред (содержащих 5%-10% FBS).
- Подсчитайте количество клеток и разбавьте клеточную суспензию до получения 1 х 106 клеток в максимальном объеме 1,5 мл.
- Уравновешивайте сверхнизкую насадочную 24-луночную круглодонную пластину (содержащую несколько микроскважин на скважину) путем промывки скважин 0,5 мл ростовой среды. Центрифугируйте пластину в течение 5 мин при 3000 х г , чтобы удалить пузырьки воздуха с поверхности скважины.
- Переложите клеточную суспензию в пластину и центрифугу в течение 3 мин при 120 х г.
- Инкубируют пластину в течение 24 ч при 37oCс 5% CO2 для образования сфероидов. Между тем, уравновешивайте биореактор, заполняя камеру влажности 25 мл стерильной воды, а клеточную камеру 9 мл питательной среды.
- Инкубируют биореактор, вращающийся в клиностатном инкубаторе, в течение 24 ч при 37oCс 5% CO2.
3. Рост сфероидов в биореакторах
ПРИМЕЧАНИЕ: Для сохранения структуры сфероидов для обработки 3D-структур используются широкие наконечники отверстий.
- Отделите сфероиды от сверхнизкой крепежной пластины, аккуратно пипеткой вверх и вниз с помощью наконечников отверстия шириной 1 мл и перенесите в посуду, обработанную культурой ткани.
- Вымойте тарелку 0,5 мл предварительно подогретой питательной среды и переложите в ту же посуду.
- Оцените качество сфероидов с помощью микроскопии и выберите достаточно сформированные сфероиды. Сфероиды хорошего качества имеют равномерный размер, компактность и округлость.
- Перенос сфероидов в уравновешенные биореакторы, заполненные 5 мл свежих питательных сред. После переноса сфероидов полностью заполните биореактор свежими питательными средами.
- Поместите биореактор в инкубатор клиностата и отрегулируйте скорость вращения до 10-11 об/мин.
- Обменивайтесь питательными средами каждые 2-3 дня, удаляя 10 мл старых носителей и заменяя их 10 мл свежих носителей.
- Отрегулируйте скорость вращения в соответствии с ростом сфероидов, увеличиваясь по мере увеличения размера и количества сфероидов.
- После 18 дней в культуре сфероиды готовы к обработке и/или сбору
4. Обработка и сбор сфероидов
ПРИМЕЧАНИЕ: В этом протоколе сфероиды HepG2/C3A обрабатывают бутиратом натрия (NaBut) и сукцинатом натрия (NaSuc) для оценки уровней гистоновых меток, содержащих ацетилирование и сукцинилирование, соответственно.
- Готовят питательную среду с соответствующей рабочей концентрацией соединения (например, 20 мМ NaBut или 10 мМ NaSuc). Обмен среды в биореакторе с обработанными средами.
ПРИМЕЧАНИЕ: Чтобы установить контрольное условие, либо соберите достаточно сфероидов для экспериментов перед добавлением обработки, либо назначьте биореактор для необработанных сфероидов. - Соберите сфероиды для протеомного анализа после достаточного времени лечения (например, от 48 ч до 1 недели для лечения NaSuc или 48-72 ч для лечения NaBut).
ПРИМЕЧАНИЕ: Для извлечения гистонов с использованием этого протокола было собрано от шести до восьми сфероидов, содержащих приблизительно 1 х 106 клеток.- Удалите 3-5 мл среды из биореактора через верхний порт.
- Откройте передний порт и используйте наконечник отверстия шириной 1 мл, чтобы удалить сфероиды и поместить их в микроцентрифужные трубки.
- Центрифугируйте сфероиды при 100 х г в течение 5 мин и отбрасывайте среду.
ПРИМЕЧАНИЕ: Среда в биореакторе может быть изменена, и биореактор может быть возвращен в инкубатор для дополнительного времени лечения или восстановления. - Промывайте сфероиды 200 мкл HBSS для удаления FBS. Центрифугу при 100 х г в течение 5 мин и удаляют супернатант.
ПРИМЕЧАНИЕ: Сфероиды могут храниться при - 80oCдо обработки.
5. Добыча гистонов
ПРИМЕЧАНИЕ: Многие основные аминокислотные остатки, присутствующие в гистонах, позволяют им тесно взаимодействовать с ДНК, которая имеет основу фосфорной кислоты. Поскольку гистоны являются одними из самых основных белков в ядре, при их извлечении ледяной серной кислотой (0,2 M H2SO4) загрязнение минимально. Негистоновые белки будут выпадать в осадок в сильной кислоте. Высококонцентрированная трихлоруксусная кислота (ТЦА), разбавленная до конечной концентрации 33%, используется впоследствии для осаждения гистонов из серной кислоты. Храните все образцы, трубки и реагенты на льду в течение всей добычи гистонов.
- Добавьте пять объемов (~100 мкл) холодного 0,2 M H2SO4 в ячейку гранулы (~10-20 мкл) и пипетку вверх и вниз, чтобы разрушить гранулу и высвободить гистоны.
- Инкубировать трубки до 4 ч при постоянном вращении или встряхивать при 4oС.
ПРИМЕЧАНИЕ: Для повторно суспендированных образцов, которые имеют объем более 500 мкл, инкубации 2 ч достаточно для извлечения гистонов (более длительная инкубация может привести к экстракции других основных ядерных белков). Для повторно суспендированных образцов с объемом менее 200 мкл требуется инкубация 4 ч для лучшего выхода. - Центрифуга при 3 400 х г в течение 5 мин при 4 °C. Соберите супернатант в новую трубку и выбросьте гранулу позже.
- Добавьте холодный концентрированный TCA таким образом, чтобы он составлял конечные 25%-33% v/v (например, 40-60 мкл холодного TCA: 120 мкл супернатанта) и перемешайте, перевернув трубку несколько раз.
- Инкубировать трубки в течение не менее 1 ч при постоянном вращении или встряхивании при 4oС.
ПРИМЕЧАНИЕ: Для небольших начальных размеров гранул рекомендуется ночная инкубация. - Центрифуга при 3,400 х г в течение 5 мин при 4oС. Откажитесь от супернатанта путем пипетки. Тщательно аспирировать супернатант; не прикасайтесь к боковым сторонам трубки или гранулы.
ПРИМЕЧАНИЕ: Гистоны осаждаются с обеих сторон и дна трубки. Белая нерастворимая гранула, образующаяся в самом низу трубки, содержит в основном негистоновые белки и другие биомолекулы. - Промыть трубку (стенки и гранулу) холодным ацетоном + 0,1% HCl с помощью стеклянной пипетки Пастера (~500 мкл/трубка).
- Центрифуга при 3 400 х г в течение 5 мин при 4oС. Откажитесь от супернатанта, перевернув трубку.
- Промыть трубку (стенки и гранулы) 100% холодным ацетоном с помощью стеклянной пипетки Пастера (~500 мкл/трубка). Центрифуга при 3 400 х г в течение 5 мин при 4oС.
- Выбросьте супернатант, перевернув трубку и вытащив оставшийся ацетон. Откройте крышку и высушите образец на воздухе на скамейке в течение ~20 минут.
- Приступают к пропионилированию или хранят образцы при - 80oСдо начала использования.
6. Первый раунд дериватизации
ПРИМЕЧАНИЕ: Использование трипсина для переваривания гистоновых белков приводит к чрезмерно малым пептидам, которые трудно идентифицировать с помощью традиционных установок протеомики. По этой причине пропионический ангидрид используется для химического дериватизации ɛ-аминогрупп немодифицированных и монометиллизиновых остатков. Это ограничивает протеолиз трипсина С-концевыми остатками аргинина. Для проб в 96-луночных плитах рекомендуется использовать многоканальные пипетки и резервуары для подбора реагентов (рисунок 2А). Дериватизация также проводится после переваривания для маркировки свободных N-терминов пептидов, увеличивающих гидрофобность пептидов и, таким образом, хроматографическое удержание обратной фазы.
- Повторное суспендирование образцов в 20 мкл 15%-20% ацетонитрила в бикарбонате аммония 100 мМ (рН 8,0). Вихрь в течение 15 с, а затем вращение вниз при 1000 x g в течение 30 с.
- Если имеется восемь или более образцов, перенесите каждый повторно суспендированный образец в 96-луночную пластину.
ПРИМЕЧАНИЕ: Если образцы не были перенесены на 96-луночную пластину, на этапах 6.3-6.7, 7.1-7.5 и 8.1-8.5 можно использовать одноканальную пипетку. - Под капот добавьте 2 мкл пропионового ангидрида с помощью многоканальной пипетки. Перемешайте путем пипетки вверх и вниз в 5 раз.
- Быстро добавьте 10 мкл гидроксида аммония с помощью многоканальной пипетки. Перемешайте путем пипетки вверх и вниз в 5 раз.
ПРИМЕЧАНИЕ: Пропионовая кислота является продуктом реакции между пропионовым ангидридом и свободными аминами из пептидов и может снижать рН образца. pH 8 может быть восстановлен путем добавления гидроксида аммония в образец в соотношении 1:5 (v/v). - Убедитесь, что pH равен 8, используя тестовую бумагу pH. Если рН < 8, отрегулируйте, добавив 1 мкл гидроксида аммония. Если pH > 8, отрегулируйте, добавив 1 мкл муравьиной или уксусной кислоты. Когда pH > 10, возможна маркировка других аминокислотных остатков с более высоким pKa.
- Инкубировать при комнатной температуре в течение 10 мин.
- Повторите шаги 6.3–6.6. Двойной раунд пропионилирования гистонов обеспечивает практически полную эффективность реакции.
- Сухая пластина в вакууме со скоростью до полного высыхания всех скважин (~9 ч).
- Приступают к перевариванию трипсина или хранят образцы при - 80oСдо начала употребления.
7. Сбраживание гистонов
ПРИМЕЧАНИЕ: Гистоны перевариваются в пептиды с использованием трипсина, который разрезает на карбоксильной стороне остатки аргинина и лизина. Однако, поскольку пропионилирование модифицирует остатки лизина, расщепляются только остатки аргинина (рисунок 2B).
- Готовят раствор трипсина (25 нг/мкл в 50 мМ NH4HCO3, рН 8,0). Добавьте 20 мкл трипсина (500 нг) к каждому образцу.
- Для приготовления 50 мМ раствора NH4HCO3 разбавьте 100 мМ NH4HCO3 раствор 1:1 в/об водой класса ВЭЖХ.
- Убедитесь, что pH равен 8, используя тестовую бумагу pH. Если рН < 8, отрегулируйте, добавив 1 мкл гидроксида аммония. Если рН > 8, отрегулируйте, добавив 1 мкл муравьиной или уксусной кислоты.
- Переварить при комнатной температуре на ночь или инкубировать при 37oСв течение 6-8 ч.
- Если возможно, проверьте рН после ~ 3 ч пищеварения, так как он мог снизиться. Если рН < 8, отрегулируйте, добавив 1 мкл гидроксида аммония.
- Добавьте дополнительно 5 мкл раствора трипсина 50 нг/мкл (250 нг) и продолжайте пищеварение.
- Приступают ко второму раунду пропионилирования или хранят образцы при - 80oСдо начала использования.
8. Дериватизация пептида N-терминов
ПРИМЕЧАНИЕ: Пропионилирование гистоновых пептидов на их N-конце улучшает удержание кратчайших пептидов с помощью жидкостной хроматографии с обратной фазой (например, аминокислот 3-8 гистона H3), поскольку пропионильная группа увеличивает гидрофобность пептидов.
- Под капот добавьте 2 мкл пропионового ангидрида с помощью многоканальной пипетки. Перемешайте путем пипетки вверх и вниз в 5 раз.
- Быстро добавляйте 10 мкл гидроксида аммония с помощью многоканальной пипетки. Перемешайте путем пипетки вверх и вниз в 5 раз.
ПРИМЕЧАНИЕ: Пропионовая кислота является продуктом реакции между пропионовым ангидридом и свободными аминами из пептидов и может снижать рН образца. pH 8 может быть восстановлен путем добавления гидроксида аммония в образец в соотношении 1:5 (v/v). - Убедитесь, что pH равен 8, используя тестовую бумагу pH. Если рН < 8, отрегулируйте, добавив 1 мкл гидроксида аммония. Если pH > 8, отрегулируйте, добавив 1 мкл муравьиной или уксусной кислоты. Когда pH > 10, возможна маркировка других аминокислотных остатков с более высоким pKa.
- Инкубировать при комнатной температуре в течение 10 мин.
- Повторите шаги 8.1–8.4. Двойной раунд пропионилирования гистонов обеспечивает практически полную эффективность реакции.
- Сухая пластина в вакууме со скоростью до полного высыхания всех скважин (~9 ч).
- Перейдите к этапу обессоливания или сохраните образцы при - 80oCдо использования.
9. Обессоливание и очистка образцов
ПРИМЕЧАНИЕ: Соли, присутствующие в образце, препятствуют масс-спектрометрическому анализу. Соли также ионизируются во время электрораспыления и могут подавлять сигналы от пептидов. Соли могут образовывать ионные аддукты на пептидах, которые заставляют аддуктированный пептид иметь другую массу. Это снижает интенсивность сигнала пептида и препятствует правильной идентификации и количественной оценке. Настройка обессоливания показана на рисунке 2C.
- Начните смешивание смолы HLB (50 мг/мл в 100% ацетонитриле) на магнитной пластине перемешивания.
- Убедитесь, что под 96-луночной полипропиленовой фильтрующей пластиной помещена 96-луночная пластина для сбора потока.
- Добавьте 70 мкл суспензии HLB на лунку к фильтрующей пластине. Осторожно включите вакуум, чтобы предотвратить брызги. Отбросьте сквозной поток.
- Промыть смолу 100 мкл 0,1% TFA. Осторожно включите вакуум, чтобы предотвратить брызги. Отбросьте сквозной поток.
- Повторно суспендировать каждый образец в 100 мкл 0,1% TFA. Проверьте pH; он должен быть ~2-3.
- Загрузите каждый образец в каждую скважину. Осторожно включите пылесос, чтобы предотвратить брызги. Отбросьте сквозной поток.
- Промыть со 100 мкл 0,1% TFA. Осторожно включите пылесос, чтобы предотвратить брызги. Отбросьте сквозной поток.
- Замените коллекционную пластину новой коллекционной пластиной из 96 скважин.
- Добавьте 60 мкл 60% ацетонитрила/0,1% TFA на лунку. Осторожно включите пылесос, чтобы предотвратить брызги. Соберите сквозной поток и высушите в вакууме со скоростью.
- Перейдите к LC-MS/MS или храните образцы при -80 oCдо использования.
10. Анализ гистоновых пептидов с помощью жидкостной хроматографии в сочетании с масс-спектрометрией
- Подготовьте подвижные фазы к работе на высокоэффективной жидкостной хроматографии (ВЭЖХ). Подвижная фаза А (MPA): 2% ацетонитрила класса ВЭЖХ + 0,1% муравьиной кислоты. Мобильная фаза B (MPB): 80% ацетонитрила класса ВЭЖХ + 0,1% муравьиной кислоты.
- Программируйте метод ВЭЖХ следующим образом: (1) 4%-34% MPB в течение 30 мин; (2) 34%-90% MPB в течение 5 мин; и (3) изократические 90% MPB в течение 5 мин. Используйте следующие рекомендуемые свойства колонки: C18 упаковочный материал 3 мкм, внутренний диаметр 75 мкм, длина 20-25 см. Установите скорость потока 250-300 нл/мин для наноколонок с внутренним диаметром 75 мкм.
- В случае, если ВЭЖХ не запрограммирована на автоматизацию выравнивания колонн перед загрузкой образца, включите (4) 90%-4% MPB в течение 1 мин и (5) изократические 4% MPB в течение 10 мин.
- Запрограммируйте метод получения MS.
- Убедитесь, что прибор выполняет одно полное сканирование MS в начале каждого рабочего цикла. Рекомендуется использовать приборы с высоким разрешением (например, орбитальные аппараты или анализаторы времени пролета) из-за точности массы, которая может быть использована во время извлечения сигнала. Однако приборы с низким разрешением также могут быть использованы, как описано ранее27,28.
- Убедитесь, что за полным сканированием MS следует 16 событий сканирования MS/MS, каждое из которых имеет ширину изоляции 50 м/з, охватывающий диапазон m/z 300-1100. Например, первое сканирование должно изолировать сигналы при 300-350 м/з, второе при 350-400 м/з и т.д. Если возможно, также получите MS/ MS сканирование в высоком разрешении, но достаточно более низкого разрешения по сравнению с полным сканированием MS (из-за меньших масс фрагментов ионов по сравнению с интактными ионами).
- Метод ВЭЖХ будет генерировать хроматографические сигналы с пиковой шириной ~3-40 с; для обеспечения надлежащей количественной оценки сигнала убедитесь, что масс-спектрометр выполняет не менее 10 рабочих циклов на хроматографический пик (т.е. рабочий цикл 3 с или выше).
- При использовании анализатора массы в стиле треппинга (орбитрап, ионная ловушка) убедитесь, что ограничение по времени впрыска ионов установлено равным <200 мс; для других анализаторов (квадрупольный, время пролета) это не проблема из-за их более быстрого времени сканирования. Может потребоваться предварительное испытание.
ПРИМЕЧАНИЕ: Более подробную информацию о методах MS для анализа гистоновых пептидов можно найти в следующих ссылках 27,28,29.
- Повторное суспендирование образца в 10 мКЛ МПА, что соответствует ~1 мкг/мкл переваренного образца гистона. Точное количество загрузки не является критическим (также не тривиальным для оценки), если все образцы в партии загружены с использованием аналогичных разбавлений и объемов.
- Загрузите 1 мкл образца в колонну ВЭЖХ.
- Запустите метод LC-MS/MS, запрограммированный на шагах 10.1-10.3.
11. Анализ данных
- Импортируйте файлы необработанных данных MS в программное обеспечение, предназначенное для интеграции пиковой области.
ПРИМЕЧАНИЕ: EpiProfile 30,31 используется в текущем исследовании и обычно рекомендуется, так как он оптимизирован для надежной экстракции известных гистоновых пептидов в районе пика. Тем не менее, другое свободно доступное программное обеспечение для извлеченной ионной хроматографии, такое как Skyline32,33, подходит. - Рассчитайте относительное содержание данного (не)модифицированного пептида как площадь одного пептида, деленную на общую площадь пептида во всех его модифицированных формах. Программное обеспечение, такое как EpiProfile30,31, уже содержит библиотеки пептидов для извлечения сигнала. В противном случае генерируйте библиотеку интересующих пептидов либо вручную, либо с помощью идентификации пептидов с использованием обычных конвейеров протеомики.
Результаты
В этом протоколе сфероиды HepG2/C3A обрабатывали 20 мМ NaBut и 10 мМ NaSuc, оба из которых влияли на глобальные уровни гистоновых ПТМ (рисунок 3А). Затем гистоновые ПТМ были идентифицированы и количественно определены на уровне одного остатка с помощью сбора MS/MS (рисунок 3B).
Когда образцы запускаются в репликах, статистический анализ может быть выполнен для оценки обогащения изменения складки PTM между образцами, а также воспроизводимости наблюдения. Показанные данные демонстрируют, что пептиды, модифицированные ацетилированием, обогащаются сфероидами, обработанными NaBut по сравнению с контролем (рисунок 3C), в то время как образцы, обработанные NaSuc, имеют более высокое относительное содержание гистоновых пептидов, модифицированных сукцинированием лизина (рисунок 3D). Эти расчеты были выполнены в программе электронных таблиц, как подробно описано в отдельной публикации34. Общее увеличение данной модификации гистонов может быть лучше представлено на радиолокационных графиках, где наблюдение за более высоким глобальным изобилием определенной модификации становится более интуитивным, даже при сохранении подробной информации об анализируемых местах модификации (рисунок 3E, F).
Этот протокол генерирует пептид из аминокислотных остатков гистона H3 9-17, которые включают часто модифицированные остатки K9, S10 и K14. Показанные данные показывают, что лечение NaBut повышает уровни H3K14ac, но только на гистонах, совместно модифицированных с H3K9me2, а не H3K9me3 (рисунок 4A). Частота сосуществования между двумя модификациями может быть представлена более интуитивно в виде кольцевого графа, где узлы представляют отдельные модификации, в то время как толщина соединительных линий представляет частоту сосуществования между двумя PTM (рисунок 4B). Иногда частота сосуществования не затрагивается, но данные, представленные в виде штриховых графиков, могут вводить в заблуждение. Например, данные, представленные на рисунке 4A , указывают на то, что комбинация H3K9me2K14ac более распространена при лечении NaBut, чем при контроле. Это правильно, но данная комбинация является наиболее частой независимо от лечения. На рисунке 4B ясно показано, что H3K9me2K14ac и H3K9me3K14ac являются наиболее частыми комбинаторными паттернами независимо от обработки (толщины линии), но что глобальные уровни H3K14ac (узел) - это то, что действительно меняется в эксперименте.
Этот протокол генерирует пептид из остатков гистона H4 4-17, который включает модифицируемые остатки в положениях K5, K8, K12 и K16 (в основном путем ацетилирования). При сравнении контроля и лечения NaBut можно наблюдать увеличение комбинаций ацетилирования, представляя данные в виде, например, облаков слов (рисунок 4C). Это представление ясно подчеркивает, что немодифицированная версия гистона H4 наиболее распространена в контрольном образце, в то время как сфероиды, обработанные NaBut, обогащаются двумя, тройными и четырехкратно ацетилированными протеоформами гистона H4. Однако облака слов ограничены в отображении точных значений; относительное обилие гистонового кода должно быть развито размером текста, который может быть неточно оценен. Поэтому диаграммы Венна или более современные эквиваленты, такие как представлениеUpSetR 35 , могут быть использованы для демонстрации точной количественной оценки сосуществующих гистоновых ПТМ (рисунок 4D, E). Показанные данные еще раз подчеркивают, что выбранные комбинации ацетилирования на гистоне H4 относительно более распространены при лечении NaBut по сравнению с контролем.
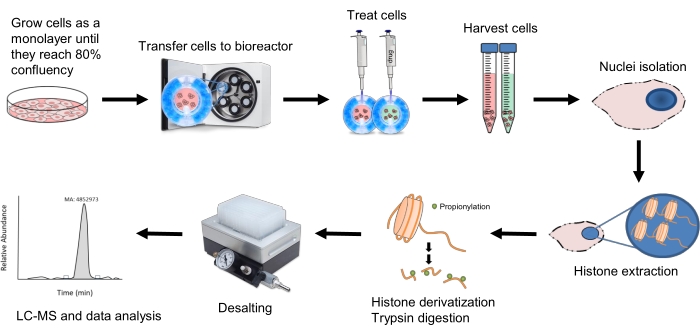
Рисунок 1: Рабочий процесс анализа гистоновых пептидов 3D-сфероидов. Клетки HepG2 /C3A сначала выращивают в 2D-культуре, пока они не достигнут 80% слияния. Затем клетки переносятся в уравновешенный биореактор и помещаются в инкубатор клиностата, где они будут вращаться со скоростью 10-11 оборотов в минуту с образованием сфероидов. Через 18 дней сфероиды обрабатывают либо 20 мМ NaBut, либо 10 мМ NaSuc и собирают после соответствующих им временных точек. Ядра выделяют из клеток и экстракцию гистонов проводят с 0,2 М H2SO4. Затем проводится дериватизация гистонов пропионовым ангидридом до и после переваривания трипсина для обеспечения удержания полученных коротких пептидов с помощью жидкостной хроматографии. Образцы обессоливаются, а затем запускаются с использованием метода LC-MS/MS, упомянутого на шаге 10, и полученные данные анализируются, как описано на шаге 11. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
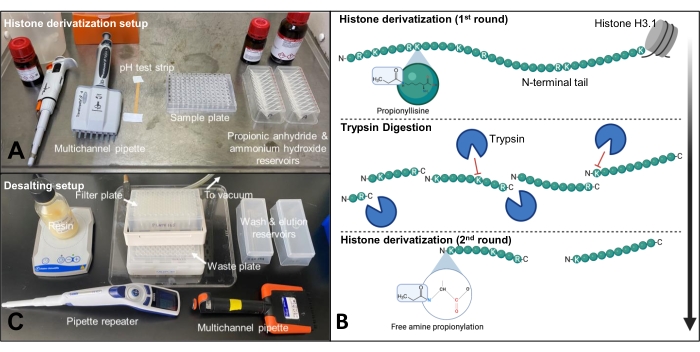
Рисунок 2: Настройка для этапов пропионилирования и обессоливания. (А) Пропионилирование выполняется в вытяжном шкафу, и все компоненты выложены таким образом, чтобы этапы могли быть выполнены в быстрой последовательности. (B) Схема первого раунда пропионилирования, переваривания трипсина и второго раунда пропионилирования на хвосте гистона H3.1. (C) Обессоливание осуществляется на стенде с использованием вакуумного коллектора из 96 скважин и 96-луночной полипропиленовой фильтрующей пластины. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
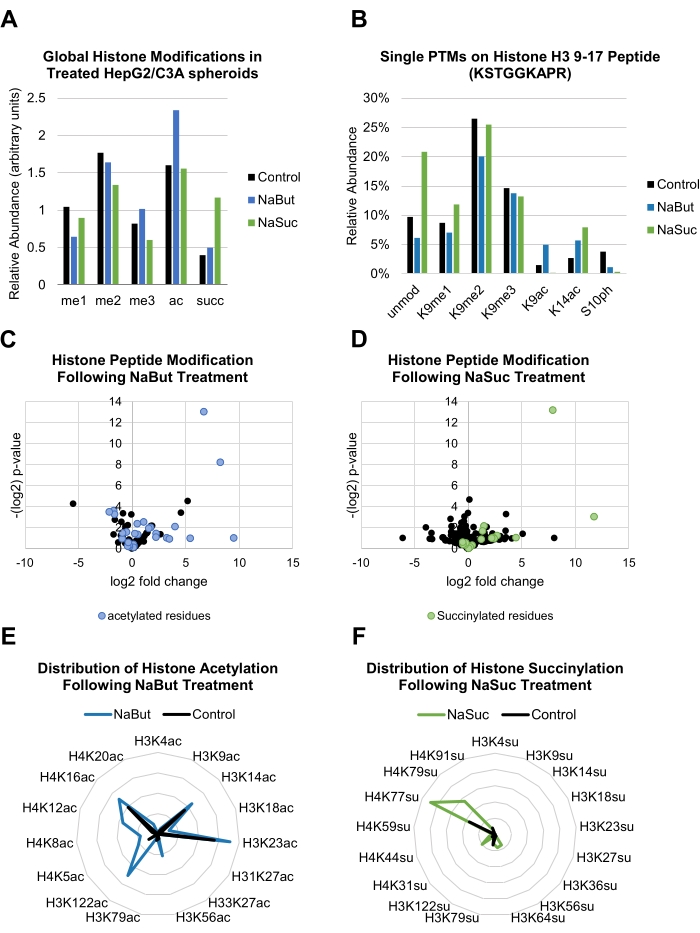
Рисунок 3: Представление отдельных модификаций гистонов. (A) Гистограмма, показывающая относительное обилие общих глобальных модификаций гистонов в контролируемых и обработанных (20 мМ NaBut или 10 мМ NaSuc) сфероидов HepG2/C3A. (B) Гистограмма, показывающая обилие одиночных гистоновых ПТМ, встречающихся на остатках 9-17 пептида гистона H3 (KSTGGKAPR) в контролируемых и обработанных (20 мМ NaBut или 10 мМ NaSuc) сфероидов HepG2/C3A. (С,Г) Вулканические графики, показывающие изменение складки и значимость дифференциальной экспрессии гистоновых пептидных ПТМ после обработки 20 мМ NaBut (C) или 10 мМ NaSuc (D). Выделенные синие и зеленые точки представляют собой ацетилированные и сукцинированные остатки соответственно. (Э,Ф) Радиолокационные графики, показывающие обилие ацетилирования одиночного гистонового пептида (E) или сукцинилирования (F) после обработки 20 мМ NaBut или 10 мМ NaSuc соответственно по сравнению с контролем. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.

Рисунок 4: Представление сосуществующих модификаций гистонов. (A) Гистограмма, показывающая обилие комбинаторных гистоновых ПТМ, встречающихся на остатках 9-17 гистона H3 (KSTGGKAPR) в контроле и обработанных (20 мМ NaBut или 10 мМ NaSuc) сфероидов HepG2/C3A. (B) Кольцевые графики, показывающие взаимосвязь между комбинаторными гистоновыми ПТМ на остатках 9-17 гистона H3 (KSTGGKAPR) в контроле и обработанными (20 мМ NaBut) сфероидами HepG2/C3A. Интенсивность цвета узла соответствует обилию одного ПТМ в его группе обработки, в то время как толщина линии соответствует частоте совместного возникновения ПТМ. (C) Облака слов, показывающие частоту комбинаторных гистоновых ПТМ на остатках гистона H4 в контролируемом и обработанном (20 мМ NaBut) сфероидах HepG2/C3A. Размер текста соответствует обилию заданного комбинаторного ПТМ. (Д,Д) Диаграмма Венна, представляющая частоту сосуществующих модификаций на гистоновых пептидных остатках Н4 4-17 в контрольных и обработанных 20 мМ NaBut образцах. Данные отображаются с помощью ShinyApp UpSetR35. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Дополнительная таблица 1: Список пептидов, обнаруженных с помощью этого протокола. Пожалуйста, нажмите здесь, чтобы загрузить эту таблицу.
Обсуждение
Анализ гистоновых ПТМ принципиально отличается от типичного конвейера анализа протеомики. Большинство гистоновых ПТМ по-прежнему имеют загадочные биологические функции; в результате аннотации, такие как Генная онтология или базы данных путей, недоступны. Существует несколько ресурсов, которые связывают модификации гистонов с ферментом, ответственным за их катализ, или белками, содержащими домены, которые связывают эти ПТМ (например, HISTome36). Кроме того, можно спекулировать на общем состоянии хроматина, когда регулируются глобальные уровни гистоновых ПТМ. Например, общее увеличение ацетилирования гистонов или других ацилирования, таких как сукцинилирование, обычно связано с деконденсацией хроматина37,38.
Анализ РС дает более подробную информацию об этих модификациях, например, их точную локализацию на аминокислотной последовательности. В этом протоколе сбор MS / MS используется для идентификации и количественной оценки гистоновых PTM, которые могут иметь решающее значение для биологической интерпретации. Например, триметилирование на лизине 4 гистона H3 (H3K4me3) обогащается промоторами активно транскрибируемых генов39, в то время как такая же модификация на лизине 9 (H3K9me3) эталонах конститутивного гетерохроматина40. Модификации гистонов в настоящее время используются в качестве биомаркеров при конкретных заболеваниях; таким образом, анализ гистонов может быть использован для изучения патологии заболевания в дополнение к ответу на лечение (например, эпигенетическими препаратами)41,42.
Более сложно визуально представить взаимодействия между несколькими ПТМ, а не с одними ПТМ. Хотя существующие диаграммы, такие как кольцевые графики, могут показывать частоту сосуществования двух PTM, они не могут представлять частоту сосуществования между более чем двумя PTM одновременно, поскольку для этого потребуется трехмерное представление сети. По этой причине другие представления могут быть более подходящими для выделения изменений в гистоновых кодах при рассмотрении трех или более ПТМ. В целом, диверсификация представления данных дает больше шансов наблюдать значительные изменения между выборками. В этом протоколе представлены примеры различных иллюстраций для отображения правил гистоновых ПТМ и сосуществующих ПТМ.
Хотя этот протокол генерирует относительно небольшие гистоновые пептиды из-за переваривания трипсина (примерно 4-20 аминокислот), выбранные пептиды содержат несколько модифицируемых остатков. Анализ этих пептидов позволяет количественно оценить частоты сосуществования ПТМ, что может выявить важную информацию о том, какие комбинаторные гистоновые метки регулируются в данном наборе данных. Примечательно, что во время подготовки образца нет этапов, на которых выполняется количественная оценка гистонов. Для этого есть четыре причины: (1) трипсин обладает широким спектром активности и может использоваться в широком диапазоне соотношений ферментов к образцам (1: 10-1: 200). Даже когда экспериментальный выход экстрагированных гистонов отличается от ожидаемого, проблемы с пищеварением не возникали при использовании этого протокола. (2) Этот протокол предназначен для мельчайших количеств материала, где количественное определение гистонов может быть затруднено из-за отсутствия чувствительности. (3) Используя постоянную концентрацию трипсина независимо от количества гистонового материала, мы можем использовать триптические пептиды (в виде аутолизов трипсина) для сравнения производительности хроматографии. Незначительные изменения в выходе образца будут нормализованы программным обеспечением для анализа данных (этап 11), которое использует все (не)модифицированные сигналы для данного пептида в качестве знаменателя в процессе нормализации. (4) Наконец, резкая недооценка количества исходного материала может создать проблемы перегрузки хроматографической колонки nanoLC. Однако выполнение этапа обессоливания, указанного в этом протоколе, предотвращает возникновение этой проблемы. В случае чрезмерного количества исходного материала (например, >100 мкг) предел мощности обессоливающей смолы будет превышен, и любой избыточный образец будет смыт на этапе загрузки.
Важно отметить, что не все пептиды, обнаруженные в результате этого анализа, были выделены на рисунках 3 и 4. Кроме того, не все модификации гистонов можно обнаружить с помощью этих конкретных методов подготовки и сбора проб. В дополнительной таблице 1 приведен список всех пептидных сигналов, которые извлекаются с помощью описанного конвейера. Несколько известных модификаций в таблице не перечислены, так как описанная пробоподготовка не подходит для их обнаружения. Примечательными примерами являются убиквитинилированные пептиды из гистона H2A и H2B и фосфорилирование гистона H2A. X (общий маркер повреждения ДНК). Это связано с тем, что пропионилирование пептидов, связанных с этими ПТМ, приводит к чрезмерно длинным пептидам, которые не подходят для хроматографии C18 и описанного метода обнаружения РС. Другие модификации, которые присутствуют в литературе, но не присутствуют в Дополнительной таблице 1 , представляют собой модификации очень низкого содержания (в настоящее время они обнаруживаются только с использованием РС после стратегий обогащения, таких как иммунопреципитация или специфическая клеточная обработка), такие как лактилирование43 или серотонилирование44. Модификации гистонов с непредсказуемыми сдвигами массы, вызванными полимеризацией или гетерогенным ковалентным связыванием с гистоновой последовательностью, также не рассматриваются (например, поли-АДФ-рибозилирование45 и гликирование46). Кроме того, этот протокол использует NaSuc и NaBut для лечения сфероидов HepG2 / C3A, но он может быть модифицирован для использования с другими препаратами / эпигенетическими модификаторами и типами 2D / 3D клеточных культур.
Раскрытие информации
У авторов нет конкурирующих финансовых интересов.
Благодарности
Лаборатория Сидоли с благодарностью отмечает Фонд исследований лейкемии (Hollis Brownstein New Investigator Research Grant), AFAR (sagol Network GerOmics award), Deerfield (премия Xseed), Relay Therapeutics, Merck и Офис директора NIH (1S10OD030286-01).
Материалы
| Name | Company | Catalog Number | Comments |
| 0.05% trypsin-EDTA solution | Gibco | 25300054 | |
| 0.5-20 µL pipet tips | BRAND | 13-889-172 (Fisher Scientific) | |
| 1.5 mL microcentrifuge tubes | Bio-Rad | 2239480 | |
| 10 µL multi-channel pipette | BRAND | BR7059000 (Millipore Sigma) | |
| 10 mL syringe | Henke Sass Wolf | 14-817-31 (Fisher Scientific) | Luer lock tip, graduated to 12 mL |
| 10, 20, 200, and 1000 µL single-channel pipettes | Eppendorf | 14-285-904 (Fisher Scientific) | |
| 1000 µL pipet tips | Rainin | 30389164 | |
| 18 G syringe needle | Air-Tite | 14-817-100 (Fisher Scientific) | 3" length, 0.05" diameter |
| 200 µL multi-channel pipette | Corning | 4082 | |
| 2-200 µL pipet tips | BRAND | Z740118 (Millipore Sigma) | |
| 24-well ultra-low attachment microplate | Corning | 07-200-602 | |
| 75 cm2 U-shaped cell culture flask | Corning | 461464U | Untreated, with vent cap |
| 96-well skirted plate | Axygen | PCR-96-FS-C (Corning) | |
| Acetone | Fisher Scientific | A949-1 | Acetone should be used cold |
| Ammonium bicarbonate (NH4HCO3) | Sigma-Aldrich | A6141-25G | |
| Ammonium hydroxide solution | Fisher Scientific | AC423300250 | |
| Cell culture grade water | Corning | 25-055-CV | |
| ClinoReactor | CelVivo | 10004-12 | Bioreactor for 3D cell culture |
| ClinoStar | CelVivo | N/A | Clinostat CO2 incubator for 3D cell culture |
| Control unit | CelVivo | N/A | Tablet for ClinoStar settings |
| Dulbecco's Modified Eagle's Medium (DMEM) | Corning | 17-205-CV | 1X solution with 4.5 g/L glucose and sodium pyruvate, without L-glutamine and phenol red |
| Fetal bovine serum (FBS) | Corning | 35-010-CV | |
| Formic acid | Thermo Scientific | 28905 | |
| Fume hood | Mott | N/A | Model 7121000 |
| Glass Pasteur pipette | Fisher Scientific | 13-678-8B | 9", cotton-plugged, borosilicate glass, non-sterile |
| Glutagro supplement | Corning | 25-015-CI | 200 mM L-ananyl-L-glutamine |
| Hank’s Balanced Salt Solution (HBSS) | Corning | 21-022-CV | 1X solution without calcium, magnesium, and phenol red |
| HPLC grade acetonitrile | Fisher Scientific | A955-4 | |
| HPLC grade water | Fisher Scientific | W6-1 | |
| Hydrochloric acid (HCl) | Fisher Scientific | A481-212 | |
| Ice | N/A | N/A | |
| MEM non-essential amino acids | Corning | 25-025-CI | 100X solution |
| Oasis HLB resin | Waters | 186007549 | Hydrophilic-Lipophilic-Balanced (HLB) Resin with 30µm particle size |
| Orbitrap Fusion Lumos Tribrid mass spectrometer | Thermo Fisher Scientific | IQLAAEGAAPFADBMBHQ | High resolution mass spectrometer |
| Oro-Flex I polypropylene filter plate | Orochem | OF1100 | 96-well polypropylene filter plate w/ 10 µM PE frit |
| Penicillin-Streptomycin | Corning | 30-002-CI | 100X solution |
| pH paper | Hydrion | Z111848 (Sigma-Aldrich) | 0-13 pH test paper |
| Pipette gun | Eppendorf | Z666467 (Millipore Sigma) | |
| Polymicro capillary | Molex | 50-110-7740 (Fisher Scientific) | Flexible fused silica capillary tubing with polymide coating, 75 µM ID x 363 µM OD |
| Polystyrene 10 mL serological pipets, sterile | Fisher Scientific | 1367549 | |
| Propionic anhydride | Sigma-Aldrich | 240311-50G | |
| Refrigerated centrifuge | Thermo Scientific | 75-217-420 | |
| Reprosil-Pur resin | MSWIL | R13.AQ.0003 | 120 Å pore size, C18-AQ phase, 3 µM bead size |
| Rotator | Clay Adams | 25477 (American Laboratory Trading) | Nutator Mixer 1105 |
| Sequencing grade modified trypsin | Promega | V5111 | |
| Sodium butyrate | Thermo Scientific | A11079 | |
| Sodium succinate dibasic | Sigma-Aldrich | 14160-100G | |
| SpeedVac vacuum concentrator (1.5 mL microcentrifuge tubes) | Savant | 20249 (American Laboratory Trading) | |
| SpeedVac vacuum concentrator (96-well) | Thermo Scientific | 15308325 | Savant SPD1010 |
| Sterile hood | Thermo Scientific | 1375 | Class II, Type A2 |
| Sulfuric acid (H2SO4) | Fisher Scientific | 02-004-375 | Baker Analyzed ACS reagent |
| Tissue-culture treated 100 mm x 20 mm dish | Fisher Scientific | 08-772-23 | |
| Trichloroacetic acid (TCA) | Thermo Scientific | AC421451000 | Resuspend 100% w/v in HPLC grade water |
| Trifluoroacetic acid (TFA) | Fisher Scientific | PI28904 | Sequencing grade |
| Vacuum manifold 96-well | Millipore | MAVM0960R | |
| Vortex | Sigma-Aldrich | Z258415 | |
| Water bath | Fisher Scientific | FSGPD10 | |
| Wide bore pipet tips 1000 µL | Axygen | 14-222-703 (Fisher Scientific) | |
| Wide bore pipet tips 200 µL | Axygen | 14-222-730 (Fisher Scientific) |
Ссылки
- Kapalczynska, M., et al. 2D and 3D cell cultures - a comparison of different types of cancer cell cultures. Archives of Medical Science. 14 (4), 910-919 (2018).
- Breslin, S., O'Driscoll, L. Three-dimensional cell culture: the missing link in drug discovery. Drug Discovery Today. 18 (5-6), 240-249 (2013).
- Kim, J. B. Three-dimensional tissue culture models in cancer biology. Seminars in Cancer Biology. 15 (5), 365-377 (2005).
- Duval, K., et al. Modeling physiological events in 2D vs. 3D cell culture. Physiology (Bethesda). 32 (4), 266-277 (2017).
- Wrzesinski, K., et al. The cultural divide: exponential growth in classical 2D and metabolic equilibrium in 3D environments. PLoS One. 9 (9), 106973 (2014).
- Wrzesinski, K., Fey, S. J. Metabolic reprogramming and the recovery of physiological functionality in 3D cultures in micro-bioreactors. Bioengineering (Basel). 5 (1), 22 (2018).
- Gonda, S. R., et al. Three-dimensional transgenic cell model to quantify genotoxic effects of space environment. Advances in Space Research. 27 (2), 421-430 (2001).
- Yamada, K. M., Cukierman, E. Modeling tissue morphogenesis and cancer in 3D. Cell. 130 (4), 601-610 (2007).
- Tvardovskiy, A., et al. Top-down and middle-down protein analysis reveals that intact and clipped human histones differ in post-translational modification patterns. Molecular and Cellular Proteomics. 14 (12), 3142-3153 (2015).
- Azad, G. K., et al. Modifying chromatin by histone tail clipping. Journal of Molecular Biology. 430 (18), 3051-3067 (2018).
- Kragesteen, B. K., Amit, I. Heads or tails: histone tail clipping regulates macrophage activity. Nature Immunology. 22 (6), 678-680 (2021).
- Dhaenens, M. Histone clipping: the punctuation in the histone code. EMBO Reports. 22 (8), 53440 (2021).
- Anderson, L. C., et al. Analyses of histone proteoforms using front-end electron transfer dissociation-enabled orbitrap instruments. Molecular and Cellular Proteomics. 15 (3), 975-988 (2016).
- Morgan, M. A. J., Shilatifard, A. Reevaluating the roles of histone-modifying enzymes and their associated chromatin modifications in transcriptional regulation. Nature Genetics. 52 (12), 1271-1281 (2020).
- Chan, J. C., Maze, I. Nothing is yet set in (hi)stone: novel post-translational modifications regulating chromatin function. Trends in Biochemical Sciences. 45 (10), 829-844 (2020).
- Jenuwein, T., Allis, C. D. Translating the histone code. Science. 293 (5532), 1074-1080 (2001).
- Fischle, W., et al. Molecular basis for the discrimination of repressive methyl-lysine marks in histone H3 by Polycomb and HP1 chromodomains. Genes and Development. 17 (15), 1870-1881 (2003).
- Onder, O., et al. Progress in epigenetic histone modification analysis by mass spectrometry for clinical investigations. Expert Review of Proteomics. 12 (5), 499-517 (2015).
- Sidoli, S., Cheng, L., Jensen, O. N. Proteomics in chromatin biology and epigenetics: Elucidation of post-translational modifications of histone proteins by mass spectrometry. Journal of Proteomics. 75 (12), 3419-3433 (2012).
- Egelhofer, T. A., et al. An assessment of histone-modification antibody quality. Nature Structural and Molecular Biology. 18 (1), 91-93 (2011).
- Moradian, A., et al. The top-down, middle-down, and bottom-up mass spectrometry approaches for characterization of histone variants and their post-translational modifications. Proteomics. 14 (4-5), 489-497 (2014).
- Zheng, Y., Huang, X., Kelleher, N. L. Epiproteomics: quantitative analysis of histone marks and codes by mass spectrometry. Current Opinion in Chemical Biology. 33, 142-150 (2016).
- Sidoli, S., Garcia, B. A. Middle-down proteomics: a still unexploited resource for chromatin biology. Expert Review of Proteomics. 14 (7), 617-626 (2017).
- Stampar, M., et al. Hepatocellular carcinoma (HepG2/C3A) cell-based 3D model for genotoxicity testing of chemicals. Science of the Total Environment. 755, 143255 (2021).
- Calitz, C., et al. Toxicity and anti-prolific properties of Xysmalobium undulatum water extract during short-term exposure to two-dimensional and three-dimensional spheroid cell cultures. Toxicology Mechanisms and Methods. 28 (9), 641-652 (2018).
- Garcia, B. A., et al. Chemical derivatization of histones for facilitated analysis by mass spectrometry. Nature Protocols. 2 (4), 933-938 (2007).
- Sidoli, S., et al. Sequential window acquisition of all theoretical mass spectra (SWATH) analysis for characterization and quantification of histone post-translational modifications. Molecular and Cellular Proteomics. 14 (9), 2420-2428 (2015).
- Sidoli, S., et al. Low resolution data-independent acquisition in an LTQ-orbitrap allows for simplified and fully untargeted analysis of histone modifications. Analytical Chemistry. 87 (22), 11448-11454 (2015).
- Karch, K. R., Sidoli, S., Garcia, B. A. Identification and quantification of histone PTMs using high-resolution mass spectrometry. Methods in Enzymology. 574, 3-29 (2016).
- Yuan, Z. F., et al. EpiProfile quantifies histone peptides with modifications by extracting retention time and intensity in high-resolution mass spectra. Molecular and Cellular Proteomics. 14 (6), 1696-1707 (2015).
- Yuan, Z. F., et al. EpiProfile 2.0: a computational platform for processing epi-proteomics mass spectrometry data. Journal of Proteome Research. 17 (7), 2533-2541 (2018).
- MacLean, B., et al. Skyline: an open source document editor for creating and analyzing targeted proteomics experiments. Bioinformatics. 26 (7), 966-968 (2010).
- Pino, L. K., et al. The Skyline ecosystem: Informatics for quantitative mass spectrometry proteomics. Mass Spectrometry Reviews. 39 (3), 229-244 (2020).
- Aguilan, J. T., Kulej, K., Sidoli, S. Guide for protein fold change and p-value calculation for non-experts in proteomics. Molecular Omics. 16 (6), 573-582 (2020).
- Lex, A., et al. UpSet: Visualization of intersecting sets. IEEE Transactions on Visualization and Computer Graphics. 20 (12), 1983-1992 (2014).
- Shah, S. G., et al. HISTome2: a database of histone proteins, modifiers for multiple organisms and epidrugs. Epigenetics and Chromatin. 13 (1), 31 (2020).
- Xie, Z., et al. Lysine succinylation and lysine malonylation in histones. Molecular and Cellular Proteomics. 11 (5), 100-107 (2012).
- Liu, J., et al. Histone succinylation and its function on the nucleosome. Journal of Cellular and Molecular Medicine. 25 (15), 7101-7109 (2021).
- Howe, F. S., et al. Is H3K4me3 instructive for transcription activation. Bioessays. 39 (1), 1-12 (2017).
- Nicetto, D., Zaret, K. S. Role of H3K9me3 heterochromatin in cell identity establishment and maintenance. Current Opinion in Genetics and Development. 55, 1-10 (2019).
- Wojcik, J. B., et al. Histone H3K27 dimethyl loss is highly specific for malignant peripheral nerve sheath tumor and distinguishes true PRC2 loss from isolated H3K27 trimethyl loss. Modern Pathology. 32 (10), 1434-1446 (2019).
- Sellers, W. R., et al. Next-generation characterization of the cancer cell line encyclopedia. Nature. 569 (7757), 503-508 (2019).
- Zhang, D., et al. Metabolic regulation of gene expression by histone lactylation. Nature. 574 (7779), 575-580 (2019).
- Farrelly, L. A., et al. Histone serotonylation is a permissive modification that enhances TFIID binding to H3K4me3. Nature. 567 (7749), 535-539 (2019).
- Chen, Q., et al. ADP-ribosylation of histone variant H2AX promotes base excision repair. The EMBO Journal. 40 (2), 104542 (2021).
- Zheng, Q., et al. Reversible histone glycation is associated with disease-related changes in chromatin architecture. Nature Communications. 10 (1), 1289 (2019).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены