Method Article
Стабильные водные суспензии ферритовых кластеров марганца с настраиваемым наноразмерным размером и составом
В этой статье
Резюме
Мы сообщаем о гидротермальном синтезе ферритовых кластеров марганца (MFC) в одном горшке, который предлагает независимый контроль над размерами и составом материала. Магнитная сепарация обеспечивает быструю очистку, в то время как функционализация поверхности с использованием сульфированных полимеров гарантирует, что материалы не агрегируются в биологически значимой среде. Полученные продукты хорошо позиционируются для биомедицинских применений.
Аннотация
Марганцевые ферритовые кластеры (MFC) представляют собой сферические сборки от десятков до сотен первичных нанокристаллов, магнитные свойства которых ценны в различных приложениях. Здесь описано, как сформировать эти материалы в гидротермальном процессе, позволяющем самостоятельно контролировать размер кластера продуктов (от 30 до 120 нм) и содержание марганца в полученном материале. Такие параметры, как общее количество воды, добавляемой в спиртовую реакционную среду, и отношение марганца к предшественнику железа, являются важными факторами в достижении нескольких типов наноразмерных продуктов MFC. Метод быстрой очистки использует магнитную сепарацию для восстановления материалов, что делает производство граммов магнитных наноматериалов довольно эффективным. Мы преодолеваем проблему агрегации магнитных наноматериалов, применяя высокозаряженные сульфонатные полимеры к поверхности этих наноматериалов, давая коллоидно стабильные MFC, которые остаются неагрегирующими даже в средах с высоким содержанием соли. Эти неагрегирующие, однородные и перестраиваемые материалы являются отличными перспективными материалами для биомедицинских и экологических применений.
Введение
Включение марганца в качестве легирующего вещества в решетку оксида железа может при соответствующих условиях увеличить намагниченность материала при высоких полях прикладывания по сравнению с чистыми оксидами железа. В результате наночастицы марганцевого феррита (MnxFe3-xO4) являются очень желательными магнитными наноматериалами из-за их высокой намагниченности насыщения, сильной реакции на внешние поля и низкой цитотоксичности1,2,3,4,5. Как однодоменные нанокристаллы, так и кластеры этих нанокристаллов, называемых многодоменными частицами, были исследованы в различных биомедицинских приложениях, включая доставку лекарств, магнитную гипертермию для лечения рака и магнитно-резонансную томографию (МРТ)6,7,8. Например, группа Hyeon в 2017 году использовала однодоменные наночастицы феррита марганца в качестве катализатора Фентона для индуцирования гипоксии рака и использовала T2contrast материала для отслеживания МРТ9. В свете этих и других положительных исследований ферритовых материалов удивительно, что существует мало демонстраций in vivo по сравнению с чистыми наноматериалами оксида железа (Fe3O4) и нет зарегистрированных применений у людей9,10.
Одной из огромных проблем, с которыми приходится сталкиваться при переводе особенностей ферритовых наноматериалов в клинику, является создание однородных, неагрегирующих, наноразмерных кластеров11,12,13,14. В то время как традиционные синтетические подходы к монодоменным нанокристаллам хорошо развиты, мультидоменные кластеры типа интереса к этой работе нелегко получить единообразным и контролируемым образом15,16. Кроме того, ферритовая композиция обычно не является стехиометрической и не просто связана с начальной концентрацией предшественников, и это может еще больше затемнить систематическую структурно-функциональную характеристику этих материалов9,12,13,17. Здесь мы решаем эти проблемы, демонстрируя синтетический подход, который дает независимый контроль как над размером кластера, так и над составом наноматериалов марганцевого феррита.
Эта работа также предоставляет средства для преодоления плохой коллоидной стабильности ферритовых наноматериалов18,19,20. Магнитные наночастицы, как правило, склонны к агрегации из-за сильного притяжения частиц-частиц; Ферриты больше страдают от этой проблемы, поскольку их большая чистая намагниченность усиливает агрегацию частиц. В соответствующих биологических средах эти материалы дают достаточно большие агрегаты, которые материалы быстро собирают, тем самым ограничивая их пути воздействия на животных или людей20,21,22. Hilt et al. обнаружили еще одно последствие агрегации частиц-частиц в своем исследовании магнитотермического нагрева и деградации красителя23. При несколько более высоких концентрациях частиц или увеличенном времени воздействия на поле эффективность материалов снижалась по мере агрегирования материалов с течением времени и уменьшения площадей поверхности активных частиц. Эти и другие приложения выиграли бы от кластерных поверхностей, предназначенных для обеспечения стерических барьеров, исключающих взаимодействия частиц с частицами24,25.
Здесь мы сообщаем о синтетическом подходе к синтезу ферритовых кластеров марганца (MFC) с контролируемыми размерами и составом. Эти многодоменные частицы состоят из сборки первичных нанокристаллов феррита марганца, которые жестко агрегированы; тесная ассоциация первичных нанокристаллов усиливает их магнитные свойства и обеспечивает общий размер кластера, 50-300 нм, хорошо соответствующий оптимальным размерам для наномедицины. Изменяя количество воды и предшественника хлорида марганца, мы можем самостоятельно контролировать общий диаметр и состав. Метод использует простые и эффективные гидротермальные реакции с одним горшком, которые позволяют часто экспериментировать и оптимизировать материал. Эти МФУ могут быть легко очищены в концентрированный раствор продукта, который дополнительно модифицируется сульфированными полимерами, которые придают коллоидную стабильность. Их настраиваемость, однородность и стабильность фазы раствора имеют большое значение для применения наноматериалов в биомедицинской и экологической инженерии.
протокол
1. Синтез МФЦ с контролем общего диаметра и ферритового состава МФЦ
- Вымойте и тщательно высушите всю стеклянную посуду, которая будет использоваться в синтезе. Количество воды в синтезе влияет на размеры MFC, поэтому крайне важно обеспечить, чтобы в стеклянной посуде не было остаточной воды16,26.
- Чтобы вымыть стеклянную посуду, промойте водой и моющим средством и потрите щеткой для удаления мусора. Тщательно промойте, чтобы удалить все моющее средство и закончите полосканием деионизированной водой.
- Чтобы высушить стеклянную посуду, стряхните капли воды с поверхности стеклянной посуды и поместите в духовку при 60°C до полного высыхания.
- Промыть реакторы с полифениленовой футеровкой (PPL) 37% соляной кислотой, чтобы удалить любой мусор из предыдущего использования. Для этого поместите реакторы и их колпачки в большой стакан и засыпьте соляной кислотой до тех пор, пока реакторы полностью не будут погружены. Оставьте на 30 минут, прежде чем вылить соляную кислоту. Непрерывно промывайте стакан, содержащий реакторы, водой в течение 1-2 мин, а затем поместите реакторы в печь для сушки.
- Используйте автоматическую пипетку для переноса 20 мл этиленгликоля в стакан емкостью 50 мл с магнитным перемешивателем.
- Взвесьте необходимое количество хлорида железа (III) (FeCl3·6H2O, твердое вещество) для достижения конечной концентрации 1,3 мМ и добавьте его в стакан. Положите стакан на перемешиваемую пластину и включите его при 480 оборотах в минуту, чтобы начать непрерывное перемешивание стакана.
ПРИМЕЧАНИЕ: Поскольку это гидрат, его необходимо быстро измерить и добавить, чтобы избежать нежелательного поглощения воды из окружающего воздуха. - Взвесьте 250 мг полиакриловой кислоты (PAA, Mw ~ 6000, порошок) и добавьте ее в стакан. После добавления ПАА раствор становится непрозрачным и немного светлее по цвету.
- Взвесьте 1,2 г мочевины (CO(NH2)2, порошок) и добавьте ее в стакан.
- Используя пипетку, добавьте в стакан 0,7 мМ хлорида марганца(II) (MnCl2·6H2O aq, 3,5 М, 0,2 мл).
- Наконец, с помощью пипетки добавьте в стакан необходимое количество (0,5 мл) сверхчистой воды.
- Дайте раствору помешиваться в течение 30 минут и обратите внимание на изменение цвета. Он будет представлен в виде полупрозрачного, темно-оранжевого цвета.
- Перенесите реакционную смесь в реактор с полифениленовой футеровкой (PPL). Обратите внимание, что после того, как раствор перемешался, некоторые твердые вещества могли скопиться по бокам стакана.
- Используйте магнит (кубический постоянный редкоземельный магнит, 40 x 40 x 20 мм, далее именуемый «магнитом» для всех процедур разделения и магнитного сбора), чтобы перетащить перемешивание вокруг стенок стакана, чтобы гарантировать, что любые твердые вещества, которые накопились по бокам, диспергируются в реакционном растворе.
- Как только раствор будет перемешан и готов, перенесите его в реактор с ППЛ объемом 50 мл.
- Используйте зажим и рычаг, чтобы как можно плотнее запечатать реактор в автоклаве из нержавеющей стали. Зажмите корпус реактора к стабильной поверхности и, используя стержень, вставленный в колпачок в качестве рычага, подтолкните реактор к уплотнению. Обратите внимание, что герметичный реактор не должен быть открыт вручную. Это имеет решающее значение, поскольку среда высокого давления в печи требует плотного уплотнения на реакторе.
- Поместите реактор в духовку на 20 ч при температуре 215 °C.
- После того, как гидротермальная реакция завершена, извлеките реактор из печи и дайте ему остыть до комнатной температуры. Давление в печи позволит открыть реактор вручную. Отметим, что в этот момент реактор будет содержать продукт MFC, диспергированный в этиленгликоле с другими примесями, такими как непрореагировавший полимер, и будет представлять собой непрозрачный черный раствор. Продукт будет изолирован на следующих этапах.
2. Магнитная сепарация и очистка МФУ
- Поместите 200 мг стальной ваты в стеклянный флакон. Заполните стеклянный флакон наполовину реакционной смесью из реактора. Наполните оставшуюся часть флакона ацетоном и хорошо встряхните. Отметим, что стальная вата увеличивает напряженность магнитного поля во флаконе и поможет магнитному отделению нанокластеров от раствора.
- Поместите флакон на магнит для магнитного сбора. В результате получится полупрозрачный раствор с осадком внизу.
- Вылейте раствор супернатанта, в то время как MFC магнитно захвачены стальной ватой, удерживая магнит на дне флакона во время заливки. Этиленгликоль будет в основном удален на этом этапе.
- Начинайте промывку с низким соотношением ацетона к воде и увеличивайте соотношение в последующих смывах до чистоты. Сделайте это 3-4 раза.
- Извлеките флакон из магнита и наполните его водой. Хорошо встряхните, чтобы растворить МФЦ. Теперь продукт будет полностью диспергироваться в воде.
- Повторите предыдущие два шага несколько раз, пока водный раствор MFC не произведет пузырьков при встряхивании. В результате получится темная, непрозрачная ферромагнитная жидкость, которая будет сильно реагировать на магниты.
ПРИМЕЧАНИЕ: При типичном синтезе с 20 мл этиленгликоля будет получено приблизительно 80 мг продукта MFC.
3. Поверхностная функционализация МФУ в сторону сверхвысокой коллоидной стабильности
ПРИМЕЧАНИЕ: Синтез нитродофамина и поли(AA-co-AMPS-co-PEG) можно найти в нашей предыдущей работе16. Сополимер производится путем свободнорадикальной полимеризации. Добавьте 0,20 г 2,2'-Азобиса (2-метилпропионитрила) (AIBN), 0,25 г акриловой кислоты (AA), 0,75 г 2-акриламидо-2-метилпропансульфоновой кислоты (AMPS) и 1,00 г поли(этиленгликоля) метилового эфира акрилата (PEG) в 10 мл N,N-диметилформамида (DMF). Нагрейте смесь на водяной бане при температуре 70 °C в течение 1 ч и переложите ее в диализный мешок (целлюлозная мембрана, 3 кДа) в воде. Весовое соотношение AA, AMPS и PEG составляет 1:3:4. Полимеризация для этих мономеров имеет 100% коэффициент конверсии, подтвержденный сублимационной сушкой и взвешиванием.
- Смешайте 10 мл очищенных наночастиц (около 100 мг) во флаконе объемом 20 мл с 10 мл насыщенного раствора N-[2-(3,4-дигидроксифенил)этил]нитрамида (нитро-дофамина) (~1 мг/мл). Подождите 5 мин.
- Промывайте МФУ с нитродофаминовым покрытием с помощью магнитной сепарации. Вылейте бледно-желтый супернатант. Добавьте воды и энергично встряхните. Затем вылейте воду, используя магнит, чтобы сохранить продукт. Повторите эту промывку несколько раз, оставив темно-коричневый сбор во флаконе.
ПРИМЕЧАНИЕ: Готовят водный раствор с концентрацией 20 мг/мл, буферный раствор с концентрацией 100 мг/мл и поли(AA-co-AMPS-co-PEG) полимерный раствор с концентрацией 20 мг/мл. - Смешайте 1 мл раствора EDC, 1 мл буфера MES и 3 мл раствора полимера. Слегка перемешайте, покрутив смесь, и дайте ей постоять примерно 5 минут. Это должен быть прозрачный и бесцветный раствор при полном сочетании.
- Добавьте эту смесь в коллекцию MFC и поместите флакон в ледяную ванну. Опустите зондовый ультразвуковой аппарат в раствор, а затем включите его (мощность 250 Вт при 20 кГц).
- После 5-минутной обработки ультразвуком добавьте примерно 5 мл сверхчистой воды во флакон, пока ультразвуковой аппарат все еще работает. Продолжайте следить за судном, чтобы убедиться, что продукт не разливается. Поддерживайте лед в смеси льда и воды, так как часть исходного льда растает из-за интенсивности и тепла обработки ультразвуком.
- Дайте смеси настояться ультразвуком в течение дополнительных 25 минут, в общей сложности 30 минут.
- Поместите флакон поверх магнита, чтобы отделить MFC и вылить раствор супернатанта.
- Промыть модифицированные МФУ деионизированной водой несколько раз.
- Наполните флакон, содержащий МФУ, сверхчистой водой. Пипетка этой жидкости в вакуумную систему фильтрации с мембранным фильтром полиэфирсульфона 0,1 мкм для удаления любых необратимо агрегированных МФУ. Обязательно промывайте стенки воронки, чтобы свести к минимуму потерю продукта.
- Вакуумная фильтрация раствора. Повторите этот процесс 2-3 раза. В результате получится очищенный водный раствор монодисперсных МФУ.
ПРИМЕЧАНИЕ: Примерно 10% продукта будет необратимо агрегировано, и этот материал останется на фильтре и должен быть выброшен.
Результаты
После гидротермической обработки реакционная смесь превращается в вязкую черную дисперсию, как видно на рисунке 1. Что получается после очистки, так это высококонцентрированный раствор MFC, который ведет себя как ферромагнитная жидкость. Жидкость во флаконе реагирует в течение нескольких секунд при размещении рядом с ручным магнитом (<0,5 Тл), образуя макроскопическую черную массу, которую можно перемещать, когда магнит размещается в разных местах.
Этот синтез дает продукты, размер и состав которых зависят от количества добавленной воды и соотношения марганца к предшественнику железа в реакционной смеси. На рисунке 2 показано, как морфология кластера зависит от концентрации воды и прекурсоров; в нем также подробно описываются условия реакции, используемые для получения образцов, перечисленных в таблице 1. Мы находим, что диаметр MFC зависит от количества добавленной воды, а состав MFC зависит от соотношения железа и марганца в предшественниках. Таким образом, оба параметра могут независимо контролироваться, чтобы создать библиотеку MFC с различными размерами и содержанием марганца.
Хотя это очень простая синтетическая процедура, ошибки в выполнении метода могут привести к сбоям продуктов. На рисунке 3 показаны образцы с неправильной морфологией MFC. На рисунке 3А МФУ нечетной формы получаются, если вода полностью исключена из реакционной среды. Нехватка воды препятствует динамической сборке первичных нанокристаллов и приводит к очень широкому распределению нанокластерных размеров и несферических форм16. Образцы, показанные на рисунке 3B , имели недостаточное время реакции (6-12 ч) и, как следствие, не имели достаточного роста первичных нанокристаллов. Эти плохие результаты демонстрируют, что для достижения последовательных и однородных кластеров необходимо соответствующее количество реагента, а также время реакции.
После завершения гидротермального синтеза ферритовые МФЦ отделяли и очищали с помощью магнитной сепарации. Магнит помещали под раствор, чтобы заставить их собирать на дне сосуда. Примеси и немагнитные побочные продукты, образующиеся в синтезе, наряду с избыточным растворителем, затем могут быть декантированы с получением чистых и монодисперсных MFC27. На рисунке 4 показано время, необходимое для почти полного магнитного сбора МФУ с добавлением и без добавления стальной ваты. Стальная вата, помещенная во флакон во время магнитной сепарации, увеличивает градиент магнитного поля внутри флакона, что позволяет гораздо быстрее отделять28.
МФУ, очищенные с помощью магнитной сепарации, демонстрируют высокую степень однородности по сравнению с теми, которые очищаются с использованием более традиционного процесса ультрацентрифугирования. На рисунке 5 показано распределение по размерам МФУ, полученных с помощью магнитной сепарации (A и B), по сравнению с теми, которые используют ультрацентрифугирование (5000 г в течение 30 мин) (C и D). Магнитная сепарация приводит к более узкому распределению диаметра кластера по сравнению с ультрацентрифугированием и является предпочтительной стратегией очистки для MFC.
Ас-синтезированные MFC покрыты полиакрилатом (PAA), который обеспечивает отрицательно заряженную поверхность и некоторую степень отталкивания межчастиц, что предотвращает агрегацию межчастиц (рисунок 6A). Однако, выполняя реакцию замены лиганда нитродоамином (рисунок 6B), мы можем заменить покрытие PAA сополимерным покрытием P(AA-co-AMPS-co-PEG), которое обеспечивает большую стабильность в растворах с более высокой ионной прочностью. На рисунке 7 показана схема этого процесса функционализации поверхности. Коллоидная стабильность MFC, диспергированных в буфере PBS, показана на рисунке 8. Синтезированные АСФК, покрытые ПАА, быстро агрегируются и отделяются от раствора в течение 30 мин и мало используются в биологических применениях. Напротив, МФУ, функционализированные полисульфонатным покрытием, оставались хорошо диспергированными в этом растворе в течение более 2 дней без каких-либо признаков агрегации. Описанная здесь модификация поверхности постсинтеза обеспечивает путь формирования однородных растворов МФУ, пригодных для интродукции в биологические среды.
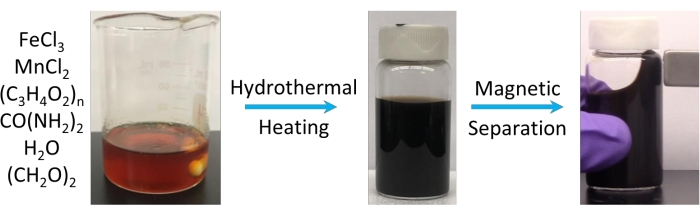
Рисунок 1: Схема синтеза нанокластеров марганцевого феррита. Реагенты, хлорид железа (III), хлорид марганца (II), полиакриловая кислота (PAA), мочевина, вода и этиленгликоль объединяются в гидротермальных условиях для получения нанокластеров марганцевого феррита. Этот продукт образует стабильный коллоидный раствор в чистой воде, как показано посередине. Количество воды, добавляемой при синтезе, и отношение марганца к железу в прекурсорах используется для настройки размера кластера и ферритового состава соответственно. После магнитного разделения нанокластеры образуют ферромагнитную жидкость, как показано справа, что указывает на то, что они очень чувствительны даже к небольшим приложенным магнитным полям. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.

Рисунок 2: Попередающий электронный микроскоп (ТЭМ) изображения нанокластеров марганцевого феррита и их распределения диаметров. На изображениях A-D диаметр кластера (Dc) увеличивается в результате уменьшения количества воды, добавляемой в синтез. Средний диаметр кластера составляет 31, 56, 74 и 120 нм для A, B, C и D соответственно с постоянным составом Mn0.15Fe2.85O4. На изображениях E-H ферритовая композиция монотонно изменяется пропорционально соотношению Mn/Fe предшественников. Несмотря на их различный состав, достигается почти эквивалентный диаметр кластера. Наш синтез позволяет независимо контролировать как диаметр кластера, так и состав феррита, оба признака, которые важны для магнитных свойств наноразмерных ферритов. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
| Метка на рисунке 2 | H2O (мл) | FeCl3 (ммоль) | MnCl2 (ммоль) | Ферритовый состав | Dc (нм) | |
| A | 1.5 | 1.3 | 0.7 | Mn0.15Fe2.85O4 | 34 | |
| B & G | 0.7 | 1.3 | 0.7 | Mn0.15Fe2.85O4 | 56 | |
| C | 0.5 | 1.3 | 0.7 | Mn0.15Fe2.85O4 | 74 | |
| D | 0.1 | 1.3 | 0.7 | Mn0.15Fe2.85O4 | 120 | |
| E | 1.3 | 2 | 0 | Фе3О4 | 56 | |
| F | 0.6 | 1.5 | 0.5 | Mn0.06Fe2.94O4 | 56 | |
| H | 2 | 1 | 1 | Mn0.6Fe2.4O4 | 55 | |
Таблица 1: Условия реакции синтеза образцов нанокластеров, показанных на рисунке 2. Другими параметрами синтеза являются: 20 мл этиленгликоля, 250 мг ПАА и 1,2 г мочевины. Реакционные смеси гидротермически нагревают при 200 °C в течение 20 ч. Для A, B, C и D уменьшение содержания воды при сохранении других параметров постоянным приводило к образованию кластеров большего диаметра. Для E, F, G и H увеличение отношения MnCl2 к FeCl3 в исходной реакционной смеси привело к образованию кластеров с более высокими пропорциями марганца в кластерной структуре. Изменение количества воды E, F, G и H одновременно позволяет создавать кластеры различного состава, но близкие к эквивалентным диаметрам.
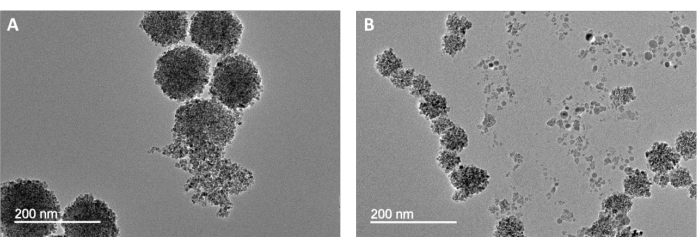
Рисунок 3: Изображения ТЭМ неудачных и неполных реакций. Небольшие, низкоконтрастные особенности, наблюдаемые на этих изображениях, являются первичными нанокристаллами, которые не развились в нанокластеры. Образец на фиг.3А готовили без дополнительной воды, в то время как материал, показанный на фиг.3В , имел недостаточное четырехчасовое время реакции. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
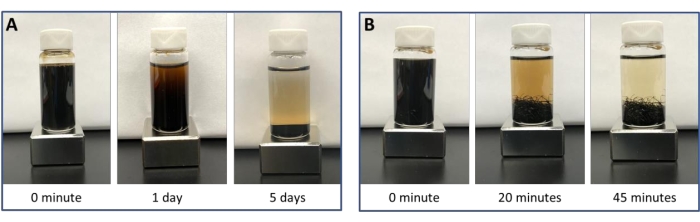
Рисунок 4: Сравнение магнитной сепарации нанокластеров. Сравнение магнитной сепарации нанокластеров без (А) и с (В) добавлением стальной ваты в контейнер. Стальная вата увеличивает градиент магнитного поля внутри флакона, чтобы обеспечить более быстрое магнитное разделение нанокластеров. В результате можно эффективно масштабировать производство нанокластеров без ущерба для качества образцов. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.

Рисунок 5: Сравнение ультрацентрифугирования и магнитной сепарации. Сравнение ультрацентрифугирования (А,В) и магнитной сепарации (С,D) и их влияние на однородность очищенных кластеров. A и C - это изображения ТЕА очищенных кластеров, а B и D - распределения размеров кластеров в A и C, соответственно. Ось y представляет собой количество подсчитанных кластеров, и для каждой выборки было обследовано в общей сложности 150 кластеров. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
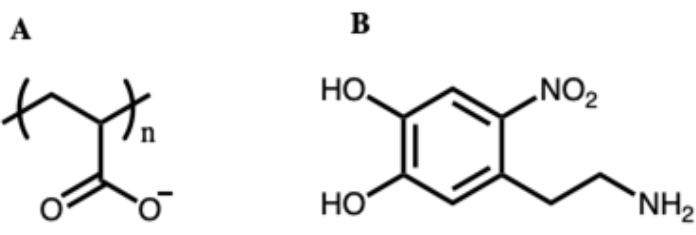
Рисунок 6: Структура поли(акриловой кислоты) (PAA) (A) и нитродофамина (B), используемых на стадии модификации поверхности. Исходное покрытие PAA, используемое в синтезе, не является идеальным в биологических или кислых средах из-за того, что карбоновая кислота легко протонируется. Нитро-дофамин используется для замены покрытия PAA, создавая функциональную группу для закрепления сульфированного сополимера. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
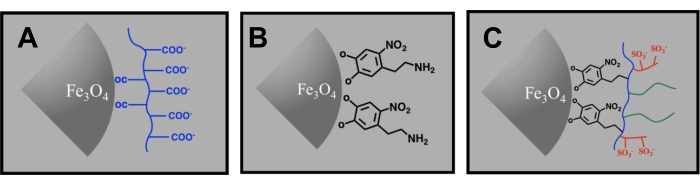
Рисунок 7: Схемы процесса модификации поверхности кластера. (A) оригинальное покрытие PAA, (B) промежуточное нитродофаминовое покрытие и (C) конечное P(AA-co-AMPS-co-PEG) покрытие. В (C) синяя, красная и зеленая кривые представляют единицы AA, AMPS и PEG соответственно. Состав кластера может быть либо Fe3O4, либо MnxFe3-xO4. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.

Рисунок 8: Поверхностная функционализация нанокластеров полисульфонатом приводит к материалам, которые коллоидно стабильны во многих различных водных условиях. Кластеры с двумя различными поверхностными покрытиями, как синтезированные PAA с покрытием (A) и P(AA-co-AMPS-co-PEG) поверхностно функционализированные (B), растворяются в буферном растворе PBS, который имеет отношение к биологическим условиям и наблюдается за их коллоидной стабильностью с течением времени. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Обсуждение
Данная работа демонстрирует модифицированный полиольный синтез нанокристаллов марганцевого феррита, сгруппированных вместе в однородные наноразмерные агрегаты29. При этом синтезе хлорид железа(III) и хлорид марганца(II) подвергаются принудительной реакции гидролиза и восстановления, образуя молекулярную MnxFe3-xO4. Эти молекулы феррита образуют первичные нанокристаллы при высокой температуре и высоком давлении в реакторах, в конечном итоге собираясь в сферические агрегаты, называемые здесь магнетитовыми ферритовыми кластерами (MFC). Без достаточного времени реакции или достаточного количества воды процесс агрегации не может полностью завершиться, что приводит к неоднородным, плохо сформированным частицам. И наоборот, при наличии достаточного количества времени и достаточного количества воды процесс кристаллизации и сборки оксида металла завершен и дает однородный сферический кластер, состоящий из десятков и сотен первичных нанокристаллов. Первичные нанокристаллы в этих материалах жестко агрегированы, разделяя некоторые кристаллические интерфейсы, что приводит к высокой начальной восприимчивости и выраженной магнитной реакции даже на небольшие поля, доступные от портативных постоянных магнитов27. В результате эти материалы имеют большой потенциал для применения в доставке лекарств, магнитной гипертермии, магнитно-резонансной томографии и визуализации магнитных частиц30,31,32.
Мы обнаружили, что количество воды, добавленной в начальную реакционную смесь, контролирует диаметр собранных кластеров. По мере увеличения содержания воды в реагентах уменьшается диаметр кластеров и количество агрегированных первичных нанокристаллов. Оптимальный диапазон составляет от 0,8 М до 5,0 М воды, условия, которые дают, соответственно, диаметр кластера в диапазоне от 150 нм до 30 нм. Вода играет важную роль в этом процессе, поскольку она необходима для обеспечения быстрого гидролиза предшественников металлов, более быстрой агрегации первичных кристаллитов и, следовательно, меньших кластеров16. Поскольку синтез чрезвычайно чувствителен к воде, реагенты, обрабатываемые в условиях окружающей среды переменной влажности, могут поглощать различное количество воды из воздуха. Это может повлиять на последующие размеры и морфологию продукта. Хотя контроль влажности в большинстве исследовательских лабораторий (например, 30-60% относительной влажности) достаточен для минимизации этой проблемы, это является одним из источников систематической ошибки в описанной процедуре. Контроль соотношения марганца к железу в продукте достигается путем изменения соотношения марганца к прекурсорам железа. Это удивительно, так как во многих гидротермальных реакциях уровень легирования продуктов часто не просто связан со стехиометрией исходных материалов4,6,8,12,13,17. Для этих условий, однако, состав продукта хорошо прогнозируется соотношением предшественников металла. Взятые вместе, независимый контроль как диаметра кластера, так и его состава возможен путем простого манипулирования исходными смесями реагентов.
Часто очистка наночастиц от реакционной среды является наиболее трудоемким и сложным этапом в получении высококачественных материалов. Ультрацентрифугирование часто применяется для этой цели, и, хотя это эффективно при отделении наночастиц от молекулярных побочных продуктов, оно плохо подходит для удаления нежелательных твердых продуктов. При применении здесь для очистки наноматериалов ультрацентрифугирование производит относительно полидисперсные частицы с переменными размерами и формами. Гораздо эффективнее использовать магнитную реакцию этих материалов, применяя магнитную сепарацию для улучшения однородности и чистоты конечного продукта. Мы ускоряем магнитную сепарацию, создавая очень высокие градиенты магнитных полей в макроскопическом флаконе с использованием стальной ваты, погруженной в раствор, и редкоземельного постоянного магнита, приложенного вне контейнеров для образцов. Такое расположение позволяет извлекать однородные образцы менее чем за тридцать минут с высокой урожайностью (~90%). Важно сопоставить количество стальной ваты, введенной в раствор, с ожидаемыми диаметрами кластера MFC. Например, MFC со средним диаметром 40 нм требует от 100 до 200 мг стальной ваты для быстрого разделения, в то время как более крупные материалы могут потребовать гораздо меньше или даже не требовать стальной ваты. Хорошо известно, что меньшие магнитные наночастицы менее чувствительны к приложенным полям в силу их меньшего магнитного объема15,17,26. Таким образом, процесс магнитной сепарации обеспечивает средства для повышения однородности этих материалов, поскольку меньшие кластеры не удерживаются так эффективно процессом16. Использование этого метода магнитной сепарации не только экономит время в лаборатории, но и приводит к продуктам с большей однородностью в диаметре.
Хотя синтезированные как МФУ стабильны в чистой воде, они демонстрируют плохую коллоидную стабильность в растворах с более низким рН или более высокой ионной прочностью. Ферриты марганца имеют большие плотности намагниченности, и в результате для этих диаметров кластеры обладают магнитными диполями, которые приводят к притяжению межчастиц. Нативное полиакрилатное покрытие, используемое при формировании материалов, придает отрицательный заряд поверхностям частиц и помогает предотвратить агрегацию частиц-частиц. Однако при более низком рН карбоновые группы полностью протонируются, эффективно удаляя электростатическое отталкивание, необходимое для поддержания однородных дисперсий MFC; в качестве альтернативы, в средах с более высокой ионной силой отталкивание заряда уменьшается, что приводит к большей агрегации частиц. Агрегация MFC создает макроскопические материалы, которые не однородно диспергируются в растворе, что затрудняет использование материалов in vivo или в приложениях, требующих больших и доступных поверхностей наночастиц. По этим причинам мы вводим второй полимер в реакцию для замены оригинального покрытия PAA. Сополимер P(AA-co-AMPS-co-PEG) включает нейтральный полиэтиленгликоль (PEG) для обеспечения биосовместимости и некоторой степени стерической помехи. Кроме того, полисульфонатный компонент (PAMPS) предлагает как большую плотность заряда, чем полиакрилат, так и функциональную группу, которая имеет гораздо более низкий pKa и, следовательно, больший рабочий диапазон pH (pKa ~ 1,2)24. Ферритовые кластеры марганца, модифицированные этими поверхностными покрытиями, демонстрируют резко повышенную стабильность в кислых и биологических средах. Однако процедура обеспечения правильной модификации поверхности детализирована и должна тщательно соблюдаться, чтобы обеспечить эффективное покрытие образцов. В частности, способ требует постоянного мониторинга реакционной смеси во время ее обработки зондовым ультразвуковым аппаратом для обеспечения однородной, полной замены исходного полиакрилатного покрытия. Также важно использовать стеклянную посуду соответствующего размера, чтобы свести к минимуму любые потери продукта во время энергичной обработки ультразвуком и нанести ледяную ванну на смесь ультразвука, чтобы свести к минимуму термическую деградацию полимеров, вызванную зондовой обработкой ультразвуком.
В заключение, этот метод позволяет быстро и эффективно производить марганцевые ферритовые кластеры (MFC) с настраиваемыми диаметрами и составами марганца к железу. Содержание воды в реагенте, а также соотношение железа и марганца являются важными параметрами при определении характеристик материала. Простой метод магнитной сепарации с использованием ручного магнита и стальной ваты обеспечивает эффективное средство для очистки продукта после синтеза, давая более однородные кластеры. Наконец, сульфированный сополимер ПЭГ наносится на материалы, чтобы гарантировать, что они остаются неагрегированными в различных средах рН и ионной прочности. Повышенная магнитная реакция этих легированных марганцем оксидов железа по сравнению с чистыми наноматериалами оксида железа (Fe3O4) делает разработку устройств для применения внешних полей для манипулирования материалами in vivo. Их улучшенные поверхностные покрытия также важны, поскольку приложения для магнитных наночастиц в доставке лекарств, рекультивации воды и передовых системах визуализации требуют материалов, которые не агрегируются и однородны в различных биологических и экологических средах.
Раскрытие информации
Авторам нечего раскрывать.
Благодарности
Эта работа была щедро поддержана Университетом Брауна и Advanced Energy Consortium. Мы с благодарностью благодарим д-ра Цинбо Чжана за его установленный синтетический метод МФУ оксида железа.
Материалы
| Name | Company | Catalog Number | Comments |
| 0.1 Micron Vaccum Filtration Filter | Thermo Fisher Scientific | NC9902431 | for filtration of aggregated clusters after synthesis and surface coating to achieve a uniform solution |
| 2-Acrylamido-2-methylpropane sulfonic acid (AMPS, 99%) | Sigma-Aldrich | 282731-250G | reagent used in copolymer to surface coat nanoclusters and functionalize them for biological media |
| 2,2′-Azobis(2-methylpropionitrile) (AIBN) | Sigma-Aldrich | 441090-100G | reagent used in copolymer making as the free ridical generator |
| 4-Morpholineethanesulfonic acid, 2-(N-Morpholino)ethanesulfonic acid (MES) | Sigma-Aldrich | M3671-250G | acidic buffer used to stabilize nanocluster surface coating process |
| Acrylic acid | Sigma-Aldrich | 147230-100G | reagent used in copolymer to surface coat nanoclusters and functionalize them for biological media; anhydrous, contains 200 ppm MEHQ as inhibitor, 99% |
| Analytical Balance | Avantor | VWR-205AC | used to weigh out solid chemical reagents for use in synthesis and dilution |
| Digital Sonifier and Probe | Branson | B450 | used to sonicate nanocluster solution during surface coating to break up aggregates |
| Dopamine hydrochloride | Sigma-Aldrich | H8502-25G | used in surface coating for ligand exchange reaction |
| Ethylene glycol (anhydrous, 99.8%) | Sigma-Aldrich | 324558-2L | reagent used as solvent in hydrothermal synthesis of nanoclusters |
| Glass Vials (20mL) | Premium Vials | B1015 | container for nanocluster solution during washing and surface coating as well as polymer solutions |
| Graduated Beaker (100mL) | Corning | 1000-100 | container for mixing of solid and liquid reagents during hydrothermal synthesis (to be transferred into autoclave reactor before oven) |
| Handheld Magnet | MSC Industrial Supply, Inc. | 92673904 | 1/2" Long x 1/2" Wide x 1/8" High, 5 Poles, Rectangular Neodymium Magnet low strength magnet used to precipitate nanoclusters from solution (field strength is increased with steel wool when needed) |
| Hydrochloric acid (ACS grade, 37%) | Fisher Scientific | 7647-01-0 | for removing leftover nanocluster debris and cleaning autoclave reactors for next use |
| Hydrothermal Autoclave Reactor | Toption | TOPT-HP500 | container for finished reagent mixture to withstand high temperature and pressure created by the oven in hydrothermal synthesis |
| Iron(III) Chloride Hexahydrate (FeCl3·6H2O, ACS reagent, 97%) | ACS | 236489-500G | reagent used in synthesis of nanoclusters as source of iron (III) that becomes iron (II) in finished nanocluster product (keep dry and weigh out quickly to avoid water contamination) |
| Labware Washer Brushes | Fisher Scientific | 13-641-708 | used to wash and clean glassware before synthesis |
| Magnetic Stir Plate | Thermo Fisher Scientific | 50093538 | for mixing of solid and liquid reagents during hydrothermal synthesis |
| Manganese chloride tetrahydrate (MnCl2·4H2O, 99.0%, crystals, ACS) | Sigma-Aldrich | 1375127-2G | reagent used in synthesis of nanoclusters as source of manganese |
| Micropipette (100-1000μL) | Thermo Fisher Scientific | FF-1000 | for transferring liquid reagents such as water and manganese chloride |
| N-(3-Dimethylaminopropyl)-N′-ethylcarbodiimide hydrochloride (EDC) | Sigma-Aldrich | 25952-53-8 | used in surface coating to assist in ligand exchange of copolymer (keep bulk chemical in freezer and diluted solution in refrigerator) |
| N,N-Dimethylformamide (DMF) | Sigma-Aldrich | 227056-2L | reagent used in copolymer making as the solvent |
| Polyacrylic acid sodium salt (PAA, Mw~6,000) | PolyScience Inc. | 06567-250 | reagent used in hydrothermal synthesis to initially coat the nanoclusters (eventually replaced in surface coating step) |
| Poly(ethylene glycol) methyl ether acrylate | Sigma-Aldrich | 454990-250ML | reagent used in copolymer to surface coat nanoclusters and functionalize them for biological media; average Mn 480, contains 100 ppm BHT as inhibitor, 100 ppm MEHQ as inhibitor |
| Reagents Acetone, 4L, ACS Reagent | Cole-Parmer | UX-78920-66 | used as solvent to precipitate nanoclusters during washing |
| Single Channel Pipette, Adjustable 1-10 mL | Eppendorf | 3123000080 | for transferring ethylene glycol and other liquids |
| Steel Wool | Lowe's | 788470 | used to increase the magnetic field strength in the vial to aid in precipitation of nanoclusters for washing and surface coating |
| Stirring Bar | Thomas Scientific | 8608S92 | for mixing of solid and liquid reagents during hydrothermal synthesis |
| Table Clamp | Grainger | 29YW53 | for tight sealing of autoclave reactor to withstand high pressure of oven during hyrothermal synthesis |
| Urea (ACS reagent, 99.0%) | Sigma-Aldrich | U5128-500G | reagent used in hydrothermal synthesis to create a basic solution |
| Vaccum Filtration Bottle Tops | Thermo Fisher Scientific | 596-3320 | for filtration of aggregated clusters after synthesis and surface coating to achieve a uniform solution |
| Vacuum Controller V-850 | Buchi | BU-V850 | for filtration of aggregated clusters after synthesis and surface coating to achieve a uniform solution |
| Vacuum Oven | Fisher Scientific | 13-262-51 | used to create high temperature and pressure needed for nanocluster formation in hydrothermal synthesis |
Ссылки
- Makridis, A., et al. In vitro application of Mn-ferrite nanoparticles as novel magnetic hyperthermia agents. Journal of Materials Chemistry B. 2 (47), 8390-8398 (2014).
- Nelson-Cheeseman, B., Chopdekar, R., Toney, M., Arenholz, E., Suzuki, Y. Interplay between magnetism and chemical structure at spinel-spinel interfaces. Journal of Applied Physics. 111 (9), 093903 (2012).
- Otero-Lorenzo, R., Fantechi, E., Sangregorio, C., Salgueiriño, V. Solvothermally driven Mn doping and clustering of iron oxide nanoparticles for heat delivery applications. Chemistry-A European Journal. 22 (19), 6666-6675 (2016).
- Mohapatra, J., et al. Enhancement of magnetic heating efficiency in size controlled MFe 2 O 4 (M= Mn, Fe, Co and Ni) nanoassemblies. Rsc Advances. 5 (19), 14311-14321 (2015).
- Qi, Y., et al. Carboxylic silane-exchanged manganese ferrite nanoclusters with high relaxivity for magnetic resonance imaging. Journal of Materials Chemistry B. 1 (13), 1846-1851 (2013).
- Anandhi, J. S., Jacob, G. A., Joseyphus, R. J. Factors affecting the heating efficiency of Mn-doped Fe3O4 nanoparticles. Journal of Magnetism and Magnetic Materials. 512, 166992 (2020).
- Del Bianco, L., et al. Mechanism of magnetic heating in Mn-doped magnetite nanoparticles and the role of intertwined structural and magnetic properties. Nanoscale. 11 (22), 10896-10910 (2019).
- Padmapriya, G., Manikandan, A., Krishnasamy, V., Jaganathan, S. K., Antony, S. A. Enhanced catalytic activity and magnetic properties of spinel Mn x Zn 1−x Fe 2 O 4 (0.0≤x≤1.0) nano-photocatalysts by microwave irradiation route. Journal of Superconductivity and Novel Magnetism. 29 (8), 2141-2149 (2016).
- Kim, J., et al. Continuous O2-evolving MnFe2O4 nanoparticle-anchored mesoporous silica nanoparticles for efficient photodynamic therapy in hypoxic cancer. Journal of the American Chemical Society. 139 (32), 10992-10995 (2017).
- Silva, L. H., Cruz, F. F., Morales, M. M., Weiss, D. J., Rocco, P. R. Magnetic targeting as a strategy to enhance therapeutic effects of mesenchymal stromal cells. Stem Cell Research & Therapy. 8 (1), 1-8 (2017).
- Otero-Lorenzo, R., Ramos-Docampo, M. A., Rodriguez-Gonzalez, B., Comesaña-Hermo, M., Salgueiriño, V. Solvothermal clustering of magnetic spinel ferrite nanocrystals: a Raman perspective. Chemistry of Materials. 29 (20), 8729-8736 (2017).
- Aghazadeh, M., Karimzadeh, I., Ganjali, M. R. PVP capped Mn2+ doped Fe3O4 nanoparticles: a novel preparation method, surface engineering and characterization. Materials Letters. 228, 137-140 (2018).
- Li, Z., et al. Solvothermal synthesis of MnFe 2 O 4 colloidal nanocrystal assemblies and their magnetic and electrocatalytic properties. New Journal of Chemistry. 39 (1), 361-368 (2015).
- Guo, P., Zhang, G., Yu, J., Li, H., Zhao, X. Controlled synthesis, magnetic and photocatalytic properties of hollow spheres and colloidal nanocrystal clusters of manganese ferrite. Colloids and Surfaces A: Physicochemical and Engineering Aspects. 395, 168-174 (2012).
- Pardo, A., et al. Synthesis, characterization, and evaluation of superparamagnetic doped ferrites as potential therapeutic nanotools. Chemistry of Materials. 32 (6), 2220-2231 (2020).
- Xiao, Z., et al. Libraries of uniform magnetic multicore nanoparticles with tunable dimensions for biomedical and photonic applications. ACS Applied Materials & Interfaces. 12 (37), 41932-41941 (2020).
- Choi, Y. S., Young Yoon, H., Sung Lee, J., Hua Wu, J., Keun Kim, Y. Synthesis and magnetic properties of size-tunable Mn x Fe3−x O4 ferrite nanoclusters. Journal of Applied Physics. 115 (17), (2014).
- Creixell, M., et al. The effect of grafting method on the colloidal stability and in vitro cytotoxicity of carboxymethyl dextran coated magnetic nanoparticles. Journal of Materials Chemistry. 20 (39), 8539-8547 (2010).
- Latorre, M., Rinaldi, C. Applications of magnetic nanoparticles in medicine: magnetic fluid hyperthermia. Puerto Rico Health Sciences Journal. 28 (3), (2009).
- Yeap, S. P., Lim, J., Ooi, B. S., Ahmad, A. L. Agglomeration, colloidal stability, and magnetic separation of magnetic nanoparticles: collective influences on environmental engineering applications. Journal of Nanoparticle Research. 19 (11), 1-15 (2017).
- Lee, S. -. Y., Harris, M. T. Surface modification of magnetic nanoparticles capped by oleic acids: Characterization and colloidal stability in polar solvents. Journal of Colloid and Interface Science. 293 (2), 401-408 (2006).
- Yeap, S. P., Ahmad, A. L., Ooi, B. S., Lim, J. Electrosteric stabilization and its role in cooperative magnetophoresis of colloidal magnetic nanoparticles. Langmuir. 28 (42), 14878-14891 (2012).
- Wydra, R. J., Oliver, C. E., Anderson, K. W., Dziubla, T. D., Hilt, J. Z. Accelerated generation of free radicals by iron oxide nanoparticles in the presence of an alternating magnetic field. RSC Advances. 5 (24), 18888-18893 (2015).
- Bagaria, H. G., et al. Iron oxide nanoparticles grafted with sulfonated copolymers are stable in concentrated brine at elevated temperatures and weakly adsorb on silica. ACS Applied Materials & Interfaces. 5 (8), 3329-3339 (2013).
- Park, J. C., Park, T. Y., Cha, H. J., Seo, J. H. Multifunctional nanocomposite clusters enabled by amphiphilic/bioactive natural polysaccharides. Chemical Engineering Journal. 379, 122406 (2020).
- Hemery, G., et al. Tuning sizes, morphologies, and magnetic properties of monocore versus multicore iron oxide nanoparticles through the controlled addition of water in the polyol synthesis. Inorganic Chemistry. 56 (14), 8232-8243 (2017).
- Lartigue, L., et al. Cooperative organization in iron oxide multi-core nanoparticles potentiates their efficiency as heating mediators and MRI contrast agents. ACS Nano. 6 (12), 10935-10949 (2012).
- Yavayo, C. T., et al. Low-field magnetic separation of monodisperse Fe3O4 nanocrystals. Science. 314 (5801), 964-967 (2006).
- Matijević, E., Scheiner, P. Ferric hydrous oxide sols: III. Preparation of uniform particles by hydrolysis of Fe (III)-chloride,-nitrate, and-perchlorate solutions. Journal of Colloid and Interface Science. 63 (3), 509-524 (1978).
- Weizenecker, J., Gleich, B., Rahmer, J., Dahnke, H., Borgert, J. Three-dimensional real-time in vivo magnetic particle imaging. Physics in Medicine & Biology. 54 (5), 1 (2009).
- Zhu, X., Li, J., Peng, P., Hosseini Nassab, N., Smith, B. R. Quantitative drug release monitoring in tumors of living subjects by magnetic particle imaging nanocomposite. Nano Letters. 19 (10), 6725-6733 (2019).
- Tay, Z. W., et al. Magnetic particle imaging-guided heating in vivo using gradient fields for arbitrary localization of magnetic hyperthermia therapy. ACS Nano. 12 (4), 3699-3713 (2018).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены