Method Article
Suspensões aquosas estáveis de aglomerados de ferrite de manganês com dimensão e composição de nanoescala tunable
Neste Artigo
Resumo
Relatamos uma síntese hidrotérmica de um pote de aglomerados de ferrita de manganês (MFCs) que oferece controle independente sobre a dimensão e a composição do material. A separação magnética permite a purificação rápida enquanto a funcionalização da superfície usando polímeros sulfoados garante que os materiais não sejam agregados em meio biologicamente relevante. Os produtos resultantes estão bem posicionados para aplicações biomédicas.
Resumo
Os aglomerados de ferrite de manganês (MFCs) são conjuntos esféricos de dezenas a centenas de nanocristais primários cujas propriedades magnéticas são valiosas em diversas aplicações. Aqui descrevemos como formar esses materiais em um processo hidrotérmico que permite o controle independente do tamanho do cluster do produto (de 30 a 120 nm) e o teor de manganês do material resultante. Parâmetros como a quantidade total de água adicionada à mídia de reação alcoólica e a razão entre manganês e precursor de ferro são fatores importantes para alcançar múltiplos tipos de produtos nanoescala MFC. Um método de purificação rápida usa a separação magnética para recuperar os materiais que fazem a produção de gramas de nanomateriais magnéticos bastante eficiente. Superamos o desafio da agregação de nanomateriais magnéticos aplicando polímeros sulfonatos altamente carregados à superfície desses nanomateriais que produzem MFCs coloidalmente estáveis que permanecem não agregando mesmo em ambientes altamente salinos. Esses materiais não agregadores, uniformes e incompará-los são excelentes materiais prospectivos para aplicações biomédicas e ambientais.
Introdução
A inclusão de manganês como dopant em uma rede de óxido de ferro pode, sob as condições adequadas, aumentar a magnetização do material em campos de alta aplicação em comparação com óxidos de ferro puros. Como resultado, as nanopartículas de manganês ferrite (MnxFe3-xO4) são nanomateriais magnéticos altamente desejáveis devido à sua alta magnetização de saturação, forte resposta a campos externos e baixa citotoxicidade1,2,3,4,5. Tanto os nanocristais de domínio único quanto os agrupamentos desses nanocristais, denominados partículas multidomainas, têm sido investigados em diversas aplicações biomédicas, incluindo entrega de medicamentos, hipertermia magnética para tratamento do câncer e ressonância magnética (RM)6,7,8. Por exemplo, o grupo Hyeon em 2017 usou nanopartículas de ferrite de manganês de domínio único como um catalisador fenton para induzir a hipóxia do câncer e explorou o T2contrast do material para rastreamento de ressonância magnética9. É surpreendente à luz desses e outros estudos positivos de materiais ferritais que há poucas demonstrações in vivo em comparação com nanomateriais de óxido de ferro puro (Fe3O4), e nenhuma aplicação relatada em humanos9,10.
Um imenso desafio enfrentado na tradução das características dos nanomateriais ferrite para a clínica é a geração de aglomerados uniformes, não agregadores e nanoescala11,12,13,14. Embora as abordagens sintéticas convencionais para os nanocristais monodomínios sejam bem desenvolvidas, os aglomerados multidomain do tipo de interesse neste trabalho não são facilmente produzidos de forma uniforme e controlada15,16. Além disso, a composição ferrita geralmente não é estequiométrica e não apenas está relacionada à concentração inicial dos precursores e isso pode obscurecer ainda mais a caracterização sistemática estrutura-função desses materiais9,12,13,17. Aqui, abordamos essas questões demonstrando uma abordagem sintética que produz controle independente sobre a dimensão do cluster e a composição de nanomateriais de ferrite de manganês.
Este trabalho também fornece um meio de superar a pobre estabilidade coloidal dos nanomateriais ferrite18,19,20. As nanopartículas magnéticas são geralmente propensas à agregação devido à forte atração de partículas de partículas; ferrites sofrem mais com esse problema à medida que sua magnetização líquida maior amplifica a agregação de partículas. Em meios biológicos relevantes, esses materiais produzem grandes agregados suficientes que os materiais coletam rapidamente, limitando assim suas rotas de exposição a animais ou pessoas20,21,22. Hilt et al. encontraram outra consequência da agregação de partículas-partículas em seu estudo de aquecimento magnetotémico e degradação de corante23. Em concentrações de partículas ligeiramente maiores, ou aumento do tempo de exposição ao campo, a eficácia dos materiais foi reduzida à medida que os materiais agregados ao longo do tempo e as áreas de superfície de partículas ativas diminuíram. Essas e outras aplicações se beneficiariam de superfícies de cluster projetadas para fornecer barreiras estéricas que impediam interações partículas-partícula24,25.
Aqui relatamos uma abordagem sintética para sintetizar os aglomerados de ferrite de manganês (MFCs) com dimensões e composição controláveis. Essas partículas de multidomaina consistem em um conjunto de nanocristais de ferrite de manganês primários que são agregados duramente; a associação próxima dos nanocristais primários melhora suas propriedades magnéticas e fornece um tamanho total de cluster, 50-300 nm, bem combinado com as dimensões ideais para uma nanomedicina. Alterando a quantidade de água e o precursor do cloreto de manganês, podemos controlar independentemente o diâmetro e a composição globais. O método utiliza reações hidrotérmicas simples e eficientes de um pote que permitem experimentação frequente e otimização de materiais. Esses MFCs podem ser facilmente purificados em uma solução concentrada de produtos, que é ainda modificada por polímeros sulfoados que transmitem estabilidade coloidal. Sua sintonia, uniformidade e estabilidade de fase de solução são características de grande valor nas aplicações de nanomateriais em engenharia biomédica e ambiental.
Protocolo
1. Síntese de MFCs com controle sobre o diâmetro geral dos MFCs e composição ferrita
- Lave e seque completamente todos os vidros para serem usados na síntese. A quantidade de água na síntese impacta as dimensões dos MFCs, por isso é crucial garantir que o vidro não tenha água residual nele16,26.
- Para lavar os vidros, enxágue com água e detergente e esfregue com uma escova de frasco para remover os detritos. Enxágue bem para remover todo o detergente e finalize com uma lavagem de água deionizada.
- Para secar os vidros, retire as gotículas de água da superfície do vidro e coloque em um forno a 60°C até secar completamente.
- Enxágüe os reatores revestidos de polifeneno (PPL) com 37% de ácido clorídrico para remover quaisquer detritos do uso anterior. Para isso, coloque os reatores e suas tampas em um grande béquer e encha com ácido clorídrico até que os reatores estejam completamente submersos. Deixe isso descansar por 30 minutos antes de derramar o ácido clorídrico. Enxágue continuamente o béquer contendo os reatores com água por 1-2 min e, em seguida, coloque os reatores no forno para secar.
- Use uma pipeta automática para transferir 20 mL de etileno glicol em um béquer de 50 mL com uma barra de agitação magnética.
- Pesar a quantidade necessária de cloreto de ferro (III) (FeCl3·6H2O, sólido) para alcançar uma concentração final de 1,3 mM e adicioná-lo ao béquer. Coloque o béquer em uma placa de agitação e ligue-o a 480 rpm para começar a agitação contínua do béquer.
NOTA: Como se trata de um hidrato, deve ser medido e adicionado rapidamente para evitar a absorção indesejada de água do ar ambiente. - Pese 250 mg de ácido poliacrílico (PAA, Mw ~6.000, pó) e adicione-o ao béquer. Após a adição do PAA, a solução se torna opaca e ligeiramente mais clara na cor.
- Pesar 1,2 g de ureia (CO(NH2)2, pó) e adicioná-lo ao béquer.
- Usando uma pipeta, adicione cloreto de manganês de 0,7 mM (II) (MnCl2·6H2O aq, 3,5 M, 0,2 mL) ao béquer.
- Por fim, usando uma pipeta adicione a quantidade necessária (0,5 mL) de água ultra-pura ao béquer.
- Deixe a solução mexer por 30 minutos e observe a mudança de cor. Ele se apresentará como uma cor laranja translúcida e escura.
- Transfira a mistura de reação para o reator forrado de polifeneno (PPL). Note que depois que a solução mexeu alguns sólidos podem ter se acumulado nas laterais do béquer.
- Use um ímã (ímã de terra rara permanente cúbica, 40 x 40 x 20 mm, doravante chamado de "ímã" para todos os procedimentos de separação e coleta magnética) para arrastar a barra de agitação ao redor das paredes do béquer para garantir que quaisquer sólidos que tenham se acumulado nas laterais sejam dispersados na solução de reação.
- Uma vez que a solução esteja mista e pronta, transfira-a para o reator forrado PPL de 50 mL.
- Use um grampo e uma alavanca para selar o reator na autoclave de aço inoxidável o mais firmemente possível. Fixar o vaso do reator em uma superfície estável, e usando uma haste inserida na tampa como alavanca, empurre o reator para selar. Observe que o reator selado não deve ser capaz de ser aberto manualmente. Isso é crucial, pois o ambiente de alta pressão do forno requer uma vedação apertada no reator.
- Coloque o reator em forno por 20 h a 215 °C.
- Depois que a reação hidrotérmica for feita, remova o reator do forno e deixe esfriar até a temperatura ambiente. A pressão do forno permitirá que o reator seja aberto manualmente. Observe que neste ponto, o reator conterá o produto MFC dispersado em etileno glicol com outras impurezas, como polímero não redigido, e será uma solução preta opaca. O produto será isolado nas etapas seguintes.
2. Separação magnética e purificação de MFCs
- Coloque 200 mg de lã de aço em um frasco de vidro. Encha o frasco de vidro no meio do caminho com a mistura de reação do reator. Encha o resto do frasco com acetona e agite bem. Observe que a lã de aço aumenta a força do campo magnético no frasco e ajudará a separação magnética dos nanoaglomerados da solução.
- Coloque o frasco em um ímã para que a coleta magnética ocorra. O resultado será uma solução translúcida com precipitação na parte inferior.
- Despeje a solução sobrenante enquanto os MFCs são magneticamente presos pela lã de aço, segurando o ímã até o fundo do frasco enquanto derramam. O etileno glicol será removido principalmente nesta etapa.
- Comece a lavar com a baixa proporção de acetona para água e aumente a proporção em lavagens subsequentes até ficar pura. Faça isso 3-4 vezes.
- Retire o frasco do ímã e encha-o com água. Agite bem para dissolver os MFCs. Agora o produto estará totalmente disperso na água.
- Repita as duas etapas anteriores várias vezes até que a solução aquosa dos MFCs não produz bolhas quando abalada. O resultado será um ferrofluido escuro e opaco que responderá fortemente aos ímãs.
NOTA: Em uma síntese típica com 20 mL de etileno glicol, aproximadamente 80 mg de produto MFC serão obtidos.
3. Funcionalidade superficial de MFCs em direção à estabilidade coloidal ultra-alta
NOTA: A síntese de nitro-dopamina e Poly (AA-co-AMPS-co-PEG) pode ser encontrada em nosso trabalho anterior16. O copolímero é feito através da polimerização radical livre. Adicionar 0,20 g de 2,2′-Azobis(2-metilpropionitrilo) (AIBN), 0,25 g de ácido acrílico (AA), 0,75 g de 2-Acrilamido-2-ácido sulfônico de metilpropano (AMPS) e 1,00 g de Polítil glicol (etileno glicol) acrilato de metila (PEG) em 10 mL de N,N-Dimetilformamida (DMF). Aqueça a mistura em um banho de água de 70 °C por 1h e transfira para um saco de diálise (Membrana de Celulose, 3 kDa) na água. A razão de peso de AA, AMPS e PEG é de 1:3:4. A polimerização desses monômeros tem uma taxa de conversão de 100%, confirmada pela secagem e pesagem congelantes.
- Combine 10 mL de nanopartículas purificadas (cerca de 100 mg) em um frasco de 20 mL com 10 mL de solução de N-[2-(3,4-dihidroxilfenil)etil]niramida (nitro-dopamina) (~1 mg/mL). Espere por 5 min.
- Lave os MFCs revestidos de nitro-dopamina usando separação magnética. Despeje o supernatante amarelo-pálido. Adicione água e agite vigorosamente. Em seguida, despeje água usando o ímã para reter o produto. Repita esta lavagem várias vezes deixando a coleção marrom escura no frasco.
NOTA: Prepare uma solução aquosa com concentração de 20 mg/mL, uma solução tampão com concentração de 100 mg/mL, e uma solução polímera poli (AA-co-AMPS-co-PEG) com concentração de 20 mg/mL. - Misture 1 mL de solução EDC, 1 mL de tampão MES e 3 mL da solução de polímero. Mexa levemente girando a mistura, e deixe descansar por aproximadamente 5 minutos. Deve ser uma solução clara e incolor quando totalmente combinada.
- Adicione essa mistura à coleção MFC e coloque o frasco em um banho de gelo. Abaixe o sonicator da sonda na solução e ligue-o (250 watts de potência a 20 kHz).
- Após um tratamento de sonicação de 5 minutos, adicione cerca de 5 mL de água ultra-pura ao frasco enquanto o sonicator ainda está funcionando. Continue monitorando a embarcação para garantir que nenhum produto derrame. Mantenha o gelo na mistura de água gelada, pois parte do gelo inicial derreterá devido à intensidade e calor da sônicação.
- Deixe a mistura sonicar por mais 25 minutos, totalizando 30 min.
- Coloque o frasco em cima de um ímã para separar os MFCs e despeje a solução sobrenatante.
- Lave os MFCs modificados com água desionizada várias vezes.
- Encha o frasco contendo os MFCs com água ultra-pura. Pipeta este fluido em um sistema de filtragem de vácuo com um filtro de membrana de polietroéfone de 0,1 μm para remover quaisquer MFCs irreversivelmente agregados. Certifique-se de lavar as paredes do funil para minimizar qualquer perda do produto.
- Filtro de vácuo a solução. Repita este processo 2-3 vezes. O resultado será uma solução aquosa purificada de MFCs monodispersed.
NOTA: Cerca de 10% do produto será irreversivelmente agregado e este material permanecerá no filtro e deve ser descartado.
Resultados
Após o tratamento hidrotérmico, a mistura de reação se transforma em uma dispersão negra viscosa como pode ser visto na Figura 1. O que resulta após a purificação é uma solução MFC altamente concentrada que se comporta como um ferrofluido. O fluido no frasco responde em segundos quando colocado perto de um ímã portátil (<0,5 T), formando uma massa negra macroscópica que pode ser movida à medida que o ímã é colocado em diferentes locais.
Esta síntese produz produtos cuja dimensão e composição ferrita dependem da quantidade de água adicionada e da razão de manganês ao precursor de ferro na mistura de reação. A Figura 2 ilustra como a morfologia do cluster depende da água e da concentração precursora; também detalha as condições de reação utilizadas para obter as amostras listadas na Tabela 1. Descobrimos que o diâmetro do MFC é afetado pela quantidade de água adicionada, e a composição do MFC depende da razão de ferro e manganês nos precursores. Ambos os parâmetros podem, portanto, ser controlados independentemente para fazer uma biblioteca de MFCs com dimensões distintas e conteúdo de manganês.
Embora este seja um procedimento sintético muito simples, erros na execução do método podem levar a produtos com falha. A Figura 3 retrata amostras com morfologias irregulares de MFC. Na Figura 3A, os MFCs de forma ímpar resultam se a água for completamente excluída do ambiente de reação. A falta de água dificulta a montagem dinâmica dos nanocristais primários e resulta em uma distribuição muito ampla da dimensão do nanocíster e formas não esféricas16. As amostras apresentadas na Figura 3B apresentaram tempo de reação insuficiente (6-12 h) e, como resultado, não apresentaram crescimento nanocristal primário suficiente. Esses resultados ruins demonstram que uma quantidade adequada do reagente, bem como o tempo de reação, é necessária para alcançar clusters consistentes e uniformes.
Após a conclusão da síntese hidrotérmica, os MFCs ferrita foram separados e purificados por meio da separação magnética. Um ímã foi colocado sob a solução para forçar sua coleta no fundo do vaso. Impurezas e subprodutos não magnéticos formados na síntese, juntamente com o excesso de solvente, poderiam então ser decantados para produzir MFCs 27 puros e monodispersados. A Figura 4 ilustra o tempo necessário para uma coleta magnética quase completa dos MFCs com e sem a adição de lã de aço. A lã de aço colocada no frasco durante a separação magnética aumenta o gradiente do campo magnético dentro do frasco, permitindo uma separação muito mais rápida28.
Os MFCs purificados usando separação magnética mostram um alto grau de uniformidade em comparação com aqueles purificados usando um processo de ultracentrifugação mais convencional. A Figura 5 mostra a distribuição de tamanho dos MFCs obtidos por meio da separação magnética (A e B) em comparação com aqueles que usam ultracentrifugação (5.000 g por 30 min) (C e D). A separação magnética resulta em uma distribuição mais estreita do diâmetro do cluster em comparação com a ultracentrifugação e é a estratégia de purificação preferida para os MFCs.
Os MFCs sintetizados são revestidos com poliacrilato (PAA), que fornece uma superfície carregada negativamente e algum grau de repulsão interpartícula que impede a agregação interparticulas (Figura 6A). No entanto, realizando uma reação de substituição de ligantes com nitrodopamina (Figura 6B), podemos substituir o revestimento PAA por um revestimento copolímero de P(AA-co-AMPS-co-PEG), o que permite maior estabilidade em soluções de maior resistência iônica. A Figura 7 mostra o esquema deste processo de funcionalização superficial. A estabilidade coloidal dos MFCs dispersos em um tampão PBS é aparente na Figura 8. MFCs sintetizados revestidos com PAA rapidamente agregados e separados da solução dentro de 30 minutos e são de pouca utilidade em aplicações biológicas. Em contrapartida, os MFCs funcionais com um revestimento polissulfonato permaneceram bem dispersos nesta solução por mais de 2 dias sem qualquer sinal de agregação. A modificação da superfície pós-síntese descrita aqui fornece uma rota para a formação de soluções homogêneas de MFCs apropriadas para introdução em ambientes biológicos.
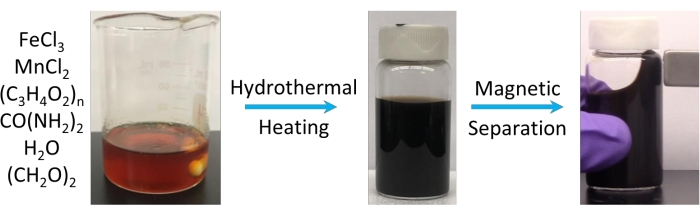
Figura 1: O esquema para a síntese de nanoaglomerados de ferrite de manganês. Os reagentes, cloreto de ferro(III), cloreto de manganês(II), ácido poliacrílico (PAA), ureia, água e etileno glicol são combinados em condições hidrotermais para produzir os nanoaglomerados de ferrite de manganês. Este produto forma uma solução coloidal estável em água pura, como mostrado no meio. A quantidade de água adicionada na síntese e a razão entre manganês e ferro nos precursores são usadas para ajustar o tamanho do cluster e a composição do ferrite, respectivamente. Após a separação magnética, os nanoaglomerados formam um ferrofluido como mostrado à direita, indicando que são altamente responsivos até mesmo pequenos campos magnéticos aplicados. Clique aqui para ver uma versão maior desta figura.

Figura 2: Imagens do microscópio eletrônico de transmissão (TEM) dos nanoaglomerados de ferrite de manganês e suas distribuições de diâmetro. Nas imagens A-D, o diâmetro do cluster (Dc) aumenta como resultado da redução da quantidade de água adicionada na síntese. O diâmetro médio do cluster é de 31, 56, 74 e 120 nm para A, B, C e D, respectivamente, com composição constante de Mn0.15Fe2.85O4. Nas imagens E-H, a composição da ferrita muda monotonicamente em proporção à razão Mn/Fe dos precursores. Apesar de suas diferentes composições, um diâmetro de cluster quase equivalente é alcançado. Nossa síntese permite controle independente sobre o diâmetro do cluster e a composição ferrita, ambas características que são importantes para as propriedades magnéticas dos ferrites nanoescala. Clique aqui para ver uma versão maior desta figura.
| Etiqueta na Figura 2 | H2O (mL) | FeCl3 (mmol) | MnCl2 (mmol) | Composição ferrita | Dc (nm) | |
| Um | 1.5 | 1.3 | 0.7 | Mn0.15Fe2.85O4 | 34 | |
| B & G | 0.7 | 1.3 | 0.7 | Mn0.15Fe2.85O4 | 56 | |
| C | 0.5 | 1.3 | 0.7 | Mn0.15Fe2.85O4 | 74 | |
| D | 0.1 | 1.3 | 0.7 | Mn0.15Fe2.85O4 | 120 | |
| E | 1.3 | 2 | 0 | Fe3O4 | 56 | |
| F | 0.6 | 1.5 | 0.5 | Mn0.06Fe2.94O4 | 56 | |
| H | 2 | 1 | 1 | Mn0.6Fe2.4O4 | 55 | |
Tabela 1: Condições de reação para a síntese das amostras de nanoaglomerados mostradas na Figura 2. Outros parâmetros de síntese são: 20 mL glicol de etileno, 250 mg de PAA e 1,2 g de ureia. As misturas de reação são hidrotermicamente aquecidas a 200 °C por 20 h. Para A, B, C e D, diminuir o teor de água, mantendo outros parâmetros constantes resultou em aglomerados de diâmetros maiores. Para E, F, G e H, o aumento da razão de MnCl2to FeCl3in a mistura de reação inicial resultou em clusters com maiores proporções de manganês na estrutura do cluster. Variar a quantidade de água E, F, G e H ao mesmo tempo permite agrupamentos de diferentes composições, mas diâmetros quase equivalentes.
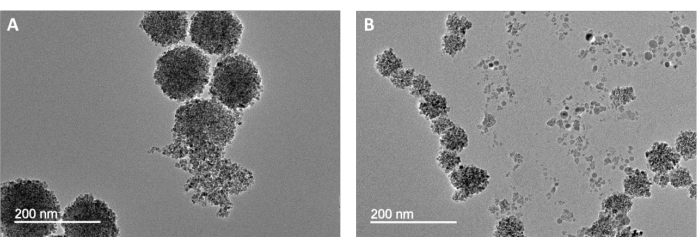
Figura 3: Imagens TEM de reações falhadas e incompletas. As pequenas características de contraste baixas observadas nessas imagens são nanocristais primários que não se desenvolveram em nanoglomerados. A amostra na Figura 3A foi preparada sem água adicional, enquanto o material mostrado na Figura 3B teve um tempo de reação insuficiente, de quatro horas. Clique aqui para ver uma versão maior desta figura.
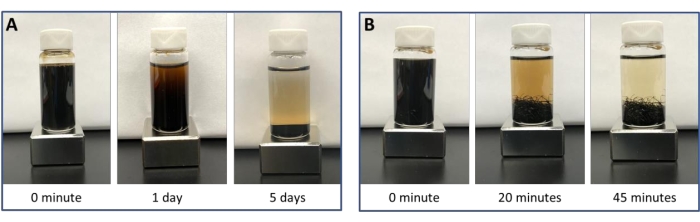
Figura 4: Comparação da separação magnética dos nanoaglomerados. Comparação da separação magnética de nanoaglomerados sem (A) e com (B) a adição de lã de aço no recipiente. A lã de aço aumenta o gradiente do campo magnético dentro do frasco para permitir uma separação magnética mais rápida dos nanoaglomerados. Como resultado, é possível ampliar a produção de nanoaglomerados de forma eficiente sem sacrificar a qualidade da amostra. Clique aqui para ver uma versão maior desta figura.

Figura 5: Comparação da ultracentrifugação e separação magnética. Comparação da ultracentrifugação (A,B) e separação magnética (C,D) e seu impacto na uniformidade dos aglomerados purificados. A e C são as imagens TEM dos clusters purificados, e B e D são as distribuições de tamanho dos clusters em A e C, respectivamente. O eixo y representa o número de clusters contados, e para cada amostra, foram pesquisados um total de 150 clusters. Clique aqui para ver uma versão maior desta figura.
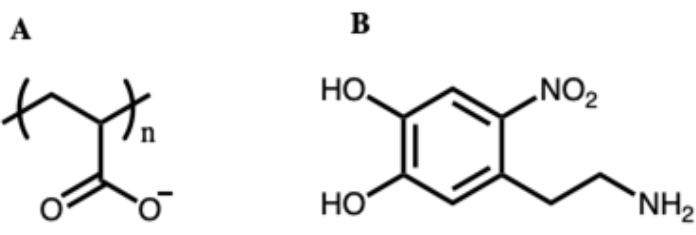
Figura 6: A estrutura de poli(ácido acrílico) (PAA) (A) e nitro-dopamina (B) utilizada na etapa de modificação da superfície. O revestimento inicial de PAA usado na síntese não é ideal em mídia biológica ou ácida devido, pois o ácido carboxílico é facilmente protoado. Nitro-dopamina é usado para substituir o revestimento PAA criando um grupo funcional para ancorar um copolímero sulfoto. Clique aqui para ver uma versão maior desta figura.
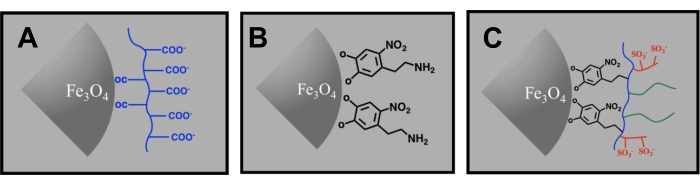
Figura 7: Esquemas do processo de modificação da superfície do cluster. (A) revestimento PAA original, (B) revestimento intermediário de nitro-dopamina e (C) o revestimento P (AA-co-AMPS-co-PEG). Em (C), as curvas azul, vermelha e verde representam as unidades AA, AMPS e PEG, respectivamente. A composição do cluster pode ser Fe3O4 ou MnxFe3-xO4. Clique aqui para ver uma versão maior desta figura.

Figura 8: A funcionalidade superficial dos nanoaglomerados com polisulfonato leva a materiais que são coloidalmente estáveis sob muitas condições aquosas diferentes. Os clusters com dois revestimentos de superfície diferentes, como sintetizado, a superfície revestida de PAA (A) e P(AA-co-AMPS-co-PEG) são dissolvidas na solução tampão PBS que é relevante para configurações biológicas e observada para sua estabilidade coloidal ao longo do tempo. Clique aqui para ver uma versão maior desta figura.
Discussão
Este trabalho demonstra uma síntese de poliol modificada de nanocristais de ferrite de manganês agrupados em agregados de nanoescala uniforme29. Nesta síntese, o cloreto de ferro (III) e o cloreto de manganês(II) sofrem uma reação e redução da hidrólise forçada, formando MnxFe3-xO4 molecular. Estas moléculas de ferrite formam nanocristais primários sob a alta temperatura e alta pressão nos reatores, finalmente se reunindo em agregados esféricos denominados aqui aglomerados de ferrite magnetita (MFCs). Sem tempo de reação suficiente ou água suficiente, o processo de agregação não pode completar totalmente levando a partículas não uniformes e mal formadas. Por outro lado, dado tempo suficiente e água suficiente, o processo de cristalização e montagem de óxido de metal é completo e produz um aglomerado esférico uniforme composto por dezenas a centenas de nanocristais primários. Os nanocristais primários nesses materiais são duramente agregados, compartilhando algumas interfaces cristalinas, levando a uma alta suscetibilidade inicial, e resposta magnética pronunciada até mesmo aos pequenos campos disponíveis a partir de ímãs permanentes portáteis27. Como resultado, esses materiais têm grande potencial para aplicações na entrega de drogas, hipertermia magnética, ressonância magnética e imagem de partículas magnéticas30,31,32.
Descobrimos que a quantidade de água adicionada à mistura de reação inicial controla o diâmetro dos aglomerados montados. À medida que o teor de água nos reagentes é aumentado, o diâmetro dos aglomerados e o número de nanocristais primários agregados diminui. A faixa ideal é de 0,8 M a 5,0 M de água, condições que produzem, respectivamente, diâmetros de cluster variando de 150 nm a 30 nm. A água tem um papel importante nesse processo porque é necessário garantir a hidrólise rápida dos precursores metálicos, a agregação mais rápida de cristais primários e, consequentemente, aglomerados menores16. Como a síntese é extraordinariamente sensível à água, os reagentes manuseados sob condições ambientais de umidade variável podem absorver diferentes quantidades de água do ar. Isso pode afetar as dimensões subsequentes e a morfologia do produto. Embora o controle de umidade na maioria dos laboratórios de pesquisa (por exemplo, 30%-60% RH) seja suficiente para minimizar esse problema, esta é uma fonte de erro sistemático no procedimento relatado. O controle da relação manganês/ferro no produto é alcançado variando a proporção de manganês para precursores de ferro. Isso é surpreendente, pois em muitas reações hidrotérmicas o nível de doping dos produtos muitas vezes não está simplesmente relacionado com a estequiometria dos materiais iniciais4,6,8,12,13,17. Para essas condições, no entanto, a composição do produto é bem prevista pela razão dos precursores metálicos. Em conjunto, o controle independente tanto do diâmetro do cluster quanto de sua composição é possível através da manipulação direta das misturas reagentes iniciais.
Muitas vezes, a purificação de nanopartículas da mídia de reação é o passo mais demorado e intrincado na geração de materiais de alta qualidade. A ultracentrifugação é frequentemente aplicada para este fim e, embora isso seja eficaz na separação de nanopartículas de subprodutos moleculares, ela é mal adequada para remover produtos sólidos indesejados. Quando aplicada aqui à purificação de nanomateriais, a ultracentrifugação produz partículas relativamente polidisperses com dimensões e formas variáveis. É muito mais eficiente aproveitar a resposta magnética desses materiais aplicando separação magnética para melhorar a uniformidade e a pureza do produto final. Aceleramos a separação magnética criando gradientes muito altos de campos magnéticos dentro de frascos macroscópicos usando lã de aço imersa na solução e um ímã permanente de terras raras aplicado fora dos recipientes de amostra. Este arranjo permite que amostras uniformes sejam recuperadas em menos de trinta minutos com altos rendimentos (~90%). É importante combinar a quantidade de lã de aço introduzida à solução com os diâmetros esperados do cluster MFC. Por exemplo, um MFC com um diâmetro médio de 40 nm requer entre 100 a 200 mg de lã de aço para uma separação rápida, enquanto materiais maiores podem exigir muito menos ou até mesmo nenhuma lã de aço. Está bem estabelecido que menores das nanopartículas magnéticas são menos responsivas aos campos aplicados em virtude de seu menor volume magnético15,17,26. O processo de separação magnética fornece, assim, um meio de aguçar a uniformidade desses materiais, uma vez que os clusters menores não são retidos tão eficientemente pelo processo16. O uso deste método de separação magnética não só economiza tempo em laboratório, mas também resulta em produtos com maior uniformidade de diâmetro.
Embora os MFCs sintetizados sejam estáveis em água pura, eles apresentam baixa estabilidade coloidal em soluções com pH mais baixo ou maior resistência iônica. Ferrites de manganês têm grandes densidades de magnetização, e como resultado para esses diâmetros os aglomerados possuem dipolos magnéticos que levam à atração interpartícula. O revestimento nativo de poliacrilato usado durante a formação dos materiais transmite uma carga negativa às superfícies das partículas e ajuda a prevenir a agregação de partículas-partículas. No entanto, no pH inferior, os grupos carboxílicos são totalmente protoados, removendo a repulsão eletrostática necessária para manter dispersões homogêneas de MFC; alternativamente, em uma maior mídia de força iônica, a repulsão de carga é reduzida levando a mais agregação de partículas. A agregação dos MFCs cria materiais macroscópicos que não são homogeneamente dispersos na solução, tornando desafiador o uso dos materiais in vivo ou em aplicações que requerem superfícies de nanopartículas grandes e disponíveis. Por essas razões, introduzimos um segundo polímero na reação para substituir o revestimento PAA original. O copolímero, P(AA-co-AMPS-co-PEG), inclui polietileno glicol neutro (PEG) para fornecer biocompatibilidade e algum grau de obstáculo estérico. Além disso, o componente polissulfonato (PAMPS) oferece tanto uma densidade de carga maior do que o poliacrilato, bem como um grupo funcional que tem uma pKa muito menor e, consequentemente, uma maior faixa de pH de trabalho (pKa ~ 1,2)24. Os aglomerados de ferrite de manganês modificados com esses revestimentos superficiais mostram uma estabilidade dramaticamente aumentada nos meios ácidos e biológicos. O procedimento para garantir a modificação correta da superfície é detalhado, no entanto, e deve ser seguido cuidadosamente para garantir que as amostras sejam efetivamente revestidas. Especificamente, o método requer monitoramento constante da mistura de reação enquanto é tratado com um sônico sonda para garantir a substituição homogênea e completa do revestimento poliacrilato inicial. Também é importante usar vidros de tamanho adequado para minimizar qualquer perda de produto durante a sônica vigorosa e aplicar um banho de gelo na mistura de sônica para minimizar a degradação térmica dos polímeros causados pela sônica da sonda.
Em conclusão, este método permite a produção rápida e eficiente de aglomerados de ferrite de manganês (MFCs) com diâmetros tíficos e manganês para composições de ferro. O teor de água reagente, bem como a razão entre ferro e manganês são parâmetros importantes na definição das características do produto material. Uma simples técnica de separação magnética utilizando um ímã portátil e lã de aço fornece um meio eficiente de purificar o produto após a síntese produzindo clusters mais uniformes. Finalmente, um copolímero PEG sulfoado é aplicado aos materiais para garantir que eles permaneçam não agregando em uma variedade de diferentes pH e mídia de força iônica. O aumento da capacidade de resposta magnética desses óxidos de ferro dopados por manganês em comparação com os nanomateriais puros de óxido de ferro (Fe3O4) torna mais simples, mais barato e mais fácil desenvolver dispositivos para aplicar campos externos para manipular os materiais in vivo. Seus revestimentos de superfície melhorados também são importantes como aplicações para nanopartículas magnéticas na entrega de drogas, remediação da água e sistemas avançados de imagem, todos requerem materiais que não agregam e homogêneos em uma variedade de mídias biológicas e ambientais.
Divulgações
Os autores não têm nada a revelar.
Agradecimentos
Este trabalho foi generosamente apoiado pela Universidade Brown e pelo Consórcio de Energia Avançada. Agradecemos ao Dr. Qingbo Zhang por seu método sintético estabelecido de MFCs de óxido de ferro.
Materiais
| Name | Company | Catalog Number | Comments |
| 0.1 Micron Vaccum Filtration Filter | Thermo Fisher Scientific | NC9902431 | for filtration of aggregated clusters after synthesis and surface coating to achieve a uniform solution |
| 2-Acrylamido-2-methylpropane sulfonic acid (AMPS, 99%) | Sigma-Aldrich | 282731-250G | reagent used in copolymer to surface coat nanoclusters and functionalize them for biological media |
| 2,2′-Azobis(2-methylpropionitrile) (AIBN) | Sigma-Aldrich | 441090-100G | reagent used in copolymer making as the free ridical generator |
| 4-Morpholineethanesulfonic acid, 2-(N-Morpholino)ethanesulfonic acid (MES) | Sigma-Aldrich | M3671-250G | acidic buffer used to stabilize nanocluster surface coating process |
| Acrylic acid | Sigma-Aldrich | 147230-100G | reagent used in copolymer to surface coat nanoclusters and functionalize them for biological media; anhydrous, contains 200 ppm MEHQ as inhibitor, 99% |
| Analytical Balance | Avantor | VWR-205AC | used to weigh out solid chemical reagents for use in synthesis and dilution |
| Digital Sonifier and Probe | Branson | B450 | used to sonicate nanocluster solution during surface coating to break up aggregates |
| Dopamine hydrochloride | Sigma-Aldrich | H8502-25G | used in surface coating for ligand exchange reaction |
| Ethylene glycol (anhydrous, 99.8%) | Sigma-Aldrich | 324558-2L | reagent used as solvent in hydrothermal synthesis of nanoclusters |
| Glass Vials (20mL) | Premium Vials | B1015 | container for nanocluster solution during washing and surface coating as well as polymer solutions |
| Graduated Beaker (100mL) | Corning | 1000-100 | container for mixing of solid and liquid reagents during hydrothermal synthesis (to be transferred into autoclave reactor before oven) |
| Handheld Magnet | MSC Industrial Supply, Inc. | 92673904 | 1/2" Long x 1/2" Wide x 1/8" High, 5 Poles, Rectangular Neodymium Magnet low strength magnet used to precipitate nanoclusters from solution (field strength is increased with steel wool when needed) |
| Hydrochloric acid (ACS grade, 37%) | Fisher Scientific | 7647-01-0 | for removing leftover nanocluster debris and cleaning autoclave reactors for next use |
| Hydrothermal Autoclave Reactor | Toption | TOPT-HP500 | container for finished reagent mixture to withstand high temperature and pressure created by the oven in hydrothermal synthesis |
| Iron(III) Chloride Hexahydrate (FeCl3·6H2O, ACS reagent, 97%) | ACS | 236489-500G | reagent used in synthesis of nanoclusters as source of iron (III) that becomes iron (II) in finished nanocluster product (keep dry and weigh out quickly to avoid water contamination) |
| Labware Washer Brushes | Fisher Scientific | 13-641-708 | used to wash and clean glassware before synthesis |
| Magnetic Stir Plate | Thermo Fisher Scientific | 50093538 | for mixing of solid and liquid reagents during hydrothermal synthesis |
| Manganese chloride tetrahydrate (MnCl2·4H2O, 99.0%, crystals, ACS) | Sigma-Aldrich | 1375127-2G | reagent used in synthesis of nanoclusters as source of manganese |
| Micropipette (100-1000μL) | Thermo Fisher Scientific | FF-1000 | for transferring liquid reagents such as water and manganese chloride |
| N-(3-Dimethylaminopropyl)-N′-ethylcarbodiimide hydrochloride (EDC) | Sigma-Aldrich | 25952-53-8 | used in surface coating to assist in ligand exchange of copolymer (keep bulk chemical in freezer and diluted solution in refrigerator) |
| N,N-Dimethylformamide (DMF) | Sigma-Aldrich | 227056-2L | reagent used in copolymer making as the solvent |
| Polyacrylic acid sodium salt (PAA, Mw~6,000) | PolyScience Inc. | 06567-250 | reagent used in hydrothermal synthesis to initially coat the nanoclusters (eventually replaced in surface coating step) |
| Poly(ethylene glycol) methyl ether acrylate | Sigma-Aldrich | 454990-250ML | reagent used in copolymer to surface coat nanoclusters and functionalize them for biological media; average Mn 480, contains 100 ppm BHT as inhibitor, 100 ppm MEHQ as inhibitor |
| Reagents Acetone, 4L, ACS Reagent | Cole-Parmer | UX-78920-66 | used as solvent to precipitate nanoclusters during washing |
| Single Channel Pipette, Adjustable 1-10 mL | Eppendorf | 3123000080 | for transferring ethylene glycol and other liquids |
| Steel Wool | Lowe's | 788470 | used to increase the magnetic field strength in the vial to aid in precipitation of nanoclusters for washing and surface coating |
| Stirring Bar | Thomas Scientific | 8608S92 | for mixing of solid and liquid reagents during hydrothermal synthesis |
| Table Clamp | Grainger | 29YW53 | for tight sealing of autoclave reactor to withstand high pressure of oven during hyrothermal synthesis |
| Urea (ACS reagent, 99.0%) | Sigma-Aldrich | U5128-500G | reagent used in hydrothermal synthesis to create a basic solution |
| Vaccum Filtration Bottle Tops | Thermo Fisher Scientific | 596-3320 | for filtration of aggregated clusters after synthesis and surface coating to achieve a uniform solution |
| Vacuum Controller V-850 | Buchi | BU-V850 | for filtration of aggregated clusters after synthesis and surface coating to achieve a uniform solution |
| Vacuum Oven | Fisher Scientific | 13-262-51 | used to create high temperature and pressure needed for nanocluster formation in hydrothermal synthesis |
Referências
- Makridis, A., et al. In vitro application of Mn-ferrite nanoparticles as novel magnetic hyperthermia agents. Journal of Materials Chemistry B. 2 (47), 8390-8398 (2014).
- Nelson-Cheeseman, B., Chopdekar, R., Toney, M., Arenholz, E., Suzuki, Y. Interplay between magnetism and chemical structure at spinel-spinel interfaces. Journal of Applied Physics. 111 (9), 093903 (2012).
- Otero-Lorenzo, R., Fantechi, E., Sangregorio, C., Salgueiriño, V. Solvothermally driven Mn doping and clustering of iron oxide nanoparticles for heat delivery applications. Chemistry-A European Journal. 22 (19), 6666-6675 (2016).
- Mohapatra, J., et al. Enhancement of magnetic heating efficiency in size controlled MFe 2 O 4 (M= Mn, Fe, Co and Ni) nanoassemblies. Rsc Advances. 5 (19), 14311-14321 (2015).
- Qi, Y., et al. Carboxylic silane-exchanged manganese ferrite nanoclusters with high relaxivity for magnetic resonance imaging. Journal of Materials Chemistry B. 1 (13), 1846-1851 (2013).
- Anandhi, J. S., Jacob, G. A., Joseyphus, R. J. Factors affecting the heating efficiency of Mn-doped Fe3O4 nanoparticles. Journal of Magnetism and Magnetic Materials. 512, 166992 (2020).
- Del Bianco, L., et al. Mechanism of magnetic heating in Mn-doped magnetite nanoparticles and the role of intertwined structural and magnetic properties. Nanoscale. 11 (22), 10896-10910 (2019).
- Padmapriya, G., Manikandan, A., Krishnasamy, V., Jaganathan, S. K., Antony, S. A. Enhanced catalytic activity and magnetic properties of spinel Mn x Zn 1−x Fe 2 O 4 (0.0≤x≤1.0) nano-photocatalysts by microwave irradiation route. Journal of Superconductivity and Novel Magnetism. 29 (8), 2141-2149 (2016).
- Kim, J., et al. Continuous O2-evolving MnFe2O4 nanoparticle-anchored mesoporous silica nanoparticles for efficient photodynamic therapy in hypoxic cancer. Journal of the American Chemical Society. 139 (32), 10992-10995 (2017).
- Silva, L. H., Cruz, F. F., Morales, M. M., Weiss, D. J., Rocco, P. R. Magnetic targeting as a strategy to enhance therapeutic effects of mesenchymal stromal cells. Stem Cell Research & Therapy. 8 (1), 1-8 (2017).
- Otero-Lorenzo, R., Ramos-Docampo, M. A., Rodriguez-Gonzalez, B., Comesaña-Hermo, M., Salgueiriño, V. Solvothermal clustering of magnetic spinel ferrite nanocrystals: a Raman perspective. Chemistry of Materials. 29 (20), 8729-8736 (2017).
- Aghazadeh, M., Karimzadeh, I., Ganjali, M. R. PVP capped Mn2+ doped Fe3O4 nanoparticles: a novel preparation method, surface engineering and characterization. Materials Letters. 228, 137-140 (2018).
- Li, Z., et al. Solvothermal synthesis of MnFe 2 O 4 colloidal nanocrystal assemblies and their magnetic and electrocatalytic properties. New Journal of Chemistry. 39 (1), 361-368 (2015).
- Guo, P., Zhang, G., Yu, J., Li, H., Zhao, X. Controlled synthesis, magnetic and photocatalytic properties of hollow spheres and colloidal nanocrystal clusters of manganese ferrite. Colloids and Surfaces A: Physicochemical and Engineering Aspects. 395, 168-174 (2012).
- Pardo, A., et al. Synthesis, characterization, and evaluation of superparamagnetic doped ferrites as potential therapeutic nanotools. Chemistry of Materials. 32 (6), 2220-2231 (2020).
- Xiao, Z., et al. Libraries of uniform magnetic multicore nanoparticles with tunable dimensions for biomedical and photonic applications. ACS Applied Materials & Interfaces. 12 (37), 41932-41941 (2020).
- Choi, Y. S., Young Yoon, H., Sung Lee, J., Hua Wu, J., Keun Kim, Y. Synthesis and magnetic properties of size-tunable Mn x Fe3−x O4 ferrite nanoclusters. Journal of Applied Physics. 115 (17), (2014).
- Creixell, M., et al. The effect of grafting method on the colloidal stability and in vitro cytotoxicity of carboxymethyl dextran coated magnetic nanoparticles. Journal of Materials Chemistry. 20 (39), 8539-8547 (2010).
- Latorre, M., Rinaldi, C. Applications of magnetic nanoparticles in medicine: magnetic fluid hyperthermia. Puerto Rico Health Sciences Journal. 28 (3), (2009).
- Yeap, S. P., Lim, J., Ooi, B. S., Ahmad, A. L. Agglomeration, colloidal stability, and magnetic separation of magnetic nanoparticles: collective influences on environmental engineering applications. Journal of Nanoparticle Research. 19 (11), 1-15 (2017).
- Lee, S. -. Y., Harris, M. T. Surface modification of magnetic nanoparticles capped by oleic acids: Characterization and colloidal stability in polar solvents. Journal of Colloid and Interface Science. 293 (2), 401-408 (2006).
- Yeap, S. P., Ahmad, A. L., Ooi, B. S., Lim, J. Electrosteric stabilization and its role in cooperative magnetophoresis of colloidal magnetic nanoparticles. Langmuir. 28 (42), 14878-14891 (2012).
- Wydra, R. J., Oliver, C. E., Anderson, K. W., Dziubla, T. D., Hilt, J. Z. Accelerated generation of free radicals by iron oxide nanoparticles in the presence of an alternating magnetic field. RSC Advances. 5 (24), 18888-18893 (2015).
- Bagaria, H. G., et al. Iron oxide nanoparticles grafted with sulfonated copolymers are stable in concentrated brine at elevated temperatures and weakly adsorb on silica. ACS Applied Materials & Interfaces. 5 (8), 3329-3339 (2013).
- Park, J. C., Park, T. Y., Cha, H. J., Seo, J. H. Multifunctional nanocomposite clusters enabled by amphiphilic/bioactive natural polysaccharides. Chemical Engineering Journal. 379, 122406 (2020).
- Hemery, G., et al. Tuning sizes, morphologies, and magnetic properties of monocore versus multicore iron oxide nanoparticles through the controlled addition of water in the polyol synthesis. Inorganic Chemistry. 56 (14), 8232-8243 (2017).
- Lartigue, L., et al. Cooperative organization in iron oxide multi-core nanoparticles potentiates their efficiency as heating mediators and MRI contrast agents. ACS Nano. 6 (12), 10935-10949 (2012).
- Yavayo, C. T., et al. Low-field magnetic separation of monodisperse Fe3O4 nanocrystals. Science. 314 (5801), 964-967 (2006).
- Matijević, E., Scheiner, P. Ferric hydrous oxide sols: III. Preparation of uniform particles by hydrolysis of Fe (III)-chloride,-nitrate, and-perchlorate solutions. Journal of Colloid and Interface Science. 63 (3), 509-524 (1978).
- Weizenecker, J., Gleich, B., Rahmer, J., Dahnke, H., Borgert, J. Three-dimensional real-time in vivo magnetic particle imaging. Physics in Medicine & Biology. 54 (5), 1 (2009).
- Zhu, X., Li, J., Peng, P., Hosseini Nassab, N., Smith, B. R. Quantitative drug release monitoring in tumors of living subjects by magnetic particle imaging nanocomposite. Nano Letters. 19 (10), 6725-6733 (2019).
- Tay, Z. W., et al. Magnetic particle imaging-guided heating in vivo using gradient fields for arbitrary localization of magnetic hyperthermia therapy. ACS Nano. 12 (4), 3699-3713 (2018).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados