Method Article
Sospensioni acquose stabili di cluster di ferrite di manganese con dimensioni e composizione su scala nanometrica sintonizzabili
* Questi autori hanno contribuito in egual misura
In questo articolo
Riepilogo
Riportiamo una sintesi idrotermale one-pot di cluster di ferrite di manganese (MFC) che offre un controllo indipendente sulla dimensione e la composizione del materiale. La separazione magnetica consente una rapida purificazione, mentre la funzionalizzazione superficiale con polimeri solfonati garantisce che i materiali non siano aggregati in mezzi biologicamente rilevanti. I prodotti risultanti sono ben posizionati per applicazioni biomediche.
Abstract
Gli ammassi di ferrite di manganese (MFC) sono assemblaggi sferici da decine a centinaia di nanocristalli primari le cui proprietà magnetiche sono preziose in diverse applicazioni. Qui descriviamo come formare questi materiali in un processo idrotermale che consente il controllo indipendente della dimensione del cluster di prodotto (da 30 a 120 nm) e del contenuto di manganese del materiale risultante. Parametri come la quantità totale di acqua aggiunta al mezzo di reazione alcolico e il rapporto tra manganese e precursore del ferro sono fattori importanti per ottenere più tipi di prodotti su scala nanometrica MFC. Un metodo di purificazione veloce utilizza la separazione magnetica per recuperare i materiali rendendo la produzione di grammi di nanomateriali magnetici abbastanza efficiente. Superiamo la sfida dell'aggregazione magnetica dei nanomateriali applicando polimeri solfonati altamente carichi sulla superficie di questi nanomateriali producendo MFC colloidali stabili che rimangono non aggreganti anche in ambienti altamente salini. Questi materiali non aggreganti, uniformi e sintonizzabili sono eccellenti materiali prospettici per applicazioni biomediche e ambientali.
Introduzione
L'inclusione del manganese come drogante in un reticolo di ossido di ferro può, nelle condizioni appropriate, aumentare la magnetizzazione del materiale in campi applicati elevati rispetto agli ossidi di ferro puri. Di conseguenza, le nanoparticelle di ferrite di manganese (MnxFe3-xO4) sono nanomateriali magnetici altamente desiderabili grazie alla loro elevata magnetizzazione a saturazione, alla forte risposta ai campi esterni e alla bassa citotossicità1,2,3,4,5. Sia i nanocristalli a dominio singolo che i cluster di questi nanocristalli, chiamati particelle multidominio, sono stati studiati in diverse applicazioni biomediche, tra cui la somministrazione di farmaci, l'ipertermia magnetica per il trattamento del cancro e la risonanza magnetica (MRI)6,7,8. Ad esempio, il gruppo Hyeon nel 2017 ha utilizzato nanoparticelle di ferrite di manganese a dominio singolo come catalizzatore Fenton per indurre l'ipossia del cancro e ha sfruttato il contratto T2 del materiale per il monitoraggio della risonanza magnetica9. È sorprendente alla luce di questi e di altri studi positivi sui materiali in ferrite che ci siano poche dimostrazioni in vivo rispetto ai nanomateriali di ossido di ferro puro (Fe3O4) e nessuna applicazione segnalata nell'uomo9,10.
Un'immensa sfida affrontata nel tradurre le caratteristiche dei nanomateriali di ferrite nella clinica è la generazione di cluster uniformi, non aggregati, su scala nanometrica11,12,13,14. Mentre gli approcci sintetici convenzionali ai nanocristalli monodominio sono ben sviluppati, i cluster multidominio del tipo di interesse in questo lavoro non sono facilmente prodotti in modo uniforme e controllato15,16. Inoltre, la composizione della ferrite è solitamente non stechiometrica e non semplicemente correlata alla concentrazione iniziale dei precursori e questo può ulteriormente oscurare la caratterizzazione sistematica struttura-funzione di questi materiali9,12,13,17. Qui, affrontiamo questi problemi dimostrando un approccio sintetico che produce un controllo indipendente sia sulla dimensione del cluster che sulla composizione dei nanomateriali di ferrite di manganese.
Questo lavoro fornisce anche un mezzo per superare la scarsa stabilità colloidale dei nanomateriali di ferrite18,19,20. Le nanoparticelle magnetiche sono generalmente inclini all'aggregazione a causa della forte attrazione particella-particella; le ferriti soffrono maggiormente di questo problema poiché la loro maggiore magnetizzazione netta amplifica l'aggregazione delle particelle. Nei mezzi biologici rilevanti, questi materiali producono aggregati abbastanza grandi che i materiali raccolgono rapidamente, limitando così le loro vie di esposizione agli animali o alle persone20,21,22. Hilt et al. hanno trovato un'altra conseguenza dell'aggregazione particella-particella nel loro studio del riscaldamento magnetotermico e della degradazione del colorante23. A concentrazioni di particelle leggermente più elevate o ad un aumento del tempo di esposizione al campo, l'efficacia dei materiali è stata ridotta man mano che i materiali si aggregavano nel tempo e le aree superficiali delle particelle attive diminuivano. Queste e altre applicazioni trarrebbero beneficio dalle superfici a grappolo progettate per fornire barriere steriche che precludessero le interazioni particella-particella24,25.
Qui riportiamo un approccio sintetico per sintetizzare cluster di ferrite di manganese (MFC) con dimensioni e composizione controllabili. Queste particelle multidominio sono costituite da un insieme di nanocristalli primari di ferrite di manganese che sono aggregati duramente; la stretta associazione dei nanocristalli primari ne esalta le proprietà magnetiche e fornisce una dimensione complessiva del cluster, 50-300 nm, ben abbinata alle dimensioni ottimali per una nanomedicina. Modificando la quantità di acqua e precursore del cloruro di manganese, possiamo controllare in modo indipendente il diametro e la composizione complessivi. Il metodo utilizza reazioni idrotermali one-pot semplici ed efficienti che consentono frequenti sperimentazioni e ottimizzazione dei materiali. Questi MFC possono essere facilmente purificati in una soluzione di prodotto concentrato, che viene ulteriormente modificata da polimeri solfonati che conferiscono stabilità colloidale. La loro sintoniabilità, uniformità e stabilità della fase di soluzione sono tutte caratteristiche di grande valore nelle applicazioni dei nanomateriali nell'ingegneria biomedica e ambientale.
Protocollo
1. Sintesi di MFC con controllo del diametro complessivo e della composizione della ferrite delle MFC
- Lavare e asciugare accuratamente tutti gli oggetti in vetro da utilizzare nella sintesi. La quantità di acqua nella sintesi influisce sulle dimensioni delle MFC, quindi è fondamentale assicurarsi che la vetreria non contenga acqua residua16,26.
- Per lavare i bicchieri, risciacquare con acqua e detersivo e strofinare con una spazzola a palloncino per rimuovere i detriti. Risciacquare abbondantemente per rimuovere tutto il detergente e terminare con un risciacquo di acqua deionizzata.
- Per asciugare la vetreria, scuotere le gocce d'acqua dalla superficie della vetreria e metterle in forno a 60 ° C fino a completa asciugatura.
- Risciacquare i reattori rivestiti di polifenilene (PPL) con il 37% di acido cloridrico per rimuovere eventuali detriti dall'uso precedente. Per fare questo, posizionare i reattori e i loro tappi in un grande becher e riempire con acido cloridrico fino a quando i reattori non sono completamente sommersi. Lasciare riposare per 30 minuti prima di versare l'acido cloridrico. Risciacquare continuamente il becher contenente i reattori con acqua per 1-2 minuti, quindi posizionare i reattori nel forno ad asciugare.
- Utilizzare una pipetta automatica per trasferire 20 mL di glicole etilenico in un becher da 50 mL con una barra magnetica.
- Pesare la quantità richiesta di cloruro di ferro (III) (FeCl3·6H2O, solido) per ottenere una concentrazione finale di 1,3 mM e aggiungerla al becher. Metti il becher su una piastra di agitazione e accendilo a 480 giri / min per iniziare a mescolare continuamente il becher.
NOTA: Poiché si tratta di un idrato, deve essere misurato e aggiunto rapidamente per evitare l'assorbimento indesiderato di acqua dall'aria ambiente. - Pesare 250 mg di acido poliacrilico (PAA, Mw ~ 6.000, polvere) e aggiungerlo al becher. Dopo l'aggiunta di PAA, la soluzione diventa opaca e leggermente più chiara.
- Pesare 1,2 g di urea (CO(NH2)2, polvere) e aggiungerlo al becher.
- Utilizzando una pipetta, aggiungere 0,7 mM di cloruro di manganese (II) (MnCl2·6H2O aq, 3,5 M, 0,2 mL) al becher.
- Infine, utilizzando una pipetta aggiungere la quantità richiesta (0,5 ml) di acqua ultrapura al becher.
- Lasciare che la soluzione si mescoli per 30 minuti e notare il cambiamento di colore. Si presenterà come un colore arancione scuro traslucido.
- Trasferire la miscela di reazione nel reattore rivestito di polifenilene (PPL). Si noti che dopo che la soluzione è stata mescolata alcuni solidi potrebbero essersi accumulati sui lati del becher.
- Utilizzare un magnete (magnete cubico permanente in terre rare, 40 x 40 x 20 mm, di seguito denominato "magnete" per tutte le procedure di separazione e raccolta magnetica) per trascinare la barra di agitazione attorno alle pareti del becher per garantire che tutti i solidi che si sono accumulati sui lati siano dispersi nella soluzione di reazione.
- Una volta che la soluzione è miscelata e pronta, trasferirla nel reattore rivestito in PPL da 50 ml.
- Utilizzare un morsetto e una leva per sigillare il reattore nell'autoclave in acciaio inossidabile il più strettamente possibile. Bloccare il recipiente del reattore su una superficie stabile e, utilizzando un'asta inserita nel cappuccio come leva, spingere il reattore a sigillare. Si noti che il reattore sigillato non dovrebbe poter essere aperto a mano. Questo è fondamentale in quanto l'ambiente ad alta pressione del forno richiede una tenuta ermetica sul reattore.
- Mettere il reattore in un forno per 20 ore a 215 °C.
- Al termine della reazione idrotermale, rimuovere il reattore dal forno e lasciarlo raffreddare a temperatura ambiente. La pressione del forno consentirà di aprire il reattore a mano. Si noti che a questo punto, il reattore conterrà il prodotto MFC disperso nel glicole etilenico con altre impurità, come il polimero non reagito, e sarà una soluzione nera opaca. Il prodotto verrà isolato nei seguenti passaggi.
2. Separazione magnetica e purificazione delle MFC
- Introdurre 200 mg di lana d'acciaio in un flaconcino di vetro. Riempire il flaconcino di vetro a metà strada con la miscela di reazione del reattore. Riempire il resto del flaconcino con acetone e agitare bene. Si noti che la lana d'acciaio aumenta l'intensità del campo magnetico nella fiala e aiuterà la separazione magnetica dei nanocluster dalla soluzione.
- Posizionare il flaconcino su un magnete per la raccolta magnetica. Il risultato sarà una soluzione traslucida con precipitato nella parte inferiore.
- Versare la soluzione surnatante mentre le MFC sono intrappolate magneticamente dalla lana d'acciaio tenendo il magnete sul fondo del flaconcino durante il versamento. Il glicole etilenico sarà per lo più rimosso in questa fase.
- Iniziare il lavaggio con il basso rapporto tra acetone e acqua e aumentare il rapporto nei lavaggi successivi fino a quando non è puro. Fallo 3-4 volte.
- Rimuovere il flaconcino dal magnete e riempirlo d'acqua. Agitare bene per sciogliere gli MFC. Ora il prodotto sarà completamente disperso in acqua.
- Ripetere più volte i due passaggi precedenti fino a quando la soluzione acquosa degli MFC non produce bolle quando viene scossa. Il risultato sarà un ferrofluido scuro e opaco che risponderà fortemente ai magneti.
NOTA: In una sintesi tipica con 20 ml di glicole etilenico, si otterranno circa 80 mg di prodotto MFC.
3. Funzionalizzazione superficiale delle MFC verso un'altissima stabilità colloidale
NOTA: La sintesi di nitro-dopamina e Poly(AA-co-AMPS-co-PEG) può essere trovata nel nostro lavoro precedente16. Il copolimero è realizzato attraverso la polimerizzazione dei radicali liberi. Aggiungere 0,20 g di 2,2′-Azobis(2-metilpropionitrile) (AIBN), 0,25 g di acido acrilico (AA), 0,75 g di acido 2-acrilammido-2-metilpropano solfonico (AMPS) e 1,00 g di policil(glicole etilenico) acrilato di metile (PEG) in 10 ml di N,N-dimetilformammide (DMF). Riscaldare la miscela a bagnomaria a 70 °C per 1 ora e trasferirla in una sacca per dialisi (Membrana di Cellulosa, 3 kDa) in acqua. Il rapporto di peso di AA, AMPS e PEG è 1:3:4. La polimerizzazione per questi monomeri ha un tasso di conversione del 100%, come confermato dalla liofilizzazione e dalla pesatura.
- Combinare 10 mL di nanoparticelle purificate (circa 100 mg) in un flaconcino da 20 mL con 10 mL di soluzione satura di N-[2-(3,4-diidrossifenil)etil]nitramide (nitro-dopamina) (~1 mg/mL). Attendere 5 minuti.
- Lavare gli MFC rivestiti con nitro-dopamina utilizzando la separazione magnetica. Versare il surnatante giallo pallido. Aggiungere acqua e agitare energicamente. Quindi, versare acqua usando il magnete per trattenere il prodotto. Ripetere questo lavaggio più volte lasciando la raccolta marrone scuro nel flaconcino.
NOTA: Preparare una soluzione acquosa con una concentrazione di 20 mg/ml, una soluzione tampone con una concentrazione di 100 mg/mL e una soluzione polimerica poli(AA-co-AMPS-co-PEG) con una concentrazione di 20 mg/ml. - Miscelare 1 mL di soluzione EDC, 1 mL di tampone MES e 3 mL di soluzione polimerica. Mescolare leggermente facendo roteare il composto e lasciarlo riposare per circa 5 minuti. Dovrebbe essere una soluzione chiara e incolore quando completamente combinata.
- Aggiungere questa miscela alla raccolta MFC e posizionare il flaconcino in un bagno di ghiaccio. Abbassare il sonicatore della sonda nella soluzione, quindi accenderlo (250 watt di potenza a 20 kHz).
- Dopo un trattamento di sonicazione di 5 minuti, aggiungere circa 5 ml di acqua ultrapura alla fiala mentre il sonicatore è ancora in funzione. Continuare a monitorare la nave per assicurarsi che nessun prodotto fuoriuscisca. Mantenere il ghiaccio nella miscela ghiaccio-acqua poiché parte del ghiaccio iniziale si scioglierà a causa dell'intensità e del calore della sonicazione.
- Lasciare sonicare la miscela per altri 25 minuti, per un totale di 30 minuti.
- Posizionare il flaconcino sopra un magnete per separare gli MFC e versare la soluzione surnatante.
- Lavare più volte gli MFC modificati con acqua deionizzata.
- Riempire il flaconcino contenente gli MFC con acqua purissima. Pipettare questo fluido in un sistema di filtrazione sotto vuoto con un filtro a membrana di polietersolfone da 0,1 μm per rimuovere eventuali MFC aggregati irreversibilmente. Assicurarsi di lavare le pareti dell'imbuto per ridurre al minimo qualsiasi perdita di prodotto.
- Filtrare a vuoto la soluzione. Ripeti questo processo 2-3 volte. Il risultato sarà una soluzione acquosa purificata di MFC monodispersi.
NOTA: Circa il 10% del prodotto sarà aggregato in modo irreversibile e questo materiale rimarrà sul filtro e dovrà essere scartato.
Risultati
Dopo il trattamento idrotermale, la miscela di reazione si trasforma in una dispersione nera viscosa come si può vedere nella Figura 1. Ciò che risulta dopo la purificazione è una soluzione MFC altamente concentrata che si comporta come un ferrofluido. Il fluido nel flaconcino risponde in pochi secondi quando viene posizionato vicino a un magnete portatile (<0,5 T), formando una massa nera macroscopica che può essere spostata mentre il magnete viene posizionato in posizioni diverse.
Questa sintesi produce prodotti la cui dimensione e composizione della ferrite dipendono dalla quantità di acqua aggiunta e dal rapporto tra manganese e precursore del ferro nella miscela di reazione. La Figura 2 illustra come la morfologia del cluster dipenda dalla concentrazione di acqua e precursori; descrive inoltre in dettaglio le condizioni di reazione utilizzate per ottenere i campioni elencati nella tabella 1. Troviamo che il diametro MFC è influenzato dalla quantità di acqua aggiunta e la composizione MFC dipende dal rapporto tra ferro e manganese nei precursori. Entrambi i parametri possono quindi essere controllati in modo indipendente per creare una libreria di MFC con dimensioni distinte e contenuto di manganese.
Sebbene si tratti di una procedura sintetica molto semplice, errori nell'esecuzione del metodo possono portare a prodotti falliti. La Figura 3 illustra campioni con morfologie MFC irregolari. Nella Figura 3A, gli MFC di forma dispari si verificano se l'acqua è completamente esclusa dall'ambiente di reazione. La mancanza di acqua ostacola l'assemblaggio dinamico dei nanocristalli primari e si traduce in una distribuzione molto ampia delle dimensioni nanocluster e delle forme non sferiche16. I campioni mostrati nella Figura 3B avevano un tempo di reazione insufficiente (6-12 ore) e di conseguenza non avevano una crescita nanocristallina primaria sufficiente. Questi scarsi risultati dimostrano che una quantità appropriata del reagente, così come il tempo di reazione, è necessaria per ottenere cluster coerenti e uniformi.
Dopo il completamento della sintesi idrotermale, le MFC di ferrite sono state separate e purificate utilizzando la separazione magnetica. Un magnete è stato posto sotto la soluzione per forzare la loro raccolta sul fondo della nave. Le impurità e i sottoprodotti non magnetici formati nella sintesi, insieme al solvente in eccesso, potrebbero quindi essere travasati per produrre MFC puri e monodispersi27. La figura 4 illustra il tempo necessario per la raccolta magnetica quasi completa degli MFC con e senza l'aggiunta di lana d'acciaio. La lana d'acciaio posta nel flaconcino durante la separazione magnetica aumenta il gradiente del campo magnetico all'interno del flaconcino, consentendo una separazione molto più rapida28.
Le MFC purificate mediante separazione magnetica mostrano un elevato grado di uniformità rispetto a quelle purificate utilizzando un processo di ultracentrifugazione più convenzionale. La Figura 5 mostra la distribuzione dimensionale delle MFC ottenute utilizzando la separazione magnetica (A e B) rispetto a quelle che utilizzano l'ultracentrifugazione (5.000 g per 30 min) (C e D). La separazione magnetica si traduce in una distribuzione del diametro del cluster più stretta rispetto all'ultracentrifugazione ed è la strategia di purificazione preferita per le MFC.
Gli MFC as-synthesized sono rivestiti con poliacrilato (PAA), che fornisce una superficie caricata negativamente e un certo grado di repulsione interparticellare che impedisce l'aggregazione interparticellare (Figura 6A). Tuttavia, eseguendo una reazione di sostituzione del ligando con nitrodopamina (Figura 6B), possiamo sostituire il rivestimento PAA con un rivestimento copolimero di P (AA-co-AMPS-co-PEG), che consente una maggiore stabilità in soluzioni a resistenza ionica più elevata. La Figura 7 mostra lo schema di questo processo di funzionalizzazione delle superfici. La stabilità colloidale delle MFC disperse in un buffer PBS è evidente nella Figura 8. Le MFC sintetizzate rivestite con PAA si aggregano rapidamente e si separano dalla soluzione entro 30 minuti e sono di scarsa utilità nelle applicazioni biologiche. Al contrario, le MFC funzionalizzate con un rivestimento in polisolfonato sono rimaste ben disperse in questa soluzione per oltre 2 giorni senza alcun segno di aggregazione. La modifica della superficie post-sintesi qui descritta fornisce un percorso per la formazione di soluzioni omogenee di MFC appropriate per l'introduzione in ambienti biologici.
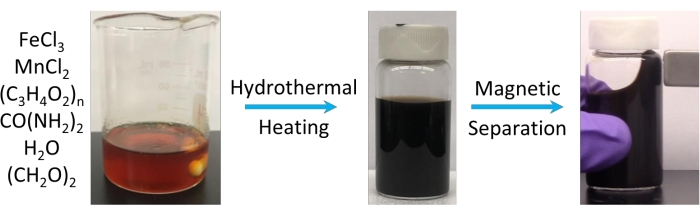
Figura 1: Lo schema per la sintesi dei nanocluster di ferrite di manganese. I reagenti, cloruro di ferro (III), cloruro di manganese (II), acido poliacrilico (PAA), urea, acqua e glicole etilenico sono combinati in condizioni idrotermali per produrre i nanocluster di ferrite di manganese. Questo prodotto forma una soluzione colloidale stabile in acqua pura come mostrato nel mezzo. La quantità di acqua aggiunta nella sintesi e il rapporto tra manganese e ferro nei precursori viene utilizzata per regolare rispettivamente la dimensione del cluster e la composizione della ferrite. Dopo la separazione magnetica, i nanocluster formano un ferrofluido come mostrato a destra, indicando che sono altamente reattivi anche a piccoli campi magnetici applicati. Fare clic qui per visualizzare una versione più grande di questa figura.

Figura 2: Immagini al microscopio elettronico a trasmissione (TEM) dei nanocluster di ferrite di manganese e delle loro distribuzioni di diametro. Nelle immagini A-D, il diametro dell'ammasso (Dc) aumenta a causa della riduzione della quantità di acqua aggiunta nella sintesi. Il diametro medio del cluster è 31, 56, 74 e 120 nm per A, B, C e D, rispettivamente, con una composizione costante di Mn0.15Fe2.85O4. Nelle immagini E-H, la composizione della ferrite cambia monotonamente in proporzione al rapporto Mn/Fe dei precursori. Nonostante le loro diverse composizioni, si ottiene un diametro del cluster quasi equivalente. La nostra sintesi consente un controllo indipendente sia sul diametro del cluster che sulla composizione della ferrite, entrambe caratteristiche importanti per le proprietà magnetiche delle ferriti su scala nanometrica. Fare clic qui per visualizzare una versione più grande di questa figura.
| Etichetta nella Figura 2 | H2O (mL) | FeCl3 (mmol) | MnCl2 (mmol) | Composizione ferrite | DC (nm) | |
| Un | 1.5 | 1.3 | 0.7 | Mn0.15Fe2.85O4 | 34 | |
| B&G | 0.7 | 1.3 | 0.7 | Mn0.15Fe2.85O4 | 56 | |
| C | 0.5 | 1.3 | 0.7 | Mn0.15Fe2.85O4 | 74 | |
| D | 0.1 | 1.3 | 0.7 | Mn0.15Fe2.85O4 | 120 | |
| E | 1.3 | 2 | 0 | Fe3O4 · | 56 | |
| F | 0.6 | 1.5 | 0.5 | Mn0.06Fe2.94O4 | 56 | |
| H | 2 | 1 | 1 | Mn0.6Fe2.4O4 | 55 | |
Tabella 1: Condizioni di reazione per la sintesi dei campioni di nanocluster mostrati in Figura 2. Altri parametri di sintesi sono: 20 ml di glicole etilenico, 250 mg di PAA e 1,2 g di urea. Le miscele di reazione vengono riscaldate idrotermalmente a 200 °C per 20 ore. Per A, B, C e D, diminuendo il contenuto di acqua mantenendo costanti altri parametri si sono verificati gruppi di diametri maggiori. Per E, F, G e H, l'aumento del rapporto tra MnCl2 e FeCl3 nella miscela di reazione iniziale ha portato a cluster con proporzioni più elevate di manganese nella struttura del cluster. Variando la quantità di acqua E, F, G e H allo stesso tempo si possono creare gruppi di diversa composizione ma di diametro quasi equivalente.
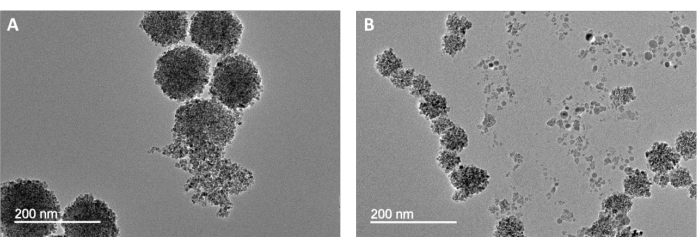
Figura 3: Immagini TEM di reazioni fallite e incomplete. Le caratteristiche piccole e a basso contrasto osservate in queste immagini sono nanocristalli primari che non si sono sviluppati in nanocluster. Il campione nella Figura 3A è stato preparato senza acqua aggiuntiva, mentre il materiale mostrato nella Figura 3B ha avuto un tempo di reazione insufficiente, di quattro ore. Fare clic qui per visualizzare una versione più grande di questa figura.
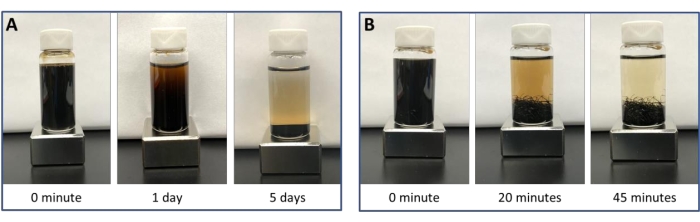
Figura 4: Confronto della separazione magnetica dei nanocluster. Confronto della separazione magnetica dei nanocluster senza (A) e con (B) l'aggiunta di lana d'acciaio nel contenitore. La lana d'acciaio aumenta il gradiente del campo magnetico all'interno del flaconcino per consentire una separazione magnetica più rapida dei nanocluster. Di conseguenza, è possibile aumentare la produzione di nanocluster in modo efficiente senza sacrificare la qualità del campione. Fare clic qui per visualizzare una versione più grande di questa figura.

Figura 5: Confronto tra ultracentrifugazione e separazione magnetica. Confronto tra ultracentrifugazione (A,B) e separazione magnetica (C,D) e loro impatto sull'uniformità dei cluster purificati. A e C sono le immagini TEM dei cluster purificati, e B e D sono le distribuzioni dimensionali dei cluster in A e C, rispettivamente. L'asse y rappresenta il numero di cluster contati e, per ogni campione, sono stati rilevati un totale di 150 cluster. Fare clic qui per visualizzare una versione più grande di questa figura.
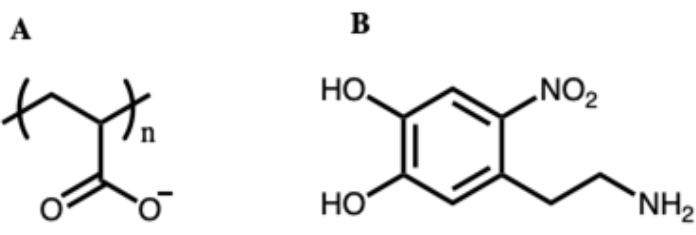
Figura 6: La struttura del poli(acido acrilico) (PAA) (A) e della nitro-dopamina (B) utilizzati nella fase di modifica della superficie. Il rivestimento PAA iniziale utilizzato nella sintesi non è ideale in mezzi biologici o acidi a causa del fatto che l'acido carbossilico è facilmente protonato. La nitro-dopamina viene utilizzata per sostituire il rivestimento PAA creando un gruppo funzionale per ancorare un copolimero solfonato. Fare clic qui per visualizzare una versione più grande di questa figura.
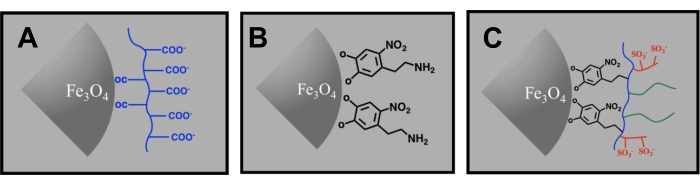
Figura 7: Schemi del processo di modifica della superficie del cluster. (A) rivestimento PAA originale, (B) rivestimento intermedio nitro-dopamina e (C) rivestimento P (AA-co-AMPS-co-PEG) finale. In (C), le curve blu, rossa e verde rappresentano rispettivamente le unità AA, AMPS e PEG. La composizione del cluster può essere Fe3O4 o MnxFe3-xO4. Fare clic qui per visualizzare una versione più grande di questa figura.

Figura 8: La funzionalizzazione superficiale dei nanocluster con polisolfonato porta a materiali che sono colloidali stabili in molte diverse condizioni acquose. I cluster con due diversi rivestimenti superficiali, paA rivestito (A) e P (AA-co-AMPS-co-PEG) funzionalizzato (B) sono disciolti nella soluzione tampone PBS che è rilevante per le impostazioni biologiche e osservata per la loro stabilità colloidale nel tempo. Fare clic qui per visualizzare una versione più grande di questa figura.
Discussione
Questo lavoro dimostra una sintesi di polioli modificata di nanocristalli di ferrite di manganese raggruppati insieme in aggregati uniformi su scala nanometrica29. In questa sintesi, il cloruro di ferro (III) e il cloruro di manganese (II) subiscono una reazione e una riduzione di idrolisi forzata, formando MnxFe3-xO4 molecolare. Queste molecole di ferrite formano nanocristalli primari sotto l'alta temperatura e l'alta pressione nei reattori, assemblandosi infine in aggregati sferici chiamati qui cluster di ferrite di magnetite (MFC). Senza un tempo di reazione sufficiente o acqua sufficiente, il processo di aggregazione non può essere completamente completato portando a particelle non uniformi e scarsamente formate. Al contrario, dato abbastanza tempo e abbastanza acqua, il processo di cristallizzazione e assemblaggio dell'ossido di metallo è completo e produce un cluster sferico uniforme che comprende da decine a centinaia di nanocristalli primari. I nanocristalli primari in questi materiali sono aggregati duri, condividendo alcune interfacce cristalline, portando ad un'elevata suscettibilità iniziale e a una risposta magnetica pronunciata anche ai piccoli campi disponibili dai magneti permanenti portatili27. Di conseguenza, questi materiali hanno un grande potenziale per applicazioni nella somministrazione di farmaci, ipertermia magnetica, risonanza magnetica e imaging di particelle magnetiche30,31,32.
Troviamo che la quantità di acqua aggiunta alla miscela di reazione iniziale controlla il diametro dei cluster assemblati. Man mano che il contenuto di acqua nei reagenti aumenta, il diametro dei cluster e il numero di nanocristalli primari aggregati diminuiscono. L'intervallo ottimale è compreso tra 0,8 M e 5,0 M di acqua, condizioni che producono, rispettivamente, diametri di cluster che vanno da 150 nm a 30 nm. L'acqua ha un ruolo importante in questo processo perché è necessario garantire una rapida idrolisi dei precursori metallici, una più rapida aggregazione di cristalliti primari e di conseguenza cluster più piccoli16. Poiché la sintesi è straordinariamente sensibile all'acqua, i reagenti gestiti in condizioni ambientali di umidità variabile potrebbero assorbire diverse quantità di acqua dall'aria. Ciò potrebbe influire sulle dimensioni e sulla morfologia successive del prodotto. Mentre il controllo dell'umidità nella maggior parte dei laboratori di ricerca (ad esempio, 30% -60% RH) è sufficiente per ridurre al minimo questo problema, questa è una fonte di errore sistematico nella procedura segnalata. Il controllo del rapporto manganese/ferro nel prodotto si ottiene variando il rapporto tra manganese e precursori del ferro. Ciò è sorprendente in quanto in molte reazioni idrotermali il livello di drogaggio dei prodotti spesso non è semplicemente correlato alla stechiometria dei materiali di partenza4,6,8,12,13,17. Per queste condizioni, tuttavia, la composizione del prodotto è ben prevista dal rapporto tra i precursori metallici. Nel loro insieme, il controllo indipendente sia del diametro del cluster che della sua composizione è possibile attraverso una semplice manipolazione delle miscele di reagenti di partenza.
Spesso la purificazione delle nanoparticelle dai mezzi di reazione è il passo più lungo e complesso nella generazione di materiali di alta qualità. L'ultracentrifugazione viene spesso applicata a questo scopo e mentre questo è efficace nel separare le nanoparticelle dai sottoprodotti molecolari, è poco adatto per rimuovere i prodotti solidi indesiderati. Quando applicato qui alla purificazione dei nanomateriali, l'ultracentrifugazione produce particelle relativamente polidisperse con dimensioni e forme variabili. È molto più efficiente sfruttare la risposta magnetica di questi materiali applicando la separazione magnetica per migliorare l'uniformità e la purezza del prodotto finale. Acceleriamo la separazione magnetica creando gradienti molto elevati di campi magnetici all'interno della fiala macroscopica utilizzando lana d'acciaio immersa nella soluzione e un magnete permanente in terre rare applicato all'esterno dei contenitori del campione. Questa disposizione consente di recuperare campioni uniformi in meno di trenta minuti con rese elevate (~ 90%). È importante abbinare la quantità di lana d'acciaio introdotta nella soluzione ai diametri dei cluster MFC previsti. Ad esempio, un MFC con un diametro medio di 40 nm richiede tra 100 e 200 mg di lana d'acciaio per una rapida separazione, mentre i materiali più grandi possono richiedere molto meno o addirittura nessuna lana d'acciaio. È ben noto che le nanoparticelle magnetiche più piccole sono meno reattive ai campi applicati in virtù del loro volume magnetico più piccolo15,17,26. Il processo di separazione magnetica fornisce quindi un mezzo per affinare l'uniformità di questi materiali poiché i cluster più piccoli non vengono trattenuti in modo efficiente dal processo16. L'utilizzo di questo metodo di separazione magnetica non solo consente di risparmiare tempo in laboratorio, ma si traduce anche in prodotti con una maggiore uniformità di diametro.
Sebbene gli MFC sintetizzati siano stabili in acqua pura, mostrano una scarsa stabilità colloidale in soluzioni con pH inferiore o maggiore forza ionica. Le ferriti di manganese hanno grandi densità di magnetizzazione e, di conseguenza, per questi diametri gli ammassi possiedono dipoli magnetici che portano all'attrazione interparticellare. Il rivestimento in poliacrilato nativo utilizzato durante la formazione dei materiali conferisce una carica negativa alle superfici delle particelle e aiuta a prevenire l'aggregazione particella-particella. Tuttavia, a pH più basso i gruppi carbossilici sono completamente protonati in effetti rimuovendo la repulsione elettrostatica necessaria per mantenere omogenee le dispersioni MFC; in alternativa, nei mezzi a più alta forza ionica, la repulsione di carica è ridotta portando a una maggiore aggregazione di particelle. L'aggregazione delle MFC crea materiali macroscopici che non sono dispersi in modo omogeneo nella soluzione, rendendo difficile l'uso dei materiali in vivo o in applicazioni che richiedono superfici di nanoparticelle ampie e disponibili. Per questi motivi, introduciamo un secondo polimero nella reazione per sostituire il rivestimento PAA originale. Il copolimero, P (AA-co-AMPS-co-PEG), include glicole polietilenico neutro (PEG) per fornire biocompatibilità e un certo grado di ostacolo sterico. Inoltre, il componente polisolfonato (PAMPS) offre sia una maggiore densità di carica rispetto al poliacrilato sia un gruppo funzionale che ha un pKa molto più basso e di conseguenza un intervallo di pH di lavoro maggiore (pKa ~ 1,2)24. I cluster di ferrite di manganese modificati con questi rivestimenti superficiali mostrano una stabilità notevolmente aumentata in mezzi acidi e biologici. La procedura per garantire la corretta modifica della superficie è tuttavia dettagliata e deve essere seguita attentamente per garantire che i campioni siano rivestiti in modo efficace. In particolare, il metodo richiede un monitoraggio costante della miscela di reazione mentre viene trattata con un sonicatore a sonda per garantire una sostituzione omogenea e completa del rivestimento iniziale in poliacrilato. È anche importante utilizzare vetreria di dimensioni adeguate per ridurre al minimo qualsiasi perdita di prodotto durante la sonicazione vigorosa e applicare un bagno di ghiaccio alla miscela di sonicazione per ridurre al minimo la degradazione termica dei polimeri causata dalla sonicazione della sonda.
In conclusione, questo metodo consente la produzione rapida ed efficiente di cluster di ferrite di manganese (MFC) con diametri sintonizzabili e composizioni da manganese a ferro. Il contenuto di acqua reagente e il rapporto tra ferro e manganese sono parametri importanti nella definizione delle caratteristiche del prodotto materiale. Una semplice tecnica di separazione magnetica che utilizza un magnete portatile e lana d'acciaio fornisce un mezzo efficiente per purificare il prodotto dopo la sintesi producendo grappoli più uniformi. Infine, un copolimero PEG solfonato viene applicato ai materiali per garantire che rimangano non aggreganti in una varietà di diversi mezzi di pH e forza ionica. La maggiore reattività magnetica di questi ossidi di ferro drogati con manganese rispetto ai nanomateriali di ossido di ferro puro (Fe3O4) rende più semplice, economico e più facile sviluppare dispositivi per l'applicazione di campi esterni per manipolare i materiali in vivo. I loro rivestimenti superficiali migliorati sono anche importanti in quanto le applicazioni per le nanoparticelle magnetiche nella somministrazione di farmaci, nella bonifica dell'acqua e nei sistemi di imaging avanzati richiedono materiali non aggreganti e omogenei in una varietà di mezzi biologici e ambientali.
Divulgazioni
Gli autori non hanno nulla da rivelare.
Riconoscimenti
Questo lavoro è stato generosamente sostenuto dalla Brown University e dall'Advanced Energy Consortium. Ringraziamo con gratitudine il Dr. Qingbo Zhang per il suo metodo sintetico stabilito di MFC di ossido di ferro.
Materiali
| Name | Company | Catalog Number | Comments |
| 0.1 Micron Vaccum Filtration Filter | Thermo Fisher Scientific | NC9902431 | for filtration of aggregated clusters after synthesis and surface coating to achieve a uniform solution |
| 2-Acrylamido-2-methylpropane sulfonic acid (AMPS, 99%) | Sigma-Aldrich | 282731-250G | reagent used in copolymer to surface coat nanoclusters and functionalize them for biological media |
| 2,2′-Azobis(2-methylpropionitrile) (AIBN) | Sigma-Aldrich | 441090-100G | reagent used in copolymer making as the free ridical generator |
| 4-Morpholineethanesulfonic acid, 2-(N-Morpholino)ethanesulfonic acid (MES) | Sigma-Aldrich | M3671-250G | acidic buffer used to stabilize nanocluster surface coating process |
| Acrylic acid | Sigma-Aldrich | 147230-100G | reagent used in copolymer to surface coat nanoclusters and functionalize them for biological media; anhydrous, contains 200 ppm MEHQ as inhibitor, 99% |
| Analytical Balance | Avantor | VWR-205AC | used to weigh out solid chemical reagents for use in synthesis and dilution |
| Digital Sonifier and Probe | Branson | B450 | used to sonicate nanocluster solution during surface coating to break up aggregates |
| Dopamine hydrochloride | Sigma-Aldrich | H8502-25G | used in surface coating for ligand exchange reaction |
| Ethylene glycol (anhydrous, 99.8%) | Sigma-Aldrich | 324558-2L | reagent used as solvent in hydrothermal synthesis of nanoclusters |
| Glass Vials (20mL) | Premium Vials | B1015 | container for nanocluster solution during washing and surface coating as well as polymer solutions |
| Graduated Beaker (100mL) | Corning | 1000-100 | container for mixing of solid and liquid reagents during hydrothermal synthesis (to be transferred into autoclave reactor before oven) |
| Handheld Magnet | MSC Industrial Supply, Inc. | 92673904 | 1/2" Long x 1/2" Wide x 1/8" High, 5 Poles, Rectangular Neodymium Magnet low strength magnet used to precipitate nanoclusters from solution (field strength is increased with steel wool when needed) |
| Hydrochloric acid (ACS grade, 37%) | Fisher Scientific | 7647-01-0 | for removing leftover nanocluster debris and cleaning autoclave reactors for next use |
| Hydrothermal Autoclave Reactor | Toption | TOPT-HP500 | container for finished reagent mixture to withstand high temperature and pressure created by the oven in hydrothermal synthesis |
| Iron(III) Chloride Hexahydrate (FeCl3·6H2O, ACS reagent, 97%) | ACS | 236489-500G | reagent used in synthesis of nanoclusters as source of iron (III) that becomes iron (II) in finished nanocluster product (keep dry and weigh out quickly to avoid water contamination) |
| Labware Washer Brushes | Fisher Scientific | 13-641-708 | used to wash and clean glassware before synthesis |
| Magnetic Stir Plate | Thermo Fisher Scientific | 50093538 | for mixing of solid and liquid reagents during hydrothermal synthesis |
| Manganese chloride tetrahydrate (MnCl2·4H2O, 99.0%, crystals, ACS) | Sigma-Aldrich | 1375127-2G | reagent used in synthesis of nanoclusters as source of manganese |
| Micropipette (100-1000μL) | Thermo Fisher Scientific | FF-1000 | for transferring liquid reagents such as water and manganese chloride |
| N-(3-Dimethylaminopropyl)-N′-ethylcarbodiimide hydrochloride (EDC) | Sigma-Aldrich | 25952-53-8 | used in surface coating to assist in ligand exchange of copolymer (keep bulk chemical in freezer and diluted solution in refrigerator) |
| N,N-Dimethylformamide (DMF) | Sigma-Aldrich | 227056-2L | reagent used in copolymer making as the solvent |
| Polyacrylic acid sodium salt (PAA, Mw~6,000) | PolyScience Inc. | 06567-250 | reagent used in hydrothermal synthesis to initially coat the nanoclusters (eventually replaced in surface coating step) |
| Poly(ethylene glycol) methyl ether acrylate | Sigma-Aldrich | 454990-250ML | reagent used in copolymer to surface coat nanoclusters and functionalize them for biological media; average Mn 480, contains 100 ppm BHT as inhibitor, 100 ppm MEHQ as inhibitor |
| Reagents Acetone, 4L, ACS Reagent | Cole-Parmer | UX-78920-66 | used as solvent to precipitate nanoclusters during washing |
| Single Channel Pipette, Adjustable 1-10 mL | Eppendorf | 3123000080 | for transferring ethylene glycol and other liquids |
| Steel Wool | Lowe's | 788470 | used to increase the magnetic field strength in the vial to aid in precipitation of nanoclusters for washing and surface coating |
| Stirring Bar | Thomas Scientific | 8608S92 | for mixing of solid and liquid reagents during hydrothermal synthesis |
| Table Clamp | Grainger | 29YW53 | for tight sealing of autoclave reactor to withstand high pressure of oven during hyrothermal synthesis |
| Urea (ACS reagent, 99.0%) | Sigma-Aldrich | U5128-500G | reagent used in hydrothermal synthesis to create a basic solution |
| Vaccum Filtration Bottle Tops | Thermo Fisher Scientific | 596-3320 | for filtration of aggregated clusters after synthesis and surface coating to achieve a uniform solution |
| Vacuum Controller V-850 | Buchi | BU-V850 | for filtration of aggregated clusters after synthesis and surface coating to achieve a uniform solution |
| Vacuum Oven | Fisher Scientific | 13-262-51 | used to create high temperature and pressure needed for nanocluster formation in hydrothermal synthesis |
Riferimenti
- Makridis, A., et al. In vitro application of Mn-ferrite nanoparticles as novel magnetic hyperthermia agents. Journal of Materials Chemistry B. 2 (47), 8390-8398 (2014).
- Nelson-Cheeseman, B., Chopdekar, R., Toney, M., Arenholz, E., Suzuki, Y. Interplay between magnetism and chemical structure at spinel-spinel interfaces. Journal of Applied Physics. 111 (9), 093903 (2012).
- Otero-Lorenzo, R., Fantechi, E., Sangregorio, C., Salgueiriño, V. Solvothermally driven Mn doping and clustering of iron oxide nanoparticles for heat delivery applications. Chemistry-A European Journal. 22 (19), 6666-6675 (2016).
- Mohapatra, J., et al. Enhancement of magnetic heating efficiency in size controlled MFe 2 O 4 (M= Mn, Fe, Co and Ni) nanoassemblies. Rsc Advances. 5 (19), 14311-14321 (2015).
- Qi, Y., et al. Carboxylic silane-exchanged manganese ferrite nanoclusters with high relaxivity for magnetic resonance imaging. Journal of Materials Chemistry B. 1 (13), 1846-1851 (2013).
- Anandhi, J. S., Jacob, G. A., Joseyphus, R. J. Factors affecting the heating efficiency of Mn-doped Fe3O4 nanoparticles. Journal of Magnetism and Magnetic Materials. 512, 166992 (2020).
- Del Bianco, L., et al. Mechanism of magnetic heating in Mn-doped magnetite nanoparticles and the role of intertwined structural and magnetic properties. Nanoscale. 11 (22), 10896-10910 (2019).
- Padmapriya, G., Manikandan, A., Krishnasamy, V., Jaganathan, S. K., Antony, S. A. Enhanced catalytic activity and magnetic properties of spinel Mn x Zn 1−x Fe 2 O 4 (0.0≤x≤1.0) nano-photocatalysts by microwave irradiation route. Journal of Superconductivity and Novel Magnetism. 29 (8), 2141-2149 (2016).
- Kim, J., et al. Continuous O2-evolving MnFe2O4 nanoparticle-anchored mesoporous silica nanoparticles for efficient photodynamic therapy in hypoxic cancer. Journal of the American Chemical Society. 139 (32), 10992-10995 (2017).
- Silva, L. H., Cruz, F. F., Morales, M. M., Weiss, D. J., Rocco, P. R. Magnetic targeting as a strategy to enhance therapeutic effects of mesenchymal stromal cells. Stem Cell Research & Therapy. 8 (1), 1-8 (2017).
- Otero-Lorenzo, R., Ramos-Docampo, M. A., Rodriguez-Gonzalez, B., Comesaña-Hermo, M., Salgueiriño, V. Solvothermal clustering of magnetic spinel ferrite nanocrystals: a Raman perspective. Chemistry of Materials. 29 (20), 8729-8736 (2017).
- Aghazadeh, M., Karimzadeh, I., Ganjali, M. R. PVP capped Mn2+ doped Fe3O4 nanoparticles: a novel preparation method, surface engineering and characterization. Materials Letters. 228, 137-140 (2018).
- Li, Z., et al. Solvothermal synthesis of MnFe 2 O 4 colloidal nanocrystal assemblies and their magnetic and electrocatalytic properties. New Journal of Chemistry. 39 (1), 361-368 (2015).
- Guo, P., Zhang, G., Yu, J., Li, H., Zhao, X. Controlled synthesis, magnetic and photocatalytic properties of hollow spheres and colloidal nanocrystal clusters of manganese ferrite. Colloids and Surfaces A: Physicochemical and Engineering Aspects. 395, 168-174 (2012).
- Pardo, A., et al. Synthesis, characterization, and evaluation of superparamagnetic doped ferrites as potential therapeutic nanotools. Chemistry of Materials. 32 (6), 2220-2231 (2020).
- Xiao, Z., et al. Libraries of uniform magnetic multicore nanoparticles with tunable dimensions for biomedical and photonic applications. ACS Applied Materials & Interfaces. 12 (37), 41932-41941 (2020).
- Choi, Y. S., Young Yoon, H., Sung Lee, J., Hua Wu, J., Keun Kim, Y. Synthesis and magnetic properties of size-tunable Mn x Fe3−x O4 ferrite nanoclusters. Journal of Applied Physics. 115 (17), (2014).
- Creixell, M., et al. The effect of grafting method on the colloidal stability and in vitro cytotoxicity of carboxymethyl dextran coated magnetic nanoparticles. Journal of Materials Chemistry. 20 (39), 8539-8547 (2010).
- Latorre, M., Rinaldi, C. Applications of magnetic nanoparticles in medicine: magnetic fluid hyperthermia. Puerto Rico Health Sciences Journal. 28 (3), (2009).
- Yeap, S. P., Lim, J., Ooi, B. S., Ahmad, A. L. Agglomeration, colloidal stability, and magnetic separation of magnetic nanoparticles: collective influences on environmental engineering applications. Journal of Nanoparticle Research. 19 (11), 1-15 (2017).
- Lee, S. -. Y., Harris, M. T. Surface modification of magnetic nanoparticles capped by oleic acids: Characterization and colloidal stability in polar solvents. Journal of Colloid and Interface Science. 293 (2), 401-408 (2006).
- Yeap, S. P., Ahmad, A. L., Ooi, B. S., Lim, J. Electrosteric stabilization and its role in cooperative magnetophoresis of colloidal magnetic nanoparticles. Langmuir. 28 (42), 14878-14891 (2012).
- Wydra, R. J., Oliver, C. E., Anderson, K. W., Dziubla, T. D., Hilt, J. Z. Accelerated generation of free radicals by iron oxide nanoparticles in the presence of an alternating magnetic field. RSC Advances. 5 (24), 18888-18893 (2015).
- Bagaria, H. G., et al. Iron oxide nanoparticles grafted with sulfonated copolymers are stable in concentrated brine at elevated temperatures and weakly adsorb on silica. ACS Applied Materials & Interfaces. 5 (8), 3329-3339 (2013).
- Park, J. C., Park, T. Y., Cha, H. J., Seo, J. H. Multifunctional nanocomposite clusters enabled by amphiphilic/bioactive natural polysaccharides. Chemical Engineering Journal. 379, 122406 (2020).
- Hemery, G., et al. Tuning sizes, morphologies, and magnetic properties of monocore versus multicore iron oxide nanoparticles through the controlled addition of water in the polyol synthesis. Inorganic Chemistry. 56 (14), 8232-8243 (2017).
- Lartigue, L., et al. Cooperative organization in iron oxide multi-core nanoparticles potentiates their efficiency as heating mediators and MRI contrast agents. ACS Nano. 6 (12), 10935-10949 (2012).
- Yavayo, C. T., et al. Low-field magnetic separation of monodisperse Fe3O4 nanocrystals. Science. 314 (5801), 964-967 (2006).
- Matijević, E., Scheiner, P. Ferric hydrous oxide sols: III. Preparation of uniform particles by hydrolysis of Fe (III)-chloride,-nitrate, and-perchlorate solutions. Journal of Colloid and Interface Science. 63 (3), 509-524 (1978).
- Weizenecker, J., Gleich, B., Rahmer, J., Dahnke, H., Borgert, J. Three-dimensional real-time in vivo magnetic particle imaging. Physics in Medicine & Biology. 54 (5), 1 (2009).
- Zhu, X., Li, J., Peng, P., Hosseini Nassab, N., Smith, B. R. Quantitative drug release monitoring in tumors of living subjects by magnetic particle imaging nanocomposite. Nano Letters. 19 (10), 6725-6733 (2019).
- Tay, Z. W., et al. Magnetic particle imaging-guided heating in vivo using gradient fields for arbitrary localization of magnetic hyperthermia therapy. ACS Nano. 12 (4), 3699-3713 (2018).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon