Method Article
Оптимизированная реакция Griess для UV-Vis и Голый глаз Определение противомалярийных Primaquine
* Эти авторы внесли равный вклад
В этой статье
Резюме
Этот протокол описывает новый колористетрический метод для обнаружения противомалярийных примахин (ПМЗ) в синтетических мочах и сыворотках человека.
Аннотация
Primaquine (ПМЗ), важный противомалярийный препарат, был рекомендован Всемирной организацией здравоохранения (ВОЗ) для лечения опасных для жизни инфекций, вызванных P. vivax и ovale. Тем не менее, ПМЗ имеет нежелательные побочные эффекты, которые приводят к острому гемолизу у пациентов с дефицитом глюкозы-6-фосфат дегидрогеназы (G6PD). Существует необходимость в разработке простых и надежных методов определения ПМЗ с целью мониторинга дозировки. В начале 2019 года мы сообщили о УФ-Вис и невооруженным глазом подход для PM' колористельной количественной оценки. Обнаружение было основано на Griess-подобной реакции между ПМЗ и анилинами, которые могут генерировать цветные продукты азо. Предел обнаружения для прямого измерения ПМЗ в синтетической моче находится в наномолярном диапазоне. Кроме того, этот метод показал большой потенциал для количественной оценки ПМЗ из образцов сыворотки человека в клинически значимых концентрациях. В этом протоколе мы опишите технические детали, касающиеся синтеза и характеристики цветных продуктов азо, подготовки реагента, а также процедур определения ПМЗ.
Введение
ПМЗ является одним из наиболее важных противомалярийных препаратов, он работает не только как шизонтоцид тканей для предотвращения рецидива, но и как геймтоцитоцид, чтобы прервать передачу болезни1,2,3,4. Внутрисосудистый гемолизявляется является одним из связанных побочных эффектов ПМЗ, который становится чрезвычайно серьезным в тех, дефицит G6PD. Известно, что генетическое заболевание G6PD распространяется по всему миру с частотой генов между 3-30% в эндемичных по малярии районах. Тяжесть слабости ПМЗ зависит от степени дефицита G6PD, а также дозы и продолжительности воздействия ПМЗ5,6. Для снижения риска ВОЗ рекомендовала для лечения малярии одну низкую дозу (0,25 мг базы/кг) ПМЗ. Тем не менее, это по-прежнему оспаривается изменения в чувствительности пациента наркотиков5,7. Мониторинг дозы необходим для оценки фармакокинетики после введения ПМЗ, что может повлиять на корректировку дозировки для успешного лечения с ограниченной токсичностью.
Высокопроизводительная жидкая хроматография (HPLC) является наиболее широко используемым методом клинического определения ПМЗ. Эндох и др. сообщили о системе HPLC с УФ-детектором для количественной оценки сыворотки с помощью колонки полимерного геля C-188. В их системе белки сыворотки сначала осаждались ацетонитрилом, а затем ПМЗ в супернатанте был отделен для HPLC. Кривая калибровки была линейной над диапазоном концентрации от 0,01-1,0 мкг/мл8. Другой метод, основанный на обратной фазе HPLC с УФ-обнаружением на уровне 254 нм, был зарегистрирован для количественной оценки ПМЗ и его основных метаболитов9. Кривая калибровки для ПМЗ была линейной в диапазоне от 0,025-100 мкг/мл. Дополнительная жидко-жидкая экстракция со смешанным гексаном и этиловым ацетатом в качестве органической фазы использовалась для разделения ПМЗ с процентным восстановлением, достигаемым до 89%9. Совсем недавно, Миранда и др. разработали метод UPLC с УФ-обнаружения на 260 нм для анализа ПМЗ в таблетках формулировки с пределом обнаружения на 3 мкг /мл10.
Хотя методы HPLC демонстрируют многообещающую чувствительность в определении наркотиков и чувствительность может быть дополнительно улучшена, если HPLC оснащен масс-спектрометр, Есть еще некоторые недостатки. Прямые измерения лекарственных средств в биологических жидкостях, как правило, недоступны HPLC, так как многие биомолекулы могут значительно влиять на анализ. Дополнительные экстракции необходимы для удаления эндогенных молекул до анализа HPLC11,12. Кроме того, обнаружение ПМЗ с помощью детектора HPLC-UV обычно выполняется на максимальной длине волны поглощения (260 нм); однако в биологических жидкостях много эндогенных молекул с сильным абсорбцией на уровне 260 нм (например, аминокислоты, витамины, нуклеиновые кислоты и урохромные пигменты), что мешает обнаружению УФ-излучения ПМЗ. Необходимо разработать простые и экономически эффективные методы определения ПМЗ с разумной чувствительностью и избирательностью.
Реакция Griess впервые была представлена в 1879 году в качестве колориметрического теста для обнаружения нитритов13,14,15,16. В последнее время эта реакция была широко изучена для обнаружения не только нитрита, но и других биологически значимых молекул17,18,19,20. Ранее мы сообщали о первом систематическом исследовании неожиданной реакции Грисса с ПМЗ(рисунок 1). В этой системе, ПМЗ способен образовывать цветные азо, когда в сочетании с заменой анилин в присутствии нитритов ионов в кислых условиях. Мы также обнаружили, что цвет азов варьировался от желтого до синего при увеличении эффекта пожертвований электрона на анилин21. Уф-виз поглощения на основе колористического метода для количественной оценки ПМЗ был разработан с помощью оптимизированной реакции между 4-метоксианилин и ПМЗ. Этот метод показал большой потенциал для чувствительного и селективного обнаружения ПМЗ в биосоответствующих жидкостях. Здесь мы стремимся описать подробные процедуры определения ПМЗ, основанные на этой колористельной стратегии.
протокол
1. Синтез цветного азоса
- В 25 мл круглой нижней колбы (RBF), растворить анилин (0,1 ммоль) и примахин бисфосфат (45,5 мг, 0,1 ммоль) в 10 мл H3PO4 раствор (5% v/v). Положите RBF на ледяную ванну, добавить перемешать бар с соответствующим размером в раствор, и положить RBF на перемешать пластины.
ПРИМЕЧАНИЕ: Для синтеза азо 3г (рисунок 2),используйте 0,2 ммоль примакина бисфосфата. - Растворите NaNO2 (6,9 мг, 0,1 ммоль) в 1 мл охлажденной воды, а затем добавьте в реакционную смесь dropwise. Удалите ледяную ванну и держите реакционную смесь перемешивание при комнатной температуре.
- Мониторинг реакции с кремнезема гель покрытием тонкослойной хроматографии (TLC) пластины. Используйте смесь дихлорметана (DCM)/метанола (MeOH) (vol/vol 5:1) в качестве eluent для TLC. Продукт азо имеет цветные пятна на пластине TLC, которую легко различить невооруженным глазом. Остановите реакцию, когда пятна PM' исчезают на TLC.
- Отрегулируйте реакционную смесь на рГ no10 на NaOH (2 M) на ледяной ванне. Используйте 50 мл разделения воронки для извлечения смеси 3 раза с 20 мл этилового ацетата для каждого, объединить и концентрировать органическую фазу под вакуумом с помощью роторного испарителя.
ПРИМЕЧАНИЕ: Перед извлечением отрегулируйте значение рН реакционных растворов более 10. Это может поддерживать первичный амин в качестве его неионизированной формы, тем самым облегчая добычу. - Очистите остатки с помощью флэш-хроматографии с обратной фазы кремнезема гель под нормальным давлением, используя MeOH/H2O как eluent. Сухие раствор продукта через лиофилизации, чтобы дать желаемые продукты азо.
ПРИМЕЧАНИЕ: Такая же реакция может быть выполнена и в разбавленных растворах HCl (0,2 м).
2. УФ-Вис измерения и теоретические расчеты
- Растворите чистый азо (50 мкм) в дистиллированной воде или в 5% H3PO4 раствор (pH 1.1), соответственно. Запись УФ-виз-спектра поглощения (250-700 нм) на спектрофотометре при комнатной температуре (25 градусов по Цельсию). Экспорт данных как файлы .xls/.xlsx для дальнейшего анализа.
-
Выполняйте все теоретические расчеты для самого ПМЗ и продуктов азо с помощью программы Gaussian 16. Используйте функциональную теорию зависимости от времени плотности (TD-DFT) с базовым набором 6-31G. Включить эффекты растворителя с помощью поляризуемой модели континуума (PCM) с использованием воды.
- Используйте программное обеспечение (например, Chemdraw Office) для рисования структур, а затем сохраните структуру в качестве гаусского файла ввода (.gif).
- Откройте файл GIF с Гаусс Посмотреть и нажмите кнопку Рассчитать. Выберите гауссийский расчет настройки, Opt-Freq, и наземные государства-DFT-B3LYP-6-31G; затем нажмите Отправить. Оптимизация геометрии будет генерировать файл .log.
- Следуя вышеупомянутой процедуре, используйте Gauss View, чтобы открыть этот файл журнала. Нажмите Рассчитать-Gaussian Расчет настройки и выбрать энергию и TD-SCF-DFT-B3LYP-6-31G-Singlet только. Затем отправить. Расчет энергии будет генерировать другой файл журнала и кубический файл.
- Используйте вид Gauss, чтобы открыть файл журнала из расчета энергии. Нажмите Результаты-УФ/Вис, чтобы увидеть прогнозируемое поглощение.
- Используйте вид Gauss, чтобы открыть файл куба. Нажмите Results и выберите поверхностные и контурные поверхностные действия и новую поверхность, чтобы увидеть орбиты.
-
Сравните результаты как экспериментального измерения, так и гауссовского расчета. Рассчитать процентную погрешность между рассчитанными и измеренными значениями, согласно следующему уравнению.
Ошибка в г. (Wmax cal.-Wmaxexper.) / WмаксExper. | 100%
где Wmax cal. представляет максимальную длину волны поглощения от теоретического расчета и Wmax exper. представляет длину волны от экспериментального результата.
3. Определение ПМЗ
- Измерение ПМЗ с использованием 96-колодецной пластины(рисунок 5)
- Растворите 4-метоксианилин в 0,2 М ЛЦ для анилина для 200 мМ, R1. Растворите нитрит натрия в дистиллированной воде, чтобы получить раствор 5 мМ, R2. Храните все растворы в холодильнике при 4 градусах Цельсия перед использованием.
- Добавьте 100 qL R1 в 96-колодую пластину и добавьте 50 л ПМЗ, содержащий образец, в тарелку, чтобы смешаться с R1. Затем добавьте в тарелку 50 л R2. Смешайте растворы путем повторного пипетки.
- Держите пластину при комнатной температуре в течение 15 минут, а затем запишите уф-виз абсорбции на 504 нм. Повторите 3x для каждого теста. Продукт азо стабилен с воздействием света комнаты; не нужно держать тарелку в темноте.
- Экспорт данных как файлы .xls/.xlsx для дальнейшего анализа.
- Кривая калибровки для прямого измерения ПМЗ в образце мочи
- Подготовка растворов ПМЗ с использованием синтетической мочи с концентрациями ПМЗ в 0, 1, 2, 5, 10, 20, 50, 100, 200 мкм, соответственно.
- Добавьте 100 qL R1 в 96-колодую пластину и добавьте 50 л раствора мочи ПМЗ, чтобы смешать сястой с R1. Затем добавьте 50 зл R2 в вышеупомянутую смесь. Смешайте растворы путем повторного пипетки. Держите пластину при комнатной температуре в течение 15 минут, а затем запишите уф-виз абсорбции на 504 нм.
- Создайте кривую калибровки на основе концентраций абсорбции I504 и ПМЗ. Используйте значения из скважин без PM, как пробел, и вычесть пустые значения из всех тестов до обработки данных.
- Выполните линейную подгонку для создания линейных уравнений, как Y и aX'b, где Y является интенсивность поглощения на 504 нм, X является концентрация ПМЗ, является склон, и b является y-перехват линейной линии.
- Кривая калибровки для прямого измерения ПМЗ в образце сыворотки человека
- Подготовьте решения ПМЗ с использованием сыворотки человека с концентрациями ПМЗ по 0, 1, 2, 5, 10, 20, 50, 100, 200, ММ соответственно.
- Добавьте 100 qL R1 в 96-колодую пластину и добавьте 50 л раствора сыворотки PM, чтобы смешать с R1. Добавьте 50 кЛ R2 в приведенную выше смесь и смешайте растворы путем повторного пипетки. Держите пластину при комнатной температуре в течение 15 минут, а затем запишите УФ-виз абсорбции на 504 нм. Экспорт данных как файл .xls/.xlsx для дальнейшего анализа.
- Создайте кривую калибровки на основе концентраций абсорбции I504 и ПМЗ. Используйте значения из скважин без PM, как пробел, и вычесть пустые значения из всех тестов до обработки данных.
- Выполните линейную подгонку для создания линейных уравнений, как Y и aX'b, где Y является интенсивность поглощения на 504 нм, X является концентрация ПМЗ, является склон, и b является y-перехват линейной линии.
- Извлечение ПМЗ из сыворотки
- Добавьте определенное количество ПМЗ в сыворотку человека, чтобы имитировать сыворотку, содержащую ПМЗ. Для извлечения ПМЗ добавьте 6 мл смеси этилового ацетата/гексана (7:1 v/v) в 2 мл сыворотки, содержащей ПМЗ, в 15 мл центрифуги в метро 15 мл.
- Добавьте в систему экстракции 100 л гидроксида натрия (2 М). Яростно встряхните трубку с помощью вихревого смесителя на 30 с. Соберите органический слой и сконцентрируйте его с помощью роторного испарителя под вакуумом.
- Растворите остатки с 200 л дистиллированной воды и удалите нерастворимые липидные компоненты путем фильтрации через дискообразную мембрану с размером 220 нм пор. Используйте окончательное решение для тестирования.
- Определить ПМЗ из сыворотки с экстракции
- Выполните шаги 3.2 или 3.3 для создания кривой калибровки для ПМЗ в дистиллированной воде. Извлекайте ПМЗ из сывороток, содержащих ПМЗ, в соответствии с шагом 3.4.
- Добавьте 100 л раствора R1 и 50 л раствора PM' в 96-колодую пластину. Добавьте 50 кЛ R2 выше смеси, и смешать растворы путем повторного пипетки.
- Держите пластину при комнатной температуре в течение 15 минут и запишите уф-виз абсорбции на 504 нм. Используйте скважины с R1 и R2, но без PM' в качестве элементов управления. Экспорт данных как файлы .xls/.xlsx для дальнейшего анализа.
- Вычесть значения управления из значений абсорбции I504 для каждого теста, а затем использовать результат для расчетов концентрации в соответствии с уравнением лайнера из кривой калибровки.
ПРИМЕЧАНИЕ: Предел обнаружения (LOD) для ПМЗ во всех случаях может быть рассчитан по стандартному методу22. Расчет был основан на функции калибровки: LOD 3.3 SD/b, где SD является стандартным отклонением пустой и b является наклоном регрессионной линии
Результаты
Для оптимизации условий реакции(Рисунок 2), различные анилины были использованы для пары с ПМЗ через реакцию Griess. Мы достигли серии азо с разными цветами. Было установлено, что анилины с электронным заменяющим заменитель может вызвать красный сдвиг в УФ-виз абсорбции спектра. Теоретические расчеты проводились с помощью временной зависимости плотности функциональной теории (TD-DFT). Как уотчки 2A,результат расчета был в хорошем согласовании с оптическими измерениями со средней погрешностью 3,1%. 4-метоксианилин был затем использован для проведения реакции обнаружения Pm q из-за его хорошей производительности в скорости реакции, растворимость продукта, и стабильность21. Кроме того, продукт азо из 4-метоксанилина красного цвета, который легко различить невооруженным глазом. Таким образом, эта реакция предлагает потенциал для обнаружения невооруженным глазом PM » (Рисунок 3).
Рисунок 4A показывает влияние рН на спектр поглощения УФ-виз азо продукта 3d. Я504 не меняется при увеличении рН с 1,0 до 6,0. Я504 под рН 7.0 показывает небольшое снижение, в то время как основные рН (8,0 и 9,0) значительно влияет на поглощение. На рисунке 4B показаны эффекты pH решений Pm' на реакцию Griess. ПМЗ (50 мкм) в буфере PBS с различными рН (4,0, 5,0 ,6,0, 7,0, 8,0, 9,0) были индивидуально смешаны с реагентом тестирования, описанным в разделе 3.1. Я504 затем измеряется после 15 минут при комнатной температуре. Как указано, основные рН (8,0, 9,0) решений ПМЗ потенциально влияют на реакцию. На рисунке 5 показана общая процедура выполнения реакции Griess для обнаружения ПМЗ. Как описано в разделе протокола, для получения данных поглощения I504 для анализа требуется четыре шага. На рисунке 6A и 6B показаны кривые калибровки для прямого обнаружения ПМЗ из образцов мочи и сыворотки, соответственно, без предварительной обработки образцов. Превосходная линейная связь (R2 и 0.998) была обнаружена, когда ПМЗ в синтетической моче колеблется от 0 до 200 мкм. В период сыворотки образца, линейная связь была обнаружена в концентрации от 10 до 200 мкм.
На рисунке 7A показана процедура извлечения ПМЗ из сыворотки. Остатки были растворены в дистиллированной воде после извлечения и концентрации, а затем фильтруются. Для имитации реальной сыворотки, содержащей ПМЗ, ПМЗ был добавлен в сыворотку человека с конечными концентрациями в 0, 0,2, 0,5, 1,0, 2,0 мкм. При использовании шагов 3,4 и 3,5 концентрации ПМЗ в сыворотках составили 0,02, 0,14, 0,44, 0,90 и 1,78 мкм соответственно(рисунок 7С). На основании результата, процент восстановления ПМЗ было установлено, что около 90%, когда ПМЗ был более 0,5 мкм в сыворотке, что было сопоставимо с предыдущими докладами9.

Рисунок 1: Схема реакции Грисса на ПМЗ. (A) Классическая реакция Грисса для нитрита анализа. (B) Реакция Griess в предложенном методе обнаружения PM. Эта цифра была изменена с разрешения предыдущей работы21. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.

Рисунок 2: Фотофизические свойства синтетических азов. (A)УФ-вис измерения и теоретического расчета максимального поглощения азо, порожденных из различных анилин. Номера за пределами скобки представляют для максимального измерения абсорбции в дистиллированной H2O вблизи нейтральных условиях рН; цифры в скобках относятся к измерению в 5% H3PO4 решение (pH 1.1). abs/nm exper. представляет данные эксперимента и abs/calc.— теоретические данные расчета. Eexc является энергией возбуждения (eV), а f - силой осциллятора. (B) Фотоизображения ПМЗ и продуктов азо с различными заменительами, 50 мкм в 5% раствор фосфорной кислоты. (C) УФ-вис спектра синтетических продуктов. Значения были нормализованы в диапазоне от 0 до 1. Эта цифра была изменена с разрешения предыдущей работы21. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
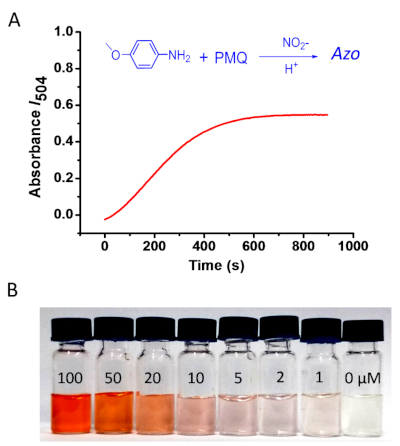
Рисунок 3: Колориметрическое определение ПМЗ. (A) Мониторинг абсорбции изменения на максимум е504 в зависимости от времени образом. Реакция была выполнена с использованием 4-метоксианилин, и ПМЗ был использован на 100 мкм; (B) Изменение цвета реакции с различными концентрациями ПМЗ: 400 л 4-метоксанилийнина (200 мМ в 0,2 М Л Л) и 200 л нитрита натрия в воде (5 мМ), с 200 л раствора ПМЗ различных концентраций (0, 1, 2, 5 , 10, 20, 50, 100 мкм). Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
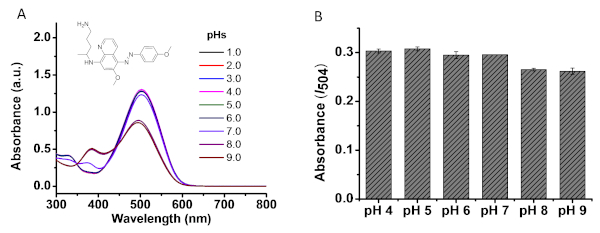
Рисунок 4: влияние рН на обнаружение ПМЗ. (A) рН воздействие на УФ-виз абсорбции азо продукт 3d (50 мкм); (B) ПМЗ (50 мкм) в буфере PBS с различными рН (4,0, 5,0, 6,0, 7,0, 8,0, 9,0) были использованы для выполнения реакции, как описано в шаге 3.1. Пятнадцать минут спустя, абсорбция на 504 нм был измерен. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
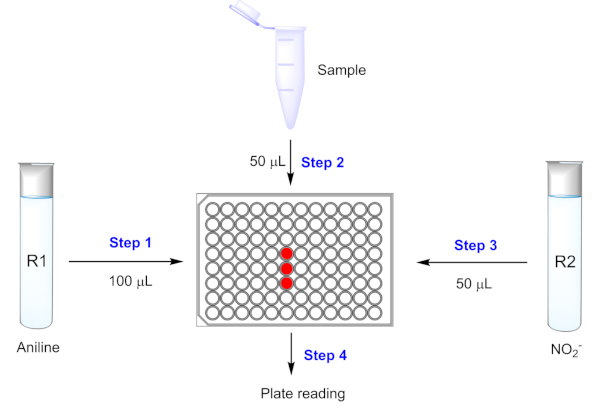
Рисунок 5: Определение ПМЗ через реакцию Griess на 96-хорошо пластины на основе системы. R1 относится к раствору 200 мМ 4-метоксианилин в 0,2 М HCl; R2 относится к 5 мМ нитрита натрия в дистиллированной воде. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.

Рисунок 6: Кривые калибровки для определения ПМЗ из (A) синтетической мочи и (B) образцов сыворотки человека. Концентрация ПМЗ колеблется от 0-200 мкм. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
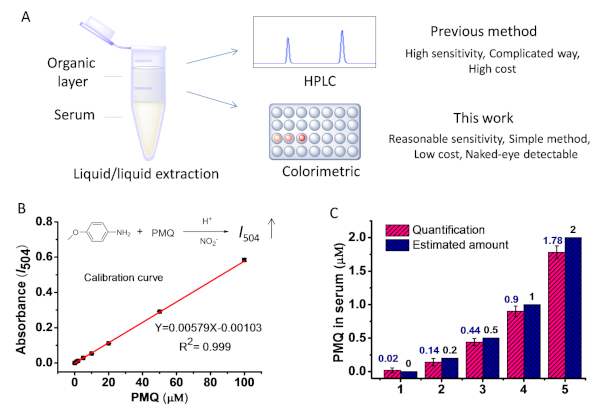
Рисунок 7: Определение ПМЗ из образцов сыворотки. (A) Схематическая иллюстрация извлечения ПМЗ из образцов сыворотки для количественного анализа. (B) Линейные отношения, найденные между I504 и концентрацией ПМЗ в пределах от 0 до 100 мкм. (C)ПМЗ в сыворотке была количественно по методу реакции Griess по сравнению с точной суммой, добавленной в сыворотку. Эта цифра была изменена с разрешения предыдущей работы21. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
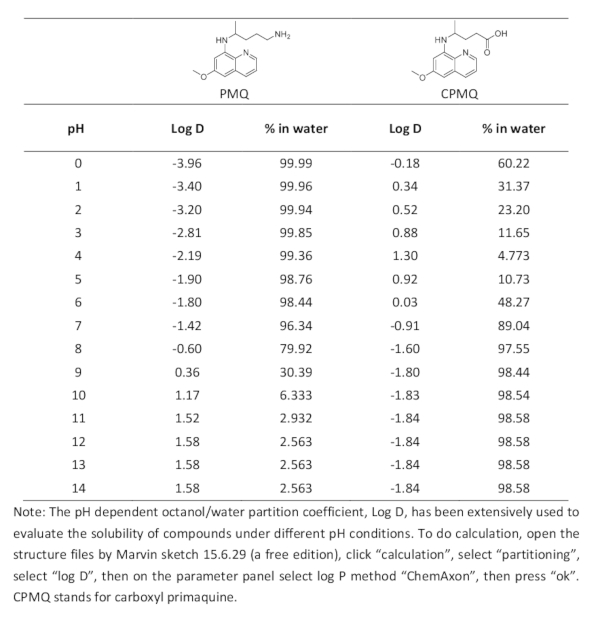
Таблица 1. Теоретический расчет журнала D и процент распределения воды пМЗ и КПМЗ.
Обсуждение
Мы описали колористетрический метод для удобной количественной оценки ПМЗ. Потенциально это самый простой и экономически эффективный текущий метод. Что еще более важно, этот метод предлагает позволяет невооруженным глазом измерения PM, без использования какого-либо оборудования.
Оптимизированная реакция Griess для обнаружения ПМЗ может генерировать красный цвет азо с максимальным поглощением на уровне 504 нм. Потенциальное влияние УФ-визпоглощения эндогенных биомолекул ограничено, что делает метод перспективным для прямого измерения ПМЗ в биологических жидкостях. Как указано в результате, отличная линейная связь (R2 и 0,998) была обнаружена для обнаружения мочи ПМЗ над диапазоном концентрации 0-200 мкм(рисунок 6A). Было установлено, что предел обнаружения (LOD) для ПМЗ составляет 0,63 мкм. Этот метод также показал большой потенциал для прямого измерения ПМЗ в сыворотке человеческой сыворотки. Превосходная линейная связь была обнаружена в концентрации от 10 до 200 мкм для обнаружения сыворотки(рисунок 6B). Мы можем еще больше улучшить чувствительность путем предварительного лечения образца сыворотки путем извлечения и концентрации. Как показано на рисунке 7 с помощью простого процесса экстракции, этот метод может количественно количественно сыворотки PM в клинически соответствующих диапазонах. Основываясь на механизме реакции, основной метаболит карбоксила ПМЗ (КПМЗ) потенциально может образовывать продукт азо с аналогичными свойствами УФ-Виз. Тем не менее, экстракция жидкоста и жидкости в базовых условиях рН потенциально может свести к минимуму помехи от CPM. В таблице 1 показаны расчетный журнал D и распределение воды как PM, так и CPM. Как показано, на рН ,gt;10, менее 6,33% от ПМЗ будет найдено в фазе воды, в то время как более 98,54% CPM ' будет в фазе воды. Таким образом, теоретически, более 93,7% ПМЗ и менее 1,56% КПМЗ могут быть извлечены для тестирования. Можно сделать вывод, что помехи от основного метаболита КПМЗ ограничены.
Процедура обнаружения ПМЗ очень проста в обращении. Взяв в качестве примера 96-хорошую систему на основе пластин, вся процедура состоит из четырех этапов: 1) добавление 100 кЛ 4-метоксианина (200 мМ в 0,2 М ЛК) R1 в 96-хорошую пластину; 2) добавление 50 л неизвестен концентрационно-неизвестен образец ПМЗ для смешивания с R1; 3) добавление 50 кЛ R2 (5 мМ нитрита раствора) для выполнения реакции при комнатной температуре; и 4) запись поглощения УФ-виза на уровне 504 нм с помощью спектрометра. Концентрация ПМЗ из неизвестного образца может быть рассчитана на основе интенсивности поглощения I504 и линейного уравнения из кривой калибровки. Вся процедура проводится при комнатной температуре без необходимости инкубации. Темная среда не является необходимой для всей процедуры, так как цветной продукт не чувствителен к комнатному свету.
Следует отметить, что время для реакции решения для достижения его насыщенных I504 зависит от температуры. Как показано на рисунке 3, по крайней мере 12 минут требуется при комнатной температуре (25 градусов по Цельсию). Время реакции будет больше при выполнении реакции при температурах ниже 25 градусов по Цельсию. Основное состояние рН решений ПМЗ потенциально может повлиять на абсорбцию I504. Чтобы решить эту проблему, отрегулируйте pH решения PM, чтобы быть менее 7.0. В противном случае для решения с рН свыше 7,0 необходима новая кривая калибровки. Кроме того, внутренние нитриты в проверенных образцах могут влиять на обнаружение. Однако это может произойти только тогда, когда концентрация внутренних нитритов чрезвычайно высока, так как высокая концентрация нитрита (5 мМ) была использована в стандартном тесте.
Раскрытие информации
Авторам нечего декларировать.
Благодарности
Авторы признают, что Грант стартапа от Университета китайской медицины Гуанчжоу и молодежный проект подготовки научных исследований ГЗУКМ (2019 г.н.). Мы также признаем Лингнан медицинский исследовательский центр Гуанчжоу Университета китайской медицины за поддержку на объектах.
Материалы
| Name | Company | Catalog Number | Comments |
| 4-Methoxyaniline | Aladdin | K1709027 | |
| 2,4-Dimethoxyaniline | Heowns | 10154207 | |
| 3,4-Dimethoxyaniline | Bidepharm | BD21914 | |
| 4-Methylaniline | Adamas-beta | P1414526 | |
| 4-Nitroaniline | Macklin | C10191447 | |
| 96-wells,Flat Botton | Labserv | 310109008 | |
| Gaussian@16 software | Gaussian, Inc | Version:x86-64 SSE4_2-enabled/Linux | |
| Hydrochloric acid | GCRF | 20180902 | |
| Marvin sketch (software) | CHEMAXON | free edition: 15.6.29 | |
| Phosphoric acid | Macklin | C10112815 | |
| Primaquine bisiphosphate | 3A Chemicals | CEBK200054 | |
| Sodium nitrite | Alfa Aesar | 5006K18R | |
| Sulfonamides | TCI(shanghai) | GCPLO-BP | |
| Varioskan LUX Plate reader | Thermo Fisher | Supplied with SkanIt Software 4.1 |
Ссылки
- Fernando, D., Rodrigo, C., Rajapakse, S. Primaquine in vivax malaria: an update and review on management issues. Malar Journal. 10, 351 (2011).
- Deng, C., et al. Large-scale Artemisinin-Piperaquine Mass Drug Administration With or Without Primaquine Dramatically Reduces Malaria in a Highly Endemic Region of Africa. Clinical Infectious Diseases. 67 (11), 1670-1676 (2018).
- Pavic, K., et al. Primaquine hybrids as promising antimycobacterial and antimalarial agents. European Journal of Medical Chemistry. 143, 769-779 (2018).
- McQueen, A., et al. Synthesis, characterization, and cellular localization of a fluorescent probe of the antimalarial 8-aminoquinoline primaquine. Bioorganic & Medicinal Chemistry Letters. 27 (20), 4597-4600 (2017).
- Ashley, E. A., Recht, J., White, N. J. Primaquine: the risks and the benefits. Malaria Journal. 13 (1), 418 (2014).
- Watson, J., Taylor, W. R., Menard, D., Kheng, S., White, N. J. Modelling primaquine-induced haemolysis in G6PD deficiency. Elife. 6, (2017).
- Beutler, E. Glucose-6-phosphate dehydrogenase deficiency: a historical perspective. Blood. 111 (1), 16-24 (2008).
- Endoh, Y. S., et al. High-performance liquid chromatographic determination of pamaquine, primaquine and carboxy primaquine in calf plasma using electrochemical detection. Journal of Chromatography B: Biomedical Sciences and Applications. 579 (1), 123-129 (1992).
- Dua, V. K., Kar, P. K., Sarin, R., Sharma, V. P. High-performance liquid chromatographic determination of primaquine and carboxyprimaquine concentrations in plasma and blood cells in Plasmodium vivax malaria cases following chronic dosage with primaquine. Journal of Chromatography B: Biomedical Applications. 675 (1), 93-98 (1996).
- Miranda, T. A., Silva, P. H. R., Pianetti, G. A., César, I. C. Simultaneous quantitation of chloroquine and primaquine by UPLC-DAD and comparison with a HPLC-DAD method. Malaria Journal. 14, 29 (2015).
- Tatsuno, M., Nishikawa, M., Katagi, M., Tsuchihashi, H. Simultaneous determination of illicit drugs in human urine by liquid chromatography-mass spectrometry. Journal of Analytical Toxicology. 20 (5), 281-286 (1996).
- Erni, F. Use of high-performance liquid chromatography in the pharmaceutical industry. Journal of Chromatography A. 507, 141-149 (1990).
- Tsikas, D. Analysis of nitrite and nitrate in biological fluids by assays based on the Griess reaction: Appraisal of the Griess reaction in the l-arginine/nitric oxide area of research. Journal of Chromatography B. 851 (1), 51-70 (2007).
- Zurcher, D. M., Adhia, Y. J., Romero, J. D., McNeil, A. J. Modifying a known gelator scaffold for nitrite detection. Chemical Communications. 50 (58), 7813-7816 (2014).
- Kunduru, K. R., Basu, A., Tsah, T., Domb, A. J. Polymer with pendant diazo-coupling functionality for colorimetric detection of nitrates. Sensors and Actuators B: Chemical. 251, 21-26 (2017).
- Li, D., Ma, Y., Duan, H., Deng, W., Li, D. Griess reaction-based paper strip for colorimetric/fluorescent/SERS triple sensing of nitrite. Biosensors and Bioelectronics. 99, 389-398 (2018).
- Deng, T., et al. A novel strategy for colorimetric detection of hydroxyl radicals based on a modified Griess test. Talanta. 195, 152-157 (2019).
- Pang, H., et al. A photo-responsive macroscopic switch constructed using a chiral azo-calix[4]arene functionalized silicon surface. Chemical Communications (Camb). 54 (24), 2978-2981 (2018).
- Kaur, N., Dhaka, G., Singh, J. Simple naked-eye ratiometric and colorimetric receptor for anions based on azo dye featuring with benzimidazole unit. Tetrahedron Letters. 56 (9), 1162-1165 (2015).
- Liu, F., Lou, J., Hristov, D. X-Ray responsive nanoparticles with triggered release of nitrite, a precursor of reactive nitrogen species, for enhanced cancer radiosensitization. Nanoscale. 9 (38), 14627-14634 (2017).
- Deng, T., et al. An unexpected Griess reaction on the important anti-malarial drug primaquine and its application for drug determination. Journal of Pharmaceutical and Biomedical Analysis. 171, 8-14 (2019).
- Shrivastava, A., Gupta, V. Methods for the determination of limit of detection and limit of quantitation of the analytical methods. Chronicles of Young Scientists. 2 (1), 21-25 (2011).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены