Method Article
Murine линии на основе модели хронического ингибивания CDK9 для изучения широко распространенных негенетических дефектов транскрипционной удлинения (TEопределенно) в раках
В этой статье
Резюме
Протокол детализирует модель карциномы in vitro murine негенетической дефектной удлиненности транскрипции. Здесь, хроническое ингибирование CDK9 используется для подавления продуктивного удлинения РНК Пол II вдоль провоспалительных генов ответ для имитации и изучения клинически overserved TEопределенно явление, настоящее примерно в 20% всех типов рака.
Аннотация
Мы ранее сообщали, что подмножество раковых заболеваний определяется глобальной транскрипционной дерегуляции с широко распространенными недостатками в удлинении транскрипции мРНК (TE) - мы называем такие виды рака, как TEопределенно. Примечательно, что TEопределенно рака характеризуются ложной транскрипции и неисправной обработки мРНК в большой набор генов, таких как интерферон / JAK / STAT и TNF / NF-ЗБ пути, что приводит к их подавления. TEопределенно подтип опухолей в почечно-клеточной карциномы и метастатической меланомы пациентов значительно коррелируют с плохой реакцией и результатом в иммунотерапии. Учитывая важность исследования TEопределенно рака, как это предвещает значительный блокпост против иммунотерапии-цель этого протокола заключается в создании в пробирке TEопределенно мыши модели для изучения этих широко распространенных, не генетических транскрипционные аномалии в раковых заболеваниях и получить новые идеи, новые использует для существующих препаратов, или найти новые стратегии против таких видов рака. Мы подробно использование хронического флавопиридола опосредованного торможения CDK9 для отмены фосфорилирования остатков серина 2 на C-терминале повторенного домена (CTD) РНК-полимеразы II (РНК Пол II), подавляя выпуск РНК Пол II в продуктивную транскрипцию Удлинение. Учитывая, что TEопределенно рака не классифицируются под какой-либо конкретной соматической мутации, фармакологическая модель является выгодным, и лучше всего имитирует широко распространенные транскрипции и эпигенетические дефекты наблюдается в них. Использование оптимизированной сублетальной дозы флавопиридола является единственной эффективной стратегией в создании обобщенной модели негенетических широко распространенных нарушений в пробертионации и дефектах обработки мРНК, тесно имитирующих клинически наблюдаемые TE определенно характеристики. Таким образом, эта модель TEопределенно может быть использовандля для вскрытия, клеток автономных факторов, позволяющих им в противостоянии иммунной опосредоченной атаки клеток.
Введение
Ограничивающим ключевую ставку шагом в выражении почти всех активных генов является переход РНК-полимеразы II (РНК Пол II) от промоторно-проксимальной паузы к продуктивному удлинению1,2. Учитывая, что эпигенетическая дисрегуляция транскрипционной удлинения помогает в прогрессировании нескольких злокачественных новообразований человека определяется как TEопределенно, что приводит к субоптимальной сигнализации в провоспалительных пути реагирования, что составляет плохой ответ и результат иммунотерапии3, общей целью этого протокола является создание полезной модели in vitro для изучения этих широко распространенных негенетических транскрипционных аномалий при раковых заболеваниях. В этом свете использование хронического фармакологического ингибирования CDK9 является эффективной стратегией для создания обобщенной модели негенетических широко распространенных нарушений в удлинении транскрипции и дефектов обработки мРНК. Обоснование мнимой по задиы использования хронического торможения CDK9 является то, что он аннулирует фосфорилирование остатков серина 2 на C-терминале повторного домена (CTD) РНК Pol II, тем самым подавляя выпуск РНК Пол II в продуктивной удлинение транскрипции. Кроме того, TEопределенно рака, описанные ранее нашей группой3, не классифицируются под какой-либо конкретной соматической мутации. Поэтому негенетическая (фармакологическая) модель выгодна и лучше всего имитирует широко распространенные транскрипционные и эпигенетические дефекты, наблюдаемые в них. Метод здесь детализирует поколение и характеристику хронической модели обработки flavopiridol обработки клеток рака murine. Этот метод явно нарушает удлинение транскрипции по генам, характеризующихся более длинной геномной длиной, с готовыми промоутерами и индуцированными выражениями, такими как TNF/NF-- B и интерферон/STAT сигнализация, глубоко контролируемая на уровне транскрипции удлинения3,4,5. В целом, это оптимизированная модель линии клеток морин транскрипционного удлинения - единственная модель, к нашим знаниям для изучения недавно описанных опухолей TE определенно-диски устойчивость к противоопухолевой иммунной атаки, что делает полезную систему для использования и изучить уязвимости негенетических дефектов в основных транскрипционных механизмов в раковых заболеваний по отношению к иммунной опосредошной атаки клеток.
протокол
Институциональный комитет по уходу и использованию животных и Институциональный комитет по биобезопасности Фонда детских исследований Цинциннати одобрили все экспериментальные процедуры для животных (протокол IACUC #2017-0061 и протокол МКБ #IBC2016-0016), и эти эксперименты проводились в соответствии со стандартами, описанными в Руководстве NIH по уходу и использованию лабораторных животных.
1. Хроническое ингибирование РНК Пол II путем лечения флавопиридола-основная стратегия
- Семена B16/F10 клетки меланомы мыши в клетках низкой плотности (0,2 х 106) в 10 см культурная пластина в соответствующей среде (Dulbecco's Модифицированный орел Средний (DMEM), 10% фетальной сыворотки крупного рогатого скота (FBS), 1% пенициллин и стрептомицин »Pen/Strep) и инкубировать на ночь в 37 градусах Цельсия, 5% CO2 увлажняемый инкубатор.
- После дня, мыть клетки с 1x фосфат-буферный солевой раствор (PBS) и добавить новую партию культуры средств массовой информации с сублетальной дозой (оценивается как 25 нм) флавопиридола-ингибитор РНК Пол II удлинение фактор p-TEFb (циклин T/CDK9) - в течение одной недели без дальнейших суб-культивирование.
- После недели лечения флавопиридолом, выполнить подтверждающие анализы для оценки способности модели для повторения различных атрибутов транскрипционного удлинения дефектов видели в TEопределенно рака.
2. Подтверждение иммуноблота анализ для оценки дефектной функции РНК Пол II и нарушение интерферона (IFN) пути и фактор некроза опухоли (TNF) путь сигнализации в сгенерированной мыши TEопределенно модели
- Культура равное количество (105) флавопиридолов лечение B16/F10 клетки меланомы мыши B16/F10 мыши в двух различных наборов из 12 скважин пластин (один набор для РНК Пол II функциональной характеристики, а другой набор для цитокинов стимуляции) при 37 градусах Цельсия в 5% CO2 увлажненного инкубатора на ночь.
- На следующий день обработайте клетки в наборе стимуляции цитокинов с помощью мыши IFN-я, IFN-я (5 нг/мл) или TNF-я (5 нг/мл) в течение 45 мин при 37 градусах По Цельсию.
- Теперь, извлечь белок из клеток в обоих цитокинов и РНК Пол II функциональных наборов характеристик с использованием радиоиммунопреционных анализ (RIPA) лиза буфера в следующем порядке:
- Вымойте клетки с 1x PBS и лизировать его с 50 зл испуг буфера лиза на хорошо. Очистите, а затем гранулы лисизированные клетки при 4 градусах По Цельсия, 21 130 х г.
- Измерьте протеин в супернататах лизата клетки используя стандартный colorimetric анализ для концентрации протеина следуя за solubilization моющего средства (Bradford или подобный анализ).
- Загрузите одинаковое количество измеренного белка (15 мкг) из каждого образца для запуска в 4%-18% полиакриламидного геля натрия (SDS) и перенесите их на поливилинидидные дифлуоридные (PVDF) мембраны.
- Блокировать pVDF мембраны в 5% сухого молока в трис-буферизированный солевой раствор 20 (TBST) в течение 1 ч с последующим ночной инкубации при 4 кС с первичными антителами (RNA Pol II 1:1000; p-SER2 RNA Pol II 1:1000; p-SER5 RNA Pol II 1:1000; p-SER5 RNA Pol II 1:1000; p-SER5 RNA Pol II 1:1000; p-SER5 RNA Pol II 1:1000; p-SER5 RNA Pol II 1:1000; p-SER5 RNA Pol II 1:1000; p-SER5 RNA Pol II 1:1000; p-SER5 RNA Pol II 1:1000; p-SER5 RNA Pol II 1:1000; p-SER5 RNA Pol II 1:1000; p-SER5 RNA Pol II 1:1000; p-SER5 RNA Pol II 1:1000; p-SER5 RNA Pol II 1:1000; p-SER5 RNA Pol H3K36me3 1:2000; всего H3 1:2000; STAT1 1:1000; p-STAT1 1:1000; НФЗБ 1:1000; р-НФЗБ 1:1000; 1:5000) в 5% сыворотки крупного рогатого скота.
- После дня, мыть PVDF мембраны с 1x TBST в течение 15 минут при комнатной температуре (RT), и инкубировать их с соответствующими вторичными антителами (анти-крыса 1:5000) для РНК Пол II, p-SER2 РНК Пол II, и p-SER5 РНК Пол II; анти-кролик (1:5000) для H3K36me3, всего H3, всего H3, STAT1, p-STAT1, НФЗБ и р-НФЗБ) в течение 50 мин на RT. Обнаружить белковые сигналы с помощью коммерчески доступного кунча пероксидаза (HRP) субстрата с усиленной хемилюминесценцией.
ПРИМЕЧАНИЕ: основной используется для основного использования HRP- conjugated, поэтому он может быть разработан без вторичного.
3. Подтверждение ацензии для оценки дефектов обработки мРНК в сгенерированной модели мыши TEопределенно
- Семя равное количество (0,2 х 106) флавопиридолов лечение B16/F10 мыши меланомы клеток и родительских B16/F10 клетки меланомы мыши в 6-колодцев пластин при 37 градусов по Цельсию в 5% CO2 увлажненный инкубатор ночь.
- Извлекайте общую РНК из культивируемых клеток при 60% смоте с помощью реагента или комплекта для извлечения РНК(Таблица материалов).
- Истощайте рРНК из общей добытой РНК следующим образом:
ПРИМЕЧАНИЕ: Протокол с низким уровнем ввода был кооптирован из коммерчески доступного комплекта для истощения rRNA- Установите одну водяную ванну или тепловой блок до 70-75 градусов по Цельсию, а другой водяной бане или тепловом блоке при температуре 37 градусов По Цельсию.
- Добавьте общую РНК (100–500 нг в 2 л безнужной воды) с 1 qL селективного зонда истощения rRNA и 30 qL буфера гибридизации в микроцентрифуге трубки, аккуратно перемешайте вихрем и инкубируя их при 70-75 градусов по Цельсию в течение 5 минут.
- Теперь перенесите трубки в водяную ванну/теплоблок 37 градусов по Цельсию и дайте образцу остыть до 37 градусов по Цельсию в течение 30 мин.
- Отдохните селективное рРНК истощение зондмагнитных бусин вихрей, и aliquot 75 л бусин в 1,5 мл RNase свободной микроцентрифуговой трубки.
- Поместите подвеску из бисера на магнитный сепаратор на 1 мин. Разрешить бисеру, чтобы осесть. Аккуратно аспирируйте и отбросьте супернатант. Повторите мытье бисера еще раз, добавив 75 злител безнужной воды и отбрасывая супернатант после магнитного разделения.
- Отрежь промытые бусинки в буфере гибридизации в 75 qL, и aliquot 25 зл ими в другую трубку и поддерживать его при 37 градусах По Цельсия для последующего использования.
- Поместите оставшиеся шарики 50 л на магнитный сепаратор в течение 1 мин и отбросьте супернатант. Приостановите действие бисера в 20 qL буфера гибридизации и сохранить его на уровне 37 градусов по Цельсию для последующего использования.
- После охлаждения РНК / селективного рРНК истощения зонда смеси до 37 градусов по Цельсию в течение 30 минут, кратко центрифуги трубки для сбора образца в нижней части трубки.
- Передача 33 ЗЛ смеси зонда истощения РНК/селективного РНК к подготовленным магнитным бусинам со ступени 3.3.7. Смешайте с низкой скоростью вихря.
- Инкубировать трубку при 37 градусах по Цельсию в течение 15 мин. Во время инкубации, осторожно смешать содержимое время от времени. Затем краткое центрифугации, чтобы собрать образец в нижней части трубки.
- Поместите трубку на магнитный сепаратор на 1 мин, чтобы гранулировать рнка-зондный комплекс. На этот раз не отбрасывайте супернатант. Супернатант содержит РНК-исчерпанную РНК.
- Поместите трубку из 25 л бусин со ступени 3.3.6 на магнитный сепаратор в течение 1 мин. Аспирируйте и отбросьте супернатант. Добавьте супернатант со ступени 3.3.11 в новую трубку из бисера. Смешайте с низкой скоростью вихря.
- Инкубировать трубку при 37 градусах по Цельсию в течение 15 мин. Во время инкубации, осторожно смешать содержимое время от времени. Кратко центрифуги трубки для сбора образца в нижней части трубки.
- Поместите трубку на магнитный сепаратор на 1 мин, чтобы гранулировать рнка-зондный комплекс. Не отбрасывайте супернатант. Перенесите супернатант (около 53 л), содержащий РНК-исчерпанную РНК, на новую трубку.
- Измерьте концентрацию выхода РНК с помощью спектрофотометра.
- Используйте половину рРНК-обедированных образцов в качестве ввода магнитных бусин, содержащих олиго (dT)25 для извлечения полиАи РНК следующим образом:
ПРИМЕЧАНИЕ: Этот протокол изоляции полиА хвост посланник РНК с использованием олиго dT последовательностей, связанных с поверхностью магнитных бусин был кооптирован из коммерчески доступного комплекта (Таблица материалов).- Resuspend олиго dT бисера во флаконе, кратко вихря для йgt;30 s и передачи 200 л олиго dT бисера на трубу. Добавьте тот же объем (200 л) связывающего буфера и приостановите.
- Поместите трубку в магнит на 1 мин и отбросьте супернатант. Теперь снимите трубку с магнита и приостановите промытые бусины олиго dT в 100 л связывающего буфера.
- Отрегулируйте объем входиного rRNA-исчерпанного общего образца РНК до 100 кЛ с 10 мм Tris-HCl pH 7.5. Теперь добавьте 100 юаней связывающего буфера.
- Нагрейте до 65 градусов по Цельсию в течение 2 мин, чтобы нарушить вторичные структуры РНК. Теперь сразу же поставить на лед.
- Добавьте 200 л общей РНК в 100 юл промытых бусин. Тщательно перемешайте и позвольте связываться, непрерывно вращаясь на роторе в течение 5 мин на РТ.
- Поместите трубку на магнит на 1-2 мин и тщательно удалить все супернатант и тщательно удалить все супернатанты.
- Снимите трубку с магнита и добавьте 200 Зл стирального буфера.
- Измерьте чистоту и концентрацию извлеченной полиАи РНК с помощью спектрофотометра.
ПРИМЕЧАНИЕ: Соотношение 260/280 1,90–2,00 и соотношение 260/230 2,00–2,20 для всех образцов РНК считаются приемлемыми. - Используйте оставшуюся половину рРНК-обедизованных образцов из раздела 3.3 в качестве ввода в колонки белка А (при условии, что в комплекте РНК иммунопреципиции (RIP), Таблица материалов) для иммунопрецитицита пяти-премьерных РНК с использованием моноклональных 7-метилгуанозин антитела следующим образом:
ПРИМЕЧАНИЕ: Этот протокол изоляции m7G ограничен посланник РНК с использованием коммерчески доступных РНК иммунопреципации комплект был кооптирован и дальнейшего изменения.- Вымойте белок Магнитные бусы, полученные из комплекта RIP в соответствии с протоколом производителя, чтобы предварительно связать антитела к бисеру.
- Передача 3 мкг 7-метилгуанозин антитела (кролик IgG, предусмотренных в комплекте может быть использован отрицательный контроль) в бисер в микроцентрифуге трубки приостановлено в 100 зЛ мыть буфер из комплекта.
- Инкубировать с низкой скоростью вращения в течение 30 минут на RT. Центрифуга труб кратко, а затем поместить трубки на магнитный сепаратор, удалить и отбросить супернатанта.
- Удалите трубки и добавьте 500 кЛ буфера для мытья из комплекта и вихря кратко. Centrifuge труб кратко следуют магнитное разделение еще раз, удалить и отбросить супернатант.
- Повторите шаг 3.6.4 еще раз.
- Добавить около 120 нг рРНК истощены (из раздела 3.3) к предварительно промытые 7-метилгуанозин антитела связаны бусы. Добавьте 1 зл ингибитора RNase. Инкубировать на RT за 1'1,5 ч с мягким волнением.
- Спин вниз шарики на 300 х г в течение 10 с и удалить супернатант, содержащий uncapped (не-7-метилгуанозин) мРНК в новую микроцентрифугую трубку.
- Добавьте 100 кл буфера стирки и промойте его еще два раза аналогичным образом. Бассейн собранного супернатанта в той же микроцентрифуговой трубке с надписью uncapped (не-7-метилгуанозин) мРНК. Хранить на льду.
- Elute ограничен (7-метилгуанозин) мРНК из бисера с 300 л мочевины лисис буфера (ULB), содержащий 7 M мочевины, 2% SDS, 0,35 M NaCl, 10 мМ EDTA и 10 мм Tris, pH 7,5 путем нагрева бисера на 65 градусов по Цельсию в течение 2 х 3 мин.
- Смешайте 300 л элетированных образцов (ограниченных и необнаруженных мРНК) с 300 зл и содержанием фенола: хлороформ:изоамильный спирт (25:24:1; коммерчески доступный) (хранится при 4 кВ). Хорошо перемешать путем инвертирования и оставить около 10 мин, то снова аккуратно перемешать.
- Центрифуга на 18928 х г в течение 2 мин и тщательно пипетка верхний слой к свежей трубке и отбросить нижний слой.
- Добавьте в образцы 300 кл/ фенол: хлороформ: изоамил овый спирт (25:24:1; хранится при 4 градусах Цельсия). Хорошо перемешать путем инвертирования, а затем центрифуги на 18928 х г в течение 1 мин. Осторожно, пипетка верхний слой в свежей трубке и отбросить нижний слой.
- Добавьте 300 кЛ 2-порпанола и 30 л из 3 М ацетата натрия (pH 5.2) в ограниченный и незакрытый РНК. Перевернуть образец несколько раз и положить его на -20 градусов по Цельсию в течение 20 ч.
- Теперь центрифуга образцов на 18,928 х г в течение 10 мин при 4 c. Тщательно удалите супернатант и добавьте 500 зл 70% этанола.
- Центрифуга снова на 18,928 х г в течение 10 мин при 4 c. Тщательно отбросьте супернатант и высушите гранулы на RT менее чем на 5 мин. Отрежьте гранулы в безнучащей воде.
- Измерьте чистоту и концентрацию выхода РНК с помощью спектрофотометра. Соотношение 260/280 должно находиться в диапазоне 1,90–2,00, а соотношение 260/230 в диапазоне 2,00–2,20 для всех образцов РНК.
4. Подтверждение асссы для оценки реакции мыши TEопределенно модель FasL опосредоподтвердили смерти клеток
- Семя равное количество (30000 клеток) флавопиридола лечение B16/F10 клетки меланомы мыши И родительских B16/F10 клетки меланомы мыши в 96-хорошо культуры пластины в соответствующей среде (DMEM), и инкубировать на ночь в 37 КС, 5% CO2 увлажненный Инкубатор.
- Лечить клетки в культуре капот с различными концентрациями чего6FasL (0,1-1000 нг/мл) в присутствии 10 мкг/мл анти-Его антитела и инкубировать для 24 ч при 37 кВ, 5% CO2 увлажненный инкубатор.
- Удалите мертвые клетки путем мытья с буфером 1x PBS. Исправить прикрепленные клетки в 4% параформальдегида в течение 20 мин на RT. Отбросьте 4% параформальдегида (не нужно мыть), и пятно с кристаллофиолетовым раствором (20% метанола, 0,5% кристаллфиол в 1x PBS) в течение 30 мин.
- Удалите излишки пятна, аккуратно промыть пластины в водопроводной воде. Держите пластины, чтобы высохнуть на RT.
- Повторно растворить кристаллфиолетовый в 100 л 1x неионического сурфактанта, растворенного в 1x PBS, и измерить плотность клеток путем измерения абсорбции на 570 нм в микроплите читателя.
5. Исследовательский асспой для оценки реакции мыши TEопределенно модель антигена конкретных цитотоксических Т-клеток атаки
- Изоляция и активация цитотоксической Т-клеточной атаки OT-I CD8 (CTL)
- Очистка клеток CD8 от селезенок OT-I TCR Tg RAG-1/) мышей путем разделения магнитных клеток с помощью набора изоляции клеток CD8 T мыши следующим образом:
- Урожай две селезенки из двух OT-I TCR Tg RAG-1 /" мышей в полном носителе RPMI.
- Размять селезенки в фильтре 70 мкм, хранящихся на трубке 50 мл, заполненной 20 мл RPMI, используя заднюю часть шприца, пока только жир остается в фильтре.
- Центрифуга поток через на 220 х г в течение 5 мин при 4 c. Отбросьте супернатант.
- Добавьте 1 мл буфера лиза из красных кровяных телец (РБК) в пеллету селезенки с предыдущего шага центрифугации и пипетку смесь в течение 1 мин.
- Нейтрализуем раствор, добавляя до 10 мл RPMI.
- Центрифуга при 220 х г в течение 5 мин при 4 градусах По цельсию. Откажитесь от супернатанта и отбросьте в 10 мл RPMI.
- Возьмите небольшой аликот для подсчета. Центрифуга оставшиеся на 220 х г в течение 5 мин при 4 C.
- На каждый миллион подсчитанных ячеек повторно приостанавливается действие гранул ы в 1 мл коммерчески доступного буфера магнитной системы разделения (буфер Mojo или аналогичный буфер).
- Приготовьте коктейль из антител объемом 100 л на каждые 1 мл пеллетных клеток в шаге 5.1.1.8. Коктейль из антител включает в себя: биотин анти-CD4, CD105, CD45R/B220, CD11c, CD49b, TER-119, CD19, CD11b, TCR q/q и CD44.
- Добавьте этот коктейль в 1 мл пеллетных клеток и держите на льду 15 мин.
- Добавьте 100 л магнитных (стрептавидин) бусин к каждые 100 л коктейля антител, добавленных в 1 мл resuspended гранулированных клеток селезенки. Держите на льду в течение 15 минут.
- Добавьте 7 мл коммерчески доступного буфера магнитной системы разделения. Теперь, aliquot около 3'4 мл смеси в свежей трубке. Хорошо перемешать и зафиксировать его к магниту в течение 5 минут.
- Декант жидкости (содержит клетки CD8 ' ) в свежей трубке на льду. Теперь, aliquot оставшиеся 3'4 мл смеси от шага 5.1.1.12 к трубе и исправить его к магниту в течение 5 мин. Декант жидкости (вторая партия CD8 "клеток изолированы) в той же трубке, содержащей первую партию клеток CD8 "хранится на льду.
- Семена инженерии адепт фибробласта APC-(MEC. B7. SigOVA) линия, чтобы выразить конкретные овальбумин (OVA) полученных, H-2Kb-ограниченный пептид эпитоп OVA257-264 (SIINFEKL), наряду с костимуляторной молекулы B7.1, на 75000 клеток на скважину в 24-хорошо пластин, при 37 градусов по Цельсию, 5% CO2 humidified into.
ПРИМЕЧАНИЕ: Используемый фибробласт адепта является подарком от лаборатории доктора Эдит Янссен в CCHMC. Линия была создана первоначально в лаборатории доктора Стивена. Шёнбергера в Институте аллергии и иммунологии Ла Хойя6. - После 24 ч, мыть монослой БТР один раз с iscove в модифицированных Dulbecco в среднем (IMDM) коммерчески доступны с HEPES буфера, пируват натрия, L-глутамин и высокая глюкоза), и добавить 0,5 х 106 наивных OT-I CD8 "клетки (от шага 5.1.1.13) в 2 мл IMMD дополнено 50 мМ-ММ-МЭ, 2 мл EDTA, 4 мм L-глютамин и HEPES и 10% FBS.
- После 20 ч аккуратно собирайте неадекватные клетки OT-I (путем сбора носителей в культурном блюде с плавающими клетками OT-I и гранулированием клеток при 191 х г в течение 2 мин; подсчитайте жизнеспособные от-I-клетки) и перенесите их для совместной культуры.
- Очистка клеток CD8 от селезенок OT-I TCR Tg RAG-1/) мышей путем разделения магнитных клеток с помощью набора изоляции клеток CD8 T мыши следующим образом:
- Сокультура клеток CD8 с клетками B16/F10-OVA
- Семена OT-I-полученных CD8 "клетки в соотношении 1:1 (300 000 клеток каждый) в совместной культуре с B16/F10 (отсутствие антигена ovalbumin), необработанные B16/F10-OVA, и B16/F10-OVA клетки предварительно обработаны flavopiridol (25 nM) в течение 1 недели, в 6-м блюд носителей для 20 ч при 37 градусах Цельсия в 5% CO2 увлажненный инкубатор.
- После 20 ч удалите клетки CD8, полученные ИЗ OT-I (путем сбора носителей в культурном блюде с плавающими клетками OT-I). Вымойте адепт B16/F10-OVA клетки в 1x PBS.
- Трипсинизуйте три группы прикрепленных клеток B16/F10-OVA в 0,05% EDTA, содержащий трипсин в течение 5 мин. Пелле трипсинизированные клетки при 191 х г в течение 5 мин.
- Пятно собранных B16/F10-OVA клеток путем инкубации их в холодной PBS (содержащий 0,5% FBS и 0,05% азида натрия) с выживаемости красителя и соответствующих помеченных антител (фиксируемые жизнеспособность окрашивания красителя e780, AF647-конъюгированных мыши CD8 и BV421-конъюгированных мыши CD45 ).
- Проанализируйте жизнеспособность трех групп клеток B16/F10-OVA с помощью цитометрии потока.
Результаты
Здесь мы предоставляем подробную схему (Рисунок 1) для создания TEопределенно клеточной модели, полученной хроническим суб-смертельным(Рисунок 2) лечение флавопиридолом на 25 нм. На рисунке 3, на 3 дня лечения флавопиридолом, B16 OVA клетки показывают частичные характеристики TEопределенно, но после одной недели лечения, B16/F10 OVA клетки показывают глубокую потерю фосфорилирования на засечение 2 позиции на CTD РНК Пол II вдоль со значительным снижением H3K36me3 - модификации гистона, замешанной в определении границ экзона и ингибитором захудалых загадочных транскрипций. Как следствие, TEопределенно клеточная модель показывает критические дефекты обработки мРНК с явно повышенным соотношением неправильно ограничен и не-поли-адениатерированных мРНК(рисунок 4A,B). Кроме того, конкретные репрессии ключевых воспалительных пути пути генов и FasL опосредованного пути смерти клеток видны на рисунке 5 и рисунке 6. Навязанная устойчивость к интерферону (IFN-я, IFN) и ТНФ-з стимулировала фосфорилирование STAT1 и NF-B, а устойчивость к клеточной смерти рецептором смерти ligand FasL резко снижает цитотоксичность нападения иммунных клеток против TEопределенно Опухоли. Эти подтверждающие методы предназначены для проверки степени влияния хронического возмущения удлинения транскрипции имеет на широкий спектр стимул-ответных генов, и является ли такое возмущение в данной модели линии мыши достаточно, чтобы подскакние острого недостатка функциональной мРНК в воспалительных реакции сигнализации генов, имитируя основные основы TEопределенно рака клинически. Основываясь на нашем исследовании лечения флавопиридола, подавление фосфорилирования на втором остатке серина (pSER2) РНК Пол II CTD имеет решающее значение, так как он знаменует транскрипции удлинения. Сублетальная доза для любой данной линии клеток карциномы мыши должна достичь снижения уровня pSER2 в дополнение к незначительному влиянию на темпы роста и жизнеспособность клеточной линии. Хотя мы постоянно видим снижение уровня pSER2 и H3K36me3 на 25 нм флавопиридолов лечения, это не гарантирует подавление как pSTAT1 и pNF -B уровня (на IFN-З, IFN и TNF-- стимуляции, соответственно). Каждая линия клеток карциномы мыши уникальна (B16/F10 OVA или CT26 клетки культивируются в различных лабораториях в течение определенного периода времени, возможно, слегка измененные эффекты), и они могут иметь либо JAK1 или CCNT1 частично спасая эффекты флавопиридола в подавлении воспалительные пути реакции генов. В таких случаях, кинетика уровней pSTAT1 и pNF-B, возможно, потребуется проверить в разных временных точках (5–70 минут), чтобы понять временность опосредованного эффекта флавопиридола и его спасение либо JAK1, либо CCNT1. Соответственно, для создания этой модели, возможно, потребуется сбить JAK1 и/или CCNT1.
После того, как модель флавопиридола устанавливается и характеризуется с помощью вышеупомянутых анализов, мы предоставляем исследовательский анализ, чтобы проверить, если TEопределенно клеточной модели дает устойчивость к цитотоксическомУ Т-клеток (CTL) атаки. Основываясь на нашем оптимизированном протоколе, флавопиридол лечил клетки B16/F10, уступив гену OVA (B16 OVA), совместно инкубированным с активированными CD8» CTL (специфическим для эпитопа OVA257-264), имеющим селективную токсичность для OVA-expressing клеток (подарок от Доктора. Лаборатория Стивена. Шёнбергера6) не были восприимчивы к OT-I CTL-опосредованного опухолевого лиза. Клетки B16/F10 OVA (не обработанные флавопиридолом) подверглись массовой клеточной смерти в этой системе, в то время как родительские клетки B16/F10 выжили, так как они не выражают антиген OVA(рисунок 7). Из результатов предлагаемого исследовательского исследования ясно, что хронический флавопиридол-индуцированных TEопределенно может даровать средства, чтобы избежать противоопухолевой иммунной атаки даже in vivo. Это может быть дополнительно протестировано в in vivo моделей опухоли, чтобы проверить склонность TEопределенно модели, чтобы избежать врожденных и адаптивных противоопухолевых иммунных реакций. Анти-азиало лечения могут быть использованы для регулирования деятельности НК-клеток in vivo в опухоли подшипников мышей. Кроме того, иммунная контрольная терапия (анти-CTLA4 и анти-PD1) может быть введена для TEопределенно опухоли подшипников мышей.
В совокупности, TEопределенно подтверждающие анализы вместе с предлагаемым исследовательским анализом вместе продемонстрировать полезность включения этой модели т.д.определенно клеточной в целом ряде других опухолевых иммунных условий тестирования. Эта модель может помочь разобрать молекулярные детали в результате дефектной транскрипционной удлинение в опухолевых клетках и их ответ на иммунные клетки взаимодействия.

Рисунок 1: Схематическое представление рабочего потока. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.

Рисунок 2: Характеристики роста клеток Клеток клеток клеток B16 OVA хронически обработаны с низкими дозами флавопиридола: Жизнеспособность (измеренная реагентом жизнеспособности) контроля и флавопиридолов лечения клеток B16 OVA в указанные дни после лечения. Эта цифра была изменена от Modur и др.3. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.

Рисунок 3: Подтверждающий анализ для оценки РНК Пол II и гистон профиля: Иммуноблоты указал гистон и РНК Пол II марок в B16 OVA клеток, обработанных флавопиридол в течение 72 ч или 1 неделю. Эта цифра была изменена от Modur и др.3. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
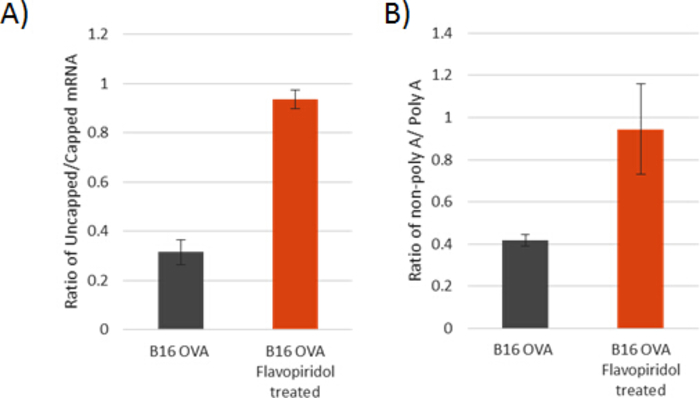
Рисунок 4: Подтверждающий аттестинг для оценки серьезных дефектов в обработке мРНК. Коэффициенты от 5 "непокрытые до 5" крышкой (A) и 3 "не-полиаденетилированных до 3"-полиаденила(B) концентрации мРНК после истощения rRNA в указанных клеточных линий. Бары ошибок представляют собой стандартное отклонение на основе трех технических повторений. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.

Рисунок 5: Подтверждающий ассоциационный осмотр для оценки профиля стимуляции цитокинов. Иммуноблоты STAT1, pSTAT1, НФЗБ и НФЗБ в контроле и флавопиридоле предварительно обработанных клеток B16 OVA, стимулируемых с помощью IFN-з, IFN или TNF-я в течение 30 мин при 5 нг/мл. Эта цифра была изменена от Modur и др.3. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
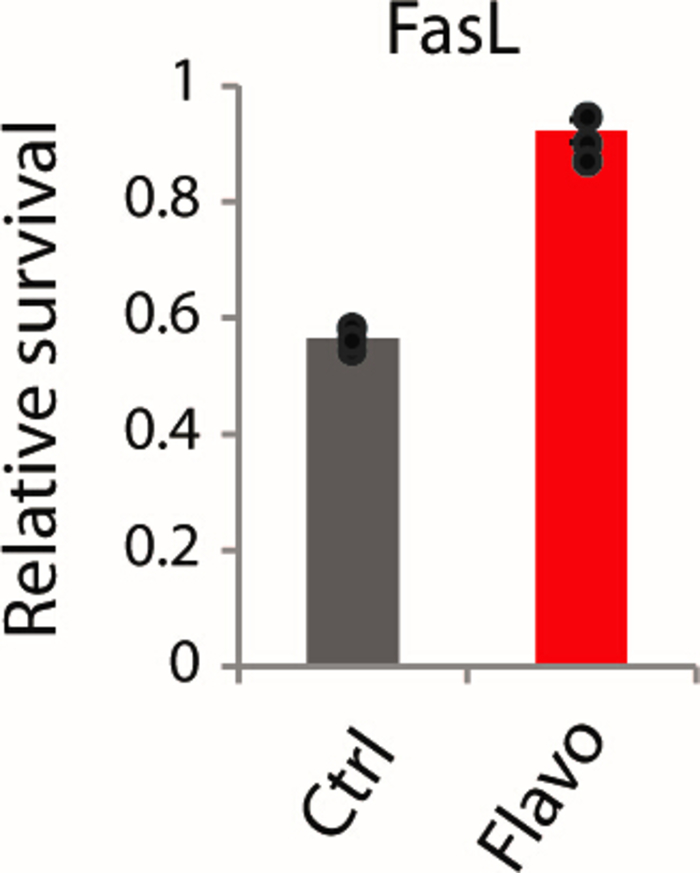
Рисунок 6: Подтверждающий анализ для оценки устойчивости к FasL опосредошной смерти клеток в пробирке. Контроль и флавидидол предварительно обработанных B16 OVA клеток, обработанных FasL для 24 h считывание измеряется жизнеспособностью асссе. Эта цифра была изменена от Modur и др.3. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
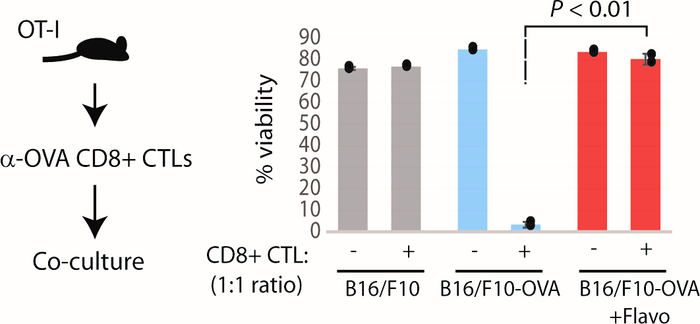
Рисунок 7: Исследовательский анализ для оценки устойчивости TEопределенно модели антигена ограниченный цитотоксический Т-клеток опосредоченной атаки в пробирке. Слева: схематическая схема исследовательского исследования. Справа: относительная жизнеспособность клеток B16/F10-OVA, совместно культурных с активированными CD8 и CTL (коэффициент 1:1), изолированными от селезенок мышей OT-I. P: Уэлч два образца t-тест. Эта цифра была изменена от Modur и др.3. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
Обсуждение
Контроль удлинения РНК Пол II стал решающим рычагом для регулирования стимул-ответных экспрессии генов в пользу злокачественных клеток5,7,8. Преодоление промоутер-проксимальной паузы на удлинение и последующее производство мРНК требует киназы деятельности P-TEFb9,10,11. Наша модель использует флавидидол (25 нм), ингибитор основных циклин-зависимых киназы CDK9, чтобы имитировать дефекты, наблюдаемые во время удлинения Пол II в TEопределенно рака-ранее неизвестный фенотип в раковых заболеваниях, обнаруженных нашей группой ранее3.
CDK9 киназы деятельности уже давно известно, что имеет важное значение для фосфорилирования остатков серина 2 в CTD большого подразделения Pol II. Критически, мы преуспели в оптимизации флавопиридола лечение хронического ингибирования CDK9 (25 нм в течение 1 недели) в B16/F10 OVA таким образом, что, в дополнение к ингибированию ЦТД фосфорилирования, 25 нМ flavopiridol лечение в течение 1 недели предотвращает надлежащее посттранскрипции модификации мРНК непредвиденным образом и фактически аннулирует p-TEFb-зависимое продуктивное удлинение вдоль длинных генов, таких как провоспалительные сигнальные гены, значительно изменяя их модели выражения как на мРНК, так и уровень белка. Насколько нам известно, в литературе нет другой модели, которая эффективно добивается того же.
Это легко установить, обобщаемая модель TEопределенно может быть использовано для вскрытия, как транскрипционные и эпигенетические изменения, позволяющие TEопределенно рака адаптироваться к иммунной опосредоченной атаки клеток. Кроме того, эта модель мурина сохраняет свой TEопределенно-как сокращение общего и фосфо-РНК Пол II уровнях 21 дней после флавопиридола релиз в in vivo анализа роста3 (не упоминается в протоколе здесь), предлагая степень стабильности этого негенетической модели для дальнейших экспериментов в vivo. Тем не менее, необходимо позаботиться о том, чтобы оптимизировать точную сублетальную дозу флавопиридола для других линий мурина (например, около 20 нм флавопиридола лечение в течение 1 недели является сублетальной дозой для линии карциномы MC38 murine; не используется в этом протоколе), влияние изменения в клетках плотность покрытия, культурные условия и условия стимуляции цитокинов могут варьироваться для различных линий мурин. Описанный здесь протокол дает базовую основу для минимизации переменных, которые, как известно, имеют решающее значение для генерацииTE, каки особенности хронического торможения CDK9. Кроме того, человеческие линии клеток карциномы, такие как T47D и CAL51 были протестированы с краткосрочными (3 дня) флавопиридола лечения, что приводит к аналогичным TEопределенно-как РНК Пол II профилей, что свидетельствует о полезности флавопиридола основе хронического ингибирования CDK9 опосредоченной транскрипции удлинение в создании даже модели человеческих линий для изучения TEопределенно.
Раскрытие информации
Авторам нечего раскрывать.
Благодарности
Эта работа была частично поддержана NCI (CA193549) и CCHMC Research Innovation Pilot награды Какаджан Комуров, и Министерство обороны (BC150484) награду Навнит Сингх. Содержание является исключительно ответственностью авторов и не обязательно представляют официальные взгляды Национального института рака или Министерства обороны. Спонсоры не принимали никакого значения в разработке, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Материалы
| Name | Company | Catalog Number | Comments |
| hhis6FasL | Cell Signaling | 5452 | |
| 10X TBS | Bio-Rad | 170-6435 | |
| 12 well plates | Falcon | 353043 | |
| 20% methanol | Fisher Chemical | A412-4 | |
| 24-well plates | Falcon | 351147 | |
| 4–18% SDS polyacrylamide gel | Bio-Rad | 4561086 | |
| 4% Paraformaldehyde | Thermo Fisher Scientific | AAJ19943K2 | |
| 5% dry milk | Bio-Rad | 170-6404 | |
| 7-Methylguanosine antibody | BioVision | 6655-30T | |
| 96-well plates | Cellstar | 655180 | |
| AF647-conjugated mouse CD8 | Biolegend | 100727 | |
| antibiotic and antimycotic | Gibco | 15240-062 | |
| anti-His antibody | Cell Signaling | 2366 P | |
| Anti-Rabit | Cell Signaling | 7074 | Dilution 1:5000 |
| Anti-Rat | Cell Signaling | 7077S | Dilution 1:5000 |
| Bradford assay Kit | Bio-Rad | 5000121 | |
| BSA | ACROS Organics | 24040-0100 | |
| BV421-conjugated mouse CD45 | Biolegend | 109831 | |
| crystal violet | Sigma | C3886-100G | |
| DMEM | Gibco | 11965-092 | |
| Dynabeads Oligo (dT)25 | Ambion | 61002 | |
| FBS | Gibco | 45015 | |
| Fixable Live/Dead staining dye e780 | eBioscience | 65-0865-14 | |
| Flavopiridol | Selleckchem | S1230 | |
| H3k36me3 | Abcam | ab9050 | Dilution 1:2000 |
| IFN-α | R&D systems | 12100-1 | |
| IFN-γ | R&D systems | 485-MI-100 | |
| IMDM | Gibco | 12440053 | |
| Immobilon Western Chemiluminescent HRP Substrate | Millipore | WBKLS0500 | |
| MojoSort Mouse CD8 T Cell Isolation Kit | Biolegend | 480007 | |
| NF-κB | Cell Signaling | 8242s | Dilution 1:1000 |
| PBS | Gibco | 14190-144 | |
| p-NF-κB | Cell Signaling | 3033s | Dilution 1:1000 |
| p-Ser2-RNAPII | Active Motif | 61083 | Dilution 1:500 |
| p-Ser5-RNAPII | Active Motif | 61085 | Dilution 1:1000 |
| p-STAT1 | Cell Signaling | 7649s | Dilution 1:1000 |
| RiboMinu Eukaryote Kit | Ambion | A10837-08 | |
| RIPA buffer | Santa Cruz Biotechnology | sc-24948 | |
| RNAPII | Active Motif | 61667 | Dilution 1:1000 |
| STAT1 | Cell Signaling | 9175s | Dilution 1:1000 |
| TNF-α | R&D systems | 410-MT-010 | |
| total H3 | Cell Signaling | 4499 | Dilution 1:2000 |
| Tri reagent | Sigma | T9424 | |
| Triton | Sigma | T8787-50ML | |
| Tween 20 | AA Hoefer | 9005-64-5 | |
| β-Actin | Cell Signaling | 12620S | Dilution 1:5000 |
| β-ME | G Biosciences | BC98 |
Ссылки
- Adelman, K., Lis, J. T. Promoter-proximal pausing of RNA polymerase II: emerging roles in metazoans. Nature Reviews Genetics. 13 (10), (2012).
- Margaritis, T., Holstege, F. C. Poised RNA polymerase II gives pause for thought. Cell. 133 (4), 581-584 (2008).
- Modur, V., et al. Defective transcription elongation in a subset of cancers confers immunotherapy resistance. Nature Communications. 9 (1), 4410 (2018).
- Hargreaves, D. C., Horng, T., Medzhitov, R. Control of inducible gene expression by signal-dependent transcriptional elongation. Cell. 138 (1), 129-145 (2009).
- Adelman, K., et al. Immediate mediators of the inflammatory response are poised for gene activation through RNA polymerase II stalling. Proceedings of the National Academy of Sciences of the United States of America. 106 (43), 18207-18212 (2009).
- van Stipdonk, M. J., Lemmens, E. E., Schoenberger, S. P. Naïve CTLs Require a Single Brief Period of Antigenic Stimulation for Clonal Expansion and Differentiation. Nature Immunology. 2 (5), 423-429 (2001).
- Gilchrist, D. A., et al. Regulating the regulators: the pervasive effects of Pol II pausing on stimulus-responsive gene networks. Genes & Development. 26 (9), 933-944 (2012).
- Danko, C. G., et al. Signaling pathways differentially affect RNA polymerase II initiation, pausing, and elongation rate in cells. Molecular Cell. 50 (2), 212-222 (2013).
- Nechaev, S., Adelman, K. Pol II waiting in the starting gates: Regulating the transition from transcription initiation into productive elongation. Biochimica et Biophysica Acta (BBA)-Gene Regulatory Mechanisms. 1809 (1), 34-45 (2011).
- Zhou, M., et al. Tat modifies the activity of CDK9 to phosphorylate serine 5 of the RNA polymerase II carboxyl-terminal domain during human immunodeficiency virus type 1 transcription. Molecular and Cellular Biology. 20 (14), 5077-5086 (2000).
- Palancade, B., Bensaude, O. Investigating RNA polymerase II carboxyl‐terminal domain (CTD) phosphorylation. European Journal of Biochemistry. 270 (19), 3859-3870 (2003).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены