Method Article
نموذج خط خلية Murine القائم على تثبيط CDK9 المزمن لدراسة عيوب الاستطالة غير الوراثية الواسعة الانتشار (TEبالتأكيد)في السرطانات
In This Article
Summary
يفصّل البروتوكول نموذج سرطان المورين في المختبر لاستطالة النسخ المعيبة غير الوراثية. هنا، يستخدم تثبيط المزمن من CDK9 لقمع استطالة الإنتاجية من RNA Pol II على طول الجينات استجابة المؤيدة للالتهابات لتقليد ودراسة ظاهرة TE المفرطة سريريابالتأكيد، موجودة في حوالي 20٪ من جميع أنواع السرطان.
Abstract
لقد سبق لنا أن أبلغنا أن مجموعة فرعية من السرطانات يتم تعريفها عن طريق إلغاء اللوائح النسخية العالمية مع أوجه القصور على نطاق واسع في استطالة النسخ mRNA (TE) - ونحن ندعو مثل هذه السرطانات كما TEبالتأكيد. وتجدر الإشارة إلى أن السرطانات TEتتميز بالتأكيد بالنسخ الهامشي ومعالجة الحمض النووي الريبي الخاطئ في مجموعة كبيرة من الجينات، مثل مسارات الإنترفيرون/جاك/ستات وTNF/NF-ņB، مما يؤدي إلى قمعها. وTEبالتأكيد النوع الفرعي من الأورام في سرطان الخلايا الكلوية ومرضى الورم الميلانيني النقيلي ترتبط بشكل كبير مع ضعف الاستجابة والنتيجة في العلاج المناعي. وبالنظر إلى أهمية التحقيق في سرطان TEبالتأكيد - كما أنه ينذر بحاجز كبير ضد العلاج المناعي - والهدف من هذا البروتوكول هو إنشاء في المختبر TEبالتأكيد نموذج الماوس لدراسة هذه واسعة النطاق، غير وراثية التشوهات النسخية في السرطانات والحصول على رؤى جديدة، والاستخدامات الجديدة للأدوية الموجودة، أو العثور على استراتيجيات جديدة ضد مثل هذه السرطانات. نحن بالتفصيل استخدام الفلافوبيريدول المزمن بوساطة CDK9 تثبيط لإلغاء الفوسفور من بقايا سيرين 2 على C-محطة تكرار المجال (CTD) من الحمض النووي الريبي بوليميراز الثاني (RNA Pol II)، وقمع الإفراج عن RNA Pol II في النسخ المنتجة استطاله. وبالنظر إلى أن السرطانات TEبالتأكيد لا تصنف تحت أي طفرة جسدية محددة، نموذج الدوائية مفيد، وأفضل يحاكي العيوب النسخية والجينية على نطاق واسع لوحظ في نفوسهم. استخدام جرعة شبه قاتلة الأمثل من flavopiridol هو الاستراتيجية الفعالة الوحيدة في خلق نموذج قابل للتعميم من اضطراب غير وراثي على نطاق واسع في استطالة النسخ وعيوب معالجة الحمض النووي الريبي، وتقليد عن كثب TE لوحظ سريريا بالتأكيد الخصائص. ولذلك، فإن هذا النموذج من TEبالتأكيد يمكن الاستفادة من تشريح، والعوامل الخلية المستقلة تمكنهم من مقاومة هجوم الخلايا بوساطة المناعة.
Introduction
خطوة رئيسية الحد من معدل في التعبير عن جميع الجينات النشطة تقريبا هو انتقال بوليميراز الحمض النووي الريبي الثاني (RNA Pol II) من التوقف المروج القريب إلى استطالة الإنتاجية1،2. وبالنظر إلى أن خلل التنظيم الجيني للاستطالة النسخية يساعد في تطور الأورام الخبيثة البشرية المتعددة التي تعرف بأنها TEبالتأكيد، مما يؤدي إلى إشارات دون المستوى الأمثل في مسارات الاستجابة المؤيدة للالتهابات التي تصل إلى استجابة ضعيفة والنتيجة للعلاج المناعي3، والهدف الشامل من هذا البروتوكول هو إنشاء نموذج مفيد في المختبر لدراسة هذه التشوهات غير الوراثية على نطاق واسع في السرطان. في ضوء ذلك، فإن استخدام التثبيط الدوائي المزمن لCDK9 هو استراتيجية فعالة لخلق نموذج قابل للتعميم من اضطراب غير وراثي على نطاق واسع في استطالة النسخ وعيوب معالجة الحمض النووي الريبي. الأساس المنطقي وراء استخدام تثبيط CDK9 المزمن هو أنه يلغي الفوسفور من بقايا سيرين 2 على C-محطة تكرار المجال (CTD) من RNA Pol II، وبالتالي قمع الإفراج عن RNA Pol II في استطالة النسخ المنتجة. أيضا، TEبالتأكيد السرطانات، التي وصفت سابقا من قبل مجموعتنا3، لا تصنف تحت أي طفرة جسدية محددة. ولذلك، فإن النموذج غير الوراثي (الدوائي) مفيد ويحاكي على أفضل وجه العيوب النسخية والجينية المنتشرة التي لوحظت فيها. الطريقة هنا تفاصيل توليد وتوصيف نموذج العلاج المزمن فلافوبيريدول من الخلايا السرطانية المورين. هذا الأسلوب يعطل بشكل واضح استطالة النسخ على طول الجينات التي تتميز أطوال الجينوم أطول، مع المروجين تستعد والتعبيرات اللاإستطيعة مثل TNF / NF-ņB والتداخل / STAT الإشارات، تسيطر عليها بعمق على مستوى استطالة النسخ3،4،5. بشكل عام، هذا النموذج الأمثل خط الخلية المورين من عيوب استطالة النسخ - النموذج الوحيد لمعلمتنا لدراسة الأورام TE وصفها حديثابالتأكيد - يدفع المقاومة للهجوم المناعي المضادة للورم، مما يجعل نظام مفيد لاستغلال و دراسة نقاط الضعف من العيوب غير الوراثية في آلات النسخ الأساسية في السرطانات في مواجهة هجوم الخلايا المناعية بوساطة.
Protocol
وافقت اللجنة المؤسسية لرعاية الحيوانات واستخدامها واللجنة المؤسسية للسلامة البيولوجية التابعة لمؤسسة سينسيناتي لبحوث الأطفال على جميع الإجراءات التجريبية الحيوانية (بروتوكول IACUC #2017-0061 وبروتوكول IBC #IBC2016-0016)، وهذه الإجراءات أجريت التجارب وفقا للمعايير كما هو موضح في دليل المعاهد القومية للصحة لرعاية واستخدام الحيوانات المختبرية.
1. تثبيط مزمن من الحمض النووي الريبي بول الثاني عن طريق العلاج flavopiridol - الاستراتيجية الأساسية
- البذور B16/F10 خلايا الورم الميلانيني الماوس في كثافة منخفضة (0.2 × 106)في لوحة ثقافة 10 سم في وسطها المقابلة (دولبكو تعديل النسر المتوسط [DMEM]، 10٪ مصل البقر الجنيني [FBS]، 1٪ البنسلين والعقدية [القلم / العقدية]) وحضانة بين عشية وضحاها في حاضنة 37 درجة مئوية، 5٪ CO2 ترطيب.
- بعد يوم، غسل الخلايا مع 1X الفوسفات المخزنة المالحة (PBS) وإضافة دفعة جديدة من وسائل الإعلام الثقافة مع جرعة دون قاتلة (تقدر ب25 nM) من flavopiridol - مثبط اتطالية RNA Pol II عامل p-TEFb (سيكلين T / CDK9) - لمدة أسبوع واحد دون مزيد من شبه زراعة.
- بعد أسبوع من العلاج فلافوبيريدول, إجراء الاختبارات المؤكدة لتقييم قدرة النموذج على تلخيص سمات مختلفة من عيوب استطالة النسخ ينظر في TEالسرطان بالتأكيد.
2. اختبار المناعية تأكيدية لتقييم خلل الحمض النووي الريبي Pol II وظيفة وضعف مسار الإنترفيرون (IFN) وعامل نخر الورم (TNF) مسار إشارة في الماوس المولدTE نموذجبالتأكيد
- ثقافة يساوي عدد (105)من flavopiridol تعامل B16/F10 خلايا الورم الميلانيني الماوس والآباء B16/F10 خلايا الورم الميلانيني الماوس في مجموعتين مختلفتين من 12 لوحات جيدا (مجموعة واحدة لRNA Pol II توصيف وظيفي ومجموعة أخرى للسيتوكين التحفيز) في 37 درجة مئوية في 5٪ CO2 حاضنة رطبة بين عشية وضحاها.
- في اليوم التالي، علاج الخلايا في التحفيز السيتوكين تعيين مع الماوس IFN-γ، IFN-α (5 نانوغرام / مل)، أو TNF-α (5 نانوغرام / مل) لمدة 45 دقيقة عند 37 درجة مئوية.
- الآن، استخراج البروتين من الخلايا في كل من السيتوكين وRNA Pol II مجموعات توصيف وظيفية باستخدام اختبار الاشعاعالمناعي الترسيب (RIPA) الليسيا العازلة بالطريقة التالية:
- غسل الخلايا مع 1X PBS وlyse مع 50 درجة مئوية من العازلة lysis لكل بئر. كشط، ومن ثم بيليه الخلايا lysed في 4 درجة مئوية، 21،130 × ز.
- قياس البروتين في الخلايا lysate supernatants باستخدام فحص قياس اللون القياسية لتركيز البروتين بعد الذوبان المنظفات (برادفورد أو فحص مماثل).
- قم بتحميل كمية متساوية من البروتين المقاس (15 ميكروغرام) من كل عينة لتشغيلها في هلام بولي أكريلاميد بولي أكريلايد (PVDF) من كبريتات دوديسيل الصوديوم 4%-18%، وينقلها إلى أغشية ثنائي الفينيل الدين ديفيلوريد (PVDF).
- منع أغشية PVDF في 5% من الحليب الجاف في الحليب الجاف الـ tris-buffered-polysorbate 20 (TBST) لمدة ساعة واحدة متبوعاً بحضانة بين عشية وضحاها عند درجة حرارة 4 درجة مئوية مع الأجسام المضادة الأولية (RNA Pol II 1:1000; p-SER2 RNA Pol II 1:1000; p-SER5 RNA Pol II 1:1000; H3K36me3 1:2000; مجموع H3 1:2000؛ STAT1 1:1000; p-STAT1 1:1000; NFיB 1:1000; ع-NFיB 1:1000; β-أكتين 1:5000) في 5٪ ألبوم المصل البقري.
- بعد يوم، غسل أغشية PVDF مع 1X TBST لمدة 15 دقيقة في درجة حرارة الغرفة (RT)، واحتضانها مع الأجسام المضادة الثانوية المناسبة (المضادة للفئران [1:5000] لRNA Pol II، p-SER2 RNA Pol II، و p-SER5 RNA Pol II؛ المضادة للأرنب (1:5000) لH3K36me3، مجموع H3، STAT1, p-STAT1, NFיB, and p-NFיB) لمدة 50 دقيقة في RT. الكشف عن إشارات البروتين باستخدام البيروكسيداز الفجل المتاحة تجاريا (HRP) الركيزة مع chemiluminescenceence تعزيز.
ملاحظة: β-أكتين الابتدائية المستخدمة هي HRP-مترافقة، وبالتالي فإنه يمكن تطويرها دون الثانوية.
3. اختبار تأكيدي لتقييم عيوب معالجة mRNA في نموذج TE الماوس ولدتبالتأكيد
- البذور عدد متساو (0.2 × 106)من flavopiridol علاج B16 /F10 خلايا الورم الميلانيني الماوس والخلايا الميلانوما الماوس B16/F10 الوالدين في لوحات 6-جيدا في 37 درجة مئوية في 5٪ CO2 حاضنة رطبة بين عشية وضحاها.
- استخراج الجيش الملكي النيبالي الكلي من الخلايا المستزرعة في 60٪ من الملاءمة باستخدام كاشف استخراج الحمض النووي الريبي أو عدة(جدول المواد).
- [بفور] [رنا] من ال [رنا] إجماليّة يستخرج في الطريقة تالي:
ملاحظة: تم اختيار بروتوكول منخفض الإدخال من مجموعة متاحة تجارياً لاستنفاد rRNA- تعيين حمام مائي واحد أو كتلة الحرارة إلى 70-75 درجة مئوية، وحمام مائي آخر أو كتلة الحرارة عند 37 درجة مئوية.
- أضف إجمالي الحمض النووي الريبي (100-500 نانوغرام في 2 ميكرولتر من المياه الخالية من النوكل) مع 1 ميكرولتر من مسبار استنفاد rRNA الانتقائي و30 ميكرولتر من حاجز التهجين في أنبوب الطرد المركزي الصغير، ومزجه بلطف عن طريق التدوام واحتضانه عند 70-75 درجة مئوية لمدة 5 دقائق.
- الآن، نقل الأنابيب إلى حمام المياه 37 درجة مئوية / كتلة الحرارة، والسماح للعينة لتبرد إلى 37 درجة مئوية على مدى فترة 30 دقيقة.
- إعادة تعليق الداخلية الإلكترونية الانتقائية استنفاد استنفاد الخرز المغناطيسي عن طريق الدوامة، وaliquot 75 ميكرولتر من الخرز في أنبوب الطرد المركزي خالية من RNase 1.5 مل.
- وضع تعليق حبة على فاصل المغناطيسي لمدة 1 دقيقة. يستنشق بلطف وتجاهل supernatant. كرر غسل الخرز مرة أخرى عن طريق إضافة 75 درجة مئوية من المياه الخالية من nuclease والتخلص من supernatant بعد فصل المغناطيسي.
- إعادة تعليق الخرز المغسول في 75 درجة مئوية من العازلة التهجين، وaliquot 25 ميكرولتر منه إلى أنبوب آخر والحفاظ عليه في 37 درجة مئوية للاستخدام في وقت لاحق.
- ضع حبات 50 ميكرولتر المتبقية على فاصل مغناطيسي لمدة دقيقة واحدة وتجاهل supernatant. إعادة تعليق الخرز في 20 درجة مئوية من العازلة التهجين والحفاظ عليه في 37 درجة مئوية للاستخدام في وقت لاحق.
- بعد التبريد من ال [رنا]/انتقائيّة [ررنا] استنفاد تحقيق خليط إلى 37 [ك] ل 30 دقائق, بإيجاز طارد ة جهاز دفع مركزيّ الأنبوبأن يجمع العينة إلى القعر من الأنبوبة.
- نقل 33 درجة مئوية من خليط مسبار استنفاد الحمض النووي الريبي/rRNA الانتقائي إلى الخرز المغناطيسي المعد من الخطوة 3-3-7. مزيج من سرعة منخفضة الدوامة.
- حضانة الأنبوب عند 37 درجة مئوية لمدة 15 دقيقة. أثناء الحضانة، قم بخلط المحتويات بلطف في بعض الأحيان. تليها الطرد المركزي وجيزة لجمع العينة إلى الجزء السفلي من الأنبوب.
- وضع الأنبوب على فاصل المغناطيسي لمدة 1 دقيقة لبيليه مجمع rRNA-التحقيق. هذه المرة لا تتخلى عن الخارق. يحتوي ال [سوبرنتنت] [ررنا-درّب] [رنا].
- ضع أنبوب 25 ميكرولتر من الخرز من الخطوة 3.3.6 على فاصل مغناطيسي لمدة دقيقة واحدة. إضافة supernatant من الخطوة 3.3.11 إلى أنبوب جديد من الخرز. مزيج من سرعة منخفضة الدوامة.
- حضانة الأنبوب عند 37 درجة مئوية لمدة 15 دقيقة. أثناء الحضانة، قم بخلط المحتويات بلطف في بعض الأحيان. بإيجاز الطرد المركزي الأنبوب لجمع العينة إلى الجزء السفلي من الأنبوب.
- وضع الأنبوب على فاصل المغناطيسي لمدة 1 دقيقة لبيليه مجمع rRNA-التحقيق. لا تتخلى عن الـ supernatant. نقل supernatant (حوالي 53 درجة مئوية) التي تحتوي على الحمض النووي الريبي المنضب rRNA إلى أنبوب جديد.
- قياس تركيز العائد RNA بواسطة مقياس الطيف الضوئي.
- استخدم نصف العينات المستنفدة لـ rRNA كإدخال على الخرز المغناطيسي الذي يحتوي على القلة (dT) 25 لاستخراج بوليا+ RNA بالطريقة التالية:
ملاحظة: تم اختيار هذا البروتوكول من عزل بوليا الذيل رسول RNA باستخدام تسلسل dT oligo ملزمة إلى سطح الخرز المغناطيسي من مجموعة متاحة تجاريا(جدول المواد).- إعادة تعليق الخرز dT oligo في القارورة عن طريق دوامة لفترة وجيزة ل > 30 ثانية ونقل 200 درجة مئوية من الخرز dT oligo إلى أنبوب. إضافة نفس وحدة التخزين (200 μL) من المخزن المؤقت الربط وإعادة الإيقاف المؤقت.
- وضع الأنبوب في المغناطيس لمدة 1 دقيقة وتجاهل supernatant. الآن، إزالة الأنبوب من المغناطيس وإعادة تعليق الخرز dT oligo غسلها في 100 درجة مئوية من العازلة ملزمة.
- ضبط حجم المدخلات rRNA المنضب عينة RNA الكلي إلى 100 درجة مئوية مع 10 mM Tris-HCl درجة الحموضة 7.5. الآن، إضافة 100 μL من المخزن المؤقت الربط.
- الحرارة إلى 65 درجة مئوية لمدة 2 دقيقة لتعطيل هياكل الحمض النووي الريبي الثانوية. الآن، ضع على الفور على الجليد.
- إضافة 200 درجة مئوية من مجموع الحمض النووي الريبي إلى 100 ميكرولتر الخرز غسلها. يُمزج المزيج جيداً ويُسمح بالتجليد عن طريق الدوران باستمرار على الدوار لمدة 5 دقائق في RT.
- وضع الأنبوب على المغناطيس لمدة 1-2 دقيقة وإزالة بعناية كل supernatant وإزالة بعناية كل supernatant.
- إزالة الأنبوب من المغناطيس وإضافة 200 درجة مئوية من الغسيل العازلة.
- قياس نقاء وتركيز بوليا المستخرجة+ RNA بواسطة مقياس الطيف الضوئي.
ملاحظة: تعتبر نسبة 260/280 1.90-2.00 ونسبة 260/230 2.00-2.20 لجميع عينات الحمض النووي الريبي مقبولة. - استخدام النصف المتبقي من العينات المستنفدة لـ rRNA من القسم 3.3 كإدخال للبروتين A الأعمدة (المقدمة في مجموعة الترسيب المناعي الحمض النووي الريبي [RIP] ، جدول المواد)للتعجيل المناعي بـ RNAs ذات الخمسة أوفير باستخدام أحادي النسيلة 7-ميثيلجوانوسين الأجسام المضادة على النحو التالي:
ملاحظة: تم اختيار هذا البروتوكول لعزل m7G متوجرسول RNA باستخدام مجموعة الترسيب المناعي RNA المتاحة تجاريا وتعديلها مرة أخرى.- غسل البروتين الخرز المغناطيسي التي تم الحصول عليها من عدة RIP وفقا لبروتوكول الشركة المصنعة لربط ما قبل الأجسام المضادة إلى الخرز.
- نقل 3 ميكروغرام من 7-methylguanosine الأجسام المضادة (أرنب IgG المقدمة في مجموعة يمكن استخدام السيطرة السلبية) إلى الخرز في أنبوب الطرد المركزي الدقيقة علقت في 100 درجة مئوية غسل العازلة من عدة.
- حضانة مع دوران سرعة منخفضة لمدة 30 دقيقة في RT. أنابيب الطرد المركزي لفترة وجيزة ومن ثم وضع الأنابيب على فاصل المغناطيسي، وإزالة وتجاهل supernatant.
- إزالة الأنابيب وإضافة 500 درجة مئوية من العازلة غسل من عدة ودوامة لفترة وجيزة. الطرد المركزي الأنابيب تليها لفترة وجيزة فصل مغناطيسي مرة أخرى، وإزالة وتجاهل supernatant.
- كرر الخطوة 3.6.4 مرة أخرى.
- إضافة حوالي 120 نانوغرام من rRNA المنضب (من القسم 3.3) إلى 7-ميثيلغوانوسين الخدوة 7-ميثيلجوانوسين الأجسام المضادة ملزمة الخرز. إضافة 1 ميكرولتر من مثبطات RNase. الحضانة في RT لمدة 1−1.5 ساعة مع التحريض خفيفة.
- تدور أسفل الخرز في 300 × ز لمدة 10 ق وإزالة supernatant التي تحتوي على غير متوج (غير 7-methylguanosine) mRNA إلى أنبوب جديد microcentrifuge.
- إضافة 100 درجة مئوية من العازلة غسل وغسلها مرتين أكثر بالمثل. تجمع supernatant التي تم جمعها في نفس أنبوب الطرد المركزي الصغير المسمى غير متوج (غير 7-ميثيلجوانوسين) mRNA. تخزين على الجليد.
- Elute المتوج (7-ميثيلغوانوسين) mRNA من الخرز مع 300 ميكرولتر من اليوريا الليسيه العازلة (ULB) التي تحتوي على 7 M اليوريا، 2٪ SDS، 0.35 M كلوريد مأكولات، 10 MM EDTA و 10 mM Tris، الرقم الهيدروجيني 7.5 عن طريق تسخين الخرز في 65 درجة مئوية لمدة 2−3 دقيقة.
- مزيج 300 ميكرولتر من العينات المعبّدة (الميرنا المتوجة وغير المتوجة) مع 300 ميكرولتر من الفينول: الكلوروفورم: كحول إيزواميل (25:24:1؛ متوفر تجارياً) (مخزن عند 4 درجة مئوية). يُخلط المزيج جيّداً بعكسه ويُترك لمدّة 10 دقائق ثمّ يُخلط مرة أخرى برفق.
- الطرد المركزي في 18,928 × ز لمدة 2 دقيقة وبعناية ماصة الطبقة العليا إلى أنبوب جديد وتجاهل الطبقة السفلية.
- إضافة 300 ميكرولتر من الفينول: الكلوروفورم: كحول isoamyl (25:24:1؛ المخزنة في 4 درجة مئوية) إلى العينات. يُمزج جيداً عن طريق الانعكاس ثم الطرد المركزي عند 18,928 × ز لمدة دقيقة واحدة.
- إضافة 300 درجة مئوية من 2-porpanol و 30 درجة مئوية من خلات الصوديوم 3 M (درجة الحموضة 5.2) إلى RNA متوج وغير متوج. عكس العينة عدة مرات ووضعها في -20 درجة مئوية لمدة 20 ساعة.
- الآن، الطرد المركزي العينات في 18،928 × ز لمدة 10 دقيقة في 4 درجة مئوية. قم بإزالة الـ supernatant بعناية وأضف 500 لتر من الإيثانول بنسبة 70%.
- الطرد المركزي مرة أخرى في 18,928 × ز لمدة 10 دقيقة في 4 درجة مئوية. تخلص بعناية من البيليه وجففه في RT لمدة أقل من 5 دقائق.
- قياس نقاء وتركيز العائد RNA بواسطة مقياس الطيف الضوئي. يجب أن تكون نسبة 260/280 في حدود 1.90-2.00، ونسبة 260/230 في نطاق 2.00-2.20 لجميع عينات الحمض النووي الريبي.
4. اختبار تأكيدي لتقييم استجابة الماوس TEنموذج بالتأكيد لوفاة الخلية FasL بوساطة
- البذور يساوي عدد (30،000 خلية) من flavopiridol تعامل B16/F10 خلايا الورم الميلانيني الماوس والخلايا الميلانوما الماوس B16/F10 الوالدين في لوحة ثقافة 96 جيدا في وسطها المقابلة (DMEM)، وحضانة بين عشية وضحاها في 37 درجة مئوية، 5٪ CO2 ترطيب حاضنه.
- علاج الخلايا في غطاء محرك السيارة الثقافة مع تركيزات مختلفة من ح له 6FasLله(0.1-1000 نانوغرام / مل) في وجود 10 ميكروغرام / مل المضادة له الجسم المضاد وحضانة لمدة 24 ساعة في 37 درجة مئوية، 5٪ CO2 حاضنة مرطبة.
- إزالة الخلايا الميتة عن طريق الغسيل مع 1X PBS العازلة. إصلاح الخلايا المرفقة في 4٪ paraformaldehyde لمدة 20 دقيقة في RT. تجاهل 4٪ paraformaldehyde (لا حاجة لغسل)، وصمة عار مع محلول الكريستال البنفسجي (20٪ الميثانول، 0.5٪ الكريستال البنفسجي في 1X PBS) لمدة 30 دقيقة.
- إزالة وصمة عار الزائدة عن طريق الرينت بلطف لوحات في مياه الصنبور. الحفاظ على لوحات لتجف في RT.
- إعادة حل البنفسج الكريستال في 100 درجة مئوية من 1X السطحي غير الأيونية المذابة في 1X PBS، وقياس كثافة الخلايا عن طريق قياس امتصاص في 570 نانومتر في قارئ لوحة ميكروت.
5. اختبار استكشافي لتقييم استجابة الماوس TEنموذج بالتأكيد لمستضد هجوم الخلية T السامة للخلايا الخلوية محددة
- عزل وتفعيل هجوم الخلايا T السامة للخلايا الخلوية OT-I CD8+ (CTL)
- تنقية خلايا CD8+ من طحال الفئران OT-I TCR TG RAG-1−/− عن طريق فصل الخلايا المغناطيسية باستخدام مجموعة عزل الخلايا CD8 T الماوس على النحو التالي:
- حصاد اثنين من الطحال من اثنين من الفئران OT-I TCR TG RAG-1−/−في وسائط RPMI كاملة.
- هرس الطحال في مرشح 70 ميكرومتر أبقى على أنبوب 50 مل مليئة 20 مل من RPMI، وذلك باستخدام الجزء الخلفي من حقنة حتى يتم ترك الدهون فقط وراءها في مرشح.
- طرد مركزي تدفق من خلال في 220 × ز لمدة 5 دقائق في 4 درجة مئوية. تجاهل الـ supernatant.
- إضافة 1 مل من خلايا الدم الحمراء (RBC) الليسيس العازلة إلى بيليه الطحال من الخطوة المركزية السابقة والماصة الخليط لمدة 1 دقيقة.
- تحييد الحل عن طريق إضافة ما يصل إلى 10 مل من RPMI.
- الطرد المركزي في 220 × ز لمدة 5 دقائق في 4 درجة مئوية. تجاهل supernatant وإعادة تعليق في 10 مل من RPMI.
- خذ aliquot صغيرة للعد. الطرد المركزي المتبقية في 220 × ز لمدة 5 دقائق في 4 درجة مئوية.
- لكل مليون خلية تم عدها، أعد تعليق بيليه في 1 مل من المخزن المؤقت لنظام الفصل المغناطيسي المتوفر تجارياً (موجو العازلة أو عازلة مماثلة).
- إعداد كوكتيل الأجسام المضادة من حجم 100 درجة مئوية لكل 1 مل من الخلايا الكريات في الخطوة 5.1.1.8. ويشمل كوكتيل الأجسام المضادة: البيوتين المضادة CD4، CD105، CD45R /B220، CD11c، CD49b، TER-119، CD19، CD11b، TCR γ/δ، وCD44.
- يُضاف هذا الكوكتيل إلى الخلايا الـ 1 مل البيليه ويُحفظ على الثلج لمدّة 15 دقيقة.
- إضافة 100 درجة مئوية من الخرز المغناطيسي (streptavidin) إلى كل 100 درجة مئوية من كوكتيل الأجسام المضادة المضافة إلى 1 مل إعادة تعليق خلايا الطحال بيليت. يُحفظ على الثلج لمدّة 15 دقيقة.
- إضافة 7 مل من المخزن المؤقت نظام الفصل المغناطيسي المتاحة تجاريا. الآن، aliquot حوالي 3-4 مل من الخليط إلى أنبوب جديد. مزيج جيدا وإصلاحه إلى المغناطيس لمدة 5 دقائق.
- Decant السائل (يحتوي على خلايا CD8 + ) إلى أنبوب جديد على الجليد. الآن، aliquot المتبقية 3-4 مل من الخليط من الخطوة 5.1.1.12 إلى الأنبوب وإصلاحه إلى المغناطيس لمدة 5 دقائق.
- البذور هندسيا التمسك الليفي APC-(MEC. B7. SigOVA) خط للتعبير عن ovalbumin محددة (OVA) مشتقة، H-2Kb مقيدة الببتيد EPItope OVA257-264 (SIINFEKL)، جنبا إلى جنب مع جزيء التحفيز المشترك B7.1، في 75،000 خلية في بئر في لوحات 24 جيدا، في 37 درجة مئوية، 5٪ CO2 حاضنة رطبة.
ملاحظة: الليفية الملتصقة المستخدمة هي هدية من مختبر الدكتور إديث يانسن في CCHMC. تم إنشاء الخط في الأصل في مختبر الدكتور ستيفن ب. شونبيرغر في معهد لا جولا للحساسية والمناعة6. - بعد 24 ساعة، اغسل الطبقة الأحادية من APC مرة واحدة مع وسيط Dulbecco المعدل (IMDM) من Iscove المتوفر تجارياً مع عازل HEPES، وبياليومات الصوديوم، والجلوتامين والجلوكوز العالي)، وإضافة 0.5 × 106 خلايا ساذجة OT-I CD8+ (من الخطوة 5.1.1.13) في 2 مل من IMDM تستكمل مع 50 مليون بيتا-ME، 2 مل EDTA، 4 مل L-الجلوتامين وHEPES و 10٪ FBS.
- بعد 20 ساعة، حصاد بلطف الخلايا OT-I غير الملتصقة (عن طريق جمع وسائل الإعلام في طبق الثقافة مع الخلايا العائمة OT-I وبيليه الخلايا في 191 × ز لمدة 2 دقيقة؛ عد الخلايا OT-I القابلة للحياة) ونقلها للثقافة المشتركة.
- تنقية خلايا CD8+ من طحال الفئران OT-I TCR TG RAG-1−/− عن طريق فصل الخلايا المغناطيسية باستخدام مجموعة عزل الخلايا CD8 T الماوس على النحو التالي:
- الثقافة المشتركة لخلايا CD8+ مع خلايا B16/F10-OVA
- خلايا CD8+ المشتقة من البذور OT-I بنسبة 1:1 (300,000 خلية لكل منها) في ثقافة مشتركة مع B16/F10 (تفتقر إلى مستضد أوفالبومين)، B16/F10-OVA غير المعالجة، وخلايا B16/F10-OVA المعالجة مسبقًا مع flavopiridol (25 nM) لمدة أسبوع واحد، في أطباق 6 آبار مع DMEM كاملة وسائل الإعلام لمدة 20 ساعة في 37 درجة مئوية في حاضنة CO2 5٪ ترطيب.
- بعد 20 ساعة، قم بإزالة خلايا CD8+ المشتقة من OT-I (عن طريق جمع الوسائط في طبق الثقافة مع خلايا CD8+ المشتقة من OT-I العائمة). اغسل خلايا B16/F10-OVA الملتصقة في 1x PBS.
- جرب المجموعات الثلاث من الخلايا المرفقة B16/F10-OVA في 0.05٪ EDTA التي تحتوي على التربسين لمدة 5 دقائق.
- وصمة عار الخلايا B16/F10-OVA حصادها عن طريق احتضانلهم في PBS الباردة (تحتوي على 0.5٪ FBS و 0.05٪ أزيد الصوديوم) مع صبغ البقاء والأجسام المضادة ذات الصلة المسمى (قابلة للتثبيت سلامة تلطيخ صبغ e780، AF647-المترافقة الماوس CD8 وBV421-مترافق ة الماوس CD45 ).
- تحليل صلاحية المجموعات الثلاث من خلايا B16/F10-OVA عن طريق قياس التدفق.
النتائج
هنا، ونحن نقدم خطة مفصلة (الشكل 1)لإنشاء نموذج خلية TEبالتأكيد التي تم الحصول عليها من قبل المزمنة شبه القاتلة (الشكل 2)العلاج مع flavopiridol في 25 nM. في الشكل 3، في 3 أيام من العلاج مع flavopiridol ، B16 خلايا OVA تظهر خصائص جزئية من TEبالتأكيد ولكن بعد أسبوع واحد من العلاج ، وخلايا B16 /F10 OVA تظهر فقدان عميق للفسفورية في موقف سيرين 2 على CTD من RNA Pol II على طول مع انخفاض كبير في H3K36me3 - تعديل الهيستون المتورطة في تحديد حدود الأيونات المجردة ومثبط للنسخ خفي هارب. ونتيجة لذلك، TEبالتأكيد نموذج الخلية يظهر عيوب معالجة mRNA الحرجة مع زيادة واضحة في نسب mRNAs متوجة بشكل غير صحيح وغير متعددة adenylated(الشكل 4A،B). أيضا، وينظر القمع المحدد للجينات مسار الاستجابة الالتهابية الرئيسية ومسار موت الخلايا بوساطة FasL في الشكل 5 والشكل 6. المقاومة المفروضة على الإنترفيرون (IFN-α، IFNγ) وTNF-α حفز الفسفورية من STAT1 و NFיB، ومقاومة موت الخلية من قبل مستقبلات الموت ligand FasL يقلل بشكل كبير من السمية الخلوية لهجوم الخلايا المناعية ضد TEبالتأكيد الاورام. تم تصميم هذه التقنيات التأكيدلاختبار مدى تأثير الاضطراب المزمن استطالة النسخ على مجموعة واسعة من الجينات استجابة للتحفيز، وما إذا كان مثل هذا الاضطراب في نموذج خط خلية الماوس معين يكفي بما فيه الكفاية ل دفع ندرة حادة من mRNA وظيفية في الاستجابة الالتهابية تشير الجينات، وتقليد الضروريات الأساسية من TEالسرطان بالتأكيد سريريا. استنادا ً إلى دراستنا لعلاج فلافوبيريدول، فإن قمع الفسفورية في بقايا سيرين الثانية (pSER2) من الحمض النووي الريبي Pol II CTD أمر بالغ الأهمية، كما أنه علامات استطالة النسخ. يجب أن تحقق الجرعة دون المميتة لأي خط خلية سرطان الماوس معين انخفاض في مستويات pSER2 بالإضافة إلى وجود تأثير ضئيل على معدل نمو وصلاحية خط الخلية. على الرغم من أننا نرى باستمرار انخفاضا في مستويات pSER2 و H3K36me3 على 25 علاجات flavopiridol nM، فإنه لا يضمن قمع كل من مستويات pSTAT1 و pNFיB (على IFN-α، IFNγ وTNF-α التحفيز، على التوالي). كل خط خلية سرطان الماوس فريدة من نوعها (B16 /F10 OVA أو CT26 الخلايا المستزرعة في مختبرات مختلفة على مدى فترة من الزمن قد يكون لها آثار تغيرت قليلا) وأنها قد يكون إما JAK1 أو CCNT1 إنقاذ جزئيا آثار flavopiridol في قمع جينات مسار الاستجابة الالتهابية. في مثل هذه الحالات، قد تحتاج حركية مستويات pSTAT1 وpNFיB إلى فحص في نقاط زمنية مختلفة (5-70 دقيقة) لفهم وقت آثار فلافوبيريدول الوسيطة وإنقاذها إما عن طريق JAK1 أو CCNT1. وبناء على ذلك، قد تحتاج JAK1 و/أو CCNT1 إلى أن تُسقط لإنشاء هذا النموذج.
مرة واحدة يتم تأسيس نموذج flavopiridol وتتميز باستخدام الاختبارات المذكورة أعلاه, ونحن نقدم اختبار استكشافي لاختبار ما إذا كان نموذج الخلية TEبالتأكيد يضفي مقاومة لهجوم الخلايا السامة للخلايا الخلوية (CTL). استناداً إلى بروتوكولنا الأمثل، عالجت flavopiridol خلايا B16/F10 بشكل ملحوظ الإفراط في التعبير عن جين OVA (B16 OVA) التي تم احتضانها مع CTLs CD8+ المنشط (محددة لEPItope OVA257-264) لها سمية انتقائية للخلايا التي تعبر عن OVA (هدية من الدكتور. ستيفن ب. شونبيرغر مختبر6) لم تكن عرضة لOT-I CTL بوساطة الانموس الورم. شهدت خلايا B16/F10 OVA (لم تعالج مسبقا مع flavopiridol) موت الخلايا واسعة النطاق في هذا النظام، في حين نجا B16/F10 الخلايا الأبوية، لأنها لا تعبر عن مستضد OVA(الشكل 7). ومن الواضح من نتائج الفحص الاستكشافي المقترح أن TE المزمنة التي يسببها flavopiridol يمكنبالتأكيد منح وسيلة للهروب من هجوم المناعة المضادة للورم حتى في الجسم الحي. هذا يمكن أن يكون مزيد من الاختبار في نماذج الورم في الجسم الحي للتحقق من ميل نماذج TEبالتأكيد للهروب من الاستجابات المناعية الفطرية والتكيفية المضادة للورم. يمكن استخدام العلاجات المضادة للاسيالو لتنظيم نشاط خلايا ناغورني كاراباخ في الجسم الحي في الفئران الحاملة للورم. أيضا، يمكن أن تدار العلاج نقاط التفتيش المناعية (المضادة لCTLA4 ومكافحة PD1) إلى TEبالتأكيد الفئران تحمل الورم.
في المجموع، فإن اختبارات TE المؤكدةبالتأكيد جنبا إلى جنب مع الفحص الاستكشافي المقترح معا تبين فائدة دمج هذا النموذج الخلية TEبالتأكيد في مجموعة كاملة من غيرها من حالات اختبار المناعة الورم. هذا النموذج يمكن أن تساعد في تحليل التفاصيل الجزيئية الناتجة عن استطالة النسخ المعيبة في الخلايا السرطانية واستجابتها لتفاعلات الخلايا المناعية.

الشكل 1: التمثيل التخطيطي لتدفق العمل. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.

الشكل 2: خصائص نمو الخلايا من خلايا B16 OVA المعالجة بشكل مزمن مع جرعة منخفضة flavopiridol: جدوى (تقاس بكاشف الصلاحية) من السيطرة والخلايا المعالجة فلافوبيريدول B16 OVA في الأيام المشار إليها بعد العلاج. وقد تم تعديل هذا الرقم من Modur وآخرون3. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.

الشكل 3: الفحص المؤكد لتقييم الحمض النووي الريبي بول الثاني وملف الهيستون: المناعية من علامات الهيستون والحمض النووي الريبي Pol II في خلايا أوفا B16 تعامل مع flavopiridol لمدة 72 ساعة أو 1 أسبوع. وقد تم تعديل هذا الرقم من Modur وآخرون3. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
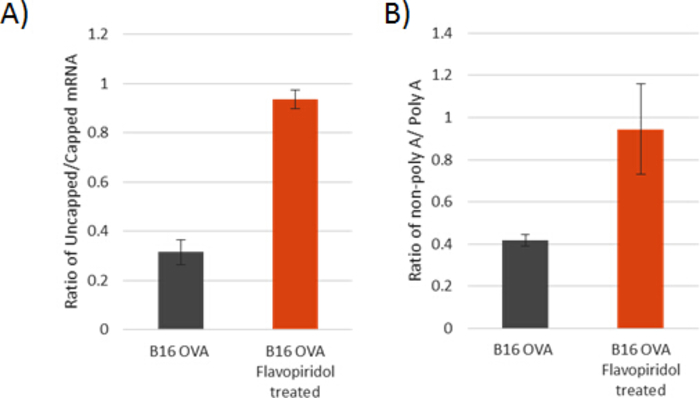
الشكل 4: التبيّن التأكيدي لتقييم العيوب الشديدة في معالجة الحمض النووي الريبي. نسب 5′-uncapped إلى 5′-capped (A) و 3′-غير polyadenylated إلى 3′-polyadenylated(B)تركيزات mRNA بعد استنفاد rRNA في خطوط الخلية المشار إليها. تمثل أشرطة الخطأ الانحراف المعياري استناداً إلى ثلاثة عمليات نسخ متماثلة تقنية. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.

الشكل 5: التبيّن التأكيدي لتقييم ملف تحفيز السيتوكين. المناعة من STAT1، pSTAT1، NFיB و p NFיB في السيطرة وflavopiridol قبل المعالجة B16 خلايا OVA حفز مع IFN-α، IFNγ أو TNF-α لمدة 30 دقيقة في (5 نانوغرام / مل). وقد تم تعديل هذا الرقم من Modur وآخرون3. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
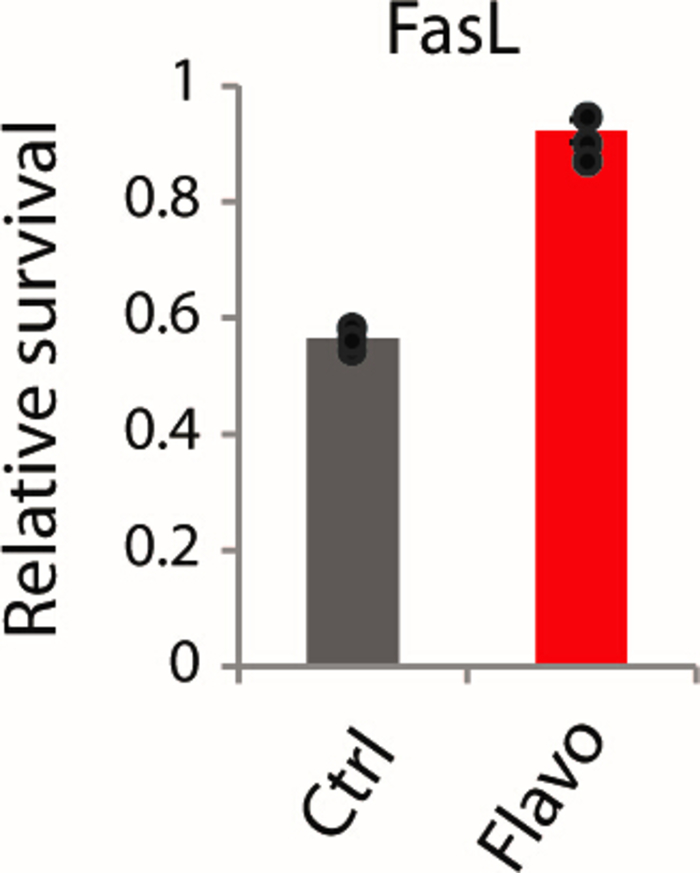
الشكل 6: الاختبار المؤكد لتقييم مقاومة موت الخلايا بوساطة FasL في المختبر. التحكم وflavopiridol المعالجة مسبقا B16 خلايا OVA تعامل مع FasL لمدة 24 ح قراءة تقاس باختبار الصلاحية. وقد تم تعديل هذا الرقم من Modur وآخرون3. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
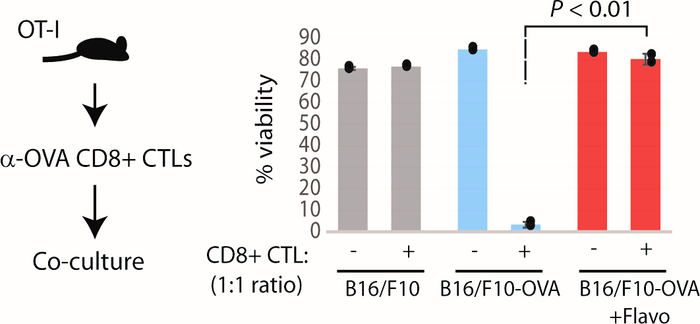
الشكل 7: اختبار استكشافي لتقييم مقاومة TEنموذج بالتأكيد لمستضد مقيد ة سامة للخلايا T بوساطة هجوم في المختبر. اليسار: مخطط الرسم التخطيطي للاستطلاع الاستكشافي. الحق: الجدوى النسبية لخلايا B16/F10-OVA التي تم ثقافتها بـ CD8 + CTLs (نسبة 1:1) المعزولة عن طحال فئران OT-I. P: ويلش اثنين من عينة ر-اختبار. وقد تم تعديل هذا الرقم من Modur وآخرون3. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
Discussion
وقد ظهرت السيطرة على استطالة RNA Pol II كرافعة حاسمة لتنظيم التعبير الجيني استجابة التحفيز لصالح الخلايا الخبيثة5،7،8. التغلب على التوقف المروج القريب استطالة وإنتاج mRNA اللاحقة يتطلب نشاط كيناز من P-TEFb9،10،11. يستخدم نموذجنا flavopiridol (25 nM)، وهو مثبط للكيناز CDK9 الأساسية المعتمدة على السيكلين، لمحاكاة العيوب التي لوحظت خلال استطالة Pol II في TEبالتأكيد السرطانات - وهو النمط الظاهري غير معروف سابقا في السرطانات التي اكتشفتها مجموعتنا في السابق3.
ومن المعروف منذ فترة طويلة أن نشاط كيناز CDK9 ضروري للفسفور من بقايا سيرين 2 في CTD من الوحدة الفرعية الكبيرة للشرطة الثانية. بشكل حاسم، لقد نجحنا في تحسين فلافوبيريدول علاج تثبيط المزمن من CDK9 (25 nM لمدة 1 أسبوع) في B16/F10 OVA بحيث، بالإضافة إلى تثبيط الفسفور CTD، 25 nM علاج فلافوبيريدول لمدة 1 أسبوع يمنع السليم بعد النسخ تعديلات mRNA بطريقة غير متوقعة ويلغي بشكل فعال p-TEFb تعتمد على استطالة الإنتاجية على طول الجينات الطويلة مثل الاستجابة المؤيدة للالتهابات تشير الجينات، وتغيير كبير في أنماط التعبير على حد سواء في mRNA و مستويات البروتين. وعلى حد علمنا، لا يوجد نموذج آخر موصوف في الأدب يحقق الشيء نفسه على نحو فعال.
هذا من السهل إنشاء، نموذج قابل للتعميم من TEبالتأكيد يمكن الاستفادة من تشريح، على حد سواء التعديلات النسخي والجيني تمكين TEبالتأكيد السرطانات للتكيف مع هجوم الخلايا بوساطة المناعة. وعلاوة على ذلك، يحتفظ هذا النموذج murine TEبالتأكيد-- مثل الحد من مجموع وفوسفو - RNA Pol II مستويات 21 يوما بعد الإفراج عن flavopiridol في في اختبار النمو في الجسم الحي3 (لم يذكر في البروتوكول هنا)، مما يشير إلى مدى الاستقرار من هذا نموذج غير وراثي لمزيد من التجارب في الجسم الحي. ومع ذلك، يجب توخي الحذر لتحسين الجرعة دون المميتة بالضبط من flavopiridol لخطوط المورين الأخرى (على سبيل المثال، حوالي 20 nM flavopiridol العلاج لمدة أسبوع واحد هو الجرعة دون المميتة لخط سرطان المورين MC38؛ لا تستخدم في هذا البروتوكول)، وتأثير الاختلاف في الخلية قد تختلف كثافة الطلاء، وظروف الثقافة، وظروف تحفيز السيتوكين لخطوط المورين المختلفة. البروتوكول الموصوف هنا يعطي إطارا أساسيا لتقليل المتغيرات المعروفة بأنها حاسمة لتوليد TEبالتأكيد- مثل الميزات الناجمة عن تثبيط CDK9 المزمنة. وبالإضافة إلى ذلك، تم اختبار خطوط الخلايا السرطانية البشرية، مثل T47D وCAL51 مع علاجات فلافوبيريدول قصيرة الأجل (3 أيام) مما يؤدي إلى TE مماثلةبالتأكيد- مثل الحمض النووي الريبي Pol II ملامح، مما يدل على فائدة تثبيط المزمن القائم على flavopiridol من CDK9 بوساطة استطالة النسخ في خلق خطوط الإنسان حتى نموذج لدراسة TEبالتأكيد.
Disclosures
وليس لدى أصحاب البلاغ ما يكشفون عنه.
Acknowledgements
وقد تم دعم هذا العمل جزئيا من قبل NCI (CA193549) وCCHMC البحوث الابتكار التجريبية جوائز لKakajan Komurov، ووزارة الدفاع (BC150484) جائزة نافيت سينغ. المحتوى هو فقط من مسؤولية المؤلفين ولا يمثل بالضرورة وجهات النظر الرسمية للمعهد الوطني للسرطان أو وزارة الدفاع. ولم يكن للممولين أي دور في تصميم الدراسة، أو جمع البيانات وتحليلها، أو اتخاذ قرار بنشر المخطوطة أو إعدادها.
Materials
| Name | Company | Catalog Number | Comments |
| hhis6FasL | Cell Signaling | 5452 | |
| 10X TBS | Bio-Rad | 170-6435 | |
| 12 well plates | Falcon | 353043 | |
| 20% methanol | Fisher Chemical | A412-4 | |
| 24-well plates | Falcon | 351147 | |
| 4–18% SDS polyacrylamide gel | Bio-Rad | 4561086 | |
| 4% Paraformaldehyde | Thermo Fisher Scientific | AAJ19943K2 | |
| 5% dry milk | Bio-Rad | 170-6404 | |
| 7-Methylguanosine antibody | BioVision | 6655-30T | |
| 96-well plates | Cellstar | 655180 | |
| AF647-conjugated mouse CD8 | Biolegend | 100727 | |
| antibiotic and antimycotic | Gibco | 15240-062 | |
| anti-His antibody | Cell Signaling | 2366 P | |
| Anti-Rabit | Cell Signaling | 7074 | Dilution 1:5000 |
| Anti-Rat | Cell Signaling | 7077S | Dilution 1:5000 |
| Bradford assay Kit | Bio-Rad | 5000121 | |
| BSA | ACROS Organics | 24040-0100 | |
| BV421-conjugated mouse CD45 | Biolegend | 109831 | |
| crystal violet | Sigma | C3886-100G | |
| DMEM | Gibco | 11965-092 | |
| Dynabeads Oligo (dT)25 | Ambion | 61002 | |
| FBS | Gibco | 45015 | |
| Fixable Live/Dead staining dye e780 | eBioscience | 65-0865-14 | |
| Flavopiridol | Selleckchem | S1230 | |
| H3k36me3 | Abcam | ab9050 | Dilution 1:2000 |
| IFN-α | R&D systems | 12100-1 | |
| IFN-γ | R&D systems | 485-MI-100 | |
| IMDM | Gibco | 12440053 | |
| Immobilon Western Chemiluminescent HRP Substrate | Millipore | WBKLS0500 | |
| MojoSort Mouse CD8 T Cell Isolation Kit | Biolegend | 480007 | |
| NF-κB | Cell Signaling | 8242s | Dilution 1:1000 |
| PBS | Gibco | 14190-144 | |
| p-NF-κB | Cell Signaling | 3033s | Dilution 1:1000 |
| p-Ser2-RNAPII | Active Motif | 61083 | Dilution 1:500 |
| p-Ser5-RNAPII | Active Motif | 61085 | Dilution 1:1000 |
| p-STAT1 | Cell Signaling | 7649s | Dilution 1:1000 |
| RiboMinu Eukaryote Kit | Ambion | A10837-08 | |
| RIPA buffer | Santa Cruz Biotechnology | sc-24948 | |
| RNAPII | Active Motif | 61667 | Dilution 1:1000 |
| STAT1 | Cell Signaling | 9175s | Dilution 1:1000 |
| TNF-α | R&D systems | 410-MT-010 | |
| total H3 | Cell Signaling | 4499 | Dilution 1:2000 |
| Tri reagent | Sigma | T9424 | |
| Triton | Sigma | T8787-50ML | |
| Tween 20 | AA Hoefer | 9005-64-5 | |
| β-Actin | Cell Signaling | 12620S | Dilution 1:5000 |
| β-ME | G Biosciences | BC98 |
References
- Adelman, K., Lis, J. T. Promoter-proximal pausing of RNA polymerase II: emerging roles in metazoans. Nature Reviews Genetics. 13 (10), (2012).
- Margaritis, T., Holstege, F. C. Poised RNA polymerase II gives pause for thought. Cell. 133 (4), 581-584 (2008).
- Modur, V., et al. Defective transcription elongation in a subset of cancers confers immunotherapy resistance. Nature Communications. 9 (1), 4410 (2018).
- Hargreaves, D. C., Horng, T., Medzhitov, R. Control of inducible gene expression by signal-dependent transcriptional elongation. Cell. 138 (1), 129-145 (2009).
- Adelman, K., et al. Immediate mediators of the inflammatory response are poised for gene activation through RNA polymerase II stalling. Proceedings of the National Academy of Sciences of the United States of America. 106 (43), 18207-18212 (2009).
- van Stipdonk, M. J., Lemmens, E. E., Schoenberger, S. P. Naïve CTLs Require a Single Brief Period of Antigenic Stimulation for Clonal Expansion and Differentiation. Nature Immunology. 2 (5), 423-429 (2001).
- Gilchrist, D. A., et al. Regulating the regulators: the pervasive effects of Pol II pausing on stimulus-responsive gene networks. Genes & Development. 26 (9), 933-944 (2012).
- Danko, C. G., et al. Signaling pathways differentially affect RNA polymerase II initiation, pausing, and elongation rate in cells. Molecular Cell. 50 (2), 212-222 (2013).
- Nechaev, S., Adelman, K. Pol II waiting in the starting gates: Regulating the transition from transcription initiation into productive elongation. Biochimica et Biophysica Acta (BBA)-Gene Regulatory Mechanisms. 1809 (1), 34-45 (2011).
- Zhou, M., et al. Tat modifies the activity of CDK9 to phosphorylate serine 5 of the RNA polymerase II carboxyl-terminal domain during human immunodeficiency virus type 1 transcription. Molecular and Cellular Biology. 20 (14), 5077-5086 (2000).
- Palancade, B., Bensaude, O. Investigating RNA polymerase II carboxyl‐terminal domain (CTD) phosphorylation. European Journal of Biochemistry. 270 (19), 3859-3870 (2003).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved