Method Article
Синтез и Bioconjugation тиоловых реактивной реагентов для создания сайта выборочно изменять Immunoconjugates
В этой статье
Резюме
В этом протоколе мы будем описывать синтез СТРУЧКИ, phenyoxadiazolyl метил на основе сульфона реагент для сайта селективные крепление грузов тиолы биомолекул, особенно антител. Кроме того мы будем описывать синтеза и характеристика бифункциональных хелатором СТРУЧКИ подшипника и его спряжение модель антитела к.
Аннотация
Maleimide подшипник бифункциональных зонды были использованы на протяжении десятилетий для сайта селективные модификации тиолы в биомолекулы, особенно антител. Еще на основе maleimide конъюгатов отображения ограниченное стабильности в естественных условиях, потому что succinimidyl тиоэфиры связь может пройти ретро Майкл реакции. Это, конечно, может привести к выпуска радиоактивных полезных данных или обмена с биомолекулами тиоловых подшипник в обращении. Оба этих процессов может производить повышенной активности концентрации в здоровых органов, а также снижение активности концентрации в тканях-мишенях, обусловило уменьшение контрастность изображений и ниже терапевтические показатели. В 2018 году, мы сообщили создание модульный, стабильный и легко доступны phenyloxadiazolyl метил сульфона реагент — называли «СТРУЧКИ» — как платформы на базе тиоловых bioconjugations. Мы наглядно продемонстрировали, что на основе СТРУЧКИ сайт селективного bioconjugations можно воспроизвести и энергично создать однородную, четко определенных, весьма иммунореактивных и высокостабильных radioimmunoconjugates. Кроме того доклинические эксперименты в мышиных моделях колоректального рака показали, что эти сайт выборочно помечены radioimmunoconjugates выставка намного превосходят в естественных условиях производительности по сравнению с radiolabeled антитела синтезируются через на основе maleimide спряжения. В этом протоколе мы будем описывать четырехступенчатая синтез СТРУЧКИ, создание бифункциональных СТРУЧКИ подшипник вариант вездесущие хелатором DOTA (СТРУЧКИ-DOTA) и спряжение СТРУЧКИ-DOTA к трастузумаб HER2-таргетинг антитела.
Введение
Радиофармацевтические химики давно эксплуатируемых избирательности и специфичность антител для биомаркеров болезни для обеих ядерных изображений и целевых радиотерапии1. Далеко и прочь наиболее общий подход к radiolabeling антител основывается на неизбирательное придание radiolabeled протезно групп или radiometal энтеросорбенты аминокислоты — наиболее часто lysines — в рамках структуры иммуноглобулина ( Рисунок 1A)2. Хотя эта стратегия является безусловно эффективным, его случайные, сайт неспецифический характер может создать проблемы. В частности традиционные bioconjugation подходы производят плохо определены и гетерогенных immunoconjugates состоит из смеси тысяч различных regioisomers, каждый со своим собственным набором биологических и фармакологические свойства3. Кроме того случайных bioconjugation могут препятствовать иммунореактивности антител, если груз добавляется иммуноглобулина антиген связывая доменов.
С годами разнообразные bioconjugation участкам и сайт селективные стратегии были разработаны с целью решения этих проблем4,5. Наиболее распространенные из этих подходов основывается на лигирование maleimide подшипник зондов сульфгидрильных групп, по которым (рис. 1B). IgG1 антитела естественно содержат 4 Интер цепи дисульфидных мостов, связей, которые могут быть выборочно сведены к дают бесплатные тиолы способных претерпевает Майкл реакции с малеинимидов в форме succinimidyl тиоэфиры облигаций. Использование тиолами и малеинимидов, безусловно, улучшение по сравнению с традиционными методами и широкий спектр maleimide подшипник синтонов и бифункциональных хелаторов в настоящее время доступны. Однако важно отметить, что эта методология имеет также серьезные ограничения. На основе Maleimide immunoconjugates выставку ограниченное стабильности в естественных условиях, потому что тиоэфиры связь может пройти ретро Майкл реакции (рис. 2)6,,78,9, 10. это, конечно, может привести к выпуска радиоактивных полезных данных или обмен с биомолекулами тиоловых подшипник в обращении (например, глутатион или альбумина в сыворотке крови). Оба из этих процессов можно увеличения концентрации деятельности в здоровых органов, а также уменьшение концентрации деятельности в тканях-мишенях, обусловило уменьшение контрастность изображений и ниже терапевтические показатели. Были разработаны несколько альтернативных тиоловых реактивной реагентов в попытке обойти эти проблемы, включая tosylates, bromo - и Иодо acetyls и винил сульфонов11,12,13, 14 , 15 , 16 , 17. Однако все эти подходы имеют ограничения, которые препятствуют их широкое применение.
Около пяти лет назад, в лаборатории в конце Карлос Barbas III научно-исследовательском институте Скриппса пионером в использовании phenyloxadiazolyl метил сульфонов как реагенты для селективного формирования высокостабильных связей с тиолами (Рисунок 1 c и рис. 3) 18 , 19. авторы заняты phenyloxadiazolyl метил сульфон подшипник вариант флуоресцеин изменить несколько антител, спроектирован, чтобы содержать остатки свободной цистеина, в конечном счете производства immunoconjugates с более высокой стабильности, чем аналогичные конструкции, созданные с помощью датчиков на основе maleimide. Увидев этой перспективной работы, мы были несколько удивлены тем, что эта технология использовалась только вряд в радиохимии и еще не было вообще используется в синтезе бифункциональных хелаторов или radioimmunoconjugates20,21 . Эта нехватка приложений, однако, вскоре начал делать больше смысла: несколько попыток закупки реагент от Sigma-Aldrich привело к получения сложных смесей продуктов разложения с < 15% нужного соединения. Кроме того, обобщение сообщенных реагент себя был не является реалистичным вариантом либо, как опубликованные синтетических маршрут несколько громоздкой и требует сложных органической химии оборудование, большинство радиохимии и Молекулярное воображение лаборатории — включая ours — просто не обладают.
В ответ на эти препятствия мы намереваемся создать легко доступны и очень стабильной phenyloxadiazolyl метил сульфона реагент, который может быть получен через надежную и разумно снисходительный синтетических маршрут. Ранее в этом году, мы сообщили создание модульный, стабильный и легко доступны phenyloxadiazolyl метил сульфона реагент — называли «СТРУЧКИ» — как платформы на основе тиоловых bioconjugations (Рисунок 1 c и рис. 3)22. Ключевое различие между СТРУЧКИ и реагент сообщил Barbas, et al. является, что бывший использует анилин кольцо, прикрепленное к phenyloxadiazolyl метил сульфона остаток, в то время как последняя имеет фенола в таком же положении (рис. 4). Это изменение облегчает более простой и доступной синтетических маршрутов, а также — если наш опыт с коммерчески доступные соединения является символом — более стабильной окончательный реагент. В этой работе, мы также синтезируется пару СТРУЧКИ подшипник бифункциональных хелаторов — СТРУЧКИ-ДФО и СТРУЧКИ-CHX-A''-DTPA — содействовать созданию 89Zr - и 177Лу меченых radioimmunoconjugates, соответственно. Как мы будем обсуждать, мы продемонстрировали, что на основе СТРУЧКИ сайт селективного bioconjugations можно воспроизвести и энергично создать однородную, четко определенных, весьма иммунореактивных и высокостабильных radioimmunoconjugates. Кроме того доклинические эксперименты в мышиных моделях колоректального рака показали, что эти сайт выборочно помечены radioimmunoconjugates выставку Улучшенный в естественных условиях производительности по сравнению с radiolabeled антитела синтезируются через на основе maleimide спряжения.
Сквозные цель этой работы заключается в содействии созданию четко, однородной, очень стабильный и высоко иммунореактивных immunoconjugates для приложений в vitro и in vivo. Синтетический подход является достаточно простым, чтобы выполняться в почти любой лаборатории, и родитель СТРУЧКИ реагента могут быть изменены с множеством различных энтеросорбенты, флуорофоров или грузов. В этот протокол и сопровождающих видео мы будем описывать простые, четырехступенчатая синтез СТРУЧКИ (рис. 5); Создание СТРУЧКИ подшипник вариант DOTA, широко используемый хелатором для координации 64Cu, 68Ga, 111, 177Лу и 225переменного тока (рис. 6); и bioconjugation СТРУЧКИ-DOTA в модели антитела, трастузумаб HER2-таргетинг IgG1 (рис. 7).
протокол
1. синтез 4-[5-(methylthio)-1,3,4-oxadiazol-2-yl]-aniline (1)
Примечание: Из-за света чувствительность комплекса, держите все реакции в фольги, покрытой судов.
- В 10 мл вокруг нижней колбе, растворить 100 мг (0,517 ммоль, эквивалентный 1) 5-(4-aminophenyl)-1,3,4-oxadiazole-2-thiol в 3 мл метанола.
- В этот раствор добавить 360 мкл diisopropylethylamine (DIPEA; 2.07 ммоль; 4 эквиваленты; безводный) и малых магнитных перемешать бар. Обложка колбу с резиновой пробкой и перемешать раствор на 10 минут при комнатной температуре.
- С помощью шприца стекла 1 мл, засуните отверстие через резиновую пробку и быстро добавить 32 мкл (0,517 ммоль, эквивалентный 1) йодометан в этой смеси. Позвольте смеси реагировать на 45 минут при комнатной температуре.
Примечание: Из-за потенциального вредного воздействия йодометан, эта реакция должно быть сделано в химической зонта. - Установите водяной бане роторный испаритель до 40 ° C и медленно снижают давление для удаления растворителя позволить белое вещество.
- Растворяют твердые в 3 мл этилацетата и мыть по крайней мере три раза с 5 мл раствора карбоната натрия 0,1 М, используя воронку separatory.
Примечание: Периодически принимать спот тесты водной фазы под УФ-лампы; как только ничего не видно под лампу, вы можете остановить стирок. - Собирать органические фазы в воронку separatory и промойте его водой до тех пор, пока рН водной фазы достигает 6,8-7,0 (с помощью РН бумаги).
- Собирать органические фазы и добавлять сульфат магния для удаления любых следов воды.
Примечание: Сульфат магния следует добавить небольшой шпателем, после чего следует закрученных решение. Если до сих пор видны мелкие частицы сушильного агента, решение сухой. Если нет, добавить небольшое количество сульфата магния, до тех пор, пока можно увидеть тонкодисперсных частиц. - Фильтр смесь с использованием средних стекло фритта или фильтровальной бумаги.
- Испарится летучих веществ, используя роторный испаритель, процесс, который должен произвести необходимый продукт как белые иглы.
2. синтез tert-butyl[18-({4-[5-(methylthio)-1,3,4-oxadiazol-2-yl]phenyl}amino)-15,18-dioxo-4,7,10-trioxa-14-azaoctadecyl] карбамат (2)
Примечание: Из-за света чувствительность комплекса, держите все реакции в фольги, покрытой судов.
- В 25 мл вокруг нижней колбе, распустить 387 мг (0,92 ммоль, 1.0 эквивалент) NBoc-N′-succinyl-4,7,10-trioxa-1,13-tridecanediamine 10 мл дихлорметаном.
- В этот раствор добавить 480 мкл (2.76 ммоль, 3 эквиваленты) DIPEA, 264 мг (1,38 ммоль; 1,5 эквиваленты) N-этил - N′-[3-(диметиламино) пропил] Карбодиимиды гидрохлорид (EDCI) и 200 мг (0.97 ммоль, 1.1 эквиваленты) 1. Уплотнение сосуда с стеклянной пробкой и пусть реакции перемешать в течение 5 дней при комнатной температуре.
Примечание: Помните Испарения дихлорметаном. Если необходимо, добавьте больше на протяжении недели. - Вымойте смесь в воронку separatory раствором 1 М соляной кислоты (3 x 5 мл).
- Собирать органические фазы и продолжать мыть его в воронку separatory, сначала с раствором 1 М Na2CO3 (2 x 5 мл), а затем с водой (3 x 5 мл).
- Собирать органические фазы и добавлять сульфат магния для удаления любых следов воды (см. шаг 1.7). Фильтр смесь с использованием средних стекло фритта или фильтровальной бумаги.
- Использование роторный испаритель, удалите летучих растворителей при сниженном давлении для позволить беловатого твердых.
- Повторно распустить этот твердый в 10 мл этилацетата и осадка продукта через постепенное (например, 2 мл, в то время) Добавление 30 мл циклогексан.
- Фильтр решение с фильтровальной бумаги или среднего стекла фритта для получения продукта как белый порошок.
3. синтез tert-butyl[18-({4-[5-(methylsulfonyl)-1,3,4-oxadiazol-2-yl]phenyl}amino)-15,18-dioxo-4,7,10-trioxa-14-azaoctadecyl] карбамат (3)
Примечание: Из-за света чувствительность комплекса, держите все реакции в фольги, покрытой судов.
- В 10 мл раунд нижней колбе растворяют 30 мг (0,05 ммоль; 1 эквивалент) 2 в 4 мл дихлорметаном.
- Медленно, добавить в эту смесь в 49 мг (0,2 ммоль; 4 эквиваленты) 70% m хлорпербензойной кислоты и охватывают реакционный сосуд с стеклянной пробкой. Перемешайте раствор на ночь при комнатной температуре, в конечном итоге приносит желтая смесь.
- Вымойте желтая смесь в воронку separatory, сначала с 0,1 М раствором NaOH (3 x 5 мл), а затем с водой (3 x 5 мл).
- Сухие органические фазы с магния сульфатом и фильтровать смесь с использованием средних стекло фритта или фильтровальная бумага.
- Использование роторный испаритель, удалите растворителей при сниженном давлении для получения продукта как бледные тела.
4. синтез N1-(3-{2-[2-(3-aminopropoxy)ethoxy]-ethoxy}propyl)-N4- сукцинимидные {4-[5-(methylsulfonyl)-1,3,4-oxadiazol-2-yl] фенил} (бобы)
- В 25 мл вокруг нижней колбе, растворяют 30 мг 3 2.0 мл дихлорметаном.
- Добавить 400 мкл trifluoroacetic кислоты и печатью колбу с стеклянной пробкой.
- Перемешайте смесь реакции при комнатной температуре на 3 часа.
- Использование роторный испаритель, удалите летучих веществ при пониженном давлении при комнатной температуре, оставляя жирных следов.
- Распустить маслянистый остаток 7 мл воды и, используя воронку separatory, мыть с этилацетат (3 x 4 мл). Держите водный слой.
- Lyophilize водный слой, чтобы позволить СТРУЧКИ как белый порошок.
Примечание: Коэффициенты молярной абсорбции для СТРУЧКИ на 280 и 298 Нм составляет 9900 и 12400 см-1M-правовая-1, соответственно.
5. синтез СТРУЧКИ-DOTA
- В пробки microcentrifuge 1,5 мл растворяют 10 мг СТРУЧКИ в 300 мкл диметилсульфоксида (0,018 ммоль; 1 эквивалент) и добавить 26 мкл n, N-diisopropylethylamine (0,15 ммоль; 8 эквиваленты).
- Распустить 15.2 мг в 100 мкл диметилсульфоксид DOTA-Bn-НК (0.02 ммоль; 1,2 эквиваленты) и объединить это решение с решением от шаг 5.1. Уплотнение пробки microcentrifuge.
- Разрешить реакция инкубировать на ночь при комнатной температуре.
- Очищайте продукт с помощью реверс фаза C18 хроматография ВЭЖХ для удаления любых непрореагировавшего DOTA-Bn-NCS.
Примечание: Время удержания зависят очевидно оборудование ВЭЖХ каждой лаборатории (насосы, колонки, трубы и т.д.), и соответствующие элементы управления должны выполняться до очистки. Однако представить пример, если градиент 5: 95 MeCN/H2O (оба с 0.1% TFA) до 70: 30 MeCN/H2O (оба с 0.1% TFA) используются более 30 минут, полу препаративные 19 x 250 мм C18 столбец и скорость потока 6 мл/мин , СТРУЧКИ, p-СКС-Bn-DOTA и СТРУЧКИ-DOTA будут иметь время удержания вокруг 14.4, 18.8 и 19.6 мин, соответственно. Все три соединения могут контролироваться в 254 Нм.
6 bioconjugation СТРУЧКИ-DOTA в трастузумаб
Примечание: Этот шаг, мы начали с фондовых раствором трастузумаб 16.4 мг/мл.
- В трубке microcentrifuge 1,5 мл привязки низкое содержание белка разбавляют 61 мкл трастузумаб Стоковый раствор (1 мг; 6.67 нмоль, эквивалентный 1) с 859 мкл-фосфатный буфер (рН 7,4).
- К этой смеси добавьте 6.7 мкл свежеприготовленные 10 мм раствора TCEP в H2O (66,7 нмоль, 10 эквиваленты).
- Подготовить раствор 1 мг/мл СТРУЧКИ-DOTA в ДМСО и добавить 73 мкл раствора этой СТРУЧКИ-DOTA в реакционной смеси (66.67 нмоль, 10 эквиваленты).
- Уплотнение пробки microcentrifuge и инкубировать и решение для 2 часа при комнатной температуре.
- После 2 часов очищайте immunoconjugate, с использованием предварительно упакованные одноразовые размер исключения опреснительной столбца.
- Во-первых сбалансировать размер исключение столбцов, как описано поставщиком для удаления консервантов в столбце во время хранения. Типичная процедура включает в себя мытье столбце 5 раз с объемом PBS, что соответствует объему столбца: 5 x 2,5 мл ФСБ.
- Затем добавьте смесь реакции в столбце Размер исключения, отмечая объем реакционной смеси.
- После того, как реакционную смесь вступил столбца, добавьте соответствующее количество PBS довести общий объем раствора добавляется в столбец до 2,5 мл. Например если спряжение реакция привела к общим объемом 1,3 мл, 1,2 мл дополнительных PBS будет нужно быть добавлены к столбцу.
- Наконец собирайте продукта с помощью 2 мл PBS как элюента.
- Концентрат окончательный immunoconjugate с центробежной фильтрации единиц с 50 kDa молекулярный вес отсечения.
Результаты
Первые четыре шага этого протокола — синтез СТРУЧКИ — были разработаны для быть прочным и надежным. Deprotonation и замена 5-(4-aminophenyl)-1,3,4-oxadiazole-2-thiol сформировать желаемый тиоэфиры продукта дает тиоэфиры в > 99% доходности после всего за 45 минут. Далее перевязка между 1 и N-Boc-N'-succinyl-4,7,10-trioxa-1,13-tridecanediamine было достигнуто через стандартный пептид муфты процедуры, что приводит к коллекции продукта (2) в 55% доходности. Затем окисление 2 была выполнена с помощью m-chloroperoxybenzoic кислоты, широко используется окислитель. После стирки шагов 3 был получен как бледные тела в ~ 90% урожая. Наконец удаление защиты группы трет butyloxycarbonyl с 3 было сделано согласно стандартных процедур, с использованием в соотношении 4:1 dichloromethane:trifluoroacetic кислоты. После лиофилизации водной фазы, наш продукт — СТРУЧКИ — был получен как белый порошок в 98% доходности. Прогресс реакции последовал через тонкий слой хроматографии, и личность каждого продукта был подтвержден через 1H ЯМР, 13C-ЯМР и СУЛР-ESI (Таблица 1).
Одним из главных преимуществ реагента СТРУЧКИ является ее модульности. Целый ряд энтеросорбенты, флуорофоров, токсинов или другие грузы могут быть добавлены соединения Кулон аминов. В протоколе рукой мы используем вездесущие хелатором DOTA (1,4,7,10-tetraazacyclododecane-1,4,7,10-tetraacetic кислота) как представитель полезной нагрузки. DOTA, конечно, был использован в широкий спектр биомолекулярных радиофармацевтических препаратов как хелатором для radiometals, включая 68Ga, 64Cu, 111в, 90Y, 177Лу и 225переменного тока. С этой целью Изотиоцианаты подшипник вариант DOTA (p СКС-Bn-DOTA) был занятых и в сочетании с Кулон Амин СТРУЧКИ через простой муфта условий. Результирующая бифункциональных хелатором был затем очищается через обратная фаза C18 ВЭЖХ и изолированных в ~ 75% урожая. Как и в случае других прекурсоров, ход реакции последовал через тонкий слой хроматографии, и идентификатор продукта был подтвержден через 1H ЯМР, 13C-ЯМР и СУЛР-ESI (Таблица 1).
На последнем шаге протокола мы обсуждаем сайт селективного bioconjugation СТРУЧКИ-DOTA в модели иммуноглобулинов, трастузумаб HER2-таргетинг антитела. С этой целью дисульфидных связей региона антитело петли выборочно сокращаются с восстанавливающего агента TCEP [tris(2-carboxyethyl) фосфин]. После этого этапа сокращения Антитела инкубированы с СТРУЧКИ-DOTA 2 ч при комнатной температуре и впоследствии очищенной через размер гель-проникающей хроматографии. В этом случае очищенный, DOTA-подшипник immunoconjugate был получен в ~ 80% доходности, и MALDI-ToF анализ показал степень маркировки (DOL) ~1.8 DOTA/МАБ. Вообще говоря мы обнаружили, что 10 эквиваленты TCEP, 10 эквиваленты реагент СТРУЧКИ, и 2 ч инкубации достаточно дают immunoconjugate с DOL 2 СТРУЧКИ в МАБ (Таблица 2). Этот результат остается последовательной в диапазоне человека, гуманизированные и химерных IgG1 антител; Однако те же условия производят immunoconjugates с DOL только ~1.5 при работе с мышиных антител IgG1. Все это говорит, исследователи должны оптимизировать эти реакции условия для новых антител и СТРУЧКИ подшипник грузов. Наконец и, главное что касается конечного продукта, мы неоднократно и герметизации нашли что на основе СТРУЧКИ immunoconjugates выставки иммунореактив равных или лучше, чем аналогичные конструкции, созданные с помощью случайных или на основе maleimide Спряжение стратегии.
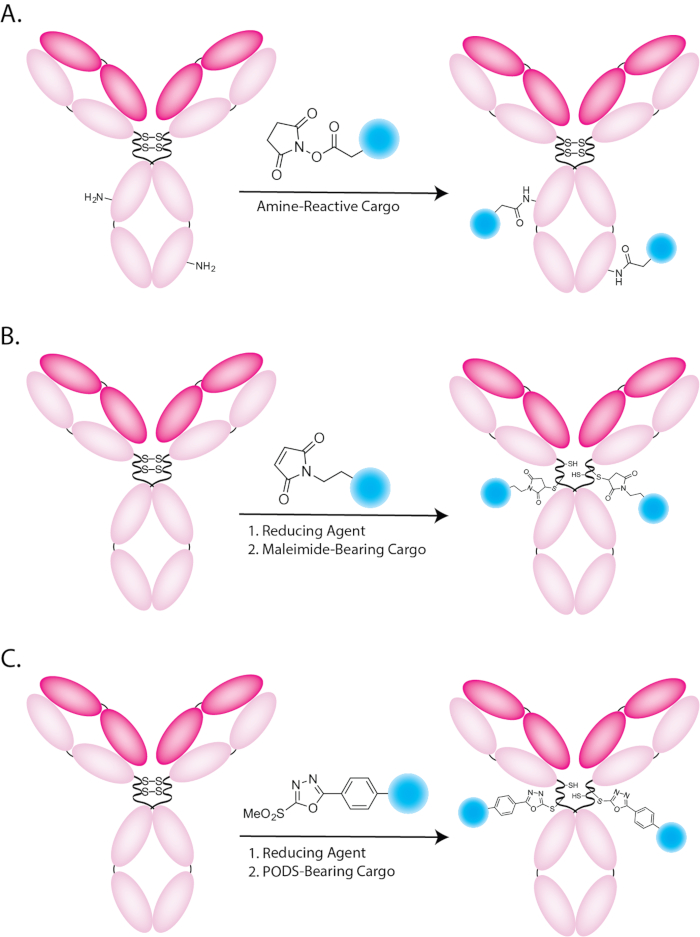
Рисунок 1: Схематическое изображение bioconjugations с помощью Амин реактивной, (A) maleimide подшипник (B) и (C) СТРУЧКИ подшипник грузов. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.

Рисунок 2: Майкл добавлением тиоловых подшипник биомолекулы (зеленый) и радионуклидов подшипник maleimide (желтый) сформировать radiolabeled биоконъюгатов, а также дополнительные реакции, которые radiolabeled конструкции могут пройти в присутствии эндогенного молекулы тиоловых подшипник (розовый). RT = комнатной температуре. Рисунок, перепечатано с разрешения Adumeau, стр., Давыдова, м., Zeglis, б. м. тиоловых-реактивной бифункциональных хелаторов для создания из сайта-выборочно изменения Radioimmunoconjugates с улучшена стабильность. Химии биоконъюгатов. 29, 1364-1372 (2018). Авторское право 2018 американского химического общества. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
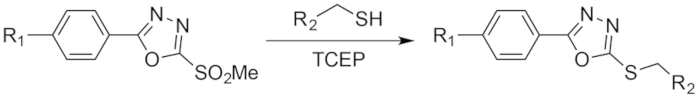
Рисунок 3: Схематическое изображение реакции между СТРУЧКИ и тиоловых. Рисунок, перепечатано с разрешения Adumeau, стр., Давыдова, м., Zeglis, б. м. тиоловых-реактивной бифункциональных хелаторов для создания из сайта-выборочно изменения Radioimmunoconjugates с улучшена стабильность. Химии биоконъюгатов. 29, 1364-1372 (2018). Авторское право 2018 американского химического общества. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
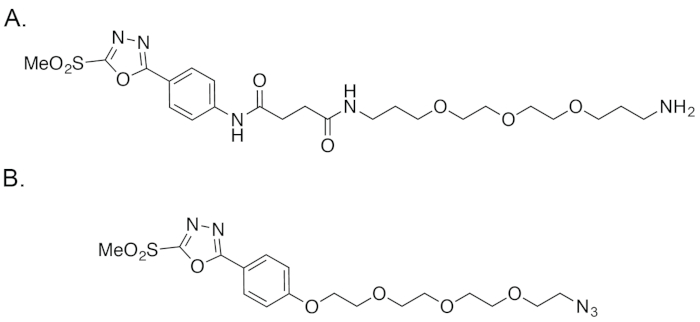
Рисунок 4: В структуре СТРУЧКИ (A) , а также (B) реагента сообщил Barbas, et al.18,19пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
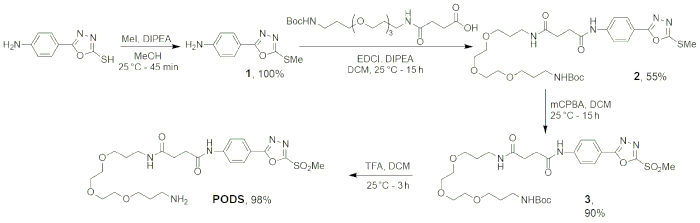
Рисунок 5: Схема 4 шаг синтеза СТРУЧКИ. Рисунок, перепечатано с разрешения Adumeau, стр., Давыдова, м., Zeglis, б. м. тиоловых-реактивной бифункциональных хелаторов для создания из сайта-выборочно изменения Radioimmunoconjugates с улучшена стабильность. Химии биоконъюгатов. 29, 1364-1372 (2018). Авторское право 2018 американского химического общества. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.

Рисунок 6: Схема синтеза СТРУЧКИ-DOTA. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
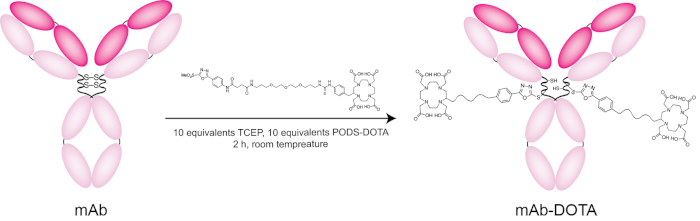
Рисунок 7: Схема bioconjugation трастузумаб с СТРУЧКИ-DOTA. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.

Рисунок 8: Сравнение поведения в естественных условиях 89Zr меченых radioimmunoconjugates huA33, созданных на основе СТРУЧКИ (89Zr-ДФО-СТРУЧКИ huA33) и bioconjugation стратегии на основе maleimide (89Zr-ДФО mal-huA33). Плоскостной (слева) и максимальная интенсивность проекции (справа) ПЭТ изображения обнаженной мышей Атинические подшипник A33 антиген выражая SW1222 колоректального рака ксенотрасплантатов (белая стрелка) после инъекции 89Zr-ДФО-СТРУЧКИ huA33 и 89 ZR ДФО mal-huA33 (140 Μки, 60-65 мкг). Корональные срезы пересекаются центр опухоли. Рисунок, перепечатано с разрешения Adumeau, стр., Давыдова, м., Zeglis, б. м. тиоловых-реактивной бифункциональных хелаторов для создания из сайта-выборочно изменения Radioimmunoconjugates с улучшена стабильность. Химии биоконъюгатов. 29, 1364-1372 (2018). Авторское право 2018 американского химического общества. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
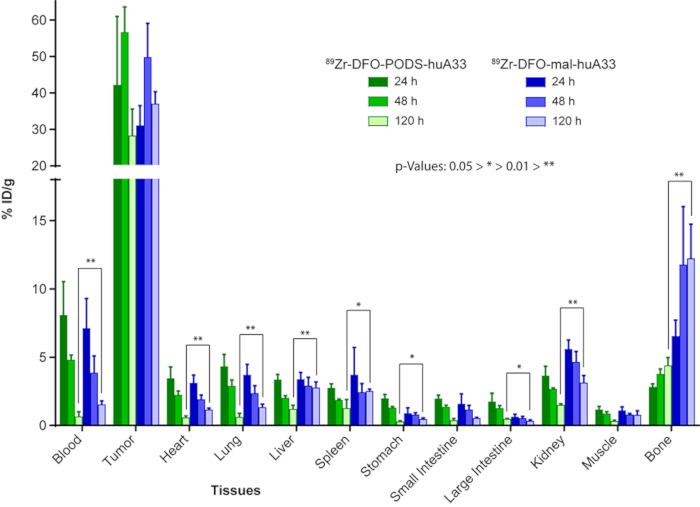
Рисунок 9: Сравнение поведения в естественных условиях 89Zr меченых radioimmunoconjugates huA33, созданных на основе СТРУЧКИ (89Zr-ДФО-СТРУЧКИ huA33) и bioconjugation стратегии на основе maleimide (89Zr-ДФО mal-huA33). Накопление данных после отправления 89Zr-ДФО-СТРУЧКИ huA33 и Zr-ДФО mal-huA33 (30 Μки, 15-18 мкг) 89Обнаженная мышей Атинические подшипник A33 антиген выражая подкожной SW1222 человека колоректального рака ксенотрасплантатов. Значения для желудка, тонкой кишки и толстой кишки включают содержимое. Рисунок, перепечатано с разрешения Adumeau, стр., Давыдова, м., Zeglis, б. м. тиоловых-реактивной бифункциональных хелаторов для создания из сайта-выборочно изменения Radioimmunoconjugates с улучшена стабильность. Химии биоконъюгатов. 29, 1364-1372 (2018). Авторское право 2018 американского химического общества. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
| Соединение | 1 H-ЯМР смены | 13 C-ЯМР смены | HRMS | |||
| 1 | (500 МГц, CDCl3) 7.79 (2 H, d, J = 8,5 Гц), 6.72 (2 H, d, J = 8,5 Гц), 4.04 (2 H, br s), 2,75 (3 H, s) | (125 МГц, CDCl3) 166.3 163.7, 149.7, 128,5, 114.8, 113.5, 14,8 | m/z Calcd [C9H9N3OS + H]+: 208.0539; Найдено: 208.0539; Δ: 0.0 ppm | |||
| 2 | (500 МГц, CDCl3) 9,68 (1H, s), 7.91 (2H, d, J = 9.0 Гц), 7.71 (2H, d, J = 8,5 Гц), 6,82 (1H, s), 4.99 (1H, s), 3.70-3.45 (12H, m), 3.41 (2H, q, J = 6.0 Гц), 3,20 (2H, q, J = 6,5 Гц), 2.76 (3H, s), 2.71 (2H, m), 2,63 (2 Ч. м), 1.80-1.70 (4 H, m), 1,42 (9 H, s) | (125 МГц, CDCl3) 172.6, 171.3, 165,8, 164.6, 156.2, 141,8, 127,7, 119.6, 118,6, 79,2, 70,6, 70,5, 70,3, 70,1, 69,6, 38,8, 38,5, 33,5, 31,6, 29,9, 28,6, 14,8 | m/z Calcd [C28H43N5O8S + Na]+: 632.2725; Найдено: 632.2722; Δ: -0.47 ppm | |||
| 3 | (500 МГц, CDCl3) 9.99 (1 H, s), 7.98 (2 H, d, J = 9.0 Гц), 7,75 (2 H, d, J = 8,5 Гц), 6,88 (1 H, s), 4.99 (1 H, s), 3.66-3.50 (15 H, m), 3.41 (2 H, q, J = 6.0 Гц), 3,20 (2 H, q, J = 6,5 Гц), 2.71 (2 H, m), 2,65 (2 H, m) , 1.80-1.70 (4H, m), 1,43 (9H, s) | (125 МГц, CDCl3) 172.6, 171,5, 166,5, 161,6, 156.1, 143,4, 128.7, 119.6, 116.4, 79.1, 70,5, 70,4, 70,2, 70,0, 69,4, 43,0, 38,8, 38,4, 33,2, 31.3, 29,7, 28,4 | m/z Calcd [C28H43N5O10S + H]+: 642.2803; Найдено: 642.2797; Δ:-0.93 ppm | |||
| СТРУЧКИ | (500 МГц, Д2O) 7,85 (2 H, d, J = 9.0 Гц), 7.55 (2 H, d, J = 8,5 Гц), 3,60-3,45 (15 H, m), 3,45 (2 H, t, J = 6,5 Гц), 3,20 (2 H, t, J = 6,5 Гц), 3,04 (2 H, t, J = 7.0 Гц), 2.67 (2 H, t, J = 6,5 Гц), 2,54 (2 Ч. t, J = 6,5 Гц), 1.87 (2 H, qt, J = 6,5 Гц), 1.70 (2 H, qt, J = 6,5 Гц) | (125 МГц, Д2O) 174,5, 173.2, 166.8, 161,4, 142.2, 128,6, 120,3, 116.6, 69,4, 69,4, 69,3, 69.2, 68,2, 68,2, 42,5, 37,6, 36,2, 31,9, 30,7, 28,2, 26.4 | m/z Calcd [C23H35N5O8S + H]+: 542.2279; Найдено: 542.2281; Δ: 0,37 ppm | |||
| СТРУЧКИ DOTA | (600 МГц, ДМСО d6) 10,46 (1 H, s), 9,74 (1 Ч., bs), 8.04 (2 H, d, J = 8.6 Гц), 7,99 (1 H, s), 7,90 (1 H, t, J = 5,0 Гц), 7,86 (2 H, d, J = 6,5 Гц), 7.44 (2 H, d, J = 7.9 Гц), 7.24 (2 H, d, J = 7.1 Гц), 4,35-2,41 (45 H, m) , 3.70 (3H, s), 1,76 (2H, q, J = 6,3 Гц), 1.61 (Ч. 2, q, J = 6,5 Гц) | (125 МГц, ДМСО d6) 171.8, 171.4, 166.1, 162,2, 158,8, 158,6, 129,8, 129.0, 127,6, 123.3, 119,5, 118,5, 116,5, 116.4, 70,2, 70,1, 70,0, 68,7, 68,5, 43,4, 41,8, 36,3, 32,2, 30,4, 29,8, 29,1 | m/z Calcd [C47H68N10O16S2+ H]+: 1093.4334; Найдено: 1093.4327; Δ: -0.64 ppm | |||
Таблица 1. Характеристика данных для синтетических интермедиатов описал СТРУЧКИ и СТРУЧКИ-DOTA.
| Антитела | Тип | Постоянный регион | Отношение СТРУЧКИ: МАБ |
| Человеческой плазмы IgG | Человека | IgG человека | 2.1 ± 0,1 |
| Трастузумаб | Гуманизированные | Человеческие IgG1 | 2,0 ± 0,1 |
| huA33 | Гуманизированные | Человеческие IgG1 | 2.1 ± 0,1 |
| Cetuximab | Химерных | Человеческие IgG1 | 2.2 ± 0,1 |
| AR 9.6 | Мурина | Мышиных IgG1 | 1.4 ± 0,1 |
| Плазмы мыши IgG | Мурина | Мурина IgG | 1,5 ± 0,1 |
Таблица 2. Степень маркировки различных антител после сопряжения с Флюорофор СТРУЧКИ подшипника. Значения показываются стандартных отклонений. Таблица, перепечатано с разрешения Adumeau, стр., Давыдова, м., Zeglis, б. м. тиоловых-реактивной бифункциональных хелаторов для создания из сайта-выборочно изменения Radioimmunoconjugates с улучшена стабильность. Химии биоконъюгатов. 29, 1364-1372 (2018). Авторское право 2018 американского химического общества.
Обсуждение
В настоящем докладе мы решили не включать любые протоколы для radiolabeling или в естественных условиях экспериментов. Причины просты. Что касается первого, radiolabeling на основе СТРУЧКИ immunoconjugate не отличается от того из immunoconjugate, синтезируются с помощью других bioconjugation стратегии, и эти процедуры были всесторонне рассмотрены в других странах2 . Что касается последнего специфика доклинических в экспериментах in vivo (то есть, мыши модели, дозы и т.д.) могут широко варьироваться в зависимости от приложения и системы антитела/antigen.
Наши предыдущие расследования с 89Zr помечены варианты huA33 обеспечивают убедительные иллюстрации преимуществ на основе СТРУЧКИ bioconjugations. HuA33 это гуманизированные антитела IgG1, ориентированном A33 антигена, трансмембранный гликопротеин, выраженные на > 95% колоректального рака23,24. В наших предыдущих рукопись22мы сообщаем синтез 89Zr-ДФО huA33 radioimmunoconjugate с помощью обоих СТРУЧКИ и maleimide-стратегии на основе bioconjugation. Два radiolabeled антител — 89Zr-ДФО-СТРУЧКИ huA33 и 89Zr-ДФО mal-huA33 — были произведены в почти идентичных урожайности, чистоты, специфика деятельности и иммунореактивности. Крайне важно, однако, два radioimmunoconjugates выставлены резко различных графену в сыворотке крови человека: после инкубации на семь дней при 37 ° C, 89Zr-ДФО-СТРУЧКИ huA33 сохранились 86 ± 1%, в то время как его двоюродный брат, на основе maleimide был только 61 ± 5% нетронутыми. In vivo PET изображений и накопление экспериментов в Атинические обнаженной мышей с учетом A33 антиген выражая SW1222 человека колоректального рака ксенотрасплантатов показали резкий различия в в естественных условиях поведение двух radioimmunoconjugates (рис. 8 и Рисунок 9). Zr-ДФО-СТРУЧКИ huA33 89и 89Zr-ДФО mal-huA33 производят концентрации высокой активности в опухолевой ткани: 56.4 ± 6.9%ID/g и 49,6 ± 9.3%ID/g, соответственно, 48 ч после приема. Однако на основе maleimide radioimmunoconjugate производится значительно выше концентрации деятельности в здоровых тканях, чем агент на основе СТРУЧКИ. Например, 89Zr-ДФО mal-huA33 производится концентрации деятельности 3.1 ± 0.5, 2,7 ± 0,4 и 12.2 ± 0,4% ID/g в почках, печени и костей, соответственно, на 120 h впрыск, значения которого значительно превышают концентрации деятельности производимые 89Zr-ДФО-СТРУЧКИ huA33 в том же тканях (1.4 ± 0.1, 1,2 ± 0,3 и 4,3 ± 0,6% ID/g). Действительно, 89Zr-ДФО-СТРУЧКИ huA33 производства более низкой концентрации активности во всех тканях непромысловых (за исключением толстой кишки) на 120 ч после инъекции, по сравнению с 89Zr-ДФО mal-huA33. В результате коэффициенты концентрации активности опухоли орган для 89Zr-ДФО-СТРУЧКИ huA33 обычно превосходят 89Zr-ДФО mal-huA33; в частности, опухоли на печени, опухоли в селезенке, опухоль почки и концентрация активности опухоли кость коэффициенты почти вдвое для immunoconjugate на основе СТРУЧКИ, по сравнению с его двоюродный брат, maleimide производные. Учитывая, что основное различие между двумя radioimmunoconjugates был bioconjugation ручку хелатором, повышенной стабильности СТРУЧКИ тиоловых связь почти наверняка отвечает за этого производительность в естественных условиях.
Принимая более широкий взгляд, сайт неизбирательной bioconjugation зонды для lysines в пределах антитела правда простым и легким подход к модификации антител. Однако наличие нескольких lysines, распределенных по всей структуре иммуноглобулинов означает, что невозможно контролировать точное сайта или степень bioconjugation2. В результате это случайные стратегии часто производит плохо определены и весьма неоднородной immunoconjugates, которые могут exhibit снижение иммунореактивности если перешнуровок происходят в пределах антиген связывая доменов3. Преимущества сайта селективных подходов к bioconjugation были проиллюстрированы неоднократно для обеих radioimmunoconjugates и антитела наркотиков конъюгатов8,14,25,26, 27,28,29,30. Короче говоря не только производят более четко bioconjugation сайт селективные стратегии и однородной immunoconjugates чем традиционные методики, они также создают изображения агентов, radioimmunotherapeutics и АЦП с улучшенными характеристиками в естественных условиях. Тем не менее, где на основе СТРУЧКИ перешнуровок стойте в сравнении с другими стратегиями сайт селективный модификации? Вообще говоря, подходы к сайт селективные модификации антител можно подразделить на четыре категории: (1) перешнуровок остатков цистеина, (2) манипуляции гликанов тяжелые цепи, преобразования (3) chemoenzymatic и (4) использование генной инженерии4,5. Конечно эта система классификации не является совершенным, и некоторые подходы (например, модификация гликанов тяжелые цепи с ферментами) неизбежно претендовать на две категории. Каждая стратегия имеет свои преимущества и недостатки. Подходы на основе генной инженерии обеспечивают изысканный контроль над сайт спряжение, но они являются сложными и дорогими в31,,3233. Окислительного муфты для тяжёлой цепи гликанов недорогой и простой, но они рискуют оксидативное повреждение структурной целостности иммуноглобулина34,,3536,37 ,38.
Главным преимуществом на основе тиоловых bioconjugations — СТРУЧКИ включены — является их простота и модульности. С другой стороны, их основные ограничения, проистекает из присутствия нескольких тиолы внутри антитела, черта, которая уменьшает степень контроля над как сайт спряжение и количество изменений на антитела. В этом смысле сочетание на основе тиоловых перешнуровок и антител, которые генетически обладают бесплатно хвоща остатков является особенно привлекательным подходом. Как мы уже отмечали, другой на основе maleimide тиоловых перешнуровок ограничены восприимчивости облигации тиоэфиры succinimidyl ретро Майкл дополнений в естественных условиях. Тем не менее критически, использование СТРУЧКИ аннулирует эту проблему.
Прежде чем мы завершим, важно отметить, что возникающие характер СТРУЧКИ технологии можно создать свой собственный набор препятствий. Например бифункциональных хелаторов не СТРУЧКИ подшипник коммерчески доступны (в настоящее время) и нет данных адресации клинической фармакологии, токсикологии или иммуногенности на основе СТРУЧКИ immunoconjugates. Однако мы считаем, что на основе СТРУЧКИ bioconjugations имеют потенциал, чтобы коренным образом изменить способ immunoconjugates синтезированы как в лабораторных, так и в клинике. В настоящее время, мы только подали этот химической технологии для развития radioimmunoconjugates для ядерных изображений и радиоиммунотерапия, хотя конъюгатов расследования в полезности такого подхода для строительства антител наркотиков и в настоящее время ведутся другие биомолекулярных лекарства. В конце концов, мы искренне надеемся, что этот протокол — и особенно простой химии, которую мы разработали — будет способствовать использование phenyloxadiazolyl метил сульфонов для на основе сульфгидрильных спряжения и стимулировать переход в поле от малеинимидов к более стабильной и более надежной альтернативы.
Раскрытие информации
Авторы не имеют ничего сообщать.
Благодарности
Авторы благодарят доктор Sai Kiran Шарма за полезные беседы.
Материалы
| Name | Company | Catalog Number | Comments |
| 5-(4-aminophenyl)-1,3,4-oxadiazole-2-thiol | Sigma-Aldrich | 675024 | |
| 1.5 mL LoBind Microcentrifugal Tube | Eppendorf | 925000090 | |
| 1.5 mL Microcentrifugal Tube | Fisherbrand | 05-408-129 | |
| Acetonitrile | Fisher Scientific | A998-4 | |
| Amicon Ultra-2 Centrifugal Filter Unit | EMD Millipore | EN300000141G | |
| Cyclohexane | Fisher Scientific | C556-4 | |
| Dichloromethane | Fisher Scientific | AC383780010 | |
| Diisopropylethylamine | MP Biomedicals, LLC | 150915 | |
| Dimethylsulfoxide | Fisher Scientific | 31-727-5100ML | |
| Ethyl Acetate | Fisher Scientific | E145 4 | |
| Hydrochloric Acid | Fisher Scientific | A144-500 | |
| Iodomethane | Sigma-Aldrich | 289566-100G | |
| Magnesium Sulfate | Acros Organics | 413485000 | |
| m-chloroperbenzoic acid | Sigma-Aldrich | 273031 | |
| Methanol | Fisher Scientific | A412 1 | |
| NBoc-N′-succinyl-4,7,10-trioxa-1,13-tridecanediamine | Sigma-Aldrich | 671401 | Store at -80 °C |
| N-ethyl-N′- [3- (dimethylamino)propyl] carbodiimide hydrochloride | Sigma-Aldrich | 3450 | |
| Phosphate Buffered Saline | Sigma-Aldrich | P5493 | 10× Concentration |
| p-SCN-Bn-DOTA | Macrocyclics | B-205 | Store at -80 °C |
| Sephadex G-25 in PD-10 Desalting Columns | GE Healthcare | 17085101 | |
| Sodium Carbonate | Sigma-Aldrich | S7795 | |
| Sodium Hydroxide | Fisher Scientific | S318-1 | |
| TCEP | ThermoFischer Scientific | 20490 | |
| Triethylamine | Fisher Scientific | AC157911000 | |
| Trifluoroacetic Acid | Fisher Scientific | A116-50 |
Ссылки
- Wu, A. M. Antibodies and antimatter: The resurgence of immuno-PET. Journal of Nuclear Medicine. 50 (1), 2-5 (2009).
- Zeglis, B. M., Lewis, J. S. A practical guide to the construction of radiometallated bioconjugates for positron emission tomography. Dalton Transactions. 40 (23), 6168-6195 (2011).
- Agarwal, P., Bertozzi, C. R. Site-specific antibody-drug conjugates: the nexus of bioorthogonal chemistry, protein engineering, and drug development. Bioconjugate Chemistry. 26 (2), 176-192 (2015).
- Adumeau, P., Sharma, S. K., Brent, C., Zeglis, B. M. Site-specifically labeled immunoconjugates for molecular imaging-part 1: Cysteine residues and glycans. Molecular Imaging and Biology. 18 (1), 1-17 (2016).
- Adumeau, P., Sharma, S. K., Brent, C., Zeglis, B. M. Site-specifically labeled immunoconjugates for molecular imaging-part 2: Peptide tags and unnatural amino acids. Molecular Imaging and Biology. 18 (1), 153-165 (2016).
- Alley, S. C., et al. Contribution of linker stability to the activities of anticancer immunoconjugates. Bioconjugate Chemistry. 19 (3), 759-765 (2008).
- Baldwin, A. D., Kiick, K. L. Tunable degradation of maleimide-thiol adducts in reducing environments. Bioconjugate Chemistry. 22 (10), 1946-1953 (2011).
- Shen, B. -. Q., et al. Conjugation site modulates the in vivo stability and therapeutic activity of antibody-drug conjugates. Nature Biotechnology. 30 (2), 184-189 (2012).
- Jackson, D., et al. In vitro and in vivo evaluation of cysteine and site specific conjugated herceptin antibody-drug conjugates. Plos One. 9 (1), (2014).
- Ponte, J. F., et al. Understanding how the stability of the thiol-maleimide linkage impacts the pharmacokinetics of lysine-linked antibody-maytansinoid conjugates. Bioconjugate Chemistry. 27 (7), 1588-1598 (2016).
- Stimmel, J. B., et al. Site-specific conjugation on serine -> cysteine variant monoclonal antibodies. Journal of Biological Chemistry. 275 (39), 30445-30450 (2000).
- Li, L., et al. Reduction of kidney uptake in radiometal labeled peptide linkers conjugated to recombinant antibody fragments. site-specific conjugation of DOTA-peptides to a cys-diabody. Bioconjugate Chemistry. 13 (5), 985-995 (2002).
- Li, J., Wang, X. H., Wang, X. M., Chen, Z. L. Site-specific conjugation of bifunctional chelator BAT to mouse IgG(1) Fab' fragment. Acta Pharmacologica Sinica. 27 (2), 237-241 (2006).
- Tinianow, J. N., et al. Site-specifically Zr-89-labeled monoclonal antibodies for ImmunoPET. Nuclear Medicine and Biology. 37 (3), 289-297 (2010).
- Li, L., et al. Site-specific conjugation of monodispersed DOTA-PEGn to a thiolated diabody reveals the effect of increasing PEG size on kidney clearance and tumor uptake with improved 64-copper PET imaging. Bioconjugate Chemistry. 22 (4), 709-716 (2011).
- Khalili, H., Godwin, A., Choi, J. -. w., Lever, R., Brocchini, S. Comparative binding of disulfide-bridged PEG-Fabs. Bioconjugate Chemistry. 23 (11), 2262-2277 (2012).
- Koniev, O., Wagner, A. Developments and recent advancements in the field of endogenous amino acid selective bond forming reactions for bioconjugation. Chemical Society Reviews. 44 (15), 5495-5551 (2015).
- Patterson, J. T., Asano, S., Li, X., Rader, C., Barbas, C. F. Improving the serum stability of site-specific antibody conjugates with sulfone linkers. Bioconjugate Chemistry. 25 (8), 1402-1407 (2014).
- Toda, N., Asano, S., Barbas, C. F. Rapid, stable, chemoselective labeling of thiols with Julia-Kocienski-like reagents: A serum-stable alternative to maleimide-based protein conjugation. Angewandte Chemie-International Edition. 52 (48), 12592-12596 (2013).
- Zhang, Q., et al. Last-step enzymatic F-18-fluorination of cysteine-tethered RGD peptides using modified Barbas linkers. Chemistry-a European Journal. 22 (31), 10998-11004 (2016).
- Chiotellis, A., et al. Novel chemoselective F-18-radiolabeling of thiol-containing biomolecules under mild aqueous conditions. Chemical Communications. 52 (36), 6083-6086 (2016).
- Adumeau, P., Davydova, M., Zeglis, B. M. Thiol-reactive bifunctional chelators for the creation of site-selectively modified radioimmunoconjugates with improved stability. Bioconjugate Chemistry. 29, 1364-1372 (2018).
- Sakamoto, J., Kojima, H., Kato, J., Hamashima, H., Suzuki, H. Organ-specific expression of the intestinal epithelium-related antigen A33, a cell surface target for antibody-based imaging and treatment in gastrointestinal cancer. Cancer Chemotherapy and Pharmacology. 46, S27-S32 (2000).
- Sakamoto, J., et al. A phase I radioimmunolocalization trial of humanized monoclonal antibody huA33 in patients with gastric carcinoma. Cancer Science. 97 (11), 1248-1254 (2006).
- Junutula, J. R., et al. Site-specific conjugation of a cytotoxic drug to an antibody improves the therapeutic index. Nature Biotechnology. 26 (8), 925-932 (2008).
- Pillow, T. H., et al. Site-specific trastuzumab maytansinoid antibody-drug conjugates with improved therapeutic activity through linker and antibody engineering. Journal of Medicinal Chemistry. 57 (19), 7890-7899 (2014).
- Boswell, C. A., et al. Enhanced tumor retention of a radiohalogen label for site-specific modification of antibodies. Journal of Medicinal Chemistry. 56 (23), 9418-9426 (2013).
- Boswell, C. A., et al. Impact of drug conjugation on pharmacokinetics and tissue distribution of anti-STEAP1 antibody-drug conjugates in rats. Bioconjugate Chemistry. 22 (10), 1994-2004 (2011).
- Alvarez, V. L., et al. Site-specifically modified 111In labelled antibodies give low liver backgrounds and improved radioimmunoscintigraphy. Nuclear Medicine and Biology. 13 (4), 347-352 (1986).
- Strop, P., et al. Location matters: SIte of conjugation modulates stability and pharmacokinetics of antibody drug conjugates. Chemistry, Biology. 20 (2), 161-167 (2013).
- Hallam, T. J., Wold, E., Wahl, A., Smider, V. V. Antibody conjugates with unnatural amino acids. Molecular Pharmaceutics. 12 (6), 1848-1862 (2015).
- Axup, J. Y., et al. Synthesis of site-specific antibody-drug conjugates using unnatural amino acids. Proceedings of the National Academy of Sciences. 109 (40), 16101-16106 (2012).
- Lang, K., Chin, J. W. Cellular incorporation of unnatural amino acids and bioorthogonal labeling of proteins. Chemical Reviews. 114 (9), 4764-4806 (2014).
- Yamasaki, R. B., Osuga, D. T., Feeney, R. E. Periodate oxidation of methionine in proteines. Analytical Biochemistry. 126 (1), 183-189 (1982).
- Wang, W., et al. Impact of methionine oxidation in human IgG1 Fc on serum half-life of monoclonal antibodies. Molecular Immunology. 48 (6-7), 860-866 (2011).
- O'Shannessy, D. J., Dobersen, M. J., Quarles, R. H. A novel procedure for labeling immunoglobulins by conjugation to oligosaccharide moieties. Immunology Letters. 8 (5), 273-277 (1984).
- Panowski, S., Bhakta, S., Raab, H., Polakis, P., Junutula, J. R. Site-specific antibody drug conjugates for cancer therapy. Mabs. 6 (1), 34-45 (2014).
- Hu, M. D., et al. Site-specific conjugation of HIV-1 tat peptides to IgG: a potential route to construct radioimmunoconjugates for targeting intracellular and nuclear epitopes in cancer. European Journal of Nuclear Medicine and Molecular Imaging. 33 (3), 301-310 (2006).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены