Method Article
Определение транспортных Оценить ксенобиотиков и наноматериалы через плаценту помощью
В этой статье
Резюме
Экс естественных условиях Двойной рециркуляции плаценты человека модели перфузии может быть использован для исследования передачи ксенобиотиков и наночастиц через плаценты человека. В этом видео мы опишем протокол оборудования и методов, необходимых для успешного выполнения перфузии плаценты.
Аннотация
Несколько десятилетий назад плаценты человека считалось непроницаемый барьер между матерью и еще не родившегося ребенка. Однако открытие талидомида индуцированных врожденных дефектов и многие более поздние исследования впоследствии доказал обратное. На сегодняшний день некоторые вредные ксенобиотиков как никотин, героин, метадон или наркотиков, а также загрязнение окружающей среды были описаны для преодоления этого барьера. С ростом использования нанотехнологий, плацента, вероятно, вступают в контакт с новыми наночастицы либо случайно, в результате воздействия или умышленно в случае потенциального наномедицинские устройства. Данные экспериментов на животных не могут быть экстраполированы на людей, потому что плацента является наиболее видоспецифической органом млекопитающих 1. Таким образом, экс естественных условиях двойной рециркуляции перфузии плаценты человека, разработанная Panigel соавт. 2 в 1967 году и постоянно изменены Schneider и соавт. 3 в 1972 году, может служить отличной моделью TO изучать передачи ксенобиотиков или частиц.
Здесь мы концентрируем внимание на экс естественных условиях двойной рециркуляции плаценты человека протокол перфузии и его дальнейшее развитие приобретать воспроизводимые результаты.
Плаценты, полученной после информированного согласия матерей от несложных срока беременности кесарево доставки. Матери и плода сосуды интактного семядоли вводили канюлю и перфузии по крайней мере в течение пяти часов. В качестве модели частиц флуоресцентно меченых частиц полистирола с размерами 80 и 500 нм были добавлены к материнской цепи. 80 нм частиц смогли проникают через плацентарный барьер и обеспечивают идеальный пример для вещества, которое передается через плаценту к плоду в то время как 500 нм частицы были сохранены в плацентарной ткани или материнской цепи. Экс естественных человеческих плацентарной перфузии модель является одной из немногих моделей, обеспечивающих надежную информацию отранспорта поведения ксенобиотиков на важный барьер ткани, которая обеспечивает интеллектуальный и клинических соответствующих данных.
Введение
Плацента представляет собой сложный орган, который отвечает за обмен кислорода, углекислого газа, питательных веществ и отходов и в то же время в состоянии держать две цепи крови матери и растущего плода отделены друг от друга. Кроме того, он предотвращает отказ от ребенка по материнской иммунной системы и вырабатывает гормоны для поддержания беременности. Клеточный барьер образован цитотрофобласта клетки, которые сливаются и образуют истинно синцития без боковых клеточных мембран 4,5. Весь плаценты организована в несколько семядоли, которые содержат один плода ворсинок дерева и представляют собой один функциональный блок плаценты.
Изучение плацентарного барьерной функции усилилась с открытием талидомид индуцированных пороков развития в 1960-х. По понятным причинам транслокации исследований с беременными женщинами не может быть выполнена. Следовательно, различные альтернативные модели были разработаны 6,7 . Наиболее перспективным и, вероятно, наиболее соответствующих клинических модель экс естественных условиях человеческого плацентарного модели перфузии разработанный Panigel и коллег 2,3.
Многие женщины подвергаются воздействию различных ксенобиотиков, таких как наркотики или загрязнителей окружающей среды во время беременности 8. Для некоторых препаратов, которые были уже вводится регулярно во время беременности, в естественных условиях исследования может быть выполнено путем сравнения материнской крови концентрации тем, что в пуповинной крови. Однако, как правило есть только ограниченную информацию о фармакокинетике и динамики у плода и тератогенности этих веществ.
Например опиаты, такие как героин легко проникает через плацентарный барьер и может привести к внутриутробной задержки роста, преждевременных родов или самопроизвольного аборта 9,10. Так, в случае отсутствия воздержание во время беременности заместительная терапия метадоном рекомендуется. Эксестественных условиях человеческого плацентарного модели перфузии показало, что передача метадон в кровообращение плода незначительна 11, что хорошо коррелирует с расчетными пуповинной крови к материнской крови соотношение концентраций после родов 12.
Нанотехнология является развивающейся области, особенно в медицине. Так, под естественным штраф (<2,5 мкм в диаметре) и сверхтонких частиц (<0,1 мкм в диаметре) в дым лесных пожаров, извержений вулканов и в пустыне пыли, воздействия наноматериалов (по крайней мере в одном измерении <0.1 мкм 13 ) возрастает. В этой связи возникает вопрос о токсикологическом потенциале наноматериалов. Хотя никакой опасности человеку не может быть доказано тем не менее, существуют основные экспериментальные исследования, указывающие, что наночастиц может вызвать неблагоприятные биологические реакции, ведущие к результатам токсикологических 14. В последнее время некоторые исследования показали, что внутриутробное воздействиезагрязнение воздуха связано с более высокой необходимости дыхательной и воспаления дыхательных путей у новорожденных и детей 15,16. Кроме того, малые наночастицы могут быть использованы в качестве носителей лекарственных средств для лечения либо специально плода или матери. Таким образом, становится очевидным, что обширные исследования различных ксенобиотиков или наноматериалов и их способности проникать через плацентарный барьер не требуется. Фактический обзор текущих исследований о плацентарной проницаемости для наноматериалов обобщены в Менезес и соавт. 2011 17 и Buerki-Thurnherr соавт. 2012 7.
Экс естественных условиях двойной рециркуляции плаценты человека модели перфузии обеспечивает контролируемый и надежная система для изучения плацентарного транспорта различных эндогенных и экзогенных соединений 3,11,12,18,19 и широкого спектра других функций плаценты, как механизмы, ответственные за развития патологических состояний, как преэклампсия <вир> 20-22. В этом протоколе мы ориентируемся в основном на момент установки, обработки и способа, которые позволяют исследовать накопление, эффектов и транслокации темпы широкий набор ксенобиотиков или наночастиц.
протокол
1. Подготовка Система перфузии
- Настройка перфузии система, состоящая из водяной бани, перфузии камеры, две колонки для оксигенации, два перистальтических насоса, две ловушки пузырь, два нагревателя потока и одного датчика давления (рис. 1). Соединение этих компонентов с трубкой разделов состоит из силиконовых материалов и поливинилхлорида в соответствии со схемой на фиг.2. Наконец, существуют две цепи представляющего плода и матери цепи соответственно.
- Включите водяной бане, поток обогреватели и отопление для перфузии камеры. Температура должна быть 37 ° С.
- Подогреть перфузии среда (NCTC-135 тканевой культуры средой, разбавленной в соотношении 1:2 буфером Эрла (6,8 г / л хлорида натрия, 0,4 г / л хлорида калия, 0,14 г / л фосфата натрия, 0,2 г / л сульфата магния 0,2 г / л хлорида кальция, 2 г / л глюкозы) с добавлением глюкозы (1 г / л), декстран 40 (10 г / л), бычий сывороточный альбумин (10 г/ Л), натрий гепарин (2500 МЕ / л), амоксициллином (250 мг / л) и бикарбонат натрия (2,2 г / л), рН 7,4) в водяной бане.
- Последовательно промыть артериальной системы плода и материнской цепи с) в 200 мл дистиллированной воды, б) 50 мл 1% гидроксида натрия, в) 1%-ной фосфорной кислоты и г) снова 200 мл дистиллированной водой (расход: 15 - 20 мл / мин).
- Подключите плода канюли (Ø 1,2 мм; тупой иглой должны быть прикреплены к модифицированным крылатых инфузионный набор игл) к плоду артериальная труб.
- Промыть артериальной системы плода и материнской цепи с перфузионной средой, пока все трубы не содержат среды (скорость потока: 15-20 мл / мин). Во время этого этапа заполнить пузырь ловушки и удалить все пузырьки вниз по течению от ловушки. Тогда остановки насосов. Это действительно важно, что афферентные артериальной трубы всегда без пузырьков воздуха, в противном случае после катетеризации особенно тонкой плода может привести к разрыву сосудов.
- Включение газового потока. Материнские цепи кислородом Wiй 5% двуокиси углерода и 95% воздуха и синтетические плода цепь с 5% двуокиси углерода и 95% азота.
- Начало записи датчика давления.
2. Cannulating Плацента
- Получить нетронутыми плаценты от срока беременности несложный после первичного кесарева сечения. Письменное согласие должно быть дано (был получен в случае нашего исследования) матери до родов и исследование должно быть одобрено местным этическим комитетом (это было в наших исследованиях). Первый визуальный контроль должно быть сделано для обеспечения акушерок здоровыми и нетронутыми плаценты.
- Канюлированием плаценты является важным шагом! Во время перфузии каждого маленького нарушения в тканях может привести к утечке между материнской и кровообращение плода. Плацента должна быть получена в течение 30 минут после родов.
- Выберите нетронутыми семядолей в краевой зоне плаценты без видимых сбоев по материнской линии. На хорионического пластины,связать обе смежные отрасли пупочной артерии и вене вверх по течению к более поздней стороне катетеризации (к пуповине) с помощью хирургического шовного материала. Сделать всегда два узла.
- Иглу артерии плода в первую очередь. Плацентарных артериях плода всегда меньше и тоньше, чем вены.
- Сделайте шва вокруг артерии плода, но не связать его немедленно. Держите сосуд с пинцетом, разрезать судно тщательно и приложить небольшой канюли (Ø 1,2 мм) в артерии. Затем связать шва (два узла).
- Приступить к вене плода в той же манере, но использовать больший канюли (Ø 1,5-1,8 мм; тупой иглой должны быть прикреплены к модифицированным крылатых инфузионный набор игл).
- Включите плода насос (2 мл / мин). Если нет никаких видимых утечек и кровью исходит из плода канюли вену, медленно увеличить поток до 4 мл / мин. Обратите внимание на давление в артерии плода, она не должна превышать 70 мм рт. Если жидкость просачивается в плода или матеrnal канюли исправить их с другого шва.
- Поместите плаценты на держатель ткани с плода стороной вверх и потяните плацентарной мембраны и ткани над шипами. В конце перфузии семядоли должна быть в середине отверстие в держатель ткани.
- Стабилизация той части, где только мембрана удерживает плацента с мембраной силиконовые (диаметр 1 мм) или, альтернативно, две части парафином.
- Соберите полный держатель ткани, затяните винты и сократить нависающие ткани. Обратите внимание, что венозные и артериальные канюли не были зажаты, но вместо этого лежал в небольшой каналов держатель ткани.
- Поверните держатель ткани с ног на голову, положите его в перфузии камеры и добавить крышку. Теперь, с материнской стороны должны быть на самом верху. Проверка всегда если плода цепь цела и среды, вытекающей из плода трубы вену.
- Включите материнской насоса (12 мл / мин). Введем три тупой канюли (Ø 0,8 мм) в гоконец е материнской трубки в артерию межворсинчатом пространство, проникая децидуальными пластины. Для возврата перфузат к материнской цепи положил одну трубку, как венозная утечка, которая также связана с материнской насос в самое низкое положение в верхней части камеры перфузии.
- Подключите плода канюли вену плода трубку вены.
3. Выполнение пред-и экспериментальная фаза перфузии
- Чтобы разрешить ткани, чтобы оправиться от ишемического периода после родов и, чтобы избавиться от крови в межворсинчатом пространство, открытое предварительного этапа 20 мин необходимо. Это означает, что для матери и плода вены не ведут обратно в резервуар, содержащий артериальной перфузии среды. Соберите матери и плода венозного оттока в бутылку и выбросить его после предварительной фазе.
- Для оценки целостности перфузии выполнить другую предварительно этап 20 мин, но в замкнутом контуре. Используйте два отдельных резервуаров средней перфузиидля матери и плода схеме и закройте схем ведущими плода венозного оттока обратно в резервуар плода и материнской назад венозного оттока в материнской водохранилища.
- Для основного эксперимента перфузии подготовить две колбы с 120 мл перфузии среды (один для матери и один для плода водохранилища). Добавить меченого 14 С-антипирин (4 нКи / мл; служит в качестве положительного контроля; ВНИМАНИЕ: радиоактивные вещества) и флуоресцентно меченых ксенобиотиков или наночастицы, которые кто-то хочет проанализировать, в материнской водохранилища. Смешать материнской перфузат хорошо.
- Начать эксперимент по обмену чистой среды перфузии с двух подготовленных колб (матери и плода водохранилища). Закройте схем ведущими плода венозный отток обратно в резервуар плода и материнской назад венозного оттока в материнской водохранилища.
- Продолжить перфузии в течение 6 часов и регулярно брать пробы. Всегда ресуспендируйте среды в матери и плодаводохранилища до вывода.
- Управление давлением в плода артерии (не должна превышать 70 мм ртутного столба), рН в обоих контурах (должно быть в физиологическом диапазоне 7,2-7,4) и объем обоих резервуарах (потери плода объем не должен превышать 4 мл / час) в течение перфузии . При необходимости отрегулировать рН с использованием либо соляная кислота или гидроксид натрия.
- Если потеря объема в резервуаре плода превышает 4 мл / ч есть утечка в ткани, и нужно остановить перфузии. Успешность перфузии в течение 6 часов без утечки составляет около 15-20%.
- Остановите перфузии после 6 часов. Выверните насосы, водяная баня, обогреватели и потока газа.
- Удалить плаценты от держателя ткани, вырезать перфузируемом семядолей (ярче, чем unperfused ткани) и взвесить его.
- Отбор проб с unperfused (часть плаценты которая была сокращена в начале, может быть принято уже в ходе предварительного фазы) и перфузии тканей (каждая около 1 г) и хранить их при температуре -20 ° Cдо гомогенизации или в жидком азоте для последующего анализа. Фикс еще образец ткани в 4% формалине для гистологической оценки. Образцы должны включать в себя все слои плаценты.
- Очистка труб после перфузии последовательно промывку артериальной системы плода и материнской цепи с) в 200 мл дистиллированной воды, б) 50 мл 1% гидроксида натрия, в) 50 мл 1%-ной фосфорной кислоты и г) снова 200 мл дистиллированной воды (Расход: 15-20 мл / мин).
Всего рабочего Процедура эксперимента перфузии плаценты изображен на рисунке 3.
4. Анализ образцов
- Центрифуга перфузату образцов в течение 10 мин при 800 мкг до проведения анализа для удаления остаточных эритроцитов. Возьмите супернатанта для дальнейшего анализа. Образцы могут быть оставляли на ночь при 4 ° С. Для анализа лептина и ХГЧ производства образцы можно хранить при -20 ° С.
- Для оценки проницаемостиПлацента анализа 14 С-антипирин жидким сцинтилляционных. Смешать 300 мкл фетальной и материнской образцов с 3 мл сцинтилл ционной смеси и измерения в течение 5 мин в бета-счетчике.
- Для оценки переноса флуоресцентной наночастиц или ксенобиотиков интерес читать флуоресценции при возбуждении 485 нм и 528 нм эмиссия в микропланшет-ридера (указанные длины волн для анализа желто-зеленой меткой, которую мы использовали для наночастиц).
- Для определения жизнеспособности плацентарной перфузии тканей при мерой потребления глюкозы и лактата в матери и плода цепь с автоматизированной системой газового состава крови. Кроме того, оценки производства плацентарных гормонов choriongonadotropin человека (ХГЧ) и лептина в гомогенизированных образцов ткани и перфузаты путем твердофазного иммуноферментного анализа (ELISA).
Результаты
Фиг.4А показывает перфузии профилей из мелких частиц полистирола (80 нм), которые переносятся через плаценту по сравнению с большими частицы полистирола (500 нм), которые не были переданы в плода отсека. Каждая точка представляет собой среднюю концентрацию частиц в данный момент времени не менее 3 независимых экспериментов. Для наночастиц полистирола плацентарной передачи в зависимости от размера 19. Через 3 часа перфузии плаценты уже 20-30% от первоначально добавлены 80 нм частиц полистирола были переведены из материнского плода к цепи, в то время как 500 нм частиц полистирола, не указанным в схеме плода даже после 6 часов перфузии. Тем не менее, материнской концентрации 500 нм частиц уменьшается. Флуоресцентные изображения на гистологический срез ткани после перфузии показали, что эти частицы накапливаются в ворсинки плаценты (данные не показаны). Фиг.4В изображает характерный профиль перфузии меченного 14 С-антипирин. Antipyrine как небольшой липофильные молекулы распределены по плацентарный барьер с помощью пассивной диффузии и служит для управления целостности цепей. Через 4-6 часа перфузии равновесие между матери и плода антипирином концентрации должно быть построено 23. Чтобы оценить и сравнить скорость плацентарного транспорта ксенобиотиков плода к материнской концентрации препарата (F / M) соотношение обычно отображается (рис. 5).
Через анализ лактата и плацентарных гормонов (человеческий choriongonadotropin и лептин) производства, а также потребления глюкозы жизнеспособность и функциональность ткани плаценты во время перфузии можно контролировать (рис. 6). Значения для перфузии с ксенобиотиков всегда должны находиться в том же диапазоне, что и значения за управление без перфузии ксенобиотиков. Кроме того, histop athological оценки перфузии плацентарной ткани может быть выполнена. Сравнению с не-перфузии плацентарной ткани могли бы выявить патологические изменения, связанные с перфузии (например, бактериального загрязнения) и, следовательно, может служить еще одним параметром качества управления.
Дальнейшие результаты, полученные с представителем экс естественных условиях двойной рециркуляции плаценты человека модели перфузии Недавно были опубликованы 11,19.

Рисунок 1. Экс естественных плаценты человека перфузии настройки. 1) Водяная баня с матери и плода водоемов, 2) перфузии камеры, 3) пузырь ловушку, 4) оксигенатором колонны, и 5) проточный нагреватель.
load/50401/50401fig2.jpg "/>
Рисунок 2. Схематическое изображение экс естественных человеческих плацентарной перфузии модели FA: артерии плода; FV:. Вене плода; MA: материнской артерии, MV: материнские вены; BT: пузырь ловушку; PS: датчик давления
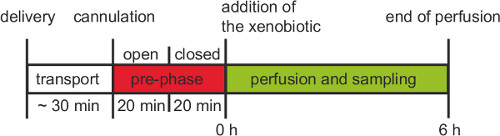
Рисунок 3. Порядок работы бывших естественных человеческих плацентарной перфузии эксперимента. После родов плацента должна быть канюли в течение 30 мин. До 6 часов экспериментальной фазе с рециркуляцией открытой предварительно фазы и закрытым предварительно фаза должна быть выполнена по крайней мере 20 минут каждый.

Рисунок 4. Перфузии профилей частицы полистирола и 14 </ Вир> C-антипирин 19. Перфузии профиль полистирола частиц по размерам 80 нм (п = 4) и 500 нм (п = 3). Первоначально 25 мкг / мл частиц и 4,2 нКи / мл 14 С-антипирин были добавлены к материнской цепи. Количество частиц (А) и 14 C-антипирин (B) были измерены в материнской (М, твердый символов) и плода (F, открытые символов) цепи после того, как указанные моменты времени. Отображаемые средняя концентрация ± SE. Нажмите здесь, чтобы увеличить рисунок .
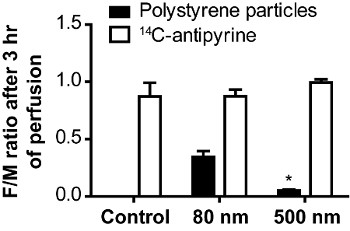
Рисунок 5. Размер-зависимой передачи частицы полистирола через плаценты человека 19. Соотношения между плода и матери концентрации 14 C-антипирин и полистирольные частицы известковоulated после 180 мин перфузии плаценты. Данные представляют собой среднее ± SE, по меньшей мере три независимых экспериментов. Колонка управления изображает перфузии без частиц, но с 14 C-антипирина. (* Р <0,05 по сравнению с 80 значение соотношения нм).

Рисунок 6. Жизнеспособность плацентарной перфузии тканей при 19. (A) Потребление глюкозы и лактата в перфузии плаценты. Отображается представляет собой сумму изменений в общем содержании в схемах (матери и плода) с течением времени, деленный на вес перфузии семядоли. (B) Нормализованный чистых производственных (NP деленное на начальное содержание ткани Т0) из плацентарных гормонов человека и choriongonadotropin лептин. Данные представляют собой среднее ± SE, по крайней Lвосток 3 независимых экспериментов.
Обсуждение
Под двойной рециркуляции перфузии показали здесь, есть несколько других экспериментальных конфигурациях возможны в зависимости от вопроса, который должен быть дан ответ. Особенно плацентарной перфузии открытым обычно используются для оценки клиренс лекарственного средства в стационарном состоянии концентрации 3. Рециркуляции перфузии настройки может также применяться для подтверждения активного транспорта эндогенных или экзогенных веществ. При таком подходе той же концентрации ксенобиотиков должен быть добавлен к материнской и фетальной циркуляции. Предполагается, что существует активный транспорт против градиента концентрации, накопление исследуемого вещества в любом из обоих контурах может наблюдаться 24. Следует отметить, что добавление испытуемого вещества только фетальный схема также возможна и может раскрыть механизм транспорта через плаценту этого вещества 25.
Протокол развивалась на протяжении Тиме и может варьироваться между различными исследовательскими группами особенно в отношении расхода, состав перфузии среды формы кислорода и нагрева 26,27. Особенно скорости потока может влиять на время, в которое трансплацентарно передача происходит. Чтобы управлять этим, добавление пассивно транспортируется эталонное соединение как антипирин имеет важное значение. Скорость передачи ксенобиотиков всегда может быть по сравнению с скоростью передачи антипирин (F / M соотношение должно быть выше 0,75) 26. Поскольку передача антипирин в основном ограничивается потоком и поверхностью теплообмена, это сравнение имеет различия в потоке и размер перфузии семядоли учетом которого может изменяться между экспериментами. Кроме того, FITC-декстрана, могут быть включены в цепь фетального служить в качестве контроля для целостности барьера 26. Плод потери объема также используется в качестве маркера для целостности барьера. Обычно потеря плода жидкость до 4 мл / ч допускается 28, ноRe не существует общепринятого предела.
Очевидно, есть некоторые недостатки бывших естественных условиях плаценты человека методом перфузии, как между индивидуальными вариациями и низкий уровень успеха (15-20%). Кроме того, перфузии течение 6 часов не может моделировать хронического медикаментозного лечения и, следовательно, не может полностью исключить передачу ксенобиотиков после длительного воздействия. Другим ограничением модели является то, что главным образом трансплацентарным передачи в срок оценивается в то время как скорость транспорта на ранних сроках беременности, когда барьер толще, остается до сих пор неизвестным. В самом деле, первая перфузии плаценты триместре возможно, но наличие этих плаценты весьма ограничен. Тем не менее, до сих пор бывших естественных условиях плацентарной перфузии методом является единственной моделью для изучения транспорта различных ксенобиотиков или наночастиц в организованной ткани плаценты человека. Хотя токсикодинамики в бывших естественных условиях модель человеческого перфузии может быть проанализирована только в PLacental ткани, эксперименты на животных действительно может обеспечить также информация о эмбриотоксичности. Хотя, из-за анатомических различий через плацентарный барьер между людьми и грызунов эти результаты не могут быть экстраполированы на людей 4,5. Другая возможность исследовать трансплацентарно передача может быть культура клеток первичной модели, как цитотропобластов, линии хориокарциномой клетки, изолированные мембранных везикул плазмы или плацентарной ткани эксплантов 29. Наиболее часто используемые модели линии BeWo клетки, эти клетки получают из злокачественной гестационный хориокарциномой и могут образовывать монослой на мембрану, так что транспортное исследования может быть выполнена. Результаты исследований транспорта с использованием модели BeWo клетки хорошо коррелируют с результатами, полученными в исключая виво плаценты человека перфузии 30. Однако, чтобы изучать детали транспорта лекарства (например, вклад конкретного транспортного белка) и обмен веществ, модель BeWo клетка может быть мруды возможным в первую очередь потому, что это проще в обращении и возможности для манипуляций, как выражение генетически измененных транспортеры или ферментов, но в отношении общих исследований передаче наркотиков надежность этой модели ограничена. Это испытывает недостаток в кровоток и целостность монослоя должен быть оценен тщательно, поскольку она зависит от нескольких факторов, таких как условия культуры клеток, посев плотность, продолжительность воздействия и мембрана вставки 6,29.
Различные ксенобиотиков, а также наночастицы связываются с различными белками плазмы, которые могут существенно влиять на трансплацентарным передачи 31; рассмотрении связывание с белками плазмы является важным. Перфузии среда содержит бычий сывороточный альбумин, наиболее часто белками плазмы. В последнее время исследования показали, что коэффициент передачи различных веществ, полученных с экс естественных человеческих плацентарной перфузии модель хорошо коррелируют с пуповинной крови в естественных условиях материнскойсоотношения концентраций кровь, когда коэффициент передачи были скорректированы в зависимости от степени связывания с белками плазмы 12.
В целом, экс естественных условиях плацентарной перфузии модели является действительным и надежным способом для изучения транспорта через плаценты человека и прогнозировать в естественных условиях плаценту ксенобиотиков и наночастиц.
Раскрытие информации
Авторы заявляют, что у них нет конкурирующих финансовых интересов.
Благодарности
Эта работа осуществляется при финансовой поддержке Швейцарского национального фонда (NRP 64 программы, грант № 4064-131232).
Материалы
| Name | Company | Catalog Number | Comments |
| NCTC-135 medium | ICN Biomedicals, Inc. | 10-911-22C | could be replaced by Medium 199 from Sigma (M3769) |
| Sodium chloride (NaCl) | Sigma-Aldrich, Fluka | 71381 | |
| Potassium chloride (KCl) | Hospital pharmacy | also possible: Sigma (P9541) | |
| Monosodium phosphate (NaH2PO4 · H2O) | Merck | 106346 | |
| Magnesium sulfate (MgSO4 · H2O) | Sigma-Aldrich, Fluka | 63139 | |
| Calcium chloride (CaCl, anhydrous) | Merck | 102388 | |
| D(+) Glucose (anhydrous) | Sigma-Aldrich, Fluka | 49138 | |
| Sodium bicarbonate (NaHCO3) | Merck | 106329 | |
| Dextran from Leuconostoc spp. | Sigma-Aldrich | 31389 | |
| Bovine serum albumin (BSA) | Applichem | A1391 | |
| Amoxicilline (Clamoxyl) | GlaxoSmithKline AG | 2021101A | |
| Sodium heparin | B. Braun Medical AG | 3511014 | |
| Sodium hydoxide (NaOH) pellets | Merck | 106498 | CAUTION: corrosive |
| Ortho-phosphoric acid 85% (H3PO4) | Merck | 100573 | CAUTION: corrosive |
| Maternal gas mixture: 95% synthetic air, 5% CO2 | PanGas AG | ||
| Fetal gas mixture: 95% N2, 5% CO2 | PanGas AG | ||
| Antipyrine (N-methyl-14C) | American Radiolabeled Chemicals, Inc. | ARC 0108-50 μCi | CAUTION: radioactive material (specific activity: 55mCi/mmol) |
| Scintillation cocktail (IrgaSafe Plus) | Zinsser Analytic GmbH | 1003100 | |
| Polystyrene particles 80 nm | Polyscience, Inc. | 17150 | |
| Polystyrene particles 500 nm | Polyscience, Inc. | 17152 | |
| EQUIPMENT | |||
| Water bath | VWR | 462-7001 | |
| Thermostat | IKA-Werke GmbH Co. KG | 3164000 | |
| Peristaltic pumps | Ismatec | ISM 833 | |
| Bubble traps (glass) | UNI-GLAS Laborbedarf | ||
| Flow heater | UNI-GLAS Laborbedarf | ||
| Pressure sensor + Software for analyses | MSR Electronics GmbH | 145B5 | |
| Notebook | Hewlett Packard | ||
| Miniature gas exchange oxygenator | Living Systems Instrumentation | LSI-OXR | |
| Tygon Tube (ID: 1.6 mm; OD: 4.8 mm) | Ismatec | MF0028 | |
| Tubes for pumps (PharMed BPT; ID: 1.52 mm) | Ismatec | SC0744 | |
| Blunt cannulae ( 0.8 mm) | Polymed Medical Center | 03.592.81 | |
| Blunt cannulae ( 1.2 mm) | Polymed Medical Center | 03.592.90 | |
| Blunt cannulae ( 1.5 mm) | Polymed Medical Center | 03.592.94 | |
| Blunt cannulae ( 1.8 mm) | Polymed Medical Center | 03.952.82 | |
| Parafilm | VWR | 291-1212 | |
| Perfusion chamber with tissue holder (plexiglass) | Internal technical department | Similar equipment is available from Hemotek Limited, UK | |
| Surgical suture material (PremiCron) | B. Braun Medical AG | C0026005 | |
| Winged Needle Infusion Set (21G Butterfly) | Hospira, Inc. | ASN 2102 | |
| Multidirectional stopcock (Discofix C-3) | B. Braun Medical AG | 16494C | |
| Surgical scissors | B. Braun Medical AG | BC304R | |
| Dissecting scissors | B. Braun Medical AG | BC162R | |
| Needle holder | B. Braun Medical AG | BM200R | |
| Dissecting forceps | B. Braun Medical AG | BD215R | |
| Automated blood gas system | Radiometer Medical ApS | ABL800 FLEX | |
| Multi-mode microplate reader | BioTek | Synergy HT | |
| Liquid scintillation analyzer | GMI, Inc. | Packard Tri-Carb 2200 | |
| Scintillation tubes 5.5 ml | Zinsser Analytic GmbH | 3020001 | |
| Tissue Homogenizer | OMNI, Inc. | TH-220 | |
| pH meter + electrode | VWR | 662-2779 | |
Ссылки
- Ala-Kokko, T. I., Myllynen, P., Vahakangas, K. Ex vivo perfusion of the human placental cotyledon: implications for anesthetic pharmacology. Int. J. Obstet. Anesth. 9, 26-38 (2000).
- Panigel, M., Pascaud, M., Brun, J. L. Radioangiographic study of circulation in the villi and intervillous space of isolated human placental cotyledon kept viable by perfusion. J. Physiol. (Paris). 59, 277 (1967).
- Schneider, H., Panigel, M., Dancis, J. Transfer across the perfused human placenta of antipyrine, sodium and leucine. Am. J. Obstet. Gynecol. 114, 822-828 (1972).
- Enders, A. C., Blankenship, T. N. Comparative placental structure. Adv. Drug Deliv. Rev. 38, 3-15 (1999).
- Takata, K., Hirano, H. Mechanism of glucose transport across the human and rat placental barrier: a review. Microsc. Res. Tech. 38, 145-152 (1997).
- Saunders, M. Transplacental transport of nanomaterials. Wiley Interdiscip. Rev. Nanomed. Nanobiotechnol. 1, 671-684 (2009).
- Buerki-Thurnherr, T., von Mandach, U., Wick, P. Knocking at the door of the unborn child: engineered nanoparticles at the human placental barrier. Swiss Med. Wkly. 142, w13559 (2012).
- Gendron, M. P., Martin, B., Oraichi, D., Berard, A. Health care providers' requests to Teratogen Information Services on medication use during pregnancy and lactation. Eur. J. Clin. Pharmacol. 65, 523-531 (2009).
- Burns, L., Mattick, R. P., Lim, K., Wallace, C. Methadone in pregnancy: treatment retention and neonatal outcomes. Addiction. 102, 264-270 (2007).
- von Mandach, U. Drug use in pregnancy. Ther. Umsch. 62, 29-35 (2005).
- Malek, A., Obrist, C., Wenzinger, S., von Mandach, U. The impact of cocaine and heroin on the placental transfer of methadone. Reprod. Biol. Endocrinol. 7, 61 (2009).
- Hutson, J. R., Garcia-Bournissen, F., Davis, A., Koren, G. The human placental perfusion model: a systematic review and development of a model to predict in vivo transfer of therapeutic drugs. Clin. Pharmacol. Ther. 90, 67-76 (2011).
- International Organization for Standardization (ISO). Technical Specification (ISO/TS) 27687. Nanotechnologies – Terminology and definitions for nano-objects – Nanoparticles, nanofibre and nanoplate. , (2008).
- Pietroiusti, A. Health implications of engineered nanomaterials. Nanoscale. 4, 1231-1247 (2012).
- Latzin, P., Roosli, M., Huss, A., Kuehni, C. E., Frey, U. Air pollution during pregnancy and lung function in newborns: a birth cohort study. Eur. Respir. J. 33, 594-603 (2009).
- Lacasana, M., Esplugues, A., Ballester, F. Exposure to ambient air pollution and prenatal and early childhood health effects. Eur. J. Epidemiol. 20, 183-199 (2005).
- Menezes, V., Malek, A., Keelan, J. A. Nanoparticulate drug delivery in pregnancy: placental passage and fetal exposure. Curr. Pharm. Biotechnol. 12, 731-742 (2011).
- Muhlemann, K., Menegus, M. A., Miller, R. K. Cytomegalovirus in the perfused human term placenta in vitro. Placenta. 16, 367-373 (1995).
- Wick, P., et al. Barrier capacity of human placenta for nanosized materials. Environ. Health Perspect. 118, 432-436 (2010).
- Dancis, J. Why perfuse the human placenta. Contrib Gynecol. Obstet. 13, 1-4 (1985).
- May, K., et al. Perfusion of human placenta with hemoglobin introduces preeclampsia-like injuries that are prevented by alpha1-microglobulin. Placenta. 32, 323-332 (2011).
- Guller, S., et al. Protein composition of microparticles shed from human placenta during placental perfusion: Potential role in angiogenesis and fibrinolysis in preeclampsia. Placenta. 32, 63-69 (2011).
- Challier, J. C. Criteria for evaluating perfusion experiments and presentation of results. Contrib. Gynecol. Obstet. 13, 32-39 (1985).
- Kraemer, J., Klein, J., Lubetsky, A., Koren, G. Perfusion studies of glyburide transfer across the human placenta: implications for fetal safety. Am. J. Obstet. Gynecol. 195, 270-274 (2006).
- leal, J. K., et al. Modification of fetal plasma amino acid composition by placental amino acid exchangers in vitro. J. Physiol. 582, 871-882 (2007).
- athiesen, L., et al. Quality assessment of a placental perfusion protocol. Reprod. Toxicol. 30, 138-146 (2010).
- Myllynen, P., et al. Preliminary interlaboratory comparison of the ex vivo dual human placental perfusion system. Reprod Toxicol. 30, 94-102 (2010).
- Malek, A., Sager, R., Schneider, H. Maternal-fetal transport of immunoglobulin G and its subclasses during the third trimester of human pregnancy. Am. J. Reprod. Immunol. 32, 8-14 (1994).
- Prouillac, C., Lecoeur, S. The role of the placenta in fetal exposure to xenobiotics: importance of membrane transporters and human models for transfer studies. Drug Metab. Dispos. 38, 1623-1635 (2010).
- Poulsen, M. S., Rytting, E., Mose, T., Knudsen, L. E. Modeling placental transport: correlation of in vitro BeWo cell permeability and ex vivo human placental perfusion. Toxicol. In Vitro. 23, 1380-1386 (2009).
- Mathiesen, L., Rytting, E., Mose, T., Knudsen, L. E. Transport of benzo[alpha]pyrene in the dually perfused human placenta perfusion model: effect of albumin in the perfusion medium. Basic Clin. Pharmacol. Toxicol. 105, 181-187 (2009).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены