Method Article
태반의 맞은 편에 생체이 물과 나노 물질의 전송 속도의 결정을 사용하여
요약
생체 이중 순환 태반 관류 모델은 인간의 태반을 통해 생체 이물질 및 나노 입자의 이동을 조사하는 데 사용할 수 있습니다. 이 비디오 프로토콜에서 우리는 장비와 태반 관류의 성공적인 수행에 필요한 기술을 설명합니다.
초록
인간의 태반 수십 년 전에이 어머니와 태아 사이에 꿰 뚫을 수없는 장벽이 될 것으로 생각되었다. 그러나 탈리도마이드에 의한 기형아 많은 나중에 연구의 발견은 나중에 반대를 증명했다. 오늘 니코틴 등 여러 가지 유해 생체이는, 헤로인, 메타돈 또는 약물뿐만 아니라 환경 오염 물질이 장벽을 극복하기 위해 설명 하였다. 나노 기술의 사용 증가와 함께, 태반는 실수로 노출을 통해 또는 의도적으로 잠재적 인 나노 메디칼 응용 프로그램의 경우 새로운 나노 입자와 접촉 할 가능성이 높습니다. 태반 대부분의 종 특정 포유류 기관 1이기 때문에 동물 실험의 데이터가 인간에게 추정 할 수 없습니다. 따라서 Panigel 등에 의해 개발 된 생체 이중 순환 태반 관류. 1,967 2 지속적 슈나이더 등으로 수정했습니다. 1,972 3, 우수한 모델 T와 같은 역할을 할 수생체이 또는 입자의 이동을 연구 O를.
여기, 우리는 재현 가능한 결과를 얻기 위해 인간의 태반 관류 프로토콜과 발전을 순환 생체 이중에 초점을 맞 춥니 다.
태반은 제왕 절개 배달을받은 단순한 용어 임신에서 산모의 동의 이후 하였다. 그대로 자엽의 태아와 산모의 배는 적어도 5 시간 유관 및 관류 하였다. 모델 입자로 80 사이즈 직경 500 nm의와 찬란 폴리스티렌 입자는 어머니의 회로에 추가되었습니다. 80 nm의 입자는 태반 장벽을 통과하고 500 nm의 입자가 태반 조직이나 산모의 회로에서 유지하는 동안 태아에게 태반을 통해 전송되는 물질에 대한 완벽한 예제를 제공 할 수 있었다. 생체 인간의 태반 관류 모델에 대한 신뢰할 수있는 정보를 제공하는 몇 가지 모델 중 하나입니다예측 및 임상 관련 데이터를 제공하는 중요한 조직 장벽의 생체 이물의 전송 동작.
서문
태반은 산소, 이산화탄소, 영양분과 노폐물과 어머니와 서로 분리 성장 태아의 두 혈액 회로를 유지할 수 동시에 교환을 담당하는 복잡한 기관이다. 또한, 그것은 산모의 면역 시스템에 의해 아이의 거부를 방지하고 임신을 유지하는 호르몬을 분비. 세포 장벽 4,5 측면 세포막없이 진정한 syncytium 퓨즈 및 양식 cytotrophoblast 세포에 의해 형성된다. 전체 태반은 하나의 태아 융모 트리를 포함하고 태반의 하나의 기능 단위를 나타내는 여러 자엽,로 구성되어 있습니다.
태반 장벽 기능의 연구는 1960 년대 탈리도마이드 유도 기형의 발견과 강화되었다. 분명한 이유를 들어 임산부 전위 연구는 수행 할 수 없습니다. 따라서, 다양한 대안 모델을 6,7를 개발되었습니다 까지. 가장 유망한 그리고 아마도 대부분의 임상 관련 모델 Panigel 및 동료 2,3에 의해 개발 된 생체 인간의 태반 관류 모델입니다.
많은 여성들은 이러한 자신의 임신 8 중 마약이나 환경 오염과 같은 다른 생체 이물질에 노출되어 있습니다. 이미 임신 중에 정기적으로 투여 된 마약의 경우, 생체 내 연구에서 제대혈의 그것과 산모의 혈중 농도를 비교하여 수행 할 수 있습니다. 그러나 일반적으로 태아 및 이들 물질의 기형에 약물 동력학 및 역학에 대한 제한된 정보가있다.
헤로인은 쉽게 태반 장벽을 통과하고 자궁 내 성장 제한, 조산이나 자연 유산 9,10으로 이어질 수있는 것처럼 예를 들어 약물. 따라서 임신 중에 실종 금욕의 경우 메타돈과 대체 요법이 권장됩니다. 전생체 인간의 태반 관류 모델은 태아 순환에 메타돈의 전송이 배달 12 후 계산 된 제대혈에 산모의 혈액 농도 비율과 잘 상관 관계를 무시할 11이라고 밝혔다.
나노 기술, 특히 의학의 성장 분야이다. 그래서 자연적으로 잘 발생 (직경 <2.5 μm의)와 산불, 화산 폭발의 연기와 사막의 먼지 미세 입자 (직경 <0.1 μm의), 나노 물질의 노출 (최소 하나의 차원 <0.1 μm의 13 아래 ) 증가하고있다. 이 나노 물질의 독성 가능성에 대한 질문을 제기했다. 어떤 사람의 위험은 아직 입증되지 수 있지만, 설계 나노 입자는 독성 결과 14로 이어지는 부작용 생물학적 반응을 일으킬 수 있음을 나타내는 주요 실험 연구가있다. 최근 일부 연구에 그 태아 노출 표시대기 오염은 신생아 및 어린이 15,16에서 더 높은 호흡 필요와기도 염증에 연결되어 있습니다. 또한, 작은 나노 입자는 특히 태아 나 어머니 중 하나를 치료하는 약물 캐리어로 사용할 수 있습니다. 따라서, 서로 다른 생체 이물질이나 나노 물질과 태반 장벽을 통과 할 수있는 능력의 광범위한 연구가 필요하다는 분명해진다. 나노 물질에 태반 투과성의 현재 연구의 실제 개요 메네 제스 등으로 요약되어 있습니다. 2,011 17 Buerki-Thurnherr 등이. 2,012 7.
인간의 태반 관류 모델을 순환 생체 이중에 대한 책임 메커니즘 등 다양한 내인성 및 외인성 화합물 3,11,12,18,19의 태반 전송 및 태반의 다른 기능의 넓은 범위를 공부 통제하고 안정적인 시스템을 제공 자간전증과 같은 병적 상태의 개발 <> 20-22을 먹다. 축적 효과와 생체 이물질이나 나노 입자의 광범위한 세트의 전위 비율의 연구를 수 있도록이 프로토콜에서 우리는 세트에 주로 최대 초점, 취급 및 방법.
프로토콜
1. 관류 시스템 준비
- 물 목욕, 재관류 챔버, 산소에 대한 두 개의 열, 두 개의 연동 펌프, 두 개의 버블 트랩, 두 개의 흐름 히터와 하나의 압력 센서 (그림 1)으로 구성된 관류 시스템을 설정합니다. 그림 2의 방식에 따라 실리콘 및 폴리 염화 비닐 재료로 구성된 튜브 섹션에서 이러한 구성 요소를 연결합니다. 마지막으로 각각 태아와 산모 회로를 나타내는 두 개의 회로가있다.
- 물 목욕, 흐름 히터 및 재관류 챔버 가열을 켭니다. 온도는 37 ° C.이어야한다
- (NCTC-135 조직 문화 매체 얼의 버퍼 (6.8 g / L 염화나트륨 0.4 g / L 칼륨 염화물, 0.14 g / L 글루타민산 소다 인산염, 0.2 g / L 황산 마그네슘 0.2 g과 1:2 희석 살포 매체를 워밍업 / L 칼슘 염화물, 2g / L 포도당) 포도당 이하 (1 g / L), 덱스 트란 40 (10 G / L), 소 혈청 알부민 (10g로 보충/ L), 나트륨 헤파린 (2,500 IU / L), amoxicilline (250 ㎎ / L)와 중탄산 나트륨 (2.2 g / L)의 물을 욕조에 산도 7.4).
- - 20 ML 15 연속 다시 증류수 200 mL (유량) 200 mL를 증류수로 태아와 산모 회로의 동맥 시스템, B) 50 ML 1 % 수산화 나트륨, C) 1 % 인산 D)를 씻어 / 분).
- 태아의 정맥에 연결합니다 (Ø 1.2 mm, 무딘 바늘 수정 된 날개 달린 바늘 주입 세트에 연결해야합니다) 태아 동맥 튜빙.
- 모든 튜브 매체 (: 15-20 ML / 분 유량)를 포함 할 때까지 관류 매체와 태아와 산모 회로의 동맥 시스템을 씻어. 이 단계에서 버블 트랩을 작성하고 트랩의 거품 스트림을 제거합니다. 그런 다음 펌프를 중지합니다. 그것은 심성 동맥 튜브는 항상 거품이 없는지 정말 중요합니다, 그렇지 않으면 도관졌다가 특히 좋은 태아 혈관이 파열 할 수 있습니다.
- 가스 흐름을 켭니다. 산모의 회로는 위스콘신에 산소 공급일 5 % 이산화탄소와 5 % 이산화탄소와 95 %의 질소와 95 %의 합성 공기와 태아 회로.
- 압력 센서의 기록을 시작합니다.
2. 태반을 Cannulating
- 기본 제왕 절개 후 단순한 용어 임신에서 그대로 태반을 구하십시오. 서면 동의는 납품의 앞에 어머니에 의해 (우리의 연구의 경우에서 얻어진) 부여되어야하며 연구 (우리의 연구의 경우 WAS) 지역 윤리위원회의 승인을 받아야합니다. 먼저 시각적 컨트롤은 건강하고 그대로 태반을 보장하기 위해 조산사에 의해 수행되어야한다.
- 태반의 도관은 중요한 단계입니다! 재관류시 조직의 모든 작은 혼란은 임산부와 태아 순환 사이의 누수가 발생할 수 있습니다. 태반은 출산 후 30 분 이내에 얻을 수있다.
- 산모의 측면에서 볼 차질없이 태반의 한계 영역에서 그대로 떡잎을 선택합니다. 융모 판에,제대 동맥 수술 봉합사를 사용하여 나중에 도관 측 (탯줄을 향해) 상류 정맥을 모두 연결 지점을 묶어. 항상 두 개의 매듭을 만든다.
- 먼저 태아 동맥 Cannulate. 태아 태반 동맥은 항상 정맥보다 작고 얇은입니다.
- 태아 동맥 주위 봉합을하지만, 즉시 묶어하지 않습니다. 집게와 배를 잡고 조심스럽게 혈관을 잘라 동맥에 작은 정맥 (Ø 1.2 mm)를 넣습니다. 다음 봉합 (2 개 매듭)를 묶어.
- 같은 방법으로 태아의 정맥을 진행하지만 더 큰 정맥을 사용 (Ø 1.5-1.8 mm, 무딘 바늘 수정 된 날개 달린 바늘 주입 세트에 연결해야합니다.)에게
- 태아 펌프 (2 ㎖ / 분)를 켭니다. 거기에 눈에 띄는 누수가없고 혈액이 태아의 정맥 정맥에서 발산하는 경우, 천천히 4 ML / 분까지의 흐름을 증가시킵니다. 태아 동맥의 압력을 관찰, 그것은 70 mmHg로를 초과하지 않아야합니다. 태아 또는 동료에 액체가 새어 경우rnal 정맥는 다른 봉합사를 고정합니다.
- 태아면 조직 홀더 태반을 놓고 스파이크를 통해 태반 막과 조직을 당겨. 결국 관류 떡잎은 조직 홀더의 구멍의 중간에 있어야합니다.
- 단지 막 실리콘 막 (Ø 1mm) 또는 양자 택일로 두 파라 필름 (parafilm) 조각과 태반을 보유하고있는 부분을 안정.
- 전체 조직 홀더를 조립 나사를 조여 걸쳐 조직을 잘라. 정맥 및 동맥 캐 뉼러가 눌리지 않았는지주의 대신 조직 홀더의 작은 채널에 누워하시기 바랍니다.
- 거꾸로 조직 홀더를 돌려 재관류 챔버에 넣고 덮개를 추가합니다. 이제, 산모 측 상단에 있어야합니다. 태아 회로 그대로이고 매체가 태아 정맥 튜브로 흐르는 경우 항상 확인합니다.
- 임산부 펌프 (12 ML / 분)를 켭니다. 일에 세 무뚝뚝한 캐 뉼러 (Ø 0.8 mm)를 소개탈락 판을 관통하여 intervillous 공간으로 모체 동맥 튜브의 전자 끝. 임산부 회로에 관류을 반환하면 재관류 챔버의 상부에 가장 낮은 위치에 산모 펌프와 연결되어 정맥 배수로서 하나의 튜브를 넣어.
- 태아 정맥 튜브에 태아 정맥 정맥을 연결합니다.
3. 관류의 사전 및 실험 단계를 실행
- 조직이 배달 후 허혈 기간에서 복구하고 intervillous 공간에 혈액을 밖으로 플러시 수 있도록, 20 분 전 단계 개방이 필요합니다. 임산부와 태아의 정맥을 의미 관류 매체를 포함 동맥 저수지로 이어지는되지 않습니다. 병에 태아와 산모의 정맥 유출을 수집하고 사전 단계 후 폐기합니다.
- 관류의 무결성을 평가하는 것은 20 분의 또 다른 사전 단계를 수행하지만, 폐쇄 회로한다. 관류 중간에 두 개의 별도의 공기통을 사용하여태아와 산모 회로와 태아 저수지와 산모 저수지 산모의 정맥 유출 뒤 다시 태아의 정맥 유출을 선도하여 회로를 닫습니다.
- 주요 관류 실험 120 ML 관류 매체 (임산부를위한 하나 태아 저수지 하나) 두 개의 플라스크를 준비합니다. 하나는 산모의 저수지에 분석하고자하는 찬란 생체 이물 또는 나노 입자 (방사성 물질; 긍정적 인 제어 역할을주의 4 NCI / ㎖)이 방사성 동위 원소 14 C-antipyrine을 추가합니다. 또한 산모의 관류를 섞는다.
- 두 준비한 플라스크 (태아와 산모 저수지)와 함께 순수 관류 매체를 교환하여 실험을 시작합니다. 태아 저수지 태아의 정맥 유출 뒤와 산모 저수지 산모의 정맥 유출 백을 선도하여 회로를 닫습니다.
- 6 시간 동안 재관류를 계속하고 정기적으로 샘플을 채취. 항상 태아와 산모의 매체를 resuspend을탈퇴하기 전에 저수지.
- 관류 동안 태아의 동맥 (70 mmHg로를 초과하지 않아야), 두 회로의 산도 (생리적 범위 7.2-7.4에 있어야) 및 저수지의 음량 (태아 볼륨 손실이 4 ML / 시간을 초과하지 않아야한다)의 압력을 조절 . 필요하다면 염산 또는 수산화 나트륨을 사용하여 산도 값을 조정합니다.
- 태아 저수지에서 볼륨 손실이 4을 초과 할 경우 ML / HR이 조직에 누수 하나는 살포를 중지 할 수 있습니다. 누출없이 6 시간 동안 재관류 성공률은 15-20 %이다.
- 6 시간 후 재관류를 중지합니다. 펌프, 수조, 흐름 히터 및 가스 흐름을 켭니다.
- 조직 홀더에서 태반을 제거, 관류 떡잎을 잘라 (unperfused 조직보다 밝게)와 무게.
- unperfused (처음에 삭감 된 태반의 일부, 이미 전 단계에서 수행 될 수 있었다)에서 샘플을 채취하고 관류 조직 (각 약 1 g) 및 -20 ° C에서 보관균질화까지 이상 분석을위한 액체 질소합니다. 조직 병리학 적 평가를 위해 포르말린 4 %에서 다른 조직 샘플을 수정합니다. 샘플은 태반의 모든 레이어를 포함해야합니다.
- ) 연속적) 200 mL를 증류수로 B를 태아와 산모 회로의 동맥 시스템을 세척하여 50 ML 1 % 수산화 나트륨, C)을 다시 50 ML 1 % 인산 d)에 증류수 200 mL를 관류 한 후 튜브를 청소 (유량 : 15-20 ML / 분).
태반 관류 실험의 전체 작업 과정은 그림 3에 묘사되어있다.
4. 샘플 분석
- 잔류 적혈구를 제거하기 위해 분석 전에 800 XG에서 10 분 동안 관류 샘플을 원심 분리기. 추가 분석을 위해 상층 액을 가져 가라. 샘플은 4 ℃에서 하룻밤 남아있을 수 있습니다 렙틴과 hCG의 생산의 분석을위한 시료는 -20 ° C.에 저장할 수 있습니다
- 의 투과성을 평가하기 위해태반은 액체 섬광에 의해 C-antipyrine 14 분석합니다. 베타 카운터 5 분 3 ML의 섬광 칵테일과 측정으로 태아와 산모의 시료 300 μl를 섞는다.
- 형광 나노 입자의 양도 또는 관심의 생체 이물이 마이크로 리더 (표시된 파장은 우리가 나노 입자에 사용되는 노란색 녹색 라벨의 분석 용)의 485 nm의 여기 및 528 nm의 방출에 형광을 읽으을 평가합니다.
- 관류 측정시 태반 조직의 포도당 소비와 자동 혈액 가스 시스템과 태아와 산모의 회로에서 젖산 생산의 가능성을 확인하십시오. 또한, 태반 호르몬 인간 choriongonadotropin (hCG를) 효소 결합 면역 분석 (ELISA)에 의한 균질 조직 샘플 및 관류 렙틴의 생산을 평가합니다.
결과
그림 4A는 태아의 구획에 전송되지 않은 큰 폴리스티렌 입자 (500 NM)에 비해 태반을 통해 전송 된 작은 폴리스티렌 입자 (80 nm의)의 재관류 프로파일을 보여줍니다. 각 데이터 포인트는 최소 3 독립적 인 실험의 주어진 시점까지의 평균 입자 농도를 나타냅니다. 폴리스티렌 태반 전송 사이즈에 따라 19입니다 나노 입자. 500 nm의 폴리스티렌 입자도 재관류 6 시간 후 태아의 회로에서 나타나지 않는 동안 태반 관류 3 시간 후에는 이미 처음에 추가 된 80 nm의 폴리스티렌 입자의 20 ~ 30 %는 태아 회로에 모체로부터 전송했습니다. 그럼에도 불구하고, 500 nm의 입자의 어머니의 농도가 감소된다. 재관류 후 조직의 조직 학적 부분에 형광 이미지는이 입자가 태반 (데이터 표시되지 않음)의 융모에 축적 것으로 나타났다. 그림 4b 방사성 동위 원소 14 C-antipyrine의 특성 관류 프로필을 보여줍니다. 작은 친 유성 분자로 Antipyrine는 수동적 인 확산을 통해 태반 장벽을 통해 배포 회로의 무결성에 대한 제어 역할을합니다. 관류 4-6 시간 후 태아와 산모 antipyrine의 농도와 평형 23를 구축해야한다. 태아에 산모 약물 농도 (F / M) 비율은 보통 표시됩니다 (그림 5) 생체 이물의 태반 전송 속도를 평가하고 비교합니다.
젖산 및 태반 호르몬 (인간 choriongonadotropin과 렙틴) 생산뿐만 아니라 포도당 소비의 분석을 통해 관류시 태반 조직의 생존과 기능은 (그림 6) 모니터링 할 수 있습니다. 생체이 물에 perfusions의 값은 항상 제어 관류에서 생체이없이 값과 동일한 범위에 있어야합니다. 또한, histop 관류 태반 조직의 athological 평가를 수행 할 수 있습니다. 비 관류 태반 조직과 비교 한 후 관류 (예 : 세균 오염)에 의한 병리학 적 변화를 공개 할 수 있으므로 다른 품질 관리 매개 변수로 제공 할 수 있습니다.
생체 이중 순환 태반 관류 모델로 얻은 또한 대표적인 결과는 최근 11,19 출판되었다.

그림 1. 생체 인간의 태반 관류 셋업. 1) 물 산모와 태아 저수지 목욕, 2) 재관류 챔버, 3) 버블 트랩, 4) 산소 공급기 열 및 5) 흐름 히터.
load/50401/50401fig2.jpg "/>
그림 2. 생체 인간의 태반 관류 모델의 개략도 FA : 태아 동맥, FV :. 태아 정맥, MA : 모체 동맥, MV : 산모의 정맥, BT : 버블 트랩, PS : 압력 센서
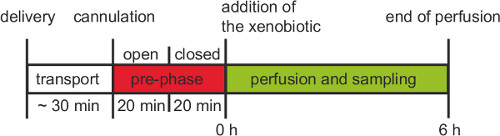
그림 3. 생체 인간의 태반 관류 실험의 절차를 작동합니다. 도착 후 태반이 30 분 내에 유관해야합니다. 재순환 6 시간 실험 단계 전에 오픈 사전 단계 및 폐쇄 전 단계는 적어도 20 분 각각에 대해 수행해야합니다.

그림 4. 폴리스티렌 입자 (14)의 관류 프로필 </> C-antipyrine 19을 먹다. 관류 크기의 폴리스티렌 입자의 프로필 80 나노 (n은 = 4)와 500 nm의 (n = 3). 처음에 25 ㎍ / ㎖ 입자와 4.2 NCI / ML 14 C-antipyrine는 산모의 회로에 추가되었습니다. 입자의 양 (A), 14 C-antipyrine (B)는 지정된 시점 이후 (F, 오픈 기호) 임산부 (M, 고체 기호)와 태아의 회로에서 측정 하였다. 평균 농도가 표시 ± SE. 큰 그림을 보려면 여기를 클릭하십시오 .
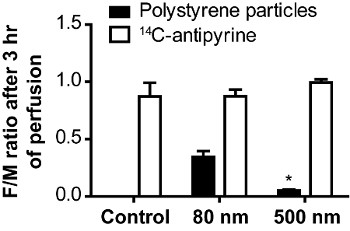
그림 5. 인간의 태반 19을 통해 폴리스티렌 입자의 크기에 의존 전송. 14 C-antipyrine 및 폴리스티렌 입자의 태아와 산모의 농도 사이의 비율은 CALC했다태반 관류의 180 분 후 ulated. 데이터는 평균 ± SE 최소 3 독립적 인 실험을 나타냅니다. 제어 열은 입자하지 않고 있지만, 14 C-antipyrine와 perfusions를 보여줍니다. (* P 80 nm의 비율 값과 비교 <0.05).

그림 6. 재관류 19시 태반 조직의 생존. (A) 포도당 소비와 관류 태반에있는 젖산 생산. 표시가 관류 자엽의 무게로 나눈 시간이 지남에 따라 회로의 총 함량의 변화 (태아와 산모)의 합이다. (B) 태반 호르몬의 정규화 된 순 생산 (NP 초기 조직의 컨텐츠 T0로 나눈 값) 인간 choriongonadotropin 및 렙틴. 데이터는 평균 ± SE의 L시를 나타냅니다지점 호텔 3 독립적 인 실험.
토론
이중 순환 살포는 여기에 보여 아래에 대답해야하는 질문에 따라 가능한 여러 가지 다른 실험 구성도이다. 특히 오픈 태반 perfusions는 일반적으로 정상 상태 농도 3시 약물 허가를 평가하는 데 사용됩니다. 순환 관류 셋업은 내인성 또는 외인성 물질의 능동 수송을 확인하기 위해 적용 할 수 있습니다. 이 방법에 대한 생체 이물의 동일한 농도는 산모와 태아 순환에 추가 할 수 있습니다. 농도 구배에 대한 능동 수송이 있다고 가정, 회로 둘 중 하나 하나의 시험 물질의 축적은 24 관찰 할 수 있습니다. 참고로, 오직 태아 회로에 시험 물질의 추가도 가능하고이 특정 물질 (25)의 태반 장벽을 통해 전송 메커니즘을 밝힐 수 있습니다.
프로토콜은 팀을 통해 진화하고있다전자 특히 유량, 관류 매체의 구성, 산소의 형태와 난방 26,27에 관한 다른 연구 그룹에 따라 다를 수 있습니다. 특히 유량은 태반 전송이 발생하는 시간에 영향을 미칠 수 있습니다. 이 제어하려면 antipyrine 같은 수동적으로 이송 참조 화합물의 첨가가 중요합니다. 생체 이물의 전송 속도는 항상 antipyrine (F / M 비는 0.75 이상이어야합니다) 26의 전송 속도를 비교할 수 있습니다. antipyrine 전송이 주로 흐름과 교환 표면에 의해 제한되어 있기 때문에,이 비교는 흐름의 차이와 실험에 따라 다를 수 있습니다 계정에 관류 자엽의 크기를합니다. 또한, FITC-덱스 트란은 장벽 (26)의 무결성을 제어 역할을 태아 회로에 추가 할 수 있습니다. 태아 볼륨 손실은 장벽 무결성을위한 마커로 사용됩니다. 보통 태아의 유체 ML / HR가 28 허용 최대 4 손실이 있지만,다시는 더 일반적으로 인정 된 제한입니다.
물론, 개인간 변이와 낮은 성공률 (15 % ~ 20 %)과 같은 생체 인간의 태반 관류 방법의 몇 가지 단점이 있습니다. 또한, 6 시간의 재관류 기간은 만성 약물 치료를 시뮬레이션 할 수 있으며 따라서 장기 노출 후 생체 이물의 전송을 제외 할 수 없습니다. 모델의 또 다른 한계는 장벽이 두꺼운 초기 임신 연령의 전송 속도는 여전히 알 수없는 남아있는 동안 장기에서 주로 태반 전송이 평가되는 것입니다. 사실, 첫 번째 임신 태반의 관류가 가능하지만, 이러한 태반의 가용성은 다소 제한됩니다. 그럼에도 불구하고, 지금까지 생체 태반 관류 방법은 조직 인간의 태반 조직에서 다양한 생체 이물질이나 나노 입자의 이동을 연구하는 유일한 모델입니다. 생체 인간의 재관류 모델에서 toxicodynamics은 PL 분석 할 수 있지만,acental 조직, 동물 실험은 참으로 또한 태아에 대한 정보를 제공 할 수 있습니다. 하지만, 때문에 인간과 설치류 사이의 태반 장벽의 해부학 적 차이의 결과는 4,5 인간에게 추정 할 수 없습니다. 태반 전송을 조사하는 또 다른 가능성은 기본 cytotrophoblasts, 융모 상피암 세포주, 고립 된 플라즈마 막 소포 또는 태반 조직 절편 29와 같은 세포 배양 모델이 될 수 있습니다. 이러한 세포는 악성 임신성 융모 상피암에서 파생되어 투과 막에 합류 단층을 형성 할 수 있으므로 전송 연구를 수행 할 수 있으며, 가장 많이 사용되는 모델은 BEWO 세포 라인입니다. BEWO 세포 모델을 사용하여 전송 연구 결과는 생체 인간의 태반 관류 30에서 얻은 결과와 상관 관계가. 그러나 약물 수송 (특정 전송 단백질의 예를 들면 기여) 및 신진 대사의 세부 사항을 연구, BEWO 세포 모델은 M 수 있습니다가능한 광석은 주로 취급하는 쉽고 유전자 조작 운송 또는 효소의 발현과 같은 조작에 취약하지만, 일반적으로 약물 전달 연구에 대한이 모델의 신뢰성이 제한되어 있기 때문에. 그것은 혈액의 흐름이 부족하고 단일 층의 무결성 6,29 인서트 농도, 노출 기간 및 막 뿌리기, 그것은 세포 배양 조건 등 여러 가지 요인에 의존하기 때문에 신중하게 평가해야합니다.
다른 생체이도 크게 태반 전송하기 31에 영향을 미칠 수있는 다양한 혈장 단백질에 바인딩을 나노 입자, 혈장 단백질에 결합을 고려는 것이 중요하다. 관류 매체는 알부민 소 혈청, 가장 자주 혈장 단백질을 포함하고 있습니다. 최근 연구는 생체 인간의 태반 관류 모델로 얻은 다양한 물질의 이동 비율은 임산부에 생체 코드 혈액과 잘 상관 관계를 보여 주었다전송 비율은 혈장 단백 결합 12의 범위에 따라 조정 된 혈중 농도 비율.
전반적으로, 생체 태반 관류 모델은 인간의 태반을 통해 수송을 연구하고 생체 이물질 및 나노 입자의 생체 태반 통로를 예측하는 유효하고 신뢰할 수있는 방법입니다.
공개
저자는 그들이 더 경쟁 재정적 이익이 없다는 것을 선언합니다.
감사의 말
이 작품은 재정적 스위스 국립 재단 (NRP 64 프로그램에는 4064-131232 권한을 부여하지 않음)에 의해 지원됩니다.
자료
| Name | Company | Catalog Number | Comments |
| NCTC-135 medium | ICN Biomedicals, Inc. | 10-911-22C | could be replaced by Medium 199 from Sigma (M3769) |
| Sodium chloride (NaCl) | Sigma-Aldrich, Fluka | 71381 | |
| Potassium chloride (KCl) | Hospital pharmacy | also possible: Sigma (P9541) | |
| Monosodium phosphate (NaH2PO4 · H2O) | Merck | 106346 | |
| Magnesium sulfate (MgSO4 · H2O) | Sigma-Aldrich, Fluka | 63139 | |
| Calcium chloride (CaCl, anhydrous) | Merck | 102388 | |
| D(+) Glucose (anhydrous) | Sigma-Aldrich, Fluka | 49138 | |
| Sodium bicarbonate (NaHCO3) | Merck | 106329 | |
| Dextran from Leuconostoc spp. | Sigma-Aldrich | 31389 | |
| Bovine serum albumin (BSA) | Applichem | A1391 | |
| Amoxicilline (Clamoxyl) | GlaxoSmithKline AG | 2021101A | |
| Sodium heparin | B. Braun Medical AG | 3511014 | |
| Sodium hydoxide (NaOH) pellets | Merck | 106498 | CAUTION: corrosive |
| Ortho-phosphoric acid 85% (H3PO4) | Merck | 100573 | CAUTION: corrosive |
| Maternal gas mixture: 95% synthetic air, 5% CO2 | PanGas AG | ||
| Fetal gas mixture: 95% N2, 5% CO2 | PanGas AG | ||
| Antipyrine (N-methyl-14C) | American Radiolabeled Chemicals, Inc. | ARC 0108-50 μCi | CAUTION: radioactive material (specific activity: 55mCi/mmol) |
| Scintillation cocktail (IrgaSafe Plus) | Zinsser Analytic GmbH | 1003100 | |
| Polystyrene particles 80 nm | Polyscience, Inc. | 17150 | |
| Polystyrene particles 500 nm | Polyscience, Inc. | 17152 | |
| EQUIPMENT | |||
| Water bath | VWR | 462-7001 | |
| Thermostat | IKA-Werke GmbH Co. KG | 3164000 | |
| Peristaltic pumps | Ismatec | ISM 833 | |
| Bubble traps (glass) | UNI-GLAS Laborbedarf | ||
| Flow heater | UNI-GLAS Laborbedarf | ||
| Pressure sensor + Software for analyses | MSR Electronics GmbH | 145B5 | |
| Notebook | Hewlett Packard | ||
| Miniature gas exchange oxygenator | Living Systems Instrumentation | LSI-OXR | |
| Tygon Tube (ID: 1.6 mm; OD: 4.8 mm) | Ismatec | MF0028 | |
| Tubes for pumps (PharMed BPT; ID: 1.52 mm) | Ismatec | SC0744 | |
| Blunt cannulae ( 0.8 mm) | Polymed Medical Center | 03.592.81 | |
| Blunt cannulae ( 1.2 mm) | Polymed Medical Center | 03.592.90 | |
| Blunt cannulae ( 1.5 mm) | Polymed Medical Center | 03.592.94 | |
| Blunt cannulae ( 1.8 mm) | Polymed Medical Center | 03.952.82 | |
| Parafilm | VWR | 291-1212 | |
| Perfusion chamber with tissue holder (plexiglass) | Internal technical department | Similar equipment is available from Hemotek Limited, UK | |
| Surgical suture material (PremiCron) | B. Braun Medical AG | C0026005 | |
| Winged Needle Infusion Set (21G Butterfly) | Hospira, Inc. | ASN 2102 | |
| Multidirectional stopcock (Discofix C-3) | B. Braun Medical AG | 16494C | |
| Surgical scissors | B. Braun Medical AG | BC304R | |
| Dissecting scissors | B. Braun Medical AG | BC162R | |
| Needle holder | B. Braun Medical AG | BM200R | |
| Dissecting forceps | B. Braun Medical AG | BD215R | |
| Automated blood gas system | Radiometer Medical ApS | ABL800 FLEX | |
| Multi-mode microplate reader | BioTek | Synergy HT | |
| Liquid scintillation analyzer | GMI, Inc. | Packard Tri-Carb 2200 | |
| Scintillation tubes 5.5 ml | Zinsser Analytic GmbH | 3020001 | |
| Tissue Homogenizer | OMNI, Inc. | TH-220 | |
| pH meter + electrode | VWR | 662-2779 | |
참고문헌
- Ala-Kokko, T. I., Myllynen, P., Vahakangas, K. Ex vivo perfusion of the human placental cotyledon: implications for anesthetic pharmacology. Int. J. Obstet. Anesth. 9, 26-38 (2000).
- Panigel, M., Pascaud, M., Brun, J. L. Radioangiographic study of circulation in the villi and intervillous space of isolated human placental cotyledon kept viable by perfusion. J. Physiol. (Paris). 59, 277 (1967).
- Schneider, H., Panigel, M., Dancis, J. Transfer across the perfused human placenta of antipyrine, sodium and leucine. Am. J. Obstet. Gynecol. 114, 822-828 (1972).
- Enders, A. C., Blankenship, T. N. Comparative placental structure. Adv. Drug Deliv. Rev. 38, 3-15 (1999).
- Takata, K., Hirano, H. Mechanism of glucose transport across the human and rat placental barrier: a review. Microsc. Res. Tech. 38, 145-152 (1997).
- Saunders, M. Transplacental transport of nanomaterials. Wiley Interdiscip. Rev. Nanomed. Nanobiotechnol. 1, 671-684 (2009).
- Buerki-Thurnherr, T., von Mandach, U., Wick, P. Knocking at the door of the unborn child: engineered nanoparticles at the human placental barrier. Swiss Med. Wkly. 142, w13559 (2012).
- Gendron, M. P., Martin, B., Oraichi, D., Berard, A. Health care providers' requests to Teratogen Information Services on medication use during pregnancy and lactation. Eur. J. Clin. Pharmacol. 65, 523-531 (2009).
- Burns, L., Mattick, R. P., Lim, K., Wallace, C. Methadone in pregnancy: treatment retention and neonatal outcomes. Addiction. 102, 264-270 (2007).
- von Mandach, U. Drug use in pregnancy. Ther. Umsch. 62, 29-35 (2005).
- Malek, A., Obrist, C., Wenzinger, S., von Mandach, U. The impact of cocaine and heroin on the placental transfer of methadone. Reprod. Biol. Endocrinol. 7, 61 (2009).
- Hutson, J. R., Garcia-Bournissen, F., Davis, A., Koren, G. The human placental perfusion model: a systematic review and development of a model to predict in vivo transfer of therapeutic drugs. Clin. Pharmacol. Ther. 90, 67-76 (2011).
- International Organization for Standardization (ISO). Technical Specification (ISO/TS) 27687. Nanotechnologies – Terminology and definitions for nano-objects – Nanoparticles, nanofibre and nanoplate. , (2008).
- Pietroiusti, A. Health implications of engineered nanomaterials. Nanoscale. 4, 1231-1247 (2012).
- Latzin, P., Roosli, M., Huss, A., Kuehni, C. E., Frey, U. Air pollution during pregnancy and lung function in newborns: a birth cohort study. Eur. Respir. J. 33, 594-603 (2009).
- Lacasana, M., Esplugues, A., Ballester, F. Exposure to ambient air pollution and prenatal and early childhood health effects. Eur. J. Epidemiol. 20, 183-199 (2005).
- Menezes, V., Malek, A., Keelan, J. A. Nanoparticulate drug delivery in pregnancy: placental passage and fetal exposure. Curr. Pharm. Biotechnol. 12, 731-742 (2011).
- Muhlemann, K., Menegus, M. A., Miller, R. K. Cytomegalovirus in the perfused human term placenta in vitro. Placenta. 16, 367-373 (1995).
- Wick, P., et al. Barrier capacity of human placenta for nanosized materials. Environ. Health Perspect. 118, 432-436 (2010).
- Dancis, J. Why perfuse the human placenta. Contrib Gynecol. Obstet. 13, 1-4 (1985).
- May, K., et al. Perfusion of human placenta with hemoglobin introduces preeclampsia-like injuries that are prevented by alpha1-microglobulin. Placenta. 32, 323-332 (2011).
- Guller, S., et al. Protein composition of microparticles shed from human placenta during placental perfusion: Potential role in angiogenesis and fibrinolysis in preeclampsia. Placenta. 32, 63-69 (2011).
- Challier, J. C. Criteria for evaluating perfusion experiments and presentation of results. Contrib. Gynecol. Obstet. 13, 32-39 (1985).
- Kraemer, J., Klein, J., Lubetsky, A., Koren, G. Perfusion studies of glyburide transfer across the human placenta: implications for fetal safety. Am. J. Obstet. Gynecol. 195, 270-274 (2006).
- leal, J. K., et al. Modification of fetal plasma amino acid composition by placental amino acid exchangers in vitro. J. Physiol. 582, 871-882 (2007).
- athiesen, L., et al. Quality assessment of a placental perfusion protocol. Reprod. Toxicol. 30, 138-146 (2010).
- Myllynen, P., et al. Preliminary interlaboratory comparison of the ex vivo dual human placental perfusion system. Reprod Toxicol. 30, 94-102 (2010).
- Malek, A., Sager, R., Schneider, H. Maternal-fetal transport of immunoglobulin G and its subclasses during the third trimester of human pregnancy. Am. J. Reprod. Immunol. 32, 8-14 (1994).
- Prouillac, C., Lecoeur, S. The role of the placenta in fetal exposure to xenobiotics: importance of membrane transporters and human models for transfer studies. Drug Metab. Dispos. 38, 1623-1635 (2010).
- Poulsen, M. S., Rytting, E., Mose, T., Knudsen, L. E. Modeling placental transport: correlation of in vitro BeWo cell permeability and ex vivo human placental perfusion. Toxicol. In Vitro. 23, 1380-1386 (2009).
- Mathiesen, L., Rytting, E., Mose, T., Knudsen, L. E. Transport of benzo[alpha]pyrene in the dually perfused human placenta perfusion model: effect of albumin in the perfusion medium. Basic Clin. Pharmacol. Toxicol. 105, 181-187 (2009).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유