Method Article
Toracoscopia com anestésico local para derrame pleural não diagnosticado
Neste Artigo
Erratum Notice
Resumo
A toracoscopia com anestésico local (LAT) é essencial para o diagnóstico de derrame pleural recorrente e não diagnosticado quando uma investigação baseada em diretrizes não fornece uma causa específica. O LAT pode ser realizado como um procedimento de caso diário por médicos torácicos. Aqui, apresentamos um passo a passo para um procedimento bem-sucedido e seguro.
Resumo
A toracoscopia com anestésico local (LAT) é um procedimento diagnóstico minimamente invasivo que ganha reconhecimento entre os médicos do tórax pelo manejo de derrames pleurais não diagnosticados. Esse procedimento de portal único é realizado com o paciente sob sedação leve e envolve uma posição de decúbito contralateral. É realizada em um ambiente estéril, tipicamente uma sala de broncoscopia ou sala cirúrgica, por um único operador com o apoio de uma enfermeira focada no procedimento e uma enfermeira focada no paciente.
O procedimento começa com uma ultrassonografia torácica para determinar o ponto de entrada ideal, geralmente no espaço intercostal IV-V ao longo da linha axilar média. A lidocaína/mepivacaína, com ou sem adrenalina, é usada para anestesiar a pele, as camadas da parede torácica e a pleura parietal. Um trocarte e cânula designados são inseridos através de uma incisão de 10 mm, atingindo a cavidade pleural com rotação suave. O toracoscópio é introduzido através da cânula para inspeção sistemática da cavidade pleural desde o ápice até o diafragma. Biópsias (tipicamente seis a dez) de lesões suspeitas da pleura parietal são obtidas para avaliação histopatológica e, quando necessário, análise microbiológica. Biópsias da pleura visceral são geralmente evitadas devido ao risco de sangramento ou vazamento de ar. A bolsa de talco pode ser realizada antes da inserção de um dreno torácico ou cateter pleural de demora através da cânula. A incisão da pele é suturada e o ar intrapleural é removido usando um sistema de drenagem torácica digital ou de três compartimentos. O dreno torácico é removido quando não há fluxo aéreo, e o pulmão se reexpande satisfatoriamente. Os pacientes geralmente recebem alta após 2-4 h de observação e são acompanhados ambulatorialmente. O sucesso da LAT depende da cuidadosa seleção, preparação e gerenciamento do paciente, bem como da educação do operador, para garantir a segurança e um alto rendimento diagnóstico.
Introdução
A incidência e a prevalência das doenças pleurais estão aumentando em todo o mundo, especialmente os derrames pleurais, que têm mais de 50 causas reconhecidas 1,2. A malignidade pleural é a principal causa de derrame pleural recorrente, principalmente devido a metástases de neoplasias extrapleurais de pulmão, mama oulinfoma3. As diretrizes existentes recomendam biópsias pleurais se a história clínica, o exame físico, a radiologia e a torneira pleural para citologia, cultura e bioquímica não fornecerem um diagnóstico4. As biópsias pleurais podem ser obtidas guiadas por imagem ou sob visão direta. As biópsias percutâneas por agulha grossa guiadas por ultrassonografia (US) ou TC permitem a amostragem da maioria das lesões na parte costal da pleura parietal, com rendimento diagnóstico de 84% e 93%, respectivamente, emrecente revisão sistemática5. A biópsia pleural guiada por US é superior em termos de menor taxa de complicações (4% vs. 7%), ausência de irradiação e disponibilidade como procedimento à beira do leito5. Relatos de casos mostram que lesões na pleura mediastinal podem ser amostradas com ecoendoscópios6.
A toracoscopia permite a inspeção visual direta e a amostragem das lesões tanto na pleura mediastinal, diafragmática ou costal, tornando-se o padrão-ouro no diagnóstico de derrame pleural recorrente de causadesconhecida4,7. A toracoscopia é realizada como toracoscopia anestésica local (LAT) ou cirurgia toracoscópica videoassistida (CTVA)8. O LAT (também conhecido como toracoscopia médica ou pleuroscopia) é um procedimento de portal único, realizado rotineiramente por pneumologistas na suíte de broncoscopia, e tem um rendimento diagnóstico para malignidade de 93%9,10. O LAT pode ser realizado com um endoscópio semirrígido ou rígido, geralmente conectado a uma fonte de imagem de vídeo. Poucas publicações discutem os benefícios e desvantagens dessas abordagens8,11,12,13. Resumidamente, o toracoscópio semirrígido assemelha-se a um broncoscópio, e as biópsias são obtidas usando pinças semelhantes. O endoscópio rígido tem maior diâmetro, é mais barato e permite biópsias maiores, embora isso não se traduza prontamente em diferenças marcantes no rendimento diagnóstico10,14,15. A segurança do LAT é alta, com taxa de mortalidade inferior a 0,5%, fortemente relacionada a condições médicas pré-existentes 3,4. As contraindicações do LAT são menores do que as da CTVA e incluem obliteração completa do espaço pleural devido a aderências, infecção cutânea no local de entrada, insuficiência respiratória, instabilidade cardíaca e coagulopatia incorrigível 7,8,12. A CTVA é um procedimento intra-hospitalar, de 2 ou 3 portas, realizado por cirurgiões torácicos, que deve ser realizado em centro cirúrgico, necessitando de anestesia geral, intubação, ventilação unipulmonar e internação pós-operatória. A CTVA tem rendimento diagnóstico e taxa de complicações semelhante à do LAT, mas permite a realização de procedimentos mais complexos10,16.
As diretrizes recomendam o LAT como toracoscopia de primeira escolha devido ao seu alto rendimento diagnóstico, baixo risco, menor custo e possibilidade de manejo de casos diurnos, reservando CTVA para casosselecionados4. A escolha de um toracoscópio rígido ou semirrígido é geralmente determinada pela preferência local. O LAT não é um procedimento novo, pois foi descrito já em meados do século 19, popularizado por Jacobaeus em 1910, cada vez mais utilizado para o tratamento da tuberculose pleural até a década de 1950 e "redescoberto" na década de 1980 como uma importante ferramenta para o diagnóstico de derrames pleurais recorrentes 8,17.
Protocolo
O protocolo a seguir descreverá como realizar o LAT em um ambiente clínico. O protocolo está de acordo com a prática clínica e as diretrizes dos hospitais dos autores (Odense, Næstved, Lleida, Bristol e Preston). O consentimento informado por escrito é obtido do paciente antes do procedimento. O principal critério de inclusão para o procedimento é derrame pleural recorrente de causa desconhecida, apesar da investigação baseada em diretrizes. Os critérios de exclusão incluem obliteração completa do espaço pleural devido a aderências, infecção de pele no local de entrada, insuficiência respiratória, instabilidade cardíaca e coagulopatia incorrigível.
1. Preparação para o procedimento
- Examinar a imagem disponível e realizar ultrassonografia (US) torácica para confirmar a presença de derrame pleural e uma distância segura (>2 cm) da pleura parietal à visceral no local de entrada esperado, preferencialmente no meio dos espaços intercostais 4 ou 5 na linha axilar média12.
- Marque o local de entrada esperado com uma caneta designada.
- Em caso de derrames de pequeno volume, induzir um pneumotórax artificial inserindo uma agulha romba (por exemplo, "agulha Boutin") ou um dreno torácico de pequeno calibre sob orientação direta por ultrassom. Após a remoção do líquido, o ar é introduzido pela agulha ou dreno, e a ultrassonografia confirma o desaparecimento do deslizamento pulmonar 8,12.
- Em caso de dúvida, realizar radiografia de tórax em decúbito lateral para confirmar a presença e a profundidade do pneumotórax.
- Colocar o paciente em decúbito lateral sobre um travesseiro ou rolo, de frente para o operador, com o derrame para cima. O travesseiro/rolo estende as costelas contralaterais, facilitando a inserção do trocarte e da cânula e minimizando o desconforto do paciente11.
- Prepare-se para o procedimento estéril de acordo com as normas locais:
- Para operador e qualquer assistente: esfoliação cirúrgica das mãos, avental e luvas estéreis, máscara, touca.
- Para o paciente: limpe a pele com uma solução esterilizante à base de álcool, use drapeados estéreis para cobertura, deixando o local de entrada esperado acessível.
- Para ferramentas: mesa estéril com faca, trocarte, cânula, endoscópio, pinças, ferramentas de sucção e sutura da pele11(ver Tabela de Materiais).
- Iniciar a sedação com um benzodiazepínico (por exemplo, midazolam 1 mg/mL) IV em doses incrementais, combinado com um opiáceo (por exemplo, fentanil 25 microgramas/mL) IV em doses incrementais para controlar a dor e a tosse. Em centros selecionados, o LAT pode ser realizado com bloqueios de nervos torácicos ou com sedação com remifentanil12.
- Certifique-se de que sedação adicional suficiente esteja disponível durante o procedimento em caso de dor, tosse ou agitação.
2. Preparo do paciente
- Anestesiar todas as camadas passo a passo com 20 mL de lidocaína a 1% (ou mepivacaína a 2%) mais adrenalina: pele, tecido subcutâneo, músculo intercostal, pleura parietal, nervo intercostal e periósteo da costela (borda caudal da borda superior e cranial da costela inferior)7,11,18.
- Finalizar a anestesia local verificando a correção do local de entrada através da aspiração de líquido pleural (ou ar se houver pneumotórax artificial) e observar a distância da pele ao espaço pleural11,12.
- Ter doses adicionais de anestesia local disponíveis durante o procedimento em caso de dor ou agitação.
- Realizar incisão na pele e inserção de trocarte e cânula.
- Faça uma incisão de aproximadamente 10 mm na pele e no tecido subcutâneo paralelo ao espaço intercostal para permitir que o trocarte e a cânula passem facilmente.
OBS: Uma incisão mais longa não acrescenta manobrabilidade e precisa ser fechada com mais pontos, o que está associado ao risco deinfecções19. - Certifique-se com a ponta do bisturi de que a anestesia pleural parietal adequada foi alcançada antes da inserção do trocarte.
- Faça uma incisão de aproximadamente 10 mm na pele e no tecido subcutâneo paralelo ao espaço intercostal para permitir que o trocarte e a cânula passem facilmente.
- Realizar uma dissecção romba cuidadosa das várias camadas entre a pele e a pleura com uma pinça reta ou curva de ponta estreita até que a cavidade pleural seja inserida e um trato de largura suficiente para permitir a passagem do trocarte e da cânula tenha sido criado.
NOTA: A liberação de fluido ou ar (este último muitas vezes ouvido como um 'silvo') confirma a localização. Opcional: A dissecção romba pode não ser necessária para procedimentos semirrígidos, dado o menor diâmetro do canal de trabalho. - Considere inserir uma sutura de fechamento ("colchão") (ver Tabela de Materiais), que é usada posteriormente para selar a pele assim que o dreno torácico pós-LAT for removido.
- Guiado pela distância da pele ao espaço pleural, insira o trocarte e a cânula com um movimento de saca-rolhas até que uma liberação súbita de resistência seja sentida. Em seguida, remova o trocarte e empurre a cânula para frente para ficar 1-3 cm dentro da cavidade pleural11,12.
3. Inspeção da cavidade pleural
- Certifique-se de que a imagem do toracoscópio esteja otimizada para correção de foco e cor e que a lente tenha sido aquecida ou tenha líquido de desembaçamento aplicado.
- Para a LAT semirrígida, insira o toracoscópio através da cânula e aplique sucção para remover o líquido restante. Para a LAT rígida, insira um tubo de sucção separado através da cânula para remover o líquido antes de inserir a câmera (Figura 1 e Figura 2).
- Inspecione a cavidade pleural sistematicamente: ápice, superfície mediastinal, diafragma e pleura costal de volta ao ápice. Assim como em outras técnicas endoscópicas, os especialistas utilizam movimentos deliberados e mínimos para alcançar a inspeção completa20,21.
NOTA: Se estiver usando uma configuração rígida, a inspeção inicial é melhor realizada usando uma lente de 50 graus antes de mudar para uma lente de 0 grau para intervenção. - A visibilidade total do espaço pleural pode ser limitada por aderências pleuropulmonares fibrosas12. Passe suavemente as aderências finas com o toracoscópio, mas evite aquelas com suprimento vascular.
4. Biópsia tecidual
- Amostra de lesões suspeitas na pleura parietal com seis a dez biópsias usando pinça apropriada com abordagem "pega e tira" (Figura 3A,B). Assegurar que haja penetração suficiente da membrana pleural parietal, pois a invasão da gordura subpleural pode afetar a classificação T do mesotelioma8,12.
- Tome cuidado para evitar a pleura visceral devido ao risco de lesão pulmonar e subsequente vazamento de ar persistente.
- Tenha cuidado para evitar o feixe neurovascular intercostal devido ao risco de sangramento e nevralgia.
NOTA: Dica de segurança: Sentir a costela com a pinça e obter biópsias da pleura parietal 'na' costela é acreditado para reduzir o risco de sangramento e danos aos vasos subjacentes. - Para procedimentos de toracoscópio semirrígido, introduzir a pinça através do canal de trabalho do endoscópio. A mudança para imagem em banda estreita pode melhorar a visualização de áreas com padrões vasculares anormais13,22.
- Para procedimentos de toracoscópio rígido, introduza pinças over-scope.
- Na ausência de infiltração maligna clara, mas com forte suspeita clínica de malignidade, realizar biópsias aleatórias11.
- Enviar 1-2 biópsias para cultura e análise da tuberculose, especialmente em áreas endêmicas ou em pacientes com fatores de risco23.
- Se houver suspeita de infecção pleural durante a LAT, remover os debris infecciosos (Figura 3C) e as aderências na medida do possível12,24. Observe que o LAT não é um procedimento ideal para a eliminação de infecção pleural complexa ougeneralizada9.
5. Terminação e inserção do dreno torácico
- Remova o toracoscópio e a cânula.
- Insira o dreno torácico pós-LAT (tipicamente 16-24 F, ver Tabela de Materiais) no espaço pleural através do trato portuário.
- Fechar a incisão com a sutura "colchão" (conforme descrito em 2.6) ou utilizar outra sutura de fechamento.
NOTA: A pleurodese com talco e/ou a colocação de cateter pleural de demora (PCI) podem ser realizadas opcionalmente em combinação com o procedimento de LAT e são agora prática padrão em muitos centros8. A descrição dos procedimentos de pleurodese ou IPC de talco está fora do escopo da presente revisão.
6. Procedimentos de acompanhamento
- Remova o dreno torácico quando a produção de ar e fluido cessar, tipicamente dentro de 1-2 h.
NOTA: Embora uma radiografia de tórax ou ultrassonografia torácica pré-remoção não seja obrigatória, ela pode ser útil para avaliar a reexpansão pulmonar. - Fechar a incisão com suturas apropriadas ou cola adesiva (ver Tabela de Materiais).
- Observe o paciente para estabilidade ao longo de 2-4 h.
NOTA: Embora uma radiografia de tórax pós-remoção ou ultrassonografia torácica não seja obrigatória, ela pode ser útil na avaliação da reexpansão pulmonar. Os pacientes que se encontram bem e estáveis após a observação recebem alta com um plano de ação por escrito em caso de sintomas graves25. - Internar pacientes frágeis na enfermaria para observação e tratamento adicionais.
Resultados
A técnica de LAT descrita com toracoscópios rígidos ou semirrígidos (Figura 1 e Figura 2) permite ao operador realizar biópsia conclusiva da pleura visceral (Figura 3) com rendimento diagnóstico de 93% em uma grande revisão sistemática sobre mais de 5000 procedimentos (Tabela 1 e Arquivo Suplementar 1) (rígido: 93% [intervalo de confiança de 95% 91%-95%]; semirrígido: 93% [89%-97%])10. O procedimento de LAT descrito é seguro, com uma taxa global de complicações de 4% (rígido: 4,2% [2,3%-6,6%]; semirrígido: 4,0% [2,0%-6,4%]10 (Tabela 1). Os óbitos são poucos e mais frequentemente relacionados à doença de base10,26.
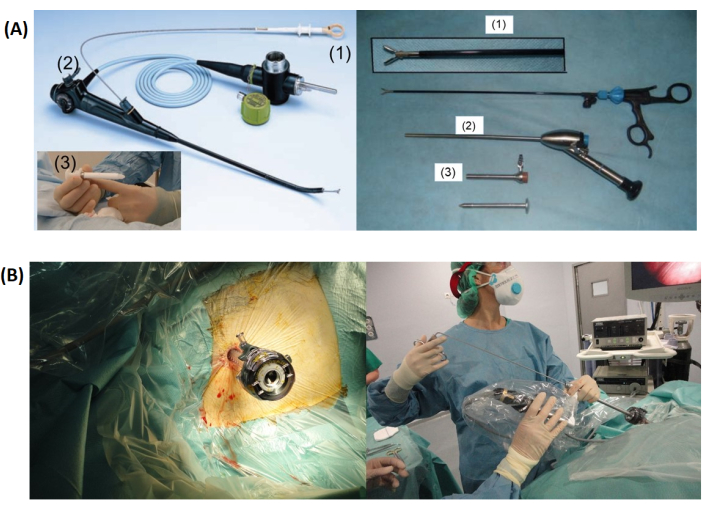
Figura 1: Configuração da toracoscopia. (A) Mostra uma comparação entre os dispositivos de toracoscopia semirrígida (esquerda) e rígida, incluindo a pinça (1), toracoscópio (2) e trocarte com cânula (3). (B) Mostra o trocarte inserido na parede torácica (esquerda) antes do LAT (Toracoscopia Anestésica Local) com toracoscópio rígido. Clique aqui para ver uma versão maior desta figura.

Figura 2: Toracoscópio semirrígido. Este desenho ilustra a colocação de um toracoscópio semirrígido na cavidade pleural acima do pulmão colapsado. Clique aqui para ver uma versão maior desta figura.

Figura 3: Imagens toracoscópicas. (A) Apresenta nódulos na pleura parietal, indicativos de adenocarcinoma pulmonar. (B) Mostra biópsia fórceps sendo realizada durante a toracoscopia. (C) Retrata septações finas não vasculares observadas em derrame pleural maligno. Clique aqui para ver uma versão maior desta figura.
Tabela 1: Metanálises da sensibilidade diagnóstica e complicações do LAT. Esta tabela apresenta um resumo das metanálises sobre a sensibilidade diagnóstica e as complicações associadas à LAT. Adaptado de Martinez-Zaya et al.10. Clique aqui para baixar esta tabela.
Arquivo Suplementar 1: O instrumento de avaliação da Toracoscopia Anestésica Local. Isso inclui oito etapas processuais do LAT semirrígido, cada uma pontuada de 1 a 5, com descritores de âncora fornecidos para os escores 1, 3 e 5. Adaptado de Nayahangan et al.27. Clique aqui para baixar este arquivo.
Discussão
Este artigo fornece uma abordagem prática para a realização da LAT.
Um único ensaio randomizado comparou LAT rígido com semirrígido e não encontrou diferenças quanto ao rendimento diagnóstico ou segurança15. As evidências sobre como otimizar as etapas críticas são escassas. Um grupo de um dos autores sugeriu oito passos críticos para o LAT semirrígido e apresentou uma lista de verificação de competências para o aprendizado do LAT em um simulador com base em suas próprias experiências, revisões narrativas 8,10,12,15,26, ensaios clínicos e revisões sistemáticas27 (Arquivo Suplementar 1). A lista de verificação separou claramente os novatos dos operadores LAT experientes e é, até agora, a única publicação que sugere uma avaliação padronizada das etapas críticas da LAT. No entanto, a lista de verificação não é exaustiva, pois se concentra estritamente em aspectos do procedimento para obter amostras de tecido com segurança e não cobre aspectos genéricos fundamentais da seleção do paciente, consentimento informado ou acompanhamento. Além disso, o checklist necessita de validação em outros centros, além de adaptação para uso clínico e inclusão de dissecção romba, etapa fundamental do uso do toracoscópio rígido7. Outra etapa fundamental é o manejo dos eventos adversos.
As complicações maiores incluem sangramento, escape aéreo persistente, infecção pleural e eventos adversos devido à medicação utilizada, enquanto as complicações menores são dor transitória, dispneia e necessidade de suplementação de oxigênio 8,14. No entanto, durante o período de especialização, o pneumologista em treinamento torna-se competente no manejo desses eventos adversos, pois estes também ocorrem após a broncoscopia e a inserção do dreno torácico, procedimentos padrão na medicina respiratória do adulto28.
Em 2018, a European Respiratory Society (ERS) revisou o currículo HERMES de 2006 para medicina respiratória de adultos, e o LAT foi considerado um procedimento chave para todos os médicos respiratórios em um nível de "know how", embora afirmando que a ERS "reconhece e apoia o desenvolvimento da toracoscopia médica realizada por pneumologistas"28. Os princípios do LAT permanecem praticamente inalterados desde que a primeira série de casos foi apresentada, há mais de 100 anos, e o aprendizado tradicional com treinamento de pacientes ainda é o método mais comum para alcançar as competências do LAT8. O treinamento em LAT não é baseado em evidências, apesar dos cursos sobre LAT com ambos os tipos de toracoscópios sendo oferecidos pela ERS e pela British Thoracic Society (BTS), envolvendo fisiologia básica, e treinamento prático de procedimentos em porcos, uma vez que as publicações sobre conteúdo e eficácia de aprendizagem são escassas29. Ao contrário, por exemplo, da broncoscopia e do ultrassom endobrônquico, não existem dispositivos de simulação de LAT disponíveiscomercialmente 27,30,31. Como em todos os procedimentos técnicos, há uma curva de aprendizado antes que a plena competência LAT seja alcançada12, mas poucos estudos relatam curvas de aprendizado de LAT. Um resumo de congresso apresentou que o rendimento diagnóstico aumentou em um período de até 2 anos após o curso de LAT da ERS32, sugerindo que os procedimentos de LAT falso-negativos potencialmente poderiam ser reduzidos acentuadamente pelo acesso ao treinamento LAT baseado em simulação31.
O presente protocolo apresenta algumas limitações importantes. Seu foco tem sido o LAT como procedimento diagnóstico e não suas aplicações terapêuticas. Portanto, o protocolo não contempla a pleurodese do talco LAT para derrame pleural recorrente ou LAT no tratamento de infecções pleurais multiloculadas ou fibrinopurulentas 8,12,24,33,34. Além disso, não abordamos os aspectos econômico-sanitários da LAT em comparação com a CTVA em um serviço pleural. Em resumo, o LAT permite o manejo de casos diurnos e a toracoscopia em pacientes com contraindicação para CTVA ou anestesia geral29,35.
Em resumo, o LAT é uma ferramenta importante no diagnóstico de derrames pleurais recorrentes ou não diagnosticados, com rendimento diagnóstico de 93%, e seu estabelecimento é baseado em metanálises e revisões sistemáticas de mais de 5.000procedimentos10. Mais pesquisas são encorajadas, incluindo o desenvolvimento de treinamento de simulação LAT baseado em evidências, para otimizar ainda mais o protocolo LAT.
Divulgações
Os autores não têm divulgações reais ou percebidas para relatar.
Agradecimentos
Nenhum financiamento foi recebido. JP e MM capturaram as fotografias mostradas na Figura 1A. RB e MM capturaram os mostrados na Figura 3.
Materiais
| Name | Company | Catalog Number | Comments |
| Chest tube | 16-24F | ||
| Forceps | narrow tip, straight or curved | ||
| Indwelling pleural catheter | Rocket Medical plc. | R55400-16-MT | or PleurX (from Becton Dickinson) or similar |
| Local anaesthetics | 20 mL of lidocaine 1% (or mepivacaine 2%) ± adrenaline | ||
| Non-absorbable suture | Eg. Dafilon 2/0 | ||
| Rigid thoracoscope | Karl Storz GmbH | Hopkins-II | with forceps 26072A and cannula+trocar 30120 NOL (or similar from eg. Richard Wolf GmbH) |
| Scalpel | triangular | ||
| Semirigid thoracoscope | Olympus | LTF-160 | with forceps FB-420K and cannula+trocar N1002130 |
Referências
- Bodtger, U., Hallifax, R. J., Maskell NA, L. C., Lee, Y. C. G., Rahman, N. M. . Pleural disease. Ers monograph 2020;87:1-12. 87, (2020).
- Froudarakis, M. E. Diagnostic work-up of pleural effusions. Respiration. 75 (1), 4-13 (2008).
- Holling, N., Patole, S., Medford, A. R. L., Maskell, N. A., Bibby, A. C. Is systemic anticancer therapy associated with higher rates of malignant pleural effusion control in people with pharmacologically sensitive tumors?: A retrospective analysis of prospectively collected data. Chest. 160 (5), 1915-1924 (2021).
- Roberts, M. E. R., et al. British thoracic society guideline for pleural disease. Thorax. 78, s1-s42 (2023).
- Mei, F., et al. Diagnostic yield and safety of image-guided pleural biopsy: A systematic review and meta-analysis. Respiration. 100 (1), 77-87 (2021).
- Bibi, R., et al. Endoscopic ultrasound-guided pleural biopsy in the hands of the pulmonologist. Respirol Case Rep. 8 (2), e00517 (2020).
- Asciak, R., et al. British thoracic society clinical statement on pleural procedures. Thorax. 78 (Suppl 3), s43-s68 (2023).
- Bhatnagar, R., Maskell, N. A. Medical pleuroscopy. Clin Chest Med. 34 (3), 487-500 (2013).
- Wei, Y., et al. Comparison between closed pleural biopsy and medical thoracoscopy for the diagnosis of undiagnosed exudative pleural effusions: A systematic review and meta-analysis. Transl Lung Cancer Res. 9 (3), 446-458 (2020).
- Martinez-Zayas, G., Molina, S., Ost, D. E. Sensitivity and complications of thoracentesis and thoracoscopy: A meta-analysis. Eur Respir Rev. 31 (166), (2022).
- Alraiyes, A. H., Dhillon, S. S. H., Kaseem, U., Kaphle, F., Kheir, Medical thoracoscopy: Technique and application. Pleura. 3 (1), 1-11 (2016).
- Loddenkemper, R., Lee, P., Noppen, M., Mathur, P. N. Medical thoracoscopy/pleuroscopy: Step by step. Breathe. 8 (2), 156-167 (2011).
- Li, D., Jackson, K., Panchal, R., Aujayeb, A. Local anaesthetic thoracoscopy for pleural effusion-a narrative review. Healthcare (Basel). 10 (10), (2022).
- Agarwal, R., Aggarwal, A. N., Gupta, D. Diagnostic accuracy and safety of semirigid thoracoscopy in exudative pleural effusions: A meta-analysis. Chest. 144 (6), 1857-1867 (2013).
- Dhooria, S., Singh, N., Aggarwal, A. N., Gupta, D., Agarwal, R. A randomized trial comparing the diagnostic yield of rigid and semirigid thoracoscopy in undiagnosed pleural effusions. Respir Care. 59 (5), 756-764 (2014).
- Ali, M. S., Light, R. W., Maldonado, F. Pleuroscopy or video-assisted thoracoscopic surgery for exudative pleural effusion: A comparative overview. J Thorac Dis. 11 (7), 3207-3216 (2019).
- Loddenkemper, R., Mathur, P. N., Lee, P., Noppen, M. History and clinical use of thoracoscopy/pleuroscopy in respiratory medicine. Breathe. 8 (2), 144-155 (2011).
- Kostroglou, A., Kapetanakis, E. I., Rougeris, L., Froudarakis, M. E., Sidiropoulou, T. Review of the physiology and anesthetic considerations for pleuroscopy/medical thoracoscopy. Respiration. 101 (2), 195-209 (2022).
- Millbourn, D., Cengiz, Y., Israelsson, L. A. Effect of stitch length on wound complications after closure of midline incisions: A randomized controlled trial. Arch Surg. 144 (11), 1056-1059 (2009).
- Cold, K. M., et al. Automatic and objective assessment of motor skills performance in flexible bronchoscopy. Respiration. 100 (4), 347-355 (2021).
- Colella, S., et al. Assessment of competence in simulated flexible bronchoscopy using motion analysis. Respiration. 89 (2), 155-161 (2015).
- Zhang, X., Wang, F., Tong, Z. Application of narrow-band imaging thoracoscopy in diagnosis of pleural diseases. Postgrad Med. 132 (5), 406-411 (2020).
- Zhao, T., et al. Medical thoracoscopy for tuberculous pleurisy: A retrospective analysis of 575 cases. Ann Thorac Med. 14 (2), 134-140 (2019).
- Sumalani, K. K., Rizvi, N. A., Asghar, A. Role of medical thoracoscopy in the management of multiloculated empyema. BMC Pulm Med. 18 (1), 179 (2018).
- Kern, R. M., Depew, Z. S., Maldonado, F. Outpatient thoracoscopy: Safety and practical considerations. Curr Opin Pulm Med. 21 (4), 357-362 (2015).
- Rahman, N. M., et al. Local anaesthetic thoracoscopy: British thoracic society pleural disease guideline 2010. Thorax. 65 Suppl 2, ii54-ii60 (2010).
- Nayahangan, L. J., et al. Assessment of competence in local anaesthetic thoracoscopy: Development and validity investigation of a new assessment tool. J Thorac Dis. 13 (7), 3998-4007 (2021).
- Tabin, N., Mitchell, S., O'connell, E., Stolz, D., Rohde, G. Update of the ers international adult respiratory medicine syllabus for postgraduate training. Breathe (Sheff). 14 (1), 19-28 (2018).
- Froudarakis, M. E., Anevlavis, S., Marquette, C. H., Astoul, P. Medical thoracoscopy implementation after a european respiratory society course held from 2003 to 2016: A survey. Respiration. 100 (6), 523-529 (2021).
- Konge, L., et al. Simulator training for endobronchial ultrasound: A randomised controlled trial. Eur Respir J. 46 (4), 1140-1149 (2015).
- Naur, T. M. H., Nilsson, P. M., Pietersen, P. I., Clementsen, P. F., Konge, L. Simulation-based training in flexible bronchoscopy and endobronchial ultrasound-guided transbronchial needle aspiration (ebus-tbna): A systematic review. Respiration. 93 (5), 355-362 (2017).
- Khanna, A., et al. Medical thoracoscopy: Learning curve of a new service. European Respiratory Journal. 40, P3362 (2012).
- Murthy, V., Bessich, J. L. Medical thoracoscopy and its evolving role in the diagnosis and treatment of pleural disease. J Thorac Dis. 9 (Suppl 10), S1011-S1021 (2017).
- Mondoni, M., et al. Medical thoracoscopy treatment for pleural infections: A systematic review and meta-analysis. BMC Pulm Med. 21 (1), 127 (2021).
- Depew, Z. S., et al. Feasibility and safety of outpatient medical thoracoscopy at a large tertiary medical center: A collaborative medical-surgical initiative. Chest. 146 (2), 398-405 (2014).
Erratum
Formal Correction: Erratum: Local Anesthetic Thoracoscopy for Undiagnosed Pleural Effusion
Posted by JoVE Editors on 1/05/2024. Citeable Link.
An erratum was issued for: Local Anesthetic Thoracoscopy for Undiagnosed Pleural Effusion. The Authors section was updated from:
Uffe Bodtger1,2
José M. Porcel3
Rahul Bhatnagar4,5
Mohammed Munavvar6,7
Casper Jensen1
Paul Frost Clementsen1,8
Daniel Bech Rasmussen1,2
1Respiratory Research Unit PLUZ, Department of Respiratory Medicine, Zealand University Hospital
2Institute of Regional Health Research, University of Southern Denmark
3Pleural Medicine Unit, Department of Internal Medicine, Hospital Universitari Arnau de Vilanova, IRBLleida
4Respiratory Department, Southmead Hospital, North Bristol NHS Trust
5Academic Respiratory Unit, University of Bristol
6Lancashire Teaching Hospitals
7University of Central Lancashire
8Centre for HR and Education, Copenhagen Academy for Medical Education and Simulation
to:
Uffe Bodtger1,2
José M. Porcel3
Rahul Bhatnagar4,5
Nick Maskell4,5
Mohammed Munavvar6,7
Casper Jensen1
Paul Frost Clementsen1,8
Daniel Bech Rasmussen1,2
1Respiratory Research Unit PLUZ, Department of Respiratory Medicine, Zealand University Hospital
2Institute of Regional Health Research, University of Southern Denmark
3Pleural Medicine Unit, Department of Internal Medicine, Hospital Universitari Arnau de Vilanova, IRBLleida
4Respiratory Department, Southmead Hospital, North Bristol NHS Trust
5Academic Respiratory Unit, University of Bristol
6Lancashire Teaching Hospitals
7University of Central Lancashire
8Centre for HR and Education, Copenhagen Academy for Medical Education and Simulation
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados