Method Article
Fraccionamento subcelular de espécimes Gastrointestinal frescos e congelados
* Estes autores contribuíram igualmente
Neste Artigo
Resumo
Aqui, apresentamos um protocolo para executar um fracionamento celular simples para a separação subcelular de proteínas citoplasmáticas e nucleares em humanas frescas e congeladas de biópsias intestinais.
Resumo
O propósito do presente protocolo é para fracionar o tecido intestinal humano obtido por endoscopia em compartimentos nucleares e citoplasmáticos para a análise de localização de proteínas específicas ou complexos de proteínas em Estados diferentes de tecido (ou seja, saudável versus doença). Este método é útil para o fraccionamento de ambas as amostras de tecido intestinal frescos e congelados; é facilmente acessível para todos os laboratórios e não demorado.
Introdução
As proteínas participam de quase todas as funções biológicas, dentro de uma célula e qualquer variação em sua estrutura, quantidade ou localização pode levar a um cenário de patogenicidade. Métodos de fracionamento de amostras de tecido são uma abordagem útil para reduzir a complexidade da doença relacionadas com análises de proteína. Alguns estudos usam informações de localização de proteínas ou enriquecem uma proteína de um compartimento celular específico, por um protocolo para reprodutível fraccionamento das proteínas intactas, é útil para responder a certas perguntas biológicas. Determinar a Localização subcellular das proteínas e monitorando sua redistribuição compartimental ou interações no basal e condições de doença ajudará a identificar a doença relacionadas com diferenças funcionais1,2. Assim, este método visa reproducibly fractionate biópsias do tecido intestinal, frescas e congeladas, em compartimentos subcellular citoplasmáticos e nucleares.
Amostras de biópsia intestinal são rotineiramente obtidas durante os procedimentos de endoscopia3 (Figura 1) e podem ser efetivamente usadas para quantificação de proteína ou estudos de imunoprecipitação. Desde que as amostras de tecido da intestinal epiteliais conterá proteínas que podem estar diretamente envolvidas na patogênese doença4, amostras de biópsia intestinal são uma fonte muito valiosa para a identificação de sucesso de específica da doença intestinal proteínas. Amostras de tecido congelado, paciente armazenado juntamente com as informações clínicas são recursos úteis para análise de proteínas, e uma preparação de amostras simples e reprodutível é uma questão-chave para fornecer informações compartimental célula usando quantidades limitantes de congelados tecido de5.
Existem vários kits disponíveis comercialmente para a separação de frações celulares, mas estes são mais caros e geralmente mais demorado do que o protocolo aqui apresentado. Protocolos com base em várias etapas centrifugação gradiente e gradientes contínuas também têm sido usados anteriormente para o fraccionamento de diversos compartimentos celulares em diferentes tecidos6,7. No entanto, manter a consistência dos gradientes contínuos é muitas vezes uma tarefa difícil. Protocolos semelhantes baseados o lysis sequencial das membranas têm sido descritos anteriormente mas geralmente precisam de mais de dois buffers e nas mãos na hora é mais8 .
Quando as amostras de tecido de fraccionamento, tenha em mente que o tecido amostras presentes célula-célula e célula-matriz interações que são não presentes em culturas de células e importante quando proceder à extração de proteínas. A repartição adequada entre células e matriz extracelular, sem afetar a qualidade da proteína será um fator crítico do tecido intestinal da proteína isolamento9. Neste protocolo, célula-célula e célula-matriz de contatos primeiro são quebrados, liberando as células e permitindo que o buffer alcançar as células individuais. Para evitar a proteína-compartimento de mistura antes de fracionamento, a repartição dos contatos deve ocorrer sem alterar a integridade das células ou as membranas nucleares.
Devido o enriquecimento de várias proteases na mucosa intestinal10, é importante controlar a degradação proteica durante a extração. Para minimizar a potencial degradação proteica, inibidor de protease múltipla deve ser incluído nos buffers de extração de proteínas. Além disso, se extratos vão ser utilizados para os ensaios funcionais, é essencial para evitar a desnaturação das proteínas ou proteólise, pois isto causará uma perda de proteína atividade11. Para este efeito, o protocolo é realizado a 4 ° C e fluoreto de phenylmethylsulfonyl fresco (PMSF) é adicionado aos buffers em uma concentração final de 0,1 mM apenas antes da utilização para inibir ainda mais a proteólise.
O primeiro passo no fracionamento celular é rompimento de tecido e lise celular. Como mencionado anteriormente, o objetivo é desagregar as células e quebra-los abrir com o mínimo de dano. Amostras de tecido intestinal devem ser homogeneizadas, e as células lysed para alcançar a máxima quebra da membrana celular. Neste protocolo, utilizamos um misturador motorizado pilão para quebrar o tecido intestinal que é homogeneizado em poucos segundos por meio de ação de alta velocidade num Vortex. Após a homogeneização, células do tecido são incubadas em um buffer hipotônica que vai estourar a membrana da célula, mas irá manter os núcleos intactos, seguido pela adição de um detergente não-desnaturação (nonilo phenoxypolyethoxylethanol) e um vórtice curto para separar os núcleos da fração citoplasmática. Após a remoção do citoplasma, a membrana do núcleo celular é de ruptura em um buffer hipertônico com agitação.
O método apresentado aqui é um método adequado para o fraccionamento subcelular de frescos e congelados de biópsias intestinais que foram obtidos durante os procedimentos endoscópicos e intervalo entre 2 e 10 mg de peso. O protocolo é fácil e pode ser reproduzido e pode ser realizado utilizando equipamentos básicos de laboratório e reagentes em menos de uma hora.
Protocolo
Este estudo foi aprovado pelo Conselho de ética Cruces University Hospital e as análises foram realizadas após consentimento informado foi obtido de todas as disciplinas ou seus pais.
1. biópsia coleção
Nota: Amostras de biópsia do duodeno distal de pacientes são obtidas durante endoscopia de rotina de diagnóstico, gerenciamento de biópsias que variam entre 2 e 10 mg de peso. Uma biópsia tecido é um tecido complexo composto por diferentes tipos de células incluindo células epiteliais, imunes e endoteliais. Gastroenterologistas clínicas realizar a endoscopia elaboradas diretrizes clínicas.
- Coloque a biópsia em um papel de filtro estéril só depois da endoscopia.
- Use fórceps para transferir as biópsias em tubos de 1,5 mL, embeba-os com PBS e colocá-lo em um criotubo.
- Manter os tubos em gelo até a chegada no laboratório.
- Inicie o processamento de biópsias frescas imediatamente.
- Para biópsias congeladas, flash congelar a biópsia contendo tubos e armazenar em nitrogênio líquido até o uso.
Nota: É importante manter a amostra congelada até que o buffer complementado frio 1 é adicionado.
2. tampão preparação
Nota: Antes de começar, complementar os buffers como segue.
- Adicionar 1 mM DTT (concentração final) e protease e fosfatase inibidor cocktail (1 x concentração final) para o buffer hipotônica hipertônico e 1 tampão 2 (tabela 1).
- Prepare-se 1,5 mL de tampão 1 e 150 µ l de tampão de 2 por amostra. DTT impede a oxidação das amostras.
- Prepare núcleos de tampão de lavagem, acrescentando 1% de detergente (nonilo phenoxypolyethoxylethanol) a uma concentração final de 0,1% para a reserva já completada 1. Prepare-se 1 mL de tampão de lavagem núcleos por amostra.
3. biópsia homogeneização
-
Biópsias de frescas
- Coloque o pilão descartável no misturador motorizado. Certifique-se de que o pilão atinge o fundo do tubo.
- Tirar a biópsia do criotubo e colocá-lo em um tubo de 1,5 mL com uma ponta da pipeta.
- Adicione 200 µ l de tampão completado 1 para o tubo de 1,5 mL.
- Homogeneizar a biópsia com o pilão, até que o tecido é completamente interrompido e mantê-lo no gelo.
- Uma vez que todas as biópsias são homogeneizadas proceda com o passo 4.
Nota: Macacos descartáveis devem ser alterados entre biópsias.
-
Biópsias congeladas
Atenção: Cuidado com nitrogênio líquido; contato de nitrogênio líquido com a pele ou olhos pode causar lesões graves de congelação. Protege as mãos e os olhos sempre quando se trabalha com nitrogênio líquido.- Leve o nitrogênio líquido em uma caixa para armazenar o cryotubes obtido o tanque de nitrogênio.
- Encontrar a biópsia no tanque de nitrogênio e coloque o criotubo na caixa com o nitrogênio líquido. Repita este passo para todas as biópsias.
- Transfira a biópsia do criotubo para um tubo de 1,5 mL.
Nota: Biópsias serão anexadas ao tubo congelado. Empurre a biópsia com uma ponta de pipeta estéril para que ele irá desanexar do tubo. - Adicione 200 µ l de tampão completado 1.
- Homogeneizar o tecido usando o pilão e almofariz, até que o tecido é completamente interrompido, manter a temperatura a 4 ° C ao longo de todo o procedimento.
Nota: Não deixe biópsias descongelar antes de adicionar o buffer.
4. o citoplasma isolamento
- Incube a biópsia homogeneizada no gelo por 10 min.
- Adicione 10 µ l de 1% de detergente (nonilo phenoxypolyethoxylethanol) para cada amostra a uma concentração final de 0,05%.
Nota: Células vão inchar e explodir por lise osmótica como o detergente vai interromper a membrana celular. - Incube no gelo por 5 minutos.
- Vórtice brevemente e centrifugar 400 x g a 4 ˚ c por 2 min.
- Após a utilização do vortex, remover o sobrenadante e transferir para um novo tubo limpo 1,5 mL; Esta será a fração citoplasmática. Não jogue fora a pelota.
5. nuclear isolamento
- Resuspenda o pellet da etapa anterior com 200 µ l de tampão de lavagem de núcleos.
- Centrifugar o tubo por 2 min em 400 x g e 4 ° C.
- Desprezar o sobrenadante e repita o procedimento de lavagem mais duas vezes.
Nota: As lavagens irão remover a contaminação citoplasmática na fração nuclear. - Após a terceira lavagem, resuspenda o pellet em 100 µ l de tampão de 2.
- Agitar vigorosamente a amostra no 4 ˚ c por 30 min. como alternativa, incubar a amostra em gelo e vórtice cada 5 min.
- Após agitação, centrifugar a amostra durante 10 minutos na velocidade máxima (> 12.000 x g) e 4 ° C.
- Após a utilização do vortex, transferi o sobrenadante para um novo 1.5 limpo. tubo mL. Esta será a fração nuclear.
6. quantificação da proteína
Nota: Quantificar as proteínas com um kit de ensaio de proteína do ácido (BCA) do bicinchoninic. A concentração de proteínas em frações irá variar entre 0,5 e 5 µ g / µ l, sendo menor na fração nuclear (ver tabela 2 para as concentrações de proteína resultantes de biópsias de 2mg).
- Preparar uma curva padrão com o seguinte de montantes (µ g) de albumina de soro bovino (BSA)12: 0-0.5-1-2-3-4-5-6.
- Prepare os reagentes necessários para a utilização de 100 µ l de mistura final do BCA por amostra.
- Pipetar 2 µ l de cada fração de proteína em uma placa de 96 bem, adicione a mistura do BCA e siga as instruções do fabricante para a leitura.
Resultados
A Figura 1 mostra uma coloração de eosina hematoxilina de uma seção de biópsia intestinal com vilosidades intactas e estruturas de cripta.
Resultados representativos de fracionamento nuclear e citoplasmático, usando este protocolo são mostrados nas figuras 2 e 3. No experimento mostrado na Figura 2, um fresco (Fh) e um congelado (Fz) biópsia foram simultaneamente fracionada seguindo o protocolo aqui apresentado e um western blot foi realizado usando 20 μg de cada amostra. As concentrações de proteína em cada fração e biópsia são mostradas na tabela 2, e as concentrações de proteína não são muito diferentes entre o fresco e o tecido congelado. O rendimento de proteína extraída de biópsias 2mg é em torno de 3-4 µ g / µ l na fração citoplasmática e aproximadamente 1,5 µ g / µ l na fração nuclear. Para verificar a pureza das frações, HSP90 e tubulina foram usados como um controles citoplasmática e HDAC1 e H3 como um controles nuclear13. Pode-se observar que o HSP90 e tubulina são primários localizado no citoplasma e HDAC1 e H3 estão localizados no núcleo com mistura muito mínimo entre as duas frações. Para avaliar se o protocolo afeta a morte celular, nós também apagou a presença de caspase 3. Da Figura 2, ambas as amostras apresentam uma coloração muito escasso para caspase 3 confirmando que o procedimento não afeta a via de morte celular mesmo após flash congelando as biópsias. Ele também foi analisado se as modificações de proteínas são mantidas após o procedimento, assim as proteínas podem ser usadas para ensaios funcionais a jusante. PhosphoSTAT1 foi usado para a coloração como a biópsia congelada usada neste fraccionamento veio de um indivíduo com uma condição inflamatória intestinal; Isso não é verdade da biópsia fresca. Como esperado, phosphoSTAT1 situa-se no citoplasma da biópsia congelado, confirmando que as modificações de proteína são mantidas após fracionamento.
A reprodutibilidade do método usando biópsias congeladas é mostrada na Figura 3. Um western blot foi realizado após fracionamento de três independente de congelados de biópsias, e as frações são limpas com proteína mínima do compartimento mistura (Figura 3A): HSP90 localizado na fração citoplasmática e HDCA1 na fração nuclear. Além disso, a proteína XPO1 que está presente em ambas as fracções nucleares e citoplasmáticos14 também estava borrada. Pode-se observar que os níveis de XPO1 quantificada pelo ImageJ são estáveis em cada fração (Figura 3B), confirmando a reprodutibilidade dos resultados usando diferentes biópsias.
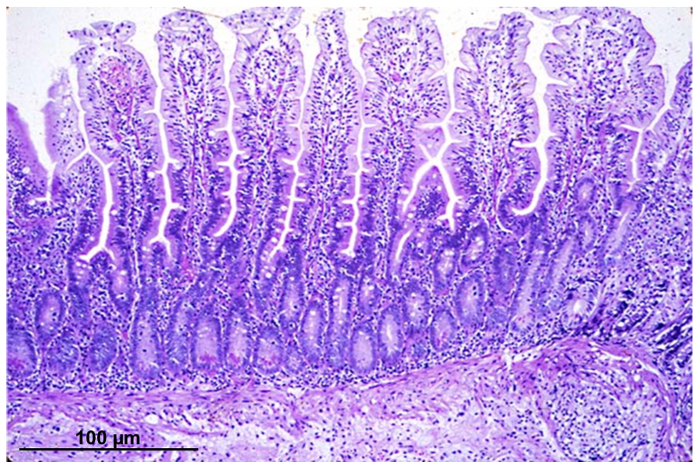
Figura 1 : Luz Micrografia de uma seção de epitélio intestinal, corada com hematoxilina-eosina, de uma biópsia adquirida pelo procedimento endoscópico. Clique aqui para ver uma versão maior desta figura.

Figura 2 : Borrão ocidental de representante de um fracionamento subcelular realizadas em um fresco (Fh) e uma biópsia (Fz) congelada. HSP90 e tubulina foram usados como controles citoplasmáticas e HDAC1 e H3 como controles nucleares. A presença de CASP3 e phosphoSTAT3 também foram avaliados.
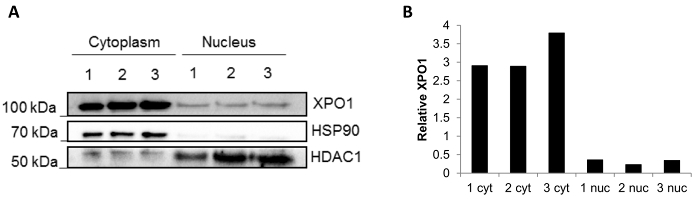
Figura 3 : Resultados de fracionamento de três independente de congelados de biópsias. (A) borrão ocidental de representante de um fracionamento subcelular realizada em três biópsias congeladas (1, 2 e 3). HSP90 foi usado como um controle citoplasmática e HDAC1 como um controle nuclear. A localização do XPO1 também foi avaliada. (B) quantificação relativa dos XPO1 em cada um da fração feita usando software ImageJ. Clique aqui para ver uma versão maior desta figura.
| Buffer de | Componentes | Notas |
| Buffer de hipotônica 1 | pH de 10 mM HEPES 7,9 | 1,5 ml de tampão/amostra |
| 10 mM KCl | ||
| EDTA 0,1 nmM | ||
| Hipertónica tampão 2 | pH HEPES 20 mM 7,9 | 150 µ l de tampão/amostra |
| 400 mM NaCl | ||
| 0,1 mM EDTA | ||
| * Nota: Buffers podem ser armazenados no 4 º c por um mês. | ||
| * * Nota: Buffers devem ser completadas com inibidores da protease e fosfatase e TDT antes da utilização | ||
Tabela 1: Composição de Buffer.
| Fresco | Congelado | |
| Citoplasma | 2.975 | 4,612 |
| Núcleo | 1.516 | 1.385 |
Tabela 2: Concentração de proteína de cada uma das frações em uma biópsia de frescos e congelados 2 mg usado em Figura 2; concentração é apresentada em μg/μL.
Discussão
O protocolo descrito aqui é usado para o fraccionamento nuclear e citoplasmático de biópsias intestinais. As proteínas purificadas não são desnaturadas e pode ser usadas não apenas na análise ocidental do borrão como mostrado na Figura 2 e 3 , mas também em ensaios que exigem nativo-dobrado proteínas tais como imunoprecipitação, ensaio de turno de mobilidade electrophoretic (EMSA) ou eletroforese em gel de poliacrilamida nativo (página).
O método descrito baseia-se na homogeneização mecânica do tecido juntamente com Lise osmótica para estourar a membrana da célula sem afetar a membrana nuclear. O resultado é um fracionamento limpo de ambas as proteínas citoplasmáticas e nucleares a ser usado para análises a jusante. É importante controlar a degradação das proteínas durante o processo pela adição de inibidores de proteína e fosfatase. Além disso, se as proteínas extraídas devem ser utilizados para os ensaios funcionais a jusante, também é importante evitar a desnaturação e proteólise das amostras. Os processos devem efectuar-se a 4 ° C e PMSF deve também ser adicionado aos buffers.
O procedimento descrito neste protocolo é simples e acessível, e o tempo de processamento da amostra é mínimo. Problemas tais como longos tempos de processamento e a utilização de kits de fracionamento caro não são restrições neste protocolo.
Frescas e congeladas de biópsias podem ser usadas no presente protocolo, com biópsias congeladas dando resultados bastante limpo e reprodutíveis fracionamento como visto na Figura 2 e 3. Se houver contaminação do compartimento, o tempo de lise celular pode ser reduzido para evitar a liberação da energia nuclear para o citoplasma e as etapas de lavagem pode ser adicionado para evitar contaminação citoplasmática no compartimento nuclear.
A possibilidade de utilizar os tecidos congelados para a análise independente para frações de proteínas nucleares e citoplasmáticos pode aumentar nosso conhecimento sobre doenças inflamatórias intestinais, na qual são armazenadas congelados de biópsias. Além disso, esta técnica pode ser adaptada para outros tipos de tecidos humanos adquiridos por biópsias. O volume de buffers usado deve ser modificado dependendo do tamanho da biópsia.
O protocolo descrito aqui é projetado para gerar frações de tecido pode ser reproduzido; no entanto, alguns intrínseca variabilidade dentro da amostra, incluindo o tamanho e o status do tecido pode levar a desvios na quantidade de proteína e distribuição gerenciados em cada fração.
Divulgações
Os autores não têm nada para divulgar.
Agradecimentos
Os autores reconhecem a assistência de Ander Lopez e Miren Telletxea para gravação e edição de vídeo. ACR é financiado por uma bolsa de Ikerbasque e um projeto de pesquisa do Asociación de Celiacos de Madrid (ACM). Orc é financiado pelo projeto ISCIII-PI16/00258 e co-financiado pela União Europeia FEDER/FSE "Uma maneira de tornar a Europa". É é financiado por uma concessão do projeto de pesquisa 2015111068 do departamento de saúde Basco. IRG e AJM são suportados pelo companheirismo predoctoral subvenções provenientes da UPV/EHU e o departamento de educação de Basco, respectivamente.
Materiais
| Name | Company | Catalog Number | Comments |
| HEPES | Sigma Aldrich | H4034-1kg | |
| KCl | Sigma Aldrich | P9333-1kg | |
| EDTA | Sigma Aldrich | E9884-100G | |
| NaCl | Sigma Aldrich | 5588886-1kg | |
| DTT | Sigma Aldrich | 10197777001 | |
| PMSF | Thermo Scientific | 36978 | |
| Proteinase and phosphatase inhibitors | Thermo Scientific | A32959 | |
| NP-40 | Sigma Aldrich | CA-630 | Detergent |
| BCA assay | Thermo Scientific | 23227 | Protein quantification kit |
| Disposable plastic pestles | Sigma Aldrich | Z359947-100EA | |
| Dounce homogeneizer | VWR | 431-0100 | |
| Microcentrifuge | Eppendorf | 5415-R | |
| Shacker | IKA | MS3 basic |
Referências
- Cox, B., Emili, A. Tissue subcellular fractionation and protein extraction for use in mass-spectrometry-based proteomics. Nature Protocols. 1 (4), 1872-1878 (2006).
- Itzhak, D. N., Tyanova, S., Cox, J., Borner, G. H. Global, quantitative and dynamic mapping of protein subcellular localization. eLife. 5, (2016).
- Preedy, V. R., Watson, R. R., Ronald, R. Methods in disease investigating the gastrointestinal tract. , Greenwich Medical Media. (1998).
- Alex, P., Gucek, M., Li, X. Applications of proteomics in the study of inflammatory bowel diseases: Current status and future directions with available technologies. Inflammatory bowel diseases. 15 (4), 616-629 (2009).
- Ericsson, C., Franzén, B., Nistér, M. Frozen tissue biobanks. Tissue handling, cryopreservation, extraction, and use for proteomic analysis. Acta oncologica (Stockholm, Sweden). 45 (6), 643-661 (2006).
- Hoffmann, K., et al. New application of a subcellular fractionation method to kidney and testis for the determination of conjugated linoleic acid in selected cell organelles of healthy and cancerous human tissues. Analytical and Bioanalytical Chemistry. 381 (6), 1138-1144 (2005).
- Foster, L. J., et al. A Mammalian Organelle Map by Protein Correlation Profiling. Cell. 125 (1), 187-199 (2006).
- Baghirova, S., Hughes, B. G., Hendzel, M. J., Schulz, R. Sequential fractionation and isolation of subcellular proteins from tissue or cultured cells. MethodsX. 2, e440-e445 (2015).
- Börner, A., et al. Subcellular protein extraction from human pancreatic cancer tissues. BioTechniques. 46 (4), 297-304 (2009).
- Antalis, T. M., Shea-Donohue, T., Vogel, S. N., Sears, C., Fasano, A. Mechanisms of disease: protease functions in intestinal mucosal pathobiology. Nature clinical practice. Gastroenterology. 4 (7), 393-402 (2007).
- Cutler, P. Protein purification protocols. , Humana Press. (2004).
- Walker, J. M. The Bicinchoninic Acid (BCA) Assay for Protein Quantitation. The Protein Protocols Handbook. , 11-14 (1996).
- McLane, L. M., et al. Differential localization of T-bet and Eomes in CD8 T cell memory populations. Journal of immunology (Baltimore, Md.: 1950). 190 (7), 3207-3215 (2013).
- Nguyen, K. T., Holloway, M. P., Altura, R. A. The CRM1 nuclear export protein in normal development and disease. International journal of biochemistry and molecular biology. 3 (2), 137-151 (2012).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados