Method Article
Síntese em fase sólida Submonomer de Polímeros Peptoid e seus Automontagem em altamente ordenada nanofolhas
Neste Artigo
Resumo
Um simples e gerais método de síntese manual de peptoid envolvendo equipamentos básicos e reagentes disponíveis comercialmente é delineado, permitindo Peptóides para ser facilmente sintetizado na maioria dos laboratórios. A síntese, purificação e caracterização de um 36mer peptoid anfifílicos é descrito, bem como a sua auto-montagem em altamente ordenado nanofolhas.
Resumo
Peptóides são uma nova classe de biomimético, não-natural, seqüência específica heteropolímeros que resistem à proteólise, apresentam atividade biológica potente, e dobre em nanoestruturas de ordem superior. Estruturalmente similares aos peptídeos, Peptóides são poli N-substituído glycines, onde as cadeias laterais estão ligados ao nitrogênio, em vez de o alfa-carbono. Sua facilidade de síntese e diversidade estrutural permite que testes de princípios básicos de design para dirigir de novo desenho e engenharia de novos materiais biologicamente ativos e nanoestruturados.
Aqui, um simples manual de protocolo de síntese peptoid é apresentado que permite a síntese de polypeptoids de cadeia longa (até 50mers) em excelentes rendimentos. Apenas equipamentos básicos, técnicas simples (por exemplo, transferência de líquidos, filtração), e reagentes disponíveis no mercado são necessários, fazendo Peptóides uma adição acessível a toolkits muitos pesquisadores. A espinha dorsal peptoid é cultivado um monômero em um tempo via o método submonomer que consiste em um ciclo de duas etapas além de monômero: acilação e deslocamento. Ácido, primeiro bromoacetic ativadas in situ com N, N'-diisopropylcarbodiimide acylates uma resina-bound amina secundária. Deslocamento, segundo nucleofílica do brometo de uma amina primária segue para introduzir a cadeia lateral. O ciclo de duas etapas é iterado até que o comprimento da cadeia desejado seja alcançado. A eficiência de acoplamento deste ciclo de dois passos rotineiramente excede 98% e permite a síntese de Peptóides enquanto 50 resíduos. Altamente sintonizável, precisa e quimicamente seqüências diversas são realizáveis com o método submonomer como centenas de aminas primárias prontamente disponíveis pode ser diretamente incorporadas.
Peptóides estão emergindo como um material versátil biomimético para pesquisa nanobioscience por causa de sua sintética flexibilidade, robustez, e ordenando a nível atômico. O dobramento de uma única cadeia, anfifílicos, informação rica em polypeptoid em um nanosheet altamente ordenado foi recentemente demonstrada. Este é um peptoid 36-mer, que consiste em apenas três diferentes monômeros comercialmente disponíveis: hidrofóbica, catiônicas e aniônicas. O cadeias laterais hidrofóbicas feniletil estão enterrados no núcleo nanosheet enquanto a amina iônicos e cadeias laterais carboxila alinhar nos rostos hidrofílico. O nanofolhas peptoid servir como uma plataforma potencial para miméticos de membrana, miméticos de proteínas, fabricação de dispositivos e sensores. Métodos para a síntese peptoid, formação da folha, e as imagens de microscopia são descritos e fornecer um método simples para que projetos futuros nanosheet peptoid.
Protocolo
1. Solid-Phase Synthesis Submonomer de Polypeptoids
Síntese em fase sólida (SPS) é uma técnica comum usada para sintetizar sequências específicas de biopolímeros passo a passo, diretamente sobre um suporte sólido inerte, tal como uma resina polimérica talão. Altos rendimentos de acoplamento e facilidade de remoção dos reagentes em excesso são grandes vantagens da SPS. Depois de uma reação de acoplamento à resina, reagentes em excesso são simplesmente drenado e as contas são lavadas para estar pronto para a fase seguinte da reacção. Após a reação de síntese final, os oligômeros de longa-metragem são clivadas a partir da resina eo material solução de fase pode ser mais bem estudadas. Aqui, adaptar o procedimento SPS para gerar polímeros seqüência específica peptoid.
- Setup: Todas as etapas da síntese peptoid manual pode ser realizada em um de polipropileno, descartáveis (PP) cartucho poroso ou um vaso de reação fritted de vidro equipado com uma torneira de 3 vias. Realizar todas as operações em uma capela. Para as incubações na gnavio lass ou cartucho plástico, conectar um braço a uma fonte de nitrogênio para gentilmente bolha a solução para a mistura correta. Alternativamente, para incubações reação no cartucho descartável, selo ambas as extremidades do cartucho com tampas e coloque em um agitador rotativo. Para drenar misturas de reacção ou lavagens, ligue para a casa de vácuo através de um sifão. O navio deve ser poroso com uma frita grosseira. Siliconize o reactor de vidro para evitar contas de degola para as paredes do recipiente de vidro. Prepare uma solução de 5% em dichlorodimethylsilane dicloroetano (v / v). Encher um recipiente de reação limpa e seca para a parte superior com solução siliconização, deixe descansar por 30 minutos, depois escorra. Lavar o vaso uma vez com DCE e depois uma vez com metanol. A solução siliconização pode ser reutilizado, por isso deve ser salvo. Ou ar seco ou sacudir qualquer excesso de solução e asse o vidro até secar após a remoção da torneira. Vaso de reação esfriar antes de adicionar resina.
- Adicionar 100 mg (0,06 mmol) de re amida Rinkpecado a um recipiente de reação fritted. Swell a resina, adicionando 2 mL de dimetilformamida (DMF). Agitar, por agitação ou borbulhamento por 10 minutos. Escorra a solução de vácuo para isolar a resina incharam.
- Adicionar 1 mL de 20% 4-methylpiperidine em DMF (v / v) para desproteger o grupo Fmoc. Agitar por 2 minutos e escorra. Repita com uma incubação de 12 minutos.
- Enxágüe da resina adicionando 2 mL de DMF, agitando por 15 segundos, e drenagem. 3x.
- Bromoacetylation: Adicionar 1 mL de 0,6 M bromoacetic ácido (0,6 mmol) em DMF e 86 mL de N, N'-diisopropylcarbodiimide (0,93 equivalente, 0,56 mmol). Incube com borbulhar suave durante 30 minutos, depois escorra e lave com 2 mL de DMF (repita 4x).
- Deslocamento: Adicionar 1 mL de 1-2 M de amina na N-methylpyrrolidinone. Incube com borbulhando para 30-120 minutos, depois escorra e lave com DMF (2 mL 4x).
- Continuar a crescer a cadeia peptoid, repetindo o ciclo submonomer, passos 1.5 (bromoacetylation) e 1.6 (displacement).
- Após o deslocamento final é feito, lavar com 2 mL de DMF (repeat 4x), em seguida, 2 mL de diclorometano (3x). Cap e armazenar o reactor até clivagem.
- Pausa na síntese (opcional): Para fazer uma pausa durante uma síntese peptoid, terminar a reação de deslocamento e avance para o passo 1.8. Para continuar crescendo a cadeia peptoid, reinicie a síntese de re-inchaço da resina seca (passo 1.2) e repetindo o ciclo submonomer (passo 1.5 e 1.6). A resina pode ser secos e armazenados após qualquer deslocamento, exceto o deslocamento segundo porque o conjugado de resina peptoid-pode formar um produto cíclico diketopiperazine lado.
- Para várias sínteses simultâneas, uma em fase sólida colector de vácuo extração é recomendada para maximizar a eficiência. Síntese Peptoid também pode ser automatizada por métodos de programação propriamente nos sintetizadores peptídeo disponíveis comercialmente, como a Apex Aapptec 396, sintetizador de microondas CEM Liberdade e Techno Proteinlogias sintetizador Prelude Inc..
2. Clivagem e Side-Chain desproteção
- Transferir todas as resinas secas em um frasco de vidro de cintilação 20 mL.
- Trabalhando dentro de um capuz e com equipamentos de protecção individual adequado, adicionar 4 mL de ácido trifluoroacético (TFA) cocktail de clivagem 1 (por exemplo, 95% aq. TFA, ver discussão) para o frasco de vidro de cintilação e tampa. Agitar durante 10 minutos a 2 horas à temperatura ambiente (ver discussão).
- Coletar a solução de clivagem TFA, filtrando a resina através de um descartáveis, cartucho PP fritted em um novo, 20 mL frasco de vidro pré-pesados de cintilação. A descartáveis, PP pipeta é conveniente para transferir as soluções cocktail de clivagem.
- Adicionar 1 mL de coquetel de clivagem doce para lavar a resina e recolher qualquer peptoid residual. 2x.
- Evaporar TFA soprando um fluxo suave de nitrogênio ou usando um Biotage V10 evaporador.
- Redissolver o petróleo bruto em 6 mLde acetonitrila / água 1:1 (v / v) para HPLC. Congelar e lyophilize. Repetir.
- Registre o peso do produto cru. Store como um pó seco a -20 ° C
- Clivagem de teste (opcional): A clivagem de teste em 0,5% da resina pode ser realizada para determinar rapidamente a pureza ea massa do peptoid sintetizado e se as condições corretas de clivagem foram escolhidos. Clivagens teste são especialmente úteis para monitorar o progresso da síntese.
3. Caracterização e Purificação da Polypeptoid
- Através de uma combinação de análise HPLC, electrospray LC-MS, e / ou MALDI-TOF, determinar a pureza do produto bruto e se o peso molecular desejado está presente.
- Prepare uma solução ~ mg / mL 50-10 do pó seco peptoid em água com acetonitrila mínimo, conforme necessário para a solubilidade. Solução clara filtro do produto peptoid bruto com 0,45 mM filtro de seringa para remover a poeira e partículas.
- Analítica HPLC e electrospray LC-MS: Prepare a ~ 20 mg / mL solução peptoid bruto. Filtro com um 200 mL 0,45 mM filtro e injectar 20 mL.
- MALDI: Misture 1 mL de ~ 20 peptoid mg / mL com 1 mL da matriz. Spot 1 mL na placa MALDI e deixar secar ao ar. Matriz e modo de aquisição está dependente da amostra (Fig. 5).
- Purificar a mistura de crude peptoid com fase reversa HPLC prep. Escolha o gradiente e coluna (C4 ou C18) com base na hidrofobicidade de polypeptoid. Combine frações purificadas, congelar e lyophilize, resultando em um pó branco macio. Registre o peso do produto final.
- Formação de HCl sal (opcional): Recolher o pó liofilizado em 100 mM HCl (aq.), com acetonitrila mínimo. Transferência para pré-pesados frasco de vidro. Congelar e re-lyophilize. 2x. Nova pesagem para determinar a massa de pó peptoid.
4. Formação Nanosheet Peptoid
Esta seção describes o protocolo para formar folhas de uma única cadeia, seqüência específica, anfifílicos 36-mer peptoid (Fig. 1). Após a vertente peptoid é sintetizado, purificado e liofilizado, como descrito acima, o pó resultante branco é dissolvido em DMSO para fazer uma solução estoque 2 mM.
- Prepare 500 mL de solução 20 mM peptoid (10 mM Tris-HCl, 100 mM NaCl, pH 8,0 em água) num frasco de vidro um dram. Tampão na formação da folha Primeiro, adicione 445 mL de água Milli-Q, 50 mL de tampão 10x folha de formação, e vortex para misturar. Em seguida, adicionar 5 mL de solução estoque 2 mM peptoid e gentilmente solução redemoinho. Tampe o frasco de vidro.
- Folhas são formadas pela agitação suave da solução aquosa diluída peptoid. Lentamente inclinar o frasco de vidro da posição horizontal para a posição vertical resultados em folhas. Suave agitação também produz folhas, no entanto, as folhas tendem a ser menores e com menos arestas retas. Uma análise mais aprofundada do mecanismo de formação da folha é reported separadamente. 2
- Para muitos de alta qualidade folhas, gire os frascos de vidro sobre o eixo horizontal lentamente (
- Diálise de nanofolhas (opcional): Em certas aplicações, pode ser necessário para remover qualquer cadeias livre peptoid ou buffers / sais. Molhe um Float-a-Lyzer 100 kD membrana no buffer desejado por 15 minutos. Carga 500 mL de solução folha peptoid na câmara de amostra. Mergulhe em 500 mL de tampão desejado, mexendo com uma barra de agitação magnética a 60 rpm. Permitir a diálise de folhas para prosseguir por 4 horas. Cada hora de troca, com um estoque fresco de uma solução tampão.
5. Microscopia de fluorescência de nanofolhas
- Imagens de fluorescência das nanofolhas foram fotografadas com Nile Red, um corante ambientalmente sensíveis, cuja intensidade de fluorescência aumenta quando ela está localizada em hydrophobic ambientes (Fig. 2).
- Adicionar 1 mL de 100 M Nile Red para 100 mL da solução nanosheet para obter uma concentração final de 1 mM de Nilo Vermelho.
- Faça uma solução de agarose 1% em água quente e despeje em uma placa de Petri de plástico. Garantir que a solução de agarose é de aproximadamente 1 / 8 de polegada de espessura e deixe a solução esfriar em repouso sobre uma superfície plana. Após os conjuntos de agarose, use uma espátula para cortar e transferir 1 cm x 1 cm e praças uma lâmina de vidro.
- Para coletar as folhas no mesmo plano, spot 1 mL de solução de folha no pedaço de agarose. Permitir que a agarose para absorver o tampão por 2 minutos, deixando as folhas na superfície. Imagem dentro de 15 minutos, caso contrário o agarose começará a deformar-se devido à desidratação.
- Às folhas de imagem em solução, 15 mL de carga dentro de uma junta de 20 milímetros 0,12 mm de diâmetro sobre uma lâmina de vidro. Cobrir com uma lamela. Se as folhas são simplesmente imprensado entre uma lâmina de vidro e lamínula sem uma junta, muitas folhas will cisalhamento ea evaporação aparentemente menor fará com que as folhas que constantemente se mover.
- Folhas de imagem sob iluminação de epifluorescência (Olympus IX81 por exemplo, um microscópio invertido equipado com um iXonEM Andor + espectros EMCCD com um vermelho Texas filtro).
6. Microscopia eletrônica de varredura (MEV) de nanofolhas
- Plasma etch de substrato de silicone (opcional): O chips de silício são gravadas plasma para auxiliar na adsorção de folhas. Colocar os chips de silício na câmara de vácuo de um aspirador de plasma (por exemplo Harrick Plasma Cleaner / Esterilizador PDC-32G). Bomba de até 200 mTorr e definir a bobina de RF para 18W (alta definição para PDC-32G). Etch por 2 minutos.
- Queda de 20 mL de solução de folha de peptoid sobre um substrato de silício plasma tratado. Deixe descansar por 3 minutos. Retire o excesso de solução com a ponta do Kim-wipe. Pipeta mL 20 de água sobre a superfície e remover o excesso de solução novamente para remover tampão e sais. Repita 4x.
- Alternativamente, disqueyze as soluções folha peptoid contra água para retirar tampão eo sal. Queda de 20 mL de solução de folha de dialisado de plasma em substratos tratados com silício. O ar seco da amostra.
- Folhas de imagem com SEM (por exemplo Zeiss Gémeos Ultra-55 Microscópio Eletrônico de Varredura Analítica) com um detector na lente e no feixe de energias entre 1 kV e 5 kV (Fig. 3).
7. Notas de Segurança:
- Dimetilformamida e diclorometano são razoavelmente suspeitos carcinógenos.
- N, N'-Diisopropylcarbodiimide, 4-methylpiperdine e ácido bromoacetic são perigosos para a pele, olhos e trato respiratório. Eles devem ser usados na capa com cuidado. Pode ser tóxico se inalado ou absorvido através da pele, ea exposição pode resultar em sensibilização. Recipientes vazios retêm resíduos do produto (líquido / vapor) e devem ser cuidadosamente lavados antes de removê-los do capô.
- TFA é um ácido forte, e é extremamente destrutivo para o trato respiratório superior, olhos epele. TFA também é volátil-keep soluções concentradas de TFA na capa em todos os momentos, para evitar danos respiratórios. Utilizar EPI adequado e cuidado ao manusear soluções de TFA. Luvas de mudar rapidamente se eles entram em contato com TFA, e imediatamente limpar todos os derramamentos.
8. Resultados representativos:
Esta seção descreve a síntese, caracterização e purificação de uma seqüência específica de cadeia peptoid 36-mer que se dobra em um nanosheet altamente ordenada 3 (Fig. 1).
O bloco de carga peptoid H-[Nae-NPE] 9 - [NPE-nce] 9-NH 2 foi sintetizado em 100 mg de resina amida Rink. A 2 M de solução de amina foi usado para todas as reações de deslocamento, que foram realizadas por 60 minutos para o resíduo de 18/01 e 120 minutos para o resíduo 19-36. t-butil beta-alanina HCl foi convertido para a base livre (ver discussão), enquanto feniletilamina e boc-etilenodiamina foram ambos usados directly. A resina foi clivado com TFA 95%, triispropylsilane 2,5%, 2,5% de água por 2 horas. TFA foi evaporado eo óleo viscoso resultante (~ 180 mg) foi re-dissolvido em 6 mL de acetonitrila: água 1:1 (v / v). Pureza do produto (Fig. 4) e presença da massa do produto foi confirmada por análise de RP-HPLC (30-80% em acetonitrila gradiente de água, ambos contendo 0,1% (v / v) TFA, em 1 mL / min, durante 30 minutos a 60 ° C com um C18, 5 mm, 50 X coluna mm 2) e MALDI (Fig. 5).
Purificação com fase reversa HPLC em uma coluna C18 Vydac (10 mM, 22 mm x 250 mm) procedeu, utilizando um gradiente de 30-60% de acetonitrila em água com TFA 0,1% mais de 60 minutos a 10 mL / min. A coluna foi carregada com 60 mg de produto bruto para cada corrida cromatográfica. As frações purificadas foram combinadas com base na pureza da RP-HPLC analítico (Fig. 4) e liofilizados para produzir ~ 80 mg de um pó branco macio.
Purificada peptoid bloco carga molecularde peso foi confirmado por MALDI. 1 mL de 100 M purificada peptoid em acetonitrila: água 1:1 (v / v) foi misturada com 1 mL da matriz (5 mg / mL de ácido α-ciano-4-hidroxicinâmicos em acetonitrila: água 1:1 v / v e 0,1% TFA) e 1 mL foi visto na placa de MALDI. Após a amostra seca ao ar, foi colocado no 4800 MALDI Applied Biosystem / MDS SCIEX Analyzer TOF / TOF. Os modos de aquisição e processamento foram de baixa massa linear. O peso calculado foi inserido na massa direcionados para ajustar automaticamente para o tempo de atraso. A intensidade do laser foi definido para 3400. A massa observada, 4981,2, corresponde intimamente à massa calculada de 4981,74.
O pó liofilizado purificado foi dissolvido em DMSO para fazer uma solução estoque 2 mM, o que pode ser armazenado a 4 ° C. Folhas foram preparados pelo protocolo referido e fotografada com microscopia óptica de fluorescência e SEM (Fig. 2 e 3). Uma variedade de formas com tamanhos recurso que variam até 300 mm, são observados, e notably, bordas retas são proeminentes.

Figura 1 Seqüência do bloco de carga peptoid H-[Nae-NPE] 9 -. [NPE-nce] 9-NH 2. A única cadeia, taxa de bloco, polypeptoid anfifílicos 36-mer auto-montagem em altamente ordenado, bidimensional nanofolhas 3. O peso molecular é calculada 4.981,74.

Figura 2. Imagens de microscopia de fluorescência nanofolhas peptoid. Folhas foram formadas a partir de uma solução de 20 mM peptoid em 10 mM Tris, 100 mM NaCl, pH 8,0. As folhas foram fotografadas em agarose com 1 Hm Nilo Vermelho. Barras de escala são 100 mm.

Figura 3. Digitalizando imagens de microscopia eletrônicade nanofolhas peptoid. Folhas foram formadas a partir de uma solução de 20 mM peptoid em 10 mM Tris, 100 mM NaCl, pH 8,0. Barras de escala são 5 mm.
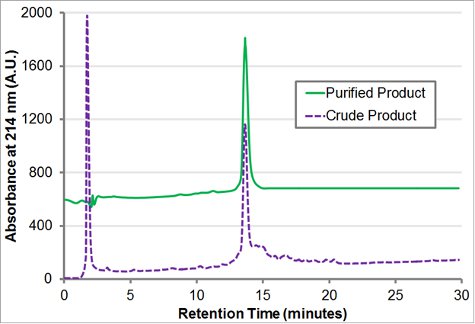
Figura 4 inverter fase analítica HPLC traço de H-[Nae-NPE] 9 -. [Nce-NPE] 9-NH 2. O petróleo bruto e purificado analítica HPLC trace (30-80% no gradiente 1 mL / min, durante 30 minutos a 60 ° C com um C18, 5 mm, 50 x coluna mm 2) do bloco bruto e purificado carga peptoid H-[ Nae-NPE] 9 - [NPE-nce] 9-NH 2 é mostrado.
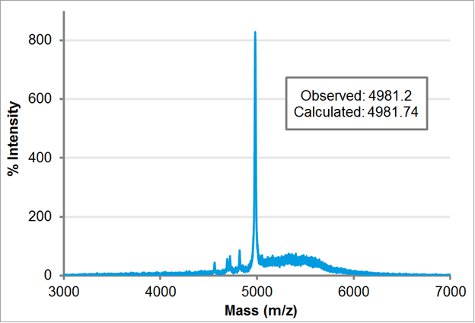
Figura 5 MALDI-TOF espectroscopia de massa traço de H-[Nae-NPE] 9 -. [Nce-NPE] 9-NH 2. A massa observada, 4981,2, está em estreita concordância com a massa calculada, 4981,74.
Discussão
Aplicações e Significado
Este protocolo descreve um método simples e eficiente de síntese peptoid eo aquosa auto-montagem do Peptóides em nanofolhas. A maioria dos laboratórios são facilmente capazes de sintetizar Peptóides porque os materiais de baixo custo, conhecimentos básicos e técnicas simples são utilizados 4. Da mesma forma, a auto-montagem de ultra-fina e altamente ordenada nanofolhas se limita a exigir repetidas frasco uma inclinação de uma solução aquosa diluída peptoid 2. Peptóides são promissores materiais para a pesquisa biomédica e nanociência, porque eles são robustos e flexíveis ainda sinteticamente seqüência específica e altamente sintonizável 5. Peptóides demonstraram atividade biológica (6,7 terapêutica, diagnóstico 8, a entrega intracelular 9-10) e dobra em nanoestruturas hierárquico 3, 11-14. Por causa de sua síntese modular, combinatória peptoid librAries 15-19 pode ser facilmente sintetizados e testados para uma ampla série de atividades ou propriedades. Em particular, o nanofolhas servir como uma plataforma potencial para andaimes bidimensional de exibição, miméticos de membrana, sensores biológicos, miméticos de proteínas e fabricação de dispositivos. Com as seqüências praticamente inesgotável diferentes possíveis, o campo da pesquisa peptoid está expandindo rapidamente.
Variáveis em fase sólida síntese submonomer de polypeptoids
Por causa da possibilidade de escolher entre um alfabeto incrivelmente grande e diversificada de monômeros de 20, o método submonomer precisa de modificações pontuais para casos em que o aumento da eficiência de acoplamento de cada etapa irá melhorar o rendimento global do produto. Incorporação de cadeias laterais desprotegidas heterocíclicos requer o uso de ácido cloroacético em vez de ácido bromoacetic 21. Maior tempo de deslocamento e maiorconcentrações de amina são geralmente empregadas após cerca de 20 engates para longas sequências peptoid ou aminas menos nucleofílico. Aquecimento do recipiente de reação a 35 ° C, usando um recipiente de reação de jaqueta de água, ajuda a conduzir a reação. Para altamente voláteis como aminas isopropilamina, cuidados devem ser tomados para evitar a evaporação.
Aminas na forma de um sal de HCl, como HCl beta-alanina t-butil, precisa ser livre baseado antes de ser introduzido na reação de deslocamento. Isto pode ser conseguido através da dissolução ou suspensão do amina em DCM (~ 5g amine/25 mL DCM), e neutralizar com uma solução equimolar de hidróxido de sódio aquoso em um funil de separação. A camada DCM é coletado ea camada aquosa é lavado com DCM adicionais. As camadas DCM combinados são secas sobre sulfato de sódio e filtrada para um balão de fundo pré-pesados rodada. Remover solvente por evaporação rotativa para produzir um óleo, e registrar o peso do produto.
During passo a clivagem, TFA cocktail de clivagem e tempo de clivagem é dependente do número e variedade de grupos protetores utilizados. Diretrizes para cocktails de clivagem são semelhantes aos tradicionais clivagens peptídeo desproteção 1. Geralmente, 10 minutos incubações são necessários para seqüências sem proteger grupos ou seqüências com poucos altamente ácido lábil grupos de proteção (por exemplo, BOC, por tritila). Duas horas incubações são recomendados para seqüências com mais difícil proteger os grupos (por exemplo, t-butil éster, Mtr, PBF) ou sequências com muitos grupos de proteção para garantir a desproteção total de cada cadeia. Crude produtos peptoid geralmente se dissolvem em acetonitrila: água 1:1 (v / v), mas maiores proporções de acetonitrila são comuns com cadeias laterais com uma alta hidrofobicidade global.
Divulgações
Não temos nada a revelar.
Agradecimentos
Os autores gostariam de agradecer Byoung-Chul Lee, Philip Choi e Samuel Ho para a assistência valiosa. Este trabalho foi realizado na Fundição Molecular do Lawrence Berkeley National Laboratory, que é apoiado pelo Escritório de Escritório Science, de ciências básicas da energia, do Departamento de Energia dos EUA no âmbito do contrato n º DE-AC02-05CH11231 e Redução de Ameaça de Defesa Agência nos termos do Contrato n º: IACRO-B0845281.
Materiais
| Name | Company | Catalog Number | Comments |
| Nome do reagente | Companhia | Número de catálogo | Comentários |
| Dimetilformamida | EMD | EM-DX1726P-1 | 99% + |
| N-methylpyrrolidinone | BDH | BDH1141-4LP | 99% |
| Ácido Bromoacetic | Acros Organics | 200000-106 | 99% |
| 4 Methylpiperidine | Sigma Aldrich | M73206 | 96% |
| N, N'-diisopropylcarbodiimide | Chem-Impex | 001100 | 99,5% |
| Diclorometano | EMD | EMD-DX0835 | ACS grau |
| Acetonitrila | EMD | EM-AX0145P-1 | 99,8% |
| Ácido trifluoroacético | Sigma Aldrich | T6508 | 99% |
| Triisopropylsilane | Sigma Aldrich | 233781 -10G | Para a clivagem TFA |
| 1,2-Dicloroetano | JT Baker | JTH076-33 | Para siliconização de vasos de reacção de vidro |
| Fenetilamina | Sigma Aldrich | 407267-100ML | > 99,5% Hydrophobic amina da cadeia lateral |
| Boc-etilenodiamina | CNH Technologies | C-1112 | Amina da cadeia lateral catiônicos |
| t-butil beta-alanina HCl | Chem-Impex Internacional | 04407 | Amina da cadeia lateral aniônicos |
| α-ciano-4-ácido hidroxicinâmicos | Sigma Aldrich | C8982-10X10MG | Para MALDI matriz |
| Nile Red | Sigma Aldrich | 19123-10mg | Para fluorescência de imagem |
| Dichlorodimethylsilane | Sigma Aldrich | 80.430-F-500G | Para siliconização de vasos de reacção de vidro |
| Carrinho PP descartáveis frittedcume | Separações Aplicada | 2416 | 6 mL de polipropileno cartucho com 20 milímetros PE fritas |
| Descartáveis de 3 vias luer adaptador | Cole Parmer | 31200-80 | Torneira para descartáveis vaso de reação manual de síntese |
| Luer Lock Ring | Cole Parmer | 45503-19 | ¼ fitting "para o recipiente de reação manual de síntese descartáveis |
| Acessórios Luer | Cole Parmer | 45500-20 | ¼ fitting "para o recipiente de reação manual de síntese descartáveis |
| Descartáveis PP pipetas | VWR | 16001-194 | Para transferências de TFA |
| Luer seringa de plástico bloqueio | Científica Nacional | S7515-5 | 6 seringas mL |
| Um frasco de vidro dram | VWR | 66011-041 | Com resinas fenólicas moldado com tampa de rosca de polivinil-faced forro de celulose |
| 20 mL Scinfrasco tillation | VWR | 66022-060 | Com tampa de PP em anexo e liner folha de celulose |
| Seguro-Seal espaçador adesiva | Invitrogen | S-24736 | Para fluorescência de imagem |
| Lâminas de vidro | Microscopia Eletrônica de Ciências | 63411 | Para fluorescência de imagem |
| Tampa de deslizamento | VWR | 48366-067 | Para fluorescência de imagem |
| 4 pastilha de silício " | Ted Pella | 16007 | Pré-dice em fichas milímetros 5x7 |
| 0,45 filtro | VWR, Acrodisc | 28143-924 | Para HPLC. Membrana de PTFE |
| Agarose | BD | 212272 | Para fluorescência de imagem |
| SPE Manifold a vácuo | Sigma Aldrich | 57044 | Exemplo de múltiplas vácuo SPE |
| Vaso poroso de vidro | Ace vidro | 6402-12 | Porosidade Cfrita |
| Plasma Cleaner / Esterilizador | Harrick Plasma | PDC-32G | Exemplo de produto de limpeza de plasma para preparar chips de silício para SEM |
Referências
- King, D. S., Fields, C. G., Fields, G. B. A cleavage method which minimizes side reactions following Fmoc solid phase peptide synthesis. Int. J. Pept. Pro. Res. 36, 255-266 (1990).
- Sanii, B., Kudirka, R., Cho, A., Venkateswaran, N., Oliver, G. K., Olson, A. M., Tran, H., Harada, R. M., Tan, L., Zuckermann, R. N. Shaken, not stirred: Collapsing a peptoid monolayer to produce free-floating, stable nanosheets. J. Am. Chem. Soc. , (2011).
- Kudirka, R., Tran, H., Sanii, B., Nam, K. T., Choi, P. H., Venkateswaran, N., Chen, R., Whitelam, S., Zuckermann, R. N. Folding of a single-chain, information-rich polypeptoid sequence into a highly-ordered nanosheet. Bioploymers: Peptide Science. 96, 586-595 (2011).
- Utku, Y., Rohatgi, A., Yoo, B., Zuckermann, R., Pohl, N., Kirshenbaum, K. Rapid multistep synthesis of a bioactive peptidomimetic oligomer for the undergraduate laboratory. J. Chem. Ed. 87, 637-639 (2010).
- Fowler, S. A., Blackwell, H. E. Structure-function relationships in peptoids: Recent advances toward deciphering the structural requirements for biological function. Org. Biomol. Chem. 7, 1508-1524 (2009).
- Zuckermann, R. N., Kodadek, T. Peptoids as potential therapeutics. Curr. Op. Mol. Ther. 11, 299-307 (2009).
- Chongsiriwatana, N. P., Patch, J. A., Czyzewski, A. M., Dohm, M. T., Ivankin, A., Gidalevitz, D., Zuckermann, R. N., Barron, A. E. Peptoids that mimic the structure, function and mechanism of helical antimicrobial peptides. , 105-2794 (2008).
- Yam, A. Y., Wang, X., Gao, C., Connolly, M. D., Zuckermann, R. N., Bleua, T., Halla, J., Fedynyshyn, J., Allauzen, S., Peretz, D., Salisbury, C. M. A Universal method for detection of amyloidogenic misfolded proteins. Biochem. 50, 4322-4329 (2011).
- Huang, C. -. Y., Uno, T., Murphy, J. E., Lee, S., Hamer, J. D., Escobedo, J. A., Cohen, F. E., Radhakrishnan, R., Dwarki, V., Zuckermann, R. N. Lipitoids - novel cationic lipids for cellular delivery of plasmid DNA in vitro. Chem. Biol. 5, 345-354 (1998).
- Schroeder, T., Niemeier, N., Afonin, S., Ulrich, A. S., Krug, H. F., Bräse, S. Peptoidic amino- and guanidinium-carrier systems: Targeted drug delivery into the cell cytosol or the nucleus. J. Med. Chem. 51, 376-379 (2008).
- Murnen, H. K., Rosales, A. M., Jaworski, J. N., Segalman, R. A., Zuckermann, R. N. Hierarchical self-assembly of a biomimetic diblock copolypeptoid into homochiral super helices. J. Am. Chem. Soc. 132, 16112-16119 (2010).
- Nam, K. T., Shelby, S. A., Marciel, A. B., Choi, P. H., Chen, R., Tan, L., Chu, T. K. Free-floating ultra-thin two-dimensional crystals from sequence-specific peptoid polymers. Nature. Mater. 9, 454-460 (2010).
- Burkoth, T. S., Beausoleil, E., Kaur, S., Tang, D., Cohen, F. E., Zuckermann, R. N. Toward the synthesis of artificial proteins: The Discovery of an amphiphilic helical peptoid assembly. Chemistry & Biology. 9, 647-654 (2002).
- Murphy, J. E., Uno, T., Hamer, J. D., Cohen, F. E., Dwarki, V., Zuckermann, R. N. A Combinatorial approach to the discovery of efficient cationic peptoid reagents for gene delivery. Proc. Natl. Acad. Sci. U. S. A. 95, 1517-1522 (1998).
- Mora, P. u. i. g., Masip, I. s. a. b. e. l., Cortés, N. u. r. i. a., Marquina, R. e. g. i. n. a., Merino, R. a. m. &. #. 2. 4. 3. ;. n., Merino, J. e. s. &. #. 2. 5. 0. ;. s., Carbonell, T. e. r. e. s. a., Mingarro, I. s. m. a. e. l., Messeguer, A. n. g. e. l., Pérez-Payá, E. n. r. i. q. u. e. Identification from a positional scanning peptoid library of in vivo active compounds that neutralize bacterial endotoxins. J. Med. Chem. 48, 1265-1268 (2005).
- Zuckermann, R. N. Discovery of nanomolar ligands for 7-transmembrane G-protein coupled receptors from a diverse (N-substituted)glycine peptoid Library. J. Med. Chem. 37, 2678-2685 (1994).
- Alluri, P., Liu, B., Yu, P., Xiao, X., Kodadek, T. Isolation and characterization of coactivator-binding peptoids from a combinatorial library. Moleular Biosystems. 2, 568-579 (2006).
- Figliozzi, G. M., Goldsmith, R., Ng, S., Banville, S. C., Zuckermann, R. N. Synthesis of N-(substituted)glycine peptoid libraries. Methods Enzymol. 267, 437-447 (1996).
- Culf, A. S., Ouellette, R. J. Solid-phase synthesis of N-substituted glycine oligomers (α peptoids) and derivatives. Molecules. 15, 5282-5335 (2010).
- Burkoth, T. S., Fafarman, A. T., Charych, D. H., Connolly, M. D., Zuckermann, R. N. Incorporation of unprotected heterocyclic side chains into peptoid oligomers via solid-phase submonomer synthesis. J. Am. Chem. Soc. 125, 8841-8845 (2003).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados