Method Article
Sintesi in fase solida Submonomer dei Polimeri Peptoid e il loro self-assembly in altamente ordinato nanosheets
In questo articolo
Riepilogo
Un manuale semplice e generale metodo di sintesi peptoid con attrezzature di base e dei reagenti disponibili in commercio è delineato, consentendo peptoids per essere facilmente sintetizzati nella maggior parte dei laboratori. La sintesi, purificazione e caratterizzazione di un 36mer peptoid anfifilici è descritto, così come la sua auto-assemblaggio in altamente ordinato nanosheets.
Abstract
Peptoids sono una nuova classe di biomimetici, non naturali, sequenza-specifica heteropolymers che resistono proteolisi, mostra una potente attività biologica, e piegare in nanostrutture di ordine superiore. Strutturalmente simili ai peptidi, peptoids sono poli per sostituzione glycines, su cui sono fissati le catene laterali al di azoto piuttosto che l'alfa-carbonio. La loro facilità di sintesi e diversità strutturale consente la sperimentazione di principi di progettazione fondamentali per guidare de novo di progettazione e ingegneria di nuovi materiali biologicamente attivi e nanostrutturati.
Qui, un semplice manuale peptoid protocollo sintesi viene presentata, che permette la sintesi di polypeptoids lunga catena (fino a 50mers) dei rendimenti eccellenti. Solo le attrezzature di base, semplici tecniche (ad esempio liquido trasferimento, filtrazione) e reagenti disponibili in commercio sono tenuti, rendendo peptoids un'aggiunta accessibile a toolkit molti ricercatori '. La spina dorsale peptoid si coltiva un monomero in un tempo vtra l'altro il metodo submonomer che consiste in due passi Oltre ciclo monomero: acilazione e spostamento. In primo luogo, l'acido bromoacetico attivate in situ con N, N-diisopropylcarbodiimide acylates una resina-legato amine secondarie. In secondo luogo, lo spostamento nucleofila del bromuro di un'ammina primaria segue l'introduzione della catena laterale. Le due fasi del ciclo è iterato fino a quando la lunghezza della catena desiderata. L'efficienza di questo accoppiamento in due fasi di ciclo supera regolarmente il 98% e permette la sintesi di peptoids i 50 residui. Diverse sequenze altamente configurabile, preciso e chimicamente sono raggiungibili con il metodo submonomer centinaia di ammine primarie prontamente disponibili possono essere direttamente incorporati.
Peptoids stanno emergendo come un materiale versatile biomimetici per la ricerca Nanobioscience a causa della loro sintesi flessibilità, robustezza, e ordinare a livello atomico. La piegatura di una singola catena, anfifilici, informazionizione ricca di polypeptoid in una altamente ordinato nanosheet è stato recentemente dimostrato. Questo peptoid è un 36-mer, che consiste in soli tre monomeri diversi disponibili in commercio: idrofobo, cationici e anionici. Le catene laterali idrofobiche feniletil sono sepolti nel nucleo nanosheet mentre l'ammina ionica e catene laterali carbossilico allinearsi sulle facce idrofilo. Il nanosheets peptoid fungere da piattaforma potenziale di mimetici di membrana, di proteine mimetici, fabbricazione del dispositivo, e sensori. Metodi per la sintesi peptoid, formazione del foglio, e immagini di microscopia sono descritti e fornire un metodo semplice per realizzare in futuro progetti nanosheet peptoid.
Protocollo
1. Sintesi in fase solida Submonomer di Polypeptoids
Sintesi in fase solida (SPS) è una tecnica comune usata per sintetizzare sequenza-specifica biopolimeri graduale, direttamente su un supporto solido inerte come un cordone di resina polimerica. Elevate rese di accoppiamento e la facilità di rimozione reagente in eccesso sono i vantaggi principali di SPS. Dopo una reazione di accoppiamento per la resina, i reagenti in eccesso sono semplicemente svuotato e le perline vengono lavati per essere pronti per la successiva fase di reazione. Dopo la reazione di sintesi finale, il full-length oligomeri sono spaccati dalla resina e la soluzione fase materiale può essere ulteriormente studiati. Qui, adattare la procedura SPS per generare la sequenza specifici polimeri peptoid.
- Setup: Tutte le fasi della sintesi peptoid manuale può essere effettuata in un usa e getta, polipropilene (PP) cartuccia poroso sinterizzato o un recipiente di reazione di vetro dotato di un rubinetto a 3 vie. Eseguire tutte le operazioni in una cappa aspirante. Per incubazioni in gnave lass o della cartuccia di plastica, collegare un braccio per una fornitura di azoto a bolla delicatamente la soluzione per la corretta miscelazione. In alternativa, per incubazioni reazione nella cartuccia usa e getta, sigillare entrambe le estremità della cartuccia con tappi e posto su un agitatore rotante. Per scaricare miscele di reazione o lava, la connessione a casa vuoto mediante una trappola dei rifiuti. Il vaso deve essere poroso con una fritta ruvida. Siliconize il recipiente di vetro per evitare di perline di attaccarsi alle pareti del recipiente di vetro. Preparare una soluzione del 5% dichlorodimethylsilane in dicloroetano (v / v). Riempire un contenitore pulito e asciutto reazione verso l'alto con la soluzione siliconatura, lasciate riposare per 30 minuti, poi scolateli. Lavare il vaso una volta con DCE e poi una volta con il metanolo. La soluzione siliconatura possono essere riutilizzati, quindi dovrebbe essere salvato. Sia aria secca o scrollarsi di dosso qualsiasi soluzione in eccesso e cuocere fino a quando la vetreria a secco dopo aver rimosso il rubinetto. Reazione nave raffreddare prima di aggiungere resina.
- Aggiungere 100 mg (0,06 mmol) di re Rink amidepeccato per un vaso di reazione poroso. Swell la resina con l'aggiunta di 2 ml di dimetilformammide (DMF). Agitare agitando o immissione per 10 minuti. Scolate la soluzione vuoto per isolare la resina si gonfiò.
- Aggiungere 1 ml di 20% 4-methylpiperidine in DMF (v / v) Deprotect gruppo Fmoc. Agitare per 2 minuti e scolateli. Ripetere con una incubazione 12 minuti.
- Sciacquare la resina con l'aggiunta di 2 ml di DMF, agitando per 15 secondi, e drenante. Ripeti 3 volte.
- Bromoacetylation: Aggiungere 1 ml di 0,6 M bromoacetico acido (0,6 mmol) in DMF e 86 ml di N, N-diisopropylcarbodiimide (0,93 equivalente, 0,56 mmol). Incubare con bolle dolce per 30 minuti, quindi scolare e sciacquare con 2 ml di DMF (ripetizione 4x).
- Cilindrata: Aggiungere 1 ml di 1-2 M amine in N-methylpyrrolidinone. Incubare con bolle di 30-120 minuti, quindi scolare e sciacquare con DMF (4x 2 mL).
- Continua a crescere la catena peptoid ripetendo il ciclo submonomer, passi 1,5 (bromoacetylation) e 1,6 (displacement).
- Dopo lo spostamento finale è fatto, sciacquare con 2 ml di DMF (repeat 4x), quindi 2 ml di diclorometano (ripetere 3 volte). Cap e conservare il recipiente di reazione fino scissione.
- Pausa in sintesi (opzionale): Per mettere in pausa durante una sintesi peptoid, finire la reazione di spostamento e passare al punto 1.8. Per continuare a crescere la catena peptoid, riavviare la sintesi di ri-rigonfiamento della resina secca (punto 1.2) e ripetendo il ciclo submonomer (punto 1.5 e 1.6). La resina può essere essiccati e conservati dopo ogni spostamento, tranne lo spostamento secondo perché la resina peptoid coniugato può formare un prodotto ciclico laterale dichetopiperazina.
- Per più sintesi simultanea, una fase solida collettore di vuoto estrazione è consigliabile per massimizzare l'efficienza. Sintesi Peptoid può anche essere automatizzato con la corretta programmazione metodi di sintetizzatori di peptidi disponibili in commercio, come il Apex Aapptec 396, CEM sintetizzatore a microonde Liberty e Techno Proteinelogie Inc. Preludio sintetizzatore.
2. Scissione e di side-chain deprotezione
- Trasferire tutti i resina essiccata per un flaconcino da 20 ml in vetro scintillazione.
- Lavorare all'interno di un cappuccio e con un equipaggiamento individuale protettivo, aggiungere 4 ml di acido trifluoroacetico (TFA) scissione cocktail 1 (es. 95% aq. TFA, vedi la discussione) al flacone di vetro e tappo di scintillazione. Agitare per 10 minuti a 2 ore a temperatura ambiente (vedi la discussione).
- Raccogliere la soluzione scissione TFA filtrando la resina con una usa e getta, cartuccia PP poroso in una nuova pre-pesava 20 flacone di vetro scintillazione ml. Un usa e getta, PP pipetta è conveniente per trasferire le soluzioni scissione cocktail.
- Aggiungere 1 ml di cocktail scissione fresca per risciacquare la resina e raccogliere qualsiasi peptoid residuo. Ripetere 2x.
- Evaporare TFA soffiando una leggera corrente di azoto o utilizzando un Biotage V10 evaporatore.
- Riprendere il petrolio greggio in 6 mLdi acetonitrile / acqua 1:1 (v / v) per HPLC. Freeze e liofilizzare. Ripeti.
- Registrare il peso del prodotto grezzo. Archiviare come una polvere secca a -20 ° C
- Scissione di prova (opzionale): Una scissione di prova sul 0,5% della resina può essere eseguita per determinare rapidamente la purezza e la massa del peptoid sintetizzati e se le condizioni di scissione sono state scelte corrette. Divisioni di prova sono particolarmente utili per monitorare l'andamento della sintesi.
3. Caratterizzazione e purificazione del Polypeptoid
- Attraverso una combinazione di analisi HPLC, electrospray LC-MS, e / o MALDI-TOF, determinare la purezza del prodotto grezzo e se il peso desiderato molecolare è presente.
- Preparare una ~ 5-10 mg / ml soluzione della polvere secca peptoid in acqua con acetonitrile come minimo necessario per solubilità. Filtro soluzione limpida di greggio prodotto peptoid con filtro da 0,45 micron siringa per rimuovere polvere e particelle.
- Analitici HElectrospray PLC e LC-MS: Preparare una ~ 20 mg / ml soluzione greggio peptoid. Filtro 200 l con un filtro da 0,45 micron e iniettare 20 l.
- MALDI: Miscelare 1 ml di ~ 20 mg / mL peptoid con 1 matrice microlitri. Spot 1 ml sulla piastra MALDI e lasciare asciugare all'aria. Matrix e modalità di acquisizione dipende dal campione (Fig. 5).
- Purificare la miscela grezza peptoid con inversione di fase di preparazione HPLC. Scegli il gradiente e la colonna (C4 o C18) in base alla idrofobicità di polypeptoid. Combina purificata frazioni, congelare, e liofilizzare, risultando in un soffice polvere bianca. Registrare il peso del prodotto finale.
- Formazione di HCl sale (opzionale): Riprendere la polvere liofilizzata in 100 mM HCl (aq.) con acetonitrile minima. Trasferimento pre-pesato flaconcino di vetro. Congelamento e ri-liofilizzare. Ripetere 2x. Pesare per determinare la massa di polvere peptoid.
4. Nanosheet Formazione Peptoid
Questa sezione describes il protocollo per formare fogli da una catena singola, specifica sequenza, anfifilici 36-mer peptoid (Fig. 1). Dopo il filone peptoid è sintetizzato, purificata e liofilizzati come sopra descritto, la polvere bianca è sciolto in DMSO per fare una soluzione madre 2 mM.
- Preparare 500 ml di soluzione di 20 mM peptoid nel buffer foglio formazione (10 mM Tris-HCl, 100 mM NaCl, pH 8.0 in acqua) in un flaconcino 1 bicchierino di vetro. In primo luogo, aggiungete 445 ml di acqua Milli-Q, 50 ml di tampone 10x formazione del foglio, e vortex per miscelare. Poi, aggiungere 5 ml di soluzione 2 magazzino peptoid mM e delicatamente soluzione turbinio. Tappo del flaconcino di vetro.
- Fogli sono formati dalla agitazione della soluzione acquosa diluita peptoid. Lentamente inclinando il flacone di vetro dalla posizione orizzontale a posizione verticale i risultati in fogli. Gentle scuotendo produce anche schede, tuttavia, i fogli tendono ad essere più piccoli e con meno bordi dritti. Un'analisi più approfondita del meccanismo di formazione del foglio è Reported separatamente 2.
- Per molti di alta qualità lenzuola, ruotare le fiale di vetro intorno all'asse orizzontale lentamente (<1 rpm) per 1-3 giorni. Un risorse tecniche adeguate RKVSD rotatori tubo Rotamix o un rocker personalizzato in grado di eseguire questo continuo.
- Dialisi di nanosheets (opzionale): In alcune applicazioni, può essere necessario rimuovere qualsiasi catene libero peptoid o buffer / sali. Immergere un Float-a-Lyzer 100 kD membrana nel buffer desiderato per 15 minuti. Carico 500 microlitri soluzione foglio peptoid nell'apposita camera. Mettere a bagno in 500 ml di tampone desiderato, mescolando con un ancoretta magnetica a 60 giri. Lasciare dialisi di fogli di procedere per 4 ore. Ogni, cambio ora con un ramo nuovo di soluzione tampone.
5. Microscopia di fluorescenza di nanosheets
- Immagini di fluorescenza del nanosheets erano ripreso con Nile Red, un colorante ecologicamente sensibili la cui intensità di fluorescenza aumenta quando è localizzata in hydrambienti ophobic (Fig. 2).
- Aggiungere 1 ml di 100 mM Nile Red a 100 microlitri della soluzione nanosheet per ottenere una concentrazione finale di 1 mM di Nile Red.
- Fare una soluzione all'1% di agarosio in acqua calda e versare in un piatto di plastica Petri. Garantire la soluzione di agarosio è di circa 1 / 8 pollici di spessore e lasciare raffreddare la soluzione indisturbato su una superficie piana. Dopo il set di agarosio, utilizzare una spatola per tagliare e trasferire 1 cm x 1 cm quadrati un vetrino.
- Per raccogliere i fogli sullo stesso piano, punto 1 ml di soluzione foglio sul pezzo di agarosio. Lasciare l'agarosio per assorbire il buffer per 2 minuti, lasciando i fogli in superficie. Immagine entro 15 minuti, altrimenti il agarosio inizierà a deformarsi a causa della disidratazione.
- Ai fogli di immagine in soluzione, 15 microlitri di carico all'interno di un 20 mm di diametro 0,12 guarnizione mm su un vetrino. Coprire con un coprioggetto. Se i fogli sono semplicemente inserita tra un vetrino e coprioggetto senza una guarnizione, molti fogli will taglio e l'evaporazione apparentemente minore causerà i fogli di muoversi in continuazione.
- Fogli immagine sotto illuminazione epifluorescenza (ad esempio un Olympus IX81 microscopio invertito dotato di un iXonEM Andor spettri + EMCCD con un filtro rosso del Texas).
6. Microscopia elettronica a scansione (SEM) di nanosheets
- Etch su substrato di silicone (opzionale) Plasma: I chip di silicio vengono incise al plasma per aiutare nella adsorbimento di fogli. Posizionare il chip di silicio nella camera a vuoto di un pulitore di plasma (es. Harrick Plasma Cleaner / Sterilizzatore PDC-32G). Pompa fino a 200 mTorr e impostare la bobina RF di 18W (impostazione alta per PDC-32G). Etch per 2 minuti.
- Calo del 20 ml di soluzione su un foglio peptoid plasma trattato substrato di silicio. Lasciare riposare per 3 minuti. Rimuovere la soluzione in eccesso con la punta di Kim-wipe. Pipettare 20 ml di acqua sulla superficie e rimuovere la soluzione in eccesso di nuovo per rimuovere tampone e sali. Ripetere 4 volte.
- In alternativa, comporreyze le soluzioni foglio peptoid contro l'acqua per rimuovere tampone e il sale. Calo del 20 ml di soluzione foglio dializzati sul plasma trattati con substrati di silicio. Aria secca del campione.
- Fogli con immagini SEM (ad esempio Zeiss Gemini Ultra-55 Analytical microscopio elettronico a scansione) con un in-lente rivelatore e ad energie del fascio tra 1 kV e 5 kV (Fig. 3).
7. Note sulla sicurezza:
- Dimetilformammide e diclorometano sono ragionevolmente sospettati agenti cancerogeni.
- N, N-Diisopropylcarbodiimide, 4-methylpiperdine e acido bromoacetico sono pericolosi per la pelle, occhi e vie respiratorie. Essi devono essere utilizzati nel cofano con cura. Può essere tossico se inalato o assorbito attraverso la pelle, e l'esposizione può provocare sensibilizzazione. I contenitori vuoti trattengono residui di prodotto (liquido / vapore) e deve essere accuratamente sciacquati prima di rimuoverle dal cofano.
- TFA è un acido forte, ed è estremamente distruttivo per il tratto respiratorio superiore, occhi epelle. TFA è anche volatili mantenere soluzioni concentrate di TFA nel cappuccio in qualsiasi momento per evitare danni respiratori. Corretto uso DPI, e l'attenzione durante la manipolazione di soluzioni di TFA. Guanti di cambiare immediatamente se entrano in contatto con TFA, e subito ripulire eventuali fuoriuscite.
8. Rappresentante dei risultati:
Questa sezione descrive la sintesi, caratterizzazione e purificazione di una sequenza-specifica 36-mer catena peptoid che si ripiega in una altamente ordinata nanosheet 3 (Fig. 1).
Il blocco-charge peptoid H-[Nae-NPE] 9 - [NCE-NPE] 9-NH 2 è stato sintetizzato in 100 mg di resina Rink amide. Una soluzione di ammina M 2 è stato utilizzato per tutte le reazioni di spostamento, che sono state effettuate per 60 minuti per i residui 1-18 e 120 minuti per i residui 19-36. t-butil beta-alanina HCl è stato convertito in base libera (vedi la discussione), mentre phenethylamine e Boc-etilendiammina erano entrambi directl utilizzatiy. La resina è stata tagliata con il 95% TFA, triispropylsilane 2,5%, 2,5% di acqua per 2 ore. TFA era evaporata e l'olio viscoso risultante (~ 180 mg) è stato re-sciolta in 6 mL acetonitrile: acqua 1:1 (v / v). La purezza del prodotto (Fig. 4) e la presenza della massa del prodotto è stata confermata da analisi di RP-HPLC (30-80% di pendenza acetonitrile acqua, entrambi contenenti 0,1% (v / v) TFA, a 1 mL / min per 30 minuti a 60 ° C con una C18, 5 micron, 50 x 2 mm di colonna) e MALDI (Fig. 5).
Depurazione mediante HPLC in fase inversa su una colonna Vydac C18 (10 micron, 22 mm x 250 mm) ha proceduto, con una pendenza del 30-60% acetonitrile in acqua con 0,1% TFA più di 60 minuti a 10 mL / min. La colonna è stato caricato con 60 mg di prodotto grezzo per ogni corsa cromatografica. Le frazioni purificate sono state combinate basato sulla purezza di analisi RP-HPLC (Fig. 4) e liofilizzato per produrre ~ 80 mg di una polvere bianca soffice.
Purificato blocco carica peptoid molecolareil peso è stato confermato da MALDI. 1 ml di 100 mM purificato peptoid in acetonitrile: acqua 1:1 (v / v) è stato mescolato con 1 ml di matrice (5 mg / ml di α-ciano-4-idrossicinnamici acido in acetonitrile: acqua 1:1 v / v e 0,1% TFA) e 1 ml è stato avvistato sulla piastra MALDI. Dopo che il campione essiccato all'aria, è stata collocata nella Applied Biosystems / MDS SCIEX 4800 MALDI TOF / TOF Analyzer. Le modalità di acquisizione ed elaborazione sono stati lineari di piccola massa. Il peso calcolato è stato inserito nella massa mirate per regolare automaticamente il tempo di ritardo. L'intensità del laser è stata impostata a 3400. La massa osservata, 4981,2, fiammiferi vicino a calcolare la massa di 4981,74.
La polvere liofilizzata purificato è stato dissolto in DMSO per fare una soluzione stock 2 mm, che possono essere conservati a 4 ° C. Schede sono state preparate dal protocollo di cui sopra e ripreso con fluorescenza microscopia ottica e SEM (Fig. 2 e 3). Una varietà di forme con dimensioni caratteristiche che vanno fino a 300 micron vengono osservati, e notabLy, bordi diritti sono prominenti.

Figura 1 Sequenza del blocco carica peptoid H-[Nae-NPE] 9 -. [NCE-NPE] 9-NH 2. Una singola catena, carica blocco, polypeptoid anfifilici 36-mer auto-assembla in altamente ordinato, bidimensionale nanosheets 3. Il peso molecolare è calcolato 4981,74.

Figura 2. Immagini di microscopia a fluorescenza di nanosheets peptoid. Lenzuola erano formati da una soluzione al 20 mM peptoid in 10 mM Tris, 100 mM NaCl, pH 8.0. Le lenzuola erano proietta sulla agarosio con 1μM Nile Red. Barre di scala sono 100 micron.

Figura 3. Acquisizione di immagini di microscopia elettronicadi nanosheets peptoid. Lenzuola erano formati da una soluzione al 20 mM peptoid in 10 mM Tris, 100 mM NaCl, pH 8.0. Barre di scala sono 5 micron.
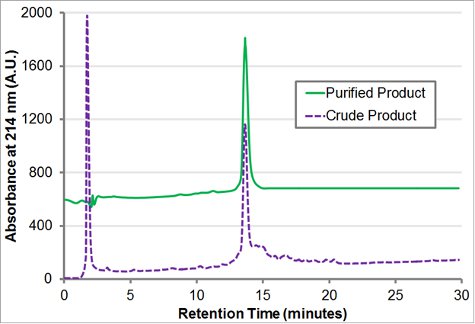
Figura 4 analitica HPLC in fase inversa traccia di H-[Nae-NPE] 9 -. [NCE-NPE] 9-NH 2. Il greggio e purificato analitiche HPLC traccia (30-80% di pendenza a 1 ml / min più di 30 minuti a 60 ° C con una C18, 5 micron, 50 x 2 mm di colonna) del greggio e purificato blocco carica peptoid H-[ Nae-NPE] 9 - [NCE-NPE] 9-NH 2 è indicata.
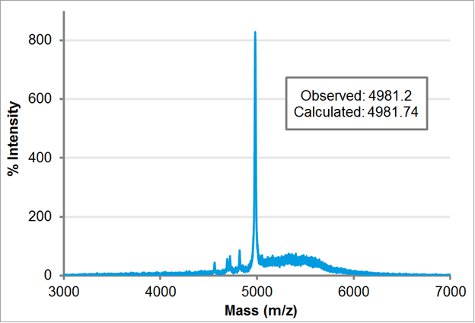
Figura 5 MALDI-TOF spettroscopia di massa traccia di H-[Nae-NPE] 9 -. [NCE-NPE] 9-NH 2. La massa osservata, 4981,2, è in accordo vicino alla massa calcolata, 4981,74.
Discussione
Applicazioni e Significato
Questo protocollo descrive un metodo semplice ed efficiente di sintesi peptoid e acquosa auto-assemblaggio del peptoids in nanosheets. La maggior parte dei laboratori sono facilmente in grado di sintetizzare peptoids quanto i materiali poco costosi, competenze di base e le tecniche semplici sono utilizzati 4. Allo stesso modo, l'auto-assemblaggio di ultra-sottile, altamente ordinato nanosheets richiede semplicemente ripetuto inclinando un flacone di una soluzione acquosa diluita peptoid 2. Peptoids sono promettenti materiali per la ricerca biomedica e la nanoscienza, perché sono robusti e flessibili ma sinteticamente sequenza-specifica e altamente configurabile 5. Peptoids hanno dimostrato l'attività biologica (6,7 terapeutici, diagnostici 8, consegna intracellulare 9-10) e pieghevole in nanostrutture gerarchico 3, 11-14. A causa della loro sintesi modulare, combinatoria peptoid librAriete 15-19 possono essere facilmente sintetizzati e sottoposti a screening per un'ampia serie di attività o proprietà. In particolare, il nanosheets fungere da piattaforma per il potenziale bidimensionale ponteggi schermo, mimetici di membrana, sensori biologici, mimetici proteine e fabbricazione del dispositivo. Con le sequenze praticamente inesauribile diverse possibili, il mondo della ricerca peptoid si sta rapidamente espandendo.
Variabili in sintesi in fase solida submonomer di polypeptoids
A causa della possibilità di scegliere tra un alfabeto incredibilmente vasta e diversificata di monomeri 20, il metodo submonomer esigenze modifiche occasionali nei casi in cui aumentare l'efficienza di accoppiamento di ogni passo sarà migliorare la resa complessiva del prodotto. Incorporazione di catene laterali non protetti eterociclici richiede l'uso di acido cloroacetico invece di acido bromoacetico 21. Tempi di spostamento estesi e superioriconcentrazioni di ammina sono di solito impiegati dopo circa 20 giunti per lunghe sequenze peptoid o ammine meno nucleofilo. Riscaldamento del recipiente di reazione a 35 ° C, utilizzando un vaso con camicia d'acqua di reazione, aiuta a provocare la reazione. Per altamente volatili, ammine, come isopropilamminico, bisogna fare attenzione per evitare l'evaporazione.
Ammine in forma di sale HCl, come t-butil beta-alanina HCl, hanno bisogno di essere liberi-based prima di essere introdotti nella reazione spostamento. Ciò può essere ottenuto sciogliendo o sospendendo l'ammina in DCM (~ 5g amine/25 mL DCM), e neutralizzare con una soluzione equimolare di idrossido di sodio in acqua in un imbuto separatore. Lo strato di DCM è raccolta e lo strato acquoso viene lavata con DCM aggiuntivi. Gli strati DCM combinate sono seccato su solfato sodico e filtrata in un pallone pre-pesato fondo rotondo. Rimuovere il solvente per evaporazione rotante per produrre un olio, e registrare il peso del prodotto.
During il passo scissione, cocktail scissione TFA e il tempo scissione dipende dal numero e dalla varietà dei gruppi protettori utilizzati. Linee guida per cocktail scissione sono simili a spaccature tradizionali deprotezione peptide 1. In generale, 10 incubazioni minuti sono necessari per le sequenze senza proteggere i gruppi o le sequenze con pochi gruppi fortemente acido labile proteggere (ad esempio BOC, tritil). Due incubazioni ora sono raccomandati per le sequenze con gruppi protettori più difficili (ad esempio t-butile, Mtr, PBF) o sequenze con molti gruppi protettori per assicurare deprotezione completo di ogni catena. Greggio prodotti peptoid generalmente si dissolvono in acetonitrile: acqua 1:1 (v / v), ma le proporzioni acetonitrile superiori sono comuni con catene laterali con un idrofobicità complessivo elevato.
Divulgazioni
Non abbiamo nulla da rivelare.
Riconoscimenti
Gli autori desiderano ringraziare Byoung-Chul Lee, Philip Ho Choi e Samuel per la preziosa assistenza. Questo lavoro è stato svolto presso la Fonderia molecolare presso il Lawrence Berkeley National Laboratory, che è sostenuto da parte dell'Ufficio della Scienza, Ufficio di Basic Sciences Energia, del Dipartimento dell'Energia degli Stati Uniti nell'ambito del contratto n. DE-AC02-05CH11231 e la Defense Threat Reduction Agenzia con il n. di contratto: IACRO-B0845281.
Materiali
| Name | Company | Catalog Number | Comments |
| Nome del reagente | Azienda | Numero di catalogo | Commenti |
| Dimetilformammide | EMD | EM-DX1726P-1 | 99 +% |
| N-methylpyrrolidinone | BDH | BDH1141-4LP | 99% |
| Acido bromoacetico | Acros Organics | 200000-106 | 99% |
| 4-Methylpiperidine | Sigma Aldrich | M73206 | 96% |
| N, N-diisopropylcarbodiimide | Chem-Impex | 001100 | 99,5% |
| Diclorometano | EMD | EMD-DX0835 | ACS grado |
| Acetonitrile | EMD | EM-AX0145P-1 | 99,8% |
| Acido trifluoroacetico | Sigma Aldrich | T6508 | 99% |
| Triisopropylsilane | Sigma Aldrich | 233781 -10G | Per la scissione TFA |
| 1,2-Dicloroetano | JT Baker | JTH076-33 | Per siliconization di reattori di vetro |
| Phenethylamine | Sigma Aldrich | 407267-100ML | > 99,5% idrofobico della catena laterale ammina |
| Boc-etilendiammina | CNH Technologies | C-1112 | Cationici side-chain ammina |
| t-butil beta-alanina HCl | Chem-Impex internazionale | 04407 | Anionici side-chain ammina |
| α-ciano-4-acido idrossicinnamici | Sigma Aldrich | C8982-10X10MG | Per MALDI matrice |
| Nile Red | Sigma Aldrich | 19123-10mg | Imaging per fluorescenza |
| Dichlorodimethylsilane | Sigma Aldrich | 80430-500G-F | Per siliconization di reattori di vetro |
| Monouso PP carrello porosocrinale | Separazioni applicata | 2416 | 6 ml in polipropilene cartuccia con 20 mm in PE fritta |
| Usa e getta a 3 vie luer adattatore | Cole Parmer | 31200-80 | Rubinetto per monouso nave reazione di sintesi manuale |
| Luer Lock anello | Cole Parmer | 45503-19 | ¼ "usa e getta per il montaggio manuale nave reazione di sintesi |
| Raccordi Luer | Cole Parmer | 45500-20 | ¼ "usa e getta per il montaggio manuale nave reazione di sintesi |
| Monouso PP pipette | VWR | 16001-194 | Per i trasferimenti TFA |
| Luer lock siringa di plastica | Scientifico Nazionale | S7515-5 | 6 siringhe mL |
| 1 bicchierino di vetro fiala | VWR | 66011-041 | Con fenolici stampato tappo a vite con polivinile faccia fodera polpa |
| 20 ml Scinlazione fiala | VWR | 66022-060 | Con annesso cappuccio in PP e fogli di rivestimento polpa |
| Secure-sigillo adesivo spacer | Invitrogen | S-24736 | Fluorescenza per immagini |
| Vetrini | Electron Microscopy Sciences | 63411 | Fluorescenza per immagini |
| Copertura antiscivolo | VWR | 48366-067 | Fluorescenza per immagini |
| 4 "wafer di silicio | Ted Pella | 16007 | Pre-dadi in chips millimetri 5x7 |
| 0,45 filtro | VWR, Acrodisc | 28143-924 | Per HPLC. Membrana in PTFE |
| Agarosio | BD | 212272 | Fluorescenza per immagini |
| SPE pressione di aspirazione | Sigma Aldrich | 57044 | Esempio di collettore sottovuoto SPE |
| Vaso di vetro poroso | Ace di vetro | 6402-12 | Porosità Cfritta |
| Plasma Cleaner / Sterilizzatore | Harrick Plasma | PDC-32G | Esempio di pulizia al plasma per preparare chip di silicio per SEM |
Riferimenti
- King, D. S., Fields, C. G., Fields, G. B. A cleavage method which minimizes side reactions following Fmoc solid phase peptide synthesis. Int. J. Pept. Pro. Res. 36, 255-266 (1990).
- Sanii, B., Kudirka, R., Cho, A., Venkateswaran, N., Oliver, G. K., Olson, A. M., Tran, H., Harada, R. M., Tan, L., Zuckermann, R. N. Shaken, not stirred: Collapsing a peptoid monolayer to produce free-floating, stable nanosheets. J. Am. Chem. Soc. , (2011).
- Kudirka, R., Tran, H., Sanii, B., Nam, K. T., Choi, P. H., Venkateswaran, N., Chen, R., Whitelam, S., Zuckermann, R. N. Folding of a single-chain, information-rich polypeptoid sequence into a highly-ordered nanosheet. Bioploymers: Peptide Science. 96, 586-595 (2011).
- Utku, Y., Rohatgi, A., Yoo, B., Zuckermann, R., Pohl, N., Kirshenbaum, K. Rapid multistep synthesis of a bioactive peptidomimetic oligomer for the undergraduate laboratory. J. Chem. Ed. 87, 637-639 (2010).
- Fowler, S. A., Blackwell, H. E. Structure-function relationships in peptoids: Recent advances toward deciphering the structural requirements for biological function. Org. Biomol. Chem. 7, 1508-1524 (2009).
- Zuckermann, R. N., Kodadek, T. Peptoids as potential therapeutics. Curr. Op. Mol. Ther. 11, 299-307 (2009).
- Chongsiriwatana, N. P., Patch, J. A., Czyzewski, A. M., Dohm, M. T., Ivankin, A., Gidalevitz, D., Zuckermann, R. N., Barron, A. E. Peptoids that mimic the structure, function and mechanism of helical antimicrobial peptides. , 105-2794 (2008).
- Yam, A. Y., Wang, X., Gao, C., Connolly, M. D., Zuckermann, R. N., Bleua, T., Halla, J., Fedynyshyn, J., Allauzen, S., Peretz, D., Salisbury, C. M. A Universal method for detection of amyloidogenic misfolded proteins. Biochem. 50, 4322-4329 (2011).
- Huang, C. -. Y., Uno, T., Murphy, J. E., Lee, S., Hamer, J. D., Escobedo, J. A., Cohen, F. E., Radhakrishnan, R., Dwarki, V., Zuckermann, R. N. Lipitoids - novel cationic lipids for cellular delivery of plasmid DNA in vitro. Chem. Biol. 5, 345-354 (1998).
- Schroeder, T., Niemeier, N., Afonin, S., Ulrich, A. S., Krug, H. F., Bräse, S. Peptoidic amino- and guanidinium-carrier systems: Targeted drug delivery into the cell cytosol or the nucleus. J. Med. Chem. 51, 376-379 (2008).
- Murnen, H. K., Rosales, A. M., Jaworski, J. N., Segalman, R. A., Zuckermann, R. N. Hierarchical self-assembly of a biomimetic diblock copolypeptoid into homochiral super helices. J. Am. Chem. Soc. 132, 16112-16119 (2010).
- Nam, K. T., Shelby, S. A., Marciel, A. B., Choi, P. H., Chen, R., Tan, L., Chu, T. K. Free-floating ultra-thin two-dimensional crystals from sequence-specific peptoid polymers. Nature. Mater. 9, 454-460 (2010).
- Burkoth, T. S., Beausoleil, E., Kaur, S., Tang, D., Cohen, F. E., Zuckermann, R. N. Toward the synthesis of artificial proteins: The Discovery of an amphiphilic helical peptoid assembly. Chemistry & Biology. 9, 647-654 (2002).
- Murphy, J. E., Uno, T., Hamer, J. D., Cohen, F. E., Dwarki, V., Zuckermann, R. N. A Combinatorial approach to the discovery of efficient cationic peptoid reagents for gene delivery. Proc. Natl. Acad. Sci. U. S. A. 95, 1517-1522 (1998).
- Mora, P. u. i. g., Masip, I. s. a. b. e. l., Cortés, N. u. r. i. a., Marquina, R. e. g. i. n. a., Merino, R. a. m. &. #. 2. 4. 3. ;. n., Merino, J. e. s. &. #. 2. 5. 0. ;. s., Carbonell, T. e. r. e. s. a., Mingarro, I. s. m. a. e. l., Messeguer, A. n. g. e. l., Pérez-Payá, E. n. r. i. q. u. e. Identification from a positional scanning peptoid library of in vivo active compounds that neutralize bacterial endotoxins. J. Med. Chem. 48, 1265-1268 (2005).
- Zuckermann, R. N. Discovery of nanomolar ligands for 7-transmembrane G-protein coupled receptors from a diverse (N-substituted)glycine peptoid Library. J. Med. Chem. 37, 2678-2685 (1994).
- Alluri, P., Liu, B., Yu, P., Xiao, X., Kodadek, T. Isolation and characterization of coactivator-binding peptoids from a combinatorial library. Moleular Biosystems. 2, 568-579 (2006).
- Figliozzi, G. M., Goldsmith, R., Ng, S., Banville, S. C., Zuckermann, R. N. Synthesis of N-(substituted)glycine peptoid libraries. Methods Enzymol. 267, 437-447 (1996).
- Culf, A. S., Ouellette, R. J. Solid-phase synthesis of N-substituted glycine oligomers (α peptoids) and derivatives. Molecules. 15, 5282-5335 (2010).
- Burkoth, T. S., Fafarman, A. T., Charych, D. H., Connolly, M. D., Zuckermann, R. N. Incorporation of unprotected heterocyclic side chains into peptoid oligomers via solid-phase submonomer synthesis. J. Am. Chem. Soc. 125, 8841-8845 (2003).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon