Method Article
En fase sólida Submonomer Síntesis de Polímeros peptoide y su auto-ensamblaje en altamente ordenadas nanoláminas
En este artículo
Resumen
Un simple y general método manual peptoide síntesis referida a un equipo y reactivos básicos, disponibles en el mercado se perfila, lo que permite peptoides para ser fácilmente sintetizada en la mayoría de los laboratorios. La síntesis, purificación y caracterización de un 36mer peptoide anfifílicas se describe, así como su auto-ensamblaje en muy ordenada nanoláminas.
Resumen
Peptoides son una nueva clase de biomimética, no natural, la secuencia específica de heteropolímeros que se resisten a la proteólisis, muestran una actividad biológica potente, y se pliegan en nanoestructuras de orden superior. Estructuralmente similar a los péptidos, peptoides son poli N-sustituidos glycines, donde las cadenas laterales están unidos al nitrógeno en lugar de la alfa-carbono. Su facilidad de síntesis y la diversidad estructural permite la prueba de los principios de diseño básicos para conducir de novo diseño y la ingeniería de nuevos materiales biológicamente activos y nanoestructurados.
Aquí, un sencillo manual de protocolo peptoide síntesis se presenta que permite la síntesis de polypeptoids de cadena larga (hasta 50mers) en excelentes rendimientos. Sólo el equipo básico, técnicas sencillas (por ejemplo, transferencia de líquido, filtración), y los reactivos disponibles en el mercado se requieren, por lo que peptoides una adición acceso a kits de muchos investigadores ". La columna vertebral peptoide se cultiva un monómero en un tiempo de via el método submonomer que consiste en un ciclo de dos pasos monómero además: acilación y el desplazamiento. Ácido en primer lugar, bromoacético activado in situ con N, N'-diisopropilcarbodiimida acilatos uno unido a resina amina secundaria. Segundo desplazamiento, nucleofílico del bromuro de una amina primaria sigue para introducir la cadena lateral. El ciclo de dos etapas se repite hasta que la longitud de la cadena deseada. La eficiencia de acoplamiento de este ciclo de dos etapas de rutina excede el 98% y permite la síntesis de peptoides de hasta 50 residuos. Diversas secuencias altamente ajustable, precisa y químicamente son alcanzables con el método submonomer como cientos de aminas primarias disponibles se puede incorporar directamente.
Peptoides se están convirtiendo en un material versátil biomiméticos para la investigación Nanobiociencia debido a su flexibilidad sintética solidez, y ordenar a nivel atómico. El plegamiento de una cadena simple, la información anfifílicas,ción rica en polypeptoid en un nanosheet muy ordenada se ha demostrado recientemente. Este peptoide es un 36-mer que consta sólo de tres monómeros diferentes disponibles en el mercado: hidrofóbico, catiónicos y aniónicos. Las cadenas hidrofóbicas feniletilo lado están enterrados en el núcleo nanosheet mientras que la amina iónicas y las cadenas laterales carboxilo se alinean en las caras hidrofílicas. El nanoláminas peptoide servir como una plataforma potencial para miméticos de membrana, miméticos de proteínas, la fabricación de dispositivos y sensores. Métodos para la síntesis de peptoide, formación de la hoja, y las imágenes de microscopía se describen y proporcionan un método sencillo para que los futuros diseños nanosheet peptoide.
Protocolo
1. En fase sólida Submonomer Síntesis de Polypeptoids
Síntesis en fase sólida (MSF) es una técnica común usada para sintetizar la secuencia específica de biopolímeros paso a paso, directamente en un sólido inerte de apoyo como una resina polimérica de cuentas. Altos rendimientos de acoplamiento y la facilidad de eliminación de reactivo en exceso son las principales ventajas de SPS. Después de una reacción de acoplamiento a la resina, reactivos en exceso simplemente se drenan y las perlas se lavan para estar listo para el paso de la reacción siguiente. Después de la reacción de síntesis final, los oligómeros de larga duración se escinde de la resina y el material de solución de fase puede ser más estudiado. En este sentido, adaptar el procedimiento de MSF para generar la secuencia específica de polímeros peptoide.
- Configuración: Todos los pasos de la síntesis peptoide manual pueden llevarse a cabo de polipropileno desechables, (PP) cartucho poroso o un recipiente de vidrio poroso reacción equipado con una llave de 3 vías. Realizar todas las operaciones en una campana extractora. De incubaciones en el gembarcación chica o un cartucho de plástico, conectar un brazo a una fuente de nitrógeno para suavemente la burbuja de la solución de una mezcla adecuada. Por otra parte, para las incubaciones de reacción en el cartucho desechable, sellar ambos extremos del cartucho con las tapas y el lugar en un agitador rotatorio. Para drenar las mezclas de reacción o se lava, se conectan a la casa de vacío a través de un sifón. El recipiente debe ser poroso con una frita de grueso. Siliconize el recipiente de reacción de vidrio para evitar granos se peguen a las paredes del recipiente de vidrio. Prepare una solución de 5% diclorodimetilsilano en dicloroetano (v / v). Llenar un recipiente de reacción limpio y seco en la parte superior con una solución de siliconado, deje reposar durante 30 minutos, y escurrir. Lavar el vaso una vez con DCE y luego una vez con metanol. La solución siliconado puede ser reutilizado, por lo que debe ser salvado. Ya sea con aire seco o deshacerse de cualquier exceso de solución y hornee hasta que se seque el material de vidrio después de quitar la llave de paso. Recipiente de reacción enfriar antes de añadir la resina.
- Añadir 100 mg (0,06 mmol) de volver a pista amidael pecado de un recipiente de reacción poroso. Swell la resina mediante la adición de 2 ml de dimetilformamida (DMF). Agite por agitación o el burbujeo durante 10 minutos. Drenaje de la solución al vacío para aislar la resina se hinchó.
- Añadir 1 ml de 20% 4-metilpiperidina en DMF (v / v) para desproteger el grupo Fmoc. Agitar durante 2 minutos y escurrir. Repita el procedimiento con una incubación de 12 minutos.
- Enjuagar la resina mediante la adición de 2 ml de DMF, agitando durante 15 segundos, y el drenaje. Repita 3 veces.
- Bromoacetylation: Añadir 1 ml de 0,6 M de ácido bromoacético (0,6 mmol) en DMF y 86 l de N, N'-diisopropilcarbodiimida (0,93 equivalente, 0,56 mmol). Incubar con suave burbujeo durante 30 minutos, escurrir y enjuagar con 2 ml de DMF (repetición 4x).
- Desplazamiento: Añadir 1 ml de 2.1 M de amina de la N-methylpyrrolidinone. Incubar con burbujas de 30-120 minutos, escurrir y enjuagar con DMF (4x 2 ml).
- Seguir creciendo la cadena peptoide repitiendo el ciclo submonomer, pasos 1,5 (bromoacetylation) y 1.6 (displacement).
- Después de que el desplazamiento final se hace, enjuague con 2 ml de DMF (repetición 4x), luego 2 ml de diclorometano (repeat 3x). Cap y guardar el recipiente de reacción hasta el escote.
- Pausa en la síntesis de (opcional): Para hacer una pausa durante una síntesis peptoide, terminar la reacción de desplazamiento y continúe con el paso 1.8. Para seguir creciendo la cadena peptoide, reinicie la síntesis de volver a la inflamación de la resina seca (paso 1.2) y repetir el ciclo submonomer (paso 1.5 y 1.6). La resina se puede secar y almacenar después de cualquier desplazamiento, salvo el desplazamiento segundo, porque el conjugado de resina peptoide puede formar un producto dicetopiperazina lado cíclico.
- Para múltiples síntesis simultánea, un colector de extracción en fase sólida de vacío se recomienda para maximizar la eficiencia. Síntesis peptoide también se puede automatizar adecuadamente métodos de programación de sintetizadores de péptidos disponibles comercialmente, tales como el Apex Aapptec 396, CEM sintetizador de microondas Libertad y Techno proteínaslogies Inc. sintetizador Prelude.
2. División y la desprotección de la Cadena Lateral
- Transferir la totalidad de resina seca a un vial de 20 ml de cristal de centelleo.
- De trabajo dentro de una campana y el uso de equipo de protección personal, añadir 4 ml de ácido trifluoroacético (TFA) cóctel división 1 (por ejemplo, 95% ac. TFA, véase la discusión) a la ampolla de vidrio de centelleo y tapa. Agitar durante 10 minutos a 2 horas a temperatura ambiente (véase la discusión).
- Recoger la solución división TFA mediante el filtrado de la resina a través de un cartucho desechable, fritada PP en un nuevo pre-pesaba 20 ml frasco de cristal de centelleo. A desechables, PP pipeta es conveniente para la transferencia de las soluciones cóctel escote.
- Añadir 1 ml de cóctel de división fresco para enjuagar la resina y recoger cualquier peptoide residual. Repetir 2 veces.
- Evaporar TFA soplando una suave corriente de nitrógeno o mediante el uso de un V10 Biotage evaporador.
- Volver a disolver el crudo en 6 mlde acetonitrilo / agua 1:1 (v / v) para HPLC. Congelar y liofilizar. Repita.
- Registrar el peso del producto en bruto. Almacenar en forma de polvo seco a -20 ° C
- División de prueba (opcional): Una división de prueba en el 0,5% de la resina se puede realizar para determinar rápidamente la pureza y la masa de la peptoide sintetizado y si las condiciones correctas de división fueron elegidos. Divisiones de prueba son de especial utilidad para controlar el progreso de la síntesis.
3. Caracterización y purificación de la Polypeptoid
- A través de una combinación de análisis HPLC, electrospray LC-MS, y / o MALDI-TOF, determinar la pureza del producto en bruto y si el peso molecular deseado está presente.
- Preparar un ~ 5.10 mg / ml solución del polvo seco peptoide en agua con un mínimo de acetonitrilo como sea necesario para la solubilidad. Filtrar la solución clara del producto peptoide crudo con filtro de 0,45 micras jeringa para eliminar el polvo y las partículas.
- Analítica HPLC y electrospray LC-MS: Preparar un ~ 20 mg / ml solución peptoide crudo. Filtro de 200 l con un filtro de 0,45 micras y se inyectan 20 mL.
- MALDI: Mezcle 1 l de ~ 20 mg / ml con una matriz de peptoide l. Spot 1 l en la placa de MALDI y dejar secar al aire. Matrix y el modo de adquisición depende de la muestra (Fig. 5).
- Purificar la mezcla de crudo peptoide con preparación de HPLC en fase reversa. Elija el gradiente y la columna (C4 o C18), basado en la hidrofobicidad de polypeptoid. Combine las fracciones purificadas, congelar y liofilizar, dando como resultado un polvo blanco esponjoso. Registrar el peso del producto final.
- Formación de HCl de sal (opcional): Volver a disolver el polvo liofilizado en 100 mM HCl (ac.) con acetonitrilo mínimo. Traslado a la pre-pesado frasco de vidrio. Congelar y volver a liofilizar. Repetir 2 veces. Se vuelve a pesar para determinar la masa de polvo peptoide.
4. Formación Nanosheet peptoide
En esta sección se describes el protocolo para formar láminas de una sola cadena, secuencia específica, anfifílicas 36-mer peptoide (Fig. 1). Después de la cadena peptoide se sintetiza, purificada y liofilizada como se describió anteriormente, el polvo blanco resultante se disuelve en DMSO para obtener una solución 2 mM de valores.
- Preparar 500 l de solución de 20 mM en tampón peptoide hoja de formación (10 mM Tris-HCl, 100 mM NaCl, pH 8,0 en agua) en un frasco de vidrio una copita. En primer lugar, añadir 445 l de agua Milli-Q, 50 l de tampón 10x formación de la hoja, y agitar para mezclar. A continuación, añadir 5 l de solución 2 mM de valores peptoide y suavemente solución de remolino. Tapar el frasco de vidrio.
- Hojas están formadas por la suave agitación de la solución acuosa diluida peptoide. Poco a poco inclinando el vaso vial desde la posición horizontal a la posición vertical los resultados en las hojas. Agitación suave también produce hojas, sin embargo, las hojas tienden a ser más pequeños y con menos bordes rectos. Un análisis más profundo del mecanismo de formación de la hoja es de Reported por separado. 2
- Para muchos de alta calidad sábanas, rotar los frascos de vidrio con respecto al eje horizontal lentamente (<1 RPM) de uno a tres días. Una recursos técnicos adecuados RKVSD rotador Rotamix tubo o un rockero personalizado puede realizar de forma continua.
- Diálisis de nanoláminas (opcional): En algunas aplicaciones, puede ser necesario para eliminar cualquier cadenas libres o tampones peptoide / sales. Remoje un Float-a-Lyzer 100 kD de membrana en el buffer deseado durante 15 minutos. Solución de carga de 500 l hoja peptoide en la cámara de la muestra. Remojo en 500 ml de buffer deseado, removiendo con una varilla de agitación magnética a 60 rpm. Permita que la diálisis de hojas de proceder durante 4 horas. Cada hora, el intercambio con un stock de la solución de buffer.
5. Microscopía de fluorescencia de nanoláminas
- Imágenes de fluorescencia de la nanoláminas fueron fotografiadas con Nile Red, un colorante ambientalmente sensibles, cuya intensidad de fluorescencia aumenta cuando está localizado en hydrentornos ophobic (Fig. 2).
- Añadir 1 l de 100 M del Nilo Red a 100 L de la solución nanosheet para obtener una concentración final de 1 mM de Nilo Rojo.
- Haga una solución al 1% de agarosa en agua caliente y verter en una placa Petri de plástico. Garantizar la solución de agarosa es aproximadamente 1 / 8 de pulgada de grosor y que la solución para enfriar tranquilamente en una superficie plana. Después de la puesta de agarosa, use una espátula para cortar y la transferencia de 1 cm x 1 cm cuadrados a un portaobjetos de vidrio.
- Para recoger las hojas en el mismo plano, punto 1 l de solución de la hoja en la pieza de agarosa. Deje que la agarosa para absorber el buffer de 2 minutos, dejando las hojas en la superficie. Imagen dentro de los 15 minutos, de lo contrario la agarosa comenzará a deformarse debido a la deshidratación.
- A las hojas de la imagen en la solución, carga de 15 ul dentro de una junta mm de diámetro 20 mm 0,12 sobre un portaobjetos de vidrio. Cubrir con un cubreobjetos. Si las hojas son simplemente intercalada entre una lámina de vidrio y cubreobjetos sin junta, muchas wi hojascorte ll y la evaporación aparentemente menor hará que las hojas se mueven constantemente.
- Las hojas de la imagen con iluminación de epifluorescencia (por ejemplo, una Olympus IX81 microscopio invertido equipado con un iXonEM Andor espectros + EMCCD con un filtro de Texas, de color rojo).
6. Electrónico de barrido microscopía de barrido (SEM) de nanoláminas
- Grabado de sustrato de silicona (opcional) Plasma: los chips de silicio se plasma grabada para ayudar en la absorción de las hojas. Coloque los chips de silicio en la cámara de vacío de un limpiador de plasma (por ejemplo, Harrick Plasma Limpiador / Esterilizador PDC-32G). Bomba de hasta 200 mTorr y establecer la bobina de RF a 18 W (valor alto para el PDC-32G). Etch durante 2 minutos.
- Caída de 20 l de solución de hoja de peptoide sobre un sustrato de silicio tratada con plasma. Deje reposar durante 3 minutos. Retire el exceso de solución con la punta de Kim-limpie. Colocar 20 L de agua sobre la superficie y eliminar el exceso de solución buffer de nuevo para eliminar y sales. Repite 4 veces.
- Como alternativa, marqueyze las soluciones de hoja de peptoide contra el agua para eliminar el buffer y la sal. Caída de 20 l de solución de hoja de dializados de plasma tratados con sustratos de silicio. El aire seco de la muestra.
- Hojas con la imagen SEM (por ejemplo, Zeiss Gemini Ultra-55 Microscopio Electrónico de Barrido de análisis) con un detector en la lente y en las energías del haz entre 1 kV y 5 kV (Fig. 3).
7. Notas de seguridad:
- Dimetilformamida y diclorometano son razonablemente posibles carcinógenos.
- N, N'-diisopropilcarbodiimida, 4 methylpiperdine y ácido bromoacético son peligrosos para la piel, ojos y tracto respiratorio. Deben ser utilizados en la campana con cuidado. Puede ser tóxico si se inhala o absorbe por la piel y la exposición puede resultar en sensibilización. Los envases vacíos retienen residuos del producto (líquido / vapor) y debe lavarse a fondo antes de sacarlos de la campana.
- TFA es un ácido fuerte, y es extremadamente destructivo para el tracto respiratorio superior, ojos yla piel. TFA es también volátil que las soluciones concentradas de ácidos grasos trans en la campana en todo momento para evitar daños en las vías respiratorias. Uso adecuado de PPE, y la precaución al manejar soluciones de ácidos grasos trans. Cambie los guantes inmediatamente si entra en contacto con TFA, e inmediatamente limpie cualquier derrame.
8. Los resultados representativos:
En esta sección se describe la síntesis, caracterización y purificación de una secuencia específica de 36-mer peptoide cadena que se pliega en una muy ordenada nanosheet 3 (Fig. 1).
El bloque de carga peptoide H-[Nae-NPE] 9 - [NCE-NPE] 9-NH 2 fue sintetizada en 100 mg de resina Rink amida. A 2 M solución de amina se utiliza para todas las reacciones de desplazamiento, que se llevaron a cabo durante 60 minutos para los residuos de 1.18 y 120 minutos para los residuos 19-36. t-butil beta-alanina HCl se convirtió en la base libre (véase la discusión), mientras que la feniletilamina y la boc etilendiamina-fueron utilizados directly. La resina se escindió con un 95% de TFA, un 2,5% triispropylsilane, 2,5% de agua durante 2 horas. TFA se evapora y el aceite viscoso resultante (~ 180 mg) se volvió a disolver en acetonitrilo 6 ml: agua 1:1 (v / v). La pureza del producto (Fig. 4) y la presencia de la masa del producto fue confirmada por análisis de RP-HPLC (30-80% de acetonitrilo en gradiente de agua, tanto que contiene 0,1% (v / v) de TFA, a 1 ml / min durante 30 minutos a 60 ° C con un C18, 5 m, 50 X 2 mm de columna) y MALDI (Fig. 5).
Purificación con HPLC en fase reversa en una columna Vydac C18 (10 micras, 22 mm x 250 mm) procedió, siguiendo un gradiente de 30-60% de acetonitrilo en agua con 0,1% TFA durante 60 minutos a 10 ml / min. La columna estaba cargado con 60 mg de producto crudo para cada corrida cromatográfica. Las fracciones purificadas se combinaron basado en la pureza de la RP-HPLC analítico (Fig. 4) y liofilizado para producir ~ 80 mg de un polvo blanco esponjoso.
Purificado bloque de carga peptoide molecularpeso fue confirmada por MALDI. 1 l de 100 M purificada peptoide en acetonitrilo: agua 1:1 (v / v) se mezcló con 1 l de la matriz (5 mg / ml de α-ciano-4-hidroxicinámico en acetonitrilo: agua 1:1 v / v, y 0,1% de TFA) y l 1 fue descubierto en la placa de MALDI. Después de la muestra secada al aire, se colocó en el Applied Biosystems / MDS Sciex 4800 MALDI TOF / TOF Analyzer. Los modos de adquisición y procesamiento de la masa lineal de baja. El peso calculado se ha introducido en la masa dirigida para ajustar automáticamente el tiempo de retardo. La intensidad del láser se estableció en 3400. La masa observada, 4981,2, se acerca mucho a la masa calculada de 4.981,74.
El polvo liofilizado purificado se disolvió en DMSO para obtener una solución 2 mM de valores, que pueden ser almacenadas a 4 ° C. Hojas fueron preparadas por el protocolo mencionado y con imágenes de microscopía de fluorescencia óptica y SEM (Fig. 2 y 3). Una gran variedad de formas con tamaños que van hasta 300 micras se observan, y notabmente, bordes rectos ocupan un lugar destacado.

Figura 1 Secuencia del bloque de carga peptoide H-[Nae-NPE] 9 -. [NCE-NPE] 9-NH 2. Una cadena única, la carga de bloques, polypeptoid anfifílicas 36-mer se constituye en altamente ordenadas, de dos dimensiones nanoláminas 3. El peso molecular calculado es 4.981,74.

Figura 2. Imágenes de microscopía de fluorescencia de nanoláminas peptoide. Las sábanas estaban formados a partir de una solución al 20 M peptoide en 10 mM Tris, 100 mM NaCl, pH 8,0. Las hojas son imágenes de agarosa con 1μM Nilo Rojo. Las barras de escala son 100 micras.

Figura 3. Digitalización de imágenes de microscopía electrónicade nanoláminas peptoide. Las sábanas estaban formados a partir de una solución al 20 M peptoide en 10 mM Tris, 100 mM NaCl, pH 8,0. Las barras de escala es de 5 micras.
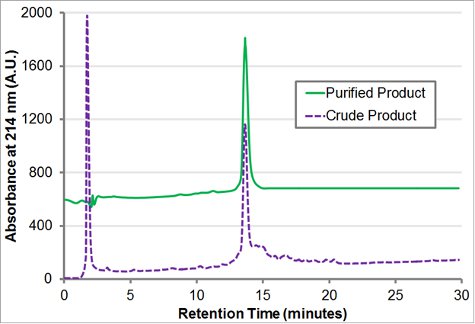
Figura 4 analítico HPLC en fase reversa rastro de H-[Nae-NPE] 9 -. [NCE-NPE] 9-NH 2. El crudo y purificado HPLC analítica de trazas (30-80% en el gradiente de 1 mL / min durante 30 minutos a 60 ° C con un C18, 5 m, 50 x 2 mm de columna) del crudo y purificado bloque de carga peptoide H-[ Nae-NPE] 9 - [NCE-NPE] 9-NH 2 se muestra.
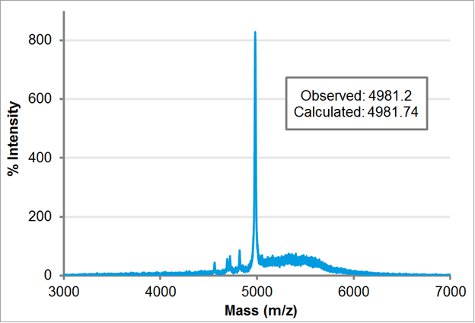
Figura 5 MALDI-TOF espectrometría de masas rastro de H-[Nae-NPE] 9 -. [NCE-NPE] 9-NH 2. La masa observada, 4981,2, está de acuerdo cerca de la masa calculada, 4981,74.
Discusión
Aplicaciones y significado
Este protocolo describe un método simple y eficiente de la síntesis de peptoide y el humor acuoso de auto-ensamblaje de la peptoides en nanoláminas. La mayoría de los laboratorios son fácilmente capaces de sintetizar peptoides por materiales de bajo costo, los conocimientos básicos y técnicas sencillas se utilizan 4. Asimismo, el auto-ensamblaje de ultra-delgada, muy ordenada nanoláminas requiere simplemente repite la inclinación un vial de una solución acuosa diluida peptoide 2. Peptoides son prometedores materiales para la investigación biomédica y la nanociencia, ya que son resistentes y flexibles de manera sintética pero la secuencia específica y altamente ajustable 5. Peptoides han demostrado actividad biológica (6,7 terapéuticos, de diagnóstico 8, el suministro intracelular 9-10) y plegado en nanoestructuras jerárquicas 3, 11-14. Debido a su síntesis modular, combinatoria peptoide librAries 15-19 puede ser fácilmente sintetizado y proyectado para una amplia serie de actividades o propiedades. En particular, el nanoláminas servir como una plataforma potencial para los andamios de la pantalla de dos dimensiones, miméticos de membranas, sensores biológicos, miméticos de la proteína y la fabricación del dispositivo. Con las posibles secuencias prácticamente inagotable diferentes, el campo de la investigación peptoide se está expandiendo rápidamente.
Variables en la síntesis en fase sólida submonomer de polypeptoids
Debido a la posibilidad de escoger entre un alfabeto muy amplio y diverso de los monómeros de 20, el método submonomer necesita modificaciones ocasionales para los casos en que el aumento de la eficiencia de acoplamiento de cada paso se mejora el rendimiento general del producto. Incorporación de las cadenas sin protección heterocíclicos lado requiere el uso de ácido cloroacético en lugar de ácido bromoacético 21. Plazo de desplazamiento y mayorlas concentraciones de aminas se emplean normalmente después de unos 20 acoplamientos para largas secuencias peptoide o aminas menos nucleofílico. El calentamiento del recipiente de reacción a 35 ° C, mediante el uso de un recipiente de reacción con camisa de agua, ayuda a impulsar la reacción. Para altamente volátil aminas tales como isopropilamina, se debe tener cuidado para evitar la evaporación.
Aminas en la forma de una sal de clorhidrato, tales como t-butil-beta-alanina HCl, necesidad de ser libre basada antes de ser introducido en la reacción de desplazamiento. Esto se puede lograr mediante la disolución o la suspensión de la amina en DCM (~ 5 g amine/25 mL DCM), y neutralizar con una solución equimolar de hidróxido de sodio acuoso en un embudo de separación. La capa de DCM y se recoge la capa acuosa se lava con DCM adicional. Las capas de DCM combinados se secan sobre sulfato de sodio y se filtró en un matraz de fondo redondo previamente pesado. Eliminar el disolvente por evaporación rotatoria para dar un aceite, y registrar el peso del producto.
During el paso de división, cóctel TFA división y el tiempo de corte depende de la cantidad y variedad de grupos protectores utilizados. Directrices para los cócteles de corte son similares a las tradicionales divisiones péptido desprotección 1. En general, 10 minutos incubaciones se requieren para las secuencias sin la protección de los grupos o secuencias con algunos muy lábil en medio ácido grupos protectores (por ejemplo, BOC, tritilo). Dos incubaciones hora se secuencias con grupos protectores más difícil (por ejemplo, t-butilo, Mtr, PBF) o secuencias con muchos grupos de protección para garantizar la total desprotección de cada cadena. Crudo productos peptoide generalmente se disuelve en acetonitrilo: agua 1:1 (v / v), pero una mayor proporción de acetonitrilo son comunes con cadenas laterales con una alta hidrofobicidad general.
Divulgaciones
No tenemos nada que revelar.
Agradecimientos
Los autores desean agradecer a Byoung-Chul Lee, Choi Ho Samuel Felipe y de una valiosa ayuda. Este trabajo se llevó a cabo en el Molecular Foundry en el Lawrence Berkeley National Laboratory, que es apoyado por la Oficina de Ciencia de la Oficina de Ciencias Básicas de Energía, del Departamento de Energía de EE.UU. bajo el contrato No. DE-AC02-05CH11231 y la Reducción de Amenazas de Defensa Agencia con el n º de contrato: IACRO-B0845281.
Materiales
| Name | Company | Catalog Number | Comments |
| Nombre del reactivo | Empresa | Número de catálogo | Comentarios |
| Dimetilformamida | EMD | EM-DX1726P-1 | 99 +% |
| N-methylpyrrolidinone | BDH | BDH1141-4LP | 99% |
| Ácido bromoacético | Acros orgánicos | 200000-106 | 99% |
| 4-metilpiperidina | Sigma Aldrich | M73206 | 96% |
| N, N'-diisopropilcarbodiimida | Chem-Impex | 001100 | 99,5% |
| Diclorometano | EMD | EMD-DX0835 | Grado ACS |
| Acetonitrilo | EMD | EM-AX0145P-1 | 99,8% |
| Ácido trifluoroacético | Sigma Aldrich | T6508 | 99% |
| Triisopropilsilano | Sigma Aldrich | 233781 -10G | Para la división TFA |
| El 1,2-dicloroetano | JT Baker | JTH076-33 | Para siliconado de recipientes de reacción de vidrio |
| Fenetilamina | Sigma Aldrich | 407267-100ML | > Hidrofóbicas 99,5% de la cadena lateral amina |
| Boc-etilendiamina | Tecnologías de la CNH | C-1112 | Catiónicos de cadena lateral amina |
| t-butil beta-alanina HCl | Chem-Impex Internacional | 04407 | Aniónicos de cadena lateral amina |
| α-ciano-4-hidroxicinámico | Sigma Aldrich | C8982-10X10MG | Por MALDI matriz |
| Nilo Rojo | Sigma Aldrich | 19123-10MG | Para la fluorescencia de imagen |
| Diclorodimetilsilano | Sigma Aldrich | 80430-F-500G | Para siliconado de recipientes de reacción de vidrio |
| Desechables carrito PP porosocresta | Separaciones Aplicada | 2416 | 6 ml de polipropileno con cartucho de 20 mm PE frita |
| Desechables de 3 vías luer adaptador | Cole Parmer | 31200-80 | Llave de paso para recipiente de reacción desechables manual de síntesis |
| Luer Lock anillo | Cole Parmer | 45503-19 | ¼ "adecuado para vasos desechables manual de reacción de síntesis |
| Accesorios Luer | Cole Parmer | 45500-20 | ¼ "adecuado para vasos desechables manual de reacción de síntesis |
| Pipetas desechables PP | VWR | 16001-194 | Para las transferencias de TFA |
| Luer jeringa de plástico | Nacional de Investigaciones Científicas | S7515-5 | 6 jeringas ml |
| Un dram vial de vidrio | VWR | 66011-041 | Con fenólica moldeada con tapón de rosca de polivinilo con cara de revestimiento de celulosa |
| 20 ml de gammagrafíadestilación vial | VWR | 66022-060 | Con tapa unida PP y el revestimiento de aluminio de celulosa |
| Secure-sello adhesivo espaciador | Invitrogen | S-24736 | De fluorescencia de imagen |
| Portaobjetos de vidrio | Microscopía electrónica de Ciencias | 63411 | De fluorescencia de imagen |
| Cubreobjetos | VWR | 48366-067 | De fluorescencia de imagen |
| 4 "de obleas de silicio | Ted Pella | 16007 | Pre-dados en los chips de 5x7 mm |
| Filtro de 0,45 | VWR, Acrodisc | 28143-924 | Por HPLC. Membrana de PTFE |
| Agarosa | BD | 212272 | De fluorescencia de imagen |
| SPE colector de vacío | Sigma Aldrich | 57044 | Ejemplo de colector de vacío SPE |
| Vaso de vidrio poroso | As de vidrio | 6402-12 | Porosidad Cfrita |
| Plasma Limpiador / Esterilizador | Harrick Plasma | PDC-32G | Ejemplo de limpiador de plasma para preparar los chips de silicio para la SEM |
Referencias
- King, D. S., Fields, C. G., Fields, G. B. A cleavage method which minimizes side reactions following Fmoc solid phase peptide synthesis. Int. J. Pept. Pro. Res. 36, 255-266 (1990).
- Sanii, B., Kudirka, R., Cho, A., Venkateswaran, N., Oliver, G. K., Olson, A. M., Tran, H., Harada, R. M., Tan, L., Zuckermann, R. N. Shaken, not stirred: Collapsing a peptoid monolayer to produce free-floating, stable nanosheets. J. Am. Chem. Soc. , (2011).
- Kudirka, R., Tran, H., Sanii, B., Nam, K. T., Choi, P. H., Venkateswaran, N., Chen, R., Whitelam, S., Zuckermann, R. N. Folding of a single-chain, information-rich polypeptoid sequence into a highly-ordered nanosheet. Bioploymers: Peptide Science. 96, 586-595 (2011).
- Utku, Y., Rohatgi, A., Yoo, B., Zuckermann, R., Pohl, N., Kirshenbaum, K. Rapid multistep synthesis of a bioactive peptidomimetic oligomer for the undergraduate laboratory. J. Chem. Ed. 87, 637-639 (2010).
- Fowler, S. A., Blackwell, H. E. Structure-function relationships in peptoids: Recent advances toward deciphering the structural requirements for biological function. Org. Biomol. Chem. 7, 1508-1524 (2009).
- Zuckermann, R. N., Kodadek, T. Peptoids as potential therapeutics. Curr. Op. Mol. Ther. 11, 299-307 (2009).
- Chongsiriwatana, N. P., Patch, J. A., Czyzewski, A. M., Dohm, M. T., Ivankin, A., Gidalevitz, D., Zuckermann, R. N., Barron, A. E. Peptoids that mimic the structure, function and mechanism of helical antimicrobial peptides. , 105-2794 (2008).
- Yam, A. Y., Wang, X., Gao, C., Connolly, M. D., Zuckermann, R. N., Bleua, T., Halla, J., Fedynyshyn, J., Allauzen, S., Peretz, D., Salisbury, C. M. A Universal method for detection of amyloidogenic misfolded proteins. Biochem. 50, 4322-4329 (2011).
- Huang, C. -. Y., Uno, T., Murphy, J. E., Lee, S., Hamer, J. D., Escobedo, J. A., Cohen, F. E., Radhakrishnan, R., Dwarki, V., Zuckermann, R. N. Lipitoids - novel cationic lipids for cellular delivery of plasmid DNA in vitro. Chem. Biol. 5, 345-354 (1998).
- Schroeder, T., Niemeier, N., Afonin, S., Ulrich, A. S., Krug, H. F., Bräse, S. Peptoidic amino- and guanidinium-carrier systems: Targeted drug delivery into the cell cytosol or the nucleus. J. Med. Chem. 51, 376-379 (2008).
- Murnen, H. K., Rosales, A. M., Jaworski, J. N., Segalman, R. A., Zuckermann, R. N. Hierarchical self-assembly of a biomimetic diblock copolypeptoid into homochiral super helices. J. Am. Chem. Soc. 132, 16112-16119 (2010).
- Nam, K. T., Shelby, S. A., Marciel, A. B., Choi, P. H., Chen, R., Tan, L., Chu, T. K. Free-floating ultra-thin two-dimensional crystals from sequence-specific peptoid polymers. Nature. Mater. 9, 454-460 (2010).
- Burkoth, T. S., Beausoleil, E., Kaur, S., Tang, D., Cohen, F. E., Zuckermann, R. N. Toward the synthesis of artificial proteins: The Discovery of an amphiphilic helical peptoid assembly. Chemistry & Biology. 9, 647-654 (2002).
- Murphy, J. E., Uno, T., Hamer, J. D., Cohen, F. E., Dwarki, V., Zuckermann, R. N. A Combinatorial approach to the discovery of efficient cationic peptoid reagents for gene delivery. Proc. Natl. Acad. Sci. U. S. A. 95, 1517-1522 (1998).
- Mora, P. u. i. g., Masip, I. s. a. b. e. l., Cortés, N. u. r. i. a., Marquina, R. e. g. i. n. a., Merino, R. a. m. &. #. 2. 4. 3. ;. n., Merino, J. e. s. &. #. 2. 5. 0. ;. s., Carbonell, T. e. r. e. s. a., Mingarro, I. s. m. a. e. l., Messeguer, A. n. g. e. l., Pérez-Payá, E. n. r. i. q. u. e. Identification from a positional scanning peptoid library of in vivo active compounds that neutralize bacterial endotoxins. J. Med. Chem. 48, 1265-1268 (2005).
- Zuckermann, R. N. Discovery of nanomolar ligands for 7-transmembrane G-protein coupled receptors from a diverse (N-substituted)glycine peptoid Library. J. Med. Chem. 37, 2678-2685 (1994).
- Alluri, P., Liu, B., Yu, P., Xiao, X., Kodadek, T. Isolation and characterization of coactivator-binding peptoids from a combinatorial library. Moleular Biosystems. 2, 568-579 (2006).
- Figliozzi, G. M., Goldsmith, R., Ng, S., Banville, S. C., Zuckermann, R. N. Synthesis of N-(substituted)glycine peptoid libraries. Methods Enzymol. 267, 437-447 (1996).
- Culf, A. S., Ouellette, R. J. Solid-phase synthesis of N-substituted glycine oligomers (α peptoids) and derivatives. Molecules. 15, 5282-5335 (2010).
- Burkoth, T. S., Fafarman, A. T., Charych, D. H., Connolly, M. D., Zuckermann, R. N. Incorporation of unprotected heterocyclic side chains into peptoid oligomers via solid-phase submonomer synthesis. J. Am. Chem. Soc. 125, 8841-8845 (2003).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados