Method Article
유리를 통해 보면 : 시간 경과 현미경 및 단일 세포의 종 추적 항암 치료를 공부하기
요약
Here, we describe a method of long-term time-lapse microscopy to longitudinally track single cells in response to anti-cancer therapeutics.
초록
항암제에 대한 단 전지의 반응은 모집단 응답을 결정하는데 크게 기여하고, 따라서 전체 결과에서 중요한 요인이다. 면역은 유동 세포 계측법 고정 세포 실험은 종종 세포가 항암제에 반응하는 방법을 연구하는 데 사용됩니다. 이러한 방법은 중요하지만, 몇 가지 단점이 있습니다. 암과 정상 세포간에, 다른 암 유래의 세포 및 과도 희귀 응답 사이의 약물 반응의 다양성 인구 평균 어 세이를 이용하여 직접 추적 종을 분석 할 수없이 이해하기 어렵다. 현미경은 특히 이미지 살아있는 세포에 적합합니다. 기술의 발전뿐만 아니라 세포 추적뿐만 아니라, 세포 반응의 다양한 관찰을 가능하게하는 해상도에서 일상적으로 이미지 세포에 우리를 가능하게한다. 우리의 연속적인 시간 경과 이미징을 허용 자세히 접근 방식을 설명기본적으로 한 일반적으로 96 시간까지 원하는대로에 대한 약물 반응 동안 세포. 접근 방법의 변형을 사용하여, 세포 주에 대해 모니터링 될 수있다. 유전자 인코딩 된 형광 바이오 센서 수많은 프로세스, 경로 및 응답의 고용으로 이어 할 수 있습니다. 우리는 추적 및 세포 성장 및 세포주기 진행 염색체 역학, DNA 손상의 정량화 및 세포 사멸 등을 실시 예를 나타낸다. 우리는 또한 기술과 유연성의 변화를 토론하고 몇 가지 일반적인 함정을 강조 표시합니다.
서문
라이브 세포 현미경 단셀 길이 추적 새로운 기술이 아니다. 최초의 현미경에서 매니아와 과학자들은 하나의 세포와 생물, 자신의 행동, 개발 1-3을 관찰하고 연구 하였다. 1950 년대에 밴더빌트 대학에서 후반 데이비드 로저스에서 유명한 예는 황색 포도상 구균 박테리아와 식균 작용 (4) 결국 프로세스를 쫓는 혈액 도말 검사에서 인간의 호중구를 보여줍니다. 이 라이브 셀 영화는 하나의 실험에서 관찰하고 상관 관계를 할 수있는 방법을 여러 프로세스의 우수한 그림이다 : 화학 그라데이션, 역학 및 세포 운동의 속도를 감지, 세포 역학, 접착 및 병원체의 식균 작용을 형성한다.
완전 자동화 현미경 고감도 디지털 카메라들의 출현은 세포 생물학 F까지의 기본적인 질문을 현미경을 사용하여 연구자의 수가 증가 가져왔다세포가 5,6를 이동하고 역학 및 멤브레인 인신 매매 9-11 소기관에 7,8를 분할하는 방법 롬. 비 형광, 1953 년 프리츠 제르 니커의 노벨상을 얻고 위상차 (PC), 미분 간섭 대비를 포함하여 시야 현미경 (DIC) 미세 소관 번들을 포함한 세포와 핵뿐만 아니라 하위 세포 구조의 관찰을 허용 , 염색체, 핵소체, 세포 기관 역학, 두꺼운 액틴 섬유 (12). 유전자 형광 단백질을 인코딩 및 세포 소기관에 대한 형광 염료의 개발은 극적으로 시간 경과 현미경 13-15 영향을하고있다. 이 기사의 초점이 아니라 동안, 세포 타원체와 현장 (생체 내에 현미경) 공 초점 및 광자 현미경을 사용하여 이미징은 접근의 또 다른 확장을 나타내고, 사용하고 이러한 방법 16-19을 논의 뛰어난 기사가있다.
안티 canc에 대한 세포의 반응어 약물이나 천연 제품은 분자 및 세포 규모에 따라 결정됩니다. 이해 세포 반응과 운명 다음 치료는 종종 단일 세포 측정 인구 평균 분석 (예., 면역, 전체 잘 측정), 또는 면역 형광 검출에 고정 된 시간 지점 및 유동 세포 계측법을 포함한다. 집단 내의 약물 단일 세포 반응의 이질성은 종양, 특히 포화에서 동일한 약제로 처리 된 세포주와 종양을 본 반응 다양성의 일부를 설명 할 수있다. 주어진 단일 셀 또는 셀의 인구를 따르지 세로 방법 장기 분자 반응 경로의 직접적인 연구 할 수있는 덜 일반적인하지만 매우 강력한 방법입니다, 서로 다른 표현형 (예., 세포 사멸 또는 세포 분열), 관찰 세포 간 집단 내의 변화 방법 및 이러한 요소 인구 응답 20-22 역학에 기여한다. 낙관적, 수있는관찰과 약물들이 종종 실패하는 이유, 작동, 및 최선의 방법을 사용하는 방법에 대한 우리의 이해를 개선하는 데 도움이됩니다 단일 세포 반응을 정량화한다.
장기적으로 시간 경과 현미경, 종 추적 및 약물 반응의 분석 기술은 많은 연구자에 사용할 수 있으며 표현형 응답 (20, 21)을 관찰하기 만 투과광을 이용하여 간단 할 수있다. 접근법의 주요 구성 요소는 : 관심있는 세포의 적당한 제제 환경 챔버와 자동화 현미경, 카메라가 획득 및 시간 경과를 검토 할 이미지를 저장하고, 소프트웨어를 측정하고, 세포를 분석하는 컴퓨터로 통합 및 형광 바이오 센서. 우리는 시야 및 / 또는 위드 epifluorescent 현미경을 사용하여만큼 몇 일 동안 배양 된 세포의 시간 경과 현미경을 수행하기위한 많은 조언과 자세한 프로토콜을 제공합니다. 배양에서 성장 될 수있는 임의의 세포주를 사용할 수있다이 프로토콜항암 치료에 대한 자신의 반응을 연구합니다. 우리는 수집 된 데이터의 예를 제공하며, 간단하게 다른 프로브 타입의 장점과 장기간 경과 및 종 추적 단점 논의 상이한 유전자 부호화 형광 바이오 센서 및 위상차 현미경의 일례를 분석하여, 어떤 일 수 비 - 직접 접근, 우리가 접근 방식을 사용하여 고려하지 않은 경험이 연구자들에게 관심과 가치가있을 것입니다 희망 약간의 변화에서 이해하기 어려운, 경험이 풍부한 연구자하다이 방법에 대해 배웠습니다.
프로토콜
다음 프로토콜은 그림 4와 6에 대한 인수 설정 및 실험 조건에서 실험에 의해 정의 된 매개 변수를 사용합니다. 이러한 파라미터의 많은 다른 실험에 맞게 수정 될 수있다 (즉, 노출 시간, 비닝 형광 채널, 등.). 모든 절차가 제도적 지침 및 규정을 준수해야하고 제도적 바이오 안전성위원회의 승인을 받아야. 현미경 제조 업체 웹 사이트 라이브 세포 이미징을위한 훌륭한 정보가 포함되어 있습니다.
1. 현미경 및 이미징 소프트웨어
- 거꾸로 현미경의 다양한 라이브 세포 이미징을 수행합니다. 가장 일반적인 현미경 표면 형광 및 회전 디스크 공 촛점을 위드 있습니다. 여기서, 200w 메탈 할라이드 광원과 자동화되고 동력 위드의 표면 형광 현미경을 사용한다.
- 무대 정상을 얻거나 환경 챔버를 현미경. 여기에서, 무대 t을 사용영업 환경 챔버.
- 시간 경과 현미경을 실행하는 유틸리티 현미경을 운영하는 상용 소프트웨어를 사용합니다.
- 이미지 분석을위한 상용 소프트웨어 또는 ImageJ에 사용합니다. 많은 분석 도구는 상업적으로 입수 가능하고, (8, 18)를 발표되었다하는 여러 맞춤형 프로그램이있다.
2. 세포 프로세스 및 표현형 응답을 시각화
- 시야 현미경으로 세포를 시각화합니다. 단독 차동 간섭 콘트라스트 및 위상 콘트라스트 항암 약물 반응에 대한 반응을 연구하는 것은 매우 유익 할 수있다. 이러한 프로세스는 유사 분열, 세포 운동성 및 세포 사멸을 포함 할 수있다.
- 형광 바이오 센서와 세포 구조, 세포 기관 및 프로세스를 시각화합니다. 형광 프로브는 특정 세포 내 프로세스를 추적하는 정보입니다. 이러한 미세 소관 역학, 미토콘드리아와 소포체 역학, 단백질 축적과 현지화 등을 포함 할 수있다분자 신호 (예., 인산화 칼슘).
샘플 3. 준비
- 표준 세포 배양 접시에 세포 인증을 성장 습한 세포 배양기 (예, 37 입출력 C, 5 % CO 2, 80 % 상대 습도).
- EBSS와 MEM에 HT1080 세포를 성장. 10 %의 v / V의 FBS, 1 % V / V 펜 / 스트렙토 1 % V / V 피루브산 나트륨, 1 % V / V 비 필수 아미노산과 미디어를 보완.
- 영상에 이틀 전에, 공인 된 멸균 층류 흐름 후드에 12 잘 # 1.5 유리 바닥 접시의 3 우물에 판 50,000 HT1080 FUCCI 세포. 실험의 시작 ~ 60 % 합류점을 달성하기 위해 도금 된 세포의 수를 조정한다. 세포주 실험 세포 밀도의 특성에 따라 덜 수있다.
주 : 세포 밀도가 세포주의 성장 및 실험 결과에 지대한 영향을 미칠 수있다. 최소화하기 위해 세포를 계산 실험 - 투 - 실험 variabilit밀도로 인해 Y.- 환경 챔버와 실험에 필요한 조건, 하나의 잘 요리의 플레이트 세포 (일반적으로 35- 또는 60-mm), 4도 35 mm 요리, 6, 12, 24 웰 세포 배양 접시, 또는에 따라 다양한 형식의 슬라이드 커버 슬립. 세포 배양 플라스틱을 통해 # 1.5 대부분의 대물 렌즈는 유리의이 두께에 최적화 된 바와 같이 유리, 및 이미징 유리 바닥 판을 사용하는 것은 매우 좋지 않습니다.
참고 : 일부 세포주의 성장과 유리에 생존하지 않습니다. 이러한 경우, 유리 (예. 폴리 라이신이나 콜라겐) 세포 접착 성을 향상시키기 위해 코팅 될 수있다. 이 실행 가능한 옵션의 경우 일부 기업은, 그것은 경험적으로 결정해야 광학 세포 배양 플라스틱을 생산하고 있습니다.
- 환경 챔버와 실험에 필요한 조건, 하나의 잘 요리의 플레이트 세포 (일반적으로 35- 또는 60-mm), 4도 35 mm 요리, 6, 12, 24 웰 세포 배양 접시, 또는에 따라 다양한 형식의 슬라이드 커버 슬립. 세포 배양 플라스틱을 통해 # 1.5 대부분의 대물 렌즈는 유리의이 두께에 최적화 된 바와 같이 유리, 및 이미징 유리 바닥 판을 사용하는 것은 매우 좋지 않습니다.
4. 환경 상공 회의소 셋업
- 모든 실험 이전에, 설정 환경 챔버 37 O C를이 습도 80 % ~에서 동작 등 샘플 위치에서의 온도가되도록. 대부분의 세포 배양 인해 배지 중탄산 나트륨 완충액 5 % CO 2 / 밸런스 공기 분위기에서 성장한다. 셋업에 따라, 중 5 % CO 2 환경 컨트롤러를 설정하고 공기와 함께 100 %의 CO 2를 혼합, 또는 5 % CO 2 / 밸런스 공기 가스 인증, 미리 혼합 사용합니다. 가스 흐름 속도에 대한 제조 업체의 지시 사항을 따르십시오.
참고 : 일부 세포주는 CO이없이 유지 될 수있는 경우에 CO 2 -independent 배지에서 자란다. 특별히 설계된 영상 미디어 autofluorescent 화합물의 첨가를 제한하는도 사용할 수 있습니다. 목적하는 세포 유형에 대한 논문 매체에서 성장 미리 실험적으로 결정되어야한다. - 촬영에 앞서, 물이 저수지는 멸균 증류수로 (제조업체의 지침에 따라) 충전되어 있는지 확인합니다. 원하는 온도 설정으로 환경 챔버를 켜고 현미경 무대 삽입에 배치합니다. 가스를 저장하려면,이 시점에서 흐름을 시작하지 마십시오.
참고 : 단계 탑 챔버와 무대 삽입 및 / 또는 실험에 모션 아티팩트를 도입 할 수 챔버에 연결 코드에 어떤 긴장 사이에 여유 공간이있는 경우.- 무대에 커플로에 실을 실을 삽입하기 전에 단계 삽입 구멍의 가장자리 위에 파라핀 필름의 조각을 놓고, 어떤 연결이 실을 당겨되지 않았는지 확인합니다.
- 챔버 (37) 오 C.에 평형을 허용 세포 생리학에 영향을 드리프트를 도입 할 수 촬상시의 온도의 변동을 방지하기 위해 안정적인 온도를 유지한다. 도달 온도 평형은 일반적으로 환경에 따라 1 시간 30 분을 필요로한다.
- 승온하면서 챔버로 우물에서 물 '더미'요리를 삽입합니다. 챔버을 위해 도움을 물을 모방하여 샘플을 가득 이미징 요리, 충분히 예열 및 안정화된다. 예열 멸균 수와 실 충진온도 안정에 필요한 시간을 감소시키고, 시험 물질의 첨가시의 온도 저하를 최소화한다.
5. 현미경 셋업
- 현미경, 관련 컴퓨터 및 필요한 주변 장치의 전원을 켭니다.
- 광원에 따라 필요할 때까지 전원을 켜 기다릴 (예., LED).
- 낮은 위치에 대물 터릿으로 사용될 20X 0.7 NA 대물 렌즈를 선택한다.
- 대물 위에 시료를 놓고 -이 샘플 챔버 내에있을 때 쉽게 셀을 찾을 수 있도록한다.
- 이들은 이전 실험으로부터 공지되어있는 경우,이 시점에서 촬상 파라미터를 정의한다.
6. 현미경 챔버에 세포를 운반
- 운송 세포 환경 챔버로 인큐베이터에서 이미지화한다. 이 비교적 낮은 CO 2의 효과를 제한하기 위해 신속하게 수행되었는지 확인 분위기는 세포에 온도를 감소. 샘플 운송 및 유출의 경우 청소에 대한 모든 제도적 바이오 안전성 가이드 라인을 따르십시오.
- 큰 환경 변화를 방지하기 위해 밀봉 된 스티로폼 용기 또는 절연 가방에 세포를 놓습니다.
- 제조업체의 지침에 따라 챔버에 샘플 영상 접시를 삽입합니다.
- 세포는 환경 챔버 내에 확보 한 후, 안정된 환경을 유지하고 즉시 분위기 가스의 소스 (S)에 설정하는 챔버를 밀봉.
- 일부 환경 챔버 타이트한 밀봉 덮개를 사용하지 않기 때문에, 성장 배지 위에 증착 멸균 층, 배아 인증 미네랄 오일을 지연한다. 유리 이미징 영역을 방해하지 않도록주의 샘플 접시의 경계-가장자리 주위 가스 투과 파라핀 필름 랩. 지역화 보조 가습 수단을 이용할 수있다. perfor을 감소 할 수있는 샘플 접시의 뚜껑에 응축명 시야 현미경 mance.
- 초기 실험 기간 동안 열 드리프트의 영향을 최소화하기 위해, 시간 경과를 시작하기 전에 30 분 동안 기다린다. 필요한 시간은 영상 접시 크기 및 기타 요인에 따라 달라집니다. 경험적으로 결정합니다.
7. 이미지 설정
- 최선의 데이터를 나타냅니다 선택 이미징 조건. , 노출 시간을 제한 낮은 강도의 빛을 이용하여 빛의 긴 파장에 의해 여기되는 프로브를 선택하여 광독성을 방지하기 위해 조치를 취하십시오.
- 각 위치에 대하여 X, Y 및 Z 평면 원하는 파장 (들)을 정의하는 묘화한다. 시간 해상도 위치와 파장의 개수에 의해 제한된다. 대부분의 세포 과정의 장기간의 시간 경과의 경우, 하나의 화상마다 취득 10 - 20 분; 높은 시간 해상도 (짧은 간격, 예. 1 분) 이상의 데이터 포인트 때문에보다 강력한 세포 추적을 제공 할뿐만 아니라 더 통합 결과빛 노출과 큰 데이터 세트.
- - 50 밀리 초, 텍사스 레드 / TRITC - 40 밀리 초, 브라이트 - 20 밀리 초 FITC / GFP : HT1080 FUCCI 동적 녹색과 적색 형광 단백질을 가지고 (대표 결과를 참조), 다음 노출 시간을 사용합니다. 2 × 2 빈을 사용합니다.
- 고급 설정에서 기본 매개 변수를 사용하여 소프트웨어 제어 자동 초점을 사용합니다. 권장 스텝 크기 10 μm의의 자동 초점 범위를 정의합니다. 시간 경과를 시작하기 전에이 작업을 수행해야합니다. 시야 이미지 자동 초점 결코 형광 광독성 및 광표백을 줄일 수 있습니다.
- 전동 무대와 모든 현미경에 소프트웨어 제어 자동 초점 시스템을 사용하여, 직접 샘플에 초점을 맞 춥니 다. 그러나, 실험의 인수 속도를 제한 할 수있다. 연속 초점 시스템이 더 위치를 허용, 시간 경과 현미경 잘 작동 속도를 향상 제어 하드웨어 이미징 또는 취득의 높은 비율합니다. 그러나공기 유리 인터페이스의 검출에 의존 우물에서 유리 두께의 변화와 샘플의 초점을 잃을 수 있습니다.
- 미디어 O 37 ℃로 가온 한 원하는 약물 농도를 함유하는 매체의 절반을 교체 일부 미디어 교체 열 드리프트를 줄일 수 있습니다. 이 실험의 조건은 차량 (DMSO), 1 μM의 selinexor 10 μM PD0332991이다.
참고 :이 단계는 또한 일시 중지 및 실험을 다시 시작하여 인수를 시작한 후 수행 할 수 있습니다. 이 단일 세포의 사전 및 사후 약물 반응의 종 추적 할 수 있습니다. 약물의 안정성이나 신진 대사하다면 일시 중지하고 미디어가 동일한 방법으로 수행 할 수 있습니다 대체 관심사입니다. 약물 분해 또는 신진 대사를 테스트하기 위해, 처리 된 세포의 미디어는 약물 작용을 테스트하는 순진 세포에 배치 할 수 있습니다. - 시간 경과를 시작합니다.
- 시간 경과가 실행됨에 따라 이미징 필드가 초점과 chambe에 남아 있는지 확인r은 습기 (37) 오 C.을 유지
- 시점 사이의 시간 간격 동안 획득을 일시 중지하여 필요에 따라 포커스를 조정한다.
- 필요한 경우, 더 이상 실험 동안 챔버에 물을 추가 할 수 있습니다. O 37 ℃에서 미리 가온 멸균 증류수를 첨가하여 냉각 실 피
8. 시간 경과 종료
- 실험이 실행을 완료하면이 자동으로 중지로 설정되지 않은 경우, 인수를 중지합니다.
- 제대로 데이터가 손실 될 수 있습니다 완료되지 않은 경우 대부분의 소프트웨어 패키지를 자동으로 수집하는 동안 저장되지만 시간 경과가 하드 드라이브에 제대로 저장되었는지 확인하십시오.
- 현미경에서 챔버를 제거하고 승인 기관 바이오 안전성 절차에 따라 생물학적 위험 폐기물로 세포를 폐기하십시오.
9. 종 추적 및 분석 시간 경과 데이터의
- 인 분석을위한 방법론을 선택관심있는 생물학적 과정에 적합합니다. 많은 ImageJ에 대한 플러그인, 매트랩을 사용하는 프로그램 및 사용자 지정 플랫폼은 특정 애플리케이션을 위해 제작되었습니다. 도 4 및도 5에 설명 된대로 다음 방법은 핵 핵 형광 프로브의 분석의 추적을 포함한다.
- ImageJ에의 활용 채널에 대한이 .tif 이미지 스택을 엽니 다. 또는, Bioformats 플러그인을 사용하여 직접 ImageJ에의 수집 프로그램에서 열려있는 기본 파일입니다.
- 시야 이미지 또는 (사용 된 경우) 핵 라벨 채널을 사용하여 하나의 세포의 핵 내에서 ROI (region of interest)를 치고, ROI 관리자에 추가. 주 : 묘화 세포 핵 라벨이있는 경우 (예를 들어, 히스톤 H2B-EGFP.) 다음, 자동 세포 추적 시간을 통해 관심 (로아) 각각의 핵을 표현 영역을 만드는 데 사용될 수있다.
- 다음에, 시점을 진행하고 동일한 nucleu 내에서 ROI의 위치를에스. 투자 수익 (ROI) 관리자에게 투자 수익 (ROI)을 추가합니다.
- 추적 셀룰러 이벤트 (분열, 세포 사멸, 등.) 또는 셀이 더 이상 추적 될 수 없다있을 때까지 개별 셀 로아을 계속 (즉., 프레임 밖으로 이동하거나 실험이 종료 됨).
- 로아 그들이 필드에있는 시간을 통해 세포 확립되었을 때, 관심있는 형광체에 채널을 중첩. 각 시점에 대한 각 채널의 평균 형광 강도를 측정한다. 나중에 사용하기 위해 ROI 목록을 저장합니다.
- 각종 측정은 다른 실험에서 애플리케이션에 대한 ROI 내에서 이루어질 수있다. (예. 투자 수익 (ROI), 통합 강도 등 내 강도를 의미한다.) 분석 방법을 선택하는 메뉴가 나타납니다 ... 분석 → 설정 측정을 클릭합니다.
- 추적하는 동안 각각의 세포에 대한 세포의 운명 (예., 세포 사멸, 분할, 생존을) 참고. 이것은 생존 곡선과 furthe의 생성을 허용R 인구 분석.
- 두 채널에 대한 평균 강도, 치료제 (그림 5B, C)에 반응하여 세포주기 역학을 표시하는 산점도를 만들 수 있습니다.
주 : 플롯 시간 동안 각 셀에 대해 생성되거나 추적 세포 집단을 통해 평균화 될 수있다. 양적 이미징은 암 치료법에 응답하여 복잡한 세포 반응 관계를 구축 중요 할 수있다. 장기간 경과 현미경 길이 추적 및 데이터 분석 현미경 및 분석 도구의 유형을위한 많은 옵션, 다단계 공정이며,도 1에 제공된 일반적인 개요를 따른다.
결과
장기 시간 경과 현미경과 직접 종 추적은 약물 반응 중 많은 항암 효과를 연구 할 수 있습니다. 도 1의 일반 개요에 따라, 세포의 여러 실시 예는 추적 항암 약물로 치료하는 것이 유효 형광 리포터 발현 도시 한 다른 방법을 이용하여 분석한다.
혼자 위상차 현미경은 매우 유익하고 견고 유사 분열, 유사 분열의 기간과 체포, 비정상적인 세포 분열 및 세포 사멸 21,23,24 대 간기에보고합니다. 세포 분열을 대상으로 약물 종종 불리는 항 - 유사 분열 약물. 개발이 계속 (500)로 처리 (2) 및 동영상 1 및 p53의 상태 만 다른 유사한 유방암 유래 MCF7 세포주의 쌍의 2 표시 예가도 그 표적 항암제의 종류 nM의장기화와 유사 분열 (20)에 발생하는 분열 모터 단백질 키네신 -5- (KSP1, Kif11, Eg5)를 억제한다. 야생형 MCF7 세포 (도 2a) p53의 의존성 세포주기 정지 25-27을 연구 패러다임이다. 야생형 세포는 결국 떠나 크게 p53의 25의 유도로 체포, 유사 분열을 입력 몇 시간 동안 유지됩니다. p53의이 안정적인 p53의 최저 (MCF7 쉬의 p53의)에 의해 제거 될 때, 대신 그들은 유사 분열을 떠날 후 체포의 세포 반복주기 (그림 2B)를 통해 이동합니다. 세포를 수동으로 추적하고, 제 분열을 입력 유사 분열 인덱스 세포의 비율 (도 2C, D) 획득 하였다. 우리는 유사 분열 오히려 체포 및 분할없이 유사 분열을 떠나보다 두 번째 라운드를 입력 할 때 쉬 p53의 세포가 분열을 추적 관찰. 여기 분열 이벤트의 지속 시간을 나타내는 것은 아니지만, 연속적인 유사 분열, 세포 분열의 퍼센트와 연관된 세포 사멸 이벤트 사이의 시간도들 수있다(20, 21)을 장착 할.
탁산는, 예를 들어, 파클리탁셀과 도세탁셀을 위해, 췌장 및 고급 유방처럼 취급하기 어려운 것을 포함하여 많은 암에 대한 일반적인 화학 요법입니다. 파클리탁셀은 미세 소관의 동적 플러스 엔드에 결합하고, 정상적인 기능을 방해을 안정화시킨다. 파클리탁셀은 용량 의존적 효과를 언급했다, 심지어 낮은 농도에서 유사 분열 진행 및 염색체 분리 16 정상을 교란 할 수 있습니다. 염색체 충실한 편 정상 세포 증식 때 비정상적인 세포주기 정지를 실행할뿐만 아니라, 암의 진행 드라이버로서 작용할 수 이수성 초래할 수 필수적이다. 안정적으로 염색질을 나타내는 3 영화 3은 자궁 경부암 유래 HeLa 세포 도표 마커 히스톤-2B mCherry 융합 정상적인 성장 배지에서 (미도시) EGFP 융합 베타 튜 불린 1 나노 파클리탁셀로 처리 하였다. 이에예, 유사 분열을 통해 입국 및 진행은 다음에 할 수 있습니다. 분열시기 그러나 염색체 정렬 및 분리 불량 염색체 분리를 나타내는 구조 인 핵 벌지 및 소핵 결과 아니라,이 셀 정상 나타난다. 소핵은 염색체 또는 염색질의 대규모 조각입니다 DNA 손상 및 chromothripsis,하는 경향이 있습니다 -이 종양 진화 (28, 29)에서 중요한 의미를 가지고있다. 여기에 표시되지는 않았지만, 다른 유사 분열 구조와 관련하여 이러한 세포의 운명과 소핵의 기원은 직접적으로 장기간의 시간 경과를 사용하여 추적 할 수 있습니다. 하는 DNA 손상 기자 염색체 편석 소핵과 DNA 손상 사이의 관계를 수립하는데 사용될 수와 또한, 염색질 마커 표현.
열거 세포 프로세스를 추적 할 새로운 기자가 지속적으로 개발되고있다 위해 형광 기자 수 있습니다. 예를 들어충분한, 세포주기는도 4. 항암 치료 표적의 개발에 특히 관심의 단계로 구성하고 영화 4는 섬유 육종 유래 세포주 안정적 두 기자 불리는 공동 발현 (HT1080) 형광 유비퀴틴 세포주기 지표를 나타낸다 (FUCCI) 30. 현재 시스템에서, Cdt1 폴리펩티드의 부분 G1 상에 mKO2 (단량체 Kusabira 오렌지 2) 증가에 융합되고 초기 S 단계에서 분해되고, geminin의 부가 MAG에 융합된다 (단량체 Azami 녹색) 중순 S-단계에서 증가하고는 anaphase (핵분열 말기)에 따라 저하된다. 이 세포는 정상적인 성장 배지이며 15 시간.도 5a는 B와 Movie 5 10 μM의 PD0332991하는 Cdk4에 / 6 억제제로 치료 정상 배지에서 동일한 셀을 보여주는 세포주기를 통해 진행한다. 세포를 G2 상을 진행 정상적으로 분할 강하게 영향의 가능성을 나타내는 후속 G1 상에 검거성장하는 종양 세포 증식 억제 효과를 필자.도 5c는, D 및 영화 6 exportin-1 (XPO1를, 일명 CRM1을, 작은 분자라는 selinexor (KPT-330), 핵 수출 단백질 억제제 강력한 치료를 일반 매체에 동일한 세포를 표시 ). 이들 화합물은 조사 (31, 32)에서 현재의 핵 수출 (SINE)과 항암 효과의 선택적 억제제 불린다. 강력한 세포주기 및 세포 표현형 죽음 33,34 SINE의 치료 결과. 이 예는 정상 반응 속도 (약 6 시간)와 G1 단계를 통해 진행 셀을 보여 주지만, 처리 SINE 모두 빨간색과 녹색 신호 (약 3 제어 시간 만 10 기간으로 표시된 바와 같이 S 상 진행 지연을 경험 ). 이 세포는 21 시간 30 분 후 늦게 S- 또는 G2 상에 죽는다; 정상 세포주기는 약 15 시간이다. selinexor의 효과는 다른 혈액 및 고형암 (35)에 대한 연구되고있다.
항암 치료의 의지는 치명적인 DNA 손상으로 인한 세포 독성이다. 예를 들어, 토포 이소 머라 제 I 및 / 또는 II 타겟팅 것과 - DNA 손상, 방사선, 백금 계 부가 물 및 소분자 약물을 포함한 많은 치료법을 통해 유도 될 수있다. 많은 조합 요법은 또한 별도의 경로를 통해 손상을 유발하거나 손상을 복구하는 세포의 능력을 차단하거나하여 DNA 손상 축 공격한다. 역학 및 손상의 수준과 경우 이는 세포 사멸이 발달 치료제에 널리 중요하다 발생 방법. 안정적으로 정상적인 성장에 이중 가닥 DNA 손상 기자, mCherry-BP1-2 (36)을 표현하는 6, 영화 7 쇼 HT1080 세포를 그림 매체는 10 μM 에토 포 시드 (VP-16), 토포 이소 머라 제 II 독으로 처리 하였다. 이 기자는 DNA 이중 가닥 브레이크 사이트 단백질의 일부, mCherry 융합되어 53BP1로 구성되어 있습니다. 이 세포의 핵은 USI를 추적했다ImageJ에와 통합 mCherry-BP1-2 신호의 분석 입자 플러그인을 ng를하는 수용성 핵 프로브를 제거 값을 임계 화 한 후 각각의 프레임을 측정 하였다. DNA 손상 제 10 시간 최소화하고 꾸준히 증가한다. 토포 이소 머라 제 II 억제제는 효소 37,38 가장 활성화 될 때, 특히 S- 및 G2 상에 영향을 미치는 것으로 알려져있다. 세포주기 관련 손상을 나타낼 수있다 본 실시 예에서 관찰 된 반응 속도; FUCCI 기자와 mCherry-BP1-2을 결합하면 다음 운명을 셀에 링크 될 수있는 피해의 타이밍을 설명 할 수있다.

항암제 응답 연구에 장기 시간 경과 현미경 및 종 추적을 사용하여 그림 1. 개요. 원하는대로 표시된 적절한 라이브 세포 이미징 요리의 세포는 세포 또는 관심 영역 추적, 이미지화되고, 데이터는 분석. 많은 방법은 몇 가지가 여기에 표시됩니다 세포를 추적하고 정량화하기 위해 존재한다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
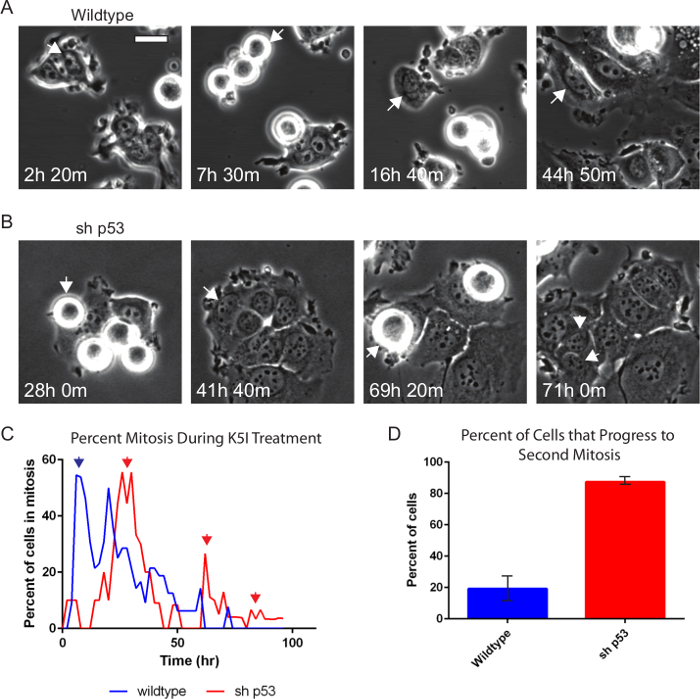
그림 2. 위상 콘트라스트 시간 경과 현미경은 안티 - 유사 분열 약물 치료. 야생형 (A) 및 p53의-최저 (B) MCF7 세포는 500 nM의 키네신-5 억제제로 처리하고, 96 매 10 분 군데 있었다 후 p53의 의존성을 보여줍니다 20 배 PH2 0.70 NA 렌즈가 위상차 현미경을 사용하여 시간. 개별 셀을 수동으로 추적하고 퍼센트 유사 분열 및 세포가 시간 경과시 또 다른 분열로 진행하는 경우 획득 된 하였다. 화살표 추적되는 셀을 나타냅니다. 쉬 p53의 전지 (B)는 제 분열 들어가면 나눈다. (C) 두 세포주 SHO높은 피크 퍼센트 (제 1 파란색과 빨간색 화살표) 유사 분열로 나타낸 바와 같이 w 연장 유사 분열 체포. (C, D) 약 90 p53이없는 세포 % (쉬 p53의 N = 87) 20 야생형의 % (N = 130)에 비해 쇼를 계속 진행 (빨간색 화살표). 오차 막대는 표준 편차를 나타냅니다. 바 = 20 μm의. 영화 1, 2. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 3. 염색질 마커 히스톤도 2b는 저용량 파클리탁셀 치료. 파클리탁셀은 세포의 성장과 분열의 복잡, 농도 의존적 결함을 초래 미세 소관 타겟 약물 후 염색체 독방 이상 유무의 증거를 보여준다. 염색질의 조직은 무대를 포함, 다른 세포 상태에 알린다유사 분열 및 세포 죽음의. 헬라 세포는 안정적으로 1 나노 파클리탁셀 처리 하였다 가설 2b-mCherry 및 β-tubulin에-EGFP를 모두 표현. 이 세포는 계면 초기에 유사 분열과 분열의 단계를 통해 진행한다. 유사 분열의 시간이 정상 표시하지만, (화살표) 해결 염색체 부착과 분리 오류의 증거가있다. 이러한 세포의 운명은 길이 추적하여 결정될 수있다. (도시하지 않음) 위상 콘트라스트와 형광 이미지는 20X PH2 0.70 NA 렌즈와 10 분마다 1 프레임에서 획득 하였다. 바 = 10 μm의. 영화 3. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 4. 형광 세포주기 마커는 세포주기 진행의 직접 모니터링 할 수.(A) 위상차 형광 의해 이미징 FUCCI 시스템을 발현하는 살아있는 HT1080 섬유 육종 세포의 필드. (B는 C) 패널 (A)에서 점선 상자의 유사 분열 세포가 따른다. 일반적으로 약 15 시간에 세포주기를 통해 진행. 유사 분열 후 세포는 잠시 희미하고, 그들이에와 G1 단계를 통해 진행으로 다음 빨간된다. 세포는 S 단계를 입력하면 빨간색 Cdt1 프로브 저하 및 녹색 geminin 프로브가 증가합니다. 모두 프로브가 존재하는 간단한 약 3 시간 기간은 초기 S-단계를 나타냅니다. 세포가 S- 및 G2 단계를 통해 향후 유사 분열로 진행하면서 그들은 녹색 남아있다. 녹색 프로브는 세포 분열의 anaphase (핵분열 말기)에 따라 저하된다. 위상 콘트라스트와 형광 이미지는 20X PH2 0.70 NA 렌즈와 10 분마다 1 프레임에서 획득 하였다. 바 = 10 μm의. 영화 4. VI에 대한 여기를 클릭하십시오이 그림의 더 큰 버전 EW.

그림 5. 세포주기 별 영향과 관련 세포 죽음. 같은 세포 그림 4와 같이 라인하지만 서로 다른 항암 목표를 나타내는 두 개의 다른 분자로 처리. 치료 후 시간이 표시됩니다. 10 μM PD0332991의 Cdk4 / 6 억제제 늦은 S / G2 상 세포 치료 후 (A, B)은, 그것을 세포 유사 분열 (M) 및 분할 정상적으로 진행한다. 한 딸 세포는 핵에 대한 관심의 영역에서 빨간색과 녹색 형광 강도를 측정하여 추적됩니다. 세포는 약 40 시간 동안 G1 단계에서 체포 상태를 유지합니다. 1 μM의 selinexor으로 늦은 G2 상 세포 치료 후 (C, D)은 그것이 세포 유사 분열 (M) 및 분할 정상적으로 진행한다. 한 딸 셀을 추적하며, G1 상 진입을 통해 진행된다장기화 초 S 상 (빨간색과 녹색 신호)에 전적으로 녹색 전환, 21 시간 30 분 후 죽는다. 데이터는 S 상 진행이 selinexor 치료에 의해 영향을받는 것이 좋습니다. 위상 콘트라스트와 형광 이미지는 20X PH2 0.70 NA 렌즈와 10 분마다 1 프레임에서 획득 하였다. 바 = 10 μm의. 영화 (5, 6). 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

약물 치료. 많은 항암 치료 후 그림 6. DNA 손상 역학은 근본적으로 세포 반응과 치료의 성공에 영향을 줄 수있는 DNA 손상이 발생할. HT1080 세포를 안정적으로 발현 모두 이중 가닥 DNA 손상 마커 mCherry-BP1-2 및 가설 2b-EGFP (도시 생략) 토포 이소 머라 제 II 약물 에토 포 시드 및 DNA (D)의 10 μM으로 처리하여amage 추적했다. (A) 수 및 에토 후 초점 증가 강도. 래그는 에토 포사이드의 공지기구에 부합 가능한 세포주기의 효과를 나타내는 초기있다. 22 시간 50 분으로이 세포 손상의 높은 수준을 축적하고있다. 여기에 도시되지는 않았지만,이 세포의 운명을 직접 추적함으로써 결정될 수있다. (B)는 가설 2b-EGFP 신호를 통해 얻은 핵에 해당하는 투자 수익 (ROI)은 ImageJ에있는 입자 추적을 사용하여 추적하고 통합 BP1-2 mCherry 신호를 정량화하고 시간이 지남에 그려졌다. 약 10 시간까지의 신호 지연은 지속적인 증가로 이어 유의한다. 형광 이미지는 40X PH2 0.75 NA 렌즈와 10 분마다 1 프레임에서 획득 하였다. 바 = 10 μm의. 영화 7. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

안티 - 유사 분열 약물 치료. 야생형 MCF7 세포 후 야생형 MCF7 세포의 영화 1 단계 대비 시간 경과 현미경은 500 nm의 키네신-5 억제제로 치료와 20 배 PH2와 위상차 현미경을 사용하여 96 시간 동안 매 10 분 군데 있었다 0.70 NA 렌즈. 그림 2에 기술 된 바와 같이 유사 분열에서 장기간 유사 분열의 체포와 출구, 관찰 할 수있다. 이 파일을 다운로드하려면 여기를 클릭하십시오.
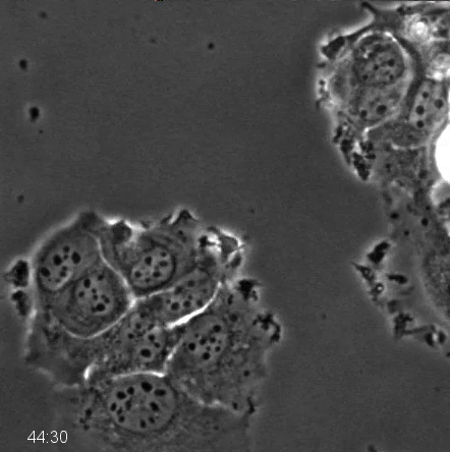
안정적으로 분해 p53의를 대상으로 작은 헤어핀 RNA를 발현하는 안티 - 유사 분열 약물 치료. MCF7 세포 후 p53의-넉다운 MCF7 세포의 영화 2 단계 대비 시간 경과 현미경은 500 nm의 키네신-5 억제제로 치료하고, 20 배 PH2 0.70 NA 렌즈가 위상차 현미경을 사용하여 96 시간 동안 10 분마다 군데. 그림 2에 기술 된 바와 같이 장기간 유사 분열의 체포와 유사 분열의 여러 라운드, 관찰 할 수있다. 이 파일을 다운로드하려면 여기를 클릭하십시오.

안정적으로 H2B - mCherry을 표현 저용량 파클리탁셀 치료. HeLa 세포와 β-tubulin에-EGFP 후 헬라 세포의 영화 3. 형광 시간 경과 현미경은 1 나노 파클리탁셀로 처리 하였다. 그림 3에 설명 된대로 염색체 부착 및 분리 문제는, 관찰 할 수있다. 이미지는 20X PH2 0.70 NA 렌즈 매 10 분을 인수했다. 이 파일을 다운로드하려면 여기를 클릭하십시오.
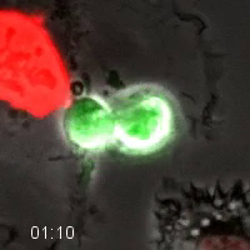
영화 4. 형광 세포주기 마커는 세포주기 진행의 직접 모니터링 할 수. FUCCI 시스템을 표현 HT1080 세포가 길이 방향으로 시간 경과 현미경 동안 추적했다. 세포는 분열을 종료 한 후 희미한 진행 한 다음 세포가 G1 단계를 통해 진행 빨간색이됩니다. 셀이 S 상 입력으로 녹색 geminin 프로브 증가와 홍 Cdt1 프로브가 분해되고, 그것은 노란색된다. 이 S- 및 G2 단계를 통해 진행 세포가 녹색으로 남아있다. 세포가 anaphase (핵분열 말기)를 입력으로 녹색이 저하됩니다. 이 세포의 정량은 그림 4에 표시됩니다. 이미지는 20X PH2 0.70 NA 렌즈 매 10 분을 인수했다. 이 파일을 다운로드하려면 여기를 클릭하십시오.
영화 5 "SRC ="/ 파일 / ftp_upload / 53994 / 53994movie5.jpg "/>
G1 상 억제제 치료 후 형광 세포주기 마커 표현 영화 5 HT1080 세포. FUCCI 시스템을 발현 HT1080 세포는 10 μM PD0332991하는 Cdk4에 / 6 억제제로 처리 하였다. 추적 세포 유사 분열 및 분할 정상적으로 진행됩니다. 한 딸 추적하고, 영화의 기간 동안 G1에 빨간 남아있다. 정량화가 그림 5에 표시됩니다. 이미지는 20X PH2 0.70 NA 렌즈를 매 10 분을 인수했다. 이 파일을 다운로드하려면 여기를 클릭하십시오.

Exportin-1 억제제, Selinexor. FUCCI 시스템을 표현 HT1080 세포에 처리 한 후 형광 세포주기 마커를 표현하는 영화 6 HT1080 세포는 치료했다1 μM의 selinexor와 에디션. 늦게 G2 상 세포 유사 분열을 추적 하였다. 딸 세포는 G1 상 (적색)을 통해 진행 및 S 상 (노란색)을 입력합니다. 늦은-S / G2 단계에 진입하고 21 시간 치료 30 분 후 사망 할 때까지 셀은 S-단계에 걸쳐 천천히 진행한다. 정량화가 그림 5에 표시됩니다. 이미지는 20X PH2 0.70 NA 렌즈를 매 10 분을 인수했다. 이 파일을 다운로드하려면 여기를 클릭하십시오.
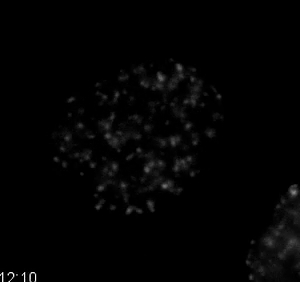
토포 이소 머라 제 II 억제제. HT1080 세포가 안정적으로 이중 가닥 DNA 손상 마커 mCherry-BP1-2 및 H2B-EGFP를 발현과 치료 후 영화 7. DNA 손상의 역학은 10 μM 에토 포 시드, 토포 이소 머라 제 II 억제제로 치료했다. mCherry-BP1-2는 영화에 표시됩니다. 치료로 계속S, mCherry-BP1-2 증가 신호는 이중 가닥 DNA 손상을 증가 나타낸다. 정량화가 그림 6에 표시됩니다. 이미지는 40X PH2 0.75 NA 렌즈를 매 10 분을 인수했다. 이 파일을 다운로드하려면 여기를 클릭하십시오.
토론
시간 경과 현미경 및 종 추적의 장점
이 연구자들은 각 셀 그들의 운명뿐만 아니라 전체 모집단을 추적 할 수 있도록, 상기 현미경은 약물 반응 종의 연구를위한 이상적인 도구이다. 세포 집단 내에서 약물 반응의 다양성은 항암 치료 설계를위한 중요한 문제입니다. 단일 세포의 종 추적 수사관이 변화를 관찰하고 세포 인구에 관한로서 기본 메커니즘과 결과를 이해하기 시작 할 수 있습니다. 형광 프로브의 다양한 활용하여 관찰하고 일반적인 희귀 응답 표현형 모두를 이해하는 방법의 군중을 제공한다. 인구 응답 타이밍과 다른 세포 운명의 기여는, 치료시 세포주 또는 국가 간의 응답의 특정 표현형과 운명, 그리고 차이 사이의 관계를 배울 수있는 예입니다. 많은 암 관련 프로세스를 연구 할 수있다. 이 문서에서 강조되지 않은 일부는 세포 사멸, 자식 작용과 세포 사멸 및 괴사 기자 39-42, 세포 침공 43, 44, 및 세포 운명 결정 (27)을 결정 p53의 역학을 포함한다. 또한,이 방법은 항암 치료제의 연구 조사에 한정되지 않는다. 같은 원리 48 신호 유사 분열 (45) 세포 골격 역학 (46, 47)와 세포를 포함한 다른 많은 생물학적 과정을 연구하는 데 사용할 수 있습니다.
시간 경과 형광 현미경은 단백질과 관심의 분자의 현지화 및 강도 데이터를 제공 할 수 있습니다. 뿐만 아니라, 약물 반응에 중요한 단백질 레벨의 변화가 있지만, 세포 내 단백질의 적절한 (또는 부적절한) 버전 이해 응답 중요하다. 시간 경과 현미경 (단백질 지역화 된 위치에 대한 데이터를 제공합니다 예., 핵, 세포질, 특정 세포 기관,등.) 약물 치료 방법과 현지화 및 전체 레벨이 단일 셀과 인구 수준에서 시간이 지남에 따라 변경 후.
도전과 한계
시간 경과 현미경 및 단일 세포의 종 방향 분석의 장점에도 불구하고, 한계가있다. 형광 기자는 안정성과 특이성에 의해 제한됩니다. 형광 융합 단백질을 설계 할 때, 광 안정 밝 프로브를 선택하는 것이 중요하지만, 그 정상적인 기능을 제대로 지역화 능력에 관한 관심의 단백질에 연결되는 형광 물질의 효과를 고려하는 것도 필요 . 이러한 문제는 다른 곳에서 자세히 설명되어 있고 15,49,50 출판 된 많은 사용 가능한 형광 태그 단백질이있다. 기타 형광 라벨 또는 태그를 세포에 첨가 할 수있어,주의가 독성되지 않도록주의해야한다. 우리의 경험에서,이 페이지가운은, 예를 들어 미토콘드리아 라벨 (막 전위) 또는 세포 투과성 DNA 염료를 들어, 쉽게 표백하는 경향으로 인해 세포 증식에 희석 아웃 될 것입니다.
또한, 성장 및 현미경에 세포를 관찰 많은 기술적 인 어려움이있다. 온도, 습도, 분위기, 광 불안정성에 관해서는 데이터 손실 또는 심지어 전체 실험의 결과, 세포에 많은 영향을 미칠 것이다. 촬상에 대한 안정성 문제 무비 1 및 2에서 볼 수있다. 이러한 효과는 (4.2 참조) 파라핀 필름의 사용을 통해 최소화 할 수있다. ImageJ에 (NIH)을 이용하여, 예를 들어 사후 - 취득 처리 가능한 이미지 안정화 알고리즘도있다. 종종 간과 장기간 경과의 양태는 데이터 관리 및 파일 크기이다. 데이터 비닝 경우에도, 하나의 시간 경과 실험 30 기가 바이트를 초과 많다. 대용량, 고속의 신뢰성있는 데이터의 저장 및 전송이 강한LY는 격려했다. 몇 군데되는 형광 바이오 센서 (들)에 따라, 예를 들면 핵이나 세포질 센서 전체 해상도 이미지를 획득하는 것이 필요하지 않습니다. 가능하면 우리는 쉽게 발생하는 데이터, 덜 까다로운 컴퓨팅 요구, 개선 된 작업 흐름으로 작은 일을 지정 크기가 파일을 유지하는 조치를 취하도록 권장합니다.
장기적으로 시간 경과 현미경을 수행 할 때 광독성 주요 관심사입니다. 높은 강도의 빛과 긴 노출 형광 프로브, 세포 스트레스와 세포 사멸의 photobleaching에 발생할 수 있습니다. 이러한 효과는 데이터에 큰 영향을 미칠 및 실험의 부실로 이어질 수 있습니다. 카메라 비닝 및 이득은 노출 시간을 감소 시키는데 사용될 수있다. 광로에 감광 필터가 샘플에 빛의 강도를 감소시킨다. 이미지에 사용되는 빛의 파장은 세포에 영향을 미칠 것입니다. 짧은 파장 (UV, 근처 UV)은 세포에 더 많은 손상하고보다 빠른 속도로 사진 표백 결과긴 파장 (예., 빨강, 멀리 빨간색). 목표의 선택은 조건 이미징에 영향을 줄 수 있습니다. 높은 개구 수 (NA)의 렌즈보다 높은 해상도의 이미지를 생성하지만, 높은 배율 적은 광이 높은 노광 배 이상 강한 빛 얻어진 샘플로부터 송신 할 수있다. 목적은 오버 샘플링없이 관심의 개체를 해결할 적절한 NA 및 배율을 선택해야합니다. 많은 경우, 가장 높은 목표는 가장 적절한 선택이 아닐 수있다. 더 많은 필드가 원하는 객체의 해상도를 손상시키지 않고, 효과적으로 샘플 크기를 증가 캡처 할 핵 프로브 (도 4, 5)으로 저배율의 목적은 허용한다. 세 가지 차원에서 장기 시간 경과로 인해 통합 된 빛의 노출에 조심스럽게 수행해야합니다. 회전하는 디스크 공 초점 현미경, 민감한 카메라를 사용 (예., EM-CCD) 카메라 이득 및 z 시리즈에 대한 빠른 압전 모터는 suggeste입니다d를 빛 노출을 줄일 수 있습니다. 고속 Z 계 획득은 획득주기 동안 발생하는 세포 이동 및 역학 때문에 모션 아티팩트를 최소화하는 것이 중요하다. 많은 서로 다른 설정을 이용하여 미처리 세포의 경험적 분석은 특정 세포주에서 또는 리포터 형광의 효과를 결정하는데 유용 할 수있다. 또한, 처리되지 않은 대조군은 실험 설정의 세포 독성 효과를 결정하기 위해 각각의 실험에 포함되어야한다.
기술의 변화
장기 시간 경과는 강력하고 매우 유연합니다. 공동 배양 기술, 다른 세포주 또는 상이한 리포터 발현 같은 세포주를 사용하는 것이 이용 될 수있다. 이것의 한 예는 뛰어난 항암 약물에 반응 죽어 표적 세포와 대 식세포를 묘화한다. 또 다른 예는 약 순 인접 셀에 셀 응답의 영향을 연구 할 수 있었다. 사진 ACTIVA와 결합teable, 사진 변환 및 사진 전환 형광 단백질, 특정 효과를 유발하는 빛에 의해 활성화 될 수있는 설계 단백질 (예., KillerRed)는 많은 가능성이있다. 더 복잡한 방법은, 예컨대, 포스터 공명 에너지 전달 (FRET)을 photobleaching에 후 형광 재분배, 슈퍼 해상도 (예., 확률 광학 재구성 현미경 (STORM) 구조 조명 현미경 (SIM)과 같은 현미경의 다양한 특화된 형태를 사용하는 것이 사용될 수있다 또는 유도 방출 고갈 (STED)), 및 많은 다른 사람과 장점과 각 방법의 제한이 있습니다.
장기 (예., 주, 월) 반응 및 약물 제거 후 세포의 회복은 항암 약물 작용을 이해하는 핵심이다. 격자 유리 바닥 요리 반복적으로 인구 / 지역 내의 특정 세포 또는 지역을 모니터링 할 수있는 유용한 도구입니다. 예를 들어, 리딩 된 접시 초기 DRUG 반응 약물을 제거 할 수 있고, 시간 경과를 사용하여 이미지화 될 수 있고, 그리드의 특정 영역을 원하는 시점에서 시간이 지남에 이미징 또는 추가 시간 경과를 실시 할 수있다. 접시에 유리 저부 스크라이브 도구 중 절단하거나 상업적 시약을 사용하여 제거 될 수 있고, 유리 셀은, 예를 노화 관련 β-galactocidase 활동에 대한 관심의 다른 마커에 대해 염색 할 수 있으며, 비교 시간 경과 세포가이 상태에 도달하는 방법의 역사를 이해합니다. 세포 집단이 충분히 큰 경우도 면역의 대상 또는 유세포있다.
두꺼운 샘플은 전통적으로 다양한 겔 물질 및 매트릭스의 예 타원체를 들어, 이미지에 어려웠다. 새로운 셀은 항암 치료제에 반응하는 방법 시츄 이해에서 행 방식을 확장하는 데 사용할 수있는 형광 공 초점 또는 다중 광자 현미경 16,18,19,51 등 접근한다. 그만큼자체 연구와 우리가 항암 약물을 사용하는 우리의 능력을 개선하는 데 도움이됩니다 단일 세포의 약물 동력학에 대한 이해를 개발하는쪽으로 이동되는 24,52-54 명확하게 보여 항암 약물 반응을 연구하기 위해 시간 경과를 사용하여 과학자의 수가 증가 보다 효과적이고, 아마 항암 약물 반응을 예측한다.
공개
The authors have no conflicts of interest to disclose.
감사의 말
We thank Joshua Marcus for technical support and Jolien Tyler, Ph.D., Director of the Richard J. McIntosh Light Microscopy Core Facility, for technical advice. This work was supported by funds from the University of Colorado Boulder and the University of Colorado Boulder Graduate School to J.D.O. R.T.B. is partially supported by pre-doctoral training grant from the NIH (T32 GM008759). We thank Karyopharm Therapeutics, Inc. for selinexor and Merck Serono for Kinesin-5 inhibitor. FUCCI plasmids are from Atsushi Miyawaki (RIKEN, Japan) via MTA. mCherry-BP1-2 was from Addgene. HeLa expressing H2b-mCherry and β-tubulin-EGFP are from Daniel Gerlich (IMBA, Austrian Academy of Sciences, Austria).
자료
| Name | Company | Catalog Number | Comments |
| Taxol (paclitaxel) | Sigma | T7191 | microtubule stabilizing drug |
| Etoposide | Selleckchem | S1225 | topoisomerase II inhibitor |
| Selinexor | Karyopharm Therapeutics | na | XPO1/CRM1 inhibitor, gift |
| Kinesin-5 inhibitor | Merck Serono | na | gift, also available from American Custom Chemicals Corporation. CAS 858668-07-2 |
| Cell growth medium | HyClone (Fisher) or Mediatech | many companies available | |
| 5% CO2/balance air, certified | Airgas | Z03NI7222004379 | |
| 35 mm Dish, 20 mm glass bottom | Cellvis | D35-20-1.5-N | many companies available |
| 35 mm 4-well Dish, 20 mm glass bottom | Cellvis | D35C4-20-1.5-N | many companies available |
| 35 mm Dish, gridded glass bottom | MatTek | P35G-2-14-CGRD | many companies available |
| Multi-well, glass bottom | Cellvis | P12-1.5H-N | many companies available |
| Olympus IX81 inverted epifluorescence microscope | Olympus | ||
| Olympus IX2-UCB controller | Olympus | ||
| PRIOR LumenPro200 | Prior Scientific | Lumen200PRO | |
| PRIOR Proscan III motorized stage | Prio Scientific | H117 | |
| STEV chamber | InVivo Scientific | STEV.ECU.HC5 STAGE TOP | |
| Environmental Controller Unit | InVivo Scientific | STEV.ECU.HC5 STAGE TOP | |
| Hamamatsu ORCA R2 CCD with controller | Hamamatsu | C10600 | |
| Nikon Eclipse Ti | Nikon | ||
| Nikon laser launch | Nikon | ||
| SOLA light engine | lumencor | ||
| iXon Ultra 897 EM-CCD | ANDOR | ||
| TOKAI HIT inclubation chamber | TOKAI HIT | TIZSH |
참고문헌
- Abercrombie, M., Heaysman, J. E., Pegrum, S. M. The locomotion of fibroblasts in culture I. Movements of the leading edge. Exp Cell Res. 59, 393-398 (1970).
- Abercrombie, M., Heaysman, J. E. Observations on the social behaviour of cells in tissue culture. I. Speed of movement of chick heart fibroblasts in relation to their mutual contacts. Exp Cell Res. 5, 111-131 (1953).
- Landecker, H. Seeing things: from microcinematography to live cell imaging. Nat Methods. 6, 707-709 (2009).
- The Chase - Panoramic QuickTime Movie of Classic Rogers Neutrophil Chasing S aureus Bacteria. Bepress. , Available from: http://works.bepress.com/gmcnamara (2012).
- van Roosmalen, W., Le Devedec, S. E., Zovko, S., de Bont, H., Bvan de Water, Functional screening with a live cell imaging-based random cell migration assay. Methods Mol Biol. 769, 435-448 (2011).
- Krueger, E. W., Orth, J. D., Cao, H., McNiven, M. A. A dynamin-cortactin-Arp2/3 complex mediates actin reorganization in growth factor-stimulated cells. Mol Biol Cell. 14, 1085-1096 (2003).
- Cluet, D., Stebe, P. N., Riche, S., Spichty, M., Delattre, M. Automated high-throughput quantification of mitotic spindle positioning from DIC movies of Caenorhabditis embryos. PLoS One. 9 (e93718), (2014).
- Held, M., et al. Cell Cognition: time-resolved phenotype annotation in high-throughput live cell imaging. Nat Methods. 7, 747-754 (2010).
- Orth, J. D., Krueger, E. W., Weller, S. G., McNiven, M. A. A novel endocytic mechanism of epidermal growth factor receptor sequestration and internalization. Cancer Res. 66, 3603-3610 (2006).
- Rowland, A. A., Chitwood, P. J., Phillips, M. J., Voeltz, G. K. ER contact sites define the position and timing of endosome fission. Cell. 159, 1027-1041 (2014).
- Merrifield, C. J., Feldman, M. E., Wan, L., Almers, W. Imaging actin and dynamin recruitment during invagination of single clathrin-coated pits. Nat Cell Biol. 4, 691-698 (2002).
- Centonze Frohlich, V. Phase contrast and differential interference contrast (DIC) microscopy. J Vis Exp. , (2008).
- Drummen, G. P. Fluorescent probes and fluorescence (microscopy) techniques--illuminating biological and biomedical research. Molecules. 17, 14067-14090 (2012).
- Guan, Y., et al. Live-cell multiphoton fluorescence correlation spectroscopy with an improved large Stokes shift fluorescent protein. Mol Biol Cell. 26, 2054-2066 (2015).
- Snapp, E. L. Fluorescent proteins: a cell biologist's user guide. Trends Cell Biol. 19, 649-655 (2009).
- Orth, J. D., et al. Analysis of mitosis and antimitotic drug responses in tumors by in vivo microscopy and single-cell pharmacodynamics. Cancer Res. 71, 4608-4616 (2011).
- Brown, E., Munn, L. L., Fukumura, D., Jain, R. K. In vivo imaging of tumors. Cold Spring Harb Protoc. (5452), (2010).
- Chittajallu, D. R., et al. In vivo cell-cycle profiling in xenograft tumors by quantitative intravital microscopy. Nat Methods. 12, 577-585 (2015).
- Nakasone, E. S., Askautrud, H. A., Egeblad, M. Live imaging of drug responses in the tumor microenvironment in mouse models of breast cancer. J Vis Exp. (50088), (2013).
- Orth, J. D., et al. Quantitative live imaging of cancer and normal cells treated with Kinesin-5 inhibitors indicates significant differences in phenotypic responses and cell fate. Mol Cancer Ther. 7, 3480-3489 (2008).
- Gascoigne, K. E., Taylor, S. S. Cancer cells display profound intra- and interline variation following prolonged exposure to antimitotic drugs. Cancer Cell. 14, 111-122 (2008).
- Yang, R., Niepel, M., Mitchison, T. K., Sorger, P. K. Dissecting variability in responses to cancer chemotherapy through systems pharmacology. Clin Pharmacol Ther. 88, 34-38 (2010).
- Orth, J. D., McNiven, M. A. Get off my back! Rapid receptor internalization through circular dorsal ruffles. Cancer Res. 66, 11094-11096 (2006).
- Li, J., et al. Co-inhibition of polo-like kinase 1 and Aurora kinases promotes mitotic catastrophe. Oncotarget. 6, 9327-9340 (2015).
- Orth, J. D., Loewer, A., Lahav, G., Mitchison, T. J. Prolonged mitotic arrest triggers partial activation of apoptosis, resulting in DNA damage and p53 induction. Mol Biol Cell. 23, 567-576 (2012).
- Batchelor, E., Loewer, A., Mock, C., Lahav, G. Stimulus-dependent dynamics of p53 in single cells. Mol Syst Biol. 7 (488), (2011).
- Purvis, J. E., et al. p53 dynamics control cell fate. Science. 336, 1440-1444 (2012).
- Zhang, C. Z., Leibowitz, M. L., Pellman, D. Chromothripsis and beyond: rapid genome evolution from complex chromosomal rearrangements. Genes Dev. 27, 2513-2530 (2013).
- Zhang, C. Z., et al. Chromothripsis from DNA damage in micronuclei. Nature. 522, 179-184 (2015).
- Sakaue-Sawano, A., et al. Visualizing spatiotemporal dynamics of multicellular cell-cycle progression. Cell. 132, 487-498 (2008).
- Neggers, J. E., et al. Identifying drug-target selectivity of small-molecule CRM1/XPO1 inhibitors by CRISPR/Cas9 genome editing. Chem Biol. 22, 107-116 (2015).
- Gravina, G. L., et al. XPO1/CRM1-Selective Inhibitors of Nuclear Export (SINE) reduce tumor spreading and improve overall survival in preclinical models of prostate cancer (PCa). Journal of hematology and oncology. 7 (46), (2014).
- Mendonca, J., et al. Selective inhibitors of nuclear export (SINE) as novel therapeutics for prostate cancer. Oncotarget. 5, 6102-6112 (2014).
- Marcus, J. M., Burke, R. T., DeSisto, J. A., Landesman, Y., Orth, J. D. Longitudinal tracking of single live cancer cells to understand cell cycle effects of the nuclear export inhibitor, selinexor. Scientific reports. 5, 14391(2015).
- Senapedis, W. T., Baloglu, E., Landesman, Y. Clinical translation of nuclear export inhibitors in cancer. Semin Cancer Biol. 27, 74-86 (2014).
- Dimitrova, N., Chen, Y. C., Spector, D. L., de Lange, T. 53BP1 promotes non-homologous end joining of telomeres by increasing chromatin mobility. Nature. 456, 524-528 (2008).
- D'Arpa, P., Beardmore, C., Liu, L. F. Involvement of nucleic acid synthesis in cell killing mechanisms of topoisomerase poisons. Cancer Res. 50, 6919-6924 (1990).
- Palmitelli, M., de Campos-Nebel, M., Gonzalez-Cid, M. Progression of chromosomal damage induced by etoposide in G2 phase in a DNA-PKcs-deficient context. Chromosome research : an international journal on the molecular, supramolecular and evolutionary aspects of chromosome biology. , (2015).
- Albeck, J. G., Burke, J. M., Spencer, S. L., Lauffenburger, D. A., Sorger, P. K. Modeling a snap-action, variable-delay switch controlling extrinsic cell death. PLoS biology. 6, 2831-2852 (2008).
- N'Diaye, E. N., et al. PLIC proteins or ubiquilins regulate autophagy-dependent cell survival during nutrient starvation. EMBO reports. 10, 173-179 (2009).
- Xu, J., Liu, Z. F., Wang, J., Deng, P., Jiang, Y. Study of localization and translocation of human high mobility group protein B1 in eukaryotic cells. Zhongguo wei zhong bing ji jiu yi xue = Chinese critical care medicine = Zhongguo weizhongbing jijiuyixue. 18, 338-341 (2006).
- Hoppe, G., Talcott, K. E., Bhattacharya, S. K., Crabb, J. W., Sears, J. E. Molecular basis for the redox control of nuclear transport of the structural chromatin protein Hmgb1. Exp Cell Res. 312, 3526-3538 (2006).
- Moshfegh, Y., Bravo-Cordero, J. J., Miskolci, V., Condeelis, J., Hodgson, L. A Trio-Rac1-Pak1 signalling axis drives invadopodia disassembly. Nat Cell Biol. 16, 574-586 (2014).
- Yu, X., Machesky, L. M. Cells assemble invadopodia-like structures and invade into matrigel in a matrix metalloprotease dependent manner in the circular invasion assay. PLoS One. 7 (e30605), (2012).
- Neumann, B., et al. Phenotypic profiling of the human genome by time-lapse microscopy reveals cell division genes. Nature. 464, 721-727 (2010).
- Burnette, D. T., et al. A role for actin arcs in the leading-edge advance of migrating cells. Nat Cell Biol. 13, 371-381 (2011).
- Matov, A., et al. Analysis of microtubule dynamic instability using a plus-end growth marker. Nat Methods. 7, 761-768 (2010).
- Wollman, R., Meyer, T. Coordinated oscillations in cortical actin and Ca2+ correlate with cycles of vesicle secretion. Nat Cell Biol. 14, 1261-1269 (2012).
- Day, R. N., Davidson, M. W. The fluorescent protein palette: tools for cellular imaging. Chemical Society reviews. 38, 2887-2921 (2009).
- Kilgore, J. A., Dolman, N. J., Davidson, M. W., et al. A review of reagents for fluorescence microscopy of cellular compartments and structures, Part II: reagents for non-vesicular organelles. Current protocols in cytometry. Robinson, J. . P. aul 66, (2013).
- Pittet, M. J., Weissleder, R. Intravital imaging. Cell. 147, 983-991 (2011).
- Shi, J., Zhou, Y., Huang, H. C., Mitchison, T. J. Navitoclax (ABT-263) accelerates apoptosis during drug-induced mitotic arrest by antagonizing Bcl-xL. Cancer Res. 71, 4518-4526 (2011).
- Tan, N., et al. Navitoclax enhances the efficacy of taxanes in non-small cell lung cancer models. Clin Cancer Res. 17, 1394-1404 (2011).
- Ramapathiran, L., et al. Single-cell imaging of the heat-shock response in colon cancer cells suggests that magnitude and length rather than time of onset determines resistance to apoptosis. J Cell Sci. 127, 609-619 (2014).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유