Method Article
LC-MS / MS를 사용하여 건조 혈액 명소에 면역 억제제 타 크롤리 무스의 정량화
요약
Here we describe a high-performance liquid chromatography-tandem mass spectrometry (HPLC-MS/MS) assay to quantify the immunosuppressant tacrolimus in dried blood spots using a simple manual protein precipitation step and online column extraction.
초록
칼시 뉴린 억제제 타 크롤리 무스는 미국에서 고체 장기 이식 후 대부분의 면역 치료 프로토콜의 초석이다. 타 크롤리 무스는 좁은 치료 지수 약물이며, 등은 치료 적 약물 모니터링 및 전체 혈액 통 농도를 기반으로 용량 조절이 필요합니다. 가정 치료 약물 및 준수 모니터링을 용이하게하기 위해, 건조 혈액 명소의 컬렉션은 매력적인 개념이다. 핑거 스틱 후, 환자는 집에서 필터 종이에 혈액 방울을 수집한다. 혈액이 건조 된 후에는 타크로리무스는 고성능 액체 크로마토 그래피 탠덤 질량 분석법을 이용하여 정량화 분석 실험실로 송부 (HPLC-MS / MS) 간단한 수동 단백질 침전 단계 및 온라인 열 추출과 조합.
타 크롤리 무스 분석을 위해, 6 mm 디스크는 혈액 스폿의 중심으로부터 펀칭 포화된다. 혈액 자리는 총알 블렌더를 사용하여 균질화ND 후 단백질은 메탄올 / 0.2 M ZnSO 4 내부 표준 D 2, C-13을 함유 타크로리무스로 침전된다. 볼 텍싱 및 원심 분리 후, 상청액 100 μL를가 온라인 추출 칼럼에 주입하고, 5 ㎖ / 0.1 포름산 / 아세토 니트릴로 세정 분 (7 : 3, V : V) 1 분. 이하, 전환 밸브가 작동하고 분석 물은 분석 컬럼에 백 플러시 (및 0.1 % 포름산 / 아세토 니트릴 구배를 사용하여 분리)된다. 타크로리무스는 탠덤 질량 분석 장치를 사용하여 다중 반응 양성 모드 (MRM)으로 정량화된다.
분석은 50 ng 내지 1 / ㎖에서 선형이다. 로 이십일에 걸쳐 평가 간 분석 변동 (3.6 % -6.1 %)과 정확성 (91.7 % -101.6 %)이 허용 기준을 충족. 평균 추출 회수는 95.5 %이다. 이월, 매트릭스 간섭 및 매트릭스 효과 아무런 관련이 없습니다. 타 크롤리 무스는 실온에서 1 주일 동안 4 ℃에서 건조 혈액 명소에서 안정적이다. 에서 추출 된 샘플오토 샘플러는 최소 72 시간 동안 4 ℃에서 안정하다.
서문
타 크롤리 무스는 마크로 라이드 구조 (8) (그림 1)이 강력한 immonosuppressant 1-7이다. 653g / L, 에탄올 : - 시스로 인한 CN 결합의 트랜스 이성질체는 역상 고성능 액체 크로마토 그래피로 분리 될 수있는 용액을 9 개의 로타 머를 형성한다 (HPLC)은 타 크롤리 무스는 알코올 (메탄올 중의 지용성 및 수용성 355 G / L), 할로겐화 탄화수소 (클로로포름 : 573g / L) 및 에테르. . 0.1 G / L 및 물 (pH를 3 : 그것은 지방족 탄화수소 (헥산에 난 용성이다. 분자가 어떤 발색단과 자외선 최대 흡수를 포함하지 않는 9 0.0047 g / L) 칼시 뉴린 억제를 통해 192 nm의 타 크롤리 무스의 역할입니다 . 그 작용 메커니즘은 참조 10,11에서 검토되었다. 현재는 미국 (12)에 고체 기관 이식 환자의 80 % 이상으로 사용된다.
타크로리무스의 치료 지수는 considere있는 것이다D 13 좁은합니다. 또한, 타 크롤리 무스 및 투여 혈중 농도 간의 상관 관계는 좋지는 14,15 및 약동학 변수이다. 이식 환자에서 타 크롤리 무스 투여를 안내하는 치료 약물 모니터링 따라서 일반적으로 임상 실습 16 ~ 20입니다. 목표는 미리 정의 된 치료 범위 내에 타크로리무스의 혈중 농도를 유지하는 것이다. 치료 창 이상의 농도가 과다 면역, 암 등의 신 독성, 신경 독성, 고혈압, 당뇨병 등의 독성에 대한 위험이 증가하는 동안 치료 적 범위보다 타크로리무스 혈중 농도는 만성 또는 급성 동종 면역 반응의 활성이 증가 될 수 있습니다. 타 크롤리 무스의 높은 약동학 내 개인 변동성 이식 기관과 환자 생존율 (21, 22) 모두에 해가 될 수있다. 타 크롤리 무스의 약동학의 간 개별 변동은 주로 CYP3A5 다형성, 내 개인에 대한 이유에 의해 발생되는 동안변동성이 포함되지만, 약물 - 약물, 질병 - 약물 및 식품 - 약물 상호 작용 14, 15에 한정되는 것은 아니다. 또한 면역 억제 치료 약물 처방을 준수의 부족은 요인 및 이식 손실 (23, 24)에 대한 주요 이유입니다.
이러한 고려 사항은 빈번한 홈 치료약 및 타크로리무스 전혈 농도 부착 모니터링 환자가 항상 원하는 치료 창 내 타크로리무스 노출을 가질 수 있도록하는 것이 유익 할 수 있음을 시사한다. 그러나, 현재의 임상 15 금지 인 물류 및 더 빈번한 모니터링 치료약의 비용 때문이다. 그 이유 중 하나는 환자 phlebotomist 그린 필요한 정맥 혈액 샘플을 가지고 참조한다는 것이다. 말린 혈액 반점은 최근에 매력적인 개념 25-28로 등장했다. 환자 스틱 간단한 손가락 한 것은 특수 필터 종이 카드 및 혈액 자리가 거라고 한 후 혈액 방울을 수집리 에드, 그것은 타 크롤리 무스의 분석과 환자가 현재 복용 될 수 있음을 다른 면역 억제제를위한 중앙 실험실로 발송 될 수있다. 이는 건조 혈액 명소 (혈액의 일반적으로 20 μL) 25,29-43로 인해 아주 작은 혈액 볼륨에서 타 크롤리 무스와 다른 면역 억제제의 정량에 매우 민감하고 특정 LC-MS는 / MS 분석의 개발이 가능하게되었다. 또 다른 장점은 건조 혈액 명소로 최소 침습, 낮은 볼륨 시료 채취 전략은 크게 어린이 (28)의 치료 적 약물 모니터링 및 약동학 적 연구를 촉진한다는 것이다.
타 크롤리 무스는 일반적으로 정맥 EDTA 전혈 (15)로 측정됩니다. 이유는 타 크롤리 무스가 광범위하게 혈액 세포로 배포하는 것이 임상 연구는 임상 이벤트 15,18 플라즈마에 비해 혈중 타 크롤리 무스 통 농도 사이 좋은 상관 관계를보고했다고한다. 비교하여, TA의 분석건조 혈액 반점에서 crolimus은 여과지 매트릭스와 혼합 모세관 혈액에 기초한다. 이것은 LC-MS / MS 분석으로 타크로리무스 및 잠재적 간섭의 가용화면에서 과제를 제시한다. 여기에서 우리는 높은 흐름 온라인 열 샘플 정리 절차 및 LC-MS / MS 분석과 함께 총알 블렌더를 사용하여 건조 혈액 자리의 균질화를 기반으로 설립 검증 분석을 제시한다. 오늘날,이 분석은 임상 시험을 성공적으로 부착 모니터링 이상의 오천 타크로리무스 건조 혈액 샘플의 스폿 정량화에 사용되었다.
프로토콜
건강한 사람에서 드 확인 된 혈액 샘플은 콜로라도 병원의 대학 (오로라, 콜로라도)에서 있었다. 유효성 연구뿐만 아니라, 구경 및 품질 대조 시료의 제조 디 식별 혈액 은행 샘플의 사용은 콜로라도 멀티위원회 (Institutional Review Board COMIRB, 오로라, 콜로라도)에서 "제외"으로 간주 하였다.
참고 문헌 및 솔루션 1. 준비
- 구매 타 크롤리 무스와 내부 표준 D 2, 재료 목록에 나열된 공급 업체의 13 C-타 크롤리 무스.
- 타크로리무스 1 ㎎ / ㎖의 농도 및 D (2) 10 ㎍ / ㎖, 13 C-타크로리무스의 농도로 순수 메탄올 중의 스톡 용액을 준비한다. 3 개의 독립적 인 가중치를 기반으로 표준 물질의 재고 솔루션을합니다. 나누어지는 재고 솔루션 및 저장 -70 ° C에서 이하.
- 단백질을 침전 솔루션을 준비합니다(: 3 V : 7 V) 물에 메탄올 / 0.2 M ZnSO 4를 사용하여 타 크롤리 무스의 압축을 풉니 다. 이 용액은 또한 내부 표준 D 2, 2.5 NG / ㎖의 농도에서 13 C-타크로리무스를 포함하고 빈 샘플의 추출을 제외한 모든 샘플 (1.3.3 참조)의 추출에 사용된다.
- 각 추출 날에 갓이 단백질 침전 솔루션을 준비하고 12 시간에서 솔루션의 만료를 설정합니다.
- 교정 곡선 및 품질 관리 (QC) 샘플의 제조
- 순수한 메탄올 원액 적절한 희석액을 행하여 타크로리무스의 스톡 용액을 준비한다.
- 교정기 및 품질 관리 샘플을 제조 EDTA 전혈로 적절히 희석 스톡 용액 20 μl를 스파이크, 20 분 및 분취위한 셀룰러 혈액 성분에 타크로리무스의 균일 분포를 허용하도록 수욕 진탕 부드러운하에 37 ℃에서 배양 1.5 ml의 용종에원뿔 바닥 ropylene 튜브 및 스냅인에 뚜껑. 유기 용매의 상대적 양이 5 %를 초과하지 않도록하십시오.
- 스팟 피펫을 사용하여 필터 카드에 각 원의 중앙으로 아군 전체 혈액의 50 μL.
- 3 시간 동안 실온에서 필터 카드에 혈액 반점을 건조.
- 1, 2.5, 5, 10, 25, 50 NG / ㎖의 농도에서 타크로리무스 EDTA 인간 전혈에 타크로리무스 검정 표준을 준비한다. 내부 표준 D 2, 13 C-타 크롤리 무스 ( "제로 샘플")을 포함하는 단백질 침전 용액으로 교정 표준 등의 추출을위한 빈 샘플을 준비합니다.
- 0, 2, 4, 20, 40 NG / ㎖의 농도로 EDTA 인간 전혈에서 QC 샘플을 준비한다. 빈 샘플을 준비합니다. 내부 표준 D 2를 함유하는 침전으로 추출 QC 샘플들과 대조적으로, C-13 타크로리무스, 않는 단백질 침전 용액이 빈 샘플을 추출내부 표준 D 2, 13 C-타 크롤리 무스 ( "빈 샘플을")가 포함되어 있지.
- 임상 샘플 컬렉션
- 43, 44에 기술 된 바와 같이 건조 혈액 명소를 수집합니다.
2. 타 크롤리 무스의 추출 건조 혈액 스팟 샘플
- 시각적으로 허용되는 샘플의 품질과 양 (45)을 보장하기 위해 건조 혈액 자리를 검사합니다.
- 6 mm의 구멍 펀치 필터 카드의 혈액 자리의 펀치 센터.
주 : 펀치의 품질은 계량에 의해 모니터링 될 수있다. 천공 포화 필터 디스크는 0.09 mg의 (: 4.83- 5.14 ㎎, N = 12 범위) ± 평균 5.02 밀리그램에 무게. - 원뿔 바닥 스냅인에 뚜껑 1.5 ml의 폴리 프로필렌 튜브에 장소 디스크.
- 각각의 튜브에 20 ~ 30 글 머리 기호를 추가합니다.
- 각각의 튜브에 (2.5 NG / ㎖의 내부 표준 V : 0.2 M ZnSO 4, 7 : 3, V 메탄올) 단백질 침전 용액 500 μl를 추가합니다. EXTR 들어빈 샘플의 동작은, 내부 표준없이 단백질 침전 솔루션을 사용합니다.
- ( "10"을 설정, 최대 속도) 1 분 동안 총알 블렌더에 디스크를 균질화.
- 10 분 동안 ( "10"을 설정, 최대 속도) 멀티 튜브의 소용돌이에 실온에서 샘플을 흔들어.
- 원심 분리기 샘플 16,000 XG, 10 분 동안 4 ° C에서.
- 300 μL 삽입 장착 유리 HPLC 바이알에 상층 액을 전송합니다. 미리 슬릿 테플론 씰을 사용합니다.
주 : 추출 된 샘플은 -20 ° C 이하에서 LC-MS / MS 분석 때까지 저장 될 수있다.
3. LC-MS / MS 분석
- 부하 (100) C8 카트리지 추출 컬럼으로 추출 된 샘플의 상등액 μL 및 7로 세척한다 : 물 중 0.1 % 포름산 : 3 비율을 5 ml의 아세토 니트릴 흐름 / 분으로 1 분 동안. 전환 밸브의 연결은도 2에 도시되고 구배 표 1 추출 펌프에 의해 실행 룽.
- 이하는 분석 컬럼에 미리 열에서 분석의 백 플러시의 결과로 전환 밸브를 활성화합니다.
- 65 ° C의 열 온도를 설정합니다.
- 표 1에 나타낸 유량과 구배를 사용하여 분석 컬럼에서 분석 물을 용리.
- 터보 전기 분무 이온화 소스를 통해 탠덤 질량 분석기로 분석 컬럼을 연결합니다. 표 2에있어서 질량 분석의 주요 파라미터를 조정한다.
- 여러 반응 모드 (MRM)의 양이온 ([M + 나] +)를 검출한다. 정량을 위해 다음과 같은 이온 전환을 사용하여 타 크롤리 무스 : M / Z (질량 / 충전) = 826.6를 616.2와 D 2, 13 C-타 크롤리 무스 → : M / Z = 619.2 → 829.6을.
참고 : 전체 실행 시간은 4.6 분입니다.
4. 정량
- 각 실행에 대해, 1.3.5 및 제조 교정기에 기초 검량선을 생성각각의 분석 실행에 포함.
- 질량 분석 소프트웨어를 사용하여 (피크 면적 [분석 대상 물질] / 피크 면적 [내부 표준]) 검체의 응답 인자 대 공칭 농도를 플로팅함으로써 교정 곡선을 생성한다.
- 1 / X 가중치와 함께 차 착용감을 사용하여 교정기를 장착한다.
- 건조 된 혈액 관광 명소 수량 타 크롤리 무스에 추출 된 MRM 크로마토 그램에서 타 크롤리 무스와 내부 표준 물질 피크를 통합 할 수 있습니다. 타 크롤리 무스에 대한 응답 인자 (피크 면적 [분석 대상 물질] / 피크 면적 [내부 표준)를 계산하고 질량 분석 소프트웨어를 사용하여 검량선과 비교한다.
5. 검증 절차
- 검출 (LLOD)의 하한과 정량 (LLOQ)의 하한.
- 검출부 (LLOD)의 하한으로서 1 : 4의 피크 - 대 - 잡음비와 낮은 타크로리무스 농도를 고려한다. 로서 정량화 (LLOQ)의 하한을 정의동일하거나 공칭 농도와 같거나 더 나은 20 %의 정밀도 (변동 계수)에서 ± 20 %의 편차를보다 나은 정확성으로 검량선의 최저 농도.
- 인트라 간 하루의 정확도 및 정밀도.
- 2 겨 / ㎖ (QC1), 4 겨 / ㎖ (QC2), 20 ng를 / ㎖ (QC3) 40 겨 / ㎖ (QC4)의 네 가지 농도 수준의 정확도와 정밀도를 테스트합니다.
- 인간의 EDTA 전체 혈액의 각 검증 하루에 품질 관리 샘플을 준비 필터 카드, 추출물 건조, 전술 한 바와 같이 분석한다.
- 품질 관리 농도 레벨 당 6 샘플 내 하루의 정확성과 정밀도를 결정합니다.
- 이십일 동안 간 일의 정확도와 정밀도를 평가합니다. 4 샘플을 매일 각각의 품질 관리 수준을 측정한다.
- 각각의 날에 품질 관리 샘플과 함께 두 교정 곡선을 분석합니다.
- 공칭 농도 % (농도에 6 샘플, 5.2.2 참조)로 내 하루 정확도를 계산합니다. 석회질변동 (CV %)의 계수로서 ulate 정밀도.
- 수용은 공칭 농도의 85 % 115 % 제한으로가 떨어지면 안 일 정밀도가 허용 고려한다. 그것은 15 % CV (변동 계수)과 같거나 더 나은 상 허용되는 경우 인트라 일 정밀도를 고려한다.
- 20 검증 일 동안 분석 각각의 품질 관리 농도에 대한 평균으로 간 하루 정확도와 정밀도를 계산합니다.
- 수용은 공칭 농도의 85 % 115 % 제한으로이 떨어지는 경우 평균 간 하루 정도는 허용 고려한다. 그것은 15 % CV (변동 계수)과 같거나 더 나은 상 허용되는 경우 일 간 정밀도를 고려한다.
- 매트릭스 간섭의 배제.
- 매트릭스 신호에 의해 발생할 수 있습니다 간섭의 배제를 들어, 빈 건조 혈액 명소 (8 다른 개인, 바람직하게는 4 명의 남성과 4 명의 여성)을 분석 할 수 있습니다.
- 시각적으로 이온 크로마토 그램을 검사합니다. 만약 고정 된 시간 내에 피크타 크롤리 무스의 창은 LLOQ에서 타 크롤리 무스와 스파이크 통합하고 빈 샘플 타 크롤리 무스 피크의 사람들과 곡선에서 자신의 영역을 비교, 검색됩니다. 빈 샘플 피크의 면적은 LLOQ에서 타 크롤리 무스의 사람들의 15 %를 초과 할 것으로 예상되지 않습니다.
- 이온 억제 / 이온 향상.
- 동시 용출 매트릭스 성분에 의한 이온 진압 / 이온 향상의 잠재적 인 간섭을 평가하기 위해 45 바와 같이 포스트 칼럼 주입 프로토콜을 사용한다.
- 0.1 % 포름산 10 ㎍ / ml의 농도에서 타크로리무스 달이다 : 메탄올 (30:70, v / v)로 포스트 - 컬럼을 10 μL / 분의 속도.
- 분석 컬럼과 질량 분석기의 전기 분무 소스 간 T 피스를 통해 시린지 펌프를 연결한다.
- 타 크롤리 무스에 대한 MRM 전이 MS / MS 데이터 신호 강도를 모니터링하고 내부 표준 (m / z = 616.2 및 m / z = 829.6 → 619.2 → 826.6)의 주입 후 extrac테드 빈 샘플 (N = 다른 개인 8 샘플).
주 : 이온 억제 신호 및 이온 인핸스 피크 딥이 발생하는 동안, 이온 억압 / 이온 충실한없는 분석 물 주입에 의한 연속 신호는, 빈 매트릭스 주사에 의해 영향을받지 않을 것이다.
- 이월.
- 가장 높은 구경 후 빈 샘플을 추출 분석하여 잠재적 인 캐리 오버 평가 (50 NG / ㎖, N = 6).
- 시각적으로 이온 크로마토 그램을 검사합니다. 타 크롤리 무스의 체류 시간 윈도우 내의 피크가 검출되는 경우에 타크로리무스 LLOQ 타서 통합 및 빈 샘플 타크로리무스 피크들과 그 곡선 아래 영역을 비교한다. 빈 샘플 피크의 면적은 LLOQ에서 타 크롤리 무스의 사람들의 15 %를 초과 할 것으로 예상되지 않습니다.
- 추출 회복.
- QC SAM 추출한 후 분석 물 신호를 비교하여 회수율을 결정PLES 빈 건조 혈액 명소들과 네 가지 농도 수준 (N = 농도 당 6)에서 추출 후 타 크롤리 무스의 상응하는 양의 스파이크.
- QCS의 4 세트 (2, 4, 20, 40 NG / ㎖ 농도 수준)을 준비한다.
- 필터 종이 카드에 빈 EDTA 전체 혈액의 50 μl를 파악하고, 2 시간 동안 건조하여 "복구 테스트 샘플을"대응의 또 다른 4 세트를 준비합니다.
- 이하, 품질 관리 및 빈 "복구 테스트 샘플"모두, 가위로 필터 카드의 전체 혈액의 자리를 잘라 원뿔 바닥과 스냅인에 뚜껑 폴리 프로필렌 튜브에 생성 된 디스크를 넣습니다.
- 모든 샘플을 추출합니다.
- 유리 HPLC 바이알에 상층 액 (400 μL)를 전송합니다.
- 2, 4, 20, 40 ng를 / ㎖ (200, 400, 2,000, 4,000 NG / ㎖ 타크로리무스 스톡 졸 4 μL의 농도에 도달하는 빈 "추출 회수 시험 샘플"에 타크로리무스 스톡 용액을 첨가상층 액 400 μL)에 용액 사용.
- LC-MS / MS 분석 한 결과, QC 샘플 및 해당 농도의 "회복 시험 샘플"모두에서 신호를 비교 (추출 / 신호 샘플이 추출 × 100 이후 아군 전에 회수 (%) = 신호 샘플은 아군).
- 희석의 무결성.
- 희석하여 무결성을 확립 시료 500, 250, 100ng의 / ㎖에서 분석 대상으로 스파이크.
- 추출 후, 단백질 침전 용액을 사용하여 시료 희석 (1:10, N = 3 농도 수준 당).
- 공칭 농도의 편차를 계산합니다. 85 % 내에서 공칭 허용의 -115 % 하락할 결과를 고려한다.
- 안정성.
- 네 농도 수준 (N = 농도에 따라 4) 다른 시간 지점에서와 다른 저장 조건에서 분석의 품질 관리 샘플을 사용하여 안정성을 조사합니다.
- 공칭 값을 저장 한 후 결과를 비교한다. R을 고려85 % 내에서 공칭 허용의 -115 % 하락 esults.
- 4 ° C, -20 ° C에서 1개월 및 -80 ° C에서 1 개월 일주, 상온에서 1 주일 동안 샘플의 안정성을 설정합니다.
- 3주기를 통해 테스트 동결 - 해동 안정성 (-20 ° C). 4 ℃로 조정 된 항온 자동 시료 주입기로 샘플을 배치하여 테스트 추출 된 샘플 및 오토 샘플러 안정성. 72 시간 후 샘플을 주입한다.
결과
블랭크 샘플의 대표적인 이온 크로마토 그램은, 샘플은도 3에 도시되어 정량화 및 환자 샘플의 하한에서 아군.
교정 곡선
검출 하한은 0.5 ml의 NG /이었고, 정량 하한은 1.0 ng를 / ㎖이었다. 높은 농도가 정상적인 상황에서 병원에 도달 할 가능성이 있습니다로 쉰 NG는 / ml로 가장 높은 교정기로 선정되었다.
교정 곡선은 갓, 인간의 EDTA 전체 혈액의 각 검증 하루에 준비 필터 카드에 건조하고 추출 된 메탄올 / 0.2 M ZnSO 4 (70:30 V / V) + 내부 표준 (내부 표준의 최종 농도 : 2.5 NG / ㎖ ). 1 일 유효성 검사를 위해 (N = 6 품질 관리 수준에 대한 교정기 및 n = 6)과 일 2 - (각 품질 관리 수준에 대한 N = 2 교정기 및 N = 4) (20) 농도 1, 2.5, 5 분석 하였다, CALIB 10, 25, 50 ng를 / ㎖쉼. 전형적인 검량선을도 4에 도시된다. 공칭 115 %로 85 %의 평균 정확도 (6 비제 교정기의 최소) 교정기의 2/3에 대한 작동 범위 내에서 수용 가능한 것으로 간주되었다. 상관의 평균 계수 (R) = 0.999 (N = 40 교정 곡선)이었다.
정확도와 정밀도
결과를 표 3에 상세히 도시되어있다.
추출 복구
평균 추출 회수율 (2 NG / ㎖), 92.2 (4 NG / ㎖), 95.5 (20 NG / ㎖), 96.2 (40 NG / mL)을 98.2 %였다.
매트릭스 간섭, 이온 억제 / 이온 향상 테스트를 사용하여 연속 포스트 열 주입 및 이월
에 대응하는 8 개의 다른 개인들 (N = 4, N = 여성 및 남성 4) 보유 시간에서 보여 신호 LLOQ (1 NG / ㎖)의 15 % 미만에서 빈 샘플 분석검출 된 타 크롤리 무스 피크 특정 고려 될 수 있음을 나타내는 타 크롤리 무스 피크. 대표적인 예는도 3에 도시되어있다. 이온 진압 / 이온 강화하여 잠재적 인 간섭은 8 개의 다른 건강한 사람에서 빈 건조 혈액 시료를 사용하여 시험 하였다. 대표적인 실험을도 5에 도시되어있다. 현저한 억제 이온 / 이온 향상의 어떠한 징후가 관찰되지 않았다. LLOQ에서 신호의 15 %를 초과하는 피크의 결과로 어떤 관련 이월은 검출되지 않았다.
희석 무결성
희석 무결성의 목표 농도에 도달하는 최고 교정기 (100, 250, 500 NG / ㎖) 이상의 농도로 제조하고, 추출 후 단백질 침전 용액 1:10 희석 된 시료를 분석하여 조사 하였다 : 10, 25, 50 NG / ml의. 정확도는 평균 공칭 농도의 115 %로 85 %의 수용 기준 내에 있도록했다. 모든 희석의 TES테드는 허용 기준 (표 4)를 만났다.
안정성
건조 혈액 명소에서 타 크롤리 무스의 안정성은 다양한 조건에서 저장된 모든 4 단계 (N = 4 / 농도)에서 품질 관리 시료를 분석하여 조사 하였다.
정확도는 평균 공칭 농도의 115 %로 85 %의 수용 기준 내에 있도록했다. 결과를 표 5에 상세히 도시되어있다. 3 동결 및 해동 사이클 후 -80 ℃에서 저장 1 개월 후 -20 ℃에서 저장 1 개월 후 4 ℃에서 저장 일주 후 실온에서 저장 일주 후 아니 손실,,,,,과 4 ° C에서 자동 샘플러에서 추출 된 샘플의 72 시간 후 분명했다.
| 추출 펌프 | 분석 (용출) 펌프 | ||||||
| 시간 [분] | 물 + 0.1 % 포름산 | 아세토 니트릴 | 유량 [μL / 분] | 시간 [분] | 물 + 0.1 % 포름산 | 아세토 니트릴 | 유량 [μL / 분] |
| 0 | (70) | (30) | 5,000 | 0 | (13) | 87 | 1,000 |
| 1 | (70) | (30) | 5,000 | (2) | (2) | (98) | 1,200 |
| 1.1 | (2) | (98) | (100) | 3.5 | (2) | (98) | 1,200 |
| 3 | (2) | (98) | (100) | 3.6 | (13) | 87 | 1,000 |
| 3.1 | (20) | (80) | 2,000 | 4.6 | (13) | 87 | 1,000 |
| 4 | (70) | (30) | 5,000 | ||||
| 4.6 | (70) | (30) | 5,000 | ||||
추출 표 1. 그라데이션 프로그램 및 분석 HPLC 펌프.
| 매개 변수 | 환경 |
| 충돌 가스 (CAD) | (10) |
| 커튼 가스 (현재) (PSI) | (30) |
| 이온 소스 가스 1 (GS1) (PSI) | (50) |
| 이온 소스 가스 미터 (GS2) (PSI) | (30) |
| 네뷸 라이저 전류 (NC) (V) | 1 |
| 온도 (TEM) (° C) | (600) |
| IonSpray 전압 (IS) (V) | 5500 |
| 인터페이스 히터 (IHE) | 에 |
| 디 클러스터링 전위 (DP) (V) | (136) |
| 입학 전위 (EP) (V) | (10) |
| 충돌 에너지 (CE) (V) | 47 |
| 충돌 셀 출구 전위 (CXP) (V) | (16) |
표 2. 터보 전자 분무 인터페이스 및 질량 분석기 매개 변수. 명명법은 질량 분석 소프트웨어에서 사용에 해당한다 (제조 업체 자세한 내용은, 재료 목록을 참조하십시오).
| 검증의 날 | 품질 관리 수준 [농도와의 %] | |||
| (2) | 4 | (20) | (40) | |
| 1 일 | 93.0 | 86.3 | 88.9 | 93.4 |
| (101) | 90.4 | 95.3 | (100) | |
| 85.6 | 95.9 | 99.0 | 97.5 | |
| 88.6 | 93.6 | (105) | (103) | |
| 85.0 | 97.4 | 97.2 | (109) | |
| 89.1 | 96.7 | (100) | (101) | |
| 안 일 정도 [%] | 90.4 | 93.4 | 97.6 | 100.7 |
| 안 일 부정확 [이력서 %] | 6.6 | 4.6 | 5.5 | 5.2 |
| 2 일 | 92.8 | 86.0 | (103) | 95.4 |
| 91.1 | 88.8 | 94.7 | 87.0 | |
| 88.6 | 90.9 | 92.8 | 94.2 | |
| 97.2 | 93.7 | 94.2 | (115) | |
| 안 일 정도 [%] | 92.4 | 89.9 | 96.2 | 97.9 |
| 안 일 부정확 [이력서 %] | 3.9 | 3.6 | 4.8 | 12.2 |
| 3 일 | 97.6 | (101) | 98.4 | (112) |
| (104) | 85.6 | (102) | (110) | |
| 99.2 | 88.4 | 99.4 | (105) | |
| 96.3 | 87.2 | (108) | 117 | |
| 안 일 정도 [%] | 99.3 | 90.6 | 102.0 | 111.0 |
| 안 일 부정확 [이력서 %] | 3.4 | 7.8 | 4.2 | 4.5 |
| 4 일 | 95.2 | 88.6 | (112) | 94.5 |
| (105) | 87.3 | 93.2 | (116) | |
| 99.8 | 96.2 | (103) | (103) | |
| (100) | (104) | 97.2 | 99.4 | |
| 안 일 정도 [%] | 100.0 | 94.0 | 101.4 | 103.2 |
| 안 일 부정확 [이력서 %] | 4.0 | 8.2 | 8.1 | 8.9 |
| 5 일 | (106) | 90.4 | (101) | (106) |
| (108) | 89.0 | (106) | (100) | |
| (102) | (101) | 96.6 | (128) | |
| (105) | 88.8 | (105) | (107) | |
| 안 일 정도 [%] | 105.3 | 92.3 | 102.2 | 110.3 |
| 안 일 부정확 [이력서 %] | 2.4 | 6.3 | 4.2 | 11.1 |
| 6 일 | 90.9 | 93.7 | 119 | (106) |
| 98.8 | 88.1 | 96.4 | (110) | |
| 94.6 | 96.3 | 99.1 | (108) | |
| (108) | (100) | (102) | (102) | |
| 안 일 정도 [%] | 98.1 | 94.5 | 104.1 | 106.5 |
| 안 일 부정확 [이력서 %] | 7.5 | 5.3 | 9.8 | 3.2 |
| 7 일 | 85.1 | 87.5 | 99.5 | 95.4 |
| 86.4 | 85.4 | 94.7 | (101) | |
| 94.5 | 87.3 | 98.9 | 94.6 | |
| 85.5 | 97.0 | (101) | 99.6 | |
| 안 일 정도 [%] | 87.9 | 89.3 | 98.5 | 97.7 |
| 안 일 부정확 [이력서 %] | 5.1 | 5.8 | 2.7 | 3.2 |
| 8 일 | 86.1 | 92.5 | 91.9 | (102) |
| 87.5 | 91.5 | 95.2 | 88.5 | |
| (115) | 85.6 | 92.1 | (102) | |
| 85.8 | 85.9 | 95.4 | (108) | |
| 안 일 정도 [%] | 93.6 | 88.9 | 93.7 | 100.1 |
| 안 일 부정확 [이력서 %] | 15.3 | 4.1 | 2.0 | 8.2 |
| 9 일 | 88.9 | 91.4 | 96.9 | (100) |
| 90.0 | 89.8 | 95.0 | (100) | |
| 69.7 | 85.9 | 95.8 | (109) | |
| 91.9 | 87.0 | (105) | (101) | |
| 안 일 정도 [%] | 85.1 | 88.5 | 98.2 | 102.5 |
| 안 일 부정확 [이력서 %] | 12.2 | 2.9 | 4.7 | 4.3 |
| 10 일째 | 90.9 | 91.3 | 96.2 | (100) |
| 97.7 | 89.5 | 94.4 | (100) | |
| 99.9 | (109) | 98.7 | 96.8 | |
| 99.1 | 90.0 | 95.7 | 96.1 | |
| 안 일 정도 [%] | 96.9 | 95.0 | 96.3 | 98.2 |
| 안 일 부정확 [이력서 %] | 4.2 | 9.9 | 1.9 | 2.1 |
| 날 11 | 92.7 | 91.9 | 88.2 | (104) |
| 96.6 | 91.2 | 97.0 | (110) | |
| 109.0 | 92.8 | (97).6 | (102) | |
| 98.3 | (107) | 93.7 | (111) | |
| 안 일 정도 [%] | 99.2 | 95.7 | 94.1 | 106.8 |
| 안 일 부정확 [이력서 %] | 7.0 | 7.9 | 4.6 | 4.1 |
| 날 12 | 87.7 | 85.5 | (105) | 95.3 |
| (112) | 88.1 | (101) | 96.1 | |
| (102) | 89.1 | 89.7 | 97.5 | |
| (106) | 92.5 | (102) | (104) | |
| 안 일 정도 [%] | 101.9 | 88.8 | 99.4 | 98.2 |
| 안 일 부정확 [이력서 %] | 10.1 | 3.3 | 6.7 | 4.0 |
| 날 13 | 실패한 | 85.7 | 93.3 | (102) |
| (101) | (105) | 88.0 | 93.9 | |
| (112) | 98.0 | 91.4 | (102) | |
| (104) | (113) | (104) | (101) | |
| 안 일 정도 [%] | 105.7 | 100.4 | 94.2 | 99.7 |
| 안 일 부정확 [이력서 %] | 5.4 | 11.5 | 7.3 | 3.9 |
| 주 (14) | 91.5 | 89.1 | 97.4 | 93.1 |
| 90.4 | 87.1 | 93.9 | 99.8 | |
| 89.7 | 97.0 | 94.8 | (106) | |
| 97.4 | 86.8 | 89.9 | 실패한 | |
| 안 일 정도 [%] | 92.3 | 90.0 | 94.0 | 99.6 |
| 안 일 부정확 [이력서 %] | 3.8 | 5.3 | 3.3 | 6.5 |
| 날 15 | 92.8 | 92.8 | 92.5 | 95.4 |
| 97.5 | 96.3 | 96.2 | 95.5 | |
| 95.5 | (108) | 97.3 | 99.3 | |
| (110) | (109) | (115) | (113) | |
| 안 일 정도 [%] | 99.0 | 101.5 | 100.3 | 100.8 |
| 안 일 부정확 [이력서 %] | 7.7 | 8.1 | 10.0 | 8.3 |
| 16 일 | 93.7 | 97.8 | 90.7 | (112) |
| 90.3 | 87.1 | 실패한 | (101) | |
| 97.9 | 88.3 | 95.5 | (107) | |
| 91.4 | 85.7 | 89.3 | 96.7 | |
| 안 일 정도 [%] | 93.3 | 89.7 | 91.8 | 104.2 |
| 안 일 부정확 [이력서 %] | 3.6 | 6.1 | 3.5 | 6.4 |
| 날 17 | 88.0 | 86.0 | 93.7 | (103) |
| 89.8 | 90.8 | 94.8 | 93.2 | |
| 85.9 | 91.1 | 99.7 | 94.8 | |
| 86.7 | 88.1 | 95.6 | 91.7 | |
| 안 일 정도 [%] | 87.6 | 89.0 | 96.0 | 95.7 |
| 안 일 부정확 [이력서 %] | 1.9 | 2.7 | 2.7 | 5.3 |
| 날 18 | 89.6 | 85.8 | 91.0 | 98.3 |
| 89.6 | 86.2 | 88.3 | 93.6 | |
| 실패한 | 86.7 | 96.8 | (104) | |
| 88.1 | 85.8 | 95.2 | (111) | |
| 안 일 정도 [%] | 89.1 | 86.1 | 92.8 | 101.7 |
| 안 일 부정확 [이력서 %] | 1.0 | 0.5 | 4.2 | 7.4 |
| 날 19 | 98.0 | 89.7 | 94.2 | (102) |
| 88.3 | 86.0 | 97.6 | (102) | |
| 91.6 | 88.1 | 95.8 | 97.5 | |
| 90.7 | 90.1 | 92.8 | 88.3 | |
| 안 일 정도 [%] | 92.2 | 88.5 | 95.1 | 97.5 |
| 안 일 부정확 [이력서 %] | 4.5 | 2.1 | 2.2 | 6.6 |
| 날 20 | 93.0 | 87.0 | 99.4 | (101) |
| 97.3 | 87.6 | 95.5 | 91.9 | |
| 89.0 | 88.4 | 91.2 | 93.5 | |
| (104) | 90.7 | 97.7 | (115) | |
| 안 일 정도[%] | 95.8 | 88.4 | 96.0 | 100.4 |
| 안 일 부정확 [이력서 %] | 6.7 | 1.8 | 3.7 | 10.5 |
간 날의 정확성과 부정확성 | ||||
| 간 하루 정확도 | 95.2 | 91.7 | 97.2 | 101.6 |
| 인터 일 부정확 | 6.1 | 4.5 | 3.6 | 4.2 |
표는 품질 관리 샘플 3. 결과를 통해 20 일. 데이터는 공칭 %로 제시됩니다. "실패"로 표시 샘플을 실험실 / 장비 오류로 손실 된 샘플입니다. 대부분의 CA에서ES, 더 피크가 전혀 검출되지 않았거나 내부 표준 물질 피크가 누락되었습니다.
| 희석 | 1시 10분 |
| 희석 후 공칭 목표 농도 | 50 ng를 / ㎖ |
| 98.6 | |
| 94.5 | |
| 91.4 | |
| 정확도 [%] | 94.8 |
| 부정확 [이력서 %] | 3.6 |
| 희석 | 1시 10분 |
| 희석 후 공칭 목표 농도 | 10 ng를 / ㎖ |
| (103) | |
| 99.5 | |
| (101) | |
| 정확도 [%] | 101.2 |
| 부정확 [이력서 %] | 1.8 |
| 희석 | 1시 10분 |
| 희석 후 공칭 목표 농도 | 25 ng를 / ㎖ |
| 91.7 | |
| 98.2 | |
| (103) | |
| 정확도 [%] | 97.6 |
| 부정확 [이력서 %] | 5.7 |
희석 무결성 테스트. 데이터 표 4. 결과 명목의 %로 제시됩니다.
| 실온에서 안정성, 1 일 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| 91.9 | 85.8 | 86.0 | (102) | |
| 86.7 | 85.7 | 88.5 | (102) | |
| 86.0 | 85.9 | 90.1 | (103) | |
| 89.2 | 98.0 | 90.8 | (112) | |
| 공칭 농도 % | 88.5 | 88.9 | 88.9 | 104.8 |
| 부정확 [%의 CV] | 2.7 | 6.1 | 2.1 | 4.9 |
| 실온에서 안정성, 3 일 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| 88.6 | (105) | (101) | (113) | |
| 94.1 | (100) | 98.5 | (103) | |
| (100) | (101) | (106) | (109) | |
| 99.5 | (102) | (102) | (108) | |
| 공칭 농도 % | 95.6 | 102.0 | 101.9 | 108.3 |
| 부정확 [%의 CV] | 5.3 | 2.2 | 3.1 | 4.1 |
| 실온에서 안정성, 7 일 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| (105) | (103) | 91.7 | (109) | |
| (101) | (107) | (100) | (110) | |
| (102) | (108) | (107) | (105) | |
| 93.8 | (105) | (109) | (111) | |
| 공칭 농도 % | 100.5 | 105.8 | 101.9 | 108.8 |
| 부정확 [%의 CV] | 4.7 | 2.2 | 7.8 | 2.6 |
| (B) | ||||
| 4 ° C를 1 일에서 안정성 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| (101) | 89.9 | 95.8 | (100) | |
| 88.9 | 91.0 | 94.1 | 99.0 | |
| 96.2 | (100) | (102) | 96.7 | |
| 89.5 | 87.8 | 95.4 | 88.6 | |
| 공칭 농도 % | 93.9 | 92.2 | 96.8 | 96.1 |
| 부정확 [%의 CV] | 5.8 | 5.4 | 3.5 | 5.2 |
| 4 ° C를 3 일에서 안정성 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| 87.3 | 85.2 | (105) | 95.3 | |
| 실패한 | 87.8 | (101) | (96) | |
| (101) | 88.8 | 89.6 | 97.5 | |
| (106) | 92.2 | (102) | (104) | |
| 공칭 농도 % | 98.1 | 88.5 | 99.4 | 98.2 |
| 부정확 [%의 CV] | 9.7 | 2.9 | 6.8 | 4.0 |
| 4 ° C를 7 일에서 안정성 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| 94.0 | 98.5 | 96.1 | (110) | |
| 92.9 | 96.4 | (109) | (109) | |
| 91.7 | 96.3 | 97.9 | (115) | |
| 94.7 | 96.9 | 99.8 | (113) | |
| 공칭 농도 % | 93.3 | 97.0 | 100.7 | 111.8 |
| 부정확[%이력서] | 1.3 | 1.0 | 5.7 | 2.8 |
| C | ||||
| -20 ° C, 3 일에서 안정성 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| 87.3 | 98.7 | (111) | (111) | |
| 93.5 | 89.6 | (108) | (105) | |
| 89.5 | 91.5 | (107) | (112) | |
| 88.2 | 99.1 | (108) | 92.4 | |
| 공칭 농도 % | 89.6 | 94.7 | 108.5 | 105.1 |
| 부정확 [%의 CV] | 2.7 | 4.9 | 1.7 | 9.0 |
| -20 ℃, 7 일에서 안정성 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| 96.5 | 98.7 | (102) | (109) | |
| 94.8 | 94.6 | (114) | (106) | |
| 95.5 | (102) | 98.1 | (108) | |
| (107) | 99.5 | (115) | (105) | |
| 공칭 농도 % | 98.5 | 98.7 | 107.3 | (107) |
| 부정확 [%의 CV] | 5.7 | 3.1 | 8.5 | 1.8 |
| -20 ℃, 일 30시 안정성 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| 82.3 | 83.1 | 90.4 | 93.2 | |
| 87.9 | 85.8 | 85.3 | 97.9 | |
| 85.7 | 88.6 | 98.3 | 98.0 | |
| 92.0 | 95.6 | (110) | (103) | |
| 공칭 농도 % | 87.0 | 88.3 | 96.0 | 98.0 |
| 부정확 [%의 CV] | 4.1 | 5.4 | 10.8 | 4.0 |
| D | ||||
| -80 ° C, 3 일에서 안정성 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| 87.5 | 96.5 | 96.7 | 실패한 | |
| 실패한 | 97.6 | 98.7 | (110) | |
| 88.8 | 96.4 | (106) | (109) | |
| 87.3 | (101) | 96.5 | (109) | |
| 공칭 농도 % | 87.9 | 97.9 | 99.5 | 109.3 |
| 부정확 [%의 CV] | 0.8 | 2.2 | 4.5 | 0.6 |
| -80 ° C, 7 일에서 안정성 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| 실패한 | 98.0 | (105) | 99.8 | |
| 97.1 | (106) | (104) | (105) | |
| 99.7 | (102) | 99.3 | (102) | |
| (101) | 99.9 | (109) | (106) | |
| 공칭 농도 % | 99.3 | 101.5 | 104.3 | 103.2 |
| 부정확 [%의 CV] | 2.0 | 3.4 | 4.0 | 2.8 |
| -80 ° C, 하루 30에서 안정성 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| 88.2 | 85.3 | 89.6 | 96.7 | |
| 96.2 | 92.6 | 85.8 | 94.1 | |
| 83.9 | 93.7 | 91.0 | (105) | |
| 95.6 | 94.0 | 98.9 | (102) | |
| 공칭 농도 % | 91.0 | 91.4 | 91.3 | 99.5 |
| 부정확 [%의 CV] | 6.0 | 4.1 | 5.5 | 4.9 |
| E | ||||
| 동결 해동 안정성, -20 ° C, 1주기 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| 92.5 | 86.2 | 90.2 | 94.3 | |
| 89.8 | 90.5 | 85.4 | (104) | |
| 94.7 | 88.6 | 93.4 | (104) | |
| (101) | 89.2 | 93.7 | 96.3 | |
| 공칭 농도 % | 94.5 | 88.6 | 90.7 | 99.7 |
| 부정확 [%의 CV] | 4.8 | 1.8 | 3.9 | 5.1 |
| 안정성 해동 동결 -20 ° C, 2주기를 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| 99.1 | 97.6 | 실패한 | 85.3 | |
| 93.1 | 88.1 | 93.4 | 92.0 | |
| 94.9 | 91.5 | 85.8 | 93.9 | |
| 실패한 | 90.5 | 86.8 | 85.4 | |
| 공칭 농도 % | 95.7 | 91.9 | 88.7 | 89.2 |
| 부정확 [%의 CV] | 3.1 | 4.0 | 4.1 | 4.5 |
| 안정성 해동 동결 -20 ° C, 3주기를 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| 95.7 | 실패한 | 86.0 | 93.3 | |
| 95.5 | 87.4 | 85.0 | 91.3 | |
| 90.5 | 89.1 | 86.0 | 86.0 | |
| 96.9 | 85.7 | 90.2 | 실패한 | |
| 공칭 농도 % | 94.7 | 87.4 | 86.8 | 90.2 |
| 부정확 [%의 CV] | 2.8 | 1.7 | 2.3 | 3.8 |
| F | ||||
| +4 ℃로, 24 시간에서 추출 된 샘플의 안정성 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| (122) | (112) | 91.0 | (104) | |
| 93.5 | (106) | 91.8 | 96.1 | |
| (111) | 94.8 | 98.2 | 93.5 | |
| 98.4 | 97.6 | 91.3 | 89.8 | |
| 공칭 농도 % | 106.2 | 102.6 | 93.1 | 95.9 |
| 부정확 [%의 CV] | 12.8 | 7.9 | 3.4 | 6.0 |
| +4 ℃로, 48 시간에서 추출 된 샘플의 안정성 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| (106) | (108) | 93.7 | (110) | |
| (105) | 98.1 | 94.6 | 98.9 | |
| (103) | 98.4 | 95.0 | 92.6 | |
| (108) | 93.1 | 89.7 | 85.5 | |
| 공칭 농도 % | 105.5 | 99.4 | 93.3 | 96.8 |
| 부정확 [%의 CV] | 2.1 | 6.2 | 2.4 | 10.4 |
| +4 ℃로, 72 시간에서 추출 된 샘플의 안정성 | ||||
| 품질 관리 수준 [NG / ㎖] | (2) | 4 | (20) | (40) |
| 96.5 | (112) | 96.4 | (104) | |
| (101) | 95.3 | (103) | 95.2 | |
| 94.2 | (105) | 93.5 | 99.5 | |
| (100) | 96.9 | 92.6 | 89.3 | |
| 공칭 농도 % | 97.9 | 102.3 | 96.4 | 97.0 |
| 부정확 [%의 CV] | 3.1 | 7.7 | 4.7 | 6.3 |
안정성 시험의 표 5. 결과. 7 일 동안 실온에서 건조 혈액 관광 명소 타 크롤리 무스의 안정성, B : 냉장고에 건조 혈액 명소 (4 ℃로) 7 일 이상에 타 크롤리 무스의 안정성 C : -20 °에서 건조 혈액 관광 명소 타 크롤리 무스의 안정성 C 이상 1개월, D : -80 ° C에서 건조 혈액 관광 명소 타 크롤리 무스의 안정성 1 개월 이상, E : 건조 혈액 관광 명소 타 크롤리 무스의 안정성 세 이상 동결 해동 사이클 (-20 ° C), F : 72 시간 동안 4 ℃에서 샘플 / 오토 샘플러 안정성을 추출. 데이터는 공칭 농도 %로 제시됩니다. "실패"로 표시 샘플을 실험실 / 장비 오류로 손실 된 샘플입니다. 대부분의 경우에는 피크는 전혀 검출되지 않았거나 내부 표준 물질 피크가 누락되었습니다.

타 크롤리 무스. 원자 번호의 그림 1. 구조는 순수 및 응용 화학 (IUPAC) 명칭의 국제 연합 (EU)을 따른다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

전환 밸브 2. 연결 그림.424fig2large.jpg "대상 ="_ 빈 ">이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
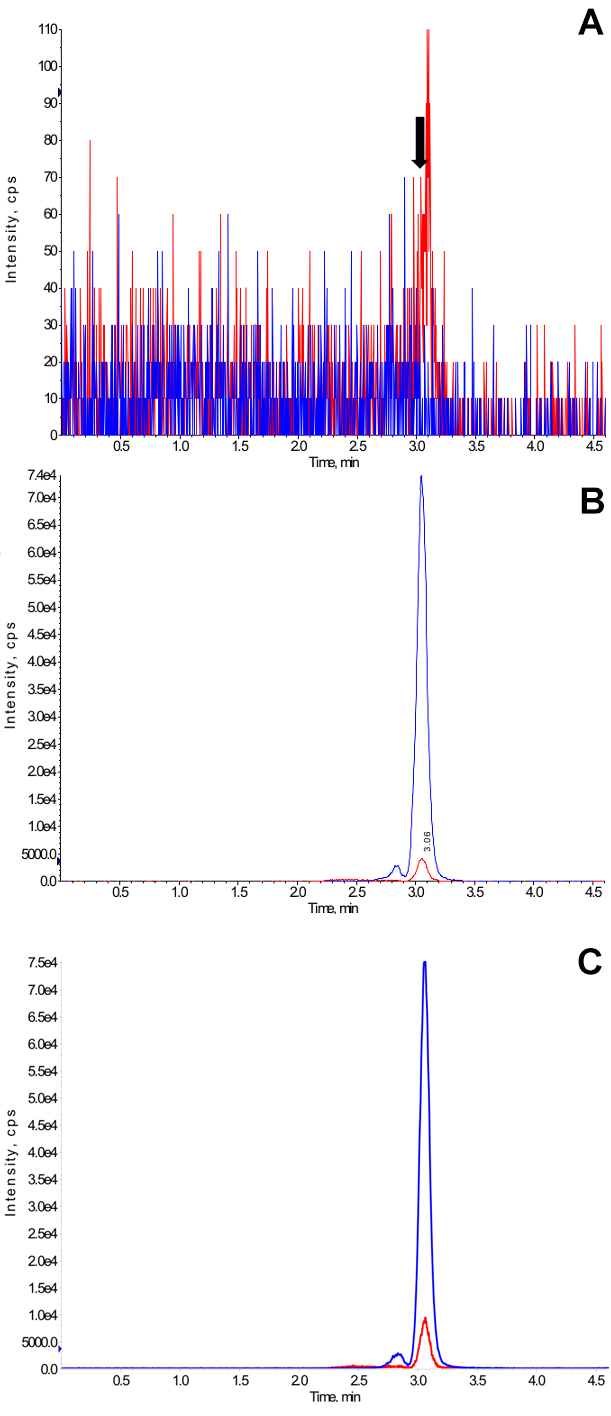
그림 3. 대표적인 이온 크로마토 그램. (A) 필터 용지에 발견 빈 혈액 샘플의 대표적인 이온 크로마토 그램 (제조 업체의 자세한 내용은, 재료 목록 참조) 및 건조. 화살표는 타크로리무스 피크 (B) 시료를 정량화 (1 NG / ㎖)의 하한에서 아군 빈 혈액의 대표적인 이온 크로마토 여과지 상에 발견하고, 건조하고 (C) 대표 이온 크로마토 그램의 머무름 시간을 표시 필터 종이에 이식 환자에 의해 수집 된 샘플의. 이 통 샘플과 측정 된 타 크롤리 무스의 농도는 2.1 NG / ㎖이었다. 이 샘플 재택 환자에 의해 수집하고 있었다 임상 시험에서하였습니다 신시내티 임상 시험 심사위원회의 대학 (신시내티, OH)에 의해 승인했다. 모든 환자는 적절한 서면 동의했다. 질량 분석 소프트웨어에 의해 생성 된 이온 크로마토 그램은 원본을 인쇄 아웃입니다 (제조 세부 사항, 재료 목록을 참조하십시오). 이온 크로마토 그램에 파란색과 빨간색 선은 내부 표준 D 2, 각각 13 C-타 크롤리 무스와 타 크롤리 무스를 나타냅니다. 주 타 크롤리 무스와 내부 표준 물질 피크의 앞에 용출 피크가 로타 머 있습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

도 4 주제 검량선. 일본어 프린트 아웃 질량 분석 소프트웨어에 의해 생성 된 바와 같이 도시된다.424 / 52424fig4large.jpg "대상 ="_ 빈 ">이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
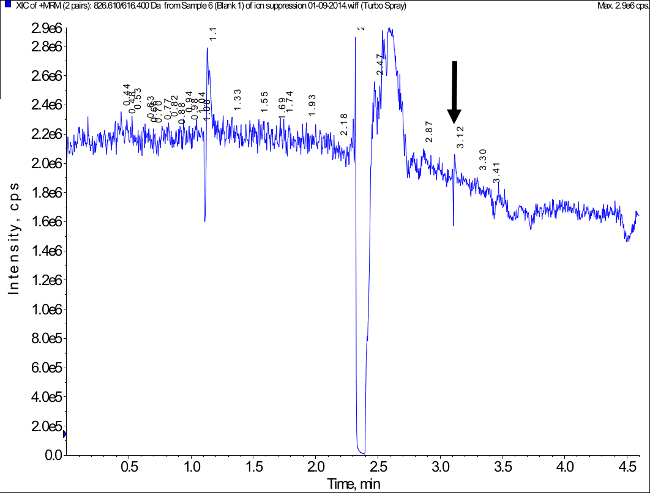
그림 5. 대표 이온 크로마토 그램 (이온 억제 / 이온 기능 향상). 화살표는 타 크롤리 무스 피크의 유지 시간을 표시하는 잠재적 인 매트릭스 효과를 평가하기 위해 추출 된 빈 혈액 샘플의 후 열 타 크롤리 무스의 주입하고 주입하는 동안 측정. 매트릭스 효과는 시험 46에 근거하여 실시 하였다. 효과가 발견 된 어떤 관련 행렬. 이 그림의 더 큰 버전을 보려면 여기를 클릭하여 주시기 바랍니다.
토론
전술 한 바와 같이, 건조 혈액 반점에 기초 치료약 및 타 크롤리 무스의 부착 모니터링 개념 매력적이며, 비록 전형적 정맥 EDTA 전혈 샘플에 타크로리무스의 LC-MS / MS 분석과 연관된 넘어 분석 과제가있다. 이들은 다음을 포함하지만, 여기에 사용되는 행렬은 필터 카드 재료와 저 혈량 (20 μL)의 코튼 린터 재료에 담가 모세관 전혈 사실, 이에 한정되지 않는다. 그럼에도 불구하고, 중앙 연구소에서 높은 처리량 분석은 강력한 특이적이고 고감도 LC-MS / MS 분석과 조합하여 매트릭스 간섭 및 매트릭스 효과 부족 시료 결과 빠르고 신뢰할 추출 방법을 필요로한다. 이미 천공 필터 카드 추출 / LC-MS / MS 분석이 실패 할 경우 재분석 방치에 충분한 재료는 일반적으로이없는 분석의 신뢰성은 중요하다.
Fi를본 연구에 사용 된 LTER 카드는 이러한 FDA의 승인 클래스 II 장치이기 때문에, NCCLS 지침 LA4-A5 (44)을 준수하고 CE 마크 유럽에 선택되었다 (제조 업체의 자세한 내용은, 재료 목록을 참조하십시오). 완전히 충전되면, 와트 903 필터 카드에 하나 원은 보유 ≈50 혈액 46 μL. 그러나, 개개의 환자에 의해 수집 된 혈액 방울의 크기는 다양하고 적절한 샘플링 기술 훈련이 필수적이다 (46).
혈액 자리 샘플 건조 펀치 아웃을 추출의 첫 번째 중요한 단계는 균질화입니다. 우리의 경험에 기초하여, 탄환 블렌더를 사용하면보다 효율적으로 초음파 및 추출 효율을 향상시키기 위해 사용되는 다른 방법들보다 더 재현. 탄환 믹서의 사용은 일관되게 90 % 이상 추출 회수율을 달성하기 위해 필수적이다. 추출 공정의 안정성을 위해, 모든 원심 temperat이되었는지 확인하는 것도 중요URE 제어 (4 ℃로)와 소용돌이로 교반 단계는 더 많은 변수 낮은 추출 회복의 결과보다 짧은 10 분, 아니었다. 또한, 타 크롤리 무스 복구 단백질 침전 용액의 정확한 조성에 매우 민감로서 메탄올 / ZnSO 4 비율이 변경되지 않는다는 것이 중요하다.
다음 과제는 매트릭스 간섭 효과를 일으킬 수 있습니다 재료의 이상적없는 깨끗한 추출물을 얻는 것입니다. 따라서, 자주 EDTA 혈액 샘플에서 타크로리무스의 추출에 사용되는 간단한 원스텝 단백질 침전 단계는 실행 가능한 옵션으로 간주되지 않았다. 단백질 (동위 원소 표지 된 내부 표준 물질을 첨가 포함) ZnSO 4를 사용하여 침전 텍싱 및 원심 분리 후, 상청액을 HPLC 2D 시스템과 온라인으로 추출 컬럼에 주입 하였다. 간단한 6 포트를 사용하여, 종래의 프리 카트리지 컬럼에 5 ㎖ / 분의 높은 흐름을 이용한 온라인 열 추출타 크롤리 무스의 분석을위한 전환 밸브 (47)는 이전에 설명되었다. 그 타 크롤리 무스 및 내부 표준 물질은 추출 컬럼의 전방에서 농축하고 정리 단계 중에 열을 통해 이동하지 않도록 이동상 선택되었다. 본 프로토콜에 사용되는 온라인 추출 부정적인 HPLC 분석에 영향을 미치지 않고 상대적으로 큰 샘플 부피의 주입 등 여러 장점을 가지고 있었다. 추출 컬럼의 상단에 분석을 풍부 후 백 플러시 ( "초점 피크") 특히 낮은 타 크롤리 무스의 농도와 샘플 소프트웨어 알고리즘에 의해보다 안정적인 통합을 가능하게 선명 피크의 결과. (48) 온라인 정리 단계는 제거하지 않았다 잠재적 매트릭스 화합물을 방해 할뿐만 아니라 시료를 탈 소금. 고용량, 고 스루풋 LC-MS / MS 분석을위한 또 하나의 중요한 문제는 거의 언급하지 인해 증가에 LC-MS / MS 시스템의 감도의 점진적인 손실대규모 배치의 분석 기간 동안 전기 분무 소스의 오염. 유의 매트릭스 효과 (이온 억제 / 이온 향상)는 관찰되지 않았다. 잠재적 인 매트릭스 효과의 부정적인 효과의 조합에 의해 / 감소를 피할 않은 다음 : 16,000 XG, 높은 흐름 온라인으로 추출, 잠재적 인 간섭 초기 용출에서 타 크롤리 무스의 명확한 크로마토 그래피 분리에 단백질 침전 후 메탄올 / ZnSO 4, 원심 분리를 이용하여 효과적인 단백질 침전 분석 컬럼 대신 같은 아스코 마이신과 같은 구조적으로 관련된 내부 표준 물질의 내부 표준으로 동위 원소 표지 된 타 크롤리 무스의 사용에서.
정량의 하한은 1 NG / ㎖, 현재 자주 EDTA 혈액 샘플 치료약의 타크로리무스 모니터링을 위해 사용되는 대부분의 면역 따라서보다 낮았다. 정량이 하한은 심지어 소위 낮은 칼시 뉴린 억제제 장기 immunosuppres 충분하다시브 유지 관리 프로토콜.
건조 블러드에 타 크롤리 무스를 정량화하기 이전에 설명한 LC-MS / MS 분석과 비교 29-34,36,39,41,42, 본 분석 일치하는 점이나 낮은 정량 한계, 추출 복구, 정확성의 측면에서 성능을 초과 정밀도와 같은 보통 건강한 사람의 혈액 샘플에 기초하여 검증하는 동안 수용 가능한 결과를 제공 한 단계 단백질 침전 방법 및 초단 크로마토 시간, 잠재적으로 위험한 개념 피해서. 그러나 이식 환자는 혈액의 구성에 영향을 미치는 사람이 여러 약물을 복용 질병을 가진 환자의 매우 복잡한 그룹입니다. 이것은 사실상 불가능 검증으로 개별 환자에 존재하고 만 가능한 전략은 그러한 잠재적 간섭의 위험을 최소화하는 방식으로 분석을 설정할 수도있다 모든 잠재적 인 간섭을 배제 할 수있다. 말린 혈액 SPOTS는 혈액 점도의 적혈구 용적률의 효과 때문에 여과지 49에 적용되는 혈액의 확산 특성과 같은 문제가있다. 이러한 효과는 이미 임상 적으로 합리적인 제한 29,32 내의 적혈구 용적률 및 타 크롤리 무스의 농도에서 건조 혈액 명소에서 타 크롤리 무스 분석에 영향을 미치지 않도록 기재되어있다 이것은 다시 여기에 테스트되지 않았습니다. 높은 온도에서 건조 혈액 명소에서 타 크롤리 무스의 또한 안정성이 이미 건조 혈액 명소에서 다른 사람과 타 크롤리 무스에 의해 연구되어왔다 건조 혈액의 선적을위한 중요한에도 60 ° C (32), 37 ℃에서 5 일간 안정 및 밝혀졌다 특히 여름 동안하지 온도 제어 조건에서 관광 명소입니다.
탄환 블렌더 균질화의 조합에 기초하여 상기 분석은, 높은 열 흐름 온라인 정리 및 LC-MS / MS 분석은 다른 IMM의 정량 생체 시료 분석법의 개발 플랫폼 전략을 제공 할 수있다단독으로 또는 동시에뿐만 아니라, 건조 혈액 자리 샘플에서 다른 약물의 unosuppressants.
공개
The authors have nothing to disclose.
감사의 말
This work was supported by the United States Federal Drug Administration (FDA) contract HHSF223201310224C and the United States National Institutes of Health/FDA grant 1U01FD004573-01.
자료
| Name | Company | Catalog Number | Comments |
| Tacrolimus | U.S. Pharmacopeial Convention | 1642802 | |
| D2,13C-Tacrolimus | Toronto Research Chemicals Inc. | F370002 | |
| Red blood cells | University of Colorado Hospital | W20091305500 V | |
| Plasma | University of Colorado Hospital | W2017130556300Q | |
| Acetone CHROMASOLV, HPLC, ≥99,9% | Sigma-Aldrich | 439126-4 L | |
| Acetonitrile Optima LC/MS, UHPLC-UV | Thermo Fisher Scientific | A955-4 | |
| Isopropanol 99.9%, HPLC | Fisher Scientific | BP2632-4 | |
| Methanol Optima LC/MS | Thermo Fisher Scientific | A452-4 | |
| Water Optima LC/MS, UHPLC-UV | Thermo Fisher Scientific | W6-4 | |
| Formic acid | Thermo Fisher Scientific | A118P-500 | |
| Phosphate-buffered saline (PBS) | Sigma-Aldrich | D8537 | |
| Zinc sulfate | Thermo Fisher Scientific | Z68-500 | |
| 0.5 – 10 µl pipet, VoluMate LIQUISYSTEMS | Mettler Toledo | 17008649 | |
| 1.5 ml Eppendorf tube | Thermo Fisher Scientific | 02-682-550 | |
| 10 – 100 µl pipet, VoluMate LIQUISYSTEMS | Mettler Toledo | 17008651 | |
| 10 μl pipet tips with filter, sterile | Neptune | BT 10XLS3 | |
| 100 – 1,000 µl pipet, VoluMate LIQUISYSTEMS | Mettler Toledo | 17008653 | |
| 100 μl pipet tips with filter, sterile | Neptune | BT 100 | |
| 1,000 μl pipet tips with filter, sterile | Multimax | 2940 | |
| 2 – 20 µl pipet, VoluMate LIQUISYSTEMS | Mettler Toledo | 17008650 | |
| 2 ml Eppendorf tube | Thermo Fisher Scientific | 02-681-258 | |
| 20 – 200 µl pipet, VoluMate LIQUISYSTEMS | Mettler Toledo | 17008652 | |
| 20 μl pipet tips with filter, sterile | GeneMate | P-1237-20 | |
| 200 μl pipet tips with filter | Multimax | 2938T | |
| 200 μl pipet tips with filter, sterile | Multimax | 2936J | |
| 50 ml Falcon tube | BD Falcon | 352070 | |
| 300 μl inserts for HPLC vials | Phenomenex | ARO-9973-13 | |
| Balance PR2002 | Mettler Toledo | 1117050723 | |
| Balances AX205 Delta Range | Mettler Toledo | 1119343379 | |
| Bullet Blender Homogenizer | Next Advance | BBX24 | |
| Centrifuge Biofuge Fresco | Heraeus | 290395 | |
| Disposable Wipes | PDI | Q55172 | |
| Glass v ials, 4 ml | Thermo Fisher Scientific | 14-955-334 | |
| Glass vials, 20 ml | Thermo Fisher Scientific | B7800-20 | |
| Gloves, nitrile | Titan Brand Gloves | 44-100S | |
| HPLC vials, 9 mm, 2 ml, clear | Phenomenex | ARO- 9921-13 | |
| Lids for HPLC vials | Phenomenex | ARO- 8952-13-B | |
| Needle, 18 G 1.5 | Precision Glide | 305196 | |
| Rack for Eppendorf tubes | Thermo Fisher Scientific | 03-448-11 | |
| Rack for HPLC Vials | Thermo Fisher Scientific | 05-541-29 | |
| Steel beads 0.9 – 2 mm | Next Advance | SSB14B | |
| Storage boxes for freezers / refrigerators | Thermo Fisher Scientific | 03-395-464 | |
| Standard multi-tube vortexer | VWR Scientific Products | 658816-115 | |
| Whatman Paper, 903 Protein Saver US 100/PK | GE Whatman | 2016-05 | |
| Autosampler | CTC PAL | PAL.HTCABIx1 | |
| Binary pump, Agilent 1260 Infinity | Agilent Technologies | 1260 G1312B | |
| Binary pump, Agilent 1290 Infinity | Agilent Technologies | 1290 G4220A | |
| Micro vacuum degasser, Agilent 1260 | Agilent Technologies | 1260 G13798 | |
| Column oven, Agilent 1290 with 2 position | Agilent Technologies | 1290 G1216C | |
| Thermostated column compartment with integrated 6 port switching valve | Agilent Technologies | 1290 G1316C | |
| HPLC pre-column cartridge, Zorbax XDB C8 (5 µm particle size), 4.6 · 12.5 mm | Phenomenex | 820950-926 | |
| HPLC analytical column, Zorbax Eclipse-XDB-C8 (5 µm particle size), 4.6 · 150 mm | Phenomenex | 993967-906 | |
| Tandem Mass Spectrometer | |||
| API5000 MS/MS with TurboIonspray source | AB Sciex | 4364257 | |
| Mass spectrometry software | AB Sciex | Analyst 1.5.1 |
참고문헌
- Goto, T., et al. Discovery of FK506, a novel immunosuppressant isolated from Streptomyces Tsukubaensis. Transplant Proc. 19 (5 Suppl 6), 4-8 (1987).
- Kino, T., Hatanaka, H., Miyata, S. FK506, a novel immunosuppressant isolated from a streptomyces. I: Fermentation, isolation and physico-chemical and biological characteristics. J. Antibiotics. 40 (9), 1249-1255 (1987).
- Starzl, T. E., et al. FK506 for liver, kidney and pancreas transplantation. Lancet. 2 (8670), 1000-1004 (1989).
- Randomised trial comparing tacrolimus (FK506) and cyclosporin in prevention of liver allograft rejection. European FK506 Multicentre Liver Study Group. Lancet. 344 (8920), 423-428 (1994).
- A comparison of tacrolimus (FK 506) and cyclosporine for immunosuppression in liver transplantation. The U.S. Multicenter FK506 Liver Study Group. N. Engl. J. Med. 331 (17), 1110-1115 (1994).
- Mayer, A. D., et al. Multicenter randomized trial comparing tacrolimus (FK506) and cyclosporine in the prevention of renal allograft rejection: a report of the European Tacrolimus Multicenter Renal Study Group. Transplantation. 64 (3), 436-443 (1997).
- Pirsch, J. D., Miller, J., Deierhoi, M. H., Vincenti, F., Filo, R. S. A comparison of tacrolimus (FK506) and cyclosporine for immunosuppression after cadaveric renal transplantation. FK506 Kidney Transplant Study Group. Transplantation. 15 (7), 977-983 (1997).
- Tanaka, H., et al. Physicochemical properties of FK506 a novel immunosuppressant isolated from Streptomyces Tsukubaensis. Transplant Proc. 14 ((5 Suppl 6)), 11-16 (1987).
- Spencer, C. M., Goa, K. L., Gills, J. C. Tacrolimus. An update of its pharmacology and clinical efficacy in the management of organ transplantation. Drugs. 54 (6), 925-975 (1997).
- Clipstone, N. A., Crabtree, G. R. Identification of calcineurin as a key signalling enzyme in T-lymphocyte activation. Nature. 357 (6380), 695-697 (1992).
- Barbarino, J. M., Staatz, C. E., Venkataramanan, R., Klein, T. E., Altman, R. B. PharmGKB summary: cyclosporine and tacrolimus pathways. Pharmacogenet. Genomics. 23 (10), 563-585 (2013).
- Annual Data Report. , Department of Health and Human Services, Health Resources and Services Administration, Healthcare Systems Bureau, Division of Transplantation. Available from: http://optn.transplant.hrsa.gov/data/annualreport.asp (2014).
- Draft Guidance on Tacrolimus. , Food and Drug Administration, Office of Generic Drugs. Available from: http://www.fda.gov/downloads/Drugs/GuidanceComplianceRegulatoryInformation/Guidances/UCM181006.pdf (2012).
- Christians, U., Benet, L. Z., Lampen, A. Mechanisms of clinically significant drug interactions associated with tacrolimus. Clin. Pharmacokinet. 41 (11), 813-851 (2002).
- Christians, U., Pokaiyavananichkul, T., Chan, L. Tacrolimus In: Pharmacokinetics and Pharmacodynamics. Principles of Therapeutic Drug Monitoring. Burton, M. E., Shaw, L. M., Schentag, J. J., Evans, W. ebb , 4th Edition, Lipincott, Wiliams, and Wilkins. =Baltimore. 529-562 (2005).
- Holt, D. W., et al. International Federation of Clinical Chemistry/ International Association of Therapeutic Drug Monitoring and Clinical Toxicology working group on immunosuppressive drug monitoring. Ther. Drug Monit. 24 (1), 59-67 (2002).
- Holt, D. W., Jones, K., Lee, T., Stadler, P., Johnston, A. Quality assessment issues of new immunosuppressive drugs and experimental experience. Ther. Drug Monit. 18 (4), 362-367 (1996).
- Jusko, W. J., et al. Consensus document: therapeutic drug monitoring of tacrolimus (FK-506). Ther. Drug Monit. 17 (6), 606-614 (1995).
- Oellerich, M., et al. Therapeutic drug monitoring of cyclosporine and tacrolimus. Update on Lake Louise Conference on cyclosporine and tacrolimus. Clin. Biochem. 31 (5), 309-316 (1998).
- Wong, S. H. Therapeutic drug monitoring for immunosuppressants. Clin. Chim. Acta. 313 (1-2), 241-253 (2001).
- Kahan, B. D., et al. Low intraindividual variability of cyclosporin A exposure reduces chronic rejection incidence and health care costs. J. Am. Soc. Nephrol. 11 (6), 1122-1131 (2000).
- Kahan, B. D., et al. Variable oral absorption of cyclosporine. A biopharmaceutical risk factor for chronic renal allograft rejection. Transplantation. 62 (5), 599-606 (1996).
- Kelly, D. A. Current issues in pediatric transplantation. Pediatr. Transplant. 10 (6), 712-720 (2006).
- Spivey, C. A., Chisholm-Burns, M. A., Damadzadeh, B., Billheimer, D. Determining the effect of immunosuppressant adherence on graft failure risk among renal transplant recipients. Clin. Transplant. 28 (1), 96-104 (2014).
- Taylor, P. J., Tai, C. H., Franklin, M. E., Pillans, P. I. The current role of liquid chromatography-tandem mass spectrometry in therapeutic drug monitoring of immunosuppressant and antiretroviral drugs. Clin. Biochem. 44 (1), 14-20 (2011).
- Edelbroek, P. M., van der Heijden, J., Stolk, L. M. Dried blood spot methods in therapeutic drug monitoring: methods, assays, and pitfalls. Ther. Drug Monit. 31 (3), 327-336 (2009).
- Meesters, R. J., Hooff, G. P. State-of-the-art dried blood spot analysis: an overview of recent advances and future trends. Bioanalysis. 5 (17), 2187-2208 (2013).
- Pandya, H. C., Spooner, N., Mulla, H. Dried blood spots, pharmacokinetic studies and better medicines for children. Bioanalysis. 3 (7), 779-786 (2011).
- Koster, R. A., Alffenaar, J. W., Greijdanus, B., Uges, D. R. Fast LC-MS/MS analysis of tacrolimus, sirolimus, everolimus and cyclosporin A in dried blood spots and the influence of the hematocrit and immunosuppressant concentration on recovery. Talanta. 115 (Oct 15), 47-54 (2013).
- Hinchliffe, E., Adaway, J., Fildes, J., Rowan, A., Keevil, B. G. Therapeutic drug monitoring of ciclosporin A and tacrolimus in heart lung transplant patients using dried blood spots. Ann Clin. Biochem. 51 (Pt 1), 106-109 (2014).
- Koop, D. R., Bleyle, L. A., Munar, M., Cherala, G., Al-Uzri, A. Analysis of tacrolimus and creatinine from a single dried blood spot using liquid chromatography tandem mass spectrometry. J. Chromatogr. B Analyt. Technol. Biomed. Life Sci.. 926 ((May 1)), 54-61 (2013).
- Sadilkova, K., Busby, B., Dickerson, J. A., Rutledge, J. C., Jack, R. M. Clinical validation and implementation of a multiplexed immunosuppressant assay in dried blood spots by LC-MS/MS. Clin. Chim. Acta.. 421 ((Jun 5)), 152-156 (2013).
- Li, Q., Cao, D., Huang, Y., Xu, H., Yu, C., Li, Z. Development and validation of a sensitive LC-MS/MS method for determination of tacrolimus on dried blood spots. Biomed. Chromatogr. 27 (3), 327-334 (2013).
- Hinchliffe, E., Adaway, J. E., Keevil, B. G. Simultaneous measurement of cyclosporin A and tacrolimus from dried blood spots by ultra-high performance liquid chromatography tandem mass spectrometry. J. Chromatogr. B Analyt. Technol. Biomed. Life Sci.. 883-884 ((Feb 1)), 102-107 (2012).
- Webb, N. J., Roberts, D., Preziosi, R., Keevil, B. G. Fingerprick blood samples can be used to accurately measure tacrolimus levels by tandem mass spectrometry). Pediatr. Transplant. 9 (6), 729-733 (2005).
- Keevil, B. G., Fildes, J., Baynes, A., Yonan, N. Liquid chromatography-mass spectrometry measurement of tacrolimus in finger-prick samples compared with venous whole blood samples. Ann. Clin. Biochem. 46 (Pt 2), 144-145 (2009).
- Yonan, N., Martyszczuk, R., Machaal, A., Baynes, A., Keevil, B. G. Monitoring of cyclosporine levels in transplant recipients using self-administered fingerprick sampling. Clin. Transpl. 20 (2), 221-225 (2006).
- Keevil, B. G., et al. Simultaneous and rapid analysis of cyclosporin A and creatinine in finger prick blood samples using liquid chromatography tandem mass spectrometry and its application in C2 monitoring. Ther Drug Monit. 24 (6), 757-767 (2002).
- Hoogtanders, K., et al. Dried blood spot measurement of tacrolimus is promising for patient monitoring. Transplantation. 83 (2), 237-238 (2007).
- Heijden, J., et al. Therapeutic drug monitoring of everolimus using the dried blood spot method in combination with liquid chromatography-mass spectrometry. J. Pharm. Biomed. Anal. 50 (4), 664-670 (2009).
- Cheung, C. Y., et al. Dried blood spot measurement: application in tacrolimus monitoring using limited sampling strategy and abbreviated AUC estimation. Transpl. Int. 21 (2), 140-145 (2008).
- Hoogtanders, K., et al. Therapeutic drug monitoring of tacrolimus with the dried blood spot method. J. Pharm. Biomed. Anal. 44 (3), 658-664 (2007).
- Wilhelm, A. J., den Burger, C. J., Vos, R. M., Chahbouni, A., Sinjewel, A. Analysis of cyclosporin A in dried blood spots using liquid chromatography tandem mass spectrometry. J. Chromatogr. B Analyt. Technol. Biomed. Life Sci. 877 (14-15), 1595-1598 (2009).
- Ostler, M. W., Porter, J. H., Buxton, M. O. Dried blood spot collection of health biomarkers to maximize participation in population studies. J. Vis. Exp. (83), e50973(2014).
- Hannon, H. W., et al. Blood collection on filter paper for neonatal screening programs, approved standard LA4-A5. , Clinical Laboratory and Standards Institute. Available from: http://www.clsi.org (2007).
- Schäfer, P., Störtzel, M., Vogt, S., Weinmann, W. Ion suppression effects in liquid chromatography-electrospray-ionisation transport-region collision induced dissociation mass spectrometry with different serum extraction methods for systematic toxicological analysis with mass spectra libraries. J. Chromatogr. B. 773 (1), 47-52 (2002).
- Peck, H. R., Timko, D. M., Landmark, J. D., Stickle, D. F. A survey of apparent blood volumes and sample geometries among filter paper bloodspot samples submitted for lead screening. Clin. Chim. Acta. 400 (1-2), 103-106 (2009).
- Christians, U., et al. Automated, fast and sensitive quantification of drugs in blood by liquid chromatography-mass spectrometry with on-line extraction: immunosuppressants. J. Chromatogr. B. 748 (1), 41-53 (2000).
- Clavijo, C., et al. Development and validation of a semi-automated assay for the highly sensitive quantification of Biolimus A9 in human whole blood using high performance liquid chromatography-tandem mass spectrometry. J. Chromatogr. B. Analyt. Technol. Biomed. Life Sci. 877 (29), 3506-3514 (2009).
- Mei, J. V., Alexander, J. R., Adam, B. W., Hannon, W. H. Use of filter paper for the collection and analysis of human whole blood specimens. J. Nutr. 131 (5), S1631-S1636 (2001).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유