Method Article
Quantificazione del immunosoppressore Tacrolimus su macchie di sangue secco Uso LC-MS / MS
In questo articolo
Riepilogo
Here we describe a high-performance liquid chromatography-tandem mass spectrometry (HPLC-MS/MS) assay to quantify the immunosuppressant tacrolimus in dried blood spots using a simple manual protein precipitation step and online column extraction.
Abstract
Il tacrolimus inibitore della calcineurina è la pietra angolare della maggior parte dei protocolli di trattamento immunosoppressivi dopo il trapianto d'organo solido negli Stati Uniti. Tacrolimus è un farmaco ristretto indice terapeutico e come tale richiede un monitoraggio terapeutico e aggiustamento della dose in base a intere sue concentrazioni ematiche. Per facilitare la casa farmaci terapeutici e monitoraggio aderenza, la raccolta di macchie di sangue essiccato è un concetto interessante. Dopo un dito bastone, il paziente raccoglie una goccia di sangue su carta da filtro a casa. Dopo che il sangue è asciugato, viene inviato al laboratorio di analisi dove tacrolimus è quantificato utilizzando la spettrometria di massa ad alta prestazione cromatografia liquida-tandem (HPLC-MS / MS) in combinazione con un manuale semplice passo precipitazione delle proteine e l'estrazione della colonna in linea.
Per l'analisi tacrolimus, un disco 6 mm è perforato dal centro satura di spot sangue. La macchia di sangue viene omogeneizzato con un proiettile frullatore unnd poi le proteine vengono precipitate con metanolo / 0,2 M ZnSO4 contenente lo standard D interno 2, 13 C-tacrolimus. Dopo vortex e centrifugazione, 100 pl di surnatante viene iniettato in una colonna di estrazione in linea e lavate con 5 ml / min di 0,1 formico acido / acetonitrile (7: 3, v: v) per 1 min. Di seguito, la valvola di commutazione viene attivato e gli analiti sono back-lavata sulla colonna analitica (e separati usando un acido formico / acetonitrile pendenza 0,1%). Tacrolimus è quantificato in modalità positiva Multi reazione (MRM) usando uno spettrometro di massa tandem.
Il saggio è lineare da 1 a 50 ng / ml. Variabilità inter-assay (3,6% -6,1%) e l'accuratezza (91,7% -101,6%), valutato in 20 giorni soddisfano criteri di accettazione. Recupero medio estrazione è 95,5%. Non ci sono rilevanti riporto, le interferenze della matrice e effetti matrice. Tacrolimus è stabile nelle macchie di sangue essiccato a temperatura ambiente ea 4 ° C per 1 settimana. Campioni estratti incampionatore sono stabili a + 4 ° C per almeno 72 ore.
Introduzione
Tacrolimus è un potente immonosuppressant 1-7 che ha una struttura macrolide 8 (Figura 1). A causa di cis - isomeria trans dei legami CN forma due rotameri in soluzione 9 che possono essere separati da fase inversa cromatografia liquida ad alta prestazione (HPLC) Tacrolimus è lipofila e solubile in alcoli (metanolo: 653 g / L, etanolo: 355 g / L), idrocarburi alogenati (cloroformio: 573 g / L) ed etere. E 'scarsamente solubile in idrocarburi alifatici (esano: 0,1 g / L e acqua (pH 3:. 0,0047 g / L) 9 La molecola non contiene alcun cromofori e la sua massima UV-assorbimento è di 192 nm Tacrolimus agisce attraverso l'inibizione della calcineurina. . Il suo meccanismo d'azione è stato rivisto in riferimenti 10,11. Attualmente è utilizzato in oltre l'80% dei pazienti sottoposti a trapianto di organi solidi negli Stati Uniti 12.
L'indice terapeutico di tacrolimus è considered per essere stretto 13. Inoltre, la correlazione tra le dosi di tacrolimus e concentrazioni nel sangue è scarsa e la farmacocinetica è variabile 14,15. Il monitoraggio terapeutico per guidare tacrolimus dosaggio in pazienti sottoposti a trapianto è pertanto la pratica clinica generale 16-20. L'obiettivo è quello di mantenere le concentrazioni di tacrolimus nel sangue entro un range terapeutico predefinito. Le concentrazioni ematiche tacrolimus al di sotto del range terapeutico possono tradursi in una maggiore attività di reazioni allo-immunitario cronici o acuti, mentre concentrazioni superiori al finestra terapeutica aumentano il rischio di sovra-immunosoppressione, il cancro e tossicità, quali nefrotossicità, neurotossicità, ipertensione e diabete. Alta farmacocinetica variabilità individuale di tacrolimus può essere dannoso sia per trapianto di organi e la sopravvivenza del paziente 21,22. Mentre variabilità inter-individuale di farmacocinetica di tacrolimus è causata principalmente da polimorfismi CYP3A5, ragioni intra-individualevariabilità includono, ma non sono limitati a, farmaco-farmaco, malattia-droga e cibo-farmaco interazioni 14,15. Anche la mancanza di aderenza alla terapia immunosoppressiva terapeutico è un fattore e una delle ragioni principali per la perdita del trapianto 23,24.
Queste considerazioni suggeriscono che spesso a casa di farmaci terapeutici e il monitoraggio di aderenza della concentrazione ematica complessiva può essere utile al fine di garantire che i pazienti abbiano l'esposizione tacrolimus all'interno della finestra terapeutica desiderata in ogni momento. Tuttavia, la logistica e il costo di più frequente monitoraggio terapeutico in quanto è in corso la pratica clinica 15 è proibitivo. Uno dei motivi è che il paziente deve vedere un prelevatore di avere il campione di sangue venoso richiesto disegnata. Macchie di sangue secco sono recentemente emersi come un concetto attraente 25-28. Dopo una semplice dito attaccare il paziente raccoglie una goccia di sangue su una speciale carta di carta da filtro e dopo che la macchia di sangue è dried, può essere inviato ad un laboratorio centrale per l'analisi di tacrolimus e qualsiasi altro immunosoppressore che il paziente può essere attualmente in corso. Questo è diventato possibile grazie allo sviluppo di test LC-MS / MS altamente sensibili e specifici per la quantificazione di tacrolimus e di altri immunosoppressori in volumi molto piccoli di sangue come macchie di sangue essiccato (in genere 20 microlitri di sangue) 25,29-43. Un altro vantaggio è che minimamente invasive, strategie a basso volume di raccolta dei campioni, come macchie di sangue essiccato facilitano notevolmente monitoraggio terapeutico e studi di farmacocinetica in bambini piccoli 28.
Tacrolimus è di solito misurata in EDTA venoso sangue intero 15. Le ragioni sono che tacrolimus distribuisce ampiamente in cellule del sangue e che gli studi clinici hanno riportato una migliore correlazione tra le concentrazioni di valle di tacrolimus nel sangue rispetto al plasma con eventi clinici 15,18. In confronto, l'analisi di tacrolimus in macchie di sangue essiccato è basato su sangue capillare che viene miscelato con la matrice carta da filtro. Questo rappresenta una sfida in termini di solubilizzazione di tacrolimus e potenziali interferenze con l'analisi LC-MS / MS. Presentiamo qui un test stabilito e convalidato in base omogeneizzazione della macchia di sangue secco con un frullatore proiettile in combinazione con un alto flusso colonna linea campione ripulire procedura e analisi LC-MS / MS. Ad oggi, questo test è stato utilizzato con successo per la quantificazione di oltre cinquemila tacrolimus secca campioni blood spot per il monitoraggio aderenza negli studi clinici.
Protocollo
Campioni di sangue de-identificati da individui sani sono stati presso la University of Colorado Hospital (Aurora, Colorado). L'uso di campioni di sangue di banca de-identificati per gli studi di validazione, così come per la preparazione di calibratori e campioni di controllo di qualità è stato considerato "esente" dal Review Board Colorado multi-istituzionale (COMIRB, Aurora, Colorado).
1. Preparazione dei riferimenti e soluzioni
- Acquisto tacrolimus e lo standard interno D 2, 13 C-tacrolimus dai venditori elencati nella Lista dei materiali.
- Preparare soluzioni in metanolo puro ad una concentrazione di 1 mg / ml per tacrolimus e una concentrazione di 10 ug / ml per D 2, 13 C-tacrolimus. Fai soluzioni stock di materiali di riferimento sulla base di tre ponderazioni indipendenti. Soluzioni madre aliquote e conservare a -70 ° C o al di sotto.
- Preparare la soluzione per precipitare le proteineed estrarre tacrolimus usando metanolo / 0,2 M ZnSO4 in acqua (7: 3, v: v). Questa soluzione contiene anche lo standard D interna 2, 13 C-tacrolimus ad una concentrazione di 2,5 ng / ml ed è usato per l'estrazione di tutti i campioni eccetto per l'estrazione di campioni bianchi (vedere 1.3.3).
- Preparare questa soluzione proteica precipitazione fresco ogni giorno estrazione e impostare la scadenza della soluzione a 12 hr.
- Preparazione della curva di calibrazione e di controllo della qualità (QC) campioni
- Preparare soluzioni di tacrolimus eseguendo appropriate diluizioni della soluzione di riserva utilizzando metanolo puro.
- Per preparare calibratori e campioni di controllo di qualità, picco di 20 ml di soluzione madre opportunamente diluito in EDTA sangue intero, incubare a 37 ° C sotto leggera agitando in un bagno d'acqua per consentire la distribuzione omogenea tacrolimus nelle cellule ematiche per 20 min e un'aliquota in 1,5 ml polipoTubi ropylene con fondo conico e scatto coperchi. Assicurarsi che il volume relativo di solvente organico non supera il 5%.
- Spot 50 ml di sangue intero a spillo nel centro di ogni cerchio sulle carte filtro utilizzando una pipetta.
- Asciugare le macchie di sangue sulle schede di filtro a temperatura ambiente per 3 ore.
- Preparare gli standard di calibrazione tacrolimus in EDTA umano sangue intero a concentrazioni di tacrolimus di 1, 2,5, 5, 10, 25, e 50 ng / ml. Preparare un campione in bianco per l'estrazione, come gli standard di calibrazione con la soluzione di precipitazione delle proteine contenente lo standard D interno 2, 13 C-tacrolimus ("campione zero").
- Preparare i campioni QC in EDTA sangue umano a concentrazioni di 0, 2, 4, 20, 40 ng / ml. Preparare un campione in bianco. In contrasto con i campioni QC che sono estratti con precipitazione contenente lo standard interno D 2, 13 C-tacrolimus, estrarre il campione bianco con soluzione proteica precipitazione che fanon contiene lo standard D interno 2, 13 C-tacrolimus ("campione in bianco").
- Raccolta dei campioni clinici
- Raccogliere macchie di sangue essiccato come descritto in 43,44.
2. Estrazione di Tacrolimus sangue secco Spot Campioni
- Ispezionare visivamente la macchia di sangue secco per garantire la qualità del campione accettabile e il volume 45.
- Centro Pugno del macchia di sangue sulla carta filtro con una perforazione di 6 mm.
Nota: La qualità dei punzoni può essere monitorato mediante pesatura. Un disco filtro saturo perforato pesa media 5.02 mg ± 0,09 mg (range: 4.83- 5.14 mg, n = 12). - I dischi posto in provette da 1,5 ml in polipropilene con fondo conico e coperchi a innesto rapido.
- Aggiungere 20-30 proiettili per ogni provetta.
- Aggiungere 500 microlitri della soluzione di precipitazione delle proteine (metanolo: 0.2 M ZnSO4, 7: 3, v: v con 2,5 ng / ml di standard interno) in ogni provetta. Per il extrazione di campioni bianchi, usare la soluzione di precipitazione proteica senza standard interno.
- Omogeneizzare i dischi nel frullatore proiettile per 1 min (velocità massima, impostando "10").
- Agitare campioni a RT su multi-tubo vorticoso (velocità massima, impostando "10") per 10 min.
- Centrifugare i campioni a 16.000 xg e 4 ° C per 10 min.
- Trasferire il surnatante in fiale di vetro HPLC dotata di inserto 300 microlitri. Utilizzare guarnizioni in Teflon di pre-taglio.
Nota: Estratto campioni possono essere conservati a -20 ° C o meno fino al momento dell'analisi LC-MS / MS.
3. LC-MS / MS Analysis
- Carico 100 pl del supernatante del campione estratto nella colonna di estrazione cartuccia C8 e lavare con 7: 3 rapporto di 0,1% di acido formico in acqua: acetonitrile ad un flusso di 5 ml / min per 1 min. Le connessioni della valvola di commutazione sono mostrati in Figura 2 e il gradiente gestito dalla pompa di estrazione in Tabella 1 .
- Di seguito, attivare la valvola di commutazione con conseguente back-flush degli analiti dalla precolonna sulla colonna analitica.
- Impostare il termostato a colonna a 65 ° C.
- Eluire gli analiti dalla colonna analitica utilizzando le portate e gradiente mostrati nella Tabella 1.
- Collegare la colonna analitica di uno spettrometro di massa tandem con la fonte di ionizzazione elettrospray turbo. Regolare i parametri chiave della spettrometro di massa in base alla tabella 2.
- Rileva ioni positivi ([M + Na] +) nella modalità di reazione multipla (MRM). Utilizzare i seguenti passaggi di ioni per la quantificazione: tacrolimus: m / z (massa / carica) = 826,6 → 616,2 e D 2, 13 C-tacrolimus: m / z = 829,6 → 619,2.
Nota: Il tempo totale di esecuzione è di 4,6 minuti.
4. Quantificazione
- Per ogni corsa, generare una curva di calibrazione in base ai calibratori preparati in 1.3.5 eincludere in ogni seduta analitica.
- Generare un diagramma di taratura riportando le concentrazioni nominali rispetto al fattore di risposta di analiti (Peak Area [Analita] / Peak Area [standard interno]) utilizzando il software spettrometro di massa.
- Montare i calibratori utilizzando un fit quadratico in combinazione con 1 / X ponderazione.
- Per tacrolimus quantità nelle macchie di sangue essiccato integrare il tacrolimus e dello standard interno nei cromatogrammi MRM estratti. Calcolare il fattore di risposta per il tacrolimus (Peak Area [Analita] / Peak Area [standard interno]) e confrontare con la curva di calibrazione utilizzando il software spettrometria di massa.
5. Procedure di convalida
- Limite inferiore di rilevamento (LLOD) e il limite inferiore di quantificazione (LLOQ).
- Si consideri la concentrazione tacrolimus più basso con un rapporto picco-a-rumore di 4: 1 come limite inferiore di rilevamento (LLOD). Definire il limite inferiore di quantificazione (LLOQ) comeconcentrazione più bassa della curva di calibrazione con precisione uguale o superiore a ± 20% deviazione dalla concentrazione nominale e precisione uguale o migliore del 20% (coefficiente di varianza).
- Intra e inter-precisioni giorno e precisioni.
- Testare l'accuratezza e la precisione a quattro livelli di concentrazione di 2 ng / ml (QC1), 4 ng / ml (QC2), 20 ng / ml (QC3) e 40 ng / ml (QC4).
- Preparare i campioni QC su ogni giorno di convalida nel sangue intero EDTA umano, asciutto su schede di filtro, estrarre e analizzare come descritto sopra.
- Determinare accuratezza e la precisione intra-day con 6 campioni per livello di concentrazione di QC.
- Valutare accuratezza e la precisione inter-giorno per 20 giorni. Misurare ogni livello di controllo qualità con 4 campioni al giorno.
- Analizzare due curve di calibrazione insieme con i campioni di QC su ogni giorno.
- Calcola la precisione intra-day come% della concentrazione nominale (sei campioni per livello di concentrazione, vedere 5.2.2). Calcprecisione Ulate come coefficiente di variazione (CV%).
- Considerare la precisione intra-day accettabile se rientra nella accettazione limita l'85% al 115% della concentrazione nominale. Considerare precisione intra-day accettabile se è uguale o migliore di un CV (coefficiente di varianza) del 15%.
- Calcola accuratezza e la precisione inter-giorno come la media per ogni livello di concentrazione QC analizzato nel corso dei 20 giorni di convalida.
- Considerare media accuratezza inter-giorno accettabile se rientra nella accettazione limita l'85% al 115% della concentrazione nominale. Considerare precisione inter-giorno accettabile se è uguale o migliore di un CV (coefficiente di varianza) del 15%.
- Esclusione di interferenze della matrice.
- Per l'esclusione di interferenze che possono essere causati da segnali a matrice, analizzare vuote macchie di sangue essiccato (8 differenti individui, preferibilmente 4 maschi e 4 femmine).
- Controllare visivamente cromatogrammi ionici. Se i picchi entro il tempo di ritenzionefinestra di tacrolimus vengono rilevati, integrare e confrontare le loro aree sotto la curva con quelle dei picchi di tacrolimus in campioni bianco arricchito con tacrolimus al LLOQ. L'area dei picchi nei campioni bianchi non dovrebbero superare il 15% di quelli di tacrolimus al LLOQ.
- Ion soppressione / valorizzazione di ioni.
- Utilizzare un protocollo di infusione post-colonna come descritto 45 per valutare la potenziale interferenza di valorizzazione ioni di soppressione / ioni causati da componenti della matrice coeluiti.
- Infondere tacrolimus ad una concentrazione di 10 ug / ml disciolti in 0,1% di acido formico: metanolo (30:70, v / v) post-colonna ad una velocità di 10 ml / min.
- Collegare una pompa a siringa con pezzo a T tra la colonna analitica e la sorgente electrospray dello spettrometro di massa.
- Monitorare l'intensità del segnale MS / MS delle transizioni MRM per tacrolimus ed il suo standard interno (m / z = 826,6 → 616,2 e m / z = 829,6 → 619,2) dopo l'iniezione di estrated campioni bianchi (n = 8 campioni provenienti da diversi individui).
Nota: In assenza di enhancement ione soppressione / ione del segnale continuo causato dalla infusione di analiti non deve essere influenzata mediante iniezione della matrice vuota, mentre soppressione ionica provoca un tuffo del segnale e ione enhancement un picco.
- Riporto.
- Valutare il potenziale riporto analizzando estratti campioni bianchi dopo i massimi calibratori (50 ng / ml, n = 6).
- Controllare visivamente cromatogrammi ionici. Se vengono rilevati picchi all'interno della finestra del tempo di ritenzione di tacrolimus, integrare e confrontare le loro aree sotto la curva con quelle dei picchi di tacrolimus in campioni bianco arricchito con tacrolimus al LLOQ. L'area dei picchi nei campioni bianchi non dovrebbero superare il 15% di quelli di tacrolimus al LLOQ.
- Recuperi estrazione.
- Determinare recuperi confrontando i segnali degli analiti dopo l'estrazione del QC samples a tutti e quattro i livelli di concentrazione (n = 6 per concentrazione) con quelli di vuoto macchie di sangue essiccato a spillo con i corrispondenti importi di tacrolimus dopo l'estrazione.
- Preparare quattro serie di QC (livelli di concentrazione: 2, 4, 20, 40 ng / ml).
- Preparare un altro 4 serie di corrispondenti "campioni di prova di ripristino" individuando 50 ml di sangue intero EDTA bianco sulle carte di carta filtro e asciugare per 2 ore.
- Hereafter, sia per il controllo di qualità e in bianco "campioni di prova di recupero", tagliare l'intera macchia di sangue sulla carta filtro con le forbici e inserire i dischi risultanti in un tubo di polipropilene con fondo conico e coperchio a scatto.
- Estrarre tutti i campioni.
- Trasferire il surnatante (400 microlitri) in fiale HPLC vetro.
- Aggiungere tacrolimus soluzione madre alle vuote "campioni di prova di recupero estratto" per raggiungere concentrazioni di 2, 4, 20 e 40 ng / ml (4 l di 200, 400, 2.000, 4.000 ng / ml tacrolimus magazzino solutions a 400 ml di surnatante).
- Dopo l'analisi LC-MS / MS, confrontare i segnali in entrambi i campioni QC e "campioni di prova di recupero" della corrispondente concentrazione (recupero% = campioni del segnale diluiti prima che i campioni di estrazione / segnale spillo dopo l'estrazione x 100).
- Integrità diluizione.
- Stabilire integrità diluizione utilizzando campioni addizionati di analiti a 500, 250 e 100 ng / ml.
- Dopo l'estrazione, diluire i campioni con soluzione proteica precipitazioni (1:10, n = 3 per livello di concentrazione).
- Calcolare deviazioni dalle concentrazioni nominali. Considerare i risultati che rientrano nel 85% -115% dei accettabili nominale.
- Stabilità.
- Indagare stabilità utilizzando i campioni QC a tutti e quattro i livelli di concentrazione (n = 4 per concentrazione) ha analizzato in diversi punti temporali e alle diverse condizioni di conservazione.
- Confrontare i risultati dopo l'immagazzinamento con i valori nominali. Considerare risultati che rientrano nel 85% -115% dei accettabili nominale.
- Stabilire stabilità campione per 1 settimana a temperatura ambiente, 1 settimana a 4 ° C, 1 mese a -20 ° C e 1 mese a -80 ° C.
- Test di stabilità di congelamento-scongelamento in tre cicli (-20 ° C). Prova campione estratto e stabilità campionatore automatico inserendo campioni nel campionatore automatico termostatato regolato a 4 ° C. Iniettare campioni dopo 72 ore.
Risultati
Cromatogrammi ionici rappresentativi di un campione in bianco, un campione addizionato al limite inferiore di quantificazione e un campione del paziente sono mostrati nella figura 3.
Le curve di calibrazione
Il limite inferiore di rilevamento era di 0,5 ng / ml e il limite inferiore di quantificazione è 1,0 ng / ml. Cinquanta ng / ml è stato scelto come il più alto calibratore come concentrazioni più elevate sono difficilmente raggiungibile in clinica in circostanze normali.
Le curve di calibrazione sono state preparate di fresco ogni giorno convalida in sangue umano intero EDTA, essiccati su schede filtra e estratti con metanolo / 0,2 M ZnSO4 (70:30 v / v) + standard interno (concentrazione finale di standard interno: 2,5 ng / ml ). Per la validazione giorno 1 (n = 6 per calibratori e n = 6 per il livello QC) e per i giorni 2 - 20 (n = 2 per calibratori e n = 4 per ciascun livello QC) sono stati analizzati con concentrazioni 1, 2,5, 5, 10, 25, 50 ng / ml per calibratori. Una curva di calibrazione tipica è mostrato in Figura 4. Media precisioni di 85% al 115% del valore nominale, nel campo di lavoro per 2/3 dei calibratori (con un minimo di 6 calibratori non zero) sono stati considerati accettabili. Il coefficiente medio di correlazione era (r) = 0,999 (n = 40 curve di calibrazione).
Precisioni e precisioni
I risultati sono mostrati in dettaglio nella Tabella 3.
Estrazione di recupero
Recuperi medi di estrazione erano 98,2% (2 ng / ml), 92,2 (4 ng / ml), 95,5 (20 ng / ml), 96,2 (40 ng / ml).
Matrix Interferenze, Ion Soppressione / Ion Enhancement Test con Infusione continua post-colonna e Riporto
L'analisi dei campioni bianchi da otto differenti individui (n = 4 femmine e maschi n = 4) ha mostrato segnali meno del 15% del LLOQ (1 ng / ml) al tempo di ritenzione corrispondente alpicco tacrolimus indica che il picco tacrolimus rilevata può essere considerata specifica. Un esempio rappresentativo è mostrato in figura 3. I potenziali interferenze da parte di ioni di soppressione / enhancement ioni sono stati testati utilizzando vuote campioni di sangue secche otto diversi individui sani. Un esperimento rappresentativo è mostrato in Figura 5. Non sono stati osservati segni di miglioramento significativo ione soppressione / ione. Non rilevante riporto conseguente picchi superiori al 15% del segnale LLOQ stati rilevati.
Diluizione Integrità
Integrità diluizione è stata studiata analizzando campioni preparati in concentrazioni superiori al calibratore più elevato (100, 250 e 500 ng / ml) e diluito 1:10 in soluzione precipitazione proteica dopo l'estrazione per raggiungere le concentrazioni target di: 10, 25, e 50 ng / ml. Precisioni medie hanno dovuto rientrare nei criteri di accettazione del 85% al 115% delle concentrazioni nominali. Tutte le diluizioni TESTed ha incontrato i criteri di accettazione (Tabella 4).
Stabilità
Stabilità di tacrolimus in macchie di sangue essiccato è stato studiato analizzando campioni QC a tutti i quattro livelli (n = 4 / livello di concentrazione), che sono stati conservati in condizioni variabili.
Precisioni medie hanno dovuto rientrare nei criteri di accettazione del 85% al 115% delle concentrazioni nominali. I risultati sono mostrati in dettaglio nella tabella 5. Nessuna perdita dopo il 1 ° settimana di conservazione a temperatura ambiente, dopo il 1 ° settimana di conservazione a 4 ° C, dopo il 1 ° mese di magazzinaggio a -20 ° C, dopo il 1 ° mese di magazzinaggio a -80 ° C, dopo i cicli di gelo e disgelo 3, e dopo 72 ore di campioni estratti in campionatore automatico a 4 ° C sono stati evidenti.
| Estrazione pompa | Analitica (eluizione) Pump | ||||||
| Tempo [min] | Acqua + 0,1% di acido formico | Acetonitrile | Portata [ul / min] | Tempo [min] | Acqua + 0,1% di acido formico | Acetonitrile | Portata [ul / min] |
| 0 | 70 | 30 | 5.000 | 0 | 13 | 87 | 1.000 |
| 1 | 70 | 30 | 5.000 | 2 | 2 | 98 | 1.200 |
| 1.1 | 2 | 98 | 100 | 3.5 | 2 | 98 | 1.200 |
| 3 | 2 | 98 | 100 | 3.6 | 13 | 87 | 1.000 |
| 3.1 | 20 | 80 | 2000 | 4.6 | 13 | 87 | 1.000 |
| 4 | 70 | 30 | 5.000 | ||||
| 4.6 | 70 | 30 | 5.000 | ||||
Tabella 1. Gradiente Programma per l'estrazione e analitica HPLC Pompe.
| Parametro | Ambiente |
| Gas Collision (CAD) | 10 |
| Gas Curtain (CUR) (psi) | 30 |
| Sorgente di ioni gas 1 (GS1) (psi) | 50 |
| Ion gas sorgente 2 (GS2) (psi) | 30 |
| Nebulizzatore corrente (NC) (V) | 1 |
| Temperatura (TEM) (° C) | 600 |
| IonSpray tensione (IS) (V) | 5500 |
| Riscaldatore dell'interfaccia (IHE) | In data |
| Declustering potenziale (DP) (V) | 136 |
| Ingresso potenziale (PE) (V) | 10 |
| Energia di collisione (CE) (V) | 47 |
| Collision potenziale uscita cella (CXP) (V) | 16 |
Tabella 2. Turbo Electrospray interfaccia e di massa spettrometro parametri. La nomenclatura corrisponde a quella utilizzata per il software spettrometria di massa (per i dettagli produttore, vedi Lista dei materiali).
| Giorno di convalida | QC Livello [% della concentrazione nominale] | |||
| 2 | 4 | 20 | 40 | |
| Giorno 1 | 93.0 | 86.3 | 88.9 | 93.4 |
| 101 | 90.4 | 95.3 | 100 | |
| 85.6 | 95.9 | 99.0 | 97,5 | |
| 88,6 | 93.6 | 105 | 103 | |
| 85.0 | 97.4 | 97,2 | 109 | |
| 89.1 | 96.7 | 100 | 101 | |
| Intra-day Accuracy [%] | 90.4 | 93.4 | 97.6 | 100.7 |
| Intra-Day Imprecisione [CV%] | 6.6 | 4.6 | 5.5 | 5.2 |
| Giorno 2 | 92.8 | 86.0 | 103 | 95.4 |
| 91.1 | 88.8 | 94,7 | 87.0 | |
| 88,6 | 90.9 | 92.8 | 94,2 | |
| 97,2 | 93,7 | 94,2 | 115 | |
| Intra-day Accuracy [%] | 92.4 | 89.9 | 96.2 | 97,9 |
| Intra-Day Imprecisione [CV%] | 3.9 | 3.6 | 4.8 | 12.2 |
| 3 ° giorno | 97.6 | 101 | 98.4 | 112 |
| 104 | 85.6 | 102 | 110 | |
| 99,2 | 88.4 | 99,4 | 105 | |
| 96,3 | 87.2 | 108 | 117 | |
| Intra-day Accuracy [%] | 99.3 | 90.6 | 102.0 | 111.0 |
| Intra-Day Imprecisione [CV%] | 3.4 | 7.8 | 4.2 | 4.5 |
| Giorno 4 | 95.2 | 88,6 | 112 | 94.5 |
| 105 | 87.3 | 93.2 | 116 | |
| 99,8 | 96.2 | 103 | 103 | |
| 100 | 104 | 97,2 | 99,4 | |
| Intra-day Accuracy [%] | 100.0 | 94.0 | 101.4 | 103.2 |
| Intra-Day Imprecisione [CV%] | 4.0 | 8.2 | 8.1 | 8.9 |
| 5 ° giorno | 106 | 90.4 | 101 | 106 |
| 108 | 89.0 | 106 | 100 | |
| 102 | 101 | 96.6 | 128 | |
| 105 | 88.8 | 105 | 107 | |
| Intra-day Accuracy [%] | 105.3 | 92.3 | 102.2 | 110.3 |
| Intra-Day Imprecisione [CV%] | 2.4 | 6.3 | 4.2 | 11.1 |
| Giorno 6 | 90.9 | 93,7 | 119 | 106 |
| 98,8 | 88.1 | 96,4 | 110 | |
| 94.6 | 96,3 | 99.1 | 108 | |
| 108 | 100 | 102 | 102 | |
| Intra-day Accuracy [%] | 98.1 | 94.5 | 104.1 | 106.5 |
| Intra Day-Imprecisione [CV%] | 7.5 | 5.3 | 9.8 | 3.2 |
| Giorno 7 | 85.1 | 87.5 | 99,5 | 95.4 |
| 86.4 | 85.4 | 94,7 | 101 | |
| 94.5 | 87.3 | 98.9 | 94.6 | |
| 85.5 | 97.0 | 101 | 99,6 | |
| Intra-day Accuracy [%] | 87,9 | 89.3 | 98,5 | 97,7 |
| Intra-Day Imprecisione [CV%] | 5.1 | 5.8 | 2.7 | 3.2 |
| Giorno 8 | 86.1 | 92.5 | 91.9 | 102 |
| 87.5 | 91.5 | 95.2 | 88.5 | |
| 115 | 85.6 | 92.1 | 102 | |
| 85.8 | 85,9 | 95.4 | 108 | |
| Intra-day Accuracy [%] | 93.6 | 88.9 | 93,7 | 100.1 |
| Intra-Day Imprecisione [CV%] | 15.3 | 4.1 | 2.0 | 8.2 |
| Giorno 9 | 88.9 | 91,4 | 96.9 | 100 |
| 90.0 | 89.8 | 95.0 | 100 | |
| 69.7 | 85,9 | 95,8 | 109 | |
| 91.9 | 87.0 | 105 | 101 | |
| Intra-day Accuracy [%] | 85.1 | 88.5 | 98,2 | 102.5 |
| Intra Day-Imprecisione [CV%] | 12.2 | 2.9 | 4.7 | 4.3 |
| Giorno 10 | 90.9 | 91.3 | 96.2 | 100 |
| 97,7 | 89.5 | 94,4 | 100 | |
| 99,9 | 109 | 98,7 | 96,8 | |
| 99.1 | 90.0 | 95.7 | 96.1 | |
| Intra-day Accuracy [%] | 96.9 | 95.0 | 96,3 | 98,2 |
| Intra-Day Imprecisione [CV%] | 4.2 | 9.9 | 1.9 | 2.1 |
| Giorno 11 | 92.7 | 91.9 | 88.2 | 104 |
| 96.6 | 91.2 | 97.0 | 110 | |
| 109.0 | 92.8 | 970,6 | 102 | |
| 98.3 | 107 | 93,7 | 111 | |
| Intra-day Accuracy [%] | 99,2 | 95.7 | 94.1 | 106.8 |
| Intra-Day Imprecisione [CV%] | 7.0 | 7.9 | 4.6 | 4.1 |
| Giorno 12 | 87,7 | 85.5 | 105 | 95.3 |
| 112 | 88.1 | 101 | 96.1 | |
| 102 | 89.1 | 89.7 | 97,5 | |
| 106 | 92.5 | 102 | 104 | |
| Intra-day Accuracy [%] | 101.9 | 88.8 | 99,4 | 98,2 |
| Intra-Day Imprecisione [CV%] | 10.1 | 3.3 | 6.7 | 4.0 |
| Giorno 13 | Impossibile | 85,7 | 93.3 | 102 |
| 101 | 105 | 88.0 | 93.9 | |
| 112 | 98.0 | 91,4 | 102 | |
| 104 | 113 | 104 | 101 | |
| Intra-day Accuracy [%] | 105.7 | 100,4 | 94,2 | 99,7 |
| Intra-Day Imprecisione [CV%] | 5.4 | 11.5 | 7.3 | 3.9 |
| Giorno 14 | 91.5 | 89.1 | 97.4 | 93.1 |
| 90.4 | 87.1 | 93.9 | 99,8 | |
| 89.7 | 97.0 | 94,8 | 106 | |
| 97.4 | 86,8 | 89.9 | Impossibile | |
| Intra-day Accuracy [%] | 92.3 | 90.0 | 94.0 | 99,6 |
| Intra-Day Imprecisione [CV%] | 3.8 | 5.3 | 3.3 | 6.5 |
| Giorno 15 | 92.8 | 92.8 | 92.5 | 95.4 |
| 97,5 | 96,3 | 96.2 | 95.5 | |
| 95.5 | 108 | 97.3 | 99.3 | |
| 110 | 109 | 115 | 113 | |
| Intra-day Accuracy [%] | 99.0 | 101.5 | 100.3 | 100,8 |
| Intra-Day Imprecisione [CV%] | 7.7 | 8.1 | 10.0 | 8.3 |
| Giorno 16 | 93,7 | 97,8 | 90.7 | 112 |
| 90.3 | 87.1 | Impossibile | 101 | |
| 97,9 | 88.3 | 95.5 | 107 | |
| 91,4 | 85,7 | 89.3 | 96.7 | |
| Intra-day Accuracy [%] | 93.3 | 89.7 | 91.8 | 104,2 |
| Intra-Day Imprecisione [CV%] | 3.6 | 6.1 | 3.5 | 6.4 |
| Giorno 17 | 88.0 | 86.0 | 93,7 | 103 |
| 89.8 | 90.8 | 94,8 | 93.2 | |
| 85,9 | 91.1 | 99,7 | 94,8 | |
| 86.7 | 88.1 | 95.6 | 91.7 | |
| Intra-day Accuracy [%] | 87.6 | 89.0 | 96.0 | 95.7 |
| Intra-Day Imprecisione [CV%] | 1.9 | 2.7 | 2.7 | 5.3 |
| Giorno 18 | 89.6 | 85.8 | 91.0 | 98.3 |
| 89.6 | 86.2 | 88.3 | 93.6 | |
| Impossibile | 86.7 | 96,8 | 104 | |
| 88.1 | 85.8 | 95.2 | 111 | |
| Intra-day Accuracy [%] | 89.1 | 86.1 | 92.8 | 101.7 |
| Intra-Day Imprecisione [CV%] | 1.0 | 0.5 | 4.2 | 7.4 |
| Giorno 19 | 98.0 | 89.7 | 94,2 | 102 |
| 88.3 | 86.0 | 97.6 | 102 | |
| 91.6 | 88.1 | 95,8 | 97,5 | |
| 90.7 | 90.1 | 92.8 | 88.3 | |
| Intra-day Accuracy [%] | 92.2 | 88.5 | 95.1 | 97,5 |
| Intra-Day Imprecisione [CV%] | 4.5 | 2.1 | 2.2 | 6.6 |
| Giorno 20 | 93.0 | 87.0 | 99,4 | 101 |
| 97.3 | 87.6 | 95.5 | 91.9 | |
| 89.0 | 88.4 | 91.2 | 93.5 | |
| 104 | 90.7 | 97,7 | 115 | |
| Intra-day Precisione[%] | 95,8 | 88.4 | 96.0 | 100,4 |
| Intra-Day Imprecisione [CV%] | 6.7 | 1.8 | 3.7 | 10.5 |
Precisione Inter-Day e Imprecisione | ||||
| Inter-giorno Precisione | 95.2 | 91.7 | 97,2 | 101.6 |
| Inter-Day Imprecisione | 6.1 | 4.5 | 3.6 | 4.2 |
Tabella 3. Risultati dei campioni di controllo di qualità da oltre 20 giorni. I dati sono presentati come% del valore nominale. I campioni elencati come "non riuscito" sono campioni che sono stati persi per errori di laboratorio / strumentali. Nella maggior parte dei cases, senza picchi sono stati rilevati a tutti o il picco dello standard interno mancava.
| Diluizione | 01:10 |
| Concentrazione target nominale dopo diluizione | 50 ng / ml |
| 98.6 | |
| 94.5 | |
| 91,4 | |
| Precisione [%] | 94,8 |
| Imprecisione [CV%] | 3.6 |
| Diluizione | 01:10 |
| Concentrazione target nominale dopo diluizione | 10 ng / ml |
| 103 | |
| 99,5 | |
| 101 | |
| Precisione [%] | 101.2 |
| Imprecisione [CV%] | 1.8 |
| Diluizione | 01:10 |
| Concentrazione target nominale dopo diluizione | 25 ng / ml |
| 91.7 | |
| 98,2 | |
| 103 | |
| Precisione [%] | 97.6 |
| Imprecisione [CV%] | 5.7 |
Tabella 4. I risultati di diluizione Verifica integrità. I dati sono presentati come% del valore nominale.
| La | ||||
| Stabilità a RT, Giorno 1 | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 91.9 | 85.8 | 86.0 | 102 | |
| 86.7 | 85,7 | 88.5 | 102 | |
| 86.0 | 85,9 | 90.1 | 103 | |
| 89.2 | 98.0 | 90.8 | 112 | |
| % Della concentrazione nominale | 88.5 | 88.9 | 88.9 | 104.8 |
| Imprecisione [% CV] | 2.7 | 6.1 | 2.1 | 4.9 |
| Stabilità a RT, 3ª giornata | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 88,6 | 105 | 101 | 113 | |
| 94.1 | 100 | 98,5 | 103 | |
| 100 | 101 | 106 | 109 | |
| 99,5 | 102 | 102 | 108 | |
| % Della concentrazione nominale | 95.6 | 102.0 | 101.9 | 108,3 |
| Imprecisione [% CV] | 5.3 | 2.2 | 3.1 | 4.1 |
| Stabilità a RT, 7ª giornata | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 105 | 103 | 91.7 | 109 | |
| 101 | 107 | 100 | 110 | |
| 102 | 108 | 107 | 105 | |
| 93.8 | 105 | 109 | 111 | |
| % Della concentrazione nominale | 100.5 | 105.8 | 101.9 | 108,8 |
| Imprecisione [% CV] | 4.7 | 2.2 | 7.8 | 2.6 |
| B | ||||
| Stabilità a 4 ° C, Giorno 1 | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 101 | 89.9 | 95,8 | 100 | |
| 88.9 | 91.0 | 94.1 | 99.0 | |
| 96.2 | 100 | 102 | 96.7 | |
| 89.5 | 87.8 | 95.4 | 88,6 | |
| % Della concentrazione nominale | 93.9 | 92.2 | 96,8 | 96.1 |
| Imprecisione [% CV] | 5.8 | 5.4 | 3.5 | 5.2 |
| Stabilità a 4 ° C, 3ª giornata | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 87.3 | 85.2 | 105 | 95.3 | |
| Impossibile | 87.8 | 101 | 96 | |
| 101 | 88.8 | 89.6 | 97,5 | |
| 106 | 92.2 | 102 | 104 | |
| % Della concentrazione nominale | 98.1 | 88.5 | 99,4 | 98,2 |
| Imprecisione [% CV] | 9.7 | 2.9 | 6.8 | 4.0 |
| Stabilità a 4 ° C, 7 ° giorno | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 94.0 | 98,5 | 96.1 | 110 | |
| 92.9 | 96,4 | 109 | 109 | |
| 91.7 | 96,3 | 97,9 | 115 | |
| 94,7 | 96.9 | 99,8 | 113 | |
| % Della concentrazione nominale | 93.3 | 97.0 | 100.7 | 111.8 |
| Imprecisione[%CV] | 1.3 | 1.0 | 5.7 | 2.8 |
| C | ||||
| Stabilità a -20 ° C, 3ª giornata | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 87.3 | 98,7 | 111 | 111 | |
| 93.5 | 89.6 | 108 | 105 | |
| 89.5 | 91.5 | 107 | 112 | |
| 88.2 | 99.1 | 108 | 92.4 | |
| % Della concentrazione nominale | 89.6 | 94,7 | 108,5 | 105.1 |
| Imprecisione [% CV] | 2.7 | 4.9 | 1.7 | 9.0 |
| Stabilità a -20 ° C, 7 ° giorno | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 96,5 | 98,7 | 102 | 109 | |
| 94,8 | 94.6 | 114 | 106 | |
| 95.5 | 102 | 98.1 | 108 | |
| 107 | 99,5 | 115 | 105 | |
| % Della concentrazione nominale | 98,5 | 98,7 | 107.3 | 107 |
| Imprecisione [% CV] | 5.7 | 3.1 | 8.5 | 1.8 |
| Stabilità a -20 ° C, Giorno 30 | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 82,3 | 83.1 | 90.4 | 93.2 | |
| 87,9 | 85.8 | 85.3 | 97,9 | |
| 85,7 | 88,6 | 98.3 | 98.0 | |
| 92.0 | 95.6 | 110 | 103 | |
| % Della concentrazione nominale | 87.0 | 88.3 | 96.0 | 98.0 |
| Imprecisione [% CV] | 4.1 | 5.4 | 10.8 | 4.0 |
| D | ||||
| Stabilità a -80 ° C, 3ª giornata | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 87.5 | 96,5 | 96.7 | Impossibile | |
| Impossibile | 97.6 | 98,7 | 110 | |
| 88.8 | 96,4 | 106 | 109 | |
| 87.3 | 101 | 96,5 | 109 | |
| % Della concentrazione nominale | 87,9 | 97,9 | 99,5 | 109,3 |
| Imprecisione [% CV] | 0.8 | 2.2 | 4.5 | 0.6 |
| Stabilità a -80 ° C, 7 ° giorno | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| Impossibile | 98.0 | 105 | 99,8 | |
| 97,1 | 106 | 104 | 105 | |
| 99,7 | 102 | 99.3 | 102 | |
| 101 | 99,9 | 109 | 106 | |
| % Della concentrazione nominale | 99.3 | 101.5 | 104.3 | 103.2 |
| Imprecisione [% CV] | 2.0 | 3.4 | 4.0 | 2.8 |
| Stabilità a -80 ° C, Giorno 30 | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 88.2 | 85.3 | 89.6 | 96.7 | |
| 96.2 | 92.6 | 85.8 | 94.1 | |
| 83.9 | 93,7 | 91.0 | 105 | |
| 95.6 | 94.0 | 98.9 | 102 | |
| % Della concentrazione nominale | 91.0 | 91,4 | 91.3 | 99,5 |
| Imprecisione [% CV] | 6.0 | 4.1 | 5.5 | 4.9 |
| E | ||||
| Fermo stabilità disgelo, -20 ° C, 1 ciclo | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 92.5 | 86.2 | 90.2 | 94.3 | |
| 89.8 | 90.5 | 85.4 | 104 | |
| 94,7 | 88,6 | 93.4 | 104 | |
| 101 | 89.2 | 93,7 | 96,3 | |
| % Della concentrazione nominale | 94.5 | 88,6 | 90.7 | 99,7 |
| Imprecisione [% CV] | 4.8 | 1.8 | 3.9 | 5.1 |
| Congelare disgelo stabilità, -20 ° C, 2 cicli | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 99.1 | 97.6 | Impossibile | 85.3 | |
| 93.1 | 88.1 | 93.4 | 92.0 | |
| 94.9 | 91.5 | 85.8 | 93.9 | |
| Impossibile | 90.5 | 86,8 | 85.4 | |
| % Della concentrazione nominale | 95.7 | 91.9 | 88,7 | 89.2 |
| Imprecisione [% CV] | 3.1 | 4.0 | 4.1 | 4.5 |
| Congelare disgelo stabilità, -20 ° C, 3 cicli | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 95.7 | Impossibile | 86.0 | 93.3 | |
| 95.5 | 87.4 | 85.0 | 91.3 | |
| 90.5 | 89.1 | 86.0 | 86.0 | |
| 96.9 | 85,7 | 90.2 | Impossibile | |
| % Della concentrazione nominale | 94,7 | 87.4 | 86,8 | 90.2 |
| Imprecisione [% CV] | 2.8 | 1.7 | 2.3 | 3.8 |
| F | ||||
| Stabilità campione estratto a +4 ° C, 24 ore | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 122 | 112 | 91.0 | 104 | |
| 93.5 | 106 | 91.8 | 96.1 | |
| 111 | 94,8 | 98,2 | 93.5 | |
| 98.4 | 97.6 | 91.3 | 89.8 | |
| % Della concentrazione nominale | 106,2 | 102.6 | 93.1 | 95.9 |
| Imprecisione [% CV] | 12.8 | 7.9 | 3.4 | 6.0 |
| Stabilità campione estratto a +4 ° C, 48 ore | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 106 | 108 | 93,7 | 110 | |
| 105 | 98.1 | 94.6 | 98.9 | |
| 103 | 98.4 | 95.0 | 92.6 | |
| 108 | 93.1 | 89.7 | 85.5 | |
| % Della concentrazione nominale | 105.5 | 99,4 | 93.3 | 96,8 |
| Imprecisione [% CV] | 2.1 | 6.2 | 2.4 | 10.4 |
| Stabilità campione estratto a +4 ° C, 72 ore | ||||
| Livello di controllo qualità [ng / ml] | 2 | 4 | 20 | 40 |
| 96,5 | 112 | 96,4 | 104 | |
| 101 | 95.3 | 103 | 95.2 | |
| 94,2 | 105 | 93.5 | 99,5 | |
| 100 | 96.9 | 92.6 | 89.3 | |
| % Della concentrazione nominale | 97,9 | 102.3 | 96,4 | 97.0 |
| Imprecisione [% CV] | 3.1 | 7.7 | 4.7 | 6.3 |
Tabella 5. Risultati dei test di stabilità. R: La stabilità di tacrolimus sulle macchie di sangue essiccato a temperatura ambiente per 7 giorni, B: Stabilità di tacrolimus sulle macchie secche di sangue in frigorifero (4 ° C) oltre 7 giorni, C: Stabilità di tacrolimus sulle macchie di sangue essiccato a -20 ° C oltre 1 mese, D: Stabilità di tacrolimus sulle macchie di sangue essiccato a -80 ° C oltre 1 mese, E: Stabilità di tacrolimus sulle macchie di sangue essiccato su tre cicli di gelo-disgelo (-20 ° C), F : Estratto campione stabilità / campionatore automatico a 4 ° C per 72 ore. I dati sono presentati come% della concentrazione nominale. I campioni elencati come "non riuscito" sono campioni che sono stati persi per errori di laboratorio / strumentali. Nella maggior parte dei casi sono stati rilevati picchi a tutti o il picco dello standard interno mancava.

Figura 1. Struttura di Tacrolimus. Numerazione Atom segue l'Unione internazionale di nomenclatura chimica pura e applicata (IUPAC). Clicca qui per vedere una versione più grande di questa figura.

Figura 2. Collegamento della valvola di commutazione.424fig2large.jpg "target =" _ blank "> Clicca qui per vedere una versione più grande di questa figura.
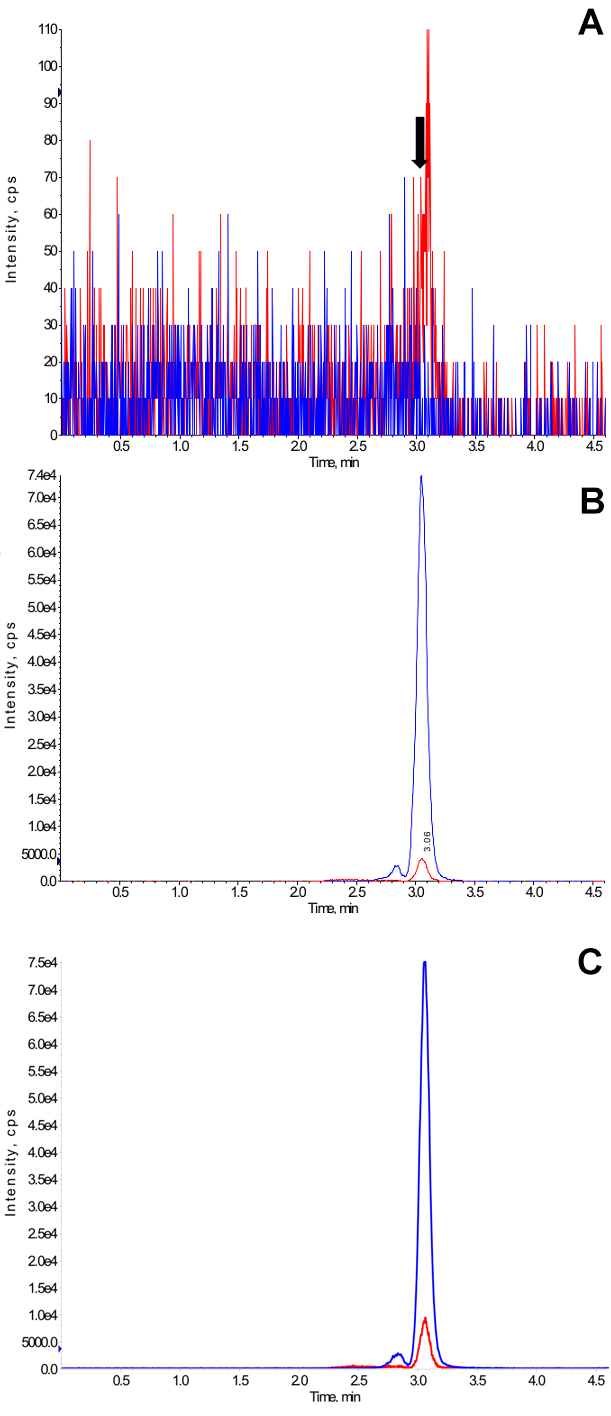
Figura 3. Rappresentante cromatogrammi Ion. (A) Rappresentante cromatogramma ionico di un vuoto campioni di sangue macchiato su carta da filtro (per i dettagli produttore, vedere Lista dei materiali) ed essiccato. La freccia indica il tempo di ritenzione del picco tacrolimus, (B) Rappresentante cromatogramma ionico di sangue vuoto campioni addizionati al limite inferiore di quantificazione (1 ng / ml) individuato sulla carta da filtro ed essiccato, e (C) Rappresentante cromatogramma ionico di un campione prelevato da un paziente con trapianto su carta da filtro. Questo è un esempio di valle e la concentrazione misurata tacrolimus era 2,1 ng / ml. Questo campione è stato raccolto dal paziente a casa ed è da uno studio clinico che era approvato con l'Università di Cincinnati Institutional Review Board (Cincinnati, OH). Tutti i pazienti hanno dato il loro adeguato consenso scritto. Cromatogrammi ionici sono stampe originali generati dal software spettrometria di massa (per i dettagli produttore, vedere Materiali List). Linee blu e rosse in cromatogrammi ionici rappresentano lo standard D interno 2, 13 C-tacrolimus e tacrolimus, rispettivamente. Il picco eluizione di fronte al tacrolimus principale e dello standard interno sono i rotameri. Clicca qui per vedere una versione più grande di questa figura.

Figura 4. Rappresentante curva di calibrazione. In seguito si propone stamparla originale generato dal software di spettrometria di massa.424 / 52424fig4large.jpg "target =" _ blank "> Clicca qui per vedere una versione più grande di questa figura.
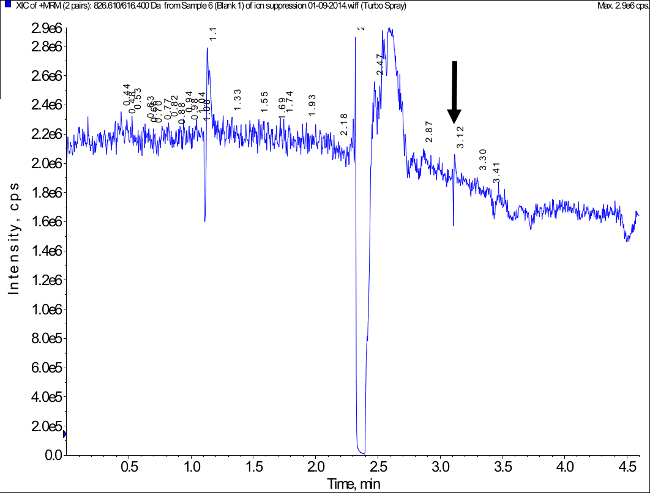
Figura 5. Rappresentante Ion Cromatogramma misurato durante post-colonna infusione di Tacrolimus e iniezione di un campione di sangue in bianco Estratto di valutare un potenziale effetto Matrix (Ion Soppressione / Ion Enhancement). La freccia indica il tempo di ritenzione del picco tacrolimus. Test effetto Matrix era basata sulla procedura descritta in 46. Non matrice rilevante è stato rilevato effetto. Clicca qui per vedere una versione più grande di questa figura.
Discussione
Anche se, come detto, il concetto di farmaco terapeutico e monitoraggio aderenza tacrolimus basato su macchie di sangue essiccato è attraente, ci sono sfide analitiche che vanno oltre quelli tipicamente associati con l'analisi LC-MS / MS di tacrolimus in EDTA venosa campioni di sangue intero. Questi includono, ma non sono limitati a, il fatto che la matrice è sangue intero capillare imbevuto nel materiale linters di cotone del materiale carta filtro usato qui e il volume di sangue (20 ml). Tuttavia, l'analisi ad alta produttività in un laboratorio centrale richiede un metodo veloce e affidabile di estrazione che si traduce in campioni che mancano interferenze matrice e gli effetti matrice in combinazione con un robusto, specifico e altamente sensibile test LC-MS / MS. L'affidabilità del saggio è critica come di solito non è sufficiente materiale sulla carta filtro già perforato lasciato per rianalisi in caso di estrazione / analisi LC-MS / MS fallisce.
Il ficarte ltro utilizzati nel presente studio (per i dettagli produttore, si rimanda Lista dei materiali) sono stati scelti come questi sono un dispositivo approvato dalla FDA classe II, sono conformi alle linee guida NCCLS LA4-A5 44 e si trovano in Europa con marchio CE. Se completamente riempito, un cerchio sulla carta filtro Whatman 903 detiene ≈50 ml di sangue 46. Tuttavia, la dimensione delle gocce di sangue prelevati da singoli pazienti variano e la formazione nella tecnica di campionamento adeguata è essenziale 46.
Il primo importante passo di estrazione di un out perforata campione essiccato macchia di sangue è di omogeneizzazione. Sulla base della nostra esperienza, l'uso di un miscelatore proiettile è più efficiente e più riproducibile rispetto ad altri metodi usati per migliorare l'efficienza di estrazione come sonicazione. L'uso del miscelatore proiettile era essenziale per ottenere sempre recuperi estrazione superiore al 90%. Per l'affidabilità della procedura di estrazione, è stato anche importante garantire che tutte le centrifughe sono stati temperatcontrollata ure (4 ° C) e che il passo vortex non era più breve di 10 minuti, che ha provocato recuperi di estrazione più variabili e inferiore. Inoltre, è importante che il rapporto metanolo / ZnSO4 non viene alterato come recupero tacrolimus è molto sensibile alla corretta composizione della soluzione di precipitazione delle proteine.
La prossima sfida è quella di ottenere un estratto pulito idealmente privi di materiali che possono causare interferenze a matrice ed effetti. Così, un semplice passo-passo come la precipitazione delle proteine spesso utilizzato per l'estrazione di tacrolimus da campioni di sangue EDTA non è stata considerata una valida opzione. Dopo la precipitazione di proteine usando ZnSO4 (inclusa l'aggiunta di uno standard interno isotopo marcato), vortex e centrifugazione, i sovranatanti sono stati iniettati in un sistema HPLC 2D e su una colonna di estrazione in linea. Estrazione colonna Online utilizzando elevati flussi di 5 ml / min a cartucce precolonna convenzionali utilizzando una semplice 6 portevalvola di commutazione per l'analisi di tacrolimus sono stati descritti prima 47. La fase mobile è stato scelto in modo che tacrolimus e il suo standard interno concentrati nella parte anteriore della colonna di estrazione e non migrano sopra la colonna durante la sottofase di cancellazione. L'estrazione linea utilizzato nel presente protocollo ha diversi vantaggi tra cui l'iniezione di relativamente grandi volumi di campione senza influenzare negativamente l'analisi HPLC. Il back-flush dopo arricchire gli analiti in cima alla colonna di estrazione ("peak focusing") ha comportato picchi più consentendo un'integrazione più affidabile dall'algoritmo software in particolare per campioni con concentrazioni di tacrolimus basse. 48 Il passo di pulitura linea non solo rimuovere potenzialmente interferenti composti a matrice, ma anche de-salato del campione. Un problema importante ma raramente discusso per grandi volumi, high throughput LC-MS / MS saggi è la graduale perdita di sensibilità del sistema LC-MS / MS a causa della crescentela contaminazione della sorgente electrospray durante l'analisi di grandi lotti. Non sono stati osservati effetti della matrice significativi (ioni di aumento di soppressione / ioni). L'effetto negativo dei potenziali effetti della matrice sono stati ridotti / evitato combinazione dei seguenti elementi: efficace precipitazione proteina utilizzando metanolo / ZnSO4, centrifugazione dopo precipitazione delle proteine a 16.000 xg, di estrazione ad alto flusso in linea, netta separazione cromatografica di tacrolimus da potenziali interferenze presto eluizione dalla colonna analitica e l'uso di tacrolimus marcati con isotopi come standard interno anziché standard interni strutturalmente correlati, come ascomycin.
Il limite inferiore di quantificazione è 1 ng / ml, e quindi inferiore a quella della maggior parte immunodosaggi che sono attualmente spesso utilizzato per monitoraggio terapeutico di tacrolimus in campioni di sangue EDTA. Questo limite inferiore di quantificazione è sufficiente anche per i cosiddetti inibitori della calcineurina basso immunosuppres a lungo termineprotocolli di manutenzione sive.
Rispetto ai precedentemente descritti test LC-MS / MS per la quantificazione tacrolimus nel Bloods secchi macchie 29-34,36,39,41,42, gli attuali incontri di analisi o supera le loro prestazioni in termini di limite inferiore di quantificazione, il recupero di estrazione, accuratezza e precisione, evitando concetti potenzialmente rischiose come il one-step procedure proteine precipitazioni e tempi cromatografia ultra-short, che di solito danno risultati accettabili durante la convalida sulla base campioni di sangue di individui sani. Tuttavia, i pazienti trapiantati hanno un gruppo molto complesso di pazienti che hanno malattie che colpiscono la composizione del sangue e che assumono più farmaci. Questo rende praticamente impossibile escludere tutte le interferenze potenziali che possono essere presenti nei singoli pazienti durante la convalida e l'unica strategia possibile è quella di impostare il test in un modo che riduce al minimo il rischio di tali potenziali interferenze. Dried spo sanguets hanno problemi come l'effetto del ematocrito sulla viscosità del sangue e così le proprietà di diffusione del sangue applicato su carta da filtro 49. Questo non è stato testato di nuovo qui come tali effetti sono già stati descritti non incidere analisi tacrolimus in macchie di sangue essiccato a ematocrito e le concentrazioni di tacrolimus entro limiti ragionevoli clinicamente 29,32. Inoltre la stabilità di tacrolimus in macchie di sangue essiccato a temperature elevate è già stato studiato da altri e tacrolimus in macchie di sangue essiccato è risultato essere stabile per 5 giorni a 37 ° C e anche 60 ° C 32, che è importante per la spedizione di sangue secco spot in condizioni non a temperatura controllata soprattutto in estate.
Questo saggio basato su una combinazione di proiettile frullatore omogeneizzazione, alta flusso della colonna linea di pulitura e l'analisi LC-MS / MS può fornire una strategia di piattaforma per lo sviluppo di saggi bioanalitici per la quantificazione di altri immunosuppressants, da soli o simultanei, così come di altri farmaci in campioni macchia di sangue secco.
Divulgazioni
The authors have nothing to disclose.
Riconoscimenti
This work was supported by the United States Federal Drug Administration (FDA) contract HHSF223201310224C and the United States National Institutes of Health/FDA grant 1U01FD004573-01.
Materiali
| Name | Company | Catalog Number | Comments |
| Tacrolimus | U.S. Pharmacopeial Convention | 1642802 | |
| D2,13C-Tacrolimus | Toronto Research Chemicals Inc. | F370002 | |
| Red blood cells | University of Colorado Hospital | W20091305500 V | |
| Plasma | University of Colorado Hospital | W2017130556300Q | |
| Acetone CHROMASOLV, HPLC, ≥99,9% | Sigma-Aldrich | 439126-4 L | |
| Acetonitrile Optima LC/MS, UHPLC-UV | Thermo Fisher Scientific | A955-4 | |
| Isopropanol 99.9%, HPLC | Fisher Scientific | BP2632-4 | |
| Methanol Optima LC/MS | Thermo Fisher Scientific | A452-4 | |
| Water Optima LC/MS, UHPLC-UV | Thermo Fisher Scientific | W6-4 | |
| Formic acid | Thermo Fisher Scientific | A118P-500 | |
| Phosphate-buffered saline (PBS) | Sigma-Aldrich | D8537 | |
| Zinc sulfate | Thermo Fisher Scientific | Z68-500 | |
| 0.5 – 10 µl pipet, VoluMate LIQUISYSTEMS | Mettler Toledo | 17008649 | |
| 1.5 ml Eppendorf tube | Thermo Fisher Scientific | 02-682-550 | |
| 10 – 100 µl pipet, VoluMate LIQUISYSTEMS | Mettler Toledo | 17008651 | |
| 10 μl pipet tips with filter, sterile | Neptune | BT 10XLS3 | |
| 100 – 1,000 µl pipet, VoluMate LIQUISYSTEMS | Mettler Toledo | 17008653 | |
| 100 μl pipet tips with filter, sterile | Neptune | BT 100 | |
| 1,000 μl pipet tips with filter, sterile | Multimax | 2940 | |
| 2 – 20 µl pipet, VoluMate LIQUISYSTEMS | Mettler Toledo | 17008650 | |
| 2 ml Eppendorf tube | Thermo Fisher Scientific | 02-681-258 | |
| 20 – 200 µl pipet, VoluMate LIQUISYSTEMS | Mettler Toledo | 17008652 | |
| 20 μl pipet tips with filter, sterile | GeneMate | P-1237-20 | |
| 200 μl pipet tips with filter | Multimax | 2938T | |
| 200 μl pipet tips with filter, sterile | Multimax | 2936J | |
| 50 ml Falcon tube | BD Falcon | 352070 | |
| 300 μl inserts for HPLC vials | Phenomenex | ARO-9973-13 | |
| Balance PR2002 | Mettler Toledo | 1117050723 | |
| Balances AX205 Delta Range | Mettler Toledo | 1119343379 | |
| Bullet Blender Homogenizer | Next Advance | BBX24 | |
| Centrifuge Biofuge Fresco | Heraeus | 290395 | |
| Disposable Wipes | PDI | Q55172 | |
| Glass v ials, 4 ml | Thermo Fisher Scientific | 14-955-334 | |
| Glass vials, 20 ml | Thermo Fisher Scientific | B7800-20 | |
| Gloves, nitrile | Titan Brand Gloves | 44-100S | |
| HPLC vials, 9 mm, 2 ml, clear | Phenomenex | ARO- 9921-13 | |
| Lids for HPLC vials | Phenomenex | ARO- 8952-13-B | |
| Needle, 18 G 1.5 | Precision Glide | 305196 | |
| Rack for Eppendorf tubes | Thermo Fisher Scientific | 03-448-11 | |
| Rack for HPLC Vials | Thermo Fisher Scientific | 05-541-29 | |
| Steel beads 0.9 – 2 mm | Next Advance | SSB14B | |
| Storage boxes for freezers / refrigerators | Thermo Fisher Scientific | 03-395-464 | |
| Standard multi-tube vortexer | VWR Scientific Products | 658816-115 | |
| Whatman Paper, 903 Protein Saver US 100/PK | GE Whatman | 2016-05 | |
| Autosampler | CTC PAL | PAL.HTCABIx1 | |
| Binary pump, Agilent 1260 Infinity | Agilent Technologies | 1260 G1312B | |
| Binary pump, Agilent 1290 Infinity | Agilent Technologies | 1290 G4220A | |
| Micro vacuum degasser, Agilent 1260 | Agilent Technologies | 1260 G13798 | |
| Column oven, Agilent 1290 with 2 position | Agilent Technologies | 1290 G1216C | |
| Thermostated column compartment with integrated 6 port switching valve | Agilent Technologies | 1290 G1316C | |
| HPLC pre-column cartridge, Zorbax XDB C8 (5 µm particle size), 4.6 · 12.5 mm | Phenomenex | 820950-926 | |
| HPLC analytical column, Zorbax Eclipse-XDB-C8 (5 µm particle size), 4.6 · 150 mm | Phenomenex | 993967-906 | |
| Tandem Mass Spectrometer | |||
| API5000 MS/MS with TurboIonspray source | AB Sciex | 4364257 | |
| Mass spectrometry software | AB Sciex | Analyst 1.5.1 |
Riferimenti
- Goto, T., et al. Discovery of FK506, a novel immunosuppressant isolated from Streptomyces Tsukubaensis. Transplant Proc. 19 (5 Suppl 6), 4-8 (1987).
- Kino, T., Hatanaka, H., Miyata, S. FK506, a novel immunosuppressant isolated from a streptomyces. I: Fermentation, isolation and physico-chemical and biological characteristics. J. Antibiotics. 40 (9), 1249-1255 (1987).
- Starzl, T. E., et al. FK506 for liver, kidney and pancreas transplantation. Lancet. 2 (8670), 1000-1004 (1989).
- . Randomised trial comparing tacrolimus (FK506) and cyclosporin in prevention of liver allograft rejection. European FK506 Multicentre Liver Study Group. Lancet. 344 (8920), 423-428 (1994).
- . A comparison of tacrolimus (FK 506) and cyclosporine for immunosuppression in liver transplantation. The U.S. Multicenter FK506 Liver Study Group. N. Engl. J. Med. 331 (17), 1110-1115 (1994).
- Mayer, A. D., et al. Multicenter randomized trial comparing tacrolimus (FK506) and cyclosporine in the prevention of renal allograft rejection: a report of the European Tacrolimus Multicenter Renal Study Group. Transplantation. 64 (3), 436-443 (1997).
- Pirsch, J. D., Miller, J., Deierhoi, M. H., Vincenti, F., Filo, R. S. A comparison of tacrolimus (FK506) and cyclosporine for immunosuppression after cadaveric renal transplantation. FK506 Kidney Transplant Study Group.. Transplantation. 15 (7), 977-983 (1997).
- Tanaka, H., et al. Physicochemical properties of FK506 a novel immunosuppressant isolated from Streptomyces Tsukubaensis. Transplant Proc. 14 ((5 Suppl 6)), 11-16 (1987).
- Spencer, C. M., Goa, K. L., Gills, J. C. Tacrolimus. An update of its pharmacology and clinical efficacy in the management of organ transplantation. Drugs. 54 (6), 925-975 (1997).
- Clipstone, N. A., Crabtree, G. R. Identification of calcineurin as a key signalling enzyme in T-lymphocyte activation. Nature. 357 (6380), 695-697 (1992).
- Barbarino, J. M., Staatz, C. E., Venkataramanan, R., Klein, T. E., Altman, R. B. PharmGKB summary: cyclosporine and tacrolimus pathways. Pharmacogenet. Genomics. 23 (10), 563-585 (2013).
- Christians, U., Benet, L. Z., Lampen, A. Mechanisms of clinically significant drug interactions associated with tacrolimus. Clin. Pharmacokinet. 41 (11), 813-851 (2002).
- Christians, U., Pokaiyavananichkul, T., Chan, L., Burton, M. E., Shaw, L. M., Schentag, J. J., Evans, W. e. b. b. Tacrolimus In: Pharmacokinetics and Pharmacodynamics. Principles of Therapeutic Drug Monitoring. , 529-562 (2005).
- Holt, D. W., et al. International Federation of Clinical Chemistry/ International Association of Therapeutic Drug Monitoring and Clinical Toxicology working group on immunosuppressive drug monitoring. Ther. Drug Monit. 24 (1), 59-67 (2002).
- Holt, D. W., Jones, K., Lee, T., Stadler, P., Johnston, A. Quality assessment issues of new immunosuppressive drugs and experimental experience. Ther. Drug Monit. 18 (4), 362-367 (1996).
- Jusko, W. J., et al. Consensus document: therapeutic drug monitoring of tacrolimus (FK-506). Ther. Drug Monit. 17 (6), 606-614 (1995).
- Oellerich, M., et al. Therapeutic drug monitoring of cyclosporine and tacrolimus. Update on Lake Louise Conference on cyclosporine and tacrolimus. Clin. Biochem. 31 (5), 309-316 (1998).
- Wong, S. H. Therapeutic drug monitoring for immunosuppressants. Clin. Chim. Acta. 313 (1-2), 241-253 (2001).
- Kahan, B. D., et al. Low intraindividual variability of cyclosporin A exposure reduces chronic rejection incidence and health care costs. J. Am. Soc. Nephrol. 11 (6), 1122-1131 (2000).
- Kahan, B. D., et al. Variable oral absorption of cyclosporine. A biopharmaceutical risk factor for chronic renal allograft rejection. Transplantation. 62 (5), 599-606 (1996).
- Kelly, D. A. Current issues in pediatric transplantation. Pediatr. Transplant. 10 (6), 712-720 (2006).
- Spivey, C. A., Chisholm-Burns, M. A., Damadzadeh, B., Billheimer, D. Determining the effect of immunosuppressant adherence on graft failure risk among renal transplant recipients. Clin. Transplant. 28 (1), 96-104 (2014).
- Taylor, P. J., Tai, C. H., Franklin, M. E., Pillans, P. I. The current role of liquid chromatography-tandem mass spectrometry in therapeutic drug monitoring of immunosuppressant and antiretroviral drugs. Clin. Biochem. 44 (1), 14-20 (2011).
- Edelbroek, P. M., van der Heijden, J., Stolk, L. M. Dried blood spot methods in therapeutic drug monitoring: methods, assays, and pitfalls. Ther. Drug Monit. 31 (3), 327-336 (2009).
- Meesters, R. J., Hooff, G. P. State-of-the-art dried blood spot analysis: an overview of recent advances and future trends. Bioanalysis. 5 (17), 2187-2208 (2013).
- Pandya, H. C., Spooner, N., Mulla, H. Dried blood spots, pharmacokinetic studies and better medicines for children. Bioanalysis. 3 (7), 779-786 (2011).
- Koster, R. A., Alffenaar, J. W., Greijdanus, B., Uges, D. R. Fast LC-MS/MS analysis of tacrolimus, sirolimus, everolimus and cyclosporin A in dried blood spots and the influence of the hematocrit and immunosuppressant concentration on recovery. Talanta. 115 (Oct 15), 47-54 (2013).
- Hinchliffe, E., Adaway, J., Fildes, J., Rowan, A., Keevil, B. G. Therapeutic drug monitoring of ciclosporin A and tacrolimus in heart lung transplant patients using dried blood spots. Ann Clin. Biochem. 51 (Pt 1), 106-109 (2014).
- Koop, D. R., Bleyle, L. A., Munar, M., Cherala, G., Al-Uzri, A. Analysis of tacrolimus and creatinine from a single dried blood spot using liquid chromatography tandem mass spectrometry. J. Chromatogr. B Analyt. Technol. Biomed. Life Sci.. 926 ((May 1)), 54-61 (2013).
- Sadilkova, K., Busby, B., Dickerson, J. A., Rutledge, J. C., Jack, R. M. Clinical validation and implementation of a multiplexed immunosuppressant assay in dried blood spots by LC-MS/MS. Clin. Chim. Acta.. 421 ((Jun 5)), 152-156 (2013).
- Li, Q., Cao, D., Huang, Y., Xu, H., Yu, C., Li, Z. Development and validation of a sensitive LC-MS/MS method for determination of tacrolimus on dried blood spots. Biomed. Chromatogr. 27 (3), 327-334 (2013).
- Hinchliffe, E., Adaway, J. E., Keevil, B. G. Simultaneous measurement of cyclosporin A and tacrolimus from dried blood spots by ultra-high performance liquid chromatography tandem mass spectrometry. J. Chromatogr. B Analyt. Technol. Biomed. Life Sci.. 883-884 ((Feb 1)), 102-107 (2012).
- Webb, N. J., Roberts, D., Preziosi, R., Keevil, B. G. Fingerprick blood samples can be used to accurately measure tacrolimus levels by tandem mass spectrometry). Pediatr. Transplant. 9 (6), 729-733 (2005).
- Keevil, B. G., Fildes, J., Baynes, A., Yonan, N. Liquid chromatography-mass spectrometry measurement of tacrolimus in finger-prick samples compared with venous whole blood samples. Ann. Clin. Biochem. 46 (Pt 2), 144-145 (2009).
- Yonan, N., Martyszczuk, R., Machaal, A., Baynes, A., Keevil, B. G. Monitoring of cyclosporine levels in transplant recipients using self-administered fingerprick sampling. Clin. Transpl. 20 (2), 221-225 (2006).
- Keevil, B. G., et al. Simultaneous and rapid analysis of cyclosporin A and creatinine in finger prick blood samples using liquid chromatography tandem mass spectrometry and its application in C2 monitoring. Ther Drug Monit. 24 (6), 757-767 (2002).
- Hoogtanders, K., et al. Dried blood spot measurement of tacrolimus is promising for patient monitoring. Transplantation. 83 (2), 237-238 (2007).
- Heijden, J., et al. Therapeutic drug monitoring of everolimus using the dried blood spot method in combination with liquid chromatography-mass spectrometry. J. Pharm. Biomed. Anal. 50 (4), 664-670 (2009).
- Cheung, C. Y., et al. Dried blood spot measurement: application in tacrolimus monitoring using limited sampling strategy and abbreviated AUC estimation. Transpl. Int. 21 (2), 140-145 (2008).
- Hoogtanders, K., et al. Therapeutic drug monitoring of tacrolimus with the dried blood spot method. J. Pharm. Biomed. Anal. 44 (3), 658-664 (2007).
- Wilhelm, A. J., den Burger, C. J., Vos, R. M., Chahbouni, A., Sinjewel, A. Analysis of cyclosporin A in dried blood spots using liquid chromatography tandem mass spectrometry. J. Chromatogr. B Analyt. Technol. Biomed. Life Sci. 877 (14-15), 1595-1598 (2009).
- Ostler, M. W., Porter, J. H., Buxton, M. O. Dried blood spot collection of health biomarkers to maximize participation in population studies. J. Vis. Exp. (83), e50973 (2014).
- Schäfer, P., Störtzel, M., Vogt, S., Weinmann, W. Ion suppression effects in liquid chromatography-electrospray-ionisation transport-region collision induced dissociation mass spectrometry with different serum extraction methods for systematic toxicological analysis with mass spectra libraries. J. Chromatogr. B. 773 (1), 47-52 (2002).
- Peck, H. R., Timko, D. M., Landmark, J. D., Stickle, D. F. A survey of apparent blood volumes and sample geometries among filter paper bloodspot samples submitted for lead screening. Clin. Chim. Acta. 400 (1-2), 103-106 (2009).
- Christians, U., et al. Automated, fast and sensitive quantification of drugs in blood by liquid chromatography-mass spectrometry with on-line extraction: immunosuppressants. J. Chromatogr. B. 748 (1), 41-53 (2000).
- Clavijo, C., et al. Development and validation of a semi-automated assay for the highly sensitive quantification of Biolimus A9 in human whole blood using high performance liquid chromatography-tandem mass spectrometry. J. Chromatogr. B. Analyt. Technol. Biomed. Life Sci. 877 (29), 3506-3514 (2009).
- Mei, J. V., Alexander, J. R., Adam, B. W., Hannon, W. H. Use of filter paper for the collection and analysis of human whole blood specimens. J. Nutr. 131 (5), S1631-S1636 (2001).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon