Method Article
형광 공명 에너지 전송과 리간드 - 수용체 상호 작용의 실시간 모니터링
요약
우리는 복합 폴리머 polydiacetylene (PDA)와 형광 분자의 감지 용 PDA liposomes의 표면에 부착 사이에 초조해 보여줍니다. PDA liposomes은 프로브로 사용되는 분자에 대한 자신의 표면에 수용체 분자가 포함되어 있습니다. 리간드 - 수용체 상호 작용이 감지 메커니즘의 기초 형광와 PDA 사이의 걱정 효율성의 변화에 연결되어 있습니다.
초록
걱정은 장거리 쌍극자 - 쌍극자 상호 작용 1 일까지 지상 상태 수용체 분자에 흥분 기증자 분자에서 에너지의 변환이 아닌 radiatively이된다 과정입니다. analyte는 PDA 2,3,4,7에 연결 수용체와 상호 작용 한 후 PDA의 UV-VIS 전자 흡수 스펙트럼 (그림 1)에서 블루 변화 : 현재 감지 분석에서 우리는 PDA의 흥미로운 속성을 사용합니다. PDA 흡수 스펙트럼에있는이 변화는 걱정 효율성의 변화로 연결 PDA (수용체)와 rhodamine (기증자) 사이의 스펙트럼 중첩의 변화 (J)를 제공합니다. 따라서, analyte (리간드)와 수용체 사이의 상호 작용은 기증자 fluorophores 및 PDA 사이에 안달을 통해 감지된다. 특히, 우리는 모델 단백질 분자 streptavidin의 감지를 보여줍니다. 우리는 또한이있는 소 혈청 알부민 (BSA)에 리포좀 표면의 공유 결합 - 바인딩 메커니즘을 초조해 보여줍니다. t 사이의 이러한 상호 작용그 이중층 liposomes과 단백질 분자는 실시간으로 감지 할 수 있습니다. 제안 된 방법은 작은 화학 및 대형 생화학 분자를 감지하는 일반적인 방법입니다. 형광은 비색법보다 본질적으로 더 민감하기 때문에, 분석의 검출 한계는 하위 nanomolar 범위 또는 8 이하인 수 있습니다. 또한, PDA는 걱정의 보편적 수용체의 역할을 할 수있는 여러 센서가 기증자와 PDA liposomes의 표면에 부착 다른 수용체와 기능화 PDA (수용체)로 개발 될 수 있다는 것을 의미합니다.
프로토콜
PDA Liposomes 4,5,6의 A. 합성 및 특성
주 1 : 모든 실험 단계에 걸쳐 모든 컨테이너에 알루미늄 호일 포장을 사용하여 빛의 PDA 솔루션을 보호 할 수 있습니다.
주 2 : 리포좀 솔루션의 두 가지 세트 (B와 C)은 다음 절차를 준비했다 A (PDA liposomes의 합성 및 특성).
1. N-hydroxysuccinimide Diacteylene의 합성 (NHS-PCDA)
- liposomes를 준비하려면 필수 요소 PCDA-NHS가 필요합니다. 우리는 다음 절차를 사용하여 PCDA-NHS를 합성했습니다
- (3 - - (디메틸 아미노) propyl)-3-ethylcarbodiimide 하이드로 클로라이드 (0.144 g, 0.713 mmol 10,12 - pentacosadiynoic 산 (PCDA) (0.267 g, 0.713 mmol), N-hydroxysuccinimide (0.0914 g, 0.786 mmol)과 1을 추가 ) 건조 CH 2 망할 CIA 2 (20 ML).
- 2 시간 동안 실온에서 솔루션을 저어.
- 조심스럽게 연구를 사용하여 용매를 제거otary 증발기는 건조 박막를 얻을 수 있습니다.
- 디 에틸 에테르 (25 ML)와 물 (25 ML) 3 번과 잔여 물을 추출 분리 유입 경로를 사용합니다.
- 30 분 동안 MgSO 4 (1.0 g)와 유기 층을 말린다. 필터 및 흰색 고체 분말을 (0.24 g,> 90 %) 얻기 위해 회전 증발하여 용매를 제거합니다.
- 핵 자기 공명 (NMR)에서 최종 화합물을 분석합니다.
- 1 H NMR (300 MHz의, DMSO), δ (ppm으로) : 0.893 (t, 3H), 1.268 (m, 26H), 1.512 (m, 4H), 1.754 (m, 2H), 2.252 (t, 4H), 2.365 (m, 1H), 2.610 (m, 1H), 2.842 (S, 2H).
2. 리포좀 준비 5,6,7
- PCDA-NHS : 1,2 - dimyristoyl-SN-glycero-3-phosphocholine (DMPC) :: 8 : 1 : dichloromethane 1 20 년 ML PCDA를 해산.
- 응집체를 제거하는 필터 종이 솔루션을 필터링 할 수 있습니다.
- 단량체의 박막을 얻을 수 있도록 완전히 용매를 증발.
- VAC 아래 박막은 하루 아침에 건조uum.
- 원하는 농도의 리포좀 솔루션 (0.65-1 MM)를하기 위해 탈 이온수 (50 ML)와 영화 수화물.
- 76 프로브 sonicator로 결과 정지 Sonicate ° C ~ 18 분에.
- 조심스럽게 지방질 집계를 제거하는 종이 필터를 통해 솔루션을 통과
- 4 단량체의 자기 조립을 홍보 할 ° C 하룻밤에 솔루션을 냉각. 최종 솔루션은 광학 명확해야합니다.
- 공기 펜 레이 UV 소스를 (4.5 MW / cm 2)를 사용 ~ 2 분을위한 UV 방사선의 254 nm의와 조사에 의해 자기 조립 diacetylene의 단량체를 (리포좀) 중합.
- 리포좀 솔루션은 최소 2 주 동안 실온에서 안정. 때 냉장 솔루션은보다 안정적이었다.
Rhodamine 태그 소 혈청 알부민 (BSA-RH) 수정 PCDA의 liposomes의 B. 준비
1. 리포좀 표면에 BSA-RH의 바인딩
- PBS 부에 BSA-RH를 해산ffer은 (이온 농도가 pH를 7.2, 0.01M이었다) BSA-Rhodamine 솔루션의 1.2 μm의 최종 농도를 확인합니다.
- 실온에서 단계 A.2. (위 참조)에서 준비 리포좀 솔루션의 10 ML에 BSA-Rhodamine 2 ML (1.2 μM)를 추가합니다.
- 단백질의 라이신 잔기의 NHS 그룹에 의해 활성화 카르 복실 산에 아민 그룹의 바인딩을위한 고전 반응은 (그림 2의 반응 방식) 다음되었습니다. NHS-PCDA은 NHS-아민 반응을 (그림 2, 2 단계)를 사용하여 liposomes와 covalently 구속력이 단백질 분자에 대해 (그림 2 단계 중 1 단계) 설계되었습니다. NHS는 전진 방향에있는 아민 - 카르 복실 산 반응을 유도하는 훌륭한 출발 요원입니다. 적절한 조건에서이 반응의 수율은 양적해야합니다.
- 무료 BSA-RH의 제거 : deionized w에서 : 스펙트럼 / 포 바이오 셀룰로오스 에스터 (CE) 멤브레인을 (100,000 MW C O) 만끽15 분에 ater. 이 멤브레인은의 투석에 사용되는 탈 이온수에 BSA-Rhodamine (분자량 66,000 ~ 다) unreacted.
- 투석 막에 솔루션을 자세히 전송합니다.
- 투석하는 동안 2 시간의 물, 8 시간, 14 시간, 24 시간 그리고 36 시간을 변경합니다.
- 알루미늄 호일로 덮여 병에 최종 솔루션을 수집합니다.
의 C. 준비 SR은 - 디아민 및 Liposomes에게 비오틴 태그
1. 대신 단계 2.1에서 DMPC를 사용, 우리는 비오틴 태그 - (을 사용합니다 1,2 - dioleoyl-SN-glycero-3-phosphoethanolamine-N-(biotinyl) (비오틴 - 마약을).
- 2.9에 2.2을 통해 모든 단계를 따르십시오.
- 대신 BSA-RH의 단계 B에서 (SR-디아민) 태그 Sulphorhodamine을 디아민 사용합니다.
- B. 모든 추가 단계를 수행
- 이 준비 liposomes가 비오틴을 포함하고 표면에 SR은 - 디아민. 이후 단계는 한 가지 예외가있는 A와 B (위 참조)과 유사했다 : streptavidin이 soluti에 추가되었습니다의 변화를 통해 비오틴 - streptavidin 상호 작용을 조사하기에하는 것은 효율성을 초조해.
D. 대표 결과
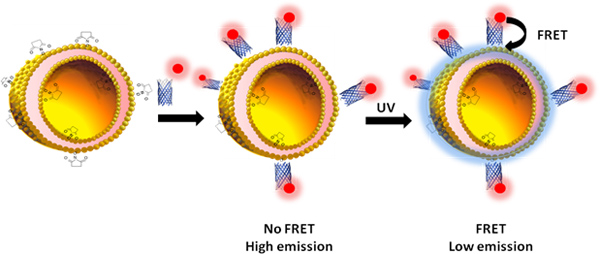
제목 그림.의 반응을 설명하는 만화와는 리포좀 표면에서 발생하는 프로세스를 (단계 B에 따라 작성) 초조해.
사용 liposomes에 단백질 첨부 파일의 A. 모니터링은 1 안달
의 모니터링은 Rhodamine과 단계 B.에 준비 PDA liposomes 사이에 안달
BSA-RH의 흥분과 방출 스펙트럼과 PDA의 흡수 스펙트럼은 (그림 3A) 이동됩니다. 우리는 명확하게 볼 수 PDA의 흡수 스펙트럼과 BSA-RH 중복의 방출 스펙트럼. 이 안달 메커니즘 공명 요구 사항을 충족시킵니다. 중합 전후 BSA-Rhodamine 태그 liposomes는 UV-V로 분석 하였다하고 형광 분광법. 고립 된 기증자와 수용체를 들어, 효율성은 기증자 - 수용체 거리 (R) 및 J 1 (J-값)에 크게 의존 초조해. 방출의 담금질로 인해 photopolymerization 후 블루 PDA의 전자 흡수 스펙트럼의 모양으로 인해 rhodamine 및 PDA 사이에 초조해의 (그림 3B) 관찰된다. 우리의 경우에는 효율성이 unpolymerized liposomes 및 Rhodamine를위한 0 ~ 걱정 때문에 J 보이는 지역 unpolymerized liposomes = 0.
우리는 자신의 표면에 NHS를 포함하지 않은 유일한 PDA liposomes와 유사한 실험을 수행했습니다. 이러한 경우에는 BSA-RH는 liposomes의 표면에 태그되지 않았습니다. 이 경우 rhodamine 및 PDA (R 평균) 사이의 평균 거리가 포스터 반경 (R 0 = 2.8 nm의)보다 훨씬 큽니다. 따라서, 우리는 형광 강도에 큰 감소를 관찰 없습니다. 이 관찰런던 심포니 오케스트라 때 R은 <2.8 nm의 형광 담금질을 지배입니다하는 것이 좋습니다.
J와 R 0 값은 다음 수식을 사용하여 계산되었습니다 [1]
J (λ) = ∫ F D (λ) ε A (λ) λ 4 dλ
R 0 = 0.211 [K 2 N -4 Q D J (λ)] 육분의 일
푸른 PDA의 흡광 계수 (ε)은 -1 이전 streptavidin의 추가에 ~ 2000-10000 M -1 cm의 범위에 있습니다. 푸른 PDA의 흡광 계수는 사진 중합 조건에 따라 달라집니다. [2] 예를 들어, ε 값은 더 이상 시간을 polymerized 된 솔루션에 대한 더 큰 것입니다. 또한, diacetylene의 단량체의 자기 조립도 ε 값에 영향을 미칠 수 있습니다. J calculations이 변경 고려, 그들은 비오틴 - streptavidin 분자 상호 작용으로 인해 PDA 흡광 계수의 변화를 반영합니다. J 값이 실험 PDA 흡수와 SR-101 방출 데이터를 사용하여 계산됩니다. J 값의 변화는이 솔루션 (그림 4C)에 streptavidin의 추가에 따라 PDA의 전자 흡수 스펙트럼의 변화로 인해 수 있습니다. J 값의 단위는 M -1 cm -1 nm의 4입니다.
의 B. 모니터링은 비오틴 태그 리포좀 솔루션에 streptavidin의 추가와 함께 안달
주 1 : Rhodamine 이상 단계 C에서 준비 PDA liposomes 사이에 초조해의 모니터링.
Sulphorhodamine 태그의 흥분과 방출 스펙트럼은 디아민 (SR-디아민) 및 PDA의 흡수 스펙트럼 (그림 4A) 이동합니다. Unpolymerized 및 polymerized 비오틴 태그 liposomes는 UV-VIS 사용 분석 하였다및 형광 분광법. rhodamine (SR-101)의 방출은 걱정 인해 방출 담금질을 제안 중합 (그림 4B) 이후 약 45 % 감소. 리포좀 솔루션 2 ML에 streptavidin 용액 40 μl aliquots (1 μM)를 추가합니다. 솔루션 streptavidin의 추가와 함께, J 값의 변화 (그림 4C) 관찰된다. 비오틴은 streptavidin, PDA 리포좀 (그림 1 ~ 645 nm의 중심)의 푸른 피크 강도에 바인딩으로 (F igure 1S) 관찰 540 나노 미터에서 흡수 피크의 증가 반면, 감소되었습니다. 그림 4D는 걱정의 변화를 보여줍니다 효율. streptavidin 농도의 증가와 함께 감소 걱정 효율성 또한 예측과 일치합니다.
streptavidin의 매 40 μl 나누어지는 첨가 한 후 SR 방출을 녹화합니다. 우리는 strept을 추가 한 후 rhodamine 방출의 꾸준한 증가를 관찰아비딘 (그림 5). rhodamine 방출이 증가 비오틴 - streptavidin 상호 작용에 따라 sulphorhodamine 방출 스펙트럼과 PDA 흡광도 스펙트럼의 J 값의 감소로 인한 것입니다. 분자 수준에서 비오틴 - streptavidin 상호 작용은 더 thermodynamically 안정 붉은 PDA 양식 2 블루 PDA 형태의 감소에 결과 PDA의 효과적인 활용 길이의 미묘한 변화로 이어집니다. 이 J 값의 변화의 기초이다. 흥미롭게도, PDA 리포좀에 covalently 또는 비 covalently 보세 비오틴에 대한 분자 상호 작용의 미묘한 차이는 우리의 감지 검정 4를 사용 탐색 할 수 있습니다.
우리는 또한 제어 실험을 수행하고 streptavidin-비오틴 시스템에 대한 그와 같은 실험 조건 하에서 제어 샘플의 방출을 감시하고 있습니다. 제어 실험으로 구성되어, 자신의 (1)에 포함 된 리포좀 솔루션은 비오틴표면은 동일한 볼륨과 집중의 버퍼 솔루션을 추가 된 및 (2)의 표면에 비오틴 수용체가없는 리포좀 솔루션은 동일한 볼륨과 집중의 streptavidin을 추가했다. streptavidin을 추가 후 비오틴 태그 리포좀 솔루션의 강도가 향상된 강도를 보여 주었다하지만 제어 실험 리포좀 솔루션의 강도가 (예를 들어, 그림 2S를 참조하십시오), 반면에,이 방출 강도에 감소 전시. 이것은 솔루션의 희석에 따라 결정됩니다. 이 실험은 명확 솔루션의 향상된 방출 특정 분자 상호 작용에 의한 있다고 지적했다.
rhodamine 및 PDA 쌍에 대한 포스터의 반경이 (R 0) (eq.2가) ~ 2.80 나노 미터로 계산됩니다. 이 연구는 2.80 nm의 경우 절연 PDA-rhodamine 쌍을 위해 흥분 상태 rhodamine 분자의 50 %가 PDA로 전송 자신의 에너지를 가지고 것을 의미합니다.
우리 obs 비오틴은 covalently PDA 백본에 부착 될 때 방출 증가 liposomes에 비 covalently 보세 비오틴보다 2 ~ 3 배 더 큰이라고 4.이 결과는 강력하게 제안 시스템이 상호 작용의 미묘한 차이를 구별에 민감하는 것이 좋습니다 erved 변환기에서 (비오틴과 리포좀 이중층 사이 링커) liposomes에 부착 covalently 및 비 covalently 보세 수용체 때문입니다. 단백질 상호 작용의 분광 광도계, 실시간 모니터링 (밀리 초에서 두 번째로 규모까지) (UV-VIS 분광의)의 스캔 및 데이터 수집 기능에 따라이 감지 시스템으로 가능합니다.
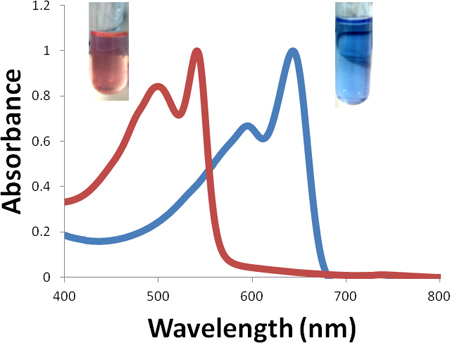
파란색과 빨간색 PDA 솔루션의 그림 1. 흡수 스펙트럼. (삽입) 광학 micrographs은 디지털 카메라로 촬영.
g "/>
그림 2. PCDA - NHS 합성 (1 단계)에 대한 반응 방식. 단백질의 아민 치환체 (2 단계)에 PCDA-NHS의 반응. 2 단계 PCDA 단량체의 카르 복실 산으로 단백질의 라이신 잔류의 구속의 기초이다. 큰 그림을 보려면 여기를 클릭하십시오 .

그림 3A. 관찰에 변경이 효율성이 PDA의 흡수 스펙트럼의 변화로 인해 초조해. 중합 전에 BSA-RH 방출과 PDA 흡수 사이하지만 걱정에 대한 요구 사항입니다 BSA-RH 방출과 중합 PDA 흡수 중복 이후로 중복이 없습니다. Rhodamine 기증자가 (빨간색)이며, polymerized PDA liposomes는 수용체 (파란색) 역할을합니다.

그림3B. 전에 (파란색)과 PCDA 중합 (적색) 후 BSA-RH 태그 liposomes의 형광 스펙트럼. rhodamine 방출의 큰 감소는 rhodamine와 PDA 사이에 걱정 때문에 관찰되었다.

.. 그림 4A 스펙트럼 오버랩 (J) PDA (파란색 또는 빨간색) 흡수 스펙트럼과 Sulphorhodamine 방출 스펙트럼 (오렌지)에 대한 변경도 4a는 극한 조건의 대표적인 스펙트럼이다; streptavidin의 초과가 솔루션에 추가되었을 때 그입니다. 그림 4a는 streptavidin의 초과의 추가에 따라 거의 완전한 블루 - 투 - 붉은 PDA 변화를 보여줍니다. 그것은 명확 J (스펙트럼 오버랩)는 PDA 흡수 스펙트럼의 청색 변화와 증가하는 볼 수있다

그림 4B. 형광 스펙트럼 전 (파란색)과 이후 (RED) 리포좀 중합.

그림 4C 안달을위한 조건 :. 기증자 (sulphorhodamine)와 리포좀 솔루션에 streptavidin 추가하면 수용체 (PDA) 사이 J 변경.
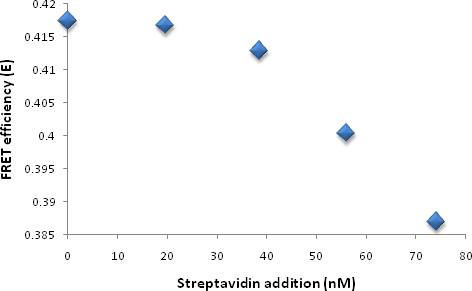
그림 4D는. 기증자 (sulphorhodamine)와 리포좀 솔루션에 streptavidin 추가하면 수용체 (PDA) 사이의 효율 변화를 안달.

그림 5. PDA 리포좀 솔루션에 streptavidin의 aliquots를 추가 한 후 Rhodamine 방출 스펙트럼. 삽입은 SR-101 스펙트럼의 방출 변화 확대를 보여줍니다.
토론
우리는 NHS-아민 반응을 사용하여 리포좀 표면에 단백질의 라이신 잔기의 선택적 바인딩을 수행했습니다. 이 기반 방법은 리포좀 표면에 바인딩 비오틴 - streptavidin을 구속하며 단백질 (BSA)의 실시간 모니터링을하고 할 수 있습니다 초조해. 비슷한 절차는 자신의 선택 수용체와 다양한 단백질 상호 작용의 바인딩 역학을 공부하고 적용 할 수 있습니다. fluorophores의 스펙트럼 특성에 따라 J 값의 변화를 제공 할 것입니다 fluorophores를 선택의 유연성이 있습니다. PDA는 보편적 인 수용체이다. 따라서, 여러 fluorophores 및 수용체와 함께 PDA (수용체)의 사용은 우리에게 여러 센서를 제공하는 가능성을 제기. 센서의 민감도는 하위 nanomolar이며, 최적화, 그것은 더 강화 될 수 있습니다. 센서의 특이성은 수용체와 리간드 사이의 분자 상호 작용의 사용을 통해 조정된다. 이 센서는 또한 사용할 수 있습니다 큰 입자의바이러스와 박테리아로 uch.
또한, 우리는 기증자 - 수용체 사이의 거리처럼 가치있는 정보를 수집 할 수있었습니다, 효율성 및 J-값 등 기증자와 수용체 사이의 거리가 2.8 nm의 것으로 계산됩니다이 초조해. 이것은 우리의 예측과 일치했다. 교활한 바이러스, 박테리아 및 다른 유해한 미생물의 모니터링의 큰 필요가, 우리는 실제 시간이 유해 분자를 감지 수행 할 수있는 손 헬드 장치를 제조하고 싶습니다.
공개
관심 없음 충돌이 선언 없습니다.
감사의 말
이 작품에 대한 재정 지원은 SIUC의 국립 과학 재단 (National Science Foundation), 건강의 국립 연구소 (NIH), 재료 기술 센터 (MTC)와 ORDA 통해 제공되었다. 우리는 FE-SEM의 구입에 대한 보조금 (CHE-0959568)에 대한 NSF 감사드립니다. 우리는 도움이 토론에 대한 교수 매튜 McCarroll 감사드립니다. 줄리아 Reyes는 그녀의 장학금 및 재정 지원을 COLCIENCIAS, 콜롬비아 기관 및 Universidad Pedagogica Y Tecnologica 드 콜롬비아를 감사합니다.
자료
| Name | Company | Catalog Number | Comments |
| 시약의 이름 | 회사 | 카탈로그 번호 | 코멘트 |
| 10,12 - pentacosadiynoic 산 (PCDA) | GFS 화학 물질 | 3261 | 민감한 빛 |
| N-hydroxysuccinimide (NHS) | Acros의 유기물 | 157270250 | 민감한 수분 |
| 1 - (3 - (디메틸 아미노) propyl)-3-ethylcarbodiimide 히드로 클로라이드 (EDC) | 화학 - impex 국제 | 00,050 | |
| 1,2 - dimyristoyl-SN-glycero-3-phosphocholine (DMPC) | 벤티 폴라 지질 | 850345P | |
| Rhodamine 태그 소 경음 ... 알부민 (BSA-RH) | 시그마 알드리치 | A4537 | |
| (1,2 - dioleoyl-SN-glycero-3-phosphoethanolamine-N-(biotinyl) (비오틴 - 마약) | 벤티 폴라 지질 | 870282 |
참고문헌
- Lakowicz, J. R. . Principles of Fluorescence Spectroscopy. , (1999).
- Charych, D. H., Nagy, J. O., Spevak, W., Bednarski, M. D. Direct Colorimetric Detection of a Receptor-Ligand Interaction by a Polymerized Bilayer Assembly. Science. 261, 585-588 (1993).
- Yoon, B., Lee, S., Kim, J. -. M. Recent Conceptual and Technological Advances in Polydiacetylene-based Supramolecular Chemosensors. Chem. Soc. Rev. 38, 1958-1968 (2009).
- Xuelian, L. i., Kohli, P. u. n. i. t. Investigating Molecular Interactions in Biosensors Based on Fluorescence Resonance Energy Transfer. J. Phys. Chem. C. 114, 6255-6264 (2010).
- Li, X., Matthews, S., Kohli, P. Fluorescence Resonance Energy Transfer in Polydiacetylene Liposomes. J. Phys. Chem. B. 112, 13263-13272 (2008).
- Li, X., McCarroll, M., Kohli, P. Modulating Fluorescence Resonance Energy Transfer in Conjugated Liposomes. Langmuir. 22, (2006).
- New, R. R. C., New, R. R. C. . Liposomes: A Practical Approach. , 33-104 (1990).
- Chen, X., Lee, J., Jou, M. J., Kim, J. -. M., Yoon, J. Colorimetric and Fluorometric Detection of Cationic Surfactants Based on Conjugated Polydiacetylene Supramolecules. Chem. Commun. , 3434-3436 (2009).
- Yarimaga, O., Im, M., Choi, Y. -. K., Kim, T. W., Jung, Y. K., Park, H. G., Lee, S., Kim, J. -. M. A Color Display System Based on Thermochromic Conjugated Polydiacetylene. Macromolecular Research. 18, 404-407 (2010).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유