Method Article
Sintesi efficiente dei Benzeni polifunzionalizzati nell'acqua attraverso la Benzannulation di composti insaturi e alchine
In questo articolo
Riepilogo
Viene segnalata una benzangolazione senza metalli promossa dal persulfatto di composti e alchini insaturi nell'acqua verso la sintesi di benzene polifunzionalisti senza precedenti.
Abstract
Le reazioni di benzannulationi rappresentano un protocollo efficace per trasformare gli elementi costitutivi ciclici in scheletri di benzene strutturalmente variati. Nonostante gli approcci classici e recenti verso i benzeni funzionalizzati, nei metodi privi di metalli d'acqua rimane una sfida e rappresenta un'opportunità per espandere ancora di più l'insieme di strumenti utilizzati per sintetizzare composti di benzene poliasppi. Questo protocollo descrive una configurazione sperimentale operativamente semplice per esplorare la benzangolazione di composti e alchini insaturi per permettersi anelli di benzene funzionalisti senza precedenti in alti rendimenti. Il persulfato di ammonio è il reagente di scelta e offre notevoli vantaggi come stabilità e facilità di manovra. Inoltre, l'uso dell'acqua come solvente e l'assenza di metalli conferiscono maggiore sostenibilità al metodo. Una procedura di workup modificata che evita l'uso di agenti di essiccazione aggiunge anche comodità al protocollo. La purificazione dei prodotti viene eseguita utilizzando solo una spina di silice. L'ambito del substrato è attualmente limitato agli alchini terminali e ai composti alipatici insaturi.
Introduzione
I benzeni funzionalizzati sono probabilmente i precursori più impiegati nella chimica organica sintetica1,2. Essi figurano nella maggior parte dei prodotti farmaceutici, prodotti naturali e materiali organici funzionali. Sono stati riportati approcci potenti per la costruzione di derivati del benzene poliasppi e, tra questi, metodi consolidati come sostituzione nucleophilica o elettrofila aromatica3, le reazioni di accoppiamento incrociato4 e la metallizzazione diretta5 sono approcci prevalenti. Tuttavia, l'applicazione diffusa di queste strategie può essere ostacolata da limitate possibilità di substrato, eccessiva reazione e regiosesia.
Le reazioni di ciclizzazione Tandem rappresentano un'alternativa molto interessante ai metodi classici per la costruzione rapida di benzene funzionalizzati in modo atom-economico6,7,8. All'interno di questo quadro, le reazioni di benzannulation rappresentano un protocollo adatto per trasformare efficacemente gli elementi costitutivi aciciclici in preziosi scheletri di benzene. Questa classe di reazione è una metodologia versatile con una varietà di materie prime chimiche, meccanismi e condizioni sperimentali9,10,11.
L'obiettivo del nostro studio è quello di sviluppare un protocollo semplice e pratico per una reazione di benzannazione per generare anelli di benzene funzionalizzati senza precedenti. A tal fine, abbiamo deciso di esplorare una benzannazione mediata senza metalli e persofato in acqua che impiega materie prime chimiche a basso costo (aumento di composti e alchine, composti insaturi e alkynes).
Si possono sottolineare diversi vantaggi rispetto ai metodi riportati nella letteratura. Le trasformazioni senza metalli hanno tutti gli attributi necessari per soddisfare i requisiti di sviluppo sostenibile. Solo per citarne alcuni, non è necessario la rimozione costosa e impegnativa delle quantità di tracce metalliche dai prodotti desiderati; le reazioni sono meno sensibili all'ossigeno e all'umidità rendendo la sua manipolazione più facile e il processo complessivo è normalmente meno costoso12. I sali di Persulfato sono stabili, facili da maneggiare e generare solo solfato come sottoprodotto, aggiungendo così slancio all'iniziativa chimica verde per ridurre al minimo l'inquinamento da rifiuti13. L'acqua è considerata un solvente verde adatto per le reazioni organiche: è non tossico, non infiammabile, ha un odore molto basso ed è disponibile a basso costo. Anche i composti organici insolubili in acqua possono essere impiegati utilizzando14 sospensioni acquose "sull'acqua" e questi semplici protocolli sintetici hanno guadagnato sempre più attenzione nel corso degli anni.
Le nostre condizioni di reazione ottimizzate e la semplice procedura di workup/purificazione forniscono l'accesso a diversi anelli di benzene funzionalizzati che offrono una ricchezza di opportunità per un'ulteriore funzionalizzazione.
Protocollo
AVVISO: Consultare le schede tecniche di sicurezza dei materiali (MSDS) prima dell'uso delle sostanze chimiche in questa procedura. Utilizzare adeguate attrezzature di protezione personale (PPE), tra cui occhiali di sicurezza, un camice da laboratorio e guanti nitrile poiché diversi reagenti e solventi sono tossici, corrosivi o infiammabili. Eseguire tutte le reazioni in una cappa di fumi. I liquidi utilizzati in questo protocollo vengono trasferiti in micropipetta.
1. Reazione di Benzannulation che impiega alchine e composti insaturi
- Aggiungere 2,0 mL di acqua distillata a una provetta da 15 mL (di 1 cm di diametro) contenente una barra di stir. In sequenza, aggiungere fenililetylene (220 , 2,00 mmol, 2,0 equiv.), 2-cyclohexen-1-one (96,8 LL, 1,00l, 1,0 equiv.) e ammonium persulfat (1,5 mL di una soluzione acquosa appena preparata 1,3 M, 2.000 equiv.) e ammonio permmota.
- Far capo voltare il tubo utilizzando un setto di gomma e inserire un ago in esso per evitare l'eventuale accumulo di pressione durante il riscaldamento.
- Posizionare il tubo in un blocco di riscaldamento in alluminio su una piastra calda e riscaldarlo a 85 gradi centigradi sotto agitazione vigorosa (1150 giri/min) per 8 h.
- Per seguire l'avanzamento della reazione, prendere un 50 l-aliquota del mezzo di reazione e trasferirlo in una fiala conica da 1,5 mL. Aggiungere 50 l di acetato di etilo nella fiala e agitarlo. Raccogliere lo strato superiore organico con un tubo capillare e analizzarlo da TLC.
NOTA: L'avanzamento della reazione è controllato da TLC confrontando la scomparsa del punto composto insaturi di z con l'aspetto del prodotto sotto la luce UV (254 nm). L'analisi TLC viene eseguita con lastre di vetro rivestite in silice e sviluppate con 92:8 exane/acetato etilico. Valori di Rf: fenilecetillene - 0,68; 2 ciclixo-1-uno - 0,23; prodotto 3e - 0,26.
ADE': Phenylacetylene e 2-cyclohexen-1-one sono irritabili infiammabili, acutamente tossici e lievi. Il persulfato di ammonio è corrosivo e può irritare le membrane mucose.
2. Lavori di estrazione e purificazione
- Raffreddare la miscela di reazione a temperatura ambiente e aggiungere l'acetato di etiliato (1 mL) alla provetta. Mescolare la sospensione per ca. 1 min e poi centrifugare la sospensione a 2.336 - g a temperatura ambiente per 1 min. Rimuovere lo strato superiore organico utilizzando una pipetta Pasteur e trasferirlo in una fiaschetta inferiore rotonda. Ripetere questo passaggio due volte.
NOTA: La fase di centrifugazione evita l'uso di agenti di essiccazione e rompe facilmente qualsiasi emulsione finale. - Concentrare la soluzione sotto pressione ridotta utilizzando un evaporatore rotante per ottenere un petrolio greggio.
- Aggiungere 55 mL di una miscela di esanei/acetato etilico al rapporto di 92:8 in un Becker contenente 7,5 g di SiO2 (dimensione del poro 60 , 35-70 m di dimensione delle particelle, per la cromatografia flash). Mescolare il pallone per ottenere un liquame omogeneo. Trasferire il liquame in una colonna (40 mm di diametro interno) e imballare la colonna eluindo il solvente. Se necessario, eluire ancora una volta per rimuovere eventuali bolle dalla fase stazionaria.
- Sciogliere il petrolio greggio in una quantità minima di acetato di etilismo, quindi trasferire questa soluzione nella colonna. Utilizzando gli stessi 55 mL di una miscela 92:8 exanes/acetato etilico, eluire il materiale, raccogliendo la colonna effluent in provette e seguendo da TLC per ottenere il prodotto puro desiderato.
- Concentrare la soluzione sotto pressione ridotta su un evaporatore rotante e rimuovere le sostanze volatili finali sotto vuoto elevato per almeno 1 h. Analizzare un campione del prodotto purificato di 1H e 13C NMR utilizzando CDCl3.
AVVISO: L'acetato di etiliato e gli esanei sono infiammabili. SiO2 polvere è un irritante respiratorio.
Risultati
Il benzene polisostituito (3b, Figura 1) è stato isolato come olio incolore (0,2741 g, 0,920 mmol, 92% di rendimento) utilizzando il nostro protocollo. La struttura e la purezza possono essere valutate negli spettri NMR 1H e 13C presentati nella Figura 2 e nella Figura 3. I picchi per i protoni aromatici sull'anello centrale del benzene , ovvero 8,37 e 7,72 ppm, sono stati utilizzati come segnali diagnostici per la formazione del prodotto.
6,8-diphenilil-3,4-dihydronaphthalen-1(2H)-uno (3b). Rf - 0,26 (92:8 exanes/acetato etile); 1H NMR (500 MHz, Cloroforma-d), 8,37 (d, J - 2,26 Hz, 1 H), 7,72 (d, J - 2,26 Hz, 1H), 7,67 (dd, J - 8,28, 1,51 Hz, 2H), 7,49-7,37 (m, 8 H), 2,89 (t, J 6,02 Hz, 2,02 Hz), 2,72 (ap t, J - 6,02 Hz, 2H), 2,09 (quint, J - 6,02 H). 13C NMR (125MHz, Chlorofor-d): 23,19, 28,01, 39.02, 124.86, 127.00, 127.46, 127.64, 128.35, 128.85, 129.19, 133.17, 133.41, 139.13, 139.78, 140.81, 142.51, 198.60. HRMS m/z (ESI): calcd. per C22H19O [M - H]- 299.1436, trovato 299.1420.
Diversi anelli di benzene polisostituiti sono stati preparati in alti rendimenti utilizzando il nostro protocollo (Figura 1). 15 Tutti i prodotti sono stati analizzati da 1H e 13C NMR, nonché da spettrometria di massa ad alta risoluzione (HRMS) al fine di caratterizzarli pienamente.
L'analisi GC può essere utilizzata come metodo alternativo per il rilevamento dei prodotti; anche se, anche l'analisi TLC funziona in modo efficiente. Tutti i prodotti sono UV-attivo e macchia in presenza di base KMnO4 soluzione aqueous. Una spina di silice è adeguata per la purificazione dei prodotti.
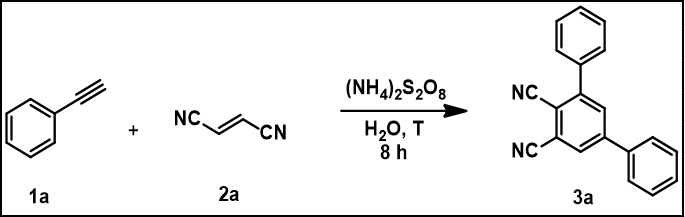
Le rese ottimali sono state ottenute quando si impiega un rapporto di 2:1 per gli alkynes e, rispettivamente, i composti insaturi di z; 2 equiv. di persulfato di ammonio e 85 gradi centigradi come temperatura di reazione. Nel processo di ottimizzazione, la reazione tra fenilecetillo 1a e fumaronititrile 2a è stata scelta come reazione modello (Tabella 1). L'aumento della quantità di composto insaturi di z, ha portato a un risultato inferiore (Tabella 1, voce 3). Sono state testate variazioni della quantità di (NH4)2S2O8 e in ogni scenario è stata osservata una diminuzione della produzione di 3a (tabella 1, voci 4 e 5). La modifica della temperatura di reazione a 25 gradi centigradi ha comportato un arresto completo della reattività(Tabella 1, voce 6). L'aumento della temperatura di reazione a 95 gradi centigradi non ha migliorato la resa(Tabella 1, voce 7).

Figura 1: Schema generale e ambito della trasformazione. Condizioni generali: 2 mL di acqua, 1 (2,0 mmol), 2 (1,0 mmol), (NH4)S2O8 (2,0 mmol, soluzione acquosa 1,3 M), 85 c, 8 h. Resa dei prodotti isolati. un Utilizzando 4.0 mmol di (NH4)S2O8, 24 h tempo di reazione. Questa cifra è stata modificata da de Souza et al.15Fare clic qui per visualizzare una versione più grande di questa figura.

Figura 2: 1H NMR di 3b. Spectrum ottenuto in CDCl3 a 400 MHz. Questa cifra è stata modificata da de Souza etal. Fare clic qui per visualizzare una versione più grande di questa figura.

Figura 3: 13C NMR di 3b. Spectrum ottenuto in CDCl3 a 400 MHz. Questa cifra è stata modificata da de Souza etal. Fare clic qui per visualizzare una versione più grande di questa figura.
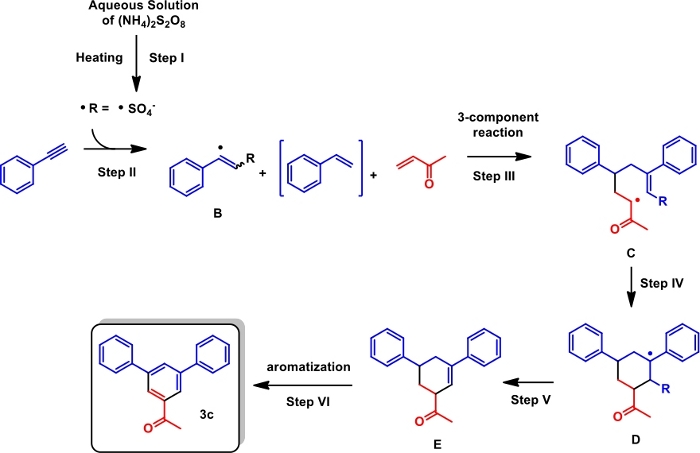
Figura 4: Meccanismo di reazione proposto. Questa cifra è stata modificata da de Souza etal. Fare clic qui per visualizzare una versione più grande di questa figura.
 | ||||
| Ingressoa | Rapporto 1a:2a | NH4S2O8 | Temperatura | Rendimento (%)b |
| (Equiv) | (T, S) | |||
| 1 | 1:1 | 2.0 | 85 | 69 |
| 2 | 2:1 | 2.0 | 85 | 90 |
| 3 | 1:2 | 2.0 | 85 | 65 |
| 4 | 2:1 | 1.0 | 85 | 56 |
| 5 | 2:1 | 3.0 | 85 | 72 |
| 6 | 2:1 | 2.0 | 25 | 0 |
| 7 | 2:1 | 2.0 | 95 | 88 |
| un Condizioni generali per l'ottimizzazione: nella sequenza, 1,0 mL di acqua, 1a (0,5 o 1,0 mmol), 2a (0,5 o 1,0 mmol), (NH4)2S28, 8 h. bRendimento del prodotto isolato. | ||||
Tabella 1. Ottimizzazione delle condizioni di reazione. Questa tabella è stata modificata da de Souza etal.
Discussione
Il metodo riportato qui è stato progettato per essere una configurazione sperimentale molto semplice e mite per la sintesi di benzeni polifunzionalizzati nell'acqua15. Nelle nostre condizioni abbiamo potuto osservare ottime rese per i prodotti attraverso l'uso di persulfato di ammonio. Dovrebbe essere utilizzata una soluzione acquisiva persulfata appena preparata; tuttavia, il persulfato di ammonio solido può anche essere impiegato senza perdita di resa. L'attenzione alla temperatura del mezzo di reazione è obbligatoria. Un aumento di 10 gradi centigradi oltre la temperatura ottimizzata (85 gradi centigradi) ha un effetto deleterio sulla resa (Tabella 1, voce 7)15. Il tempo di reazione può essere aumentato senza influenzare in modo prominente la resa. Durante la reazione, un ago deve essere inserito nel setto per alleviare la pressione finale nel tubo.
Abbiamo notato che la reazione che coinvolge l'alchino ricco di elettroni 1-ethynyl-4-methoxybenzene era lenta, quindi abbiamo deciso di utilizzare 4 equiv. di persulfato di ammonio durante 24 h di tempo di reazione per raggiungere una resa adeguata (3d, Figura 1).
L'espediente di questo protocollo comporta una fase di centrifugazione e una fase di estrazione utilizzando l'acetato di etiliato. La fase di centrifugazione rende l'intero processo di isolamento molto più facile poiché qualsiasi eventuale emulsione formata può essere rotta prontamente. Evita inoltre l'uso di agenti di essiccazione in quanto la separazione delle fasi acquose e organiche avviene in modo più efficiente. Abbiamo scelto l'acetato etitale per ragioni sostenibili16; tuttavia, possono essere utilizzati anche altri solventi comuni per l'estrazione.
Non abbiamo osservato purificazioni impegnative per i prodotti; così, è stata impiegata una spina di silice che ha reso l'intero processo più attraente dal punto di vista operativo ed economico. La maggior parte dei prodotti sono stati purificati utilizzando 92:8 (esanei / acetato di etile). (3d, Figura 1) è stato purificato utilizzando 80:20 (exanes/acetato etilico) e (3e, Figura 1) è stato purificato utilizzando 90:10 (exanes/acetato etilo).
Questo semplice protocollo fornisce una serie di anelli di benzene funzionalizzati in alte rese; tuttavia, il metodo è attualmente limitato agli alchini terminali e ai composti alipatici insaturi. 15 Gli alchini interni non hanno fornito i prodotti mirati. Nella reazione impiegando 4-fenylbut-3-yn-2-ol, una riduzione formale del triplo legame si è verificato durante la trasformazione, mentre dimetilma ma-2-ynedioate ha dato un prodotto di ciclotrimerizzazione. Il chetone aromatico 4-phenylbut-3-en-2-one ha dato il prodotto, ma non era separabile impiegando solo una spina di silice. Mentre miravamo ad impiegare la quantità più bassa possibile di silice e solventi e di conseguenza a ridurre il fattore E17,abbiamo classificato questo substrato come infruttuoso al fine di preservare la sostenibilità della trasformazione. Attualmente, stiamo esaminando le modifiche nella procedura al fine di raggiungere anche questi substrati.
Abbiamo quindi suggerito un possibile meccanismo di reazione per laconversione( Figura 4 , utilizzando il fenilcetylene e il vinile metil come substrati rappresentativi). Una soluzione acquisiva di (NH4)2S2O8 sotto il riscaldamento produce solfato radicale (Figura 4, passo I). Tale radicale è incline ad aggiungere al fenililetylene fornendo radicale B e stirene provenienti dal radicale B (Passo II). Chetone in vinile metile, radicale B e stirne partecipano a una reazione a 3 componenti per dare il radicale C (Passo III). La ciclicizzazione di C fornisce il radicale D (Passaggio IV). L'eliminazione dei rendimenti R radicali olefin E (Passo V) e l'ulteriore aromatizzazione consentono la formazione del prodotto mirato (Step VI).
In sintesi, il nostro protocollo è un metodo conveniente per esplorare la reazione di benzannazione senza metalli in acqua soddisfacendo le esigenze della chimica sostenibile e sostenendo a favore di configurazioni sperimentali operativamente semplici.
Divulgazioni
Gli autori non hanno nulla da rivelare.
Riconoscimenti
Ringraziamo il sostegno finanziario (Grant FAPESP 2017/18400-6) (Grant FAPESP 2017/18400-6). Questo studio è stato finanziato in parte dal Coordenao de Aperfei-oamento de Pessoal de N'vel Superior – Brasil (CAPES) – Finance Code 001.
Materiali
| Name | Company | Catalog Number | Comments |
| Ammonium persulfate | Vetec | 276 | |
| Chloroform-D, (D, 99.8%) | Sigma Aldrich | 570699-50G | |
| 2-cyclohexen-1-one >95% | Sigma Aldrich | C102814-25ML | |
| Ethyl Acetate, 99.9% | Synth | 01A1010.01.BJ | ACS |
| Hexanes, 98.5% | Synth | 01H1007.01.BJ | ACS |
| Phenylacetylene 98% | Sigma Aldrich | 117706-25ML | |
| Silica Gel (SiO2) | Fluka | 60738-5KG | pore size 60 Å, 35-70 μm particle size |
| Thin-layer chromatography plates | Macherey-Nagel | 818333 | 0.20 mm silica gel 60 with fluorescent indicator UV254 |
Riferimenti
- Colacot, T. J. . New Trends in Cross-Coupling. Theory and Applications. , (2015).
- Hassan, J., Sévignon, M., Gozzi, C., Schulz, E., Lemaire, M. Aryl-Aryl Bond Formation One Century after the Discovery of the Ullmann Reaction. Chemical Reviews. 102 (5), 1359 (2002).
- Snieckus, V. Directed Aromatic Functionalization and references therein. Beilstein Journal of Organic Chemistry. 7, 1215-1218 (2011).
- Ashenhurst, J. Intermolecular oxidative cross-coupling of arenes. Chemical Society Reviews. 39 (2), 540-548 (2010).
- Reich, H. Role of Organolithium Aggregates and Mixed Aggregates in Organolithium Mechanisms. Chemical Reviews. 113 (9), 7130-7178 (2013).
- van Otterlo, W. A. L., de Koning, C. B. Metathesis in the Synthesis of Aromatic Compounds. Chemical Reviews. 109, 3743-3782 (2009).
- Zhou, P., Huang, L. B., Jiang, H. F., Wang, A. Z., Li, X. W. Highly Chemoselective Palladium-Catalyzed Cross-Trimerization between Alkyne and Alkenes Leading to 1,3,5-Trienes or 1,2,4,5-Tetrasubstituted Benzenes with Dioxygen. Journal of Organic Chemistry. 75, 8279-8282 (2010).
- Li, S., Wu, X. X., Chen, S. Base-promoted direct synthesis of functionalized N-arylindoles via the cascade reactions of allenic ketones with indoles. Organic and Biomolecular Chemistry. 17, 789-793 (2019).
- Maezono, S. M. B., Poudel, T. N., Lee, Y. One-pot construction of sterically challenging and diverse polyarylphenols via transition-metal-free benzannulation and their potent in vitro antioxidant activity. Organic and Biomolecular Chemistry. 15, 2052-2062 (2017).
- Shu, W. M., Zheng, K. L., Ma, J. R., Wu, A. X. Transition-Metal-Free Multicomponent Benzannulation Reactions for the Construction of Polysubstituted Benzene Derivatives. Organic Letters. 17, 5216-5219 (2015).
- Jiang, L., et al. Secondary amine-catalyzed [3 benzannulation to access polysubstituted benzenes through iminium activation. Synthetic Communications. 48, 336-343 (2018).
- Koening, S. G. . Scalable Green Chemistry. Case Studies from the Pharmaceutical Industry. , (2013).
- Backvall, J. E. . Modern Oxidation Methods. , (2004).
- Narayan, S., et al. "On Water": Unique Reactivity of Organic Compounds in Aqueous Suspension. Angewandte Chemie International Edition. 44, 3275-3277 (2005).
- de Souza, G. F. P., Salles, A. G. Persulfate-Mediated Synthesis of Polyfunctionalized Benzenes in Water via Benzannulation of Alkynes and α,β-Unsaturated Compounds. Green Chemistry. , (2019).
- Prat, D., Wells, A., Hayler, J., Sneddon, H., McElroy, C. R., Abou-Shehada, S., Dunn, P. J. CHEM21 Selection Guide of Classical- and Less Classical-Solvents. Green Chemistry. 18, 288-296 (2015).
- Sheldon, R. A. Metrics of Green Chemistry and Sustainability: Past, Present, and Future. ACS Sustainable Chemistry & Engineering. 6, 32-48 (2018).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon