Method Article
Un metodo delle nanoparticelle d'argento per il miglioramento di sindrome di Atresia biliare nei topi
In questo articolo
Riepilogo
Questo articolo viene descritto in dettaglio un metodo basato su nanoparticelle d'argento per il miglioramento di sindrome di atresia biliare in un modello murino di atresia biliare sperimentale. Una solida comprensione del processo di preparazione del reagente e la tecnica di iniezione neonatale del mouse vi aiuterà a familiarizzare i ricercatori con il metodo utilizzato in studi di modello del mouse neonatale.
Abstract
Atresia biliare (BA) è un tipo severo di colangite con alto tasso di mortalità nei bambini di cui l'eziologia ancora completamente non è capita. Le infezioni virali possono essere una causa possibile. Il tipico modello animale utilizzato per lo studio di BA è stabilito inoculando un mouse neonatale con un rotavirus rhesus. Nanoparticelle d'argento sono state indicate per esercitare gli effetti antivirali e antibatterici; la loro funzione nel modello del topo di BA viene valutata in questo studio. Attualmente, negli esperimenti sugli animali BA, i metodi utilizzati per migliorare i sintomi dei topi BA sono generalmente sintomatici trattamenti somministrati tramite cibo o altri farmaci. Lo scopo di questo studio è di dimostrare un nuovo metodo per il miglioramento di sindrome di BA in topi tramite l'iniezione intraperitoneale di nanoparticelle d'argento e di fornire metodi dettagliati per preparare la formulazione in gel di nanoparticelle d'argento. Questo metodo è semplice e ampiamente applicabile e può essere utilizzato per ricercare il meccanismo di BA, così come nei trattamenti clinici. Basato su modello del topo di BA, quando i topi presentano ittero, il gel preparati delle nanoparticelle d'argento è iniettato intraperitonealmente alla superficie del fegato inferiore. Si osserva lo stato di sopravvivenza, e gli indicatori biochimici e l'istopatologia del fegato sono esaminati. Questo metodo consente una comprensione più intuitiva di entrambi l'istituzione del modello BA e trattamenti novelli BA.
Introduzione
BA è una forma di colestasi caratterizzata da ittero persistente e ha elevata mortalità in assenza di trapianto del fegato. Le infezioni virali sono strettamente associate con la patogenesi di BA. Il citomegalovirus, reovirus e rotavirus sono stati suggeriti come agenti patogeni in BA1,2,3. Durante il periodo neonatale, la risposta del sistema immunitario immaturo ad un'infezione virale provoca dysregulation immune contro dotti biliari extra - e intraepatiche, che portano all'apoptosi delle cellule epiteliali biliari, infiltrazione infiammatoria delle cellule nel portale zona, ostruzione dei dotti biliari intraepatici ed extrahepatic e infine, fibrosi del fegato4,5,6.
Il modello animale comunemente usato per gli studi di BA coinvolge l'inoculazione di un mouse neonatale con i rotavirus rhesus (RRV). Il mouse si sviluppa tipicamente ittero dopo 5-6 giorni, mostrando un basso peso corporeo e feci acoliche. Il ruolo della risposta immunitaria nel processo di malattia è fondamentale, soprattutto per le cellule natural killer (NK); l'esaurimento di queste cellule con l'anticorpo anti-NKG2D riduce notevolmente i danni indotti su BA7. Inoltre, altre cellule, compreso CD4+ T cellule, CD8+ T cellule, cellule dendritiche e cellule di T regolarici, sono state indicate per svolgere i ruoli nella malattia8,9,10,11. Tutti i dati suggeriscono il carattere indispensabile del sistema immunitario nel corso della BA.
Nanoparticelle d'argento (AgNPs) sono state dimostrate per avere effetti benefici contro alcune malattie infettive, tra cui infezioni batteriche12 e infezioni virali13,14,15. Tuttavia, diverso da quello d'uso dermatologico, pochi studi hanno utilizzato AgNPs in un trattamento clinico, soprattutto a causa della loro potenziale tossicità. Negli esperimenti sugli animali, i ricercatori hanno studiato in generale l'efficacia di AgNPs somministrato via orale16 o endovenosa metodi17. Tuttavia, nessun altri ricercatori hanno studiato l'efficacia di AgNPs somministrato tramite un'iniezione intraperitoneale (i.p.) nel topo neonatale esperimenti, che è un metodo semplice e veloce che conduce ad un effetto più diretto sul fegato e vie biliari mentre riducendo la tossicità di altri sistemi, quali il sistema immunitario. AgNPs hanno dimostrato di influenzare l' attività delle cellule NK18; di conseguenza, abbiamo testato gli effetti terapeutici di AgNPs somministrato tramite iniezione i.p. nel modello del topo di BA.
Protocollo
Tutti i protocolli sperimentali animali sono stati approvati dal comitato di uso del Sun Yat-Sen University laboratorio animale centro (#IACUC-DB-16-0602) e istituzionali Animal Care.
1. che stabilisce il modello del Mouse di Atresia biliare
- Mantenere incinto topi BALB/c in un ambiente privo di agente patogeno specifico nell'ambito di un ciclo di buio/luce 12 h a 25 ° C, con accesso a chow in autoclave ad libitum.
- Per preparare il ceppo RRV MMU 18006, amplificare il virus nelle cellule MA104 e misurare i titoli virali da una placca dosaggio19.
Nota: MA104 cellule sono coltivate in mezzo dell'Aquila di Dulbecco modificato (DMEM) con 10% siero bovino fetale (FBS) in un'incubatrice con atmosfera umidificata contenente 5% CO2. I passaggi di amplificazione sono brevemente descritte di seguito.- Infettare le cellule MA104 (1,5 x 107) in un matraccio di cultura2 cm 150 con tripsina attiva RRV [1.5 x 10 unità formanti placca6 (PFU)] in 30 mL di medium senza siero. Incubare le cellule infettate per 3 giorni in un incubatore a 37 ° C con 5% CO2.
- Lisare le cellule infettate nella beuta di cultura da tre cicli di gelo e disgelo, con 20 min in un congelatore a-80 ° C per ciascuno congelare fase e, quindi, lo scongelamento le cellule nuovamente a temperatura ambiente; la particella virale associato rilascerà nel surnatante. Quindi, di raccogliere e trasferire il lysate delle cellule e il supernatante di coltura in una provetta conica da 15 mL.
- Rimuovere grandi detriti cellulari dal lisato mediante centrifugazione a bassa velocità (300 x g a 4 ° C per 3 min). Poi, trasferire il surnatante contenente il virus (circa 6 mL) in una nuova provetta conica 15 mL per gli esperimenti sugli animali.
Nota: Il RRV quindi è pronto per essere titolato, aliquotati e memorizzati o utilizzati per ulteriori cicli di amplificazione. L'esposizione prolungata a temperatura ambiente può ridurre la capacità di infezione virale; il virus dovrebbe essere posti su ghiaccio e conservato a-80 ° C o in azoto liquido.
- Carico il RRV in un'insulina di piccolo volume (1 mL) siringa con un ago 29 G per l'iniezione del mouse neonatale.
Nota: Gli aghi spessi di siringhe volumetriche facilmente conducono a perdita di droga. - Entro 24 h dalla nascita, somministrare a ogni neonato 20 µ l di 1.2 x 105 PFU/mL RRV tramite i.p. itinerario; utilizzare lo stesso volume di soluzione fisiologica come controllo.
Nota: La siringa utilizzata in questo esperimento è una siringa da insulina 1 mL. Topi infetti che non sono stati alimentati dalle loro madri sono morte entro i primi 2 giorni a causa di altri motivi non sono stati inclusi nell'analisi. - Osservare da vicino tutti i topi neonatali e pesare tutti i giorni. In genere, il sesto giorno dopo l'inoculazione di RRV, ittero compare sulle orecchie e pelle nuda, lo sgabello diventa color argilla, e la pelliccia diventa oleosa, suggerendo l'istituzione del modello BA; Verifica per questi sintomi.
Nota: BA può essere confermata da un esame della sezione di tessuto epatico con H & E e immunohistochemical affermando. I topi di BA sono quindi pronti per il trattamento di AgNP.
Attenzione: Il protocollo presentato è per l'utilizzo con contemporanee ceppi RV animali ed umani, che devono essere manipolati in condizioni di livello 2 di biosicurezza (BSL-2).
2. sintesi delle nanoparticelle d'argento
- Preparare e caratterizzare il AgNPs come descritto in precedenza12,20.
Nota: I dettagli della preparazione e che caratterizzano il AgNPs sono stati descritti nelle pubblicazioni dal team di C. M. Che presso il dipartimento di chimica, Università di Hong Kong12,20. La concentrazione finale della soluzione era di 1 mM. Il diametro medio della AgNPs era 10 nm (che vanno da 5 a 15 nm) e confermato da microscopia elettronica.
3. preparazione della miscela del collagene delle nanoparticelle d'argento
Nota: La miscela di collagene AgNP è preparata e caratterizzata come precedentemente descritto21 e conservato a 4 ° C. Tutte le procedure devono essere eseguite sul ghiaccio.
- In primo luogo, per la preparazione di collagene, aggiungere 490 µ l di tipo I del collagene (4 mg/mL) in una provetta da 1,5 mL e posizionarlo sul ghiaccio.
- Aggiungere 100 µ l di tampone fosfato salino (PBS, 10x) al collagene e mescolare con una pipetta.
- Per preparare 1 L di PBS di 10 x, unire 80 g di NaCl, 2 g di KCl e 35,8 g di Na2HPO4. 12H2O a 2,4 g di KH2PO4 e conservare il tampone a temperatura ambiente.
- Quindi, aggiungere 10 µ l di NaOH (0,2 M) per la soluzione di cui sopra.
- Per preparare 0.2 M NaOH, aggiungere 8 g di NaOH in polvere o 1 L di acqua distillata.
- Infine, aggiungere 400 µ l di AgNPs (1 mM) al collagene e mescolarli con una pipetta.
Nota: Aggiungere il AgNPs Ultima per una miscelazione anche. La miscela di collagene AgNP deve essere conservata a 4 ° C; in caso contrario, si solidifica facilmente a temperatura ambiente.
4. metodo di iniezione Mouse
- Amministrare i topi infetti neonatali nel gruppo RRV curato con un'iniezione i.p. di 50 µ l della miscela di collagene AgNP dopo la comparsa di ittero; eseguire una seconda iniezione 3 d più tardi.
Nota: I topi nel gruppo di controllo RRV (controllo infetti) abbiano lo stesso volume di soluzione fisiologica, e i topi nel gruppo di controllo normale non sono dato alcun trattamento. - All'inizio dell'iniezione, premere la gamba del mouse con il dito anulare obliquamente sopra la coscia destra e introdurre l'ago lentamente ad un angolo di 15° (Figura 1). Una volta raggiunta la superficie del bordo inferiore del fegato (Figura 2), circa 0,5 cm in, iniettare la miscela di collagene AgNP; quindi, ritirare l'ago lentamente.
Nota: Fare attenzione a non introdurre aria nella siringa come, quindi, il mouse neonatale può essere ucciso. In topi neonatali, lo stomaco e la milza sono nell'addome di sinistra e lo stomaco è pieno di latte. Se l'iniezione è amministrata da questo lato, l'ago potrebbe facilmente entrare o la stomaco, provocando latte di fluire nella cavità addominale, o della milza, causando emorragie.
Attenzione: Prestate attenzione all'ago per prevenire eventuali lesioni delle dita e assicurarsi di sostituire il cappuccio dell'ago, rimuovere l'ago e metterlo in un contenitore di sharps. - Dopo tutte le iniezioni, tenere i topi dalle loro gabbie per 10 minuti consentire la miscela di collagene AgNP al gel e per impedire che la madre leccare il sito di iniezione. Quindi, restituire i topi nelle loro gabbie.
- Osservare e registrare le apparenze fisiche di tutti i topi di tutti i giorni, tra cui ittero e peso corporeo, come pure il tasso di sopravvivenza.
5. raccolta campioni ematici
Nota: I campioni di sangue di circa 120 µ l sono raccolti inserendo l'ago nel cuore. Dopo centrifugazione, il siero è raccolti (circa 70 µ l) per i test di funzionalità epatica. Il metodo di raccolta del sangue è come segue.
- Anestetizzare i topi il nono e il 12 ° giorno dopo l'inoculazione di RRV (che è di 3 giorni dopo il trattamento di AgNP) utilizzando 0,5-2,5% sevoflurane.
- Immobilizzare gli arti del mouse e sterilizzare l'addome superiore e inferiore con 75% di alcol.
- Esporre il diaframma di taglio del mouse pelle, muscolo e peritoneo lungo la linea mediana per la xifoideo con le forbici; utilizzare un tampone di cotone sterile per rimuovere il tratto gastrointestinale per esporre completamente il muscolo diaframma.
- Inserire l'ago (con una siringa da insulina scaricato 1ml) nel ventricolo sinistro del cuore e tirare lentamente indietro lo stantuffo della siringa per ottenere il volume massimo di sangue. Quindi, trasferire il sangue in una provetta da 1,5 mL.
- Lasciare il tubo a riposare per 30 min a temperatura ambiente e si centrifuga per 5 min a 400 x g. Quindi, utilizzando una pipetta di trasferimento, raccogliere e salvare il siero per ulteriore uso.
Nota: Evitare di danneggiare il diaframma, diaframma difetti facilmente conducono a pneumotorace, la morte e la coagulazione del sangue, impedendo così la raccolta del campione di sangue.
6. rilevamento dei parametri biochimica
- Utilizzare il siero raccolti nel passaggio 5.5 per un rilevamento dei parametri biochimici.
- Utilizzare un analizzatore biochimico automatico per rilevare i seguenti parametri biochimici: alanina aminotransferasi (ALT), aspartato aminotransferasi (AST), fosfatasi alcalina (ALP), proteine totali (TP), albumina (ALB), globulina (GLO), bilirubina totale (TBIL), bilirubina diretta (DBIL), bilirubina indiretta (IBIL) e acidi biliari totali (TBA).
7. extrahepatic colangiografia per osservare la pervietà dei dotti biliari Extrahepatic
Nota: Eseguire l'intero processo sotto un microscopio di dissezione.
- Esporre completamente il fegato, cistifellea e dotti biliari extrahepatic con un batuffolo di cotone.
- Osservare e fotografare l'aspetto del fegato e vie biliari sotto un microscopio di dissezione.
- Utilizzare pinze oftalmiche per premere delicatamente il fondo della cistifellea.
- Caricare una siringa da 1 mL con una soluzione di blu di metilene (0,05 wt.% in H2O). Inserire lentamente l'ago della siringa nella cavità della colecisti; quindi, afferrare l'ago con il forcipe oftalmico e infondere lentamente 10-20 µ l di blu di metilene.
- Osservare al microscopio se il colore blu passa attraverso i dotti biliari extrahepatic al digiuno e prendere una fotografia.
8. raccolta di campioni di fegato freschi per ematossilina ed eosina
- Difficoltà il mouse fresco tessuti del fegato durante la notte in formalina al 10%.
- Quindi, incorporare i tessuti del fegato fissi in paraffina e sezione li.
- Sparaffinatura le sezioni, reidratare loro con una serie di etanolo (come l'etanolo 100%, 95%, 80% e 70% in acqua distillata, ciascuna per 5 min), macchia le sezioni di tessuto con ematossilina, sottoporli a una differenziazione di alcool acido cloridrico 1% e infine, macchiare il sezioni con eosina.
- Infine, osservare l'istopatologia del fegato sotto un microscopio X 40.
9. la macchiatura di Immunohistochemical ematossilina e eosina-macchiate del tessuto sezioni
- Dopo deparaffinazione e reidratare le sezioni, è necessario eseguire un ricupero dell'antigene sommergendo le sezioni in tampone Tris-EDTA (10 mM Tris base, soluzione di EDTA 1 mM; pH 9.0) e li riscaldando in un forno a microonde per 10 min a 95 ° C.
- Rimuovere perossidasi endogena esponendo le sezioni di tessuto per 10 min a una soluzione di perossido di idrogeno 3%.
- Trattare le sezioni con 5% di siero di capra, di bloccare il legame non specifico.
- Aggiungere gli anticorpi primari coniglio-mouse NKG2D (1: 100) per le sezioni e incubare per una notte a 4 ° C.
- Incubare le sezioni con gli anticorpi secondari appropriati (sistema anti-coniglio di polimero HRP-etichetta) per 30 min a temperatura ambiente.
- Visualizzare la macchiatura di immunohistochemical che usando 3, 3'-diaminobenzidina (DAB) come cromogeno.
- Osservare le sezioni sotto un microscopio X 40, acquisire immagini e procedere ad analizzarli come desiderato.
10. l'analisi Cytometric di flusso di
- Tritare il tessuto epatico, passarlo attraverso un setaccio di cella di 70 µm e centrifugare e delicatamente 2 x 270 x g a 4 ° C per 4 min.
- Risospendere il pellet cellulare nel medium RPMI 1640 e analizzarlo di immunofluorescenza di due colori usando gli anticorpi monoclonali.
- Eseguire fenotipizzazione cellulare utilizzando specifici marcatori di superficie cellulare, tra cui della fluorescina isotiocianato - e ficoeritrina-coniugato anti-NKp46 (linfociti NK; 1:1, 000) e anti-CD4 (sottotipo di T-cellula; 1:1, 000), con un citometro a flusso e analizzare i dati con software di analisi dati di citometria a flusso.
- Selezionare popolazioni di cellule secondo avanti/side scatter, cancello, secondo i controlli di isotipo di calcolare qualsiasi fluorescenza di fondo e sottoporre i dati a un'analisi secondaria basata sui segnali di fluorescenza da anticorpi individuali.
Risultati
Basato su modello del topo di BA stabilito, i topi infetti neonatali sono stati amministrati un'iniezione i.p. di al preparato di collagene AgNP 2 x dopo aver esposto l'ittero. Sopravvivenza del mouse è stato controllato per tutti i giorni, e sono stati eseguiti test di funzionalità epatica, patologia del fegato e citometria a flusso. Rispetto ai topi non trattati di controllo BA, i topi AgNP-trattati ha mostrato ridotta ittero e mantenuto la loro peso corporeo normale (Figura 3). I livelli del metabolismo della bilirubina e delle transaminasi epatiche è sceso a valori normali di controllo, suggerendo che la AgNPs notevolmente migliorata la funzionalità epatica (tabella 1). Colangiografia extrahepatic (Figura 4) con la colorazione blu di metilene ha confermato la pervietà del dotto biliare dopo il trattamento di AgNP. H & E che macchia (Figura 5), ha mostrato un'infiltrazione delle cellule infiammatorie significativamente in diminuzione nella zona di portale epatica dei topi trattati con AgNPs, rispetto ai topi di controllo. I risultati di citometria a flusso ha mostrato significativamente meno cellule NK nei fegati dopo i trattamenti di AgNP (entrambi nei giorni 9 e 12) che nei topi RRV (Figura 6). La macchiatura di Immunohistochemical ha rivelato una sostanzialmente ridotta espressione del marcatore delle cellule NK NKG2D (Figura 7) nella triade portale dei topi trattati AgNP, confrontato ai topi RRV.

Figura 1: posizione iniziale siringa vaginale. La linea rossa tratteggiata indica la linea parallela all'addome del mouse neonatale P6; la freccia gialla indica la punta dell'ago; la freccia rossa indica l'angolo dell'ago. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 2: ago raggiunge la superficie del bordo inferiore del fegato. La linea tratteggiata gialla indica il bordo inferiore di un fegato di topo; la freccia rossa indica la posizione dell'ago durante l'iniezione. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 3: effetto del AgNPs nella sindrome di BA in un modello sperimentale di topo BA. (A), questo pannello mostra l'aspetto di topi neonatali nei giorni 9 e 12 dopo un'iniezione con RRV da solo e 3 giorni e 6 giorni dopo l'iniezione con AgNPs (RRV + AgNPs). (B), questo pannello mostra il peso dei topi in ogni gruppo in diversi momenti; la x-asse indica il numero di giorni dopo la nascita il mouse e la y-asse indica la piega-modifica del peso corporeo. P < 0.01 con di Student t-test confrontando il RRV + AgNp gruppo al gruppo di controllo RRV; n = 16 nel gruppo di controllo, n = 18 nel gruppo RRV e n = 17 nel RRV + AgNP gruppo. (C), questo pannello mostra il tasso di sopravvivenza dei topi in ogni gruppo. Questa figura è stata modificata da Zhang et al. 18. Clicca qui per visualizzare una versione più grande di questa figura.
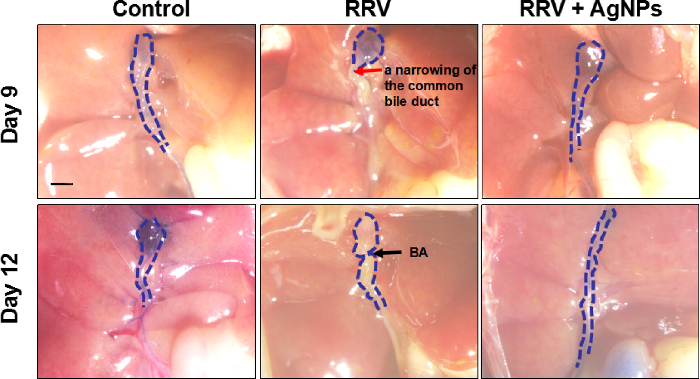
Figura 4: colangiografia Extrahepatic. Un agente di contrasto è stato usato per rilevare la pervietà dei dotti biliari extrahepatic e catturare le immagini. La linea blu tratteggiata indica la direzione del dotto biliare extraepatico; la freccia rossa indica un restringimento del dotto biliare comune; la freccia nera indica BA. Barra della scala = 1 mm. per favore clicca qui per visualizzare una versione più grande di questa figura.

Figura 5: colorazione H & E. Tessuti del fegato dei topi in ciascun gruppo nei giorni 9 e 12 sono stati raccolti, corretti, sezionati e macchiati con H & E. abbreviazioni: PV = vena portale, BD = dei dotti biliari. Barra della scala = 50 µm. Questa figura è stata modificata da Zhang et al. 18. Clicca qui per visualizzare una versione più grande di questa figura.
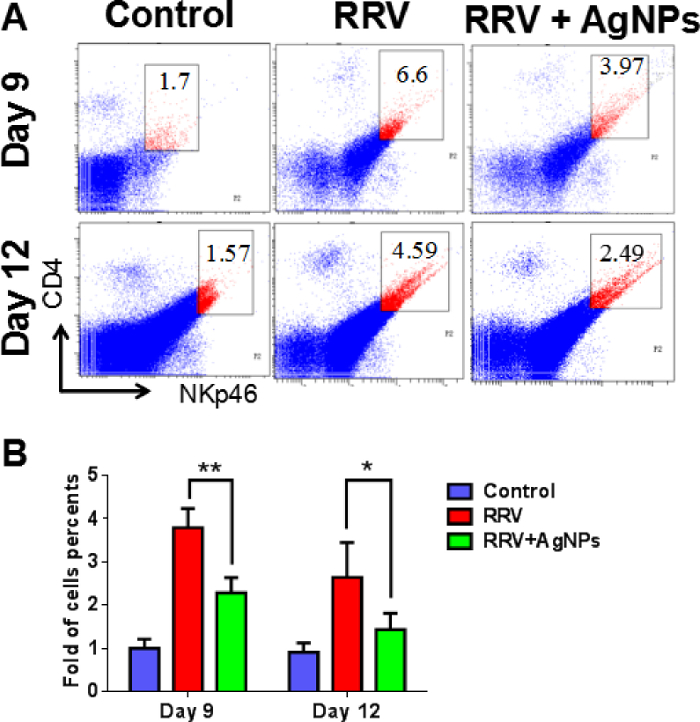
Figura 6: percentuale di NK cells nel tessuto del fegato. (A) i fegati di topi sono stati trasformati in sospensioni cellulari nei giorni 9 e 12, e la proporzione delle cellule di NK è stata rilevata tramite flusso cytometry. (B), questo pannello mostra la percentuale di cellule NK (NKp46+CD4+) in ogni gruppo in diversi momenti dopo l'iniezione di AgNP. Y-asse indica la piega-modifica della percentuale di cellule NK, che è stato calcolato rispetto le percentuali del gruppo di controllo il giorno 9 e giorno 12 *P < 0.01 e *P < 0,05, con di Student t-test confrontando il RRV + AgNp gruppo al gruppo di controllo RRV, n = 10 in ogni gruppo. Questa figura è stata modificata da Zhang et al. 18. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 7: la macchiatura Immunohistochemical per il marcatore di cellule NK NKG2D nell'area del portale dei topi in ciascun gruppo di trattamento. L'espressione del marcatore delle cellule NK NKG2D nell'area del portale dei topi in ciascun gruppo di trattamento è stato rilevato dalla macchiatura immunohistochemical. Le lunghe frecce indicano dotti biliari; le frecce breve indicano le cellule NK. Abbreviazioni: PV: vena portale, BD: dotto biliare. Sscale bar = 50 µm. Questa figura è stata modificata da Zhang et al. 18. Clicca qui per visualizzare una versione più grande di questa figura.
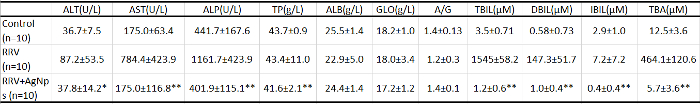
Tabella 1: esame di laboratorio clinico dei livelli del siero del fegato legato alla loro funzione molecola. Sangue periferico è stato usato per misurare la funzione del fegato nei topi in ogni gruppo. ALT: alanina aminotransferasi, AST: aspartato aminotransferasi, ALP: fosfatasi alcalina, TP: proteine, ALB totali: albumina, GLO: globulina, TBIL: bilirubina totale, DBIL: bilirubina diretta, IBIL: bilirubina indiretta e TBA = totale degli acidi biliari. P < 0.05 e * *P < 0.01, con di Student t-test per ogni coorte rispetto al RRV da solo gruppo, n = 10 in ogni gruppo. Tutti i dati relativi agli indicatori biochimici vengono visualizzati come la media ± SD Tutti i topi nei tre gruppi sono stati 12 giorni di età. Questa tabella è stata modificata da Zhang et al. 18. per favore clicca qui per scaricare questo file.
Discussione
AgNPs Mostre potenti proprietà antibatteriche ad ampio spettro e un forte permeabilità22; Inoltre, essi vengono utilizzati per produrre una gamma di prodotti medicali antibatterico23. Tuttavia, AgNPs può richiedere molto tempo per cancellare una volta che si accumulano negli organi, e questa persistenza può portare a effetti tossici24,25. Un precedente studio ha esaminato la tossicità acuta e la genotossicità di AgNPs dopo un singolo i.v. iniezione in un esperimento di ratto, e i risultati hanno mostrato che AgNPs potrebbe causare acuto fegato e danni renali. AgNPs accumulato negli organi principali sistema immunitario, tra cui il timo e la milza17. In questo modello del topo di BA, il trattamento con AgNPs ha migliorato la sindrome BA, che i nostri dati suggeriscono che è parzialmente mediata tramite inibizione delle cellule NK. Tuttavia, gli effetti a lungo termine di AgNPs richiedono un'ulteriore indagine, per valutare la potenziale tossicità per lo sviluppo del mouse e la regolazione immunitaria.
In termini di metodo, alcune note aggiuntive per un intervento chirurgico di successo sono come segue: (i) il processo di preparazione della miscela di collagene AgNP deve essere effettuato su ghiaccio perché, a temperatura ambiente, la miscela di collagene AgNP diventerà presto un gel semi-solido, che non può essere utilizzato per preparazioni iniettabili. Dopo la preparazione, la miscela di collagene AgNP deve essere conservata a 4 ° C. (ii) solo siringhe da insulina 1 mL deve essere utilizzati a causa di piccolo diametro, che riduce la dispersione del farmaco iniettato. (iii) precedenti studi in generale hanno esaminato l'effetto di AgNPs somministrato per via orale16 o tramite iniezione endovenosa17. Nei nostri esperimenti sugli animali, i soggetti dell'esperimento sono topi neonatali; così, l'iniezione endovenosa è quasi impossibile, e abbiamo usato un'iniezione i.p.. L'iniezione di AgNPs ha migliorato i sintomi di BA nei topi. (iv) all'inizio dell'iniezione, degli arti inferiori del mouse vengono fissati a mano impediscono il movimento del mouse. Questo metodo assicura che la giusta quantità di farmaco viene iniettata nella cavità addominale senza alcuna perdita e inoltre garantisce l'efficacia dell'esperimento. (v) in topi neonatali, lo stomaco e la milza sono nell'addome di sinistra e lo stomaco è pieno di latte. Per iniettare la miscela di AgNP alla superficie del bordo inferiore del fegato, l'ago è inserito da sopra la coscia di destra del mouse. Se l'ago è inserito dal lato sinistro, esso potrebbe perforare facilmente sia lo stomaco, causando latte di fluire nella cavità addominale, o della milza, causando emorragie. (vi) perché la parete addominale in topi neonatali è sottile, perdita di droga può essere prevenuta in diagonale avanzando l'ago con un angolo di 15° vicino alla parete addominale per raggiungere il bordo inferiore del fegato.
Abbiamo osservato l'effetto incoraggia di AgNPs in questo mouse indotta da RRV modello BA. Insieme con gli studi precedenti che utilizzato AgNPs nei trattamenti di malattie e infezioni da virus diversi, questi dati AgNP suggeriscono la possibilità di un'applicazione in vivo nelle infezioni di anti-virus. La limitazione di questi esperimenti è che la farmacocinetica di AgNPs non è del tutto chiara come a causa di una mancanza di metodi di misurazione per la AgNPs, che rende difficile il controllo dei dosaggi di AgNP. Ulteriore studio è necessario anche per il bersaglio intracellulare di AgNPs, che ci aiuterà a capire il meccanismo e ridurre gli effetti collaterali nei trattamenti di malattia futura.
Divulgazioni
Gli autori non hanno nulla a rivelare.
Riconoscimenti
Il AgNPs usato qui erano un regalo da C. M. Che il dipartimento di chimica, Università di Hong Kong. Questo lavoro è stato finanziato dal National Natural Science Foundation of China (No. 81600399), la scienza e la tecnologia progetto di Guangzhou (No.201707010014).
Materiali
| Name | Company | Catalog Number | Comments |
| BALB/c mouse | Guangdong Medical Experimental Animal Center | SYXK2017-0174 | Animal experiment |
| Rhesus rotavirus (RRV) | ATCC | ATCC VR-1739 | Establish biliary atresia mouse model |
| MA104 cells | ATCC | ATCC CRL-2378.1 | For laboratory use only |
| DMEM | Thermo Fisher | 10569010 | Mammalian Cell Culture |
| Fetal Bovine Serum | Thermo Fisher | 10099141 | Mammalian Cell Culture |
| collagen Type I | CORNING | 354236 | For research use only |
| PBS buffer | OXOID | BR0014G | For washing |
| NaOH | Sigma | 1310-73-2 | Adjust the PH value |
| AgNP | Antibacterial Note: The AgNps was a gift from Prof CM Che. in the Department of Chemistry, the University of Hong Kong. | ||
| Insulin syringe with integrated needle | BD | 9161635S | For medical use |
| 15 mL Centrifuge Tube | Corning | 430791 | For laboratory use only |
| 1.5 mL Microcentrifuge Tube | GEB | CT0200-B-N | For laboratory use only |
| Microscope | Nikon | ECLIPSE-Ci | For laboratory use |
| Dissecting/Intravital microscope | Nikon | SMZ 1000 | For laboratory use |
| anti-Mouse NKp46 FITC | eBioscience | 11-3351 | For research use only |
| anti-Mouse CD4 PE-Cyanine5 | eBioscience | 15-0041 | For research use only |
| Monoclonal Mouse Anti-Human CD4 | DAKO | 20001673 | For research use only |
| anti-NKG2D | RD | MAB1547 | For research use only |
| BD FACSCanto Flow Cytometer | BD Biosciences | FACS Canto Plus | For laboratory use only |
Riferimenti
- Szavay, P. O., Leonhardt, J., Czechschmidt, G., Petersen, C. The role of reovirus type 3 infection in an established murine model for biliary atresia. European Journal of Pediatric Surgery. 12 (04), 248-250 (2002).
- Coots, A., et al. Rotavirus infection of human cholangiocytes parallels the murine model of biliary atresia. Journal of Surgical Research. 177 (2), 275-281 (2012).
- Shanmugam, N. P., Jayanthi, V. Biliary atresia with cytomegalovirus. Indian Pediatrics. 49 (2), 157(2012).
- Mack, C. L., Feldman, A. G., Sokol, R. J. Clues to the Etiology of Bile Duct Injuryin Biliary Atresia. Seminars in Liver Disease. 32, 307-316 (2012).
- Muraji, T., Suskind, D. L., Irie, N. Biliary atresia: a new immunological insight into etiopathogenesis. Expert Review of Gastroenterology & Hepatology. 3 (6), 599-606 (2009).
- Sokol, R. J., Mack, C. Etiopathogenesis of Biliary Artesia. Seminars in Liver Disease. 21, 517-524 (2001).
- Shivakumar, P., Sabla, G. E., Whitington, P., Chougnet, C. A., Bezerra, J. A. Neonatal NK cells target the mouse duct epithelium via Nkg2d and drive tissue-specific injury in experimental biliary atresia. Journal of Clinical Investigation. 119 (8), 2281-2290 (2009).
- Mack, C. L., et al. Oligoclonal expansions of CD4+ and CD8+ T-cells in the target organ of patients with biliary atresia. Gastroenterology. 133 (1), 278-287 (2007).
- Shivakumar, P., et al. Effector Role of Neonatal Hepatic CD8 + Lymphocytes in Epithelial Injury and Autoimmunity in Experimental Biliary Atresia. Gastroenterology. 133 (1), 268-277 (2007).
- Saxena, V., et al. Dendritic Cells Regulate Natural Killer Cell Activation and Epithelial Injury in Experimental Biliary Atresia. Science Translational Medicine. 3 (102), 102ra194 (2011).
- Miethke, A. G., et al. Post-natal paucity of regulatory T cells and control of NK cell activation in experimental biliary atresia. Journal of Hepatology. 52 (5), 718-726 (2010).
- Tian, J., et al. Topical delivery of silver nanoparticles promotes wound healing. ChemMedChem. 2 (1), 129-136 (2010).
- Lu, L., et al. Silver nanoparticles inhibit hepatitis B virus replication. Antiviral Therapy. 13 (2), 253-262 (2008).
- Xiang, D., et al. Inhibition of A/Human/Hubei/3/2005 (H3N2) influenza virus infection by silver nanoparticles in vitro and in vivo. International Journal of Nanomedicine. 8 (Issue 1), 4103-4114 (2013).
- Elechiguerra, J. L., et al. Interaction of silver nanoparticles with HIV-1. Journal of Nanobiotechnology. 3 (1), 1-10 (2005).
- Nallanthighal, S., et al. Differential effects of silver nanoparticles on DNA damage and DNA repair gene expression in Ogg1-deficient and wild type mice. Nanotoxicology. 11 (8), 1-16 (2017).
- Wen, H., et al. Acute toxicity and genotoxicity of silver nanoparticle in rats. PLoS One. 12 (9), e0185554(2017).
- Zhang, R., et al. Silver nanoparticle treatment ameliorates biliary atresia syndrome in rhesus rotavirus inoculated mice. Nanomedicine. 13 (3), 1041-1050 (2017).
- Arnold, M., Patton, J. T., McDonald, S. M. Culturing, Storage, and Quantification of Rotaviruses. Current Protocols in Microbiology. , Chapter 15 Unit 15C.13 (2009).
- Liu, X., et al. Silver nanoparticles mediate differential responses in keratinocytes and fibroblasts during skin wound healing. ChemMedChem. 5 (3), 468-475 (2010).
- Zhang, R., et al. Silver nanoparticles promote osteogenesis of mesenchymal stem cells and improve bone fracture healing in osteogenesis mechanism mouse model. Nanomedicine. 11 (8), 1949-1959 (2015).
- Wu, J., Hou, S., Ren, D., Mather, P. T. Antimicrobial properties of nanostructured hydrogel webs containing silver. Biomacromolecules. 10 (9), 2686-2693 (2009).
- Xu, L. Genotoxicity and molecular response of silver nanoparticle (NP)-based hydrogel. Journal of Nanobiotechnology. 10 (1), 16(2012).
- Dobrzyńska, M. M., et al. Genotoxicity of silver and titanium dioxide nanoparticles in bone marrow cells of rats in vivo. Toxicology. 315 (1), 86-91 (2014).
- Mohamed, H. R. H. Estimation of TiO 2 nanoparticle-induced genotoxicity persistence and possible chronic gastritis-induction in mice. Food & Chemical Toxicology. 83 (9), 76-83 (2015).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon