הדמיית מיקרו-CT של חוט השדרה של העכבר
Overview
מקור: פיימן שהביגי-רודפושטי וסינה שהבזמהאמדי, המחלקה להנדסה ביו-רפואית, אוניברסיטת קונטיקט, סטוררס, קונטיקט
זו עובדה לא ידועה שהתגלית והשימוש (בשוגג) בצילומי רנטגן זכו בפרס נובל הראשון אי פעם לפיזיקה. תמונת הרנטגן המפורסמת של ידה של אשתו של ד"ר רונטגן משנת 1895 ששלחה גלי הלם דרך הקהילה המדעית נראית כמו רוב תמונות הרנטגן הרפואיות הדו-ממד המודרניות. למרות שזו לא הטכנולוגיה החדשה ביותר, הדמיית ספיגת קרני רנטגן היא כלי הכרחי וניתן למצוא אותה במעבדות המחקר והפיתוח והאוניברסיטאי המובילות בעולם, בתי חולים, שדות תעופה, בין היתר. ניתן לטעון שהשימושים המתקדמים ביותר בהדמיית ספיגת קרני רנטגן כוללים השגת מידע כמו זה שנמצא בצילום רנטגן רפואי 2D אך התממש בתלת-ממד באמצעות טומוגרפיה ממוחשבת (CT או מיקרו-CT). על-ידי לקיחת סדרה של תחזיות רנטגן 2D, תוכנה מתקדמת מסוגלת לשחזר נתונים כדי ליצור נפח 3D. המידע 3D יכול, וסביר להניח יכלול מידע מתוך האובייקט שנבדק מבלי שיהיה צורך לחתוך פתוח. כאן תתקבל סריקת מיקרו-CT, והגורמים העיקריים המשפיעים על איכות התמונה יידונו.
Principles
ניתן לראות צילומי רנטגן כפוטונים עם טווח אנרגיה של 0.1 - 100 keV או גלים אלקטרומגנטיים עם אורכי גל הנעים בין 0.01 - 10 ננומטר. צילומי רנטגן ניתן ליצור במספר דרכים שונות, אבל כאן הדיון מוגבל הדמיית רנטגן קרן קון ספקטרה מתמשכת. צילומי רנטגן אלה נוצרים על ידי תופעה המכונה "Bremsstrahlung", שפירושו "קרינת בלימה" בגרמנית. מצב זה מתרחש כאשר חלקיק טעון עובר תאוצה [1]. במקור רנטגן, אלקטרון טעון שלילית נורה בצינור ואקום ומשפיע על חומר יעד (בדרך כלל טונגסטן, מוליבדן, נחושת או מתכת אחרת) ובאמצעות ההאטה שלו, פולט פוטונים בקנה מידה של צילום רנטגן. ספקטרום מתמשך של צילומי רנטגן נוצר משום שההאטה אינה אחידה ואינה מיידית, אם כי ישנם קוצים בהתפלגות שבמרכזם האנרגיות האופייניות לחומר היעד כפי שניתן לראות ב[2]. ישנן עקומות שונות עבור אנרגיות שונות וחומרי יעד. זהו דבר חשוב מאוד לשקול בעת ביצוע סריקת מיקרו CT והוא יידונו בסעיף מאוחר יותר.
מערכת מיקרו-CT טיפוסית כוללת שלושה רכיבים עיקריים, כפי שמוצג ב- [3]. הרכיבים הבסיסיים של מערכת זו כוללים: א) מקור רנטגן, ב) שלב סיבובי להרכבה לדוגמה, ו- c) פאנל שטוח או מטרה אופטית עם גלאי CCD. צילומי רנטגן עוזבים את המקור ונספגים, מועברים או מפוזרים על ידי הדגימה לפני ההגעה לגלאי. ספיגה היא האינטראקציה הדומיננטית הנמדדת במיקרו-CT, שכן חומרים שונים בגוף סופגים צילומי רנטגן באופן שונה. לדוגמה, עצמות מכילות הרבה סידן אטומי, אשר סופג צילומי רנטגן היטב. לכן, עצמות חוסמות צילומי רנטגן מלהגיע לגלאי, ובסופו של דבר מופיעות בתמונה כצל. לאחר מכן המדגם מסובב בהדרגה והתהליך חוזר על עצמו עד המדגם כבר בתמונה עבור 360° או במקרים מסוימים, 180°. הפלט של הטומוגרפיה הוא סדרה של תחזיות 2D באוריינטציות שונות שניתן לשחזר לאמצעי אחסון תלת-ממדי.
מיקרו-CT הוא סוג של מיקרוסקופיה, המרוויח את שמו מיכולתו לפתור תכונות בקנה מידה מיקרו. הגבלת הרזולוציה עבור קטגוריה ספציפית זו של מיקרו-CT כפופה לגודל נקודת המקור ולהפצת האנרגיה, וסוגו ויעילותו של הגלאי; לא לפי אורך הגל של רנטגן. הרזולוציה הטובה ביותר האפשרית עבור קטגוריה זו של מיקרו-CT היא סביב 500-700 ננומטר בשלושה ממדים. עם זאת, ניתן לזהות תכונות עשירית או מאית מגודל זה.
הגדלה מתבצעת ברוב מערכות ה- CT באמצעות הגדלה גיאומטרית. התמונה ב- [3] ממחישה את הרעיון של הגדלה גיאומטרית. זה בקלות דמיין כאפקט צל. ככל שמקור האור קרוב יותר לאובייקט; ככל שצל האובייקט יופיע על קיר או על מסך גדול יותר. באופן דומה, אם הקיר או המסך היו מתרחקים ממקור האור הנייח ומדגם, הצל של האובייקט יגדל אך יתחלש. אופטימיזציה של מקור הרנטגן ומרחקי העבודה של הגלאי היא משימה מאתגרת מאוד ומעוררת נפשית כאשר נדרשים מספיק אות, רזולוציה גבוהה וזמן סריקה קצר. כמו בכל דבר, יש מגבלות על הגדלה גיאומטרית, שבה האידיאליזציה של מקור נקודה נהרסת ודאות הופכות לשתלטניות.
אחד האתגרים הרבים במיקרו-CT הוא שהאיכות החזותית של נפח תלת-ממד לא תהיה מוכרת לחוקר עד שהסריקה תסתיים ותשוחזר. עם זאת, עם מספיק ניסיון, בדיקה מדוקדקת של כמה תחזיות 2D יכול לספק מספיק מידע כדי להרגיש בטוח לגבי סריקת CT. בסעיפים הבאים, קבוצה של תרגילים תחשוף את ההשפעות של פרמטרי הדמיה שונים על ערכת נתונים ותצייד מדען בהבנה הדרושה כדי לקבל נפח תלת-ממדי נקי. לצורך חקירה זו, דגימות ביולוגיות ייבדקו למרות שההליך אינו מוגבל לסוג מדגם.
הרכבת מדגם נשמעת כמו צעד טריוויאלי אבל זה אחד החשובים ביותר להתעלם. ללא קשר ליישום, יש לטעון את המדגם בצורה הקומפקטית ביותר האפשרית. בהתחשב בתמונה ב[3], תארו לעצמכם אם טווח עמדות המקור והגלאי היה מוגבל מכיוון שהדגימה בלטה בכיוון אחד וכיצד זה ישפיע על הגדלה גיאומטרית. בנוסף למרחק העבודה, הרכבה משפיעה מאוד על התפוקה. אם המדגם היה מפרק ברך שלם מעכברוש, זה היה הגיוני לעלות על המדגם כך השוקה והירך עמדו זקופים. בדרך זו, צילומי הרנטגן יעברו מרחק קצר ויהיה מספיק אות בגלאי. הדבר האחרון שיש לקחת בחשבון בעת הרכבה על מדגם הוא יציבות. האויב הגדול ביותר למיקרו-סי-טי הוא תנועה. אם גודל תנועת המדגם מתקרב לרזולוציה של הסריקה, זה כנראה יהיה נתונים חסרי תועלת. התנועה צריכה להיות מוגבלת על ידי הידבקות מאובטחת להרכבה ועם שליטה כדי לדגום שינוי קומפוזיציה. עבור דגימות ביולוגיות, זה אומר להבטיח כי זה לא ישנה מורפולוגיה באמצעות אידוי לאורך הסריקה. השעיה בג'ל אגרוז או גלישה בשכבה דקה של סרט פרפין הן שתי גישות אפשריות כדי למנוע התייבשות ותנועה.
אנרגיית רנטגן תהיה גם השפעה רבה על איכות נפח 3D הסופי. המטרה היא להשיג אות מספיק בגלאי תוך כדי החלשת מספקת מהדגימה. הפחתה של קרני רנטגן עוקבת אחר משוואה (1), כאשר אני המספר הסופי של ספירות (עוצמה), I 0 הוא המספר הראשוני של ספירות, μ הוא מקדם ספיגת המסה הייחודי לחומר נתון ואנרגיית רנטגן (פורסם בהרחבה), ρ הוא צפיפות החומר, ו x הוא אורך נתיב הרנטגן.
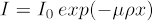 (1)
(1)
באופן אידיאלי, אני/I0 (הידוע גם כערך שידור) צריך להיות בין 5 - 95% לכל כיוון המדגם, עם התוצאות הטובות ביותר מגיעות סביב הטווח האמצעי. כדי לבדוק ערך זה, צלם תמונה של המדגם ולאחר מכן חלק את ערכי הפיקסלים של התמונה בתמונה של אוויר (כלומר עם הדוגמה מחוץ לשדה הראייה). נורמליזציה זו נמצאת בדרך כלל בזרימות עבודה של תוכנות מערכת. זה לא לעתים קרובות כי דגימות ביולוגיות דורשות את השימוש סינון רנטגן במקור, כך שלא יהיה מכוסה כאן. בנוסף לערך שידור אידיאלי, המספר האידיאלי של ספירות עבור כל חלק של המדגם הוא 5000 ספירות. כדי להבטיח זאת, ייתכן שיהיה צורך להגדיל את זמן החשיפה לכל הקרנה. פעולה זו תגדיל את זמן הסריקה הכולל. איור 1 מציג תחזיות 2D נקיות.
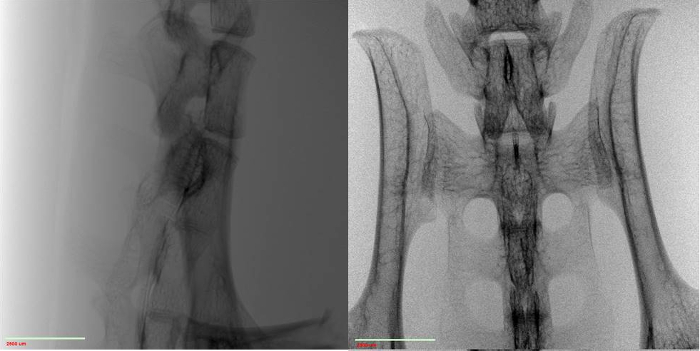
איור 1: תמונות 2D של חוט השדרה של העכבר מנורמלות נגד האוויר ב- 0° (משמאל) וב- 90° (מימין).
Procedure
1. הרכבת דגימה (עצם)
- לבחינת רשת עצמות, כמו עמוד שדרה, ישהו את המבנה בג'ל אגרוז ואפשרו לרפא בצינור פלסטיק דק מאוד (איור 2). הרזון של הצינור חשוב מאוד, משפיע מאוד על תפוקת האות ואיכות התמונה הכללית. פעולה זו משפיעה על היכולת שלך לפתור תכונות. ערך השידור של הצינור צריך להיות קרוב ככל האפשר ל -100%.
- הר את הצינור על הבמה לדוגמה עם קלטת או על ידי ביצוע עמדה מותאמת אישית, בסופו של דבר להבטיח כי המדגם הוא נייח ויציב כאשר הבמה מסתובבת.

איור 2: עמוד השדרה של העכבר תלוי בג'ל אגרוז בתוך צינור פלסטיק דק-דופן היושב על במת הדגימה של מערכת המיקרו-CT.
2. רכישת תמונות
- הפעל את מקור הרנטגן לאנרגיה סביב הטווח של 90 kV (90 kV ו- 10 W).
- לאחר שהמקור מתחמם ומתיישב על האנרגיה, לרכוש תמונה באמצעות תוכנת המערכת.
- בדוק את ערך השידור על-ידי נרמול התמונה מול תמונה של אוויר. עבור רכישת הפניה אוטומטית ויישום, ודא שהדוגמה יכולה לנוע בכיוון נתון מבלי לקרוס.
- אם לתמונה יש שידור גבוה מדי, הנמיך את האנרגיה בהדרגה עד שערך השידור יספיק. הקפידו להגדיל את זמן החשיפה בהתאם כך שהתמונה לא תיראה רועשת וגרגרית. אם לתמונה יש תיבת הילוכים נמוכה מדי, הגדל את האנרגיה בהדרגה עד שערך השידור יספיק.
- התחל להזיז את מקור הרנטגן קרוב יותר לדגימה, תוך נזהר מאוד לא לרסק אותם. הבאת המקור קרוב ככל האפשר למדגם היא צעד בכיוון של מקסום התפוקה ואבטחת הרזולוציה הטובה ביותר האפשרית.
- עם זאת, לחדד את שדה הראייה של המדגם על ידי הסטת שלב המדגם עם המפעילים הליניאריים שלה.
- התוכנה תציג פרמטר המכונה גודל פיקסל אשר מטופלים בדומה לרזולוציה הנוכחית (אם כי הוא אכן שונה).
- אם המספר עדיין גדול מדי והמקור קרוב מאוד, הגלאי יכול להתחיל להתרחק מהדגימה.
- אם המספר קטן מדי, תקרב את הגלאי בזהירות לדגימה.
- נסה מטרות אופטיות שונות עמדות גלאי גם כן, אבל להיזהר הסיבוך זה מציג כאשר מנסים לייעל את הפרמטרים סריקה.
- בדוק כל כיוון של המדגם כדי לוודא שאין קריסות כדי למצוא את זמן החשיפה הטוב ביותר. פעולה זו מתבצעת עקב שינוי מרחק העבודה, גודל הפיקסלים ומיקום הדגימה.
- סובבו את המדגם באיטיות במרווחים של 2 מעלות תוך ניטור מיקומה ביחס למקור ולגלאי באמצעות מצלמת הארון. הקפד להזיז את המקור ואת הגלאי משם אם התנגשות עלולה להתרחש.
- מצא את אורך נתיב הרנטגן הארוך ביותר המביא למספר הנמוך ביותר של ערכי ספירה/שידור ומצא את זמן החשיפה הדרוש לאבטחת כ- 5000 ספירות בכל מקום.
3. הגשה ושחזור טומוגרפיה
תהליך השחזור מנקודת מבט של משתמש אינו מסובך יותר מכל בחירות הפרמטר האחרות שבוצעו בשלבים הקודמים. עם זאת, ההוצאה התכנות והחישובית עבור תהליך זה היא למעשה די משמעותית. משתמשים חייבים לשאוף להבין בצורה הטובה ביותר מה קורה מתחת לממשק המשתמש של התוכנה החלקה וכיצד החלטות משפיעות על המוצר הסופי. מערכות CT רבות משתמשות באלגוריתמי שחזור אלגבריים איטרטיביים שבהם תחזיות הדו-מימד מומרות לסדרה של משוואות ליניאריות המתארות ערכי פיקסלים. מערכות אחרות משתמשות באלגוריתמים של הקרנה אחורית מסוננת שבהם Radon משנה את התחזיות לסינוגרמה ולאחר מכן מועברות דרך סדרה של פעולות שילוב קו. כמובן, חלקם משתמשים בגישות אחרות ואפילו בשיטות היברידיות. ברמה הנמוכה ביותר של מעורבות עם אלגוריתמים אלה, ידוע כי מספר התחזיות ואת העקירה המסתובבת הכוללת יש השפעה על נפח המשוחזר הסופי.
- ראשית, החלט אם לסרוק מעל 180° או 360° בהתבסס על יחס הגובה-רוחב של המדגם. אם המדגם כולל יחס גובה-רוחב גבוה, כך שאורך נתיב הרנטגן ארוך פי 4 או יותר בכיוון של 90 מעלות מאשר בכיוון 0° מאשר סריקה של 180°, תהיה בחירה חכמה. (הטענה היא שהמידע שנאסף באורך נתיב הרנטגן הקצר אינו שונה כל כך מצד לצד. אם ניתן להקדיש תחזיות נוספות לכיווני אורך נתיב הרנטגן הארוכים מאשר ערכת הנתונים. ההעתקה הזוויתית בין התחזיות תהיה נמוכה יותר ויהיה מידע נוסף מאותם כיוונים מסובכים המוזנים לאלגוריתמי השחזור.) אם יחס הגובה-רוחב אינו גבוה כל כך, השתמש בסריקות של 360°.
- לאחר מכן, בחר את מספר התחזיות ואת ההעתקה הזוויתית הכוללת, אשר יכתיב את הזווית בין התחזיות. ככל שזווית זו קטנה יותר, כך יתבצע פחות אינטרפולציה ומידע על תכונות עדינות פחות ייחתך. (יש לקבוע איזון מכיוון שמשמעותם של תחזיות נוספות היא זמן סריקה ארוך יותר, התואם לחלון גדול יותר שבו דגימות יכולות לנוע, פחות זמן לסריקת דברים אחרים ואורך חיים קצר יותר של מקור. כלל אצבע הוא להיות לפחות 800 תחזיות מעל 360° ולא יעלה על 3200 תחזיות.
- שלח את הסריקה.
- לאחר סיום הטומוגרפיה (בדרך כלל בין 4 ל -16 שעות), להביא סדרה 2D של תמונות לתוך מערכת (או איזה קוד פתוח) תוכנת שחזור.
- בחר את תיקון המשמרת המרכזית האופטימלי. Shift center הוא פרמטר המיישר את הפרויקטים בשורה (חשוב על חפיסת קלפים מדשדשת בערך שיש לאסוף וליישר כדי לשבת כמו ערימה מסודרת). ערך זה נמצא בדרך כלל איפשהו בין -10 ל- 10 פיקסלים.
- בחר את מקדם תיקון הקשת הקרן האופטימלי. תיקון התקשות קרן הוא הסרה מלאכותית של ניגודיות המיוצרת על ידי סינון מדגם. אם דגימה עבה מספיק או מכילה מגוון של חומרים קלים וכבדים, תהיה לה ניגודיות כוזבת המבוססת על החלה של צילומי רנטגן רכים (אנרגיה נמוכה). זה צריך להיות מיושם באופן שמרני. ערך ממוצע הוא איפשהו בין 0 - 0.5.
- שלח שחזור.
Results
התמונות הבאות נותנות סקירה כללית של תוצאות שניתן להשיג משימוש במיקרו-CT עם ההליך הנ"ל. ניתן לציין ישירות מדידות איכותיות על ספיגה משתנה בהתבסס על תמונות אלה. נתונים כמותיים כגון נקבוביות חומר, גודל תכונה והפצה, וכו 'ידרוש עיבוד תמונה נוסף בתוכנה אחרת.
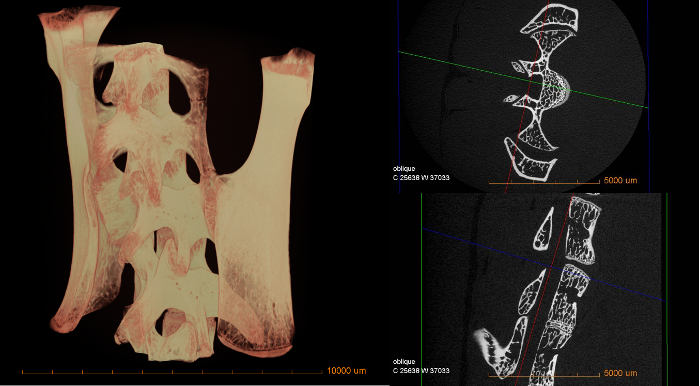
איור 3: נפח תלת-ממדי של חוט השדרה של העכבר (משמאל) ושתי פרוסות דיגיטליות חוצות חתך (מימין)
Application and Summary
ניסוי זה בחן את הגורמים הרבים שיש לקחת בחשבון בעת שימוש במיקרו-CT, במיוחד עבור מדגם ביולוגי. פרויקט זה נועד לעזור לחוקר להבין כיצד החלטותיהם ישפיעו על הנתונים שמיקרו-CT יכול לספק. כפי שהוכח ישנם פרמטרים תלויים ורגישים רבים שיש לקחת בחשבון, כולל: הרכבה, אנרגיית רנטגן, זמן חשיפה, מיקום מקור וגלאי, מספר תחזיות, ותזוזה זוויתית כוללת של הסריקה. תרגיל זה נועד כהקדמה ורק מגרד את פני השטח של שליטה על ערכת נתונים CT.
ניסוי זה התמקד במתן מבוא למיקרו-CT ביחס להדמיית מדגם ביולוגי, אך היישום של טומוגרפיה תלת-ממדית של קרני רנטגן משתרע על עולמות המיקרו-קטרונים, הגיאולוגיה, ייצור התוספים, הציפויים, תאי הדלק ועוד. מיקרוסקופים אלה משמשים לבדיקה, ניתוח כשלים, אפיון, בקרת איכות ואפילו בדיקות לא הרסניות. מכיוון שמידע תלת-ממדי אמיתי נגיש כעת באופן לא הרסני, ניתן לייבא את הגיאומטריות המופקות מ- CT לסימולציות שבהן ניתן לבדוק אובייקטים באופן וירטואלי.
References
- http://www.spectroscopyonline.com/tutorial-attenuation-X-rays-matter [cited 1 November 2017]
- http://hyperphysics.phy-astr.gsu.edu/hbase/quantum/xrayc.html [cited 1 November 2017]
- A.G. Rao, V.P. Deshmukh, L. L. Lavery, H. Bale, "3D investigation of the microstructural modification in hypereutetic aluminum silicon (Al-30Si) alloy." Microscopy and Analysis 2017 [cited 1 November 2017].
Tags
Skip to...
Videos from this collection:

Now Playing
הדמיית מיקרו-CT של חוט השדרה של העכבר
Biomedical Engineering
8.0K Views

הדמיה דגימות ביולוגיות עם מיקרוסקופיה אופטית וקונפוקל
Biomedical Engineering
35.7K Views

הדמיית SEM של דגימות ביולוגיות
Biomedical Engineering
23.5K Views

ייחוס ביולוגי של נשאי ננו-תרופות: יישומים של SEM
Biomedical Engineering
9.3K Views

הדמיית אולטרסאונד בתדר גבוה של אב העורקים בבטן
Biomedical Engineering
14.4K Views

מיפוי מאמץ כמותי של מפרצת באבי העורקים בבטן
Biomedical Engineering
4.6K Views

טומוגרפיה פוטואקוסטית לדם תמונה ולומנים בבטורה האינפרא-רנאלית
Biomedical Engineering
5.7K Views

הדמיית תהודה מגנטית לבבית
Biomedical Engineering
14.7K Views

סימולציות דינמיקה של נוזל חישובי של זרימת דם במפרצת מוחית
Biomedical Engineering
11.7K Views

הדמיית פלואורסצנטיות כמעט אינפרא אדום של מפרצות באבי העורקים בבטן
Biomedical Engineering
8.2K Views

טכניקות למדידת לחץ דם לא פולשניות
Biomedical Engineering
11.9K Views

רכישה וניתוח של אות אק"ג (אלקטרוקרדיוגרפיה)
Biomedical Engineering
104.8K Views

חוזק מתיחה של ביו-חומרים הניתנים למיחזור
Biomedical Engineering
7.5K Views

הדמיה של ניוון מפרק הברך לאחר פציעת ACL לא פולשנית בחולדות
Biomedical Engineering
8.2K Views

הדמיית SPECT ו- CT משולבת כדי להמחיש את תפקוד הלב
Biomedical Engineering
11.0K Views
Copyright © 2025 MyJoVE Corporation. All rights reserved