Method Article
קוונפיקציה של מתכת Leaching ב קיבוע מתכת זיקה כרומטוגרפיה
In This Article
Summary
אנו מציגים שיטת כימות קלה של מתכות הציגו דגימות שהוכנו באמצעות כרומטוגרפיה של זיקה מתכת ללא קיבוע. השיטה משתמשת הידרוקסילנול כחול מחוון הצבע מתכת וספקטרוסקופיה UV-Vis כמו הגלאי.
Abstract
זיהום של אנזימים עם מתכות מחורץ מתוך כרומטוגרפיה של זיקה מתכת כרומטוגרפית (IMAC) מהווה דאגה מרכזית עבור אנזימוולוגים, כמו רבים של הקטניות di-ו שולש משותף המשמש שרפים IMAC יש השפעה מעכבות על אנזימים. עם זאת, את היקף המתכת מפחיתה את ההשפעה של משחררי שונים והפחתת הריאגנטים מובנים באופן גרוע בחלק הגדול בשל העדר מתכת פשוטה ומעשית פרוטוקולי קוונפיקציה השימוש בציוד זמין בדרך כלל . מעבדות ביוכימיה כדי לטפל בבעיה זו, פיתחנו פרוטוקול כדי לכמת במהירות את כמות זיהום המתכת בדגימות שהוכנו באמצעות IMAC כצעד טיהור. השיטה משתמשת הידרוyn, כחול (HNB) כמו מחוון מטרי צביעה עבור תוכן הקטיון מתכת בפתרון מדגם UV-Vis ספקטרוסקופיה כאמצעי לכמת את כמות הקיים של המתכת, לתוך טווח nanomolar, מבוסס על השינוי בספקטרום HNB ב 647 nm. בעוד תכולת המתכת בתמיסה הייתה מבחינה היסטורית, באמצעות ספקטרוסקופיית ספיגה אטומית או בשילוב טכניקות פלזמה, שיטות אלה דורשות ציוד מיוחד והדרכה מחוץ להיקף של מעבדת ביוכימיה טיפוסית. השיטה המוצעת כאן מספקת דרך פשוטה ומהירה לביו-כימאים כדי לקבוע את תוכן המתכת של דגימות באמצעות ציוד וידע קיימים מבלי להתפשר על דיוק.
Introduction
מאז הקמתה על ידי Porath ועמיתים לעבודה1, כרומטוגרפיה של זיקה מתכת כרומטוגרפית (IMAC) הפך לשיטה של בחירה כדי להפריד במהירות חלבונים בהתבסס על יכולתם להתחבר עם יוני מתכת מעבר כגון zn2 +, Ni2 +, Cu2 +, ו-co2 +. זה נעשה בדרך כלל באמצעות הנדסה התגים פולי-histidine והוא כיום אחד שיטות הטיהור הנפוצות ביותר כרומטוגרפי לבידוד של חלבונים רקומביננטי2. IMAC יש גם מצאו יישומים מעבר לטיהור חלבון רקומביננטי כדרך לבודד quinolones, טטרציקווים, קוגליקוצידי, macrolides, ו β-lactams עבור ניתוח לדוגמה מזון3 וכצעד בזיהוי חלבון סרום דם סמנים לכבד וסרטן הלבלב4,5. לא באופן מפתיע, IMAC יש גם להיות שיטה של בחירה עבור בידוד של מספר אנזימים ביואנרגיה יליד6,7,8,9,10. עם זאת, יישום מוצלח של שיטות טיהור אלה למחקרים על חלבונים ביו-אנרגטיים פעילים ומותנים בנוכחות של רמות זניח של מתכות מתכתיות מתוך מטריצת הטור אל החומק. מתכות דיגרפיות המשמשות בדרך כלל ב-IMAC מוכרות משמעות ביולוגית פתולוגית, אפילו בריכוזים נמוכים11,12. ההשפעה הפיזיולוגית של מתכות אלה מודגשת ביותר במערכות bioenergetic, שם הם יכולים להוכיח קטלני כמו מעכבי של נשימה תאית או הפוטוסינתזה13,14,15. בעיות דומות הן בלתי נמנעת עבור רוב שיעורי החלבונים שבהם מתכות שיורית מזהם יכול להפריע לפונקציות ביולוגיות של חלבון או לאפיון עם טכניקות ביולוגיות והביופיסיים.
בעוד הרמות של זיהום מתכת תחת תנאים אוקסיגון ושימוש בסרמדול כמו הימנעות הם בדרך כלל נמוך16, חלבון בדלנים שבוצעו בנוכחות של ציסטאין מפחיתה סוכנים (dtt, β-mercaptoethanol, וכו ') או עם מכשירי כלים חזקים כמו היסטידין17,18 או ethylenediamiiiiiiiiiiiiiiiiiiiiiiiiiiiiiii באופן דומה, מאז יוני מתכת ב שרפים IMAC מתואמים לעתים קרובות על ידי קבוצות קרבוקסילית חלבון שבוצעו בתנאים חומציים צפויים גם להיות רמות גבוהות בהרבה של זיהום מתכת. תוכן מתכת בפתרונות ניתן להעריך באמצעות ספקטרוסקופיית קליטת האטום (AAS) ומצמידים באופן משולב פלזמה המוני הספקטרומטריה (הקאמרי-MS) עד למגבלה של זיהוי ב-ppb-ppt טווח21,22,23,24. למרבה הצער, AAS ו הקאמרי-MS אינם אמצעי מציאותי לאיתור במעבדה ביוכימיה מסורתית כמו שיטות אלה ידרוש גישה לציוד והדרכה מיוחדים.
העבודה הקודמת של בריטני25,26 חקרה את השימוש בהידרוינאפיול כחול (hnb) כדרך לזיהוי נוכחות של מתכות מעבר בתמיסה. עם זאת, היו כמה סתירות פנימיות בנתונים20 ועבודות אלה לא הציעו פרוטוקול הולם. מחקרים של Temel ואח '27 ופרטי ואח '28 הורחב על עבודתה של בריטני עם hnb כמחוון מתכת פוטנציאלי. עם זאת, Temel פיתח פרוטוקול שעושה שימוש AAS עבור ניתוח לדוגמה, באמצעות HNB רק כסוכן מכלפת. המחקר של פרטי השתמשו בשינוי בספקטרום של HNB בשנת 563 nm, אזור של ספקטרום הצבע החופשי HNB החופף בכבדות עם הספקטרום של מכלולי מתכת של HNB ב-pH 5.7, מה שהופך את רגישות הגישה נמוכה למדי, וכתוצאה מכך מתכת חלשה יחסית מחייבת זיקה20. כדי לטפל בבעיות במעבדה שלנו עם Ni2 + טיפת מ-IMAC, הרחבנו את העבודה שנעשתה על ידי בריטני25,26 ו ferreria28 לפתח שיטת קל מסוגל לזהות את רמות nanomolar של מספר מתכות מעבר. הראנו כי HNB נקשר ניקל ומשותף אחרים עבור מתכות IMAC עם כריכת משנה-nanomolar איגוד וטופס 1:1 מורכבות מעל מגוון רחב של ערכי pH20. הבקשה שדווחה כאן מבוססת על ממצאים אלה ומנצלת שינויי ספיגה בספקטרום HNB ב-647 ננומטר לצורך כימות מתכת. ניתן לבצע את השינוי בטווח ה-pH הפיזיולוגי באמצעות מאגרים ומכשור משותפים, המצויים במעבדת ביוכימיה טיפוסית באמצעות איתור וככמת של מכלולי מתכות לצביעת מתכת והשינוי הקשור בספיגת הצבע החופשי כאשר הוא נקשר למתכת.
Protocol
1. שיטת ההכנה של רכיב
- לקבוע את השברים הכרומטופיים באמצעות ספיגה אופטית ב-280 ננומטר או שיטות חלופיות של קוונפיקציה חלבונים כדי לזהות את החלבון שברים מועשרים.
הערה: עבור עבודה זו, השתמשנו מערך דיודה UV-Vis ספקטרוסקופיה. כדי להגביר את תפוקת התפוקה, ניתן להשתמש בקורא צלחות המסוגל למדוד ספיגת קרני UV. - הכנת רכיבי שיטת הצורך
- להכין או להשיג 10-100 mM מאגר ("לדוגמה מאגר") עם pH בין 7 ו 12.
הערה: מאגרים ביוכימיים נפוצים כגון טריס, HEPES, מגבים, ו פוספט ב-pH ניטרלי או בסיסי כולם מקובלים על הצורך. Tricine ו היסטידין ניתן להשתמש אבל ידרוש עקומות כיול כמו שניהם משמעותית יוני מתכת. דוגמה של כיול עבור היסטידין מוצג בהתייחסות20. - הכינו 12% w/v (20-קיפול מרוכז) פתרון של הידרוקסילתהפיזור כחול (HNB) במאגר לדוגמה באמצעות 120 מ"ג של המממנת של HNB עבור כל מיליליטר של פתרון מניות מוכן.
התראה: חשיפה של HNB לעין עלולה לגרום נזק חמור וגירוי. הגנה העין יש להשתמש בעת טיפול HNB וידיים יש לשטוף ביסודיות לאחר הטיפול.
הערה: HNB נמכר כפיזור ב-KCl על ידי ספקים מרכזיים של ריאגנטים מדעי. ככזה, ריכוז בפועל בפתרון ישתנה מתוך יצרנים שונים, אצוות, והיכן בבקבוק את הפיזור HNB נלקח. באופן אידיאלי, ספיגה בין 0.5-0.8 ב 647 ננומטר לאחר דילול של 20 מניות של המניה יש להשיג.
- להכין או להשיג 10-100 mM מאגר ("לדוגמה מאגר") עם pH בין 7 ו 12.
2. הכנה לדוגמא ומדידה
- הכנת ספקטרוסקופיה לאיסוף נתונים
- תדליק ותחמם את. הספקטרוסקופיה של האולטרא-נגד הגדר את הספקטרוסקופיה כדי לאסוף נתונים ב 647 ננומטר.
הערה: אם הספקטרוסקופיה מאפשרת, בנוסף לאסוף נתונים ב 850 ננומטר, או כמה אורך גל אחר ללא שינויים משמעותיים הקשורים לצבע מתכת וצבען ספקטרום, כדי לשמש תיקון בסיסית. - ריק את הספקטרוסקופיה באמצעות מאגר לדוגמה.
הערה: ניתן להשתמש בקוורץ או בעזרת כימיקלים פלסטיים חד פעמיים. כימיקלים קוורץ הם העדיפו לניתוח כמותי כפי שהם יאפשרו דיוק גבוה יותר ודיוק על פני כימיקלים פלסטיק חד פעמיות. עם זאת, כימיקלים פלסטיק לחסום אור UV, אשר עשוי להיות נוכח קרני מדידה של כמה ספקטרופוטומטרים מערך דיודה. חשיפה של HNB לאור UV אינטנסיבי גורמת השפלה לצבוע בלתי רצויות, ירידה איטית בהפחתת הפחתה שניתן להתבלבל עם כריכת מתכת איטית (למשל, ראה איור 1 בתמיכה מידע של התייחסות 20).
- תדליק ותחמם את. הספקטרוסקופיה של האולטרא-נגד הגדר את הספקטרוסקופיה כדי לאסוף נתונים ב 647 ננומטר.
- מדידת שליטה והכנה לקליטה
- הכן פתרון בקרה המכיל 50 μL של מלאי HNB לכל מיליליטר של נפח השיטת הכולל. כדי להבטיח ערבוב טוב של כל הדגימות, פיפטה הכרכים הקטנים תחילה ולאחר מכן להוסיף את מאגר לדוגמה ואחריו ערבוב ידי ליטוף. פתרון HNB מדולל צריך להיות מוכן טרי אבל המניות HNB יכול להיות מאוחסן ב 4 ° צ' מוגן מפני אור במשך שבועות ללא השפלה משמעותית.
- הרשה לפקד לעבור לפחות 3 דקות בטמפרטורת החדר.
הערה: זמן דגירה ארוך יותר עשוי להיות נחוץ עבור דגימות ב-pH אלקליין או בנוכחות של פוספט בשל היווצרות של מכלולי מתכת מסיסים גרוע וכתוצאה מכך שיווציה איטית יותר. - מדדו ומקליטים את הספיגה ב 647 ננומטר לדגימת הבקרה.
- מדידת הכנה וספיגת דגימות
- הכן את דגימות השיטת הדגימה על-ידי ערבוב של 50 μL של מלאי HNB עם 950 μL של שברים מדולל בחלבון עם מאגר לדוגמה.
הערה: מאחר שרמות זיהום מתכות שדווחו בספרות משתנות על-ידי גורם של יותר מ-1000 בהתאם לתנאי הימנעות16,20, ייתכן שיהיה צורך לנסות כמה מדלל את שברי החלבון המבודדים עם המאגר לדוגמה (ראה שלב 1.2.1 לעיל) כדי להשיג שינויי ספיגה בטווח הדינמי של המנה.
התראה: ניקל ומתכות אחרות בשימוש IMAC הם ידועים העור מגרה, חשוד להיות מסרטנים, והם מסוגלים להזיק הכליות דם לאחר חשיפה ממושכת. כפפות והגנה על העין יש להשתמש בעת טיפול דגימות חלבון מוכן IMAC. - לאפשר את המדגם כדי דגירה עבור מינימום של 3 דקות בטמפרטורת החדר ולמדוד ספיגת ב647 nm.
הערה: השלב המגביל של הבחינה במונחים של זמן המושקע הוא שלב הדגירה. הנתונים עבור נייר זה נאסף באמצעות קובט קוורץ יחיד שנשטפו בקפידה בין כל דוגמה. אפילו עם זמן הכביסה הוסיף והכנת מלאי HNB, איסוף נתונים עבור 14 דגימות והבקרה לקח כשעה וחצי וככזה, הפרוטוקול ניתן להשלים בקלות ללא צורך בהפרעה. - חזור על שלבים ה2.3.1 וה2.3.2 עבור כל שבר שיימדדו.
הערה: אם מספר כימיקלים ישמשו לדגימות מרובות, יש להכין דגימות באופן המאפשר המשך הדגירה הדומה וחשיפה לאור הסביבה.
- הכן את דגימות השיטת הדגימה על-ידי ערבוב של 50 μL של מלאי HNB עם 950 μL של שברים מדולל בחלבון עם מאגר לדוגמה.
3. קוונפיקציה מתכת
- קביעת ריכוז המתכת בכל מדגם
- מצא את ההפרש של כל ספיגת המדגם ב 647 ננומטר מהפקד HNB.
- קבע את ריכוז המתכת (ב-μM) באמצעות הנוסחה שלהלן:

כאשר DF הוא פקטור הדילול של השבר הΔAbs647 הוא שינוי ספיגה ב 647 nm, 3.65 x10-2 מייצג את מקדם המחיקה של hnb (ε = 36.5 mM-1· ס"מ-1 ראה התייחסות20 לפרטים נוספים) ו- l הוא הנתיב האופטי של קובט ס מ.
תוצאות
הספקטרום של HNB חינם ב-pH ניטרלי (קו שחור) ואת הספקטרום המייצג של שברים מאסף עבור Ni2 + מן הבידוד של MSP1E3D129 מוצגים באיור 2. סדרת שינוי מוצלחת צריכה להפגין ספיגה מצומצמת ב 647 ננומטר בהשוואה לבקרת HNB, המתאימה להיווצרות מתחמי HNB בנוכחות מתכת מעבר. שיטת הפעולה הכושל הייתה מצוינת בגידול בספיגת ה647 ננומטר. לחילופין, יותר מ 90% הירידה מספיגת הראשונית בשעה 647 ננומטר הייתה מצביעה על תוכן מתכתי גבוה מדי וצורך לאמת שברים מדוללים יותר. שיטת הפעולה שאינה שינויי ספיגה מתוך הפקד HNB חינם אינה מצביעה בהכרח על כשל. ייתכן שדגימות מכילות במהותה לא מתכות מרוסליות. עם זאת, אין זה סביר וכל מדגם שמראה שינוי ספיגה לא צריך להיות מוכן ומדד שוב, רצוי עם פחות דילול, כדי לאשר את התוצאה. בסך הכל, רוב הכשלים להתבונן בשינוי הספיגה הצפוי ניתן לייחס לליטוף לא נאות במהלך הכנת המדגם, זמן דגירה לקוי לפני מדידה, או ערכי pH מחוץ לטווח 7-12 המומלץ.
כדי להדגים את היישום של הבקשה הזו, ניתחנו 2 שלו-tag ממברנה פיגום חלבונים MSP1E3D1 (מבודד כמו ב Denisov, I. ואח '29), MSP2N2 (בודד כמו בגריקובה, Y. V.30), ורומן 3-heme מסוג ציטוכרום GSU0105 מ- geobacter sulfurter, אשר היה recombinantly ביטא E. Coli ו הסתייש עם 500 מ"מ סרמאזול. הפרופילים של Ni2 + מתוך העמודה של NI-נ. ת. ע שרף (לראות את הטבלה חומרים) ואת פרופילי החלבון המשויכים הפרופילים עבור אלה 3 חלבונים מוצגים באיור 3. כל חלבון יהיה הימנעות ניקל ייחודי שעשוי או לא יכול להתיישר עם פרופיל משחרלי חלבון כפי שנמדד ב 280 ננומטר. לדוגמה, איור 3C מראה כי החלבון Ni2 + תוכן של כל שבר עבור GSU0105 הם השתנה באופן משמעותי אחד מהשני בעוד השברים עבור MSP1E3D1 ו MSP2N2 (איור 3A, B) המכילים את רוב החלבון יש גם Ni2 + התוכן הגבוה ביותר. איור 3א, ב גם להדגים כי תוכן מתכת לא מופץ באופן שווה בין שברים שנאספו באמצעות IMAC. בהתאם לאריזה הטור, הרכב של מאגר להתחמק, ציוד שאיבה ותנאים, אפשר להיות elute מתכת בשברים רצופים בריכוזים שונים מאוד עצמאית של תוכן החלבון של שברים אלה.

איור 1: מבנה הידרוינאפיול כחול (HNB). בטווח ה-pH התפקודי של התיכול, כל קבוצות הסולוליום ואחת מקבוצות הידרוקסיל מפוגרות. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 2: ספקטרום ספיגת הMSP1E3D1 של שברים נבחרים ו-HNB. הספיגה היחסית של שלושה שברים של MSP1E3D1 (צבעים) בהשוואה לבקרת HNB (קו עבה שחור) מוצגים. הדגימות הוכנו בשנת 20 ממ טריס, pH 7.5. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
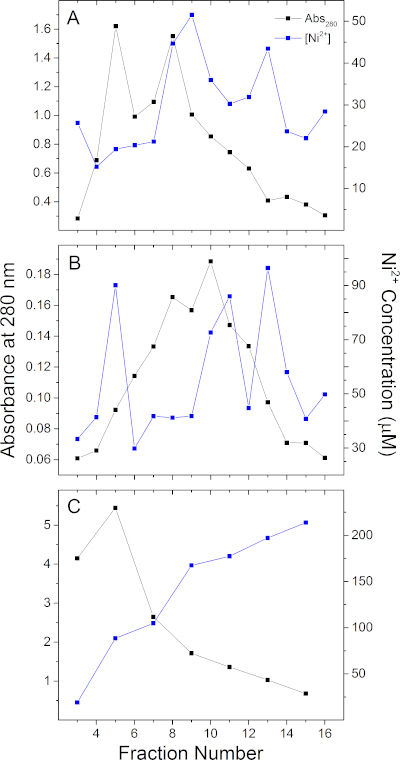
איור 3: Ni2 + קוונפיקציה עבור 3 נציג שלו-תג חלבונים. פרופילי חלבון ו-Ni2 + משחרל (א) MSP1E3D1, (ב) MSP2N2, ו-(ג) GSU0105. משחרלי חלבונים בוצעו באמצעות 300 מ"מ, 300 mM, ו 500 מילימטר ובהתאמה. Ni2 + כימות בוצעה בשנת 20 mM טריס, pH 7.5. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
Discussion
גילוי מטרי הזיהוי של מתכות באמצעות HNB מספק דרך פשוטה לכמת את מידת הזיהום של חלבון על ידי מעבר יוני מתכת מ שרפים IMAC. כפי שקבענו בשופט 20, Ni2 + נקשר ל-hnb עם 1:1 סטויכמטריה וקבוע הדיסוציאציה עבור שינויים מורכבים NI-Hnb עם pH. עם זאת, ה- K המורכב נמצא בטווח ה-nM עבור כל ערכי ה-pH המומלצים (7-12). במונחים מעשיים, זה אומר שכל Ni2 + בכל שברים נבדק יהיה לאגד hnb כל עוד לא ריאגנטים כלדירוג חזק אחרים, כמו edta, הם נוכחים. כל המאפיינים האלה יחד התוצאה היא לינארית Ni2 + טיטור עקומות, אשר התבוננו. בדו ח זה20, הקמנו גם כי שינויים ספקטרלי בשל מתכת צבע היווצרות מורכבים יהיה זהה על פני כל 7-12 pH טווח. האיתור מוגבל על-ידי המדידות המינימליות האמינות בשינוי מדידות (10-4 – 10-3 OD בהתאם לספקטרוסקופיה שבשימוש) המתאים 2.7-27 ננומטר Ni2 +. הטווח העליון מוגבל על-ידי כמות הנוכחים HNB. בעבודתנו, אנו משתמשים ~ 15 μM, המתאים ~ 0.6 OD ב 647 nm. עם זאת, זה יכול להיות גדל עד 50-80 μM HNB, במידת הצורך. למעשה, הבחנו Ni2 + רמות זיהום בשברים כרומטוגרפי דומה או גבוה יותר מאשר הגבול העליון מכריח אותנו לעשות 10 כדי 50-מקפלים השברים של שברים. עם זאת, שלב זה דילול נוסף יכול להגביר את השגיאות היחסיות תוך קביעת ריכוז ניקל בשבריר.
למרות שאנחנו לא חקרו את הפרטים, נראה כי הכריכה של מתכות אחרות בשימוש ב-IMAC שרפים (Co, Zn, Fe) יש גם קבועי דיסוציאציה משנה-μM וכמעט ללא חפיפה בין צבען וצבען מתכת ספקטרום ב647 nm, שיא הגל של חינם . בסדר. לכן, כריכת מתכת להשלים את הצבע ואת השינויים הספקטרלי הקשורים של הצבע יכול לשמש לקביעת מתכת מוחלטת על כל טווח ה-pH המומלץ.
ביצוע הפרוטוקול הוא פשוט והוא תלוי במידה רבה בטכניקת המעבדה הנכונה. ספקטרופוטומטרים מודרני יש תגובות ליניארי מאוד טווחים דינמיים של 3-4 הזמנות של גודל. כתוצאה מכך, המקום הסביר ביותר למבוא של השגיאה בשיטה הוא דרך השלבים הבאים להכנה לדוגמה. כפי שמתואר בטקסט זה, השיטה מבוססת על כימות התוכן של מתכת המבוססת על ההפרש בשיא הספיגה של HNB ב 647 ננומטר מתוך בקרת HNB חינם ודגימות עם HNB מלא עם מתכת. אם הטיפול לא נלקח במדויק בצנרת HNB ali, או אמצעי האחסון של המאגר, השוואה של השליטה וספיגת לדוגמה ב 647 ננומטר הופך לנקודת השגיאה. באופן דומה, ליטוף המסכן של שברי חלבונים להכנה לדוגמא יכול להטות את הריכוז הנתפס של המתכת בשבריר. מומלץ, בגלל הרגישות של השיטה, כל מינון המשמש לניתוח בו נדרשת כיול מדויק לפני השימוש.
המגבלות העיקריות של השיטה מגיעות עם טווח ה-pH התפקודי של הסדר והנוכחות של סוכנים חזקים. השימוש הטוב ביותר מנוצל בטווח pH מ 7-12. מתחת ל-pH 7, הספקטרום של שינויי צבען חינם HNB, לאבד את השיא ב 647 ננומטר המשמש לכמת20. מעל pH 12, הידרוקסידות מתכת רבים מתחילים לזרז, כולל אלה של מתכות נפוצות למצוא שרפים IMAC, ביצוע הכמת איטי פחות להתרבות. בעוד המקסימלי אלקליין אינו מהווה בעיה משמעותית כמו נוהלי טיהור לעתים רחוקות לקרוא ל-pH גבוה כזה, המינימום החומצי הוא סביר יותר להיות גורם מגביל. מאז מגבלות הזיהוי עבור Ni2 + ומתכות מעבר אחרות הם כ 1000 מתקפל נמוך יותר מאשר רמות זיהום מתכת הפגינו לעיל (איור 3), את מגבלת ה-ph נמוך עבור השינוי ניתן להקיף על ידי דילול של שברים חלבון חומצי המאייד במאגרים עם ערכי pH ניטרליים וקיבולת אגירה גבוהה מספיק. לחילופין, ה-pH של שברים מנותח ניתן לכוונן או פתרון המניה HNB יכול להיות חזק יותר באגירה כדי לשמור על ה-pH הרצוי לאחר ערבוב.
אם הליך הבידוד לטיהור החלבון מחייב את השימוש בחומרים מסוימים בעלי תכונות מתכת מוכרות או חשודות, שינוי בשיטה יהיה נחוץ כדי לאפשר כימות מתכות מתכתיות. עיקול סטנדרטי צריך להיות מוכן באמצעות הסוכן הכלגדירוג המשמש להתחמק חלבונים וריכוזים ידועים של תקני מתכת כדי לכמת במדויק את הריכוז של מתכת שטרם בנוכחות הכלור. דוגמה לקוונפיקציה מתכת בנוכחות היסטידין זמין בקוהאן & מרסף20.
קוונפיקציה מדויקת של מתכות בדגימות ביולוגיות עדיין תלויה במידה רבה בשימוש בטכניקות אנליטיות ומכשור, כגון AAS והקאמרי החיצוני-MS, הנותרים מחוץ לתחום הביוכימאי האופייני31,32. Bontaet al תיארו את ההכנה הפשוטה של דגימות ביולוגי על נייר מסנן משותף לניתוח באמצעות הקאמרי-MS, עם זאת, השיטה שלהם עדיין מסתמכת על מיכשור לא תקני עבור ביוכימאי31. השיטה שאנו מתארים מאפשרת מדידת תוכן מתכת במדגם להילקח ללא הכשרה נוספת על מיכשור חדש או מיקור חוץ לאחרים. הפרוטוקולים הדומים לצביעה פותחו לצורך ניתוח מתכות בדגימות ביולוגיות33. עם זאת, השיטה המתוארת על ידי שלמה et al.33 מסתמכת על שיטת הקרינה הפלואורסצנטית באמצעות בדיקה פלואורסצנטית לא זמין מסחרית המספקת מגבלה גבוהה יותר של זיהוי מאשר זה בנייר זה. בהתחשב בקלות היחסית שבה ניתן לבצע את השיטה המתוארת ואת העניין האחרון בפיתוח של פרוטוקולים ניידים זיהוי מתכת עבור דגימות מימית34,35, זה יכול להיות מותאם בקלות עבור בדיקות שדה של דגימות מים. כמבחן נייד, השיטה שלנו יכול להיות שונה לשימוש עם ספקטרוסקופיה ניידת עבור כימות או כאמצעי איכותי כדי לזהות דגימות לניתוח נוסף במיקום בדיקה קבועה.
Disclosures
. למחברים אין מה לגלות
Acknowledgements
חומר זה מבוסס על העבודה הנתמכת על ידי הקרן הלאומית למדע תחת גרנט MCB-1817448 ובפרס תומס פ' וקייט מילר ג ' וליד הזיכרון, בנק אוף אמריקה, הנאמן והתורם המצוין לוז ת'ורפ קרמן ו ג'ורג ' גיי Carman אמון.
Materials
| Name | Company | Catalog Number | Comments |
| 2xYT broth | Fisher Scientific | BP9743-500 | media for E.coli growth |
| HEPES, free acid | BioBasic | HB0264 | alternative buffer |
| HisPur Ni-NTA resin | Thermo Scientific | 88222 | |
| Hydroxynaphthol blue disoidum salt | Sigma-Aldrich | 219916-5g | |
| Imidazole | Fisher Scientific | O3196-500 | |
| Imidazole | BioBasic | IB0277 | |
| MOPS, free acid | BioBasic | MB0360 | alternative buffer |
| Sodium chloride | Fisher Scientific | S271-500 | |
| Sodium phosphate | Fisher Scientific | S369-500 | alternative buffer |
| Tricine | Gold Bio | T870-100 | |
| Tris base | Fisher Scientific | BP152-500 | |
| Triton X-100 | Sigma-Aldrich | T9284-500 |
References
- Porath, J., Carlsson, J. A. N., Olsson, I., Belfrage, G. Metal chelate affinity chromatography, a new approach to protein fractionation. Nature. 258 (5536), 598-599 (1975).
- Block, H., et al. Immobilized-Metal Affinity Chromatography (IMAC): A Review. Methods in Enzymology. 463, 439-473 (2009).
- Takeda, N., Matsuoka, T., Gotoh, M. Potentiality of IMAC as sample pretreatment tool in food analysis for veterinary drugs. Chromatographia. 72 (1/2), 127-131 (2010).
- Felix, K., et al. Identification of serum proteins involved in pancreatic cancer cachexia. Life sciences. 88 (5-6), 218-225 (2011).
- Wu, C., et al. Surface enhanced laser desorption/ionization profiling: New diagnostic method of HBV-related hepatocellular carcinoma. Journal of Gastroenterology and Hepatology. 24 (1), 55-62 (2009).
- Goldsmith, J. O., Boxer, S. G. Rapid isolation of bacterial photosynthetic reaction centers with an engineered poly-histidine tag. Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1276 (3), 171-175 (1996).
- Guergova-Kuras, M., et al. Expression and one-step purification of a fully active polyhistidine-tagged cytochrome bc1 complex from Rhodobacter sphaeroides. Protein Expression and Purification. 15 (3), 370-380 (1999).
- Mitchell, D. M., Gennis, R. B. Rapid purification of wildtype and mutant cytochrome c oxidase from Rhodobacter sphaeroides by Ni(2+)-NTA affinity chromatography. FEBS Letters. 368 (1), 148-150 (1995).
- Tian, H., White, S., Yu, L., Yu, C. A. Evidence for the head domain movement of the rieske iron-sulfur protein in electron transfer reaction of the cytochrome bc1 complex. Journal of Biological Chemistry. 274 (11), 7146-7152 (1999).
- Tian, H., Yu, L., Mather, M. W., Yu, C. A. Flexibility of the neck region of the rieske iron-sulfur protein is functionally important in the cytochrome bc1 complex. Journal of Biological Chemistry. 273 (43), 27953-27959 (1998).
- Louie, A. Y., Meade, T. J. Metal complexes as enzyme inhibitors. Chemical Reviews. 99 (9), 2711-2734 (1999).
- Tamás, M. J., Sharma, S. K., Ibstedt, S., Jacobson, T., Christen, P. Heavy Metals and Metalloids As a Cause for Protein Misfolding and Aggregation. Biomolecules. 4 (1), 252-267 (2014).
- Gerencser, L., Maroti, P. Retardation of proton transfer caused by binding of the transition metal ion to the bacterial reaction center is due to pKa shifts of key protonatable residues. Biochemistry. 40 (6), 1850-1860 (2001).
- Klishin, S. S., Junge, W., Mulkidjanian, A. Y. Flash-induced turnover of the cytochrome bc1 complex in chromatophores of Rhodobacter capsulatus: binding of Zn2+ decelerates likewise the oxidation of cytochrome b, the reduction of cytochrome c1 and the voltage generation. Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1553 (3), 177-182 (2002).
- Link, T. A., von Jagow, G. Zinc ions inhibit the QP center of bovine heart mitochondrial bc1 complex by blocking a protonatable group. Journal of Biological Chemistry. 270 (42), 25001-25006 (1995).
- Block, H., Kubicek, J., Labahn, J., Roth, U., Schäfer, F. Production and comprehensive quality control of recombinant human Interleukin-1beta: a case study for a process development strategy. Protein Expression and Purification. 57 (2), 244-254 (2008).
- Kokhan, O., Shinkarev, V. P., Wraight, C. A. Binding of imidazole to the heme of cytochrome c1 and inhibition of the bc1 complex from Rhodobacter sphaeroides: II. Kinetics and mechanism of binding. Journal of Biological Chemistry. 285 (29), 22522-22531 (2010).
- Kokhan, O., Shinkarev, V. P., Wraight, C. A. Binding of imidazole to the heme of cytochrome c1 and inhibition of the bc1 complex from Rhodobacter sphaeroides: I. Equilibrium and modeling studies. Journal of Biological Chemistry. 285 (29), 22513-22521 (2010).
- Bornhorst, J. A., Falke, J. J. Purification of proteins using polyhistidine affinity tags. Methods in Enzymology. 326, 245-254 (2000).
- Kokhan, O., Marzolf, D. R. Detection and quantification of transition metal leaching in metal affinity chromatography with hydroxynaphthol blue. Analytical Biochemistry. 582, 113347 (2019).
- Doyle, C., Naser, D., Bauman, H., Rumfeldt, J., Meiering, E. Spectrophotometric method for simultaneous measurement of zinc and copper in metalloproteins using 4-(2-pyridylazo)resorcinol. Analytical Biochemistry. 579, 44-56 (2019).
- Furrer, J., Smith, G. S., Therrien, B., Gasser, G. . Inorganic Chemical Biology. , (2014).
- Hogeling, S. M., Cox, M. T., Bradshaw, R. M., Smith, D. P., Duckett, C. J. Quantification of proteins in whole blood, plasma and DBS, with element-labelled antibody detection by ICP-MS. Analytical Biochemistry. 575, 10-16 (2019).
- Yamasaki, S., Tsumura, A., Takaku, Y. Ultratrace Elements in Terrestrial Water as Determined by High-Resolution ICP-MS. Microchemical Journal. 49 (2), 305-318 (1994).
- Brittain, H. G. Complex Formation Between Hydroxy Naphthol Blue and First Row Transition Metal Cyanide Complexes. Analytical Letters. 10 (13), 1105-1113 (1977).
- Brittain, H. G. Binding of Transition Metal Ions by the Calcium Indicator Hydroxy Naphthol Blue. Analytical Letters. 11 (4), 355-362 (1978).
- Temel, N. K., Sertakan, K., Gürkan, R. Preconcentration and Determination of Trace Nickel and Cobalt in Milk-Based Samples by Ultrasound-Assisted Cloud Point Extraction Coupled with Flame Atomic Absorption Spectrometry. Biological Trace Element Research. 186 (2), 597-607 (2018).
- Ferreira, S. L. C., Santos, B. F., de Andrade, J. B., Costa, A. C. S. Spectrophotometric and derivative spectrophotometric determination of nickel with hydroxynaphthol blue. Microchimica Acta. 122 (1), 109-115 (1996).
- Denisov, I. G., Grinkova, Y. V., Lazarides, A. A., Sligar, S. G. Directed Self-Assembly of Monodisperse Phospholipid Bilayer Nanodiscs with Controlled Size. Journal of the American Chemical Society. 126 (11), 3477-3487 (2004).
- Grinkova, Y. V., Denisov, I. G., Sligar, S. G. Engineering extended membrane scaffold proteins for self-assembly of soluble nanoscale lipid bilayers. Protein Engineering, Design and Selection. 23 (11), 843-848 (2010).
- Bonta, M., Hegedus, B., Limbeck, A. Application of dried-droplets deposited on pre-cut filter paper disks for quantitative LA-ICP-MS imaging of biologically relevant minor and trace elements in tissue samples. Analytica Chimica Acta. 908, 54-62 (2016).
- Olmedo, P., et al. Validation of a method to quantify chromium, cadmium, manganese, nickel and lead in human whole blood, urine, saliva and hair samples by electrothermal atomic absorption spectrometry. Analytica Chimica Acta. 659 (1), 60-67 (2010).
- Shyamal, M., et al. Highly Selective Turn-On Fluorogenic Chemosensor for Robust Quantification of Zn(II) Based on Aggregation Induced Emission Enhancement Feature. ACS Sensors. 1 (6), 739-747 (2016).
- Kudo, H., Yamada, K., Watanabe, D., Suzuki, K., Citterio, D. Paper-Based Analytical Device for Zinc Ion Quantification in Water Samples with Power-Free Analyte Concentration. Micromachines. 8 (4), 127 (2017).
- Liu, R., Zhang, P., Li, H., Zhang, C. Lab-on-cloth integrated with gravity/capillary flow chemiluminescence (GCF-CL): towards simple, inexpensive, portable, flow system for measuring trivalent chromium in water. Sensors and Actuators B: Chemical. 236 (C), 35-43 (2016).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved